Resumos
Duas porções do ejaculado suíno - primeiros 15mL da fração espermática rica (P1) e o restante do ejaculado (P2) - foram coletadas semanalmente de cinco varrões e submetidas a dois protocolos de resfriamento, diluição no diluidor MR-A® e conservação a 17°C (T1) ou no diluidor glicina-gema de ovo e conservação a 5°C (T2). As doses foram avaliadas no que se refere à motilidade, ao vigor e à morfologia espermáticas no sêmen a fresco e em diferentes tempos de estocagem. Todos os tratamentos mantiveram uma motilidade aceitável, superior a 50%, nas primeiras 24 horas de armazenamento. O grupo P2T2 manteve uma motilidade similar (P>0,05) ao longo de todo o período de resfriamento (72 horas), sendo inclusive superior aos demais neste período, enquanto os outros tratamentos apresentaram uma redução da motilidade no decorrer do tempo de armazenamento. Com relação às características morfológicas do sêmen, não se observaram diferenças (P>0,05) quanto às porcentagens de espermatozoides normais entre as duas frações do ejaculado fresco. Ainda, todos os tratamentos mantiveram-se dentro dos limites aceitáveis, independentemente do tempo de armazenamento. A P1 parece ser mais adequada à produção de doses para o transporte em virtude de seu pequeno volume e alta concentração, enquanto o restante do ejaculado (P2) pode ser utilizado com eficiência dentro da própria granja.
suíno; porção do ejaculado; sêmen resfriado; transporte do sêmen
Two portions of boar ejaculate - first 15mL of the sperm rich fraction (P1) and the rest of the ejaculate (P2) - were collected weekly from 5 mature boars and submitted to two cooling methods, extended in MR-A® and cooled at 17°C (T1) or extended in glycine-egg yolk and cooled at 5°C (T2). Spermatozoa motility, vigor, and morphological characteristics were evaluated immediately after collection and in different storage times. All treatments kept an acceptable motility, higher than 50%, in the first 24h of storage. The P2T2 maintained a similar motility (P>0.05) throughout the cooling storage (72h) and was superior in that period, while the other treatments presented a decrease in motility related to time. There was no difference between the two portions regarding the total number of normal spermatozoa in the fresh semen (P>0.05). All treatments showed morphological abnormalities within the acceptable thresholds, irrespectively of the storage time. Thus, due to low volume and high concentration, P1 seems to be more adequate for sperm dose transportation. Furthermore, this methodology will allow the development of new proposals concerning the transportation of swine semen, while the rest of the ejaculate could be used in farm routines to produce conventional liquid semen doses.
swine; ejaculate portions; cooled semen; semen transportation
MEDICINA VETERINÁRIA
Efeito da porção do ejaculado e do método de resfriamento sobre as características físicas do sêmen suíno
Effect of ejaculate portion and conservation method on the physical characteristics of boar semen
D.V. AlkminI; J.M. Silva FilhoII, * * Autor para correspondência ( corresponding author) ; M.S. PalharesII; A.P. SiqueiraI; G.S. MachadoIII; C.L.A. SilvaI; T.C. TarantiniIV
IAluno de pós-graduação - EV- UFMG, Belo Horizonte, MG
IIEscola de Veterinária - UFMG. Caixa Postal 567 - 30123-970 - Belo Horizonte, MG
IIIIntegrall Soluções em Produção Animal
IVMédica veterinária autônoma
RESUMO
Duas porções do ejaculado suíno - primeiros 15mL da fração espermática rica (P1) e o restante do ejaculado (P2) - foram coletadas semanalmente de cinco varrões e submetidas a dois protocolos de resfriamento, diluição no diluidor MR-A® e conservação a 17°C (T1) ou no diluidor glicina-gema de ovo e conservação a 5°C (T2). As doses foram avaliadas no que se refere à motilidade, ao vigor e à morfologia espermáticas no sêmen a fresco e em diferentes tempos de estocagem. Todos os tratamentos mantiveram uma motilidade aceitável, superior a 50%, nas primeiras 24 horas de armazenamento. O grupo P2T2 manteve uma motilidade similar (P>0,05) ao longo de todo o período de resfriamento (72 horas), sendo inclusive superior aos demais neste período, enquanto os outros tratamentos apresentaram uma redução da motilidade no decorrer do tempo de armazenamento. Com relação às características morfológicas do sêmen, não se observaram diferenças (P>0,05) quanto às porcentagens de espermatozoides normais entre as duas frações do ejaculado fresco. Ainda, todos os tratamentos mantiveram-se dentro dos limites aceitáveis, independentemente do tempo de armazenamento. A P1 parece ser mais adequada à produção de doses para o transporte em virtude de seu pequeno volume e alta concentração, enquanto o restante do ejaculado (P2) pode ser utilizado com eficiência dentro da própria granja.
Palavras-chave: suíno, porção do ejaculado, sêmen resfriado, transporte do sêmen
ABSTRACT
Two portions of boar ejaculate - first 15mL of the sperm rich fraction (P1) and the rest of the ejaculate (P2) - were collected weekly from 5 mature boars and submitted to two cooling methods, extended in MR-A® and cooled at 17°C (T1) or extended in glycine-egg yolk and cooled at 5°C (T2). Spermatozoa motility, vigor, and morphological characteristics were evaluated immediately after collection and in different storage times. All treatments kept an acceptable motility, higher than 50%, in the first 24h of storage. The P2T2 maintained a similar motility (P>0.05) throughout the cooling storage (72h) and was superior in that period, while the other treatments presented a decrease in motility related to time. There was no difference between the two portions regarding the total number of normal spermatozoa in the fresh semen (P>0.05). All treatments showed morphological abnormalities within the acceptable thresholds, irrespectively of the storage time. Thus, due to low volume and high concentration, P1 seems to be more adequate for sperm dose transportation. Furthermore, this methodology will allow the development of new proposals concerning the transportation of swine semen, while the rest of the ejaculate could be used in farm routines to produce conventional liquid semen doses.
Keywords: swine, ejaculate portions, cooled semen, semen transportation
INTRODUÇÃO
A reprodução de suínos tem passado, nos últimos anos, por um grande desenvolvimento notadamente no que se refere à utilização de técnicas que permitam um melhor controle reprodutivo, diretamente relacionadas à otimização da inseminação artificial (IA) (Levis, 2000). A grande difusão da IA na espécie suína, utilizando o sêmen resfriado, deu-se graças ao desenvolvimento de diluidores que permitem a conservação das células espermáticas por prolongados períodos de tempo e com fertilidade adequada (Gadea, 2003).
Um aspecto crucial nos procedimentos de IA é a necessidade do transporte do sêmen do local de coleta e processamento até o local onde as fêmeas estão alojadas. Esse transporte pode levar mais de 24 horas, em se tratando de locais de difícil acesso ou em países de grande extensão territorial, como o Brasil. Dessa forma, o sêmen deve ser coletado, processado, transportado e estocado de maneira a não afetar adversamente o potencial fertilizante dos espermatozoides.
Especula-se que o resfriamento do sêmen suíno à temperatura de 5ºC possibilitaria o armazenamento e/ou transporte por um período de tempo superior ao rotineiramente utilizado (15-18ºC), devido à redução do metabolismo espermático e à inibição do crescimento bacteriano, de maneira similar ao que se tem estabelecido para o sêmen de outras espécies. Assim, diferentemente do que ocorre na espécie equina, por exemplo, poucos estudos são encontrados na literatura com referência ao sistema de transporte do sêmen suíno. Roner et al. (2006) desenvolveram um contêiner para o resfriamento e a conservação do sêmen suíno bastante simples, barato, capaz de propiciar um resfriamento lento das células espermáticas e a obtenção de duas temperaturas de estocagem do sêmen resfriado em um mesmo contêiner (5±1ºC ou 17±1ºC), sendo o tempo médio de manutenção dessas temperaturas de 53 e 43 horas, respectivamente. No entanto, sabe-se que uma das principais limitações para o transporte do sêmen suíno é o grande volume necessário para compor a dose inseminante, além da temperatura e do tempo de armazenamento dessas doses.
Recentemente, tem-se dado muita importância aos componentes do plasma seminal nas diferentes frações que compõem o ejaculado do varrão e seus efeitos sobre os espermatozoides (Rodríguez-Martínez et al., 2005). Nesse sentido, Peña et al. (2003) citam que os espermatozoides oriundos dos primeiros 10mL da porção espermática rica do ejaculado de varrões resistem melhor aos procedimentos de diluição, resfriamento, congelamento e descongelamento do que aqueles contidos no restante do ejaculado fracionado (segunda porção da fração rica e fração pós-espermática). Assim, especula-se que o uso dessa porção do ejaculado possibilitaria a redução da temperatura durante o armazenamento e transporte do sêmen, sem prejuízos quanto a sua viabilidade, enquanto o restante do ejaculado poderia ser utilizado para a produção de doses utilizadas dentro da própria granja. Diante desse contexto, pretendeu-se avaliar o efeito de duas porções do ejaculado suíno, denominadas de porção 1 - primeiros 15mL da fração espermática rica - e porção 2 - restante do ejaculado -, diluídas nos diluidores MR-A® ou glicina-gema de ovo (Foote, 2002) e armazenadas a 17 ou 5ºC, respectivamente, em contêiner especial, sobre a qualidade do sêmen armazenado in vitro.
MATERIAL E MÉTODOS
Foram utilizados cinco machos da raça Landrace, pertencentes à Central de Inseminação Artificial da DB-Danbred do Brasil, com idade acima de 12 meses, de fertilidade e qualidade seminal comprovadas após avaliação do desempenho reprodutivo, baseadas nos dados de fertilidade e de exame andrológico do rebanho.
Como delineamento experimental, utilizou-se um esquema fatorial 2×2, composto por duas porções do ejaculado: porção 1 - primeiros 15mL da fração espermática rica e porção 2 - restante do ejaculado, submetidas a dois protocolos de resfriamento do sêmen (Diluição em diluidor MR-A® e estocagem a 17ºC ou diluição em diluidor glicina-gema de ovo e estocagem a 5ºC).
Para a coleta do sêmen, utilizou-se a técnica de mão enluvada descrita por Hancock e Howell (1959), realizada de forma fracionada; ou seja, após se desprezarem os primeiros jatos de sêmen (fração pré-espermática), foram coletados os primeiros 15mL da fração espermática rica (porção 1) em um tubo plástico de centrífuga graduado (tipo Falcon) com capacidade de 50mL. Acoplado ao tubo, foi usado um funil pequeno contendo sobre sua abertura um filtro descartável. O restante do ejaculado (porção 2) foi coletado imediatamente após a coleta da porção 1, em um recipiente térmico previamente aquecido. Utilizaram-se 10 ejaculados de cinco varrões, coletados a intervalos de quatro a seis dias. Após cada coleta fracionada, as porções 1 (P1) e 2 (P2) do ejaculado foram subdivididas e submetidas aos tratamentos a seguir: P1T1: porção 1 diluída no diluidor MR-A® e armazenada a 17ºC; P1T2: porção 1 diluída no diluidor glicina-gema de ovo e armazenada a 5ºC; P2T1: porção 2 diluída no diluidor MR-A® e armazenada a 17ºC; P2T2: porção 2 diluída no diluidor glicina-gema de ovo e armazenada a 5ºC.
Imediatamente após a coleta, o sêmen era encaminhado ao laboratório e avaliado quanto às características físicas (concentração, motilidade e vigor) de ambas as porções. Nesse momento, era retirada uma alíquota de sêmen de cada porção, devidamente diluída e conservada em solução de formol-salina tamponada (Hancock, 1957) para posterior avaliação da morfologia espermática. Devido à alta concentração de espermatozoides por mililitro de sêmen encontrada na porção 1, a mensuração de sua concentração foi realizada retirando-se uma alíquota de 10µL de sêmen com auxílio de uma pipeta graduada, a ser diluída em 8mL de uma solução formol-salina tamponada, a uma taxa de diluição de 1:800. Para a mensuração da concentração espermática da porção 2, utilizou-se uma alíquota de 40µL de sêmen diluída em 4mL da solução de formol-salina tamponada, a uma taxa de diluição de 1:100. Para ambas as porções, a contagem das células espermáticas foi feita em hematocitômetro (Câmara de Neubauer).
As avaliações de motilidade e vigor foram realizadas subjetivamente, colocando-se uma gota de sêmen entre lâmina e lamínula, previamente aquecidas em mesa aquecedora a 37ºC, sendo submetida imediatamente à avaliação microscópica de campo claro, com aumento de 100× e 400×.
As análises morfológicas foram realizadas em microscópio óptico com contraste de fase (1000×), constituindo-se da observação morfológica de 100 células espermáticas (Shipley, 1999) e computando-se a porcentagem de espermatozoides normais e com patologias de cabeça, peça intermediária, cauda, acrossoma, gota proximal, gota distal e defeitos totais (Manual..., 1998). As avaliações físicas do sêmen foram realizadas, em ambas as porções, no sêmen fresco, imediatamente após a diluição, e nos intervalos de 12, 24, 36, 48 e 72 horas de estocagem. Após a avaliação e diluição das duas porções coletadas, o sêmen foi resfriado e armazenado a 5 ou 17ºC em um contêiner desenvolvido especialmente para a espécie suína (Roner et al., 2006).
Os dados foram apresentados como média ± erro padrão da média. As características avaliadas subjetivamente, como motilidade e vigor espermático pré e pós-resfriamento, foram avaliadas pela abordagem não paramétrica, aplicando-se o teste de Kruskal-Wallis. Os dados correspondentes às avaliações morfológicas dos espermatozoides, expressos em porcentagem, sofreram uma transformação angular (arcsen √x), sendo as médias comparadas pelo teste SNK. Todas as análises foram processadas pelo programa estatístico (Statistical..., 1999), e significância de 95% (P<0,05).
RESULTADOS E DISCUSSÃO
Os dados referentes às características seminais de cada porção do ejaculado estão apresentados na Tab. 1. De acordo com os valores apresentados, observa-se que não houve diferenças entre as porções no que diz respeito à motilidade do sêmen fresco (P>0,05), encontrando-se esses valores (74,5% para ambas as frações) acima do proposto na literatura (60%; Flowers, 1997; Johnson et al., 2000) como critério mínimo para o processamento de um ejaculado.
Com relação ao vigor espermático, observa-se que a porção 1 apresentou um valor médio superior (P<0,05) ao encontrado na porção 2. Contudo, os valores de vigor observados nas duas porções desse experimento são superiores ao valor mínimo preconizado por Silveira e Lais (1999) para a utilização de um ejaculado - vigor espermático de três, em uma escala de 0 a 5.
A concentração espermática observada no presente experimento, para a porção 1, foi semelhante à relatada por Saravia et al. (2010). Esses pesquisadores, ao trabalharem com os primeiros 10mL da fração espermática rica, encontraram concentração média de 1600x106 de espermatozoides/mL para essa porção. Os autores citaram, ainda, que os espermatozoides presentes nesses primeiros 10mL (16x109 de espermatozoides/10mL) representaram 23,4% do número total médio de espermatozoides encontrados na fração espermática rica do ejaculado (68,4x109 de espermatozoides). Comparativamente, os dados encontrados no presente experimento demonstram que a porção 1 continha cerca de 25x109 de espermatozoides/15mL, representando 33,8% do total de espermatozoides presentes no ejaculado, o que demonstra a alta concentração espermática dessa porção, notadamente quando se considera a grande diferença de volume entre as duas porções do ejaculado (15 vs. 208mL).
Os valores médios de motilidade e vigor espermáticos do sêmen para os quatro tratamentos, nos diferentes períodos de avaliação, estão apresentados na Tab. 2. Logo após a diluição e preparação das doses (tempo 0), o valor da motilidade diferiu (P<0,05) entre os tratamentos. Assim, a motilidade espermática observada para o P2T2 (porção 2 do ejaculado diluída no diluidor glicina-gema de ovo e resfriada a 5ºC) diferiu da observada no P1T1 (porção 1 do ejaculado diluída no diluidor MR-A® e resfriada a 17ºC). No tempo de 12 horas após o resfriamento, a motilidade foi mantida em todos os tratamentos. Nota-se que, com exceção do tratamento P2T2, o qual manteve uma motilidade similar (P>0,05) por um período de 72 horas após o resfriamento, todos os outros tratamentos apresentaram uma redução da motilidade em decorrência do tempo, notadamente após as 24 horas de armazenamento. Contudo, comparando-se os tratamentos entre si ao longo do tempo de estocagem, P1T1 apresentou a maior redução da motilidade em relação a P1T2 e P2T1 (P<0,05) já a partir das 24 horas de armazenamento, sendo que essas diferenças persistiram até as 72 horas de estocagem, quando do término do experimento. P1T2 e P2T1 mantiveram uma motilidade similar por até 36 horas de estocagem. Porém, a partir das 48 horas de armazenamento, o P1T2 apresentou motilidade inferior à do P2T1. As doses submetidas ao P2T2 mantiveram uma motilidade similar (P>0,05) ao longo de todo o período de avaliação (72 horas), sendo inclusive superior aos demais nesse período. De uma maneira geral, todos os tratamentos mantiveram uma motilidade aceitável, superior a 50%, nas primeiras 24 horas de armazenamento, independentemente da porção do ejaculado e do protocolo de resfriamento empregado.
Diante dos resultados apresentados anteriormente, parece haver uma participação muito mais efetiva da porção do ejaculado do que do protocolo de resfriamento do sêmen, na manutenção da motilidade espermática. Entretanto, a superioridade (P<0,05) do P2T2 em relação aos demais, já a partir de 24 horas de estocagem, pode refletir um efeito aditivo da porção do ejaculado e do protocolo de resfriamento, incluindo a macromolécula gema de ovo e a temperatura de estocagem a 5ºC, capaz de proteger a célula espermática, reduzir seu metabolismo e a multiplicação bacteriana. Como consequência, observa-se, nesse tratamento, o aumento da longevidade espermática.
Com relação aos valores médios do vigor espermático, o grupo P2T2 apresentou os melhores resultados, similarmente ao observado para a variável motilidade espermática, enquanto o grupo P1T1 apresentou os menores valores de vigor. Segundo Silveira e Lais (1999), somente o sêmen apresentando um vigor mínimo de três é capaz de manter sua capacidade fecundante. Nesse contexto, observa-se que, em todos os tratamentos, esse valor foi mantido por até 24 horas de estocagem.
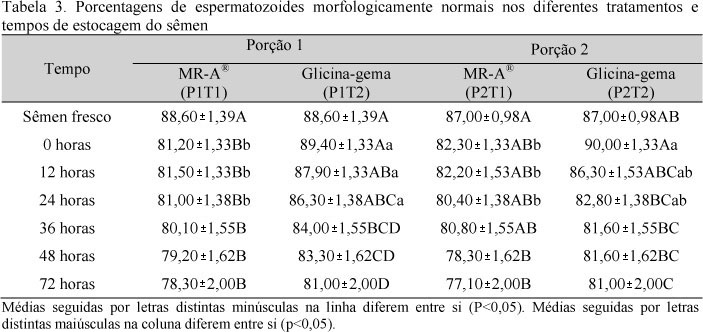
Os dados referentes às porcentagens de espermatozoides morfologicamente normais para o sêmen a fresco e nos diferentes tempos de armazenamento, entre os quatro tratamentos utilizados, estão apresentados na Tab. 3. A porção do ejaculado não influenciou (P>0,05) a porcentagem de células normais no sêmen fresco. Adicionalmente, as porcentagens médias de células normais nos diferentes períodos de tempo, considerando-se os quatro tratamentos, foram de aproximadamente 80%, como recomendado por Shipley (1999) e Johnson et al. (2000).
O sêmen diluído no diluidor glicina-gema de ovo apresentou as maiores porcentagens de espermatozoides normais logo após a diluição (0 horas), em relação ao diluído no diluidor MR-A® no mesmo tempo. Observa-se, ainda, que, nos períodos de 12 e 24 horas de armazenamento, houve uma superioridade da porção 1, diluída no diluidor glicina-gema de ovo, em relação as porções 1 e 2, diluídas em MR-A®. Entretanto, a partir das 36 horas de resfriamento, não se verificou efeito do protocolo de resfriamento do sêmen (P>0,05) sobre o percentual de células normais. Em geral, observa-se redução significativa (P<0,05) das porcentagens de células normais em todos os tratamentos, ao longo do período de armazenamento.
Com relação aos defeitos de cabeça encontrados, os percentuais médios para todos os tratamentos, nos diferentes tempos de estocagem, foram sempre inferiores a 5%, sendo esse o valor máximo aceitável em uma amostra, para que não ocorra redução da fertilidade (Manual..., 1998).
Não se observou diferença (P>0,05) entre os tratamentos, no que diz respeito aos defeitos de peça intermediária e gota citoplasmática proximal, no sêmen a fresco, estando os valores observados dentro dos limites aceitáveis para estas patologias.
Com relação aos defeitos de cauda, não se observou diferença entre as porções do ejaculado (P>0,05), no sêmen a fresco. Após a diluição (0 hora), verificou-se diferença (P<0,05) entre os tratamentos, sendo que as células espermáticas diluídas no diluidor MR-A®, independentemente da porção do ejaculado a qual pertenciam, apresentaram maiores percentuais de defeitos de cauda, comparadas àquelas diluídas no diluidor glicina-gema de ovo. Com exceção das 36 horas, observou-se diferença (P<0,05) entre os tratamentos nos diferentes tempos de estocagem avaliados (12, 24, 48 e 72 horas). Entretanto, não foi observada influência (P>0,05) do tempo de estocagem sobre o percentual de células espermáticas apresentando defeitos de cauda. De modo geral, o protocolo de resfriamento do sêmen, incluindo o diluidor glicina-gema de ovo e a temperatura de 5ºC (P1T2 e P2T2), conferiu melhor proteção às células espermáticas. Os valores verificados no presente experimento, para os defeitos de cauda, estiveram sempre próximos ao limiar máximo de 10% recomendado pelo CBRA (Manual..., 1998).
Com relação aos defeitos de acrossoma, observou-se que, de maneira geral, as células espermáticas diluídas no diluidor glicina-gema de ovo e armazenadas a 5ºC, independentemente da porção do ejaculado a qual pertenciam, apresentaram as maiores porcentagens de lesões, quando comparadas às diluídas em MR-A®, embora o valor máximo verificado para essa patologia sempre estivesse dentro do valor de 5% recomendado pela literatura (Manual..., 1998). Essa diferença possivelmente se deve à menor temperatura de estocagem associada ao diluidor glicina-gema de ovo (5ºC), em comparação à temperatura associada ao diluidor MR-A® (17ºC), o que impõe um desafio maior às membranas das células espermáticas, especialmente às dos varrões.
Quanto aos percentuais de gotas citoplasmáticas distais observados nos diferentes tratamentos e tempos de estocagem, verificou-se que, no sêmen a fresco, a porção 1 do ejaculado apresentou valores superiores aos da porção 2, independentemente do protocolo de resfriamento do sêmen. Este achado está de acordo com o relatado por Furtado et al. (2006), que citaram que as porções iniciais do ejaculado apresentam um maior percentual de gotas citoplasmáticas distais quando comparadas ao restante do ejaculado. Contudo, em nenhum momento de avaliação os valores observados para essa patologia foram superiores ao limite recomendado de 15% (Johnson et al., 2000).
Considerando-se a variável motilidade espermática, os dados encontrados no presente experimento contrastam com os observados por Peña et al. (2003) e Rodríguez-Martínez et al. (2005), que verificaram maior resistência dos espermatozoides oriundos da P1 aos procedimentos de diluição e resfriamento, comparados aos presentes no restante do ejaculado. Contudo, levando-se em consideração os resultados obtidos nas análises morfológicas, não se observou diferença (P>0,05) entre as porções do ejaculado estudadas com relação ao efeito da diluição e/ou do resfriamento.
De acordo com os dados positivos verificados para sêmen diluído no diluidor glicina-gema de ovo e considerando-se os benefícios que o resfriamento e o transporte do sêmen à temperatura de 5ºC podem trazer, em decorrência da redução do metabolismo espermático, da inibição do crescimento bacteriano e, consequentemente, de um maior tempo de armazenamento, novos experimentos nessa linha de pesquisa são justificados.
CONCLUSÕES
A utilização da P1, por meio de coleta fracionada do ejaculado, possibilita o surgimento de novas propostas no que diz respeito ao transporte do sêmen suíno, dada sua alta concentração e baixo volume, enquanto a P2 do ejaculado pode ser utilizada eficientemente dentro da própria granja. Contudo, testes de fertilidade in vivo deveriam ser realizados com o objetivo de avaliar o real potencial fertilizante dos espermatozoides, considerando-se as porções do ejaculado e os protocolos de resfriamento do sêmen.
AGRADECIMENTOS
Os autores agradecem ao proprietário da empresa DB-DanBred do Brasil, localizada no município de Patos de Minas, Minas Gerais, pela cessão dos animais e das instalações, onde foi realizado este experimento.
Recebido em 23 de julho de 2010
Aceito em 4 de julho de 2011
E-mail: silvafilhojm@gmail.com
- FLOWERS, W. Management of boars for efficient semen production. J. Reprod. Fertil., v.52, suppl., p.67-78, 1997.
- FOOTE, R.H. Within-herd use of boar semen at 5ºC, with a note on electronic monitoring of oestrus. Reprod. Dom. Anim, v.37, p.61-63, 2002.
- FURTADO, C.S.; MELLAGI, A.P.G.; VARGAS, A.J. et al Aspectos relevantes na avaliação da morfologia espermática do suíno. Suinoc. Foco, v.17, p.4-5, 2006.
- GADEA, J. Review: Semen extenders used in the artificial insemination of swine. Spanish J. Agr. Res, v.1, p.17-27, 2003.
- HANCOCK, J.L. The morphology of boar spermatozoa. J. R. Microsc. Soc, v.76, p.84-97, 1957.
- HANCOCK, J. L.; HOWELL, G.J.R. The collection of boar semen. Vet. Rec, v.71, p.664-665, 1959.
- JOHNSON, L.A.; WEITZE, K.F.; FISER P. et al Storage of boar semen. Anim. Reprod. Sci., v.62, p.143-172, 2000.
- LEVIS, D. Liquid boar semen production: current extender technology and where do we go from here! In: INTERNATIONAL CONFERENCE ON BOAR SEMEN PRESERVATION. 4., 2000, Beltsville, Maryland USA. Proceedings.. Beltsville: Allen, 2000. p.121-128.
- MANUAL para exame andrológico e avaliação do sêmen animal. 2.ed. Belo Horizonte: CBRA, 1998. 49p.
- PEÑA, F.J.; JOHANNISSON, A.; WALLGREN, M. et al Antioxidant supplementation in vitro improves boar sperm motility and mitochondrial membrane potential after cryopreservation of different fractions of the ejaculate. Anim. Reprod. Sci., v.78, p.85-98, 2003.
- RODRÍGUEZ-MARTÍNEZ, H.; SARAVIA, F.; WALLGREN, M. et al Boar spermatozoa in the oviduct. Theriogenology, v.63, p.514-535, 2005.
- RONER, M.N.B.; SILVA FILHO, J.M.; PALHARES, M.S. et al Desenvolvimento de um sistema de resfriamento e conservação de sêmen suíno. Arq. Bras. Med. Vet. Zootec., v.58, p.78-86, 2006.
- SARAVIA, F.; WALLGREN, M.; RODRÍGUEZ-MARTÍNEZA, H. Freezing of boar semen can be simplified by handling a specific portion of the ejaculate with a shorter procedure and MiniFlatPack packaging. Anim. Reprod. Sci., v.117, p.279-287, 2010.
- SHIPLEY, C. Breeding soundness examination in the boar. Swine Health Prod, v.7, p.117- 120, 1999.
- SILVEIRA, P.R.S.; LAIS, I. Curso de inseminação artificial em suínos. Concórdia, SC: EMBRAPA Suínos e Aves, 1999. 20p.
- STATISTICAL analysis system: user's guide - SAS. Version 5. Cary, NC: SAS Institute, 1999.
Datas de Publicação
-
Publicação nesta coleção
19 Dez 2011 -
Data do Fascículo
Dez 2011
Histórico
-
Recebido
23 Jul 2010 -
Aceito
04 Jul 2011