Resumos
Descreveu-se um surto de yersiniose em uma criação de pampo Trachinotus marginatus estudado no Laboratório de Piscicultura Estuarina e Marinha da Universidade Federal do Rio Grande. A enfermidade manifestou-se por transtornos natatórios, exoftalmia com panoftalmite e pela clássica boca vermelha, nome pelo qual se denomina "enfermidade da boca vermelha" (EBV). Na necropsia, foram observados focos de hemorragia peritoneal, esplenomegalia e hepatomegalia. Microscopicamente, foi observada panoftalmite com infiltrados inflamatórios densos que afetavam quase todas as estruturas oculares. Esses infiltrados estavam constituídos por granulócitos, linfócitos, macrófagos e células granulares eosinofílicas. No exsudado, observaram-se estruturas pequenas, pouco coradas, de aspecto bacteriano Gram negativo. O estudo imuno-histoquímico, que se utilizou de um anticorpo monoclonal anti-Yersinia ruckeri, resultou positivo. Este é o primeiro surto conhecido de yersiniose em Trachinotus marginatus no Brasil.
peixe; Trachinotus marginatus; yersiniose; imuno-histoquímica
In the "Laboratório de Piscicultura Estuarina e Marinha da Universidade Federal do Rio Grande" the rearing of Trachinotus marginatus (pompano) is studied, and in one of these rearing a yersioniosis outbreak occured. The disease was manifested by swimming disturbances, exophthalmiawith panophthalmitis and the classic red mouth, (red mouth disease (RMD). The necropsies revealed focus of peritoneal hemorrhage, esplenomegalyand hepatomegaly.Microscopically a panophthalmitis with dense inflammatory infiltrates was observed, which affected almost all ocular structures. These infiltrates were constituted by granulocytes, lymphocytes, macrophages and eosinophylicgranular cells (ECG), in the exudatessmall structures less colored with Gram negative bacteria aspect were observed. The immunohistochemical, which used a monoclonal antibody anti- Yersinia ruckeri waspositive. The RMD is caused by enterobacteriaGram negative, which affects both freshwater and saltwater fish, with predominance in salmonids. This is the first known yersiniosis outbreak in Trachinotus marginatus in Brazil and it is necessary to keep this disease in mind at the moment of rearing fish of this species.
fish; Trachinotus marginatus; yersiniosis; inmunohistochemical
MEDICINA VETERINÁRIA
Yersiniose em Trachinotus marginatus (pampo). Diagnóstico histopatológico e imuno-histoquímico
Yersiniosis in Trachinotus marginatus (pampo): histopathological and immunohistochemical diagnostic
L. Romano; M.B. Tesser; L.A. Sampaio; P.C. Abreu
Universidade Federal de Rio Grande - Instituto de Oceanografia - Rio Grande, RS
RESUMO
Descreveu-se um surto de yersiniose em uma criação de pampo Trachinotus marginatus estudado no Laboratório de Piscicultura Estuarina e Marinha da Universidade Federal do Rio Grande. A enfermidade manifestou-se por transtornos natatórios, exoftalmia com panoftalmite e pela clássica boca vermelha, nome pelo qual se denomina "enfermidade da boca vermelha" (EBV). Na necropsia, foram observados focos de hemorragia peritoneal, esplenomegalia e hepatomegalia. Microscopicamente, foi observada panoftalmite com infiltrados inflamatórios densos que afetavam quase todas as estruturas oculares. Esses infiltrados estavam constituídos por granulócitos, linfócitos, macrófagos e células granulares eosinofílicas. No exsudado, observaram-se estruturas pequenas, pouco coradas, de aspecto bacteriano Gram negativo. O estudo imuno-histoquímico, que se utilizou de um anticorpo monoclonal anti-Yersinia ruckeri, resultou positivo. Este é o primeiro surto conhecido de yersiniose em Trachinotus marginatus no Brasil.
Palavras-chave: peixe, Trachinotus marginatus, yersiniose, imuno-histoquímica
ABSTRACT
In the "Laboratório de Piscicultura Estuarina e Marinha da Universidade Federal do Rio Grande" the rearing of Trachinotus marginatus (pompano) is studied, and in one of these rearing a yersioniosis outbreak occured. The disease was manifested by swimming disturbances, exophthalmiawith panophthalmitis and the classic red mouth, (red mouth disease (RMD). The necropsies revealed focus of peritoneal hemorrhage, esplenomegalyand hepatomegaly.Microscopically a panophthalmitis with dense inflammatory infiltrates was observed, which affected almost all ocular structures. These infiltrates were constituted by granulocytes, lymphocytes, macrophages and eosinophylicgranular cells (ECG), in the exudatessmall structures less colored with Gram negative bacteria aspect were observed. The immunohistochemical, which used a monoclonal antibody anti- Yersinia ruckeri waspositive. The RMD is caused by enterobacteriaGram negative, which affects both freshwater and saltwater fish, with predominance in salmonids. This is the first known yersiniosis outbreak in Trachinotus marginatus in Brazil and it is necessary to keep this disease in mind at the moment of rearing fish of this species.
Keywords: fish, Trachinotus marginatus, yersiniosis, inmunohistochemical
INTRODUÇÃO
A enterite da boca vermelha (EBV) é uma enfermidade infecciosa cujo agente etiológico é a bactéria Yersinia ruckeri. Essa enfermidade foi primeiramente descrita para salmonídeos, podendo apresentar infecções em outras espécies (McArdle e Dooley-Martin, 1985). Desde que Rucker (1966) descreveu a enfermidade em Idaho, nos EUA, vários surtos têm sido reportados em pisciculturas nos Estados Unidos, no Canadá e na Europa, resultando em grandes perdas para a salmonicultura (Rodgers, 1991a).
Atualmente, uma grande variedade de espécies de peixes, tanto de águas continentais como marinhas, são criadas em todo o mundo. De acordo com a FAO (2010), a aquicultura é uma atividade em expansão, obtendo-se taxas de crescimento ao redor de 8% ao ano. A criação de espécies do gênero Trachinotus adquiriu impulso no estado da Flórida e em outras áreas do Golfo do México pertencente aos Estados Unidos, na década de 60. O interesse por sua criação está baseado em seu rápido crescimento, bom preço e aceitação no mercado consumidor. No Brasil, a espécie alvo de estudo é o pampo Trachinotus marginatus (Sampaio et al., 2003; Chaves et al., 2006; Costa et al., 2008; Cunha et al., 2009; Okamoto et al., 2009).
A EBV é principalmente uma enfermidade da truta arco-íris, no entanto outros salmonídeos, como o salmão do Atlântico, podem apresentar a mesma doença. Ainda, tem-se descrito a infecção por essa bactéria em outras espécies, como, por exemplo, em enguias, percas, gobídeos, esturjões, linguados e carpas (Stoskopf, 1993). A EBV, não foi descrita para essa espécie, entretanto não existe razão para que os pampos não se infectem. A transmissão da enfermidade é principalmente por via horizontal, durante sua fase de desenvolvimento em água doce. A infectividade do agente pode perpetuar-se e alcançar outros hospedeiros, tais como peixe ou crustáceos silvestres. Estes vetores podem, por sua vez, transmitir o agente infeccioso para os peixes posteriormente, durante sua produção em água salgada (Rodgers, 1991a).
A fase aguda da enfermidade caracteriza-se pela alta letalidade em razão do aparecimento de septicemia. As taxas de mortalidade são proporcionalmente maiores quanto menor for a idade (tamanho) dos peixes (Rodgers, 1991b). Nos peixes adultos, o quadro manifesta-se como uma infecção crônica, e os sinais clínicos são congestão capilar e venosa do cérebro e dos vasos oculares. Lesões hemorrágicas são observadas nos órgãos internos, no músculo, no intestino e e m toda superfície corporal. A tonalidade avermelhada na boca do peixe, de onde deriva o nome dessa patologia, é um sinal observado com baixa frequência, uma vez que parece manifestar-se tardiamente, nos últimos estágios da fase crônica da enfermidade.
A mortalidade devido à EBV, na maioria dos casos, inicia-se entre o quinto e o décimo dia do contato com a bactéria. O estado sanitário dos animais também influencia, visto que o estresse pode acelerar ou tardar o surto da enfermidade (Fuhrmann et al., 1983; Avci e Bürüncüoúlu, 2005).
O objetivo deste trabalho foi relatar um surto de yersinose em Trachinotus marginatus em criação de peixes.
CASUÍSTICA
Foram estudados seis exemplares de T. marginatus oriundos da Estação Marinha de Aquacultura - FURG. Os peixes foram, involuntariamente, submetidos à luminosidade intensa com lâmpadas e tubos fluorescentes de 480nm durante 24 horas. Os animais foram anestesiados com benzocaína a 5%, e a necropsia foi realizada de acordo com Romano (1987). Foram coletados cérebro, rins, fígado, intestino, baço e coração. Os tecidos foram fixados em formol tamponado 10%. Todas as amostras foram processadas em equipamento automático Bavimed 2050, e sua inclusão feita em paraplast. Os blocos foram cortados em espessura de 3 em micrótomo Leica-M123. Os cortes foram corados com hematoxilina-eosina, PAS, tricrômio de Masson, reticulina de Gomori, Giemsa, Gram, Grocott, Fite-Faraco - modificado por Parisot e Decker - e alcian blue. As microfotografias foram obtidas por microscópio Olympus B201 com sistema PM20.
A imunodetecção foi realizada com anticorpo policlonal feito em coelhos imunizados com Y. ruckeri mortas e foi ressuspendida em Freund (CIMAE, Argentina). As lâminas histológicas foram incubadas por 20 minutos em tampão Tris com 0-3% H2O2 e, posteriormente, incubadas em soro suíno diluído em tampão fosfato (PBS) 1:5 por 30 minutos. Em seguida, foram incubadas com o anticorpo policlonal anti-Y. ruckeri diluído em PBS a 1:1500.
O segundo anticorpo foi um anti-imunoglobulina de coelho feito em suínos (Dako, Argentina) diluído em PBS 1:20. O tempo de incubação do segundo anticorpo foi de 30 minutos. Foi também utilizado um complexo peroxidase-antiperoxidase (PAP) (Dakopatts) diluído em PBS durante 30 minutos. Como cromógeno, foi utilizada a diaminobenzidina em H2O2 al 0,03%, e a intensidade da coloração foi controlada. Quando atingiu a reação esperada, ela foi parada por meio de lavagem em água corrente. Como corante de contraste, foi utilizado o verde luz.
DISCUSSÃO
Como antecedente, deve-se recordar que os peixes estiveram expostos a uma luminosidade intensa, com lâmpadas e tubos fluorescentes de 480nm, durante 24 horas, o que causou estresse luminoso. Clinicamente os animais apresentaram poucos transtornos e bons reflexos ao som. Em alguns exemplares, havia hiperpigmentação dorso-caudal e todos tinham algum grau de exoftalmia uni ou bilateral. O globo ocular apresentava hemorragias escleróticas e intraoculares e petéquias perioculares. Hemorragias na região bucal, tanto externa quanto interna, foram observadas. Não se constataram ulcerações ou qualquer outra lesão no restante do corpo. Durante a necropsia, foi observado que o peritônio visceral estava aderido aos órgãos abdominais e que havia hemorragia em toda a serosa peritoneal. O fígado apresentava hepatomegalia friável. Em três casos, apresentava esplenomegalia evidente. No tubo digestório, constatou-se a serosa congestionada, e, em alguns setores, foi observado o amolecimento da parede.
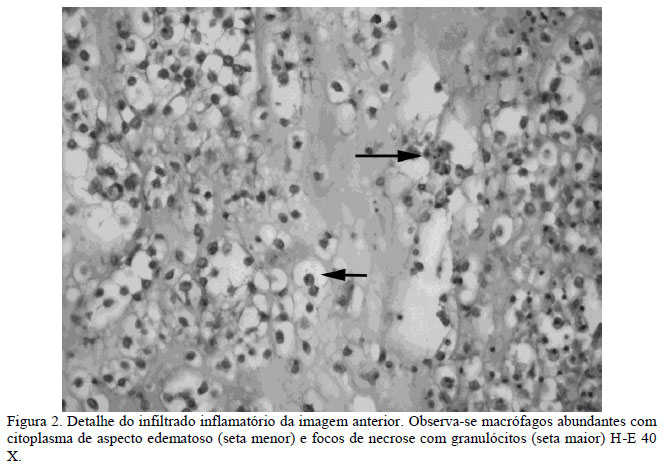
As alterações histológicas foram observadas em vários órgãos por se tratar de uma enfermidade sistêmica com alterações relacionadas com o quadro séptico bacteriano. No olho, observou-se córnea mais grossa, e a pele adjacente da conjuntiva apresentava densos infiltrados inflamatórios que se estendiam até a membrana basal (MB) epitelial. Os infiltrados estavam compostos por granulócitos, macrófagos, linfócitos e abundantes células granulares eosinofílicas (GEC); entre as células, existia exudado edematoso com pequenas estruturas bacterianas Gram negativas. Na coroide, foram observados densos infiltrados inflamatórios com hemorragia, a retina estava desprendida e edematosa, com acúmulo de material sanguíneo entre as coroides e a retina (Fig. 1 e 2).
No parênquima hepático, foram observados focos de necrose cetrolobular e infiltrados linfoides (Fig. 3). No baço, foram constatadas dilatação e congestão dos sinusoides com focos hemorrágicos e necrose. No tecido renal, observou-se pouca atividade hematopoiética e melanomacrófagos desagregados.
A imunomarcação com anticorpo policlonal contra Y. ruckeri feita no material ocular foi positiva (Fig. 4). A imuno-histoquímica é uma técnica importante para a detecção de antígenos microbianos em tecidos. A esse método podem-se somar os métodos clássicos para se obterem resultados mais rápidos e de alta sensibilidade, pois o crescimento bacteriano em meio de cultivo é lento e trabalhoso. Com o vírus, a questão é mais interessante, pois já se podem realizar diagnósticos sobre tecidos fixados sem necessariamente realizar cultivos celulares. Todavia, a possibilidade de se contar com o tecido fixado e processado permite realizar estudos retrospectivos, por exemplo, sobre novas enfermidades de cuja existência anterior não se sabia por não serem descritas ou por não contarem com o anticorpo apropriado (Jansson, 1991; Hammer, 2007; Singh, 2008).
Neste estudo, tanto pela clínica quanto pelos achados histopatológicos, a suspeita de uma yersioniose esteve sempre presente, o que foi definido pela imuno-histoquímica.
A Y. ruckeri é uma bactéria Gram negativa cuja porta de entrada é a via digestiva, gerando rapidamente septicemia com pouco ou nulo comprometimento do tubo digestório (Austin, 2003). No presente estudo, nenhum exemplar estudado apresentou lesões intestinais. A EBV é principalmente uma enfermidade de truta arco-íris criada, no entanto outras espécies podem ser infectadas e manifestar a enfermidade (Stoskopf, 1993). Neste trabalho descreveu-se, possivelmente, o primeiro surto dessa doença em T. marginatus no Brasil.
Os pampos estudados e que apresentaram EBV foram submetidos a um estresse luminoso. O excesso de luz gera imunodepressão em várias espécies de peixes (Richards et al., 2007; Karakatsouli, 2008). Os mecanismos pelos quais o excesso de luz causa a imunodepressão estão relacionados ao aumento do cortisol, que, por sua vez, inibe a produção de interleucina I, gerando falha na apresentação e uma redução na população de linfócitos (Ruchin, 2006).
Os mecanismos patogênicos dessa bactéria parecem pouco claros, no entanto a presença de ferro na bactéria parece estar associada a sua atividade hemolítica e proteolítica, sendo muito difícil que os mecanismos imunes sejam efetivos frente à Y. ruckeri (Fernández et al., 2007). O estresse intenso de qualquer etiologia favorece as infecções bacterianas em geral por uma deficiência na resposta imune específica (Raida e Buchmann, 2008 a). O surto registrado na EMA, apresentado neste trabalho, foi súbito, e a alta mortalidade não permitiu a realização de tratamento, mas sabe-se que alguns antibióticos geram bons resultados (Stoskopf, 1988). O uso desses medicamentos deve ser restringido na aquicultura, e tratamentos alternativos, como o uso de probióticos e sistemas de filtros biológicos, parecem ser úteis como preventivo de surtos dessa enfermidade (Capkin, 2009; Bomo, 2004). A solução, pelo menos parcial, para a prevenção dessa enfermidade é a utilização de vacinas sempre que o manejo da criação dos peixes for correto, sem gerar estresse ( Raida e Buchmann, 2008b; Stevenson, 1997).
Assim, confirma-se neste diagnóstico a presença de Y. ruckeri em pampos e acredita-se que é o primeiro surto diagnosticado no Brasil. No caso de essa bactéria estar disseminada nos sistemas de criação do Brasil, é possível que seja secundária a uma contaminação comum, o que reforça a necessidade de se realizarem estudos epidemiológicos para que estes gerem informações básicas, imprescindíveis para a implementação de medidas terapêuticas e profiláticas que impeçam a difusão deste microrganismo, tanto em cativeiro como no meio natural.
Este trabalho demonstra como as enfermidades constituem um desafio para os produtores e investigadores que trabalham com esses peixes, os quais devem levar em consideração a necessidade de se fazerem estudos de rotina com a EBV em peixes enfermos.
Recebido em 21 de junho de 2011
Aceito em 8 de fevereiro de 2012
E-mail: dcluis@yahoo.com
- AUSTIN, D.A.; ROBERTSON, P.A.W.; AUSTIN, B. Recovery of a new biogroup of Yersinia ruckeri from diseased rainbow trout (Oncorhynchus mykiss, Walbaum). Syst. Appl. Microbiol., v.26, p.127-131, 2003.
- AVCI, H.; BÜRÜNCÜOÚLU, S. Pathological findings in rainbow trout (Oncorhynchus mykiss Walbaum, 1792) experimentally infected with Yersinia ruckeri. Turk J. Vet. Anim. Sci., v.29, p.1321-1328, 2005.
- BOMO, A.; EKEBERG, M.D.; STEVIK, T.K. et al Retention and removal of the fish pathogenic bacterium Yersinia ruckeri in biological sand filters. J. Appl. Microbiol, v.97, p.598-608, 2004.
- CAPKIN, E.; ALTINOK, I. Effects of dietary probiotic supplementations on prevention/ treatment of yersiniosis disease. J. Appl. Microbiol, v.106, p.1147-1153, 2009.
- CHAVES, I.S.; SANTOS, R.L.; SAMPAIO, L.A.N. et al Immune adaptive response induced by Bicotylophora trachinoti (Monogenea: Diclidophoridae) infestation in pompano Trachinotus marginatus (Perciformes: Carangidae). Fish and Shellfish Immunol., v.21, p.242-250. 2006.
- COSTA, L.D.F.; MIRANDA-FILHO, K.C.; SEVERO, M.P. et al Tolerance of juvenile pompano Trachinotus marginatus to acute ammonia and nitrite exposure at different salinity levels. Aquaculture, v.285, p.270-272, 2008.
- CUNHA, V.L.; RODRIGUES, R.V.; OKAMOTO, M.H. et al Consumo de oxigênio pós-prandial de juvenis do pampo Trachinotus marginatus. Cienc. Rural, v.39, p.1257-1259, 2009.
- FAO 2010. World Review of Fisheries and Aquaculture. FOOD AND AGRICULTURE ORGANIZATION OF THE UNITED NATIONS, Rome, Italy, 2009.
- FERNÁNDEZ, L.; MÉNDEZ, J.; GUIJARRO, J.A . Molecular virulence mechanisms of the fish pathogen Yersinia ruckeri. Vet. Microbiol, v.15, p.1-10, 2007.
- FUHRMANN, H.; BOHM, K.H.; SCHLOTFELDT, H.J. An outbreak of enteric redmouth disease in West Germany. J. Fish Dis., v.6, p.309-311, 1983.
- HAMMER, A.S.; DIETZ, H.H.; HAMILTON-DUTOIT, S. Immunohistochemical detection of 3 viral infections in paraffin-embedded tissue from mink (Mustela vison): a tissue-microarray-based study. Can. J. Vet. Res, v.71, p.8-13, 2007.
- JANSSON, E.; HONGSLO, T.; LINDBERG, R. et al Detection of Renibacterium salmoninarum and Yersinia ruckeri by the peroxidase-antiperoxidase immunohistochemical technique in melanin- containing cells of fish tissues. J. Fish Dise. v.14, p.689-692, 1991.
- KARAKATSOULI, N.; PAPOUTSOGLOU, S.E.; PANOPOULOS, G. et al Effects of light spectrum on growth and stress response of rainbow trout Oncorhynchus mykiss reared under recirculating system conditions. Aquacul. Eng, v.38, p.36-42, 2008.
- MCARDLE J.F.; DOOLEY-MARTIN. C. Isolation of Yersinia ruckeri type 1 (Hagerman strain) from golsdfish Carassius auratus (L). Bull. Assoc. Fish. Pathol v.5, p.10-11, 1985.
- OKAMOTO, M.I.; TESSER, M.B.; LOUZADA, L.R. et al Benzocaína e eugenol como anestésicos para juvenis do pampo Trachinotus marginatus. Cienc. Rural, v.39, p.866-870, 2009.
- RAIDA, M.K.; BUCHMANN, K. Development of adaptive immunity in rainbow trout, Oncorhynchus mykiss (Walbaum) surviving an infection with Yersinia ruckeri. Fish Shellfish Immunol., v.25, p.533-541, 2008a.
- RAIDA, M.K.; BUCHMANN, K. Bath vaccination of rainbow trout (Oncorhynchus mykiss Walbaum) against Yersinia ruckeri: effects of temperature on protection and gene expression. Vaccine, v.26, p.1050-1062, 2008b.
- RICHARDS, S.N.; CHIPPS, S.R.; BROWN, L.M. Stress Response and Avoidance Behavior of Fishes as Influenced by High-Frequency Strobe Lights. North Am. J. Fish. Management, v.27, p.1310-1315, 2007.
- RODGERS, C.J. The usage of vaccination and antimicrobial agents for control of Yersinia ruckeri. J. Fish. Dis., v.14, p.291-301, 1991a.
- RODGERS, C.J. The control of enteric redmouth disease in fish. Maff, fish Diseases Laboratory, Weymouth, Dorset. Trouts News, v.12. p.27-30, 1991b.
- ROMANO, L.A. Estudio Histopatológico de los Peces. Documental Veter v.12, p.8-7, 1987.
- RUCHIN, A.B. Effect of light on white blood cell count in carp Cyprinus carpio. Izv. Akad. Nauk. Ser. Biol, v.5, p.634-637, 2006.
- RUCKER, R.R. Redmouth disease of rainbow trout (Salmo gairdneri). Bull. Inter. Epizoo., v.65, p.825-830, 1966.
- SAMPAIO, L.A.; TESSER, M.B.; BURKERT, D. Tolerância de juvenis do pampo Trachinotus marginatus (Teleostei, Carangidae) ao choque agudo de salinidade em laboratório. Cienc. Rural, v.33, p.757-761, 2003.
- SINGH, A.; WEISSENBÖCK, H.; HESS, M. Histomonas meleagridis: immunohistochemical localization of parasitic cells in formalin-fixed, paraffin-embedded tissue sections of experimentally infected turkeys demonstrates the wide spread of the parasite in its host. Exp. Parasitol, v.118, p.505-513, 2008.
- STEVENSON, R.M,. Immunization with bacterial antigens: yersiniosis. Dev. Biol. Stand., v.90, p.117-24, 1997.
- STOSKOPF, M.K. Fish Chemotherapeutics. Vet. Clin. North Am., v.18, p.329-346, 1988.
- STOSKOPF, M.K. (Ed.) Fish Medicine. England: Saunders, 1993. 882p.
Datas de Publicação
-
Publicação nesta coleção
31 Ago 2012 -
Data do Fascículo
Ago 2012
Histórico
-
Recebido
21 Jun 2011 -
Aceito
08 Fev 2012