Resumos
Identificou-se o efeito das aflatoxinas (AFs) sobre o gene p53 de frangos de corte, de linhagem comercial, separados em: grupo experimental, tratado (GT) com ração comercial contendo 2,8ppm de AFs totais durante 21 dias consecutivos, e grupo-controle (GC), sem exposição às AFs. Macroscopicamente, as alterações caracterizaram-se por hepatomegalia e aspecto pálido-amarelado com alguns focos hemorrágicos e, histologicamente, por desarranjo trabecular, pleomorfismo hepatocítico com cariomegalia, degeneração vacuolar intracitoplasmática, necrose com infiltração linfocítica e hiperplasia de ductos biliares. A PCR com os primers GSPT53c-1 com base no gene candidato a p53 (GenBank XM_424937.2) gerou um produto de aproximadamente 350 pares de base. O amplicon sequenciado a partir do DNA dos frangos do GT não apresentou mutação ou deleção, assim como padrão de bandas do PCR-RFLP não foi distinto entre ambos os grupos experimentais e a sequência depositada no banco de genes. Os resultados sugerem que não ocorreu transversão devido à exposição às AFs no fragmento amplificado. Conclui-se que a PCR-RFLP e o sequenciamento do produto da PCR não são ferramentas apropriadas para diagnóstico da exposição de frangos às AFs nas condições experimentais empregadas.
frango de corte; aflatoxinas; gene p53; PCR-RFLP
To identify the effects of aflatoxins (AFs), Cobb lineage poultry were separated in an experimental group in which they were treated with commercial ration containing 2.8ppm of total AFs during 21 days (TG) and a control group without AFs exposure (CG). In the liver of poultries exposed to AFs, alterations were microscopically observed, which were characterized by hepatomegaly, a pale yellowish aspect with some hemorrhagic spots, and histologically a trabecullar disarranging pleomorphic hepatocytes with cariomegaly, intracytoplasmatic vacuolar degeneration, necrosis, lymphocytic infiltration and hyperplasia of biliary ducts. The PCR with GSPT53c-1 primers based on p53 candidate gen (GenBank XM_424937.2) generated a product of approximately 350 base pairs. The sequenced amplicon obtained from the DNA of treated poultry did not display any mutation or deletion, and the PCR- RFLP bands patterns were also not distinct in both experimental groups. The results indicated that transversion did not occur in the fragment amplified due to AFs exposure. As a consequence of results obtained with p53 gene (NM_205264.1) we concluded that PCR-RFLP and sequencing of PCR product are not appropriate diagnostic tools for the detection of poultry exposure to AFs, at least in the experimental conditions performed.
broiler; aflatoxins; p53 gen; PCR-RFLP
ZOOTECNIA E TECNOLOGIA E INSPEÇÃO DE PRODUTOS DE ORIGEM ANIMAL ANIMAL SCIENCE AND TECHNOLOGY AND INSPECTION OF ANIMAL PRODUCTS
Investigação do gene p53 de frangos expostos às aflatoxinas
Investigation of p53 gene in poultries exposed to aflatoxins
A.C.F.G. CruzI; C.R.M. MadrugaI; C.A. MallmannII; E.L.T. MoreiraI; M.B.B. BoturaI; G.D.S. SilvaI; M.J.M. BatatinhaI,* * Autor para correspondência ( corresponding author), E-mail: mjmb@ufba.br
IEscola de Medicina Veterinária ‒ Universidade Federal da Bahia ‒ Salvador, BA
IIUniversidade Federal de Santa Maria ‒ Santa Maria, RS
RESUMO
Identificou-se o efeito das aflatoxinas (AFs) sobre o gene p53 de frangos de corte, de linhagem comercial, separados em: grupo experimental, tratado (GT) com ração comercial contendo 2,8ppm de AFs totais durante 21 dias consecutivos, e grupo-controle (GC), sem exposição às AFs. Macroscopicamente, as alterações caracterizaram-se por hepatomegalia e aspecto pálido-amarelado com alguns focos hemorrágicos e, histologicamente, por desarranjo trabecular, pleomorfismo hepatocítico com cariomegalia, degeneração vacuolar intracitoplasmática, necrose com infiltração linfocítica e hiperplasia de ductos biliares. A PCR com os primers GSPT53c-1 com base no gene candidato a p53 (GenBank XM_424937.2) gerou um produto de aproximadamente 350 pares de base. O amplicon sequenciado a partir do DNA dos frangos do GT não apresentou mutação ou deleção, assim como padrão de bandas do PCR-RFLP não foi distinto entre ambos os grupos experimentais e a sequência depositada no banco de genes. Os resultados sugerem que não ocorreu transversão devido à exposição às AFs no fragmento amplificado. Conclui-se que a PCR-RFLP e o sequenciamento do produto da PCR não são ferramentas apropriadas para diagnóstico da exposição de frangos às AFs nas condições experimentais empregadas.
Palavras-chave: frango de corte, aflatoxinas, gene p53, PCR-RFLP
ABSTRACT
To identify the effects of aflatoxins (AFs), Cobb lineage poultry were separated in an experimental group in which they were treated with commercial ration containing 2.8ppm of total AFs during 21 days (TG) and a control group without AFs exposure (CG). In the liver of poultries exposed to AFs, alterations were microscopically observed, which were characterized by hepatomegaly, a pale yellowish aspect with some hemorrhagic spots, and histologically a trabecullar disarranging pleomorphic hepatocytes with cariomegaly, intracytoplasmatic vacuolar degeneration, necrosis, lymphocytic infiltration and hyperplasia of biliary ducts. The PCR with GSPT53c-1 primers based on p53 candidate gen (GenBank XM_424937.2) generated a product of approximately 350 base pairs. The sequenced amplicon obtained from the DNA of treated poultry did not display any mutation or deletion, and the PCR- RFLP bands patterns were also not distinct in both experimental groups. The results indicated that transversion did not occur in the fragment amplified due to AFs exposure. As a consequence of results obtained with p53 gene (NM_205264.1) we concluded that PCR-RFLP and sequencing of PCR product are not appropriate diagnostic tools for the detection of poultry exposure to AFs, at least in the experimental conditions performed.
Keywords: broiler, aflatoxins, p53 gen, PCR-RFLP
INTRODUÇÃO
Os cereais são componentes importantes na produção de concentrados para aves, e estes têm maior probabilidade de contaminações por micotoxinas como as aflatoxinas (AFs) em regiões com clima quente e úmido, comum a várias regiões tropicais do Brasil. A presença de AFs no milho e seus derivados causa problemas para a saúde humana e a animal (Cast, 2003) e, consequentemente, econômicos, devido aos custos de tratamento da doença e potencial causa de barreira comercial aos produtos avícolas, porque há transferência das toxinas e de seus metabólitos para carne, vísceras, ovos e derivados (Bahrami, 2004). O estabelecimento de barreira ao comércio exterior teria relevância para o PIB nacional, porque o Brasil é o terceiro maior produtor mundial de carne de frango e líder no mercado internacional de exportação (União..., 2010).
Entre as AFs produzidas por algumas cepas de fungos do gênero Aspergyllus, especialmente A. flavus, A. parasiticus, A nomius e A. pseudotamarii (Batatinha et al., 2008), a AFB1 é a mais tóxica e pertence ao grupo toxicológico I, o que a caracteriza como carcinogênica segundo a Agência Internacional para Pesquisa em Câncer (International Agency for Research on Câncer-IARC). Os efeitos tóxicos da AFB1 são decorrentes da ação do seu metabólito AFB1-8,9 epóxido. Este composto é altamente reativo e interage com macromoléculas nucleofílicas, como desoxirribonucleico (DNA), ribonucleico (RNA) e proteínas, determinando a formação de adutos, os quais representam a alteração bioquímica primária produzida pelas AFs. A ligação AFB1 8,9 epóxido com bases do DNA como a guanina resulta na formação do aduto aflatoxina-N7-guanina (AFB1-N7-Gua), o qual está relacionado às ações carcinogênicas e mutagênicas das AFs (Chan et al., 2003).
A aflatoxicose crônica é mais frequentemente observada em animais, e os principais efeitos tóxicos são lesões hepáticas, imunossupressão, carcinogênese, mutagênese e teratogênese (Hollinger e Ekperigin, 1999). Isso ocorre porque a proteína codificada pelo gene p53 tem função crucial na regulação do ciclo celular e atua como supressora de tumor prevenindo mutação no genoma (Chumakov, 2000). Os sinais clínicos predominantes em frangos intoxicados por AFs estão relacionados à queda do desempenho produtivo, tais como redução da ingestão de alimentos e do ganho de peso (Franciscato et al., 2006). Embora frangos de corte apresentem sinais clínicos de aflatoxicose (Mallmann et al., 2007), as avaliações anátomo-histopatológicas objetivando identificar e correlacionar as lesões hepáticas e as mutações do gene p53 em aves ainda não foram relatadas. Essa avaliação é importante porque a suscetibilidade das aves às AFs é variável de acordo com espécie, raça, idade, sexo, condição nutricional, saúde e quantidade e tempo de exposição a essas toxinas (Shi et al., 2006).
A ação da AFB1 sobre o códon 249 do gene p53 humano causando mutação já está bem estabelecida, entretanto, nos genes ortólogos de aves, ainda não foi identificada transversão nesse códon (Duflot et al., 1994) ou em outros. A detecção de AFs nas vísceras, especialmente fígado dos animais com sugestão de aflatoxicose, é realizada por técnicas físico-químicas, cromatográficas, bioensaios e imunoensaios (Rodrigues-Amaya, 1989), mas tendo em vista o potencial mutagênico das AFs associado à transversão de uma guanina por timina, o qual ainda não foi estabelecido em aves. As técnicas de PCR-RFLP e de sequenciamento tornam-se apropriadas para essa averiguação e possível aplicação para diagnóstico de aflatoxicose, o que justificou a realização deste trabalho, o qual teve como objetivo investigar o gene p53 de frangos expostos ou não a dietas contendo AFs.
MATERIAL E MÉTODOS
Duzentos frangos de corte, linhagem Cobb, foram separados em dois grupos experimentais. Um dos grupos foi tratado com ração comercial contendo 2,8ppm de AFs totais durante 21 dias consecutivos (GT), enquanto o outro grupo recebeu apenas a ração (GC). Após esse período, foi realizada necropsia assim como exame macroscópico do fígado com subsequente coleta de fragmentos para análise histopatológica e para extração de DNA. Para o exame histológico, 25 amostras de cada grupo (GT e GC) foram selecionadas aleatoriamente e fixadas em formol neutro tamponado a 10%, enquanto para a extração do DNA, todas as amostras de fígado foram armazenadas à temperatura de -80ºC. O processamento histológico de fragmentos de fígado em inclusão em parafina foi realizado de acordo com os métodos convencionais (Prophet et al., 1992). Secções de 4,0µm de espessura foram coradas pela técnica de hematoxilina-eosina (Luna, 1968) para análise posterior. As amostras de fígado com aproximadamente 100ng foram maceradas, e o DNA foi extraído com kit comercial (PureLink Genomic DNA Kits - INVITROGEN), de acordo com as recomendações do fabricante.
As amostras de DNA foram utilizadas nas reações em cadeia da polimerase (PCRs). Essas reações foram realizadas com diferentes pares de primers desenhados com base na sequência do gene p53 de Gallus gallus existente no GenBank, XM_424937.2 e NM_205264.1 (Tab. 1).
A PCR com os primers SFTP53 foi realizada sob as seguintes condições: 10pM de cada primer, 2,5 unidades de Taq polimerase, 2,5mM de cada dNTP, 2,5mM de MgCl2 e 100ng do DNA extraído do fígado das aves. A termociclagem foi realizada com desnaturação inicial a 95oC por três minutos, seguida de 40 ciclos de 95oC por 30 segundos, 30 segundos a 55oC, e um minuto a 72oC, mais cinco minutos a 72ºC para extensão final. As PCRs com os primers GMTP53, GStTP53, SFTP53, PTP53, UGGP53. 1 e UGGP53. 2 foram executadas com vários protocolos. A PCR com os primers GSPT53c-1 foi executada com máster mix (Promega) (12,5µL), 5pmol de cada primer, 3,5µL de H20 e DNA (5ng). A detecção dos amplicons foi efetuada após eletroforese em agarose a 2%, coloração com SYBR®Gold (INVITROGEN) e com o marcador de pares de base 1Kb ladder (INVITROGEN). A visualização dos resultados foi efetuada em um transiluminador com luz ultravioleta e fotodocumentado (Bio-Doc Analyser). Para a realização da PCR-RFLP, o amplicon purificado da PCR foi digerido com a enzima de restrição HaeIII, de acordo com o protocolo indicado pelo fabricante (BIOLABS).
Os produtos da PCR selecionados foram extraídos do gel agarose e purificados com o Kit High Pure PCR Product Purification (QIAGEN®), de acordo com o protocolo descrito pelo fabricante. O material purificado foi enviado diretamente para sequenciamento ou clonado em vetor P GEM T Easy (PROMEGA®), para posterior sequenciamento.
RESULTADOS
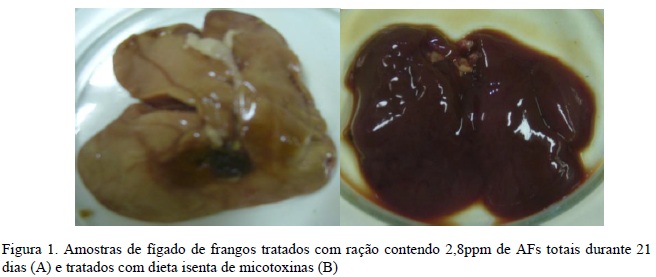
As amostras de fígado dos animais tratados com ração contendo AFs (GT) apresentaram aumento de volume com lobos bem definidos, aspecto difusamente pálido-amarelado e focos hemorrágicos na superfície parietal (Fig. 1A), diferindo das amostras do grupo- controle (GC), que não evidenciaram alterações macroscopicamente visíveis (Fig. 1B).
A análise microscópica das amostras selecionadas dos animais tratados com ração contaminada com AFs revelou, de modo geral, desarranjo trabecular e pleomorfismo hepatocítico com cariomegalia; hepatócitos dispostos aleatoriamente mostraram-se com degeneração vacuolar intracitoplasmática (Fig. 2A) e, em regiões periportais e periacinares, em necrose acompanhada de infiltração de mononucleares (Fig. 2B), muitas vezes em arranjo nodular. Os ductos biliares apresentaram hiperplasia de células epiteliais, as quais possuíam citoplasma claro e núcleos vesiculosos (Fig. 2C). Havia, em poucos casos, pericolangite linfocitária (Fig. 2D), moderado espessamento fibroso da parede de veias terminais hepáticas e em áreas portais. Ainda se pode observar, em alguns animais, moderada fibroplasia perilobular e áreas focais de hemorragia e congestão vascular. As alterações hepáticas descritas não foram observadas nas aves do grupo-controle.
A PCR com os primers GSPT53c-1 desenhados com base na sequência candidata a p53 (XM_424937.2) produziu um produto de 350pb (Fig. 3). As sequências obtidas identificaram códons com sequências semelhantes ao 249 humano e mostraram que a enzima HaeIII atua em GGCC. A PCR-RFLP apresentou o mesmo padrão de bandas tanto no grupo intoxicado como no não intoxicado, o que sugere que não houve mutação nas sequências reconhecidas por essa enzima de restrição (Fig. 4). Os três códons do fragmento amplificado e sequenciado do gene candidato da p53 de Gallus gallus que potencialmente possuíam sequências para transversão não apresentaram diferenças com relação ao mesmo fragmento do grupo-controle ou sequência depositada no banco de genes. A PCR com os primers SFTP53 produziu um produto de aproximadamente 2Kb. Entretanto, o sequenciamento desse fragmento amplificado não revelou identidade com o gene da p53 (NM 205264.1). Todas as demais PCRs com os primers desenhados com base na sequência desse gene (GMTP53, GStTP53, SFTP53, PTP53, UGGP53. 1, UGGP53. 2) produziram múltiplos amplicons com produtos com número de pares de base diferentes do esperado, os quais, quando sequenciados, não apresentaram homologia ao gene da p53.
DISCUSSÃO
O tratamento dos frangos com AFs produziu alterações hepáticas idênticas às descritas em outras espécies animais (Batatinha et al., 2008) e semelhantes às encontradas nos frangos tratados com dietas contaminadas com 1ppm (Denli et al., 2009) ou com diversos níveis de AFB1 (0,05; 0,350 e 2,450ppm), durante 42 dias (Delbianchi et al., 2005). Também há semelhança com as alterações hepáticas identificadas em pintos de um dia de idade, alimentados com ração contaminada com 3ppm de AFs (B1 + B2 + G1 + G2) por um período de 42 dias (Giacomini et al., 2006). Fígados de codornas expostas a variáveis níveis de AFs (0,1ppm, 2ppm, 1 a 4mg/kgPV) e a diferentes períodos de tempo (168 e 20 dias) (Oliveira et al., 2004; Cardozo et al., 2008) também apresentaram lesões similares. As pequenas diferenças de intensidade e natureza das lesões hepáticas entre os frangos expostos às AFs podem ser justificadas pelas variações individuais, decorrentes das diferentes quantidades de toxina ingerida ou das diferenças de capacidade de redução da toxicidade pelo processo de detoxificação hepática entre as espécies animais (Shi et al., 2006).
A ausência de formação tumoral no fígado dos frangos deste experimento possivelmente seja decorrente do período curto de exposição, bem como pelo fato de estes não estarem expostos a fatores sinérgicos, como a infecção concomitante com vírus carcinogênico, conforme ocorreu no experimento com patos que apresentaram tumor hepático após 27 meses de exposição às AFs e de infecção com vírus da hepatite B (Cova et al., 1990).
A ausência de mutação no fragmento amplificado do gene (XM_424937.2) analisado pode não estar associada ao fato da não ocorrência de tumor no grupo experimental, porque a mutação no gene p53 pode ser detectada precocemente ao surgimento do tumor (Habib et al., 2006), uma vez que a AFB1 é um agente carcinogênico direto, cuja ação decorre da ligação do seu metabólito AFB1-8,9 epóxido com bases do DNA como a guanina, resultando na formação do aduto aflatoxina-N7- guanina (AFB1-N7-Gua) (Chan et al., 2003). No frango, como em várias outras espécies animais, a mutação causada pelas AFs não ocorrerá no códon 249 como no gene p53 de humanos, pois, no códon 249 do gene candidato a p53 de Gallus gallus, não há sequência de nucleotídeos, assim como nos códons adjacentes que proporcionem a sequência GGCC, e por isso tal mutação não tem sido encontrada nos ortólogos desse gene em outras espécies (Duflot et al., 1994). A investigação de ocorrência de transversão nos códons 118, 123, 137 do fragmento amplificado do gene candidato a p53 (XM_424937.2- GeneBank) que possuem sequências similares ao códon 249 de humanos se justifica, porque há possibilidade de que essa ocorra em outros códons de genes ortólogos, pois, nos primatas não humanos, ocorre no códon 175 (Fujimoto et al., 1992); nos ratos, nos códons 247 e 280 (Lee et al., 1998); nos esquilos, no códon 176 (Rivkna et al., 1996); em tupaias, nos códons 13, 78 e 275 (Park et al., 2000); e em linhagens celulares (fibroblastos), nos códons 244 e 245 (Paget et al., 2008). Além disso, nas aves com doença de Marek, foram detectados diferentes pontos, principalmente de deleção, o que sugere que estas posições sejam potenciais para mutação (Takagi et al., 2006).
A necessidade de elucidar a ocorrência e o padrão da mutação do gene p53 em frangos expostos às AFs para obtenção de maiores conhecimentos sobre a especificidade desta mutação (Shen e Ong, 1996) nessa espécie animal é relevante devido à importância econômica dessa cadeia produtiva. Por essa razão, a não constatação de mutação nos códons analisados da sequência do gene candidato da p53 de Gallus gallus tem significado para o melhor entendimento dos mecanismos de biotransformação das AFs e de sua toxicidade (Gourama e Bullerman, 1995).
Resultados com primers com base gene NM 205264.1, apesar das várias tentativas com as diferentes condições de reações, não foram os esperados e não possibilitaram avaliações de mutação. Esse problema poderia estar associado a genes que codificam proteínas da família p53 e que possuem elevada homologia, como ocorre em mamíferos que têm dois membros adicionais p73 e p51. No futuro, quando o genoma do Gallus gallus for completamente estabelecido, será possível obter primers que amplifiquem fragmentos específicos dos genes que codifiquem as proteínas da família p53.
CONCLUSÕES
Não havendo conhecimento da ocorrência e da frequência de mutação do gene p53 de frangos expostos às AFs, as técnicas moleculares como PCR-RFLP e de sequenciamento do gene p53 não constituem ferramentas apropriadas para diagnóstico precoce da aflatoxicose nas condições experimentais executadas.
AGRADECIMENTOS
Ao CNPq e à FAPESB, pelo financiamento da pesquisa.
Recebido em 25 de agosto de 2011
Aceito em 20 de julho de 2012
- BAHRAMI, A.M. Distribution of Aflatoxin B1 from Poultry Feed to Different Tissue of Broilers In Tropical Weather. In: 11th International Conference of the Association of Institutions for Tropical Veterinary Medicine and 16th Veterinary Association Malaysia Congress, Anais... Petaling Jaya. Malaysa, 23-27 August 2004, p.244-246.
- BATATINHA, M.J.M; SIMAS, M.M.S.; GORNIAK, S.L. Micotoxicoses. In: SPINOSA, H.S.; GORNIAK, S.L.; PALERMO-NETO, J. Toxicologia Aplicada à Medicina Veterinária São Paulo: Manole, 2008. p.497-509.
- CARDOZO, S.V.; TEIXEIRA FILHO, W.L.; KRUGER, C.D. et al Alterações histopatológicas em codornas japonesas (Coturnix japonica) intoxicadas experimentalmente com diferentes doses de aflatoxina. Rev. Ciênc. da Vida, v.28, suplemento, p.16-18, 2008.
- CAST. Mycotoxins: risks in plant, animal and human systems. Council of Agricultural Science and Technology Ames: Task Force Report. n.139, 2003. 199p.
- CHAN, K.T.; HSIENTANG HSIEH, D.P.; LUNG, M.L. In vitro aflatoxin B1-induced p53 mutations. Cancer Letters, v.199, p.1-7, 2003.
- CHUMAKOV, P.M. Function of the p53 gene: choice between life and death. Biochemistry, v.65, p.28-40, 2000.
- COVA, L.; WILD, C.P.; MEHROTRA, R. et al Contribution of Aflatoxin B1 and Hepatitis B Virus Infection in the Induction of Liver Tumors in Ducks. Cancer Rese, v.50, p.2156-2163, 1990.
- DENLI, M.; BLANDON, J.C.; GUYNOT, M.E. et al Effects of dietary AflaDetox on performance, serum biochemistry, histopathological changes, and aflatoxin residues in broilers exposed to aflatoxin B1. Poult. Scie., v.88, p.14441451, 2009.
- DelBIANCHI, M.; OLIVEIRA, C.A.F.; ALBUQUERQUE, R. et al Effects of Prolonged Oral Administration of Aflatoxin B1 and Fumonisin B1 in Broiler Chickens. Poult. Scie., v.84, p.1835-1840, 2005.
- DUFLOT, A.; HOLLSTEIN, M.; MEHROTRA, R. et al Absence of p53 mutation at codn 249 in duck hepatocellular carcinomas from the high incidence area of Qidong (China). Carcinogenesis. v.15, p.1353-1357, 1994.
- FRANCISCATO, C.; LOPES, S.T.D.A.; SANTURIO, J.M. et al. Concentrações séricas de minerais e funções hepática e renal de frangos intoxicados com aflatoxina e tratados com montmorilonita sódica. Pesq. Agrop. Bras., v.41, p.1573-1577, 2006.
- FUJIMOTO, Y.; HAMPTON, L.L; LUO, L.D. et al. Low Frequency of p53 Gene Mutation in Tumors Induced by Aflatoxin Nonhuman Primates. Cancer Res., v.52, p.1044-1046, 1992.
- GIACOMINI, L.; FICK, F.A.; DILKIN, P. et al Desempenho e plumagem de frangos de corte intoxicados por aflatoxinas. Cienc. Rural, v.36, p.234-239, 2006.
- GOURAMA, H.; BULLERMAN, L.B. Aspergillus flavus and Aspergillus parasiticus: aflatoxigenic fungi of concern in foods and feds: a review. J. Food Prot v.58, p.1395-1404, 1995.
- HABIB, S.; DAID, B.S.; AHMED, T. et al Novel adenine adducts N7-guanine-AFB1 adducts, and p53 mutations in patients with shistosomiasis and aflatoxin exposure. Canc. Detec. Prev., v.30, p.491-498, 2006.
- HOLLINGER, K.; EKPERIGIN, H.E. Mycotoxicosis in food producing animals. Vet. Clin. North Am. Food anim. Pract., v.15, p.133-165, 1999.
- LEE, C.C.; LIU, J.Y.; LIN, J.K. et al p53 point mutation enhanced bya hepatic regeneration in aflatoxin B1- induced rat liver tumors and preneoplastic lesions. Canc. Letters. v.125, p.1-7, 1998.
- LUNA, L.G. Manual of histologic sataining methods of the Armed Forces Institute of Pathology 3nd ed. New York: Mac Graw Hill, 1968. p.258.
- MALLMANN, C.A.; DILKIN, P.; RAUBER, R.H. et al Desempenho produtivo de frangos de corte intoxicados com diferentes concentrações de aflatoxinas na dieta. In: Congreso Latinoamericano de Avicultura, Porto Alegre, WPSA Proceedings, 25-28 setembro 2007, p.267-268.
- OLIVEIRA, C.A.F.; BUTKEIRAITIS, P.; ROSMANINHO, J.F. et al Alterações hepáticas em codornas japonesas submetidas a intoxicação prolongada por aflatoxina B1 Cienc. Rural, v.34, p.213-217, 2004.
- PAGET, V.; SICHEL, F.; GARON, D. et al Aflatoxin B1-induced TP53 mutational pattern in normal human cells using the FASAY (Functional Analysis of Separated Alleles in Yeast). Mutation Res., v.656, p.55-61, 2008.
- PARK, U.S.; SU, J.J.; BAN, K.C. et al Mutations in the p53 tumor supresor gene in three shrew hepatocellular carcinoma associated with hepatitis B virus infection and intake of aflatoxin B1 Gene, v.251, p.73-80, 2000.
- PROPHET, E.B.; MILLS, B.; ARRINGTON, J.B. AFIP Laboratory Methods in Histotechnology. Am. Reg. Pathol., p.278, 1992.
- RIVKINA, M.B.; CULLEN, J.M.; ROBINSON, W.S. et al State of the p53 Gene in Hepatocellular Carcinomas of Ground Squirrels and Woodchucks with Past and Ongoing Infection with Hepadnaviruses. Canc. Research., v.54, p.5430-5437, 1994.
- RODRIGUES-AMAYA, D.B. Técnicas analíticas para micotoxinas. In: ENCONTRO Nacional de analistas de Alimentos, 4., 1989, Belo Horizonte. Anais.. Belo Horizonte: Sociedade Brasileira de Analista de Alimentos, 1989, p.245-247.
- SHEN, H.M.; ONG, C.N. Mutations of the p53 tumor suppressor gene and ras oncogenes in aflatoxin hepatocarcinogenesis. Mutation Rese, v.366, p.23-44, 1996.
- SHI, Y.H.; XU, Z.R.; FENG, J.L. et al Efficacy of modified montmorillonite nanocomposite to reduce the toxicity of aflatoxin in broiler chicks. Anim. Feed Scie. Technol., v.129, p.138-148, 2006.
- SOUSSI, T.; BEGUE, A.; KRESS, M. et al Nucleotide sequence of a cDNA encoding the chicken p53 nuclear oncoprotein. Nucleic Acids Res., v.16, p.11383, 1988.
- TAKAGI, M.; OHASHI, K.; MORIMURA, T. et al The presence of the p53 transcripts with truncated open reading frames in Marec's disease tumor-derived cell linnes. Leukemia Res., v.30, p.987-992, 2006.
- UNIÃO Brasileira de Avicultura - UBABEF. Relatório Anual 2010. 31p. Disponível em: <http://www.brazilianchicken.com.br/publicacoes/relatorio-anual-2010.pdf>. Acessado em: 05 abr 2011.
Datas de Publicação
-
Publicação nesta coleção
10 Jan 2013 -
Data do Fascículo
Dez 2012
Histórico
-
Recebido
25 Ago 2011 -
Aceito
20 Jul 2012