Resumos
A expressão de RNAm para leptina, receptor de leptina (obRb), adiponectina, receptor de adiponectina (AdipoR1) e resistina foi avaliada por meio da técnica de PCR em tempo real, em tecidos ovariano, hipofisário, adiposo do omento e da região perirrenal, em ovelhas alimentadas sem farelo de mamona ou com farelo de mamona detoxificada durante 14 meses. O tipo de dieta não afetou os níveis de RNAm para leptina, obRb, adiponectina, AdipoR1 e resistina nos diferentes tecidos avaliados (P>0,05). Nos tecidos ovariano e hipofisário, não foi verificada a expressão da adiponecina e da resistina, respectivamente. Como consequência, pode-se concluir que o farelo de mamona detoxificada pode ser utilizado como fonte proteica na dieta de ovelhas, sem afetar a expressão do gene resistina e dos genes leptina e adiponectina, bem como de seus receptores.
ovino; tecido adiposo; reprodução; adipocinas
The expression of leptin, leptin receptor (obRb), adiponectin, adiponectin receptor (AdipoR1) and resistin was assessed by real-time PCR technique in ovarian, pituitary, and the omental adipose perirenal tissue in sheep feed without castor meal or with detoxified castor meal. The type of diet did not affect mRNA levels for leptin, obRb, adiponectin, resistin AdipoR1 evaluated in different tissues (P>0.05). However, in pituitary and ovarian tissues there was no expression of resistin and adiponectin, respectively. The detoxified castor meal can be used in sheep diets as alternative food protein without affecting the expression of leptin and adponectin as well as their receptors and resistin.
sheep; fat; reproduction; adipokines
INTRODUÇÃO
As reservas de combustíveis fósseis têm se tornado cada vez mais escassas, e os impactos ambientais causados durante sua extração têm sido significativos. Diante disso, a utilização de biocombustíveis, como o biodiesel, vem sendo alvo de diversos estudos que têm relacionado sua participação na matriz energética mundial. Isso se deve principalmente ao fato de a produção do biodiesel ser proveniente de fontes vegetais, como as oleaginosas, dentre as quais se destacam a soja, o algodão, o girassol, o babaçu e a mamona, que, além de gerarem uma quantidade significativa de coprodutos que podem ter sua utilização na alimentação animal, têm um impacto ambiental positivo (Silva et al., 2010SILVA, D.C.D.; ALVES, A.A.; VASCONCELOS, V.R. et al. Metabolismo dos compostos nitrogenados em ovinos alimentados com dietas contendo farelo de mamona destoxificado. Acta. Sci. Anim. Sci., v.32, p.219-224, 2010.). Assim, a mamona (Ricinus communis) tem sido considerada a principal oleaginosa para a produção de biodiesel, por ser de fácil cultivo, de baixo custo e resistente à seca, além de gerar, após a sua utilização, alguns subprodutos, como o farelo e a torta (Pompeu et al., 2012POMPEU, R.C.F.F.; CÂNDIDO, M.J.D.; PEREIRA, E.S. et al. Desempenho produtivo e características de carcaça de ovinos em confinamento alimentados com rações contendo torta de mamona destoxificada em substituição ao farelo de soja. Rev. Bras. Zootec., v.41, p.726-733, 2012.).
Em virtude da possibilidade da sua utilização nas dietas de ovinos como alimento proteico alternativo, o farelo de mamona tem despertado o interesse de vários produtores (Furtado et al., 2012FURTADO, R.N.; CARNEIRO, M.S.S.; CÂNDIDO, M.J.D. et al. Valor nutritivo de dietas contendo torta de mamona submetida a métodos alternativos de destoxificação para ovinos. Arq. Bras. Med. Vet. Zootec. v.64, p.155-162, 2012.). Entretanto, o seu uso tem sido limitado devido à presença de fatores antinutricionais, como a ricina, a ricinina e complexo alergênico CB-1A. Diante disso, diversas técnicas foram desenvolvidas com o objetivo de inativar ou reduzir os componentes tóxicos presentes nos subprodutos da mamona (Pompeu et al., 2012POMPEU, R.C.F.F.; CÂNDIDO, M.J.D.; PEREIRA, E.S. et al. Desempenho produtivo e características de carcaça de ovinos em confinamento alimentados com rações contendo torta de mamona destoxificada em substituição ao farelo de soja. Rev. Bras. Zootec., v.41, p.726-733, 2012.), tornando-os viáveis para serem utilizados na alimentação de ruminantes. Recentemente, foi demonstrado que a inclusão do farelo de mamona detoxificada na dieta de ovinos não alterou o consumo e a digestibilidade, bem como o ganho de peso e as características de carcaça (Oliveira et al., 2010OLIVEIRA, A.S.D.; CAMPOS, J.M.S.; OLIVEIRA, M.R.C. et al. Nutrient digestibility, nitrogen metabolism and hepatic function of sheep fed diets containing solvent or expeller castorseed meal treated with calcium hydroxide. Anim. Feed Sci. Technol., v.158, p.15-28, 2010.). Todavia, estes ensaios foram realizados apenas em intervalos de curto (19 dias) (Silva et al., 2011SILVA, D.C.; ALVES, A.A.; OLIVEIRA, M.E. et al. Consumo e digestibilidade de dietas contendo farelo de mamona destoxificado para ovinos em terminação. Rev. Bras. Saúde Prod. Anim., v.12, p.96-106, 2011.), ou médio (60 dias) (Furtado et al., 2012FURTADO, R.N.; CARNEIRO, M.S.S.; CÂNDIDO, M.J.D. et al. Valor nutritivo de dietas contendo torta de mamona submetida a métodos alternativos de destoxificação para ovinos. Arq. Bras. Med. Vet. Zootec. v.64, p.155-162, 2012.) períodos, o que ressalta a ausência de estudos sobre os efeitos a longo prazo desses resíduos na alimentação animal.
Nesta espécie, tanto os parâmetros produtivos como os reprodutivos são influenciados pelos efeitos nutricionais nas diferentes fases de desenvolvimento (Robinson, 1996ROBINSON, J.J. Nutrition and reproduction. Anim. Reprod. Sci., v.42, p.25-34, 1996.). Além disso, esses efeitos influenciam a formação e deposição do tecido adiposo, responsável pela produção de algumas substâncias conhecidas como adipocinas, como, por exemplo, leptina, adiponectina e resistina. Essas adipocinas atuam na regulação do gasto de energia, nos metabolismos lipídico e hormonal, bem como no desempenho de diferentes funções reprodutivas (Guerre-Milo, 2008). Isto demonstra que existe uma relação direta entre nutrição, tecido adiposo e reprodução que pode ser avaliada pela identificação e pelo comportamento dessas substâncias. Uma forma eficaz de avaliar esse comportamento é por meio dos avanços na genética, que têm permitido diferenciar e identificar expressões gênicas associadas à variação na qualidade da carne, como maciez e suculência, bem como selecionar animais visando à produção de maior teor de músculos e baixas deposições de gordura (Coutinho et al., 2010COUTINHO, L.L.; JORGE, E.C.; ROSÁRIO, M.F.; REGITANO, L.C.A. A genômica na bovinocultura de corte. In: PIRES, A.V. (Ed.) Bovinocultura de corte. Piracicaba: Fealq, 2010. v.2, p.813-826. ). Além disso, atualmente, o consumidor está se preocupando não só com características de qualidade, mas também com valor nutritivo, dietético e com a origem desses produtos. Este conhecimento, de como os nutrientes da dieta promovem a expressão de genes relacionados com características produtivas e reprodutivas, pode ser mais um subsídio eficiente na rastreabilidade individual de animais e seus respectivos produtos.
A utilização das técnicas da genética molecular tem sido realizada para identificar a expressão do RNAm para leptina no hipotálamo, na hipófise e nos ovários de ruminantes (Kendall et al., 2004KENDALL, N.R.; GUITIERREZ, C.G.; SCARAMUZZI, R.J. et al. Direct in vivo effects of leptin on ovarian steroidogenesis in sheep. Reproduction. v.128, p.757-765, 2004.). Da mesma forma, a presença de adiponectina e seus receptores foi detectada na hipófise de humanos (Psilopanagioti et al., 2009PSILOPANAGIOTI, A.; PAPADAKI, H.; KRANIOTI, E.F. et al. Expression of adiponectin and adiponectin receptors in human pituitary gland and brain. Neuroendocrinology, v.89, p.38-47, 2009.) e em ovários de bovinos (Tabandeh et al., 2010TABANDEH, M.R.; HOSSEINI, A.; SAEB, M. et al. Changes in the gene expression of adiponectin and adiponectin receptors (AdipoR1 and AdipoR2) in ovarian follicular cells of dairy cow at different stages of development. Theriogenology. v.73, p.659-69, 2010.). Além disso, a resistina teve sua identificação nas células da granulosa de folículos ovarianos de vacas e ratas (Maillard et al., 2011MAILLARD, V.; FROMENT, P.; RAME, C. et al. Expression and effect of resistin on bovine and rat granulosa cell steroidogenesis and proliferation. Reproduction., v.141, p.467-479, 2011.). No entanto, ainda não se tem conhecimento acerca da substituição de concentrados proteicos, como o farelo de soja pelo farelo de mamona detoxificada, sob a expressão desses genes que participam da interação entre status nutricional e função reprodutiva em ovelhas.
O objetivo deste trabalho foi avaliar o perfil de expressão de RNAm para leptina, obRb, adiponectina, AdipoR1 e resistina em tecidos ovariano, hipofisário, adiposo do omento e da região perirrenal em ovelhas adultas e verificar se a substituição de farelo de soja por farelo de mamona dexotificada, fornecida por longos períodos, afeta a dinâmica de expressão destes genes.
MATERIAL E MÉTODOS
O presente estudo foi aprovado pela Comissão de Ética para o Uso de Animais da Universidade Estadual do Ceará (CEUA-UECE), com o número 09230950-0/74. Foram utilizadas 40 ovelhas da raça Santa Inês, homogêneas em peso, condição corporal e idade (33,07±0,83kg; 2,31±0,09 e 27,88±0,95 meses, respectivamente). Esses animais foram divididos em dois grupos alimentares: grupo sem farelo de mamona (SFM, n=20), alimentado com feno de tifton e concentrado (milho 80%, farelo de soja 15%, minerais 5%); e grupo alimentado com farelo de mamona detoxificada (FMD, n=20), alimentado com feno de tifton e concentrado com farelo de mamona detoxificada em substituição total do farelo de soja (milho 80%, farelo de mamona 15%, minerais 5%). Ambas as dietas foram fornecidas durante 14 meses, sendo isoenergéticas (74% de NDT) e isoproteicas (14% de proteína bruta na base da matéria seca) em quantidade conforme as exigências nutricionais. Todos os animais experimentais foram mantidos em baias coletivas, com acesso a sal mineral e água ad libitum.
Ao final do período experimental, 10 animais de cada grupo foram abatidos segundo as normas do RIISPOA (1980)RIISPOA. Regulamento da Inspeção Industrial e Sanitária de Produtos de Origem Animal. Brasília, DF. 1980, 166p.. Imediatamente após o abate, foram coletadas amostras de tecido ovariano (dois ovários de seis animais por grupo, n= 24), hipofisário (um por animal n=20), adiposo do omento (quatro fragmentos por animal, n=40) e adiposo da região perirrenal (quatro fragmentos por animal, n=40). Para esse procedimento, foram utilizados bisturi, tesouras e pinças. O material usado para coleta foi esterilizado e, em seguida, tanto o material como os tecidos foram lavados com água DEPC (livre de Rnase), armazenados em criotubos de 2mL contendo 300μL de trizol e mantidos em -80°C até a extração de RNA. Para extração do RNA total, foi utilizado o método trizol, conforme as instruções do fabricante (Trizol; Invitrogen Life Technologies). Posteriormente, o RNA total foi purificado com DNAse I (PROMEGA), quantificado por espectrofotometria (Bionnate 3, THERMO SCIENTIFIC), e sua integridade avaliada utilizando-se SYBR Green II (LCG BIOTECNOLOGIA) em gel de agarose a 1%.
O cDNA foi sintetizado de 1μg de RNA total, utilizando-se o kit IMPROM-II TRANSCRIPTASE (PROMEGA). As análises de PCR em tempo real foram realizadas usando o Rotor-GENE Q (QUIAGEN), com um volume total de 20μL por reação, sendo 2μL de cDNA diluído (1 cDNA: 9 H2O DEPC), 0,5μL de cada primer específico do ensaio, 10μL do QuantiFast SYBR Green PCR Kit (QUIAGEN) e 7,0μL de água, com as seguintes definições: 94ºC, durante 15 minutos, seguidos de 40 ciclos de 94ºC, durante 30 segundos, temperatura anelamento específica dos primers, que foram desenhados com base na sequência disponível no GenBan (http://www.ncbi.nlm.nih.gov/genbank/) (Tab. 1) durante 30 segundos, e 72ºC durante 45 segundos. As reações foram realizadas em triplicatas juntamente com o controle negativo. O RNA polimerase II foi utilizado como o controle endógeno.
Acesso às sequências no GenBank, sequência dos primers específicos, tamanho do produto e temperatura de pareamento
A quantificação relativa do ∆∆Ct foi realizada de acordo com Livak e Schmittgen (2001)LIVAK, K.J.; SCHMITTGEN, T.D. Analysis of relative gene expression data using real-time quantitative PCR and the 2(-∆∆CT) method. Methods. v.25, p.402-408, 2001.. A diferença entre a média do Ct do gene de interesse e a média de Ct do gene endógeno (∆CT) foi calculada para normalização. A expressão relativa de cada gene foi calculada pela forma ∆∆C, e o resultado para a expressão do gene foi determinado por um valor adimensional por meio da fórmula 2-∆∆Ct.
Os dados referentes à expressão gênica foram analisados utilizando-se ANOVA do programa estatístico Statistica (StatSoft, Inc, Tulsa, OK, USA). O fator testado foi o grupo alimentar: sem farelo de mamona (SFM) e com farelo de mamona detoxificada (FMD). A comparação entre as médias foi analisada pelo teste t de Student. A correlação entre expressão gênica e pesos dos animais, da carcaça e dos tecidos adiposos foi analisada mediante a correlação de Pearson. Os valores foram expressos como média±erro-padrão da média.
RESULTADOS E DISCUSSÃO
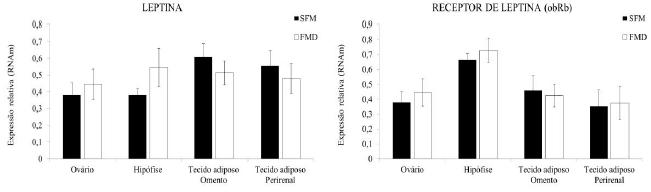
A relação entre as adipocinas secretadas pelo tecido adiposo e a reprodução está intimamente ligada com o eixo hipotálamo-hipófise-gonadal, o qual é responsável por modular diferentes funções reprodutivas (Souza et al., 2009SOUZA, A.L.; ARRUDA, I.J.; RONDINA, D. Função, Controle Transcricional e Atividade Endócrina do Tecido Adiposo nos Mamíferos. ACSA, v.5, p.1-15, 2009.). Entre as adipocinas, destaca-se a leptina, que é um hormônio produzido pelo tecido adiposo branco e exerce um efeito sobre o núcleo hipotalâmico central, contribuindo para a regulação do metabolismo energético e o comportamento do consumo de alimentos (Ahima e Flier, 2000AHIMA, R.S.; FLIER, J.S. Adipose tissue as an endocrine organ. Trends Endocrinol. Metab. v.11, p.327-32, 2000.). Sua produção é regulada pelas alterações induzidas pela insulina no adipócito, e os seus níveis correlacionam-se com a massa de tecido adiposo. Além disso, diversos estudos têm demonstrado que a leptina é um fator de ligação entre o status metabólico e a reprodução nas diferentes espécies (Havel, 2004HAVEL, P.J. Update on adipocyte hormones: regulation of energy balance and carbohydrate/ lipid metabolism. Diabetes. v.53, p.l43-151, 2004.). Tanto a leptina como o seu receptor ob-Rb têm sido identificados, por meio de técnicas como o Northern blot, a hibridização in situ e a reação em cadeia da polimerase (PCR), em vários tecidos, inclusive nos ovários (Duggal et al., 2002DUGGAL, P.S.; RYAN, N.K.; VAN DER HOEK, K.H. et al. Effects of leptin administration and feed restriction on thecal leucocytes in the preovulatory rat ovary and the effects of leptin on meiotic maturation, granulosa cell proliferation, steroid hormone and PGE2 release in cultured rat ovarian follicles. Reproduction. v.123, p.891-898, 2002.), na hipófise (Sone et al., 2001SONE, M.; NAGATA, H.; TAKEKOSHI, S. et al. Expression and localization of leptin receptor in the normal rat pituitary gland. Cell Tissue Res., v.305, p.351-356, 2001.) e no hipotálamo, cuja expressão está associada ao controle do apetite, da reprodução e do crescimento. De forma similar, neste trabalho foi identificada a presença de RNAm para leptina e obR, nos tecidos ovariano, hipofisário e adiposo do omento e da região perirrenal em ovelhas (Fig. 1). Contudo, a expressão desses genes não foi afetada pelo tipo de dieta (P>0,05).
Expressão de leptina e obRb em tecidos ovariano, hipofisário, adiposo do omento e da região perirrenal em ovelhas alimentadas SFM ou com FMD.
Bonnet et al. (2009)BONNET, M.; DELAVAUD, C.; BERNARD, L. et al. Sunflower-seed oil, rapidly-degradable starch, and adiposity up-regulate leptin gene expression in lactating goats. Dom. Anim. Endocrinol. v.37, p.93-103, 2009. verificaram que a substituição parcial do concentrado comercial por alimentos alternativos à base de óleo de girassol oleico e/ou óleo de linhaça, durante 21 dias, não alterou os níveis de RNAm para leptina nos tecidos adiposos subcutâneo, do omento e da região perirrenal em cabras lactantes. No presente estudo, o resíduo da mamona foi administrado para um período mais extenso (15 meses); mesmo assim, o gene leptina e o seu receptor foram expressos de forma similar em ambos os tratamentos, seja no tecido adiposo, no ovário e na hipófise.
Em relação ao peso dos animais, das carcaças e do tecido adiposo, estes foram similares entre os grupos e não apresentaram correlação com a expressão gênica (Tab. 2).
Além da leptina, outra importante adipocina é a adiponectina, que é responsável por coordenar diversas funções biológicas, incluindo a oxidação de lipídios no músculo esquelético e miócitos, a redução da glicose hepática (Combs et al., 2003COMBS, T.P.; BERG, A.H.; RAJALA, M.W. et al. Sexual differentiation, pregnancy, calorie restriction, and aging affect the adipocyte-specific secretory protein adiponectin. Diabetes. v.52, p.268-276, 2003.), o aumento da sensibilidade à insulina, a vasodilatação (Yamauchi et al., 2003YAMAUCHI, T.; KAMON, J.; ITO, Y. et al. Cloning of adiponectin receptors that mediate antidiabetic metabolic effects. Nature, v.423, p.762-769, 2003.), o processo inflamatório e a regulação do balanço energético. Sua presença e de seus receptores (AdipoR1 e AdipoR2) já foi identificada em diferentes tecidos (Tabandeh et al., 2010TABANDEH, M.R.; HOSSEINI, A.; SAEB, M. et al. Changes in the gene expression of adiponectin and adiponectin receptors (AdipoR1 and AdipoR2) in ovarian follicular cells of dairy cow at different stages of development. Theriogenology. v.73, p.659-69, 2010.), sendo encontrada uma alta expressão do AdipoR1 no fígado, coração, cérebro e músculo esquelético, enquanto o receptor AdipoR2 está predominantemente expresso no fígado (Yamauchi et al., 2003YAMAUCHI, T.; KAMON, J.; ITO, Y. et al. Cloning of adiponectin receptors that mediate antidiabetic metabolic effects. Nature, v.423, p.762-769, 2003.). Contudo, foi observada a presença de ambos os receptores em células pancreáticas, endoteliais e adipócitos (Motoshima et al., 2004MOTOSHIMA, H.; WU, X.; MAHADEV, K. et al. Adiponectin suppresses proliferation and superoxide generation and enhances eNOS activity in endothelial cells treated with oxidized LDL. Biochem. Biophys. Res. Commun., v.315, p.264-71, 2004.). Neste estudo, ao ser avaliado o padrão de expressão de adiponectina e seu receptor (AdipoR1), foi identificada a presença de ambos os genes nos tecidos hipofisário, adiposo do omento e da região perirenal, com comportamento similar de expressão tanto em animais alimentados SFM, quanto naqueles tratados com FMD (P>0,05).
Peso vivo ao abate, peso da carcaça e peso dos tecidos adiposos de ovelhas alimentadas sem farelo de mamona (SFM) e com farelo de mamona detoxificada (FMD).
Recentemente, diversos estudos relataram a expressão do ligante e de seus receptores no ovário em bovinos (Lagaly et al., 2008LAGALY, D.V.; AAD, P.Y.; GRADO-AHUIR, J.A. et al. Role of adiponectin in regulating ovarian theca and granulosa cell function. Mol. Cell. Endocrinol., v.284, p.38-45, 2008.) e roedores (Chabrolle et al., 2007CHABROLLE, C.; TOSCA, L.; DUPONT, J. Regulation of adiponectin and its receptors in rat ovary by human chorionic gonadotrophin treatment and potential involvement of adiponectin in granulosa cell steroidogenesis. Reproduction. v.133, p.719-731, 2007.), no hipotálamo e na hipófise de humanos (Psilopanagioti et al., 2009PSILOPANAGIOTI, A.; PAPADAKI, H.; KRANIOTI, E.F. et al. Expression of adiponectin and adiponectin receptors in human pituitary gland and brain. Neuroendocrinology, v.89, p.38-47, 2009.). No entanto, neste estudo, ao se avaliar o tecido ovariano, foi identificada apenas a presença de AdipoR1 (Fig. 2). Esta ausência de expressão de RNAm para adiponectina foi relatada anteriormente por Cikos et al. (2010)CIKOS, S.; BURKUS, J.; BUKOVSKA, A. et al. Expression of adiponectin receptors and effects of adiponectin isoforms in mouse preimplantation embryos. Hum. Reprod. v.25, p.2247-2255, 2010., em oócitos e embriões iniciais de ratas. Por outro lado, Maillard et al. (2010)MAILLARD, V.; UZBEKOVA, S.; GUIGNOT, F. et al. Effect of adiponectin on bovine granulosa cell steroidogenesis, oocyte maturation and embryo development. Reprod. Biol. Endocrinol., v.8, p.1-15, 2010., ao utilizarem as técnicas de RT-PCR, Western Blotting e imuno-histoquímica, identificaram tanto a expressão de RNAm como a presença das proteínas, adiponectina e AdipoR1 em pequenos e grandes folículos, corpo lúteo, oócito, células da granulosa, da teca e do cumulus de bovinos. Estas discrepâncias nos resultados podem estar associadas às diferenças entre as espécies estudadas, as técnicas adotadas para investigar a presença destes genes, ou mesmo à ausência de produção de adiponectina no ovário de ovelhas.
Expressão de adiponectina e AdipoR1 em tecidos ovariano, hipofisário, adiposo do omento e da região perirrenal em ovelhas alimentadas SFM ou com FMD.
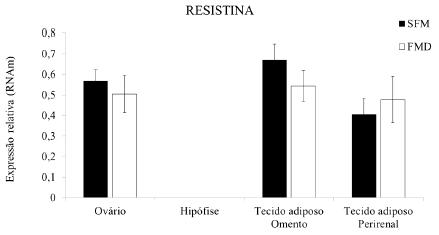
Outra importante adipocina é a resistina, que regula diversas funções celulares, como o metabolismo da glicose, os processos pró-inflamatórios no tecido adiposo, a estimulação da proliferação de células do músculo liso e a angiogênese (Robertson et al., 2009ROBERTSON, S.A.; RAE, C.J.; GRAHAM, A. Induction of angiogenesis by murine resistin: putative role of PI3-kinase and NO-dependent pathways. Regulatory Peptides, v.152, p.41-47, 2009.). Alguns estudos têm sugerido que essa adipocina é responsável por desempenhar importantes papéis no desenvolvimento de resistência à insulina e à obesidade em roedores (Lazar, 2007LAZAR, M.A. Resistin and obesity-associated metabolic diseases. Horm. Metab. Res., v.39, p.710-716, 2007.). Atualmente, acredita-se que a resistina afeta a fertilidade de indivíduos machos e fêmeas, visto que a presença de seu RNAm e proteína tem sido identificada em diversos tecidos reprodutivos, incluindo o hipotálamo, a hipófise e os testículos (Nogueiras et al., 2003NOGUEIRAS, R.; GUALILLO, O.; CAMINOS, J.E. et al. Regulation of resistin by gonadal, thyroid hormone and nutritional status. Obes. Res., v.11, p.408-414, 2003.). Estudos com roedores demonstraram que, no hipotálamo, a expressão de resistina foi correlacionada com uma inibição do apetite; na hipófise, sua expressão variou em razão do status nutricional, da idade e do sexo (Morash et al., 2004MORASH, B.A.; UR, E.; WIESNER, G. et al. Pituitary resistin gene expression: effects of age, gender and obesity. Neuroendocrinology, v.79, p.149-156, 2004.). Já em testículos de ratos, tanto essa proteína como seu RNAm foram detectados nas células de Leydig, de Sertoli e nos túbulos seminíferos, durante todo o período pós-natal de desenvolvimento, sendo essa expressão influenciada pela nutrição, bem como por hormônios, incluindo as gonadotrofinas e a leptina (Nogueiras et al., 2003NOGUEIRAS, R.; GUALILLO, O.; CAMINOS, J.E. et al. Regulation of resistin by gonadal, thyroid hormone and nutritional status. Obes. Res., v.11, p.408-414, 2003.). Porém, no presente estudo, foi verificada a expressão de RNAm para resistina nos tecidos ovariano, adiposo do omento e na região perirrenal de ovelhas, sem diferenças de expressão em relação ao tipo de alimentação (SFM ou FMD) fornecida (P>0,05). Este resultado está de acordo com o relatado por Maillard et al. (2011)MAILLARD, V.; FROMENT, P.; RAME, C. et al. Expression and effect of resistin on bovine and rat granulosa cell steroidogenesis and proliferation. Reproduction., v.141, p.467-479, 2011., os quais verificaram que a resistina foi expressa nas células da granulosa de folículos ovarianos de vacas e ratas e que essa expressão possui uma correlação positiva com a proliferação celular e a produção de hormônios esteroides no ovário. No entanto, no tecido hipofisário não foi identificada a expressão de RNAm para resistina tanto em animais alimentados SFM ou com FMD (Fig. 3), o que discorda dos estudos anteriores de Morash et al. (2002)MORASH, B.A.; WILLKINSON D.; UR E.; WILKINSON M. Resistin expression and regulation in mouse pituitary. FEBS Letters, v.526, p. 26-30, 2002., em que foi detectada a presença de resistina na hipófise de camundongos. Contudo, ainda não há estudos sobre a expressão da resistina na hipófise em outras espécies, sobretudo em ruminantes. Torna-se evidente, portanto, que ainda não existe descrito na literatura um padrão de expressão da resistina em tecidos reprodutivos, incluindo hipotálamo, hipófise e ovário. Além disso, não existem estudos que avaliem essa expressão de nenhuma das adipocinas, especialmente leptina, adiponectina e resistina, em animais alimentados com mamona por longos períodos.
Expressão de resistina em tecidos ovariano, hipofisário, adiposo do omento e da região perirrenal em ovelhas alimentadas SFM ou com FMD.
CONCLUSÕES
O farelo de mamona detoxificada em substituição ao farelo de soja pode ser utilizado com sucesso na alimentação de ovelhas por longos períodos, sem afetar a expressão de leptina, obRb, adiponectina, AdipoR1 e resistina em tecidos ovariano, hipofisário, adiposo do omento e da região perirrenal. A expressão da adiponectina não foi identificada nos ovários, e a da resistina na hipófise.
AGRADECIMENTOS
Fonte de financiamento CNPq (Proc. N.578189/2008-9). Os autores agradecem às equipes técnicas da fazenda Campo da Semente, pelo suporte técnico e auxílio no manejo dos animais. Os autores agradecem ainda à usina BOM - Brasil Óleo de Mamona Ltda, localizada em Salvador - Bahia, por ter disponibilizado o farelo de mamona.
REFERÊNCIAS
- AHIMA, R.S.; FLIER, J.S. Adipose tissue as an endocrine organ. Trends Endocrinol. Metab. v.11, p.327-32, 2000.
- BONNET, M.; DELAVAUD, C.; BERNARD, L. et al. Sunflower-seed oil, rapidly-degradable starch, and adiposity up-regulate leptin gene expression in lactating goats. Dom. Anim. Endocrinol. v.37, p.93-103, 2009.
- CHABROLLE, C.; TOSCA, L.; DUPONT, J. Regulation of adiponectin and its receptors in rat ovary by human chorionic gonadotrophin treatment and potential involvement of adiponectin in granulosa cell steroidogenesis. Reproduction. v.133, p.719-731, 2007.
- CIKOS, S.; BURKUS, J.; BUKOVSKA, A. et al. Expression of adiponectin receptors and effects of adiponectin isoforms in mouse preimplantation embryos. Hum. Reprod. v.25, p.2247-2255, 2010.
- COMBS, T.P.; BERG, A.H.; RAJALA, M.W. et al. Sexual differentiation, pregnancy, calorie restriction, and aging affect the adipocyte-specific secretory protein adiponectin. Diabetes. v.52, p.268-276, 2003.
- COUTINHO, L.L.; JORGE, E.C.; ROSÁRIO, M.F.; REGITANO, L.C.A. A genômica na bovinocultura de corte. In: PIRES, A.V. (Ed.) Bovinocultura de corte. Piracicaba: Fealq, 2010. v.2, p.813-826.
- DUGGAL, P.S.; RYAN, N.K.; VAN DER HOEK, K.H. et al. Effects of leptin administration and feed restriction on thecal leucocytes in the preovulatory rat ovary and the effects of leptin on meiotic maturation, granulosa cell proliferation, steroid hormone and PGE2 release in cultured rat ovarian follicles. Reproduction. v.123, p.891-898, 2002.
- FURTADO, R.N.; CARNEIRO, M.S.S.; CÂNDIDO, M.J.D. et al. Valor nutritivo de dietas contendo torta de mamona submetida a métodos alternativos de destoxificação para ovinos. Arq. Bras. Med. Vet. Zootec. v.64, p.155-162, 2012.
- GUERRE-MILLO, M. Adiponectin: an update. Diabetes & Metabolism. v.34, p.12-18, 2008.
- HAVEL, P.J. Update on adipocyte hormones: regulation of energy balance and carbohydrate/ lipid metabolism. Diabetes. v.53, p.l43-151, 2004.
- KENDALL, N.R.; GUITIERREZ, C.G.; SCARAMUZZI, R.J. et al. Direct in vivo effects of leptin on ovarian steroidogenesis in sheep. Reproduction. v.128, p.757-765, 2004.
- LAGALY, D.V.; AAD, P.Y.; GRADO-AHUIR, J.A. et al. Role of adiponectin in regulating ovarian theca and granulosa cell function. Mol. Cell. Endocrinol., v.284, p.38-45, 2008.
- LAZAR, M.A. Resistin and obesity-associated metabolic diseases. Horm. Metab. Res., v.39, p.710-716, 2007.
- LIVAK, K.J.; SCHMITTGEN, T.D. Analysis of relative gene expression data using real-time quantitative PCR and the 2(-∆∆CT) method. Methods. v.25, p.402-408, 2001.
- MAILLARD, V.; FROMENT, P.; RAME, C. et al. Expression and effect of resistin on bovine and rat granulosa cell steroidogenesis and proliferation. Reproduction., v.141, p.467-479, 2011.
- MAILLARD, V.; UZBEKOVA, S.; GUIGNOT, F. et al. Effect of adiponectin on bovine granulosa cell steroidogenesis, oocyte maturation and embryo development. Reprod. Biol. Endocrinol., v.8, p.1-15, 2010.
- MORASH, B.A.; UR, E.; WIESNER, G. et al. Pituitary resistin gene expression: effects of age, gender and obesity. Neuroendocrinology, v.79, p.149-156, 2004.
- MORASH, B.A.; WILLKINSON D.; UR E.; WILKINSON M. Resistin expression and regulation in mouse pituitary. FEBS Letters, v.526, p. 26-30, 2002.
- MOTOSHIMA, H.; WU, X.; MAHADEV, K. et al. Adiponectin suppresses proliferation and superoxide generation and enhances eNOS activity in endothelial cells treated with oxidized LDL. Biochem. Biophys. Res. Commun., v.315, p.264-71, 2004.
- NOGUEIRAS, R.; GUALILLO, O.; CAMINOS, J.E. et al. Regulation of resistin by gonadal, thyroid hormone and nutritional status. Obes. Res., v.11, p.408-414, 2003.
- OLIVEIRA, A.S.D.; CAMPOS, J.M.S.; OLIVEIRA, M.R.C. et al. Nutrient digestibility, nitrogen metabolism and hepatic function of sheep fed diets containing solvent or expeller castorseed meal treated with calcium hydroxide. Anim. Feed Sci. Technol., v.158, p.15-28, 2010.
- POMPEU, R.C.F.F.; CÂNDIDO, M.J.D.; PEREIRA, E.S. et al. Desempenho produtivo e características de carcaça de ovinos em confinamento alimentados com rações contendo torta de mamona destoxificada em substituição ao farelo de soja. Rev. Bras. Zootec., v.41, p.726-733, 2012.
- PSILOPANAGIOTI, A.; PAPADAKI, H.; KRANIOTI, E.F. et al. Expression of adiponectin and adiponectin receptors in human pituitary gland and brain. Neuroendocrinology, v.89, p.38-47, 2009.
- RIISPOA. Regulamento da Inspeção Industrial e Sanitária de Produtos de Origem Animal. Brasília, DF. 1980, 166p.
- ROBERTSON, S.A.; RAE, C.J.; GRAHAM, A. Induction of angiogenesis by murine resistin: putative role of PI3-kinase and NO-dependent pathways. Regulatory Peptides, v.152, p.41-47, 2009.
- ROBINSON, J.J. Nutrition and reproduction. Anim. Reprod. Sci., v.42, p.25-34, 1996.
- SILVA, D.C.; ALVES, A.A.; OLIVEIRA, M.E. et al. Consumo e digestibilidade de dietas contendo farelo de mamona destoxificado para ovinos em terminação. Rev. Bras. Saúde Prod. Anim., v.12, p.96-106, 2011.
- SILVA, D.C.D.; ALVES, A.A.; VASCONCELOS, V.R. et al. Metabolismo dos compostos nitrogenados em ovinos alimentados com dietas contendo farelo de mamona destoxificado. Acta. Sci. Anim. Sci., v.32, p.219-224, 2010.
- SONE, M.; NAGATA, H.; TAKEKOSHI, S. et al. Expression and localization of leptin receptor in the normal rat pituitary gland. Cell Tissue Res., v.305, p.351-356, 2001.
- SOUZA, A.L.; ARRUDA, I.J.; RONDINA, D. Função, Controle Transcricional e Atividade Endócrina do Tecido Adiposo nos Mamíferos. ACSA, v.5, p.1-15, 2009.
- TABANDEH, M.R.; HOSSEINI, A.; SAEB, M. et al. Changes in the gene expression of adiponectin and adiponectin receptors (AdipoR1 and AdipoR2) in ovarian follicular cells of dairy cow at different stages of development. Theriogenology. v.73, p.659-69, 2010.
- YAMAUCHI, T.; KAMON, J.; ITO, Y. et al. Cloning of adiponectin receptors that mediate antidiabetic metabolic effects. Nature, v.423, p.762-769, 2003.
Datas de Publicação
-
Publicação nesta coleção
Ago 2014
Histórico
-
Recebido
28 Out 2012 -
Aceito
12 Dez 2012