Resumos
Foram inventariadas 61 espécies de briófitas. Chiloscyphus subviridis (Hook. f. & Taylor) J.J. Engel & R.M. Schust. e Lejeunea autoica R.M. Schust. são citadas pela primeira vez para o país e Lejeunea phyllobola Nees & Mont. ex Mont, pela primeira vez para o Estado de São Paulo. Os maiores números de táxons foram registrados para as maiores ilhas com vegetação de Mata Atlântica e, os menores, para as menores ilhas com vegetação formada por árvores esparsas da Mata Atlântica ou arbustos esparsos e expostos a condições adversas. A maior parte das espécies estão restritas a uma determinada ilha. Alcatrazes e Bom Abrigo assemelham-se quanto à flora de hepáticas; Castilho assemelha-se a esse primeiro grupo de ilhas devido à flora de musgos, enquanto Casca possui a brioflora mais distinta dentre as quatro ilhas. As rochas e as cascas dos hospedeiros arbustivo-arbóreos são os substratos mais disponíveis para as briófitas. Rocha é o substrato mais disponível para determinadas espécies em Alcatrazes e Castilho e, provavelmente, o preferido por essas plantas em Bom Abrigo e Casca.
briófitas; ilhas; Estado de São Paulo; Mata Atlântica
Collections of bryophytes amount to a total of 61 species. Chiloscyphus subviridis (Hook. f. & Taylor) J.J. Engel & R.M. Schust. and Lejeunea autoica R.M. Schust. are new records for Brazil. Lejeunea phyllobola Nees & Mont. ex Mont. is new for São Paulo State. A more diversified bryophyte flora was found in the largest islands covered by the Atlantic forest and the smallest number of taxa came from the smallest islands with vegetation covered by sparse trees of the Atlantic forest or sparse shrubs exposed to adverse conditions. Most of the taxa are restricted to certain islands. Alcatrazes is similar to Bom Abrigo in liverworts. Castilho is similar to this first group of islands in mosses. The most distinct bryoflora is found in Casca island. Rock and bark are the most available sites for bryophytes. Rock is the most available substrate for certain species in Alcatrazes and Castilho, and probaly the preferred places for these plants in Bom Abrigo and Casca.
bryophytes; islands; São Paulo state; Atlantic forest
BRIÓFITAS DAS ILHAS DE ALCATRAZES, DO BOM ABRIGO, DA CASCA E DO CASTILHO, ESTADO DE SÃO PAULO, BRASIL1 1 Fonte financiadora: SMA/Gov. Est. de São Paulo
Sandra Regina Visnadi2 1 Fonte financiadora: SMA/Gov. Est. de São Paulo
Daniel Moreira Vital2 1 Fonte financiadora: SMA/Gov. Est. de São Paulo
Recebido em 03/08/00. Aceito em 07/05/01
RESUMO ¾ (Briófitas das ilhas de Alcatrazes, do Bom Abrigo, da Casca e do Castilho, estado de São Paulo, Brasil). Foram inventariadas 61 espécies de briófitas. Chiloscyphus subviridis (Hook. f. & Taylor) J.J. Engel & R.M. Schust. e Lejeunea autoica R.M. Schust. são citadas pela primeira vez para o país e Lejeunea phyllobola Nees & Mont. ex Mont, pela primeira vez para o Estado de São Paulo. Os maiores números de táxons foram registrados para as maiores ilhas com vegetação de Mata Atlântica e, os menores, para as menores ilhas com vegetação formada por árvores esparsas da Mata Atlântica ou arbustos esparsos e expostos a condições adversas. A maior parte das espécies estão restritas a uma determinada ilha. Alcatrazes e Bom Abrigo assemelham-se quanto à flora de hepáticas; Castilho assemelha-se a esse primeiro grupo de ilhas devido à flora de musgos, enquanto Casca possui a brioflora mais distinta dentre as quatro ilhas. As rochas e as cascas dos hospedeiros arbustivo-arbóreos são os substratos mais disponíveis para as briófitas. Rocha é o substrato mais disponível para determinadas espécies em Alcatrazes e Castilho e, provavelmente, o preferido por essas plantas em Bom Abrigo e Casca.
Palavras-chave ¾ briófitas, ilhas, Estado de São Paulo, Mata Atlântica.
ABSTRACT ¾ (Bryophytes from the Alcatrazes, Bom Abrigo, Casca, and Castilho islands of São Paulo State, Brazil). Collections of bryophytes amount to a total of 61 species. Chiloscyphus subviridis (Hook. f. & Taylor) J.J. Engel & R.M. Schust. and Lejeunea autoica R.M. Schust. are new records for Brazil. Lejeunea phyllobola Nees & Mont. ex Mont. is new for São Paulo State. A more diversified bryophyte flora was found in the largest islands covered by the Atlantic forest and the smallest number of taxa came from the smallest islands with vegetation covered by sparse trees of the Atlantic forest or sparse shrubs exposed to adverse conditions. Most of the taxa are restricted to certain islands. Alcatrazes is similar to Bom Abrigo in liverworts. Castilho is similar to this first group of islands in mosses. The most distinct bryoflora is found in Casca island. Rock and bark are the most available sites for bryophytes. Rock is the most available substrate for certain species in Alcatrazes and Castilho, and probaly the preferred places for these plants in Bom Abrigo and Casca.
Key words ¾ bryophytes, islands, São Paulo state, Atlantic forest.
Introdução
As ilhas são consideradas ecossistemas individualizados e isolados geograficamente devido à barreira oceânica. Os ecossistemas insulares são frágeis em sua dinâmica e, em geral, abrangem uma área pequena (Ângelo & Lino, 1989).
As ilhas brasileiras são pouco estudadas. A maioria das pesquisas nessas áreas foram realizadas no Estado de São Paulo, cuja costa possui um grande número de ilhas, ilhotas e lajes de rara beleza. Todavia, os trabalhos realizados incluem um número ainda muito pequeno desses ambientes, os quais já enfrentam problemas ligados à urbanização acelerada, especulação imobliária, atividade turística não planificada e ao uso militar (Ângelo & Lino, 1989).
No Brasil, estudos específicos sobre briófitas ocorrentes em ambientes insulares restringe-se a dois trabalhos, onde Gepp (1891) e Vital et al. (1991) listaram um total de 23 espécies para a Ilha de Fernando de Noronha. A Ilha de Marajó está ligada ao continente no estado do Pará e, portanto, não se trata de um ambiente insular propriamente dito. Todavia, ressaltam-se os trabalhos de Lisboa & Maciel (1994), Lisboa et al. (1998, 1999), que incluem um inventário de 55 briófitas para esse local.
O presente trabalho tem por objetivo inventariar a brioflora ocorrente nas ilhas de Alcatrazes, do Bom Abrigo, da Casca e do Castilho e avaliar a semelhança entre essas quatro ilhas quanto à presença de espécies e ao tipo de substrato mais utilizado pelas briófitas nesses locais.
Material e Métodos
O estudo foi realizado nas ilhas de Alcatrazes, do Bom Abrigo, da Casca e do Castilho, situadas no sudeste do Estado de São Paulo (Tab. 1), onde existem amplas planícies de deposição marinha e ilhas de origem continental e sedimentar (Ângelo & Lino, 1989).
O material foi coletado pelo segundo autor e pela estagiária Cristina Giancotti, em Dezembro de 1987 e encontra-se depositado no Herbário SP.
Para o estudo e a identificação das espécies foram necessários microscópio e estereomicroscópio, confecção de lâminas com azul de algodão para melhor visualização das estruturas e de lâminas permanentes com a solução de Hoyer (Schuster, 1966), materiais depositados no Herbário SP e consulta aos trabalhos de Bischler (1967), Buck (1986), Edwards (1980), Engel (1978, 1980), Evans (1911), Florschütz (1964), Frahm (1991), Gradstein (1994), Gradstein & Beek (1985), Gradstein & Buskes (1985), Ireland (1992), Jones (1974, 1979), Jovet-Ast (1947), Kachroo & Schuster (1961), Martius (1828-1834), Mizutani (1982), Mohamed (1979), Ochi (1980), Schuster (1980), Sharp et al. (1994), Stotler (1969), Udar & Awasthi (1982), Vanden-Bergen (1976), Visnadi (1993, 1998), Yuzawa (1988) e Yuzawa & Hattori (1988).
Aplicou-se técnicas de análise multivariada (Digby & Kempton, 1987; Manly, 1994), através da utilização dos programas "Matriz", "Coef", "Cluster" e "Ord" do pacote FITOPAC, desenvolvido por G. J. Shepherd, a fim de comparar a brioflora ocorrente entre as quatro ilhas.
Primeiramente, trabalhou-se com as seguintes matrizes de dados binários: briófitas x ilhas, briófitas sem as espécies restritas x ilhas, hepáticas x ilhas, hepáticas sem as espécies restritas x ilhas, musgos x ilhas e musgos sem as espécies restritas x ilhas, com o objetivo de avaliar a semelhança entre essas quatro localidades, quanto à presença de espécies.
A elaboração dessas seis matrizes se deve a duas razões. Uma delas refere-se ao fato de que a maior parte dos táxons (75,40%) são restritos a uma determinada ilha (Tab. 2).
Portanto, a exclusão dessas espécies, na análise dos dados, poderia distorcer o padrão existente entre esses quatro locais. A segunda razão se deve ao padrão de distribuição das espécies de briófitas. Visnadi (1998) verificou que o padrão de distribuição das briófitas, considerando-se apenas as hepáticas e os musgos, que são comuns a diferentes ecossistemas costeiros é alterado pela presença das espécies restritas. Todavia, a presença das espécies de hepáticas restritas não altera o padrão de distribuição do grupo das hepáticas entre os diferentes ambientes, mas o mesmo não se observa em relação aos musgos. Portanto, foi necessário a análise do padrão de distribuição, em separado, de cada grupo, para se chegar a conclusão que o padrão de distribuição das briófitas é alterado apenas pela presença das espécies de musgos restritas a determinados ecossistemas.
Finalmente, elaborou-se a sétima matriz de dados, contendo proporção de amostras de hepáticas e musgos, coletadas em diferentes tipos de substratos nas quatro localidades (Tab. 3). A análise desses dados teve o objetivo de verificar o tipo de substrato mais utilizado pelas briófitas em cada ilha.
Aplicou-se o índice de Sörensen às seis matrizes de dados binários e o índice de distância euclidiana simples à matriz de dados quantitivos. Os valores de similaridade e os de distância foram submetidos a uma análise de agrupamento, utilizando-se o método de ligação pela média de grupo (UPGMA). Adotou-se valores de correlação cofenética do agrupamento acima de 0,7, como indicativos de uma correspondência razoável entre o dendograma e a matriz original de dados (Sneath & Sokal, 1973). Foram também avaliados os dendogramas elaborados pelos métodos de ligação mínima, completa e média ponderada de grupo (WUPGMA), com os respectivos valores de correlação cofenética.
Aplicou-se a análise de coordenadas principais (PCO) aos valores de similaridade, a fim de confirmar os resultados observados nos dendogramas. A análise de componentes principais (PCA) centrada, utilizando-se a matriz de covariância foi aplicada à matriz de dados quantitativos, a fim de confirmar os resultados observados no dendograma e de verificar quais os grupos de briófitas que contribuem para esse agrupamento.
Resultados
Foram identificadas 61 espécies de briófitas, das quais 32 são hepáticas e 29 são musgos (Tab. 2).
Chiloscyphus subviridis (Hook. f. & Taylor) J.J. Engel & R.M. Schust. é uma espécie saxícola da Ilha da Casca, que também ocorre na Ilha João Fernandes (Oceano Pacífico), no Chile, na Argentina, nas Ilhas Malvinas e em Tristão da Cunha (Oceano Atlântico) (Menéndez, 1995). Lejeunea autoica R.M. Schust. é uma espécie corticícola da Ilha do Bom Abrigo e que ocorre em florestas na Flórida e na África (Schuster, 1980). Ambas são citadas pela primeira vez para o país.
Lejeunea phyllobola Nees & Mont. ex Mont. foi coletada em solo, rochas, caules e troncos na Ilha do Bom Abrigo e na Ilha da Casca e está sendo citada pela primeira vez para o Estado de São Paulo. Trata-se de uma espécie neotropical (Schuster, 1980), que já foi citada para o país em Rio Branco-AC (Vital & Visnadi, 1994) e Guarapari-ES (Visnadi & Vital, 1995).
Quanto à distribuição geográfica mundial das espécies inventariadas, somente Bryum argenteum Hedw. é cosmopolita. Quatro espécies ocorrem na região tropical: Cheilolejeunea trifaria (Reinw., Blume & Nees) Mizut., Lejeunea flava (Sw.) Nees, Leucolejeunea unciloba (Lindenb.) A. Evans e Lopholejeunea subfusca (Nees) Schiffn. Cinco briófitas ocorrem na região neotropical: Aphanolejeunea sicaefolia(Gottsche ex Steph.) A. Evans, Archilejeunea parviflora(Nees) Schiffn., Cheilolejeunea discoidea (Lehm. & Lindenb.) Kachroo & R.M. Schust., Lejeunea laetevirens Nees & Mont. e Groutiella apiculata (Hook.) H.A. Crum & Steere. A distribuição geográfica é mais restrita para Lejeunea villaumei (Steph.) Grolle, que ocorre somente na África e no Brasil; Frullania vitalii Yuzawa & S. Hatt., nos estados da Bahia e de São Paulo e Chiloscyphus subviridis (Hook. f. & Taylor) J.J. Engel & R.M. Schust., nas regiões temperadas da América do Sul. As restantes 48 espécies crescem em regiões tropicais e temperadas. A maior parte delas ocorre nos Hemisférios Norte e Sul. Somente duas espécies, Campylopus cryptopodioides Broth. e C. occultus Mitt. crescem apenas no Hemisfério Sul.
Quanto à distribuição geográfica no Brasil, 96,7% das espécies inventariadas ocorre nas regiões voltadas para o Oceano Atlântico, isto é, na Região Nordeste, Região Sudeste e Região Sul. Todavia, é na Região Sudeste onde se encontra a quase totalidade dessas plantas. São Paulo é o estado onde se registra a ocorrência de 95% das briófitas inventariadas aqui. Em outros estados da Região Sudeste, registram-se números menores, 50-73%, porém são ainda mais altos que os encontrados para os outros estados do país, exceto em Pernambuco, onde também se encontra 50%. Apenas 39-44% ocorre nos estados da Região Sul e 0 a 37% nos estados restantes (Visnadi & Vital, 1995, 1997; Vital & Visnadi, 1994, 2000; Yano, 1981, 1984, 1989, 1995, 1996).
Discussão e Conclusões
O número de espécies insulares está relacionado ao tamanho e isolamento da ilha e à distância entre a ilha e o continente. Quanto maior é o tamanho da ilha, maior é o número de espécies. Ilhas pertencentes a um arquipélago, ou que estão próximas do continente também possuem mais espécies que ilhas isoladas e localizadas em alto-mar (MacArthur & Wilson, 1967).
Como se observa nas tabelas 1 e 3, Bom Abrigo e Alcatrazes são as maiores ilhas. Bom Abrigo é uma das mais próximas do continente, mas Alcatrazes é a mais distante. Todavia, Alcatrazes representa um arquipélago. Visnadi (1998) verificou que a Mata Atlântica é o ecossistema costeiro mais rico em espécies de briófitas, no Núcleo Picinguaba do Parque Estadual da Serra do Mar, em Ubatuba-SP, após coletar briófitas em praia, mangue, caxetal, restinga, Mata Atlântica, topo de morro e áreas ruderais, existentes nesse local. A Mata Atlântica ocorre em Bom Abrigo e Alcatrazes, onde foram também inventariados os maiores números de espécies de briófitas, isto é 40 e 23 táxons. Casca e Castilho são as menores ilhas. Casca é a menor e mais próxima ilha do continente. Nesse local, encontrou-se poucas árvores esparsas da Mata Atlântica e 10 espécies de briófitas. Castilho tem três vezes o tamanho de Casca, mas é uma das ilhas mais distantes do continente. Nesse local, onde os arbustos esparsos da vegetação estão expostos a condições adversas, encontrou-se apenas 4 espécies de briófitas.
Semelhança entre as ilhas quanto à brioflora
A flora de hepáticas ocorrente nas quatro ilhas divide-se em três grupos a saber: Bom Abrigo-Alcatrazes, Casca e Castilho (Fig. 1). O mesmo padrão de distribuição das hepáticas foi observado nos agrupamentos elaborados pelos outros três métodos de ligação, na ordenação das ilhas pelo PCO e excluindo-se as espécies restritas na análise dos dados. A exclusão das espécies restritas evidencia apenas maior semelhança entre Bom Abrigo e Alcatrazes e quase não altera os níveis de ligação de Casca e Castilho, porque os maiores números de espécies restritas foram registrados para as duas primeiras ilhas (Tab. 3). A semelhança entre as ilhas é proporcional ao número das hepáticas em comum e ao número total dessas plantas inventariadas para cada local. O número das hepáticas restritas é menor que o número das hepáticas em comum ou igual, exceto em Bom Abrigo, onde ocorre o inverso. Todavia, é o local onde foi registrado o maior número de espécies em comum com as outras ilhas (Fig. 1 e Tab. 3).
Em relação aos musgos, verificou-se resultados bem diferentes. A flora de musgos divide-se em quatro grupos, cada um correspondendo a uma ilha (Fig. 2). Esse padrão pôde ser também constatado nos dendogramas elaborados pelos outros três métodos de ligação e nos gráficos da ordenação. Todavia, excluindo-se as espécies restritas, o padrão de variação da flora de musgos, assemelha-se ao observado para as briófitas em geral (Fig. 3), porém com níveis de ligação mais baixos nos gráficos de agrupamento. A inclusão dos musgos restritos altera o padrão de distribuição, porque o número dessas espécies é maior que o número de espécies em comum, exceto em Castilho. Alcatrazes e Bom Abrigo apresentam os maiores números de espécies restritas. Entretanto, Casca é a ilha com a flora de musgos mais distinta, devido a presença de apenas uma única espécie em comum com as outras ilhas (Fig. 2 e Tab. 3).
A brioflora divide-se em três grupos a saber: Bom Abrigo-Alcatrazes, Castilho e Casca (Fig. 3). O mesmo padrão foi observado nos agrupamentos elaborados pelos outros três métodos de ligação e na ordenação das ilhas pelo PCO. O número das briófitas em comum e o número das briófitas restritas são proporcionais ao número total de táxons inventariados para as quatro localidades. Todavia, a brioflora é muito distinta entre essas ilhas, pois as espécies restritas representam 75,40% do total inventariado e superam o número das espécies em comum, exceto em Castilho. Em compensação, o padrão de distribuição não se altera, excluindo-se as briófitas restritas na análise dos dados. A exclusão dessas espécies evidencia maior semelhança entre Bom Abrigo e Alcatrazes e pouco altera os níveis de ligação de Castilho e Casca, porque os maiores números dessas plantas foram encontrados para as duas primeiras ilhas (Tab. 2-3).
O padrão de distribuição das hepáticas difere do padrão de distribuição dos musgos. A presença de espécies restritas não altera o padrão de semelhança entre as ilhas quanto à flora de hepáticas, mas torna esses quatro locais mais distintos quanto à flora de musgos. A separação de hepáticas e musgos na análise multivariada dos dados, possibilitou verificar que Bom Abrigo e Alcatrazes assemelham-se devido à flora de hepáticas (Fig. 1, 3). Entre Bom Abrigo e Alcatrazes, foi registrado o maior número de espécies em comum (sete hepáticas e dois musgos), justificando-se o agrupamento de ambas. Existe maior número de briófitas restritas em Casca que em Castilho (Tab. 3), justificando o agrupamento da Fig. 3. Todavia, excluindo-se as espécies restritas, observa-se maior número de briófitas em comum entre Bom Abrigo-Alcatrazes e Casca (três hepáticas e um musgo) que entre Bom Abrigo-Alcatrazes e Castilho (uma hepática e dois musgos). Portanto, a semelhança entre Castilho e Casca com o agrupamento Bom Abrigo-Alcatrazes, deve-se ao número de musgos em comum (Fig. 2-3). A brioflora mais distinta foi registrada para a Ilha da Casca.
O agrupamento das ilhas dependeu em grande parte da presença das espécies em comum, devido à utilização do índice de Sörensen nos dendogramas e gráficos de ordenação. E, para o presente trabalho, considerou-se mais adequado utilizar um índice que enfatize as co-presenças das espécies, pois as co-ausências podem indicar tanto espécies não amostradas, quanto a ausência das mesmas em determinadas ilhas.
Substratos mais utilizados pelas briófitas nas ilhas
As ilhas também se assemelham, quanto à presença de grupos de briófitas associados a diferentes tipos de substratos.
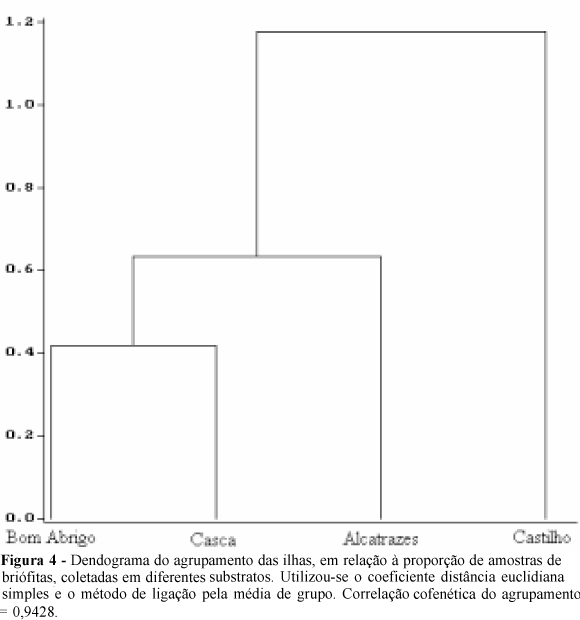
Em relação à proporção de amostras de hepáticas e musgos terrestres, saxícolas, corticícolas e os coletados em cimento (Tab. 3), a brioflora divide-se em dois grupos a saber: Bom Abrigo ¾ Casca ¾ Alcatrazes, as três ilhas que possuem vegetação de Mata Altântica e Castilho, onde a vegetação em terreno rochoso está exposta a condições adversas (Fig. 4 e Tab. 1). Esse padrão de distribuição foi também observado nos dendogramas elaborados pelos outros três métodos de ligação.
Os grupos de briófitas que contribuem para esse agrupamento são evidenciados no gráfico da ordenação pelo PCA, cuja representação dos eixos 1 e 2 já explicam 98,60% da variação dos dados. (Fig. 5). Assim, Bom Abrigo se agrupa com Casca, devido à presença de musgos terrestres e os coletados em cimento, que foram encontrados somente nesses dois locais. Alcatrazes está mais próxima desse grupo, devido à presença de hepáticas corticícolas, as quais foram coletadas somente nessas três ilhas e em proporções semelhantes. Alcatrazes também se aproxima desse agrupamento, devido à presença de musgos corticícolas, que foram coletados somente nessa ilha e em Bom Abrigo. Hepáticas e musgos saxícolas foram coletados em todas as quatro ilhas, mas as maiores proporções dessas plantas foram registradas para Castilho, que é considerada a ilha mais distinta, pela presença de briófitas exclusivamente em rochas. As hepáticas ocorrentes em solo foram coletadas somente em Bom Abrigo.
A brioflora está representada por hepáticas saxícolas e corticícolas e musgos saxícolas nas quatro ilhas visitadas (Fig. 5). Os vetores referentes a essas plantas são mais explicados pelo eixo 1, que retém 79,10% da variância dos dados. Na tabela 3, observa-se que essas plantas foram coletadas nas quatro ilhas e que estão representadas pelos maiores valores de proporção de amostras, exceto em Castilho, onde não se encontrou hepáticas corticícolas. Os vetores referentes aos musgos corticícolas, terrestres e os coletados em cimento são quase totalmente explicados pelo eixo 2, que retém apenas 19,50% da variância dos dados. Essas plantas foram encontradas em somente duas das quatro ilhas e estão representadas pelos menores valores de proporção de amostras. As hepáticas terrestres correspondem ao menor vetor, o qual atinge o tamanho máximo na representação do eixo 3, que retém apenas 1,40% da variância dos dados. Essas plantas foram encontradas somente em Bom Abrigo e estão representadas pelo valor mais baixo de proporção de amostras coletadas (Fig. 5 e Tab. 3).
Quinze espécies são citações inéditas para determinados tipos de substratos. Oito delas foram encontradas exclusivamente neles: Chonecolea doellingeri (Nees) Grolle, Lejeunea villaumei(Steph.) Grolle, Campylopus trachyblepharon (Müll. Hal.) Mitt., Fissidens submarginatus Bruch, Holomitrium crispulum Mart. e Syrrhopodon africanus (Mitt.) Paris ssp. graminicola (R.S. Williams) W.D. Reese em rochas; Chiloscyphus vermicularis (Lehm.) Hässel, na base de troncos vivos e, Groutiella apiculata (Hook.) H.A. Crum & Steere, na calçada de uma tapera. Sete espécies foram coletadas em mais de um tipo de substrato, dentre os quais alguns não foram ainda relacionados para essas briófitas na literatura disponível e se referem a solo para Helicodontium capillare(Hedw.) A. Jaeger, rochas para Cheilolejeunea discoidea (Lehm. & Lindenb.) Kachroo & R.M. Schust. (Ilha de Alcatrazes), Drepanolejeunea mosenii (Steph.) Bischl., Frullania neesiiLindenb., Lejeunea brittoniae (A. Evans) Grolle (Ilha de Alcatrazes) e Schlotheimia torquata (Hedw.) Brid.e solo e rochas para Lejeunea phyllobola Nees & Mont. ex Mont. (Ilha do Bom Abrigo).
A rocha é o substrato mais disponível para as 15 espécies relacionadas acima, que foram encontradas em Alcatrazes e Castilho, onde a costa é rochosa e existe vegetação em terreno rochoso. Em Castilho, as briófitas crescem somente em rochas sem guano. Por outro lado, a rocha pode ser o substrato preferido por essas espécies, que foram encontradas em Bom Abrigo e Casca., pois nessas duas últimas ilhas, não existe vegetação em terrenos rochosos (Tab. 1).
Comparação com a brioflora da Ilha de Marajó e de Fernando de Noronha
O maior grupo de ilhas do planeta, a Ilha de Marajó, está situado na foz do Rio Amazonas, onde o clima é equatorial úmido e, a paisagem, formada por floresta tropical úmida, campos e áreas urbanas (Lisboa & Maciel, 1994; Lisboa et al., 1998, 1999). A brioflora encontrada nas quatro ilhas paulistas é distinta da registrada para essa ilha do norte do país. O número de espécies em comum equivale a 16,4% do total inventariado para Marajó e 14,7% do total relacionado para Alcatrazes, Bom Abrigo, Casca e Castilho e se refere as seguintes espécies: Bryum apiculatum Schwägr., Callicostella pallida (Hornsch.) Ångstr., Calymperes palisotii Schwägr., Hyophila involuta (Hook.) A. Jaeger, Isopterygium tenerum (Sw.) Mitt., Octoblepharum albidum Hedw., Philonotis uncinata (Schwägr.) Brid., Sematophyllum subpinnatum (Brid.) E. Britton e Syrrhopodon incompletus Schwägr.Callicostella pallida (Hornsch.) Ångstr. é uma espécie corticícola e epífila na Ilha de Marajó, mas terrestre em Bom Abrigo e saxícola em Alcatrazes; Calymperes palisotii Schwägr. é terrestre, corticícola e epífila em Marajó, porém saxícola em Alcatrazes e Syrrhopodon incompletus Schwägr. é corticícola em Marajó, todavia saxícola em Bom Abrigo e Castilho.
Fernando de Noronha representa um grupo de ilhas vulcânicas, que se localiza próximo ao Equador. O clima é semi-árido e a vegetação, similar à caatinga encontrada na região nordeste do Brasil (Vital et al., 1991). A brioflora encontrada em Alcatrazes, Bom Abrigo, Casca e Castilho é também distinta da registrada para Fernado de Noronha. O número de espécies em comum representa 27,3% do total inventariado para esse último local e 9,8% do total relacionado para as ilhas paulistas. Os táxons em comum são Frullania ericoides (Nees) Mont., Lejeunea laetevirens Nees & Mont., Bryum coronatum Schwägr., Calymperes palisotii Schwägr., Fissidens submarginatus Bruch (como F. intermedius Müll. Hal.) e Octoblepharum albidum Hedw. Fissidens submarginatus Bruch foi coletada somente em barrancos úmidos em Fernando de Noronha e, exclusivamente em rochas, em Alcatrazes e Castilho.
Calymperes palisotii Schwägr. e Octoblepharum albidum Hedw. são as únicas espécies encontradas tanto nas ilhas do estado de São Paulo, quanto na Ilha de Marajó e de Fernando de Noronha.
Agradecimentos
Os autores gostariam de agradecer ao Dr. Dale Vitt, da Universidade de Alberta, Edmonton, Canadá, pelas valiosas sugestões que foram incorporadas ao presente trabalho.
2 Instituto de Botânica, Caixa Postal 4005, CEP 01061-970 São Paulo-SP, Brazil
- Ângelo, S. & Lino, C.F. (coord.). 1989. Ilhas do Litoral Paulista Săo Paulo (Estado), Divisăo de Reservas e Parques Estaduais da Secretaria do Meio Ambiente, Departamento de Geografia da Universidade de Săo Paulo e Conselho de Defesa do Patrimônio Histórico, Arqueológico, Artístico e Turístico do Estado de Săo Paulo da Secretaria da Cultura, 49p.
- Bischler, H. 1967. Le genre Drepanolejeunea Steph. en Amérique Centrale et Méridionale - II Revue Bryologique et Lichénologique 35 (1-4): 95-134.
- Buck, W.R. 1986. Wijkia (Sematophyllaceae) in the New World. Hikobia 9: 297-303.
- Digby, P.G.N. & Kempton, R.A. 1987. Multivariate analysis of ecological communities. Chapman & Hall. 206p.
- Edwards, S.R. 1980. A revision of West Tropical African Calymperaceae I. Introduction and Calymperes Journal of Bryology 11: 49-93.
- Engel, J.J. 1978. A taxonomic and phytogeographic study of Brunswick Peninsula (Strait of Magellan) Hepaticae and Anthocerotae Fieldiana Botany 41: 319p.
- 1980. A monograph of Clasmatocolea (Hepaticae). Fieldiana Botany, no. 3, 229p.
- Evans, A.W. 1911. Hepaticae of Puerto Rico. X. Cololejeunea, Leptocolea and Aphanolejeunea Bulletin of the Torrey Botanical Club 38 (6): 251-286.
- Florschütz, P.A. 1964. The mosses of Suriname Leiden: E.J. Brill, 271p.
- Frahm, J.-P. 1991. Flora Neotropica. Monograph 54. Dicranaceae: Campylopodioideae, Paraleucobryoideae. Organization for Flora Neotropica, New York Botanical Garden, p. 1-238.
- Gepp, A. 1891. Musci & Hepaticae. In: H.N. Ridley. Notes on the botany of Fernando de Noronha. Journal of the Linnean Society of London Botany 27: 74-75.
- Gradstein, S.R. 1994. Flora Neotropica, Monograph 62. Lejeuneaceae: Ptychantheae, Brachiolejeunea Organization for Flora Neotropica. New York Botanical Garden, p. 1-216.
- & Beek, J. van. 1985. A revision of the genus Symbezidium Trevis. Beiheft zur Nova Hedwigia 80: 221-248.
- & Buskes, G.M.C. 1985. A revision of Neotropical Archilejeunea(Spruce) Schiffn. Beiheft zur Nova Hedwigia 80: 89-112.
- Ireland, R. R. 1992. The moss genus Isopterygium (Hypnaceae) in Latin America. Tropical Bryology 6: 111-132.
- Jones, E.W. 1974. African hepatics XXVI. The Lejeunea eckloniana complex. Journal of Bryology 8 (1): 77-91.
- 1979. African hepatics XXXI. Some new or little-known Lejeuneaceae and extensions of range. Journal of Bryology 10 (4): 387-400, 1979.
- Jovet-Ast, S. 1947. Hépatiques des Antilles françaises récoltées par P. et V. Allorge en 1936. Revue Bryologique et Lichénologique 16 (1-2): 17-46.
- Kachroo, P. & Schuster, R.M. 1961. The genus Picnolejeunea and its affinities to Cheilolejeunea, Euosmolejeunea, Nipponolejeunea, Tuyamaella, Siphonolejeunea and Strepsilejeunea Journal of the Linnean Society of London Botany 56: 475-511.
- Lisboa, R.C.L. & Lima, M.J.L. de & Maciel, U.N. 1999. Musgos da Ilha de Marajó - II ž Município de Anajás, Pará, Brasil. Acta Amazonica 29 (2): 201-206.
- & Maciel, U.N. 1994. Musgos da Ilha de Marajó ž I ž Afuá (Pará). Boletim do Museu Paraense Emílio Goeldi. Sér. Botânica 10 (1): 43-55.
- & Muniz, A.C.M. & Maciel, U.N. 1998. Musgos da Ilha de Marajó ž III ž Chaves (Pará). Boletim do Museu Paraense Emílio Goeldi. Sér. Botânica 14 (2): 117-125.
- MacArthur, R.H. & Wilson, E.O. 1967. The theory of island biogeography Princeton University Press, 203p.
- Manly, B.F.J. 1994. Multivariate statistical methods - a primer Chapman & Hall. 215p.
- Martius, C.F.P. 1828-1834. Icones plantarum cryptogamicarum Monachii: Impensis auctoris, p. 1-138.
- Menéndez, G.G.H. de, 1995. Little known Chiloscyphus (Hepatophyta) species from Southern South America 2. The Journal of the Hattori Botanical Laboratory 78: 63-81.
- Mizutani, M. 1982. Notes on the Lejeuneaceae. 6. Japanese species of the genus Cheilolejeunea The Journal of the Hattori Botanical Laboratory 51: 151-173.
- Mohamed, M.A.H. 1979. A taxonomic study of Bryum billardieri Schwaegr. and related species. Journal of Bryology 10: 401-465.
- Ochi, H. 1980. A revision of the Neotropical Bryoideae, Musci (First part). The Journal of the Faculty of Education Tottori University, Natural Science 29 (2): 49-154.
- Pompéia, S.L., Pereira, A., Rossi, L., Aidar, M.P.M., Moraes, R.P. & Santos, R.P. 1994. A vegetaçăo da Ilha de Alcatrazes - Săo Paulo. Anais do III Simpósio de Ecossistemas da Costa Brasileira, Serra Negra-SP, 1993, ACIESP 2: 54-67.
- Schuster, R.M. 1966. The Hepaticae and Anthocerotae of North America. East of the Hundredth Meridian Columbia University Press, 1: 1-802.
- —. 1980. The hepaticae and anthocerotae of North America. East of the Hundredth Meridian. Columbia University 4: 1-1334.
- Sharp, A.J., Crum, H. & Eckel, P.M. (eds.). 1994. The moss flora of Mexico. Sphagnales to Bryales, Memoirs of the New York Botanical Garden 69: 1-1113.
- Sneath, P.H.A & Sokal, R.R. 1973. Numerical taxonomy. The principles and practice of numerical classification. W.H. Freeman & Co. 573p.
- Stotler, R. 1969. The genus Frullaniasubgenus Frullania in Latin America. Nova Hedwigia 18: 397-555.
- Udar, R. & Awathi, U.S. 1982. The genus Schiffneriolejeunea Verd. (Hepaticae) in India. Lindbergia 8 (1): 55-59.
- Vanden-Berghen, C. 1976. Frullaniaceae (Hepaticae) africaine. Bulletin du Jardin Botanique National de Belgique 46:1-220.
- Visnadi, S.R. 1993. Meteoriaceae (Bryopsida) da mata tropical pluvial de encosta - "Mata Atlântica"- do Estado de Săo Paulo. Dissertaçăo de Mestrado, Universidade Estadual Paulista "Júlio de Mesquita Filho", Rio Claro. 296p.
- 1998. Briófitas em ecossistemas costeiros do Núcleo Picinguaba do Parque Estadual da Serra do Mar, Ubatuba-SP. Tese de Doutorado, Universidade Estadual Paulista "Júlio de Mesquita Filho", Rio Claro. 274p.
- & Vital, D.M. 1995. Bryophytes from restinga in Setiba State Park, Espírito Santo State, Brazil, Tropical Bryology 10: 69-74.
- & Vital, D.M. 1997. Bryophytes from greenhouses of the Institute of Botany, Săo Paulo, Brazil. Lindbergia 22 (1): 44-46.
- Vital, D.M., Giancotti, C. & Pursell, R.A. 1991. The bryoflora of Fernando de Noronha, Brasil. Tropical Bryology 4: 23-24.
- & Visnadi, S.R. 1994. Bryophytes of Rio Branco Municipality, Acre, Brazil. Tropical Bryology 9: 69-74.
- & Visnadi, S.R. 2000. New records and notes on Brazilian bryophytes. The Journal of the Hattori Botanical Laboratory 88: 279-285.
- Yano, O. 1981. A checklist of Brazilian mosses. The Journal of the Hattori Botanical Laboratory 50: 279-456.
- 1984. Checklist of Brazilian liverworts and hornworts. The Journal of the Hattori Botanical Laboratory 56: 481-548.
- 1989. An additional checklist of Brazilian bryophytes. The Journal of the Hattori Botanical Laboratory 66: 371-434.
- 1995. A new additional annotated checklist of Brazilian bryophytes. The Journal of the Hattori Botanical Laboratory 78: 137-182.
- 1996. A checklist of the Brazilian bryophytes. Boletim do Instituto de Botânica de Săo Paulo 10: 47-232.
- Yuzawa, Y. 1988. Some little-known species of Frullania subgen. Diastaloba described from Latin America. The Journal of the Hattori Botanical Laboratory 64: 437-449.
- & Hattori, S. 1988. A new Frullania species from Brazil. Journal of the Japanese Botany 63 (1): 30-32.
Datas de Publicação
-
Publicação nesta coleção
25 Fev 2002 -
Data do Fascículo
Ago 2001
Histórico
-
Aceito
07 Maio 2001 -
Recebido
03 Ago 2000