Resumos
A Reserva Biológica Estadual da Praia do Sul (Ilha Grande, RJ) é um importante remanescente de restinga preservada do Rio de Janeiro. A vegetação das restingas não é homogênea, distribuindo-se em zonas de vegetação, e cada uma delas é caracterizada por sua topografia, fisionomia e florística distintas. Estudamos a comunidade de Bromeliaceae, analisando variações na riqueza, abundância, densidade e freqüência de ocorrência entre quatro zonas de vegetação. Nas quatro zonas, amostramos um total de 150 parcelas de 100 m² cada, onde contabilizamos as espécies e suas abundâncias, e medidas de estrutura da vegetação (altura e DAP das árvores e densidade de árvores e de arbustos do sub-bosque). Testamos diferenças entre zonas na abundância de rosetas e na estrutura da vegetação, e entre as abundâncias das espécies de bromélias através de ANOVA seguida do teste de Tukey. Encontramos 16 espécies de bromélias, com abundâncias e padrões de distribuição distintos entre as zonas, além de diferenças significativas entre as abundâncias das espécies. Os dados indicam que a elevada riqueza de espécies encontradas na RBEPS pode estar relacionada à heterogeneidade e à complexidade locais. As diferenças encontradas entre as zonas de vegetação podem ser devidas às diferenças na estrutura da vegetação de cada zona.
Bromeliaceae; restinga; heterogeneidade; Ilha Grande
The Praia do Sul State Biological Reserve (Ilha Grande, RJ) is an important remnant of Restinga habitat in Rio de Janeiro State. Restinga vegetation is not homogeneous and it is distributed in different vegetation zones, each zone having different topography, physiognomy and flora. We analyzed ecological parameters of the bromeliad community such as richness, abundance, density, biomass and variation in species composition in four vegetation zones. We sampled 150 plots of 100 m² (10×10 m), distributed in the four vegetation zones, recording the bromeliad species and their abundance, and measuring the height, dbh, and density of the trees. We tested differences in ramet abundance and vegetation complexity between the four vegetation zones with ANOVA followed by Tukey's test. We found a total of 16 bromeliad species, with different abundances and distribution patterns between the four vegetation zones, and with significant differences in abundance between species. The data indicate that the high species richness found in the Biological Reserve is related to local heterogeneity and complexity. The differences found between vegetation zones seem to be related to the vegetation structure of each zone.
Bromeliaceae; restinga; heterogeneity; Ilha Grande
Bromeliaceae da restinga da Reserva Biológica Estadual da Praia do Sul: composição, abundância e similaridade da comunidade
Bromeliaceae of the Praia do Sul State Biological Reserve restinga: community composition, abundance and similarity
André Felippe Nunes-FreitasI, 1 1 Autor para correspondência: afnfreitas@ufrrj.br ; Thereza Christina Rocha-PessôaII; Luciana Cogliatti-CarvalhoII; Carlos Frederico Duarte RochaII
IUniversidade Federal Rural do Rio de Janeiro, Instituto de Florestas, Departamento de Ciências Ambientais, Rodovia BR-465 km 7, 23890000 Seropédica, RJ, Brasil
IIUniversidade do Estado do Rio de Janeiro, Departamento de Ecologia, Instituto de Biologia Roberto Alcântara Gomes, Rua São Francisco Xavier 524, Maracanã, 20550-011 Rio de Janeiro, RJ, Brasil
RESUMO
A Reserva Biológica Estadual da Praia do Sul (Ilha Grande, RJ) é um importante remanescente de restinga preservada do Rio de Janeiro. A vegetação das restingas não é homogênea, distribuindo-se em zonas de vegetação, e cada uma delas é caracterizada por sua topografia, fisionomia e florística distintas. Estudamos a comunidade de Bromeliaceae, analisando variações na riqueza, abundância, densidade e freqüência de ocorrência entre quatro zonas de vegetação. Nas quatro zonas, amostramos um total de 150 parcelas de 100 m2 cada, onde contabilizamos as espécies e suas abundâncias, e medidas de estrutura da vegetação (altura e DAP das árvores e densidade de árvores e de arbustos do sub-bosque). Testamos diferenças entre zonas na abundância de rosetas e na estrutura da vegetação, e entre as abundâncias das espécies de bromélias através de ANOVA seguida do teste de Tukey. Encontramos 16 espécies de bromélias, com abundâncias e padrões de distribuição distintos entre as zonas, além de diferenças significativas entre as abundâncias das espécies. Os dados indicam que a elevada riqueza de espécies encontradas na RBEPS pode estar relacionada à heterogeneidade e à complexidade locais. As diferenças encontradas entre as zonas de vegetação podem ser devidas às diferenças na estrutura da vegetação de cada zona.
Palavras-chave: Bromeliaceae, restinga, heterogeneidade, Ilha Grande
ABSTRACT
The Praia do Sul State Biological Reserve (Ilha Grande, RJ) is an important remnant of Restinga habitat in Rio de Janeiro State. Restinga vegetation is not homogeneous and it is distributed in different vegetation zones, each zone having different topography, physiognomy and flora. We analyzed ecological parameters of the bromeliad community such as richness, abundance, density, biomass and variation in species composition in four vegetation zones. We sampled 150 plots of 100 m2 (10×10 m), distributed in the four vegetation zones, recording the bromeliad species and their abundance, and measuring the height, dbh, and density of the trees. We tested differences in ramet abundance and vegetation complexity between the four vegetation zones with ANOVA followed by Tukey's test. We found a total of 16 bromeliad species, with different abundances and distribution patterns between the four vegetation zones, and with significant differences in abundance between species. The data indicate that the high species richness found in the Biological Reserve is related to local heterogeneity and complexity. The differences found between vegetation zones seem to be related to the vegetation structure of each zone.
Key words: Bromeliaceae, restinga, heterogeneity, Ilha Grande
Introdução
As restingas são habitats característicos do litoral brasileiro, pertencentes ao Bioma Mata Atlântica, que podem ser definidas como longas faixas de depósitos arenosos marinhos (Dansereu 1947; Suguio & Tessler 1984), datados do Quaternário (Araújo 1992; Araújo et al. 1998; Scarano 2002), sobre as quais é encontrada uma comunidade vegetal característica (Lacerda et al. 1982; Rizzini 1992). Estas formações cobrem cerca de 79% da costa brasileira (Lacerda et al. 1993) e as espécies nelas encontradas apresentam um conjunto de adaptações relativas às condições extremas deste ambiente, como a elevada salinidade, a baixa disponibilidade de água e a intensa radiação solar (Scarano et al. 2001).
Os habitats de restinga vêm sendo altamente perturbados, especialmente devido à ação antrópica causada pela especulação imobiliária (Lacerda et al. 1982; Leme 1985; Rocha et al. 2003; Rocha et al. 2004). Como resultado, várias restingas têm sofrido uma sucessiva modificação da paisagem, com uma elevada taxa de desmatamento (Fundação SOS Mata Atlântica/INPE 2001; Rocha et al. 2003). Apesar da elevada pressão antrópica e da enorme perda de área sofrida por estes habitats, sabe-se que as restingas apresentam uma considerável diversidade biológica, a qual tem sido conhecida devido ao acúmulo de estudos realizados (para uma revisão veja Rocha et al. 2004).
A vegetação das restingas não é homogênea, e se distribui em diferentes zonas de vegetação ou mesohabitats (Rocha et al. 2004). Essas zonas de vegetação podem se dispor tanto paralela quanto transversalmente ao mar e cada uma delas é caracterizada por sua topografia, fisionomia e florística distintas (Ormond 1960).
A família Bromeliaceae é considerada uma das famílias mais representativas nas restingas, sendo este o segundo habitat com o maior número de espécies no Rio de Janeiro (Fontoura et al. 1991), atrás apenas da Floresta Ombrófila Densa. Muitos estudos sobre a família têm sido realizados nas restingas, em sua maioria levantamentos fitossociológicos e listas preliminares da flora (Araújo & Oliveira 1988; Fontoura et al. 1991; Araújo et al. 1998) ou de ecologia (Cogliatti-Carvalho et al. 2000; Zaluar & Scarano, 2000; Lopez & Rios 2001; Scarano 2002; Scarano et al. 2001; Sampaio et al. 2002; Mantovani & Iglesias 2001; Pinheiro & Borghetti 2003).
A Reserva Biológica Estadual da Praia do Sul (RBEPS), localizada na porção sudoeste da Ilha Grande, foi criada em 1981. Grande parte da REBPS é composta pelo ambiente de restinga, tendo sido realizados nas últimas duas décadas estudos relacionados à flora e à estrutura da vegetação da reserva (Araújo & Oliveira 1988; De Paula et al. 1994; Oliveira & Coelho Netto 1996; D.D. Toffoli, dados não publicados; Araújo et al. 1997; Toffoli & Oliveira 1999). As informações disponíveis sobre a taxocenose de bromélias na RBEPS tiveram início com o estudo de Araújo & Oliveira (1988), no qual os autores relacionaram 15 espécies de bromélias para a área. Porém, estudos enfocando especificamente a taxocenose de Bromeliaceae na RBEPS não são encontrados na literatura.
Neste estudo, avaliamos a variação nos parâmetros populacionais (densidade e abundância) e da comunidade (composição, riqueza e similaridade) da família Bromeliaceae da restinga da Praia do Sul como um todo e entre suas zonas de vegetação. Buscamos responder às seguintes questões: i) Qual a composição e a riqueza de espécies de bromeliáceas na RBEPS e em cada zona de vegetação? ii) Quais são as distribuições de abundância total de bromeliáceas na restinga como um todo e em cada uma das zonas de vegetação? iii) Qual a similaridade na composição de Bromeliaceae entre as zonas de vegetação? iv) Em que extensão a variação na composição, riqueza, diversidade, abundância e densidade de bromélias em cada zona de vegetação da restinga estão relacionadas à variação das condições ambientais e estruturais dessas zonas?
Material e métodos
Área de estudo A Reserva Biológica Estadual da Praia do Sul (RBEPS) está localizada na porção sudoeste da Ilha Grande e possui uma área de 3.600 ha (Araújo & Oliveira 1988). A reserva foi estabelecida em dezembro de 1981, e está sob a guarda da Fundação Estadual e Engenharia do Meio Ambiente (FEEMA) desde abril de 1982 (Araújo & Oliveira 1988). Cerca de 22,2% da área da RBEPS é ocupada por uma planície arenosa constituída por dois cordões de vegetação formados a partir do Holoceno (Amador 1985; 1988). O cordão mais interno apresenta uma elevação máxima de 10 m, enquanto o mais externo varia entre 4 e 6 m (Amador 1985; 1988). Os cordões são separados pelo canal que dá vazão as lagoas do Sul e do Leste, localizadas entre o cordão interno e o sopé da serra de Araçatiba. Este mesmo canal desemboca no mar, ao lado da ilhota do Leste, separando as praias do Sul e do Leste.
A planície arenosa da RBEPS, sobre a qual está a restinga, apresenta uma grande variação geomorfológica (Amador 1985). Devido a essa variação, a composição florística da restinga não é homogênea, sendo formada por diferentes comunidades vegetais (Amador 1985; Araújo & Oliveira 1988). Segundo Araújo & Oliveira (1988), na RBEPS podem ser identificadas quatro grandes comunidades vegetais: psamófila reptante de anteduna, floresta de cordão arenoso, mata alagadiça de planície e manguezal. Entre a vegetação psamófila reptante e a mata de cordão arenoso existe uma zona de vegetação densa (Araújo & Oliveira 1988), que pode ser denominada como vegetação fechada de pós-praia, segundo classificação de Araújo et al. (1998). Uma área de vegetação de transição entre a mata de cordão arenoso e a mata de encosta (Oliveira 2002) e uma área de transição entre o cordão arenoso e a mata alagadiça (este estudo) também podem ser identificadas.
Metodologia Realizamos as amostragens em quatro zonas distintas: vegetação fechada de pós-praia (FPP) - vegetação arbustiva densa, localizada após a comunidade psamófila reptante; floresta de cordão arenoso (FR) - localizada sobre o cordão externo da restinga, é uma floresta baixa (10 m de altura), com troncos relativamente finos e com o sub-bosque denso; em alguns pontos, apresenta-se descontínua, com moitas de até 5 m de altura, especialmente nas áreas onde houve ação antrópica no passado; floresta de transição (FT) - vegetação com porte semelhante ao da FR, localizada entre o cordão arenoso e a mata de encosta, apresentando elementos de transição entre essas duas áreas; Vegetação de moitas densas (MD): localizada no final do cordão externo da praia do Leste, apresenta-se como uma vegetação composta por moitas densas e de porte baixo (8 m de altura), muitas vezes contíguas, tendo sofrido ação antrópica no passado (Oliveira 2002).
Estudamos a comunidade de bromeliáceas na RBEPS estabelecendo 120 parcelas de 100 m2 (10×10 m), distribuídas entre as quatro zonas de vegetação (N = 30 parcelas por zona de vegetação). As parcelas foram feitas em linhas paralelas ao mar, estando cada parcela distante 10 m da seguinte. Em cada parcela registramos as espécies de bromeliáceas presentes e o número total de rosetas de cada espécie.
Para testarmos as diferenças na estrutura da vegetação entre as quatro zonas amostradas, medimos a altura e o diâmetro a altura do peito (DAP) das árvores presentes em cada parcela e contabilizamos a abundância daquelas árvores com DAP superior a 10 cm. Estimamos a densidade do sub-bosque, utilizando uma subparcela de 20 m2 (10×2 m), localizada no centro de cada parcela de 100 m2 e, posteriormente, transformamos para o número de indivíduos por hectare.
Calculamos a abundância, a freqüência de ocorrência e a densidade de cada uma das espécies de bromélias, tanto por zona de vegetação quanto para a área de restinga como um todo (Mueller-Dumbois & Ellenberg 1974). Testamos eventuais diferenças nas abundâncias de rosetas e nas medidas de estrutura da vegetação entre zonas através de análise de variância (ANOVA) seguida do teste de Tukey (Zar 1999). Também utilizamos a ANOVA seguida do teste de Tukey para testarmos diferenças nas abundâncias entre espécies. Quando os dados não apresentavam distribuição normal, realizamos transformação logarítmica, isto é, log (abundância + 1) (Zar 1999). Calculamos a similaridade no número de espécies entre as áreas através do índice de similaridade de Jaccard (Cj) (Magurran 1988):
Para descrevermos a similaridade relativa entre as quatro zonas de vegetação, realizamos uma análise de agrupamentos, utilizando como medida a distância Euclidiana entre as similaridades encontradas entre as zonas de vegetação (Zar 1999). Essa análise foi feita a partir de uma matriz de abundância das espécies de cada uma das quatro zonas.
Resultados
Na RBEPS foram amostradas 16 espécies de bromélias, pertencentes a oito gêneros de duas subfamílias, Bromelioideae e Tillandsioideae. A subfamília com o maior número de gêneros e espécies foi Bromelioideae, com seis gêneros e nove espécies (Aechmea distichantha Lemaire, A. nudicaulis (Linaeus) Grisebach, A. pectinata Baker, Billbergia amoena (Loddiges) Lindley, Bromelia anthiacantha Bertoloni, Edmundoa ambigua (Wanderley & Leme) Leme, E. lindenii (Regel) Leme, Neoregelia johannis (Carriére) L.B. Smith e Nidularium inocentii Lemaire), enquanto a subfamília Tillandsioideae ocorreu com dois gêneros e sete espécies (Tillandsia gardineri Lindley, T. geminiflora Brongniart, T. stricta Solander, T. tenuifolia Linnaeus, Vriesea gigantea Gaudichaud, V. procera (Martius ex Schultes f.) Wittmark, V. rodigasiana E. Morren). Dentre os gêneros, o que ocorreu com o maior número de espécies foi Tillandsia (S = 4), seguido de Vriesea e Aechmea (ambas com três espécies).
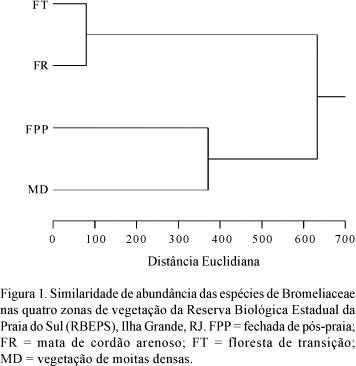
As zonas de vegetação apresentaram dois agrupamentos distintos: um entre as zonas de vegetação FPP e MD e outro entre as zonas de vegetação FR e FT, que tiveram uma menor distância (Fig. 1). As medidas de estrutura da vegetação diferiram entre as quatro zonas amostradas, sendo que FR e FT apresentaram os maiores valores de densidade de árvores, altura e DAP médios das árvores, enquanto as zonas MD e FPP apresentaram as maiores médias de densidade de sub-bosque (DSB) (Tab. 1). Houve diferenças significativas entre as zonas de vegetação nas variáveis densidade de árvores (F326 = 16,05; p < 0,001); altura das árvores com DAP ³ 10 cm (F326 = 14,41; p < 0,001); DAP das árvores (F326 = 3,47; p < 0,05); e densidade do subbosque (F326 = 30,31; p < 0,001;) (Tab. 1).
Houve diferença significativa na abundância de rosetas entre as zonas de vegetação (F326 = 4,40; p = 0,005), com diferenças entre FPP e FR (p = 0,006) e entre a FPP e a FT (p = 0,031) (Tab. 2).
A riqueza (Tab. 1) e a composição (Tab. 2) de espécies entre as quatro zonas de vegetação amostradas foi distinta. A zona de vegetação que teve a maior riqueza foi FR (S = 15), enquanto as menores riquezas foram encontradas na FPP e na MD (ambas com S = 7) (Tab. 1). A similaridade entre as zonas de vegetação variou, sendo a maior encontrada entre as zonas FR e FT (Cj = 56,3%), enquanto a menor ocorreu entre as zonas FPP e MD (Cj = 27,3%) (Tab. 3).
A abundância, freqüência de ocorrência e densidade das espécies de bromélias variaram entre as zonas de vegetação. Das 16 espécies amostradas, apenas Aechmea nudicaulis, Neoregelia johannis e Vriesea procera foram encontradas em todas as zonas de vegetação. A espécie com maiores abundância, freqüência de ocorrência e densidade na área foi Billbergia amoena, enquanto V. rodigasiana teve os menores valores para estes parâmetros (Tab. 2). Houve diferença significativa entre as abundâncias das espécies de bromélias amostradas na RBEPS (F1514 = 17,86; p < 0,005).
Discussão
Neste estudo amostramos uma riqueza total de 16 espécies de Bromeliaceae nas quatro zonas de vegetação estudadas na RBEPS. Esse valor de riqueza é semelhante ao registrado por Araújo & Oliveira (1988), que citaram 15 espécies para as diferentes zonas de vegetação da restinga e um total de 19 quando incluída a mata de encosta. Das 15 espécies registradas para a restinga por estes autores, nós amostramos 10 e acrescentamos outras cinco (Edmundoa ambigua, Neoregelia johannis, Tillandsia gardinerii, T. stricta e Vriesea gigantea) que ainda não haviam sido registradas na área. Além disso, registramos V. rodigasiana no habitat de restinga, que só havia sido citada pelos autores para as áreas de mangue e de mata de encosta (Araújo & Oliveira 1988). Nossos dados elevaram a lista de Bromeliaceae da RBEPS para um total de 24 espécies em toda a reserva, sendo 21 na área de restinga, o que deve ser resultado do esforço amostral mais intenso empregado neste estudo, que possibilitou o encontro de espécies que ocorrem em menor densidade na área. A utilização de um esforço amostral maior ou mais intenso, tanto no tempo quanto no espaço, pode levar a um aumento do conhecimento da riqueza de uma área, já que espécies consideradas raras ou pouco freqüentes podem ser mais rapidamente amostradas (e.g. Rosenzweig 1998; Thompson et al. 2003), como foi o caso das espécies acrescentadas à listagem.
Bromeliaceae tem sido citada como uma das famílias mais representativas nas restingas (Henriques et al. 1986; Sá 1992; Fabris & Pereira 1998; Pereira & Zambom 1998; Cogliatti-Carvalho et al. 2001), especialmente no leste brasileiro. Os dados disponíveis para diferentes áreas de restinga apresentam valores de riqueza entre 4 e 14 (T.C. Rocha-Pessôa, dados não publicados). Em alguns casos, essa média de riqueza é consistentemente superior, como na restinga de Ipitangas (RJ) (S = 23; Sá 1992), no Parque Estadual Paulo César Vinhas (ES) (S = 21; J.M.L. Gomes, dados não publicados) e na Ilha do Mel (PR) (S = 32; S. Menezes-Silva, dados não publicados). No total, na restinga da RBEPS registramos 21 espécies, um valor superior à média sugerida por T.C. RochaPessôa (dados não publicados). Essas diferenças de riqueza de bromélias entre as restingas podem ser explicadas primariamente pelas diferenças no esforço de amostragem e do número de zonas de vegetação amostradas.
Especialmente nas restingas, os microhabitats mais favoráveis para o estabelecimento e desenvolvimento de espécies de bromélias não ocorrem de forma homogênea, mas em manchas (Freitas et al. 2000; Cogliatti-Carvalho et al. 2001). Os recursos (substrato apropriado, luminosidade, umidade e temperatura favoráveis) localizam-se onde a vegetação é mais densa, normalmente próximo ou dentro de moitas, ou em áreas sombreadas (Franco et al. 1984; Hay & Lacerda 1984; Henriques et al. 1986; Pereira 1990; Fialho & Furtado 1993; Freitas et al. 2000; Zaluar & Scarano, 2000; Cogliatti-Carvalho et al. 2001; T.C. Rocha-Pessôa, dados não publicados). Essa disponibilidade heterogênea de recursos faz com que as espécies de bromélias com necessidades fisiológicas diferentes ocupem de forma distinta um mesmo habitat (Benzing 1980; 2000; Cogliatti-Carvalho & Rocha 2001), como é o caso das restingas. Além disso, a elevada heterogeneidade ambiental possibilita o surgimento de um maior número de microhabitats, permitindo que diferentes espécies possam ocupá-los (Huston 1994). A RBEPS apresenta grande diversidade de comunidades vegetais, que apresentam composições de espécies e estruturas bastante distintas, resultando em uma elevada heterogeneidade e complexidade na área (Araújo & Oliveira 1988). A presença de floresta de encosta contígua às formações de restinga é outro fator que contribui para a riqueza na restinga da RBEPS. Espécies que são normalmente encontradas em Florestas Ombrófilas Densas, na encosta, também ocorreram na área de restinga, como é o caso de Canistropsis microps (Leme 1998) e Edmundoa ambigua (Leme 1997).
Na RBEPS as zonas de vegetação tiveram diferenças significativas em termos de riqueza, composição e abundância de espécies de bromélias. As zonas com predominância de estrato arbóreo mais elevado (FR e FT) apresentaram maiores valores destes parâmetros e tenderam a possuir maior similaridade do que as áreas de porte predominantemente arbustivo (FPP) e arbustivo-arbóreo (MD). É possível que essa tendência seja uma resposta às diferenças existentes na estrutura da vegetação, o que já é relativamente bem descrito para as restingas (Pfadenhauer 1978; Araújo & Henriques 1984; Silva & Somner 1984; Henriques et al. 1986; Araújo & Oliveira 1988; Pereira & Araújo 1995; Araújo et al. 1998). Como as zonas de vegetação de maior porte na RBEPS apresentam uma estrutura complexa, supostamente há maior concentração de microhabitats favoráveis, resultando na estratificação de recursos, o que permite que espécies de bromélias, especialmente as epífitas, possam ocorrer nestas zonas, como acontece para outros tipos de vegetação (Bennett 1986; Hietz & Hietz-Seifert 1995).
Tem sido sugerido que nas áreas com vegetação arbórea e que estejam mais afastadas da linha da praia, as condições microclimáticas tendem a ser mais amenas do que naquelas mais abertas e próximas ao mar (Fialho & Furtado 1993; Freitas et al. 2000). A elevada salinidade, a maior ação dos ventos e a maior incidência luminosa a que está sujeita a FPP faz com que esta zona apresente condições menos propícias para abrigar um elevado número de espécies, estando presentes apenas aquelas com maior resistência a estes fatores, como por exemplo Bromelia antiacantha. Dessa forma, uma parte importante das diferenças encontradas na riqueza, na abundância e na densidade de bromélias entre as zonas de vegetação na RBEPS provavelmente se deve às condições microclimáticas mais amenas (e supostamente mais favoráveis a Bromeliaceae) encontradas em áreas mais protegidas.
As diferenças significativas nas abundâncias das espécies de bromeliáceas amostradas na RBEPS, possivelmente se devem mais às diferenças interespecíficas nas necessidades fisiológicas (Harper 1977; Crawley 1990; Dupré & Ehrlén 2002) e nas taxas de recrutamento (Eriksson & Erhlén 1992; Primack & Miao 1992; Ackerman et al. 1996; Tilman 1997; Ehrlén & Eriksson 2000; Turnbull et al. 2000) e de reprodução vegetativa (Henriques et al. 1984; Silvertown 1987; Crawley 1990; Freitas et al. 2000; Cogliatti-Carvalho & Rocha 2001). Espécies que apresentam maiores tolerâncias ecológicas e maiores taxas de reprodução vegetativa (e.g. B. antiacantha, N. johannis, Billbergia amoena e Aechmea nudicaulis) tendem a ser mais eficazes na colonização e na manutenção de populações viáveis, apresentando abundâncias e densidades mais elevadas do que aquelas espécies com necessidades fisiológicas mais específicas (Silvertown 1987).
Concluímos que a RBEPS possui uma grande diversidade de espécies de bromélias, a qual deve resultar da diversidade de zonas de vegetação e das características estruturais do habitat de cada uma delas favorecendo a ocorrência de um conjunto particular de espécies e resultando em uma variação entre zonas razoavelmente destacáveis em termos de composição, riqueza e abundância de espécies.
Agradecimentos
Este estudo foi subvencionado com recursos da FAPERJ, processo E-26/170.884/2002 e faz parte dos resultados do Programa de Ecologia, Conservação e Manejo de Ecossistemas do Sudeste Brasileiro, Departamento de Ecologia, IBRAG, Universidade do Estado do Rio de Janeiro. E. Leme e A. Costa (Museu Nacional) identificaram as espécies de bromeliáceas estudadas. M.C. Kiefer e R.D. Antonini revisaram o manuscrito, oferecendo importantes contribuições. Durante o estudo, André F. Nunes-Freitas recebeu bolsa de Doutorado (CNPq n. 990207-7) e Carlos F.D. Rocha recebeu bolsa de Produtividade e Auxílio à Pesquisa (CNPq n. 307653/2003-0 e 477981/20038).
Recebido em 7/10/2005. Aceito: 3/04/2006
- Ackerman, J.D.; Sabat, A. & Zimmerman, J.K. 1996. Seedling estabilishment in an epiphytic orchid: an experimental study of seed limitation. Oecologia 106(2): 192-198.
- Amador, E.S. 1985. Subsídios geológicos/geomorfológicos à elaboração do Plano Diretor da Reserva Biológica Estadual da Praia do Sul Rio de Janeiro, FEEMA.
- Amador, E.S. 1988. Geologia e geomorfologia da planície costeira da Praia do Sul - Ilha Grande - uma contribuição à elaboração do Plano Diretor da Reserva Biológica. Anuário do Instituto de Geociências 1987/88: 35-36.
- Araújo, D.S.D. 1992. Vegetation types of sandy coastal plains of tropical Brazil: a first aproximation. Pp. 337347. In: U. Seelingere (ed.). Coastal plant communities of Latin America San Diego, Academic Press.
- Araújo, D. & Henriques, R.P.B. 1984. Análise florística das restingas do Estado do Rio de Janeiro. Pp. 159-173. In: L.D. Lacerda; D.S.D. Araújo; R. Cerqueira & B. Turcq (eds.). Restingas: origem, estrutura, processos Niterói, CEUFF.
- Araújo, D. & Oliveira, R. 1988. Reserva Biológica Estadual da Praia do Sul (Ilha Grande, Rio de Janeiro): lista preliminar da flora. Acta Botanica Brasilica 1(2): 83-94.
- Araújo, D.S.D.; Oliveira, R.R.; Lima, E. & Netto, A.R. 1997. Estrutura da vegetação e condições edáficas numa clareira de mata de restinga na Reserva Biológica Estadual da Praia do Sul, RJ. Brazilian Journal of Ecology 1(2): 36-43.
- Araujo, D.S.D.; Scarano, F.R.; Sá, C.F.C.; Kurtz, B.C.; Zaluar, H.L.T.; Montezuma, R.C.M. & Oliveira, R.C. 1998. Comunidades vegetais do Parque Nacional da Restinga de Jurubatiba. Pp. 39-62. In: F.A. Esteves (ed.). Ecologia das Lagoas Costeiras do Parque Nacional da Restinga de Jurubatiba e do município de Macaé (RJ) Rio de Janeiro, Universidade Federal do Rio de Janeiro.
- Bennett, B.C. 1986. Patchiness, diversity, and abundance relationships of vascular epiphytes. Selbyana 9(1): 7075.
- Benzing, D.H. 1980. Biology of Bromeliads California, Mad River Press.
- Benzing, D.H. 2000. Bromeliaceae: profile of an adaptive radiation Cambridge, Cambridge Eniversity Press.
- Cogliatti-Carvalho, L.; Freitas, A.F.N.; Pessoa, T.C.R. & Rocha, C.F.D. 2000. Parâmetros da ecologia da comunidade de Bromeliaceae em cinco zonas de vegetação da Restinga de Setiba, ES. Pp. 20-30. In: Anais do V Simpósio de Ecossistemas Brasileiros: Conservação (S.Watanabe, org.). v.3. São Paulo, Publicações ACIESP.
- Cogliatti-Carvalho, L.; Nunes-Freitas, A.F.; Rocha, C.F.D. & van Sluys, M. 2001. Variação na estrutura e composição de Bromeliaceae em cinco zonas de vegetação no Parque Nacional da restinga de Jurubatiba, Macaé, RJ. Revista Brasileira de Botânica 24(1): 1-9.
- Cogliatti-Carvalho, L. & Rocha, C.F.D. 2001. Spatial distribution and preferential substrate of Neoregelia johannis (Carriére) L.B. Smith (Bromeliaceae) in a disturbed area of Atlantic Rainforest at Ilha Grande, RJ, Brazil. Revista Brasileira de Botânica 24(4): 389-394.
- Crawley, M.J. 1990. The population dynamics of plants. Philosophical Transactions of the Royal Sociaty London B 330: 125-140.
- Dansereu, P. 1947. Zonation et succession sur la restinga de Rio de Janeiro - I. Halosère. Revue Canadiense de Biologie 6(3): 447-477.
- De Paula, F.C.F.; Carvalho, C.E.V.; Ovalle, A.R.C.; Barroso, L.V.; Oliveira, R.R. & Resende, C.E. 1994. Pesquisa Orientativa na Bacia do Rio Capivari, Ilha Grande, RJ. Pp. 382-395. In: Anais do III Simpósio de Ecossistemas da Costa Brasileira São Paulo, Publicações ACIESP.
- Dupré, C. & Ehrlén, J. 2002. Habitat configuration, species traits and plant distributions. Journal of Ecology 90(5): 796-805.
- Eriksson, O. & Ehrlén, J. 1992. Seed and microsite limitation of recruitment in plant population. Oecologia 91(3): 360364.
- Ehrlén, J. & Eriksson, O. 2000. Dispersal limitation and patch occupancy in forest herbs. Ecology 81(6): 1667-1674.
- Fabris, L.C. & Pereira, O.J. 1998. Florística da formação pós-praia na restinga do Parque Estadual Paulo César Vinhas, Guarapari (ES). Pp. 165-176. In: S. Watanabe (org.). Anais do IV Simpósio de Ecossistemas Brasileiros São Paulo, Publicações ACIESP.
- Fialho, R.F. & Furtado, A.L.S. 1993. Germination of Erythroxylum ovalifolium (Erythroxylaceae) seeds within the terrestrial bromeliad Neoregelia cruenta Biotropica 22(4): 359-362.
- Fontoura, T.; Costa, A. & Wendt, T. 1991. Preliminary checklist of the Bromeliaceae of Rio de Janeiro State, Brazil. Selbyana 12: 5-45.
- Franco, A.C.; Valeriano, D.M.; Santos, F.M.; Hay, J.D.; Henriques, R.P.B. & Medeiros, R.A. 1984. Os microclimas das zonas de restinga de vegetação da praia da restinga de Barra de Maricá, Rio de Janeiro. Pp. 413-423. In: L.D. Lacerda; D.S.D. Araújo; R. Cerqueira & B. Turcq (orgs.). Restingas: origem, estrutura e processos Niterói, CEUFF.
- Freitas, A.F.N.; Cogliatti-Carvalho, L.; van Sluys, M. & Rocha, C.F.D. 2000. Distribuição espacial de bromélias na Restinga de Jurubatiba, Macaé, RJ. Acta Botanica Brasilica 14(1): 175-180.
- Fundação SOS Mata Atlântica/INPE. 2001. Atlas dos remanescentes florestais do Rio de Janeiro São Paulo, SOS Mata Atlântica e Instituto Nacional de Pesquisas Espaciais.
- Harper, J.L. 1977. The population biology of plants London, Academic Press.
- Hay, J.D. & Lacerda, L.D. 1984. Ciclagem de nutrientes no ecossitema de restinga. Pp. 459-473. In: L.D. Lacerda; D.S.D. Araújo; R. Cerqueira & B. Trcq (orgs.). Restingas: Origem, estrutura e processos Niterói, CEUFF.
- Henriques, R.P.B.; Meirelles, M.L. & Hay, J.D. 1984. Ordenação e distribuição de espécies de comunidades vegetais na praia de restinga de Barra de Maricá, Rio de Janeiro. Revista Brasileira de Botânica 7(1): 27-36.
- Henriques, R.P.B.; Araújo, D.S.D. & Hay, J.D. 1986. Descrição e classificação dos tipos de vegetação da restinga de Carapebus, Rio de Janeiro. Revista Brasileira de Botânica 9(2): 173-189.
- Hietz, P. & Hietz-Seifert, U. 1995. Composition and ecology of vascular epiphyte communities along an altitudinal gradient in central Veracruz, México. Journal of Vegetation Science 6(4): 487-498.
- Huston, M.A. 1994. Biological diversity. The coexistence of species on changing landscapes Cambridge, Cambridge University Press.
- Lacerda, L.D.; Araújo, D.S.D. & Maciel, N.C. 1982. Restingas Brasileiras: uma bibliografia Rio de Janeiro, Universidade Federal do Rio de Janeiro.
- Lacerda, L.D.; Araújo, D.S.D. & Maciel, N.C. 1993. Dry coastal ecosystems of the tropical Brazilian coast. Pp. 477-493. In: van der Maarel, E. (ed.). Dry coastal ecosystems: Africa, America, Asia, Oceania Amsterdam, Elsevier.
- Leme, M.C. 1985. Bromeliáceas dos municípios de Cabo Frio e Arraial do Cabo, RJ. Boletim FBCN - Rio de Janeiro 20(1): 57-67.
- Leme, E. 1997. Canistrum - Bromélias da Mata Atlântica Rio de Janeiro, Salamandra Consultoria Editorial Ltda.
- Leme, E. 1998. Canistropsis - Bromélias da Mata Atlântica Rio de Janeiro, Salamandra Consultoria Editorial Ltda.
- Lopez, L.C.S. & Rios, R.I. 2001. Phytotelmata faunal communities in sun-exposed versus shaded terrestrial bromeliads from southeastern Brazil. Selbyana 22(2): 219224.
- Magurran, A.E. 1988. Ecological diversity and its measurement Princeton, Princeton University Press.
- Mantovani, A. & Iglesias, R.R. 2001. Terrestrial bromeliads of the "restinga" of "Barra de Maricá", Rio de Janeiro: influence on the microclimate, soil and nutrient storage on the border of vegetation islands. Leandra 16(1): 1437.
- Mueller-Dumbois, D. & Ellenberg, H. 1974. Aims and methods of vegetation ecology New York, John Wiley & Sons.
- Oliveira, R.R. 2002. Ação antrópica e resultantes sobre a estrutura e composição da Mata Atlântica na Ilha Grande, RJ. Rodriguésia 53(82): 33-58.
- Oliveira, R.R. & Coelho Netto, A.L. 1996. O rastro do homem na floresta - a construção da paisagem na reserva Biológica Estadual da Praia do Sul a partir das intervenções antrópicas. Albertoa 10(4): 110-118.
- Ormond, W.T. 1960. Ecologia das restingas do Sudeste do Brasil: comunidades vegetais das praias arenosas. Parte I. Arquivos do Museu Nacional 50: 185-236.
- Pereira, O.J. 1990. Caracterização fitofisionômica da restinga de Setiba, Guarapari, ES. Pp. 207-219. In: S. Watanabe (org.). Anais do Simpósio de Ecossistemas da Costa Sul-sudeste Brasileira v.3. São Paulo, Publicações ACIESP.
- Pereira, O.J. & Araújo, D.S.D. 1995. Estrutura da vegetação de entre moitas da formação aberta de Ericaceae no Parque Estadual de Setiba, ES. Oecologia Brasiliensis 1: 245-257.
- Pereira, O.J. & Zambom, O. 1998. Composição florística da Restinga de Interlagos, Vila Velha (ES). Pp. 129-157. In: S. Watanabe (org.). Anais do IV Simpósio de Ecossistemas Brasileiros São Paulo, Publicações ACIESP.
- Pfadenhauer, J. 1978. Contribuição ao conhecimento da vegetação e de suas condições de crescimento nas dunas costeiras do Rio Grande do Sul, Brasil. Revista Brasileira de Biologia 38: 827-836.
- Pinheiro, F. & Borghetti, F. 2003. Light and temperature requirements for germination of seeds of Aechmea nudicaulis (L.) Griesebach and Streptocalix floribundus (Martius ex Schultes f.) Mez (Bromeliaceae). Acta Botanica Brasilica 17(1): 27-35.
- Primack, R.B. & Miao, S.L. 1992. Dispersal can limit local plant distribution. Conservation Biology 6(4): 513-519.
- Rizzini, C.T. 1992. Tratado de fitogeografia do Brasil: aspectos ecológicos e florísticos São Paulo, Âmbito Cultural Edições.
- Rocha, C.F.D.; Bergallo, H.G.; Alves, M.A.S. & van Sluys, M. 2003. A biodiversidade nos grandes remanescentes florestais do Estado do Rio de Janeiro e nas restingas da Mata Atlântica São Carlos, Editora RiMa.
- Rocha, C.F.D.; Nunes-Freitas, A.F.; Rocha-Pessôa, T.C. & Cogliatti-Carvalho, L. 2004. Habitat disturbance in Brazilian Coastal sand dune vegetation and present richness and diversity of bromeliad species. Vidalia 2(2): 50-56.
- Rosenzweig, M.L. 1998. Species diversity in space and time Cambridge, Cambridge University Press.
- Sá, C.F.C. 1992. A vegetação da restinga de Ipitangas, Reserva Estadual de Jacarepiá, Saquarema (RJ): fisionomia e listagem de angiospermas. Arquivos do Jardim Botânico do Rio de Janeiro 31: 82-102.
- Sampaio, M.C.; Perissé, L.E.; Oliveira, G.A. & Rios, R.I. 2002. The contrasting clonal architeture of two bromeliads from sandy coastal plains in Brazil. Flora 197(6): 443451.
- Scarano, F.R. 2002. Strucuture, function and floristic relationships of plant communities in stressful habitats marginal to the Brazilian Atlantic Rainforest. Annals of Botany 90(4): 517-524.
- Scarano, F.R.; Duarte, H.M.; Ribeiro, K.T.; Rodrigues, P.J.F.P & Barcellos, E.M.B. 2001. Four sites contrasting environmental stress in southeastern Brazil: relations of species, life form diversity, and geographic distribution to ecophysiological parameters. Botanical Journal of the Linnean Society 136(4): 345-364.
- Silva, J.G. & Somner, G.V. 1984. A vegetação de restinga de Barra de Maricá, RJ. Pp. 217-225. In: L.D. Lacerda; D.S.D. Araújo; R. Cerqueira & B. Turcq (orgs.). Restingas: origem, estrutura e processos Niterói, CEUFF.
- Silvertown, J. 1987. Introduction to plant population ecology 2nd New York, Longman Scientific & Technical.
- Suguio, K. & Tessler, M.G. 1984. Planícies de cordões litorâneos quaternários do Brasil: origem e nomenclatura. Pp. 15-25. In: L.D. Lacerda; D.S.D. Araújo; R. Cerqueira & B. Turcq (eds.). Restingas: Origem, Estrutura, Processos Niterói, Centro Editorial da UFF.
- Thompson, G.G.; Withers, P.C.; Pianka, E.R. & Thompson, S.A. 2003. Assessing biodiversity with species accumulation curves: inventories of small reptiles by pittrapping in Western Australia. Austral Ecology 28(4): 361-383.
- Tilman, D. 1997. Community invasibility, recruitment limitation, and grassland biodiversity. Ecology 78(1): 8192.
- Toffoli, D.D. & Oliveira, R.R. 1999. Caiçara Agroforestry Management. Pp. 302-305. In: D.A. Posey (org.). Cultural and spiritual values of biodiversity Nairobi, United Nations Environment Program, Intermediate Tecnology Publications.
- Turnbull, L.A.; Crawley, M.J. & Rees, M. 2000. Are plant populations seed-limited? A review of seed sowing experiments. Oikos 88(2): 225-238
- Zaluar, H.T. & Scarano, F.R. 2000. Facilitação em restingas de moitas: um século de buscas por espécies focais. Pp. 3-23. In: F.A. Esteves & L.D. Lacerda (eds.). Ecologia de Restingas e Lagoas Costeiras Rio de Janeiro, NUPEM/UFRJ.
- Zar, J.H. 1999. Biostatistical analysis 4th ed., Upper Saddle River, Prentice Hall.
Datas de Publicação
-
Publicação nesta coleção
27 Fev 2007 -
Data do Fascículo
Set 2006
Histórico
-
Aceito
03 Abr 2006 -
Recebido
10 Jul 2005