Resumos
Alterações morfológicas detectadas em diversas espécies vegetais em função da indução de galhas são comumente acompanhadas de mudanças químicas importantes para o estabelecimento e manutenção do sistema galhador-planta hospedeira. O estudo da variação do teor de fenóis totais e sua relação com o desenvolvimento das galhas no sistema Aspidosperma spruceanum-Cecidomyiidae foi realizado ao longo de um ano, no qual foram detectados pelo menos dois ciclos de vida dos insetos indutores. O nível de infestação foliar foi alto, atingindo 87%, e os Cecidomyiidae tiveram a região internervural como sítio preferencial de oviposição. A variação sazonal no conteúdo de fenóis totais nas amostras de folhas sadias e galhadas foi primariamente relacionada às condições abióticas e muito embora este teor tenha atingido o máximo de 10 mg EAT g-1, indicando um ambiente químico celular não favorável à indução e a sua sobrevivência, o indutor de A. spruceanum supera esta barreira química, podendo ainda ser favorecido pela proteção contra inimigos naturais propiciada pelos fenólicos.
Aspidosperma; Cecidomyiidae; galhas; interações inseto-planta; morfometria
Morphological alterations detected in several plant species due to gall induction are commonly followed by chemical changes fundamental to the establishment and maintenance of the host plant-gall maker system. The study of phenolic contents variation and its relation to gall development in Aspidosperma spruceanum-Cecidomyiidae system through a year-time detected two insect life cycles. The level of infestation was high, getting up to 87%, and the Cecidomyiidae preferentially oviposited in internervural region. Seasonal variation in phenolic contents in healthy and galled leaves detected in A. spruceanum was primarily related to abiotic conditions. Even though the levels of phenolic contents might get a maximum of 10 mg EAT g-1, which indicated a non stimulating cell chemical environment to gall induction and herbivore survivorship, A. spruceanum gall maker surpassed this chemical barrier, and might also be favored by the chemical protection against its natural enemies, that phenolic contents might confer.
Aspidosperma; Cecidomyiidae; galls; insect-plant interactions; morphometry
Relações entre o teor de fenóis totais e o ciclo das galhas de Cecidomyiida e em Aspidosperm a spruceanum Müll. Arg. (Apocynaceae)
Relationships between phenolic contents and a Cecidomyiidae gall cycle in Aspidosperma spruceanum Müll. Arg. (Apocynaceae)
Anete Teixeira FormigaI,11 Autor para correspondência: aneteformiga@gmail.com; Samuel José de Melo Reis GonçalvesI; Geraldo Luiz Gonçalves SoaresII; Rosy Mary dos Santos IsaiasI
IUniversidade Federal de Minas Gerais, Instituto de Ciências Biológicas, Departamento de Botânica, Laboratório de Anatomia Vegetal, Av. Antônio Carlos 6627, 31270-901 Belo Horizonte, MG, Brasil (rosy@icb.ufmg.br)
IIUniversidade Federal do Rio Grande do Sul, Instituto de Biociências, Departamento de Botânica, Av. Bento Gonçalves 9500, Bloco IV, Prédio 43423-2, Sala 222, 90501-970 Porto Alegre, RS, Brasil (geraldo.soares@ufrgs.br)
RESUMO
Alterações morfológicas detectadas em diversas espécies vegetais em função da indução de galhas são comumente acompanhadas de mudanças químicas importantes para o estabelecimento e manutenção do sistema galhador-planta hospedeira. O estudo da variação do teor de fenóis totais e sua relação com o desenvolvimento das galhas no sistema Aspidosperma spruceanum-Cecidomyiidae foi realizado ao longo de um ano, no qual foram detectados pelo menos dois ciclos de vida dos insetos indutores. O nível de infestação foliar foi alto, atingindo 87%, e os Cecidomyiidae tiveram a região internervural como sítio preferencial de oviposição. A variação sazonal no conteúdo de fenóis totais nas amostras de folhas sadias e galhadas foi primariamente relacionada às condições abióticas e muito embora este teor tenha atingido o máximo de 10 mg EAT g-1, indicando um ambiente químico celular não favorável à indução e a sua sobrevivência, o indutor de A. spruceanum supera esta barreira química, podendo ainda ser favorecido pela proteção contra inimigos naturais propiciada pelos fenólicos.
Palavras-chave:Aspidosperma, Cecidomyiidae, galhas, interações inseto-planta, morfometria
ABSTRACT
Morphological alterations detected in several plant species due to gall induction are commonly followed by chemical changes fundamental to the establishment and maintenance of the host plant-gall maker system. The study of phenolic contents variation and its relation to gall development in Aspidosperma spruceanum-Cecidomyiidae system through a year-time detected two insect life cycles. The level of infestation was high, getting up to 87%, and the Cecidomyiidae preferentially oviposited in internervural region. Seasonal variation in phenolic contents in healthy and galled leaves detected in A. spruceanum was primarily related to abiotic conditions. Even though the levels of phenolic contents might get a maximum of 10 mg EAT g-1, which indicated a non stimulating cell chemical environment to gall induction and herbivore survivorship, A. spruceanum gall maker surpassed this chemical barrier, and might also be favored by the chemical protection against its natural enemies, that phenolic contents might confer.
Key words:Aspidosperma, Cecidomyiidae, galls, insect-plant interactions, morphometry
Introdução
Plantas hospedeiras, de modo geral, suprem as galhas com substâncias de reserva, pois estas funcionam como um dreno para onde o fluxo de fotoassimilados é direcionado. A vascularização, a distância entre a fonte e o dreno e o tamanho da fonte influenciam no processo, sem que haja, no entanto, controle por parte dos tecidos vegetais sobre o destino dos fotoassimilados produzidos (McCrea et al. 1985; Larson & Whitham 1991). Comumente, as galhas possuem um alto conteúdo de nutrientes minerais, carbono e energia, além de acumularem substâncias do metabolismo secundário, como os fenóis totais.
Dentre os fenóis totais, há uma gama de moléculas sinalizadoras cuja variação quantitativa pode indicar diferentes padrões de resposta dos vegetais a fatores bióticos como à ação dos herbívoros galhadores e fatores abióticos, os quais podem influenciar indiretamente o sucesso no estabelecimento e desenvolvimento destes herbívoros (Fernandes & Price 1992; Hartley 1998; Nyman & Jukulnen-Tiitto 2000).
As galhas de Cecidomyiidae são geralmente abertas, com ostíolo revestido por tricomas (Meyer 1987), podendo variar desde simples galhas de cobertura até galhas em bolso (Dreger-Jauffret & Shorthouse 1992) com elevado grau de complexidade morfológica (Rohfritsch 1992). Esta variação fenotípica é decorrente de alterações morfogênicas em pequenas regiões das plantas hospedeiras, alterações estas produto da atividade alimentar dos insetos galhadores. O desenvolvimento dos tecidos da planta hospedeira é direcionado para a nutrição e proteção dos galhadores contra seus inimigos naturais (Rohfritsch 1992; Price et al. 1987; Stone & Schonrögge 2003).
Análises morfométricas destas mudanças no desenvolvimento dos tecidos, complementares às observações morfológicas, permitem quantificar as mudanças ocorridas, gerando informações matematicamente comparáveis (Thiébaut 2000). Face à freqüência dos fenólicos e sua possível interferência no desenvolvimento das galhas, relatadas amplamente na literatura (Purohit et al. 1979; Abrahamson & Weis 1997; Hartley 1998), o estudo das galhas induzidas por uma espécie não identificada de Diptera: Cecidomyiidae em Aspidosperma spruceanum Müll. Arg. (Apocynaceae) visa: (1) registrar as variações qualitativas e quantitativas de forma, tamanho e freqüência observadas ao longo do ciclo de desenvolvimento das galhas; (2) detectar possíveis sítios preferenciais de oviposição; e (3) relacionar a variação sazonal do teor de fenóis totais com o ciclo de desenvolvimento das galhas de Aspidosperma spruceanum Müll. Arg. (Apocynaceae).
Material e métodos
Ramos contendo folhas sadias e com galhas foram coletados nos meses de outubro/2001, janeiro, abril, agosto e outubro/2002, em espécimes de Aspidosperma spruceanum Müll. Arg. localizados no Campus Pampulha da Universidade Federal de Minas Gerais, Belo Horizonte, MG. O material acha-se registrado no herbário BHCB sob o nº 46.274. As coletas foram realizadas com o auxílio de podão e as amostras acondicionadas em sacos plásticos e levadas ao laboratório.
Em cada coleta foram quantificados o número de folhas sadias e folhas galhadas em ramos com cerca de 1 m compr. (n = 3) e o número de galhas por folha (n > 60). O nível de infestação (N.I.) foi calculado a partir da fórmula: (nº folhas galhadas/nº total de folhas) × 100. A posição das galhas nas lâminas foliares foi avaliada por observação direta e contagem manual das mesmas.
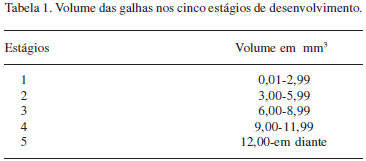
As maiores dimensões (altura e diâmetro) das galhas foram medidas com auxílio de paquímetro digital (DIGIMESS). Estes valores foram utilizados para o cálculo do volume da galha, pela fórmula de um elipsóide de revolução: V= (p.D.d.h) / 6, sendo (V) o volume, (D) o diâmetro maior, (d) o diâmetro menor e (h) a altura (Arduin et al. 1989). As galhas foram classificadas em diferentes estágios de desenvolvimento de acordo com sua variação volumétrica (Tab. 1).
As análises morfológicas e anatômicas foram feitas em material fresco. As secções foram realizadas a mão livre, na região internervural do terço médio da lâmina foliar e nas galhas em fase de maturação, segundo técnicas usuais em anatomia vegetal descritas em Johansen (1940). As lâminas foram analisadas em microscópio óptico (Olympus BH2-BHS).
Folhas sadias e galhadas foram secas separadamente à temperatura ambiente (25-30 ºC) e pulverizadas. Amostras de 6 g de cada material foram submetidas à extração em aparelho de Sohxlet (6 h) com hexano PA para eliminação dos constituintes com polaridade reduzida. Em seguida, foi feita a extração com etanol PA até a exaustão (Harborne 1984). Os extratos etanólicos brutos foram secos em banho-maria (60 ºC), pesados e diluídos à proporção de 100 mg:100 ml de etanol PA. A avaliação do teor de fenóis totais nas amostras de cada material foi feita em três repetições utilizando o método de Folin-Dennis (Waterman & Mole 1994). Os teores de fenóis totais foram obtidos por comparação das absorbâncias lidas a 760 nm em espectrofotômetro (Thermo Spectronic, modelo Genesys 10 UV) com uma curva padrão de ácido tânico.
As concentrações obtidas das amostras de Aspidosperma spruceanum foram convertidas em microgramas de equivalentes de ácido tânico (EAT) por peso seco de amostra em gramas e representadas como valores médios ± erro padrão. Diferenças significativas entre os teores de fenóis totais de folhas sadias e galhadas de uma mesma coleta e entre coletas diferentes foram detectadas pelo teste HSD de Tukey (p < 0,05).
Resultados e discussão
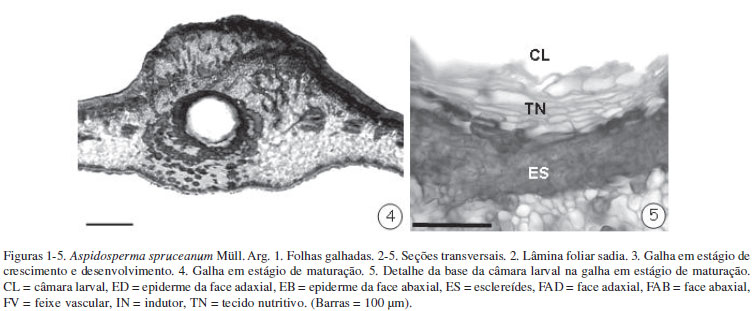
Os exemplares de Aspidosperma spruceanum estudados apresentam hábito arbóreo, folhas simples, verdes e subcoriáceas, infestadas por numerosas galhas induzidas por uma espécie não descrita de Diptera: Cecidomyiidae. As galhas desta espécie podem ser classificadas segundo Dreger-Jauffret (1992) como fanerocecídios. São sésseis, simples ou conglomeradas, esféricas, de superfície rugosa e coloração verde semelhante à da folha sadia (Fig. 1).
A lâmina foliar de A. spruceanum é dorsiventral, hipostomática e pilosa na face abaxial. A parede periclinal externa das células epidérmicas da face adaxial é marcadamente espessada e recoberta por espessa camada cuticular. Esclereídes encontram-se entremeadas às células do parênquima paliçádico. Nervuras de pequeno porte acham-se imersas no limite entre os parênquimas paliçádico e lacunoso (Fig. 2). Estas características foliares comumente relacionadas à economia hídrica (Fahn 1990; Larcher 2000) podem prover o inseto galhador com um ambiente interno foliar adequado ao seu desenvolvimento.
Em geral, a indução das galhas de Cecidomyiidae tem início quando as larvas alimentam-se na face externa das células epidérmicas (Meyer 1987). Em A. spruceanum, as características dos estágios iniciais das galhas e a não visualização de ovos na superfície foliar podem indicar que a oviposição seja interna, comum a alguns Cecidomyiidae (Gagné 1994).
As galhas de A. spruceanum localizam-se nas regiões laterais da nervura de primeira ordem, dispostas aleatoriamente e protuberantes para ambas as faces (Fig. 1). Possuem uma única câmara larval central (Fig. 3-4), sendo classificadas como do tipo monotálamo (Küster 1903 apud Mani 1964), abrigando um único inseto indutor. No primeiro estágio de desenvolvimento, apresentam formato lenticular, com volume médio de 2,09 ± 0,65 mm3, sendo a maior protuberância notada na face abaxial da lâmina foliar (Fig. 3). A câmara larval apresenta-se alongada no sentido paradérmico e possui localização central. Do segundo ao quarto estágio de desenvolvimento, nota-se o aumento da protuberância para ambas as faces foliares e o volume médio aumenta cerca de 2,5 vezes. A câmara larval apresenta formato arredondado em secção transversal, podendo assumir posição excêntrica (Fig. 4). Este aumento de volume é devido ao aumento das divisões celulares no mesofilo. No quinto estágio de desenvolvimento, a galha aumenta em todas as suas dimensões, atingindo sua forma e volume médio finais (15,64 ± 3,57 mm3). Em secção transversal, a câmara larval apresenta formato predominantemente arredondado e acha-se revestida por esclereídes dispersos em meio às células parenquimáticas (Fig. 4-5) ou agrupados em tecido contínuo externo ao tecido nutritivo.
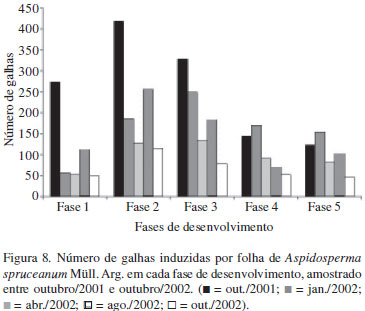
O aumento das divisões celulares é uma característica comum nos primeiros estágios de desenvolvimento das galhas, o que lhes confere ganho volumétrico. A predominância de galhas de A. spruceanum em estágios iniciais foi notada em janeiro/2002 (Fig. 8), época que coincide com grande percentual de folhas galhadas e alta disponibilidade hídrica (Fig. 6, 9). Nas fases iniciais, é notável o maior estímulo para crescimento e desenvolvimento das células e tecidos. Tendo em vista que os fenóis participam da inibição das AIA-oxidases (Hori 1992), é plausível supor que tais substâncias estejam influenciando diretamente o aumento dos teores de auxinas nas folhas galhadas de A. spruceanum e conseqüentemente na taxa de divisões celulares envolvida no considerável aumento de volume das galhas.
As variações de formato observadas ao longo do desenvolvimento das galhas acompanham as variações dos formatos das câmaras larvais. Deste modo, a forma lenticular da galha em seu primeiro estágio está relacionada ao alongamento da câmara larval no sentido paradérmico. O desenvolvimento da forma arredondada para a face abaxial coincide com a mudança de formato da câmara larval observada nos estágios seguintes. Uma vez que a variedade de formas observada nas galhas de Cecidomyiidae é decorrente da atividade alimentar dos insetos (Rohfritsch 1992), pode-se inferir que o indutor das galhas de A. spruceanum mudou seu sítio de alimentação dentro da câmara larval ao longo de seu desenvolvimento, resultando em câmaras ovaladas ou arredondadas.
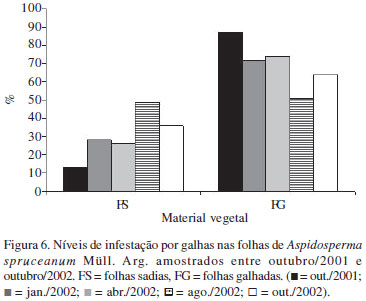
O nível de infestação das folhas pelos Cecidomyiidae variou de 87% em outubro/2001 a 64% em outubro/2002, com o menor índice em agosto/2002 (51%) (Fig. 6). A similaridade entre as freqüências de folhas galhadas e folhas sadias coincide com o auge da estação seca, muito embora no nível macroambiental, ambientes xéricos apresentem maior diversidade de espécies galhadoras quando comparados a ambientes mésicos (Fernandes & Price 1988). Em escala microambiental, no sistema A. spruceanum-Cecidomyiidae, a época de maior pluviosidade (janeiro) coincide com a maior freqüência de galhas em estágios 2 e 3, ou seja, em fase de crescimento e desenvolvimento (Fig. 8-9). Esta época coincide com diferenças significativas no nível de fenóis totais em folhas sadias e galhadas, sendo ainda um momento no qual se registrou aumento na concentração destas substâncias nos tecidos vegetais, em geral. Mais uma vez, os derivados fenólicos do metabolismo secundário podem influenciar no ciclo de desenvolvimento das galhas, tanto nas potencialidades químicas destes tecidos de responderem aos estímulos externos quanto na defesa contra inimigos naturais.
De um modo geral, os níveis de infestação observados ao longo de um ano podem ser considerados altos, comprometendo, possivelmente, o vigor da planta hospedeira, como descrito por Price et al. (1986; 1987), pois os espécimes amostrados não floresceram no período amostrado. Além dos fatores abióticos envolvidos, o estabelecimento e a manutenção de relações planta-parasita dependem da reação genética e fisiológica favorável por parte das células do hospedeiro, como apontado por Deverall (1977). Pode-se, pois, verificar que no sistema estudado, as células do sistema fundamental, antes especializadas para fotossíntese têm incremento em suas divisões, lignificação de parede e acúmulo de reservas nutritivas, favorecendo o estabelecimento do herbívoro galhador, que redireciona os processos morfogênicos em seu próprio benefício.
A relação entre os Cecidomyiidae e suas plantas hospedeiras é considerada como altamente especializada em comparação com outros sistemas galhador-planta (Mani 1964; Rohfritsch 1992). O fato de o espécime vegetal amostrado encontrar-se isolado, aliado à baixa aptidão para o vôo dos Cecidomyiidae (Gagné 1994) indicar reinfestação dos mesmos indivíduos hospedeiros e pode ser um dos fatores determinantes dos altos níveis de infestação amostrados.
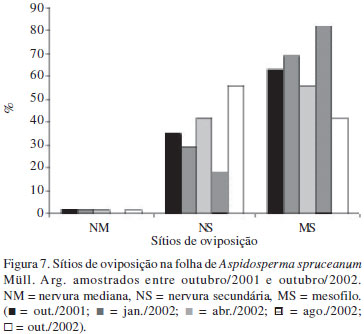
A análise dos sítios de oviposição nas folhas de A. spruceanum demonstra uma grande incidência na região internervural desde outubro/2001 até agosto/2002 (Fig. 7). Em outubro/2002, esta tendência decresce bruscamente, registrando-se maior freqüência de oviposição na região das nervuras de segunda ordem (Fig. 7), sendo este interpretado como um sítio opcional de oviposição por parte dos Cecidomyiidae. A proximidade às nervuras pode maximizar a relação fontedreno já detectada em outras galhas entomógenas (McCrea et al. 1985; Larson & Whitham 1991). Segundo Nyman & Julkunen-Tiitto (2000), há uma relação direta entre a escolha do sítio de oviposição e o sucesso do estabelecimento do galhador, sendo as posições centrais na lâmina foliar, derivadas em relação às posições basais. Levando-se em consideração tal hipótese, a mudança no sítio preferencial de oviposição em outubro/2002, coincide com a maior seca do período amostrado. Deste modo, o galhador de A. spruceanum parece apresentar um comportamento de oviposição adequado ao seu estabelecimento em condições abióticas adversas, utilizando-se de um local mais próximo ao aporte de água nos tecidos vegetais.
Além da variação no sítio preferencial de oviposição, em outubro/2002 (Fig. 7) foi observada marcante redução no número total de galhas, mantendo-se, contudo, a predominância de galhas nos estágios 2 e 3, observada em todo o período amostrado (Fig. 8). A ocorrência do estágio 1 ao longo de todo o período indica um indutor multivoltino, ou seja, com pelo menos dois ciclos de vida anuais, comportamento biológico já descrito para diferentes espécies de Cecidomyiidae (Meyer 1987).
Os teores de fenóis totais em folhas de A. spruceanum foram profundamente influenciados pela presença de galhas, cuja indução e desenvolvimento estimularam a produção dessas substâncias nos meses analisados (Fig. 9, Tab. 2). A análise das curvas de precipitação e insolação médias mensais durante o período estudado em conjunto com o resultado da análise de fenóis totais (Fig. 9), sugere que fatores abióticos estejam atuando em conjunto com as galhas na modulação da resposta química da planta hospedeira. Essa tendência é clara nos meses em que a diferença entre os teores de fenóis totais das galhas e dos tecidos sadios foi significativa.
De maneira geral, a maior produção de fenóis em todas as amostras ocorreu em períodos mais secos e/ou com máximas de insolação, isto é, nas amostras coletadas em abril, agosto e outubro/2002. Porém, o teor de fenóis totais das folhas galhadas foi significativamente maior do que o das folhas sadias nos meses de outubro/2001, janeiro/2002 e agosto/2002. Em outubro/2001, tanto os níveis de insolação quanto de pluviosidade são relativamente baixos em comparação aos máximos alcançados no período amostrado (Fig. 9). Observam-se nesse mês, os menores teores de fenóis totais nas folhas sadias e o estímulo relativamente maior de sua produção nas folhas galhadas (Fig. 9). Até janeiro/2002, a diferença significativa na produção de derivados fenólicos entre as folhas se mantém. Em abril do mesmo ano, os níveis de fenóis totais atingem o seu máximo, acompanhando altos índices de insolação, e a diferença de produção em folhas sadias e galhadas praticamente desaparece (Tab. 2; Fig. 9). Há um aumento gradativo do conteúdo total desses metabólitos, em ambos os materiais, no período de intensa luminosidade e baixa pluviosidade. A análise desses resultados sugere que o efeito estimulante da cecidogênese sobre a produção de fenólicos é maior quando a biossíntese desses aleloquímicos não está previamente estimulada pelas condições ambientais.
Como a grande maioria dos derivados fenólicos tem sua origem na via do chiquimato, em especial na porção pós-fenilalanínica desse caminho biossintético secundário, a insolação é um fator determinante na sua produção. Esse fenômeno é explicado pelo fato da enzima-chave da produção dos derivados fenólicos do chiquimato, a fenilalanina-amonialiase (PAL), sofrer estimulação transcricional pela radiação UV presente na luz solar (Jones 1984). Portanto, a produção de derivados do chiquimato pode ser considerada um mecanismo de proteção contra o estresse luminoso.
A exposição à luz solar configurou-se como um dos principais indutores da produção dos fenóis totais nas folhas de A. spruceanum. No sistema estudado, as galhas apresentam um efeito modulador da biossíntese desses metabólitos, cabendo salientar que o aumento significativo na produção de fenólicos em folhas galhadas em comparação com folhas sadias, nos meses de alta insolação, foi observado apenas em agosto/2002 (Fig. 9).
O estresse hídrico também interfere na produção de metabólitos da via do chiquimato, sendo um fator adicional que explica o perfil de variação dos fenóis totais em A. spruceanum. Por outro lado, Gershenzon (1984) afirmou não haver uma tendência clara no efeito desse estresse ambiental sobre a produção de fenólicos. Nos resultados obtidos por Gleadow e Woodrow (2002), os teores de fenóis totais e de taninos condensados (proantocianidinas) de Eucalyptus cladocalyx var. nana não foram afetados pelo estresse hídrico. Entretanto o aumento de 70% na produção de glicosídeos cianogênicos, derivados da rota do chiquimato, em plantas sob estresse hídrico moderado foi relacionado à competição por um mesmo precursor biossintético, a fenilalanina. Conclui-se pois que é possível que a competição metabólica ocorra em outras espécies vegetais e seja um fator determinante para a variação sazonal de metabólitos derivados da rota do chiquimato.
Outro fator formador do clima que pode influenciar o metabolismo fenólico das plantas é a temperatura. Rivero et al. (2001) demonstraram que o estresse térmico provocou tanto o aumento do teor de derivados fenólicos solúveis e da atividade da fenilalanina-amonialiase (PAL) quanto da diminuição na atividade de peroxidase e de polifenol oxidase em Lycopersicon esculentum e em Citrulus lanatus. Nessas plantas, o estresse térmico ativou a biossíntese de derivados fenólicos ao mesmo tempo em que inibiu a sua degradação. É oportuno mencionar que na região do estudo há basicamente uma estação seca anual (de abril até setembro), com temperaturas amenas, e uma estação chuvosa e quente (de outubro até março) (Fig. 9). Esta delimitação sazonal bem estabelecida pode gerar um estresse térmico ativador da biossíntese dos fenólicos, influenciando indiretamente o ciclo de desenvolvimento das galhas. A presença destas, por sua vez, já foi estudada em diversas espécies vegetais, não havendo, contudo, dados na literatura que permitam determinar uma tendência clara a respeito da ação da cecidogênese sobre a biossíntese desses aleloquímicos. Se, por um lado, o aumento do teor de fenóis totais é comumente associado à presença de galhas (Purohit et al. 1979; Abrahamson & Weis 1997), por outro lado, alguns autores como Hartley (1998) e Nyman e Julkunen-Tiitto (2000) observaram desde sua redução até a ausência de efeito das galhas sobre a produção de fenólicos.
Os resultados do presente estudo indicam que a condição metabólica dos tecidos de A. spruceanum corresponde primariamente aos estímulos do meio físico e o impacto desta no estabelecimento e desenvolvimento das galhas é secundário. Fica claro que o estudo de variações no conteúdo de aleloquímicos, em especial os derivados fenólicos, em tecidos sadios e galhados deve ser associado ao acompanhamento do efeito da variação de fatores climáticos (insolação, pluviosidade e temperatura) sobre a planta hospedeira (Fig. 6, 9).
A análise da variação sazonal do conteúdo de fenóis totais nas amostras de folhas sadias e folhas galhadas sugere também a atuação dessas substâncias na defesa química contra herbivoria. A maior produção de derivados fenólicos nas amostras de folhas sadias e folhas galhadas a partir de abril/2002 (Fig. 9) parece ter influenciado o nível de infestação que apresentou uma redução em agosto/2002 (Fig. 6). Esse fato indica um ambiente químico celular desestimulante à indução e/ou menos favorável a sobrevivência do indutor. Contudo, o indutor de A. spruceanum supera a barreira química constituída pelos fenóis totais, altera os padrões morfogênicos dos tecidos vegetais, em especial dos sistemas fundamental e vascular, se beneficiando tanto da estrutura da galha quanto da possível ação dos fenólicos na proteção química contra seus inimigos naturais.
Agradecimentos
Os autores agradecem à CAPES, pela bolsa de mestrado e auxílio concedido; aos biólogos Frederico Scher Caldeira Takahashi, Bruno Eduardo Fernandes Mota e César Lúcio Lopes de Faria Jr., pelo auxílio nas análises.
Recebido em 20/02/2008
Aceito em 12/05/2008
- Abrahamson, W.G. & Weis, A.E. 1997. Evolutionary ecology across three trophic levels: goldenrods, gall makers and natural enemies. Princeton, Princeton University Press.
- Arduin, M.; Kraus, J.E.; Otto, P.A. & Venturelli, M. 1989. Caracterização morfológica e biométrica de galhas foliares em Struthanthus vulgaris Mart. (Loranthaceae). Revista Brasileira de Biologia 49: 817-823.
- Deverall, B.J. 1977. Defense mechanisms of plants. New York, Cambridge Press.
- Dreger-Jauffret, F. & Shorthouse, J.D. 1992. Diversity of gall-inducing insects and their galls. In: Biology of insect-induced galls. J.D. Shorthouse & O. Rohfritsch (eds.). Oxford, Oxford University.
- Fahn, A. 1990. Plant anatomy. Oxford, Pergamon Press.
- Fernandes, G.W. & Price, P.W. 1992. The adaptive significance of insect gall distribution: survivoship of species in xeric and mesic habitats. Oecologia 90: 14-20.
- Fernandes, G.W. & Price, P.W. 1988. Biogeographical gradients in galling species richness: tests of hypotheses. Oecologia 76: 161-167.
- Gagné, R.J. 1994. The gall midges of the Neotropical region. New York, Cornell University Press.
- Gershenzon, J. 1984. Changes in the levels of plant secondary metabolites under water and nutrient stress. In: Phytochemical adaptations to stress. B.N. Timmermman; C. Sterrlink & F.A. Loewus (eds.). New York, Plenum Press.
- Gleadow, R.M. & Woodrow, I.E. 2002. Defense chemistry of cyanogenic Eucalyptus cladocalyx seedlings is affected by water supply. Tree Physiology 22: 939-945.
- Harborne, J.B. 1984. Phytochemical Methods: a guide to modern techniques of plant analysis. 2nd ed. London, Chapman and Hall.
- Hartley, S.E. 1998. The chemical composition of plant galls: are levels of nutrients and secondary compounds controlled by the gall-former? Oecologia 113: 492-501.
- Hori, K. 1992. Insect secretions and their effect on plant growth, with special reference to hemipterans. Pp. 157-170. In: J.D. Shorthouse & O. Rohfritsch. Biology of insect-induced galls. Oxford, Oxford University Press.
- Johansen, D.A. 1940. Plant microtechnique. New York, McGraw-Hill Book.
- Jones, D.H. 1984. Phenylalanine ammonia-lyase: Regulation of its induction, and its role in plant development. Phytochemistry 23: 1349-1521.
- Larcher, W. 2000. Ecofisiologia vegetal. São Carlos, RiMa Artes e Textos.
- Larson, K.C. & Whitham, T.G. 1991. Manipulation of food resources by a gall-forming aphid: the physiology of sink-source interactions. Oecologia 88: 15-21.
- Mani, M.S. 1964. Ecology of plant galls. The Hague, Dr. W. Junk. Publishers.
- McCrea, K.D.; Abrahamson, W.G. & Weis, A.E. 1985. Goldenrod ball gall effects on Solidago altissima: 14C translocation and growth. Ecology 66: 1902-1907.
- Meyer, J. 1987. Plant galls and gall inducers. Berlin, Gebrüder Borntraeger.
- Nyman, T. & Julkunen-Tiitto J. 2000. Manipulation of the phenolic chemistry of willows by gall-induced sawflies. Proceedings of the National Academy of Sciences of the United States of America 97: 13184-13187.
- Price, P.W.; Waring, G.L. & Fernandes, G.W. 1986. Hypotheses on the adaptative nature of galls. Proceedings of the Entomological Society of Washington 88: 361-363.
- Price, P.W.; Fernandes, G.W. & Waring, G.L. 1987. Adaptive nature of insect galls. Environmental Entomology 16: 15-24.
- Purohit, S.D.; Ramawat, K.G. & Arya, H.C. 1979. Phenolics, peroxidase and phenolase as related to gall formation in some arid zone plants. Current Science 48: 714-716.
- Rivero, R.M.; Ruiz, J.M.; Garcia, P.C.; López-Lefebre, L.R.; Sánchez, E. & Romero, L. 2001. Resistance to cold and heat stress: accumulation of phenolic compounds in tomato and watermelon plants. Plant Science 160: 315-321.
- Rohfritsch, O. 1992. Patterns in gall development. In: Biology of insect-induced galls. J.D. Shorthouse & O. Rohfritsch (eds.). New York, Oxford Univ. Press.
- Stone, G.N. & Schönrogge, K. 2003. The adaptive significance of insect gall morphology. Trends in Ecology and Evolution 18: 512-522.
- Thiébaut, M. 2000. A foliar morphometric approach to the study of Salicaceae. The Botanical Review 66: 423-439.
- Waterman, P.G. & Mole, S. 1994. Analysis of phenolic plant metabolites. Oxford, Blackwell Scientific Publications.
Datas de Publicação
-
Publicação nesta coleção
09 Out 2009 -
Data do Fascículo
Mar 2009
Histórico
-
Recebido
20 Fev 2008 -
Aceito
12 Maio 2008