Resumos
A síndrome hepatopulmonar consiste na tríade de doença hepática, dilatações vasculares intrapulmonares e hipoxemia. Não há relatos de síndrome hepatopulmonar associada com SIDA. Relatamos o caso de uma mulher de 43 anos portadora de SIDA e de cirrose hepática por hepatite C, em uso de cotrimoxazol profilático para pneumocistose e de terapia anti-retroviral, com dispnéia progressiva, cianose, baqueteamento digital, aranhas vasculares e exame do tórax normal. A radiografia do tórax mostrava infiltrado retículo-nodular, o gradiente alvéolo-arterial de oxigênio estava aumentado e a função hepática alterada. Shunt intrapulmonar foi evidenciado por ecocardiografia bidimensional transtorácica e por cintilografia pulmonar perfusional, confirmando-se a síndrome hepatopulmonar.
Síndrome hepatopulmonar; Síndrome da imunodeficiência humana adquirida; Hepatite viral humana; Anoxemia; Cirrose hepática
Hepatopulmonary syndrome is characterized by a triad consisting of liver disorder, pulmonary vascular dilatation, and hypoxemia. No case of hepatopulmonary syndrome associated with AIDS has been reported so far. In this study, the authors report the case of a 43-year woman with AIDS and virus C cirrhosis taking prophylactic cotrimoxazole for pneumocystosis and retroviral therapy. Upon admission, the patient presented dyspnea, cyanosis, digital clubbing, vascular spiders, and normal chest examination. Chest X-ray revealed bilateral interstitial infiltration and evidenced increased alveolar-arterial gradient and liver function impairment. Intrapulmonary shunt was evidenced by contrast-enhanced echocardiography and radionuclide perfusion scanning, thus confirming hepatopulmonary syndrome.
Hepatopulmonary syndrome; Acquired human immunodeficiency syndrome; Human viral hepatitis; Anoxemia; Liver cirrhosis
RELATO DE CASO
Síndrome hepatopulmonar em paciente com cirrose por vírus C e SIDA* * Trabalho realizado no Hospital de Clínicas de Porto Alegre ¾ Serviço de Pneumologia.
MARIA ANGÉLICA PIRES FERREIRA1 * Trabalho realizado no Hospital de Clínicas de Porto Alegre ¾ Serviço de Pneumologia. , MARCELO BASSO GAZZANA2 * Trabalho realizado no Hospital de Clínicas de Porto Alegre ¾ Serviço de Pneumologia. , SÉRGIO SALDANHA MENNA BARRETO3 * Trabalho realizado no Hospital de Clínicas de Porto Alegre ¾ Serviço de Pneumologia. , MARLI MARIA KNORST4 * Trabalho realizado no Hospital de Clínicas de Porto Alegre ¾ Serviço de Pneumologia.
A síndrome hepatopulmonar consiste na tríade de doença hepática, dilatações vasculares intrapulmonares e hipoxemia. Não há relatos de síndrome hepatopulmonar associada com SIDA. Relatamos o caso de uma mulher de 43 anos portadora de SIDA e de cirrose hepática por hepatite C, em uso de cotrimoxazol profilático para pneumocistose e de terapia anti-retroviral, com dispnéia progressiva, cianose, baqueteamento digital, aranhas vasculares e exame do tórax normal. A radiografia do tórax mostrava infiltrado retículo-nodular, o gradiente alvéolo-arterial de oxigênio estava aumentado e a função hepática alterada. Shunt intrapulmonar foi evidenciado por ecocardiografia bidimensional transtorácica e por cintilografia pulmonar perfusional, confirmando-se a síndrome hepatopulmonar. (J Pneumol 2000;27(1):52-55)
Hepatopulmonary syndrome in a patient with AIDS and virus C cirrhosis (viral cirrhosis type C)
Hepatopulmonary syndrome is characterized by a triad consisting of liver disorder, pulmonary vascular dilatation, and hypoxemia. No case of hepatopulmonary syndrome associated with AIDS has been reported so far. In this study, the authors report the case of a 43-year woman with AIDS and virus C cirrhosis taking prophylactic cotrimoxazole for pneumocystosis and retroviral therapy. Upon admission, the patient presented dyspnea, cyanosis, digital clubbing, vascular spiders, and normal chest examination. Chest X-ray revealed bilateral interstitial infiltration and evidenced increased alveolar-arterial gradient and liver function impairment. Intrapulmonary shunt was evidenced by contrast-enhanced echocardiography and radionuclide perfusion scanning, thus confirming hepatopulmonary syndrome.
Key words ¾ Hepatopulmonary syndrome. Acquired human immunodeficiency syndrome. Human viral hepatitis. Anoxemia. Liver cirrhosis.
CPT ¾ Capacidade pulmonar total
CVF ¾ Capacidade vital forçada
DLCO¾ Difusão pelo monóxido de carbono
HCV ¾ Vírus da hepatite C
HDL ¾ Desidrogenase láctica
HIV ¾ Vírus da imunodeficiência humana
NO ¾ Óxido nítrico
PCP ¾ Pneumonia por P. carinii
SHP ¾ Síndrome hepatopulmonar
SIDA ¾ Síndrome da imunodeficiência humana adquirida
TCAR ¾ Tomografia computadorizada de alta resolução
TP ¾ Tempo de protrombina
VR ¾ Volume residual
INTRODUÇÃO
A associação entre hipoxemia e hepatopatia crônica foi primeiramente sugerida por Flückiger em 1884, que descreveu o caso de uma mulher com cianose, hipocratismo digital e cirrose(1).
A síndrome hepatopulmonar (SHP) consiste na tríade de doença hepática, dilatações vasculares pulmonares e hipoxemia, caracterizada pela presença de shunt pulmonar direita-esquerda, com sangue venoso atingindo a circulação arterial, sendo considerada a principal causa de hipoxemia grave em hepatopatas crônicos(1,3).
Há evidências na literatura de que a co-infecção pelo HIV possa modificar a história natural da hepatite C, levando a uma progressão mais rápida para cirrose(10). Não há relatos anteriores de síndrome hepatopulmonar em pacientes com SIDA.
RELATO DO CASO
Mulher de 43 anos, foi admitida por dispnéia progressiva e hipoxemia. Sabia-se portadora do vírus da imunodeficiência humana (HIV) havia seis anos, com diagnóstico de síndrome da imunodeficiência humana (SIDA) havia três anos, quando apresentou contagem de linfócitos CD4 < 200 cél/ml. Relatava abuso de álcool no passado. Ex-tabagista havia cinco anos, total de 24 maços-anos. Três anos atrás recebeu o diagnóstico de cirrose, apresentando sinais de hipertensão porta por ecografia abdominal e PCR (polimerase chain reaction) no sangue positivo para o vírus da hepatite C (HCV). Estava recebendo profilaxia para pneumocistose havia dois anos com cotrimoxazol três vezes por semana. Havia seis meses vinha fazendo uso de terapia anti-retroviral composta por estavudina, lamivudina e indinavir (então com carga viral de 220 mil cópias/ml).
A paciente referia dispnéia em repouso, negava tosse e febre. Apresentava-se com cianose central, taquipnéia, baqueteamento digital, aranhas vasculares cutâneas disseminadas. Ausculta pulmonar e cardíaca, normais. Pressão arterial sistêmica de 100/60mmHg. Não apresentava sinais clínicos de ascite. Baço palpável, aumentado.
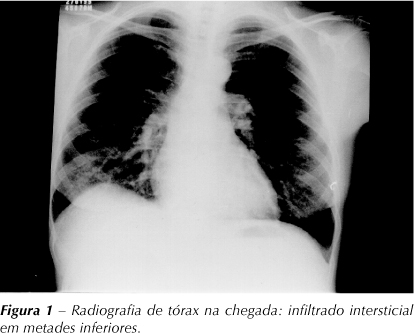
A radiografia simples de tórax mostrou infiltrado retículo-nodular em metades inferiores dos pulmões e sinais de fibroatelectasia em lobo superior direito (Figura 1). Gasometria arterial em repouso, sentada, demonstrou hipoxemia grave, com pH = 7,49, PaO2 = 52mmHg, PaCO2 = 21,3mmHg, SaO2 = 89%. Demais exames laboratoriais evidenciaram plaquetopenia (28.000/mm3), leucopenia (leucócitos totais = 5.300cél/mm3) e alteração de provas de função hepática, com TP prolongado, hipoalbuminemia (2,1mg/dL) e hiperbilirrubinemia (BT = 15,5mg/dL). Também demonstrou-se elevação de enzimas hepáticas, com alanina aminotransferase (ALT) de 162UI/L e aspartato aminotransferase (AST) de 72UI/L. HDL sérica = 267U/L (normal 210-425U/L).
Como conduta inicial prescreveu-se oxigenioterapia e cotrimoxazol em doses para pneumocistose associado a prednisona, sem melhora significativa após uma semana de tratamento. Foi submetida a tomografia computadorizada de tórax convencional, a qual foi normal, exceto por lesão fibroatelectásica em lobo superior direito (Figura 3). Procedeu-se, então, à avaliação funcional pulmonar, com os seguintes resultados: CVF = 3,44L (110% do previsto), VEF1 = 2,8L (104%), VEF1/CVF% = 81, CPT = 5,14L (106%), VR = 1,78L (110%), VR/CPT = 34,6% (107%), difusão pelo monóxido de carbono pelo método da respiração única (DLCO) = 10,33ml/min/mmHg (37,2%), DLCO/VA = 2,44ml/min/mmHg (42,5%). A PaO2 atingida no teste de inalação de oxigênio a 100% foi de 314,3mmHg, com shunt calculado de 21% do débito cardíaco.
Ecocardiografia bidimensional transtorácica com teste de microbolhas foi compatível com shunt intrapulmonar. Cintilografia pulmonar perfusional com 99mTc-MAA mostrou hipercaptação extrapulmonar intensa, com shunt corporal total estimado em 41% (Figura 2). Pesquisa de ortodeoxia foi positiva, com SaO2 = 95% na posição supina e 89% em ortostatismo. Teste da caminhada de seis minutos demonstrou dessaturação ao exercício e baixa capacidade funcional. Diagnosticou-se síndrome hepatopulmonar, sendo suspenso o tratamento para pneumocistose.
Revisão dos exames laboratoriais demonstrou que vinha cronicamente hipoxêmica havia cerca de dois anos, com aumento progressivo do gradiente alvéolo-arterial de O2 e exacerbações periódicas. Havia sido submetida a vários tratamentos empíricos para pneumocistose nos últimos três anos, sempre com lavados bronquíolo-alveolares negativos.
A paciente recebeu alta com melhora da dispnéia e da hipoxemia, com PaO2 = 75mmHg e PaCO2 = 29mmHg em repouso, em ar ambiente. Foi indicada oxigenoterapia no exercício e modificado esquema anti-retroviral com base na hepatotoxicidade das drogas. A paciente abandonou o seguimento ambulatorial.
DISCUSSÃO
Dispnéia e hipoxemia são manifestações comuns de doenças oportunísticas em sidéticos. Entre elas encontra-se a pneumonia por Pneumocistis carinii (PCP), que acomete pacientes em uma fase de imunodepressão já avançada. Outras causas incluem pneumonias bacterianas, tuberculose extensa, citomegalovirose e sarcoma de Kaposi com comprometimento pulmonar. Além disso, pneumotórax, reações a drogas (ex.: metemoglobinemia por dapsona), hiper-reatividade brônquica, hipertensão pulmonar primária e manifestações respiratórias de doenças extrapulmonares (como miocardiopatia ou nefropatia com edema pulmonar secundário) também devem ser lembrados no paciente com SIDA(2).
Anormalidades na oxigenação arterial são comuns em cirróticos. Em uma das séries tais alterações estiveram presentes em 56% dos candidatos a transplante hepático. A hipoxemia na doença hepática avançada tem sido atribuída a várias causas, as principais sendo: 1) distúrbio ventilação-perfusão; 2) defeito difusional; e 3) shunt intrapulmonar direita-esquerda, através de dilatações vasculares intrapulmonares(1,3,4). Estudos recentes encontraram prevalência de SHP de 13 a 15%, em candidatos a transplante hepático(1). A SHP mais comumente ocorre em vigência de doença hepática que leve a cirrose, mas tem sido relatada também em casos de hipertensão portal não cirrótica(1,4).
Acredita-se que na gênese dos shunts estejam implicados possíveis desequilíbrios entre substâncias vasodilatadoras e vasoconstritoras metabolizadas pelo fígado, bem como alterações na regulação da resposta à hipoxia em certos vasos pulmonares(1,5,6). Recentemente, crescente atenção vem sendo dada ao papel do óxido nítrico (NO) na patogenia da SHP. Tem sido observado nível aumentado de NO no ar exalado em pacientes com SHP em relação a cirróticos sem a síndrome(10).
Os pacientes com SHP apresentam-se mais freqüentemente com manifestações hepáticas do que com queixas respiratórias; apenas 10% se apresentam com dispnéia(1). Os sinais clínicos incluem hipocratismo digital e cianose das extremidades em vigência de hipoxemia significativa, além dos sinais de hepatopatia crônica. Clinicamente, os shunts vasculares intrapulmonares são associados com o surgimento de ortodeoxia (queda da saturação da hemoglobina em ortostatismo que melhora com o decúbito) e platipnéa, que se refere à dispnéia em ortostatismo e aliviada pelo decúbito(1,3,5).
O diagnóstico da SHP envolve a demonstração de anormalidades nas trocas gasosas evidenciadas por um gradiente alvéolo-arterial de oxigênio aumentado, bem como a presença de dilatações vasculares pulmonares, na ausência de disfunção cardiovascular ou pneumopatia associada(1,3,4).
A presença de infiltrado pulmonar intersticial nas metades inferiores dos pulmões tem sido atribuída às dilatações vasculares pulmonares, estando presente em cerca de 46% a 100% dos casos descritos da síndrome. Pode ser fonte de dúvidas diagnósticas, sugerindo erroneamente diagnósticos como fibrose pulmonar, sarcoidose ou outras doenças granulomatosas(1,5,8,9). A TCAR pode mostrar dilatações vasculares em bases, com maior número de ramos vasculares visíveis(9). No presente caso, o infiltrado intersticial à radiografia simples contribuiu para o diagnóstico inicial de pneumocistose. Infelizmente, a tomografia não foi feita com técnica de alta resolução.
Uma vez que no presente caso não foi realizado LBA, não é possível excluir com certeza o diagnóstico de pneumocistose. A melhora pronunciada da hipoxemia também não é esperada na SHP, levantando dúvidas sobre a coexistência da pneumonia por PCP. Por outro lado, é possível que ocorram exacerbações transitórias na evolução da SHP, cuja história natural não tem sido relatada mais detalhadamente na literatura. A posição em que foram coletadas as amostras para gasometria arterial também é de importância para considerar a evolução da hipoxemia, devendo ser coletadas na mesma posição, preferivelmente em ortostatismo. No presente caso, não estamos certos das condições de coleta do exame.
As provas de função pulmonar em geral evidenciam redução da DLCO, vista também em cirróticos sem a síndrome, com volumes e fluxos expiratórios normais(5). DLCO baixa, por outro lado, também ocorre na pneumocistose.
Os achados da avaliação funcional pulmonar no presente caso foram compatíveis com aqueles descritos na literatura.
A presença de dilatações vasculares intrapulmonares pode ser demonstrada por três modalidades de exames de imagem: ecocardiografia com contraste, cintilografia com macroagregado de albumina marcado por Tc-99 e arteriografia pulmonar.
O tratamento da SHP inclui a oxigenoterapia, a qual em geral tem caráter paliativo, bem como medidas que visam a reversão dos mecanismos subjacentes à hipoxemia(1,3,5).
Várias medidas farmacológicas têm sido testadas, a maioria com resultados desapontadores. Fármacos como prostaglandinas, somatostatina, almitrina e indometacina têm sido estudados, até o momento sem benefício significativo comprovado(1,3,4). Um caso de reversão transitória de hipoxemia com azul de metileno foi relatado. O efeito do azul de metileno tem sido atribuído ao bloqueio da estimulação da guanil-ciclase pelo NO, ou ainda à geração de radicais superóxido(10).
O transplante hepático tem sido considerado o principal tratamento da SHP. Em uma revisão de 81 casos de SHP submetidos a transplante, houve melhora ou normalização dos gases arteriais em 66 pacientes (82%), dentro de 15 meses após a cirurgia(4).
CONCLUSÃO
A síndrome hepatopulmonar deve ser sempre considerada como possível causa de hipoxemia em pacientes com hepatopatia avançada. Os shunts intrapulmonares, caracterizados por hipoxemia com aumento do gradiente alvéolo-arterial de oxigênio, podem ser decorrentes de diferentes mecanismos fisiopatológicos, com implicações clínicas e terapêuticas diversas.
Hipoxemia e infiltrado pulmonar podem ser manifestações de doenças não infecciosas ou não oportunísticas, as quais não devem ser esquecidas no paciente com SIDA e hepatopatia avançada.
1. Residente do 3º ano de Pneumologia.
2. Residente do 3º ano de Pneumologia; Internista.
3. Professor Titular do Departamento de Medicina Interna-UFRGS; Doutor em Pneumologia.
4. Professora Adjunta do Departamento de Medicina Interna UFRGS; Doutora em Pneumologia.
Endereço para correspondência ¾ Maria Angélica Pires Ferreira, Av. Palmeira, 540/602 ¾ 90470-300 ¾ Porto Alegre, RS. Tel. (51) 338-4785; E-mail: mapf@via-rs.com.br
Recebido para publicação em 5/6/00. Reapresentado em 16/10/00. Aprovado, após revisão, em 13/11/00.
- 1. Castro M, Krowka MJ. Hepatopulmonary syndrome. Clin Chest Med 1996;17:35-48.
- 2. Vander Els NJ, Stover DE. Approach to the patient with pulmonary disease. Clin Chest Med 1996;17:767-785.
- 3. Garcia E, Silvério AO, Melo Brandão AB, Moreira JS. Função pulmonar na cirrose hepática. J Pneumol 1997;23:225-230.
- 4. Krowka MJ, Porayko MK, Plevak DJ, Pappas C, et al. Hepatopulmonary syndrome with progressive hypoxemia as an indication for liver transplantation: case reports and literature review. Mayo Clin Proc 1997;72:44-53.
- 5. Lange AP, Stoller JK. The hepatopulmonary syndrome. Ann Intern Med 1995;122:521-529.
- 6. Augusti AGN, Roca J, Rodriguez-Roisin R. Mechanisms of gas exchange impairment in patients with liver cirrhosis. Clin Chest Med 1996;17:49-67.
- 7. Krowka M. Hepatopulmonary syndrome versus portopulmonary hypertension: distinctions and dilemmas. Hepatology 1997;25:1282-1284.
- 8. Rezende MC, Martinez JAB, Jasinowodolinski D, Rodrigues Jr M, Pereira CAC. Infiltrado intersticial pulmonar em paciente hepatopata crônico. J Pneumol 1996;22:217-219.
- 9. McAdams HP, Erasmus J, Crokett R, Mitchell J, Godwin JD, McDermott VG. The hepatopulmonary syndrome: radiologic findings in 10 patients. AJR Am J Roentgenol 1996;166:1379-1385.
- 10. Rodriguez-Roisin R, Barberà JA. Hepatopulmonary syndrome: is NO the right answer? Gastroenterology 1997;113:682-683.
- 11. Soto B, Sánchez-Quijano LR, et al. Human immunodeficiency virus infection modifies the natural history of chronic parenterally-acquired hepatitis C with an unusually rapid progression to cirrhosis. Hepatol 1997;26:1-5.
Datas de Publicação
-
Publicação nesta coleção
15 Out 2002 -
Data do Fascículo
Jan 2001
Histórico
-
Recebido
05 Jun 2000 -
Revisado
16 Out 2000 -
Aceito
13 Nov 2000