Resumos
O tecido muscular esquelético possui a maior massa do corpo humano, com 45% do peso total. As lesões musculares podem ser causadas por contusões, estiramentos ou lacerações. A atual classificação separa as lesões entre leve, moderada e grave. Os sinais e sintomas das lesões grau I são edema e desconforto; grau II, perda de função, gap e equimose eventual; grau III, rotura completa, dor intensa e hematoma extenso. O diagnóstico pode ser confirmado por: ultrassom - dinâmico, barato, porém examinador-dependente; tomografia ou ressonância magnética - maior definição anatômica, porém estático. A fase inicial do tratamento se resume ao protocolo PRICE. AINH, ultrassom terapêutico, fortalecimento e alongamento após a fase inicial e amplitudes de movimento sem dor são utilizados no tratamento clínico. Já o cirúrgico possui indicações precisas: drenagem do hematoma, reinserção e reforço musculotendíneos.
Musculoesquelético; fisiopatologia; Musculoesquelético; lesões; Musculoesquelético; cirúrgica; Regeneração
Skeletal muscle tissue has the largest mass in the human body, accounting for 45% of the total weight. Muscle injuries can be caused by bruising, stretching or laceration. The current classification divides such injuries into mild, moderate and severe. The signs and symptoms of grade I lesions are edema and discomfort; grade II, loss of function, gaps and possible ecchymosis; and grade III, complete rupture, severe pain and extensive hematoma. The diagnosis can be confirmed by: ultrasound, which is dynamic and cheap, but examiner dependent; and tomography or magnetic resonance, which gives better anatomical definition, but is static. Initial phase of the treatment can be summarized as the "PRICE" protocol. NSAIDs, ultrasound therapy, strengthening and stretching after the initial phase and range of motion without pain are used in clinical treatment. On the other hand, surgery has precise indications: hematoma drainage and muscle-tendon reinsertion and reinforcement.
Muscle; Skeletal; physiopathology; Muscle; Skeletal; injury; Muscle; Skeletal; surgery; Regeneration
ARTIGO DE ATUALIZAÇÃO
Lesão muscular - fisiopatologia, diagnóstico, tratamento e apresentação clínica
Tiago Lazzaretti FernandesI; André PedrinelliII; Arnaldo José HernandezIII
IMestrando do Departamento de Ortopedia e Traumatologia da Faculdade de Medicina da Universidade de São Paulo; Colaborador do Centro de Excelência Médica da FIFA
IIDoutor e Mestre em Ortopedia; Assistente do Grupo de Medicina do Esporte do Instituto de Ortopedia e Traumatologia do HC/FMUSP; Coordenador do Centro de Excelência Médica da FIFA
IIIProfessor Associado da Faculdade de Medicina da Universidade de São Paulo; Chefe do Grupo de Medicina do Esporte do Instituto de Ortopedia e Traumatologia do HC/FMUSP
Correspondência Correspondência: Rua Dr. Ovídio Pires de Campos, 333, 2º andar (LEM) 05403-010 - São Paulo, SP, Brasil E-mail: Tiago.lazzaretti@usp.br
RESUMO
O tecido muscular esquelético possui a maior massa do corpo humano, com 45% do peso total. As lesões musculares podem ser causadas por contusões, estiramentos ou lacerações. A atual classificação separa as lesões entre leve, moderada e grave. Os sinais e sintomas das lesões grau I são edema e desconforto; grau II, perda de função, gap e equimose eventual; grau III, rotura completa, dor intensa e hematoma extenso. O diagnóstico pode ser confirmado por: ultrassom - dinâmico, barato, porém examinador-dependente; tomografia ou ressonância magnética - maior definição anatômica, porém estático. A fase inicial do tratamento se resume ao protocolo PRICE. AINH, ultrassom terapêutico, fortalecimento e alongamento após a fase inicial e amplitudes de movimento sem dor são utilizados no tratamento clínico. Já o cirúrgico possui indicações precisas: drenagem do hematoma, reinserção e reforço musculotendíneos.
Descritores: Musculoesquelético/fisiopatologia; Musculoesquelético/lesões; Musculoesquelético/cirúrgica; Regeneração
INTRODUÇÃO
As lesões musculares são a causa mais frequente de incapacidade física na prática esportiva. Estima-se que 30 a 50% de todas as lesões associadas ao esporte são causadas por lesões de tecidos moles(1).
Apesar de o tratamento não cirúrgico resultar em bom prognóstico na maioria dos atletas com lesão muscular, as consequências da falha do tratamento podem ser dramáticas, postergando o retorno à atividade física por semanas ou até mesmo meses(2). O conhecimento de alguns princípios básicos da regeneração e dos mecanismos de reparo do músculo esquelético pode ajudar a evitar perigos iminentes e acelerar o retorno ao esporte.
Anatomia e biomecânica
As fibras musculares geralmente se originam em um osso ou tecido conectivo denso e se inserem a outro osso através de uma inserção tendínea.
Há músculos que atravessam uma ou mais articulações para gerar movimento. Os músculos com função tônica ou postural geralmente são uniarticulares, largos, planos, com velocidade de contração baixa e com capacidade de geração e manutenção de força contrátil grande. Geralmente estão localizados nos compartimentos mais profundos.
Os músculos biarticulares têm velocidade de contração e capacidade para mudança de comprimento maiores, contudo, menor capacidade de suportar tensão. Geralmente estão localizados em compartimentos superficiais.
Quanto à forma, os músculos fusiformes permitem uma maior amplitude de movimento, enquanto que os músculos penados têm maior força contrátil.
O comprimento da fibra é um determinante importante da quantidade de contração possível no músculo. Como as fibras musculares geralmente apresentam distribuição oblíqua dentro de um ventre muscular, elas geralmente são menores do que o comprimento total do músculo.
Mecanismos de lesão
As lesões musculares podem ser causadas por contusões, estiramentos ou lacerações. Mais de 90% de todas as lesões relacionadas ao esporte são contusões ou estiramento(3). Já as lacerações musculares são as lesões menos frequentes no esporte.
A força tênsil exercida sobre o músculo leva a um excessivo estiramento das miofibrilas e, consequentemente, a uma ruptura próxima à junção miotendínea. Os estiramentos musculares são tipicamente observados nos músculos superficiais que trabalham cruzando duas articulações, como os músculos reto femoral, semitendíneo e gastrocnêmio.
Classificação
A atual classificação das lesões musculares separa as lesões entre leve, moderada e grave a partir dos aspectos clínicos revelados(2).
Estiramentos e contusões leves (grau I) representam uma lesão de apenas algumas fibras musculares com pequeno edema e desconforto, acompanhadas de nenhuma ou mínima perda de força e restrição de movimentos. Não é possível palpar-se qualquer defeito muscular durante a contração muscular. Apesar de a dor não causar incapacidade funcional significativa, a manutenção do atleta em atividade não é recomendada devido ao grande risco de aumentar a extensão da lesão(4).
Estiramentos e contusões moderadas (grau II) provocam um dano maior ao músculo com evidente perda de função (habilidade para contrair). É possível palpar-se um pequeno defeito muscular, ou gap, no sítio da lesão, e ocorre a formação de um discreto hematoma local com eventual ecmose dentro de dois a três dias. A evolução para a cicatrização costuma durar de duas a três semanas e, ao redor de um mês, o paciente pode retornar à atividade física de forma lenta e cuidadosa(4).
Uma lesão estendendo-se por toda a sessão transversa do músculo e resultando em virtualmente completa perda de função muscular e dor intensa é determinada como estiramento ou contusão grave (grau III). A falha na estrutura muscular é evidente, e a equimose costuma ser extensa, situando-se muitas vezes distante ao local da ruptura. O tempo de cicatrização desta lesão varia de quatro a seis semanas. Este tipo de lesão necessita de reabilitação intensa e por períodos longos de até três a quatro meses. O paciente pode permanecer com algum grau de dor por meses após a ocorrência e tratamento da lesão(4).
FISIOPATOLOGIA
O que distingue a cicatrização da lesão muscular da cicatrização óssea é que no músculo ocorre um processo de reparo, enquanto que no tecido ósseo ocorre um processo de regeneração.
A cicatrização do músculo esquelético segue uma ordem constante, sem alterações importantes conforme a causa (contusão, estiramento ou laceração).
Três fases foram identificadas neste processo: destruição, reparo e remodelação. As duas últimas fases (reparo e remodelação) se sobrepõem e estão intimamente relacionadas.
Fase 1: destruição - caracterizada pela ruptura e posterior necrose das miofibrilas, pela formação do hematoma no espaço formado entre o músculo roto e pela proliferação de células inflamatórias.
Fase 2: reparo e remodelação - consiste na fagocitose do tecido necrótico, na regeneração das miofibrilas e na produção concomitante do tecido cicatricial conectivo, assim como a neoformação vascular e crescimento neural.
Fase 3: remodelação - período de maturação das miofibrilas regeneradas, de contração e de reorganização do tecido cicatricial e da recuperação da capacidade funcional muscular.
Como as miofibrilas são fusiformes e muito compridas, há um risco iminente de que a necrose iniciada no local da lesão se estenda por todo o comprimento da fibra. Contudo, existe uma estrutura específica, chamada de banda de contração, que é uma condensação do material citoesquelético que atua como um "sistema antifogo"(5) (Figura 1).
Uma vez que a fase de destruição diminui, o presente reparo da lesão muscular começa com dois processos simultâneos e competitivos entre si: a regeneração da miofibrila rota e a formação do tecido conectivo cicatricial. Uma progressão balanceada destes processos é pré-requisito para uma ótima recuperação da função contrátil do músculo(5).
Embora as miofibrilas sejam genericamente consideradas não mitóticas, a capacidade regenerativa do músculo esquelético é garantida por um mecanismo intrínseco que restaura o aparato contrátil lesionado. Durante o desenvolvimento embrionário, um pool de reserva de células indiferenciadas, chamado de células satélites, é armazenado abaixo da lâmina basal de cada miofibrila. Em resposta à lesão, estas células primeiramente se proliferam, diferenciam-se em miofibrilas e, finalmente, juntam-se umas às outras para formar miotúbulos multinucleados(6).
Com o tempo, a cicatriz formada diminui de tamanho, levando as bordas da lesão à uma aderência maior entre si. Contudo, não se sabe se a transecção das miofibrilas dos lados opostos da cicatriz vai, definitivamente, se fundir entre si ou se irá formar um septo de tecido conectivo entre elas(7).
Imediatamente após a lesão muscular, o intervalo formado entre a ruptura das fibras musculares é preenchido por hematoma. Dentre o primeiro dia, as células inflamatórias, incluindo os fagócitos, invadem o hematoma e começam a organizar o coágulo(8).
A fibrina derivada de sangue e a fibronectina se intercalam para formar o tecido de granulação, uma armação inicial e ancoramento do local para os fibroblastos recrutados(5). Mais importante, este novo tecido formado provê a propriedade de tensão inicial para resistir às contrações aplicadas contra ele.
Aproximadamente 10 dias após o trauma, a maturação da cicatriz atinge um ponto em que não é mais o local mais frágil da lesão muscular(9).
Apesar de a maioria das lesões do músculo esquelético curar sem a formação de tecido cicatricial fibroso incapacitante, a proliferação dos fibroblastos pode ser excessiva, resultando na formação de tecido cicatricial denso dentro da lesão muscular.
Um processo vital para a regeneração do músculo lesionado é a área de vascularização. A restauração do suprimento vascular é o primeiro sinal de regeneração e pré-requisito para as recuperações morfológica e funcional subsequentes(10).
DIAGNÓSTICO
O diagnóstico da lesão muscular inicia-se com uma história clínica detalhada do trauma, seguida por um exame físico com a inspeção e palpação dos músculos envolvidos, assim como os testes de função com e sem resistência externa(11). O diagnóstico é fácil quando uma típica história de contusão muscular é acompanhada por um evidente edema ou uma equimose distal à lesão (Figura 2).
Exames complementares
Pequenos hematomas superficiais e aqueles que são profundos podem ser de difícil identificação. Exames de imagem como ultrassom, tomografia computadorizada e ressonância magnética provêem informações úteis para se verificar e determinar a lesão com maior precisão.
A ultrassonografia (Figura 3) é tradicionalmente considerada o método de escolha para o diagnóstico da lesão muscular, visto que é um método de imagem relativamente barato e que possibilita avaliar dinamicamente a contração e rotura muscular. Possui a desvantagem de ser examinador-dependente.
A ressonância magnética (Figura 4) substitui a ultrassonografia na avaliação de muitas doenças musculoesqueléticas. Possui boa sensibilidade para edemas, cálculo do tamanho do hematoma e avaliação de desinserções musculotendíneas. Contudo, assim como a tomografia, é um exame estático.
TRATAMENTO
Os atuais princípios de tratamento da lesão muscular são carentes de bases cientificas sólidas.
A mobilização precoce induz a um aumento da vascularização local na área da lesão, melhor regeneração das fibras musculares e melhor paralelismo entre a orientação das miofibrilas regeneradas em comparação à restrição do movimento(12). Contudo, re-rupturas no sítio original do trauma são comuns se a mobilização ativa iniciar-se imediatamente após a lesão(13).
Um curto período de imobilização com enfaixamento adesivo firme ou similar é recomendado. Este período de repouso permite que o tecido cicatricial conecte novamente à falha muscular(3).
O paciente deve utilizar um par de muletas para as lesões musculares mais graves dos membros inferiores, principalmente nos três a sete dias iniciais.
Fase aguda
O tratamento imediato para a lesão do músculo esquelético ou qualquer tecido de partes moles é conhecido como princípio PRICE (Proteção, Repouso, Gelo ou Ice, Compressão e Elevação). A justificativa do uso do princípio PRICE é por ele ser muito prático, visto que as cinco medidas clamam por minimizar o sangramento do sítio da lesão(11).
Colocando-se o membro lesionado em repouso logo após o trauma, previne-se uma retração muscular tardia ou formação de um gap muscular maior por se reduzir o tamanho do hematoma e, subsequentemente, o tamanho do tecido conectivo cicatricial. Com relação ao uso do gelo, mostrou-se que o uso precoce de crioterapia está associado a um hematoma significativamente menor no gap das fibras musculares rompidas, menor inflamação e regeneração acelerada(14).
De acordo com os conhecimentos atuais, é recomendada a combinação do uso de gelo e compressão por turnos de 15 a 20 minutos, repetidos entre intervalos de 30 a 60 minutos, visto que este tipo de protocolo resulta em 3º a 7ºC de decaimento da temperatura intramuscular e a 50% de redução do fluxo sanguíneo intramuscular(15).
Finalmente, a elevação do membro acima do nível do coração resulta na diminuição da pressão hidrostática, reduzindo o acúmulo de líquido no espaço intersticial.
Medicação
Existem poucos estudos controlados utilizando anti-inflamatórios não hormonais (AINH) ou glicocorticoides no tratamento de lesões musculares em humanos. O'Grady et al reportaram que o uso de anti-inflamatórios no tratamento da necrose in situ, o tipo mais leve de lesão muscular, em curto prazo, resulta em uma melhora transitória na recuperação da lesão muscular induzida pelo exercício(16). Apesar do fato da falta de evidência, os efeitos do AINH têm sido bem documentados. Järvinen defendeu que o uso em curto período na fase precoce da recuperação diminuiu a reação inflamatória celular sem efeitos colaterais no processo de cicatrização, na força tênsil ou na habilidade de contração muscular.
Além disso, os AINH não retardam as habilidades ativadas pelas células satélites em se proliferar ou a formação dos miotúbulos(17). Contudo, o uso crônico parece ser prejudicial no modelo de contração excêntrica nas lesões por estiramento como discutido por Mishra et al(18).
Com relação ao uso de glicocorticoides, foram reportados atrasos na eliminação do hematoma e tecido necrótico, retardo no processo de regeneração e redução da força biomecânica do músculo lesionado(19).
Tratamento pós-fase aguda
1. Treinamento isométrico (ie. contração muscular em que o comprimento do músculo se mantém constante e a tensão muda) pode ser iniciado sem o uso de pesos e posteriormente com o acréscimo deles. Especial atenção deve ser tomada para garantir que todos os exercícios isométricos sejam realizados sem dor.
2. Treinamento isotônico (ie. contração muscular em que o tamanho do músculo muda e a tensão se mantém) pode ser iniciado quando o treino isométrico for realizado sem dor com cargas resistidas.
3. O exercício isocinético com carga mínima pode ser iniciado uma vez que os dois exercícios anteriores sejam realizados sem dor (Figura 5).
A aplicação local de calor ou "terapia de contraste" (quente e frio) pode ser de valor, acompanhado de cuidadoso alongamento passivo e ativo do músculo afetado. Ressalta-se que qualquer atividade de reabilitação deve ser iniciada com o aquecimento adequado do músculo lesionado(20).
Outra razão para o alongamento é distender o tecido cicatricial maduro durante a fase em que ele ainda é plástico. Alongamentos da cicatriz sem dor podem ser adquiridos por estiramentos graduais, começando com turnos de 10 a 15 segundos e, então, progredindo para períodos de até um minuto.
Contudo, se os sintomas causados pela lesão não melhorarem entre três e cinco dias após o trauma, deve-se considerar a possibilidade da existência de um hematoma intramuscular ou um tecido lesionado extenso que necessitará de atenção especial. A punção ou aspiração do hematoma pode ser necessária.
Ultrassom
O ultrassom terapêutico é difusamente recomendado e utilizado no tratamento da lesão muscular, embora exista vaga evidência científica de sua efetividade(21). O fato de o ultrassom produzir micromassagens pelas ondas de alta frequência, aparentemente, funciona para o alívio da dor.
Tratamento cirúrgico
Há indicações precisas em que a intervenção cirúrgica é necessária. Estas indicações incluem: pacientes com grandes hematomas intramusculares, lesões ou roturas completas (grau III) com pouca ou nenhuma musculatura agonista associada e lesões parciais em que mais da metade do músculo esteja roto(22,23).
A intervenção cirúrgica também pode ser considerada se o paciente se queixa de dor persistente à extensão por mais de quatro a seis meses, particularmente se houver déficit de extensão. Neste caso em particular, deve-se suspeitar de adesões por cicatrizes restringindo o movimento muscular no sítio da lesão.
Após o reparo cirúrgico, o músculo deve ser protegido por uma bandagem elástica ao redor do membro a fim de promover relativa imobilidade e compressão. A duração da imobilização naturalmente depende da gravidade do trauma. Pacientes com rotura completa do músculo quadríceps ou gastrocnêmio são instruídos a não colocarem carga no membro por pelo menos quatro semanas.
Se o gap ou falha muscular for excepcionalmente largo, a porção desnervada pode gerar um déficit neurológico permanente e consequente atrofia muscular(9). O reparo cirúrgico nestas circunstâncias aumenta a chance de reinervação e o desenvolvimento de tecido cicatricial espesso pode ser evitado.
Novas perspectivas
O uso terapêutico de fatores de crescimento e a terapia gênica, sozinhos ou em combinação, e a aplicação de células-tronco proporcionam as últimas e mais promissoras opções terapêuticas existentes. Contudo, há, no momento, pouca validação científica para a sua intensificação no tratamento de lesões do músculo esquelético.
Os fatores de crescimento e citocinas são potentes ativadores mitogênicos para inúmeras células, incluindo as MPC durante a regeneração das células musculares lesionadas(24). Portanto, são opções terapêuticas promissoras para auxiliar na recuperação da musculatura esquelética.
Em relação às células tronco, recentemente mostrou-se que, em resposta à lesão, não somente as células tecido-específicas, como também as células tronco não musculares participam do processo de reparo(25).
Os primeiros passos da terapia gênica já foram dados. Os estudos futuros irão demonstrar em que esfera a terapia gênica poderá tornar realidade as atuais expectativas em relação ao tratamento dos traumas musculares.
APRESENTAÇÃO CLÍNICA
Lesão muscular do quadríceps
A lesão distal do quadríceps é uma lesão pouco comum, ocorrendo mais frequentemente em indivíduos acima de 40 anos(26). A lesão pode ocorrer por motivo de trauma direto, mas classicamente é relatada como uma contração excêntrica forçada em posição de leve flexão do membro inferior na tentativa de se recuperar o equilíbrio em um momento de queda.
As roturas espontâneas e as roturas bilaterais foram descritas naqueles atletas com distúrbios metabólicos sistêmicos e com uso de esteroides(27).
O diagnóstico de rotura é baseado nos achados clínicos. O paciente tipicamente apresenta, após uma queda com os joelhos fletidos, uma dor aguda acima da patela e a incapacidade de se manter na posição ortostática sem auxílio.
Durante o exame físico, o paciente não é capaz de estender ativamente o joelho e por muitas vezes existe um intervalo palpável acima da patela, conhecido como o "sinal do sulco" ou gap test. Os pacientes são capazes de fletir ativamente o joelho e possuem flexão e extensão passivas totais do joelho.
A radiografia simples é uma ferramenta barata para o diagnóstico da rotura. Apesar de não mostrar uma alteração específica da lesão, evidencia sinais indiretos da rotura. Edema de partes moles, derrame articular, calcificações, sombra da rotura do quadríceps e patela baixa são todos sinais indiretos vistos na radiografia simples(28).
O ultrassom, assim como a radiografia simples, é outro método barato para se diagnosticar a lesão muscular. A ressonância magnética é particularmente útil para melhor visualização, precisão da localização e extensão da lesão e dos detalhes anatômicos para a programação pré-operatória (Figura 6).
Para as roturas musculares completas, o tratamento é cirúrgico. O tratamento cirúrgico precoce nestes casos está associado aos melhores resultados funcionais(29) (Figura 7). Já o atraso no reparo cirúrgico está associado a um período de fisioterapia prolongado, flexão inadequada e perda de extensão total do joelho(29). Após o reparo cirúrgico, os pacientes têm o joelho imobilizado por quatro a seis semanas.
Lesão dos músculos isquiotibiais
Os músculos isquiotibiais são os menos alongados do membro inferior e, por este motivo, mais facilmente lesionados durante a contração muscular excêntrica.
A gravidade da lesão é geralmente negligenciada, especialmente na fase aguda.
O estiramento dos isquiotibiais é a lesão mais comum nos atletas(30).
O diagnóstico da lesão normalmente é realizado a partir de um alto índice de suspeita clínica e exame clínico cuidadoso. A ressonância magnética é valiosa para se diferenciar entre uma lesão completa ou incompleta e para o planejamento do tratamento (Figura 8).
A rotura completa dos músculos isquiotibiais proximalmente em sua origem é rara. A condução do caso varia entre o tratamento conservador com um imobilizador em flexão ou o reparo cirúrgico em um segundo momento. Embora o reparo cirúrgico em um segundo tempo possa apresentar bons resultados, o reparo precoce permite uma reabilitação funcional mais rápida e evita o sintoma neurológico potencial de ciática glútea.
Lesão da musculatura adutora
O grupo muscular adutor atua em conjunto com os músculos abdominais baixos para se estabilizar a pelve durante as atividades dos membros inferiores. Os atletas que participam de atividades que requerem chutes repetitivos, arranques ou mudanças de direção frequentes possuem maior incidência de dor crônica na topografia dos adutores(31).
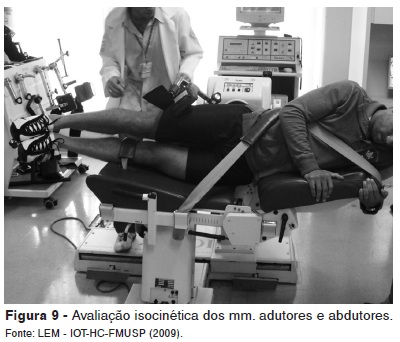
Há evidências de que atletas com fraqueza dos músculos adutores, desequilíbrio entre adutores e abdutores (Figura 9) e diminuição da amplitude do movimento do quadril estão mais propensos a adquirirem pubalgia durante a temporada(32).
Os pacientes tipicamente apresentam um dolorimento na região da virilha ou dor medial na coxa, podendo relatar ou não um fator desencadeante. Ao exame físico, apresenta-se uma dor à palpação com edema focal ao longo dos músculos adutores e diminuição da força muscular e dor ao exercício resistido de adução dos quadris.
O diagnóstico pode ser realizado com os achados do exame físico. Contudo, a ressonância magnética com contraste pode ser útil para se confirmar o diagnóstico ou realizar-se o diagnóstico diferencial entre osteíte púbica e hérnia do esporte(33).
O tratamento inicial é conservador. A infiltração da entese do adutor longo pode ser útil para o tratamento refratário. Nos casos de rotura aguda, o reparo cirúrgico aberto com colocação de âncoras e sutura tem sido descrito com bons resultados(34).
Os pacientes poderão retomar o esporte após o retorno ao padrão prévio de fortalecimento e amplitude de movimento do quadril e a resolução do quadro álgico. Devido à predisposição da lesão do adutor ser causada pelo desequilíbrio muscular, deve-se ter atenção para o fortalecimento da musculatura a fim de se prevenir novas lesões.
Lesão dos músculos gastrocnêmios
Assim como os músculos isquiotibiais e quadríceps, o gastrocnêmio é propenso a lesões, pois cruza duas articulações.
A cabeça medial do gastrocnêmio é mais comumente lesionada do que a lateral, visto que esta é mais ativa(35). A trombose venosa profunda pode estar associada ou ser um diagnóstico diferencial de dor na panturrilha, assim como a tromboflebite(36).
O termo tennis leg tem sido utilizado para se descrever a dor e a lesão na panturrilha. O termo é atribuído ao movimento do saque no tênis em que há uma extensão completa do joelho associada a uma dorsiflexão do tornozelo abrupta provocando o máximo alongamento da panturrilha. Contudo, esta lesão foi descrita também em atletas jovens durante períodos de exercícios extenuantes como basquete, corrida e musculação(37).
O aparecimento da dor é repentino com edema focal e ecmose da panturrilha. Classicamente, o tennis leg é referido como uma lesão da junção miotendínea distal, embora a lesão proximal possa ocorrer.
Por causa da natureza superficial da lesão, a avaliação ultrassonográfica é confiável, possibilita facilmente excluir a presença de trombose venosa profunda e provê a aspiração de coleções líquidas guiadas por imagem.
O tratamento da maioria das lesões do gastrocnêmio é conservador. Ocasionalmente, deve-se realizar cirurgia para se drenar hematomas, reparar uma lesão grau III ou realizar uma descompressão compartimental nos casos de síndrome compartimental.
CONSIDERAÇÕES FINAIS
A compreensão dos mecanismos fisiopatológicos que regulam a reparação muscular e sua adaptação ao treinamento físico são essenciais para o profissional que se propõe a tratar destes pacientes. São a base para o desenvolvimento dos meios de prevenção de lesões e para o tratamento adequado e reabilitação das lesões instaladas.
A respeito do tempo apropriado de retorno ao treino específico para o esporte, a decisão pode ser baseada em duas simples e pouco onerosas medidas: a habilidade de alongar o músculo lesionado tanto quanto o lado contralateral sadio, e ausência da dor no músculo lesionado em movimentos básicos.
Quando o paciente refere alcançar este ponto na recuperação, a permissão de se iniciar gradualmente os exercícios específicos para o esporte é garantida. Contudo, sempre deve ser enfatizado que a fase final de reabilitação deve ser realizada sob supervisão de profissional capacitado.
Trabalho recebido para publicação: 20/11/2010, aceito para publicação: 23/12/2010.
Trabalho realizado no Laboratório de Investigação Médica do Sistema Musculoesquelético - LIM41 do Departamento de Ortopedia e Traumatologia da FMUSP, Grupo de Medicina do Esporte do Instituto de Ortopedia e Traumatologia (IOT) do Hospital das Clínicas da FMUSP e Centro de Excelência Médica da FIFA.
- 1. Herring SA, Nilson KL. Introduction to overuse injuries. Clin Sports Med. 1987;6(2):225-39.
- 2. Pedrinelli A, Fernandes TL, Thiele E, Teixeira WJ. Lesão muscular - ciências básicas, fisiopatologia, diagnóstico e tratamento. In: Alves Júnior WM, Fernandes TD, editors. Programa de atualização em traumatologia e ortopedia (PROATO). Porto Alegre: Artmed; 2006. p. 10, 32.
- 3. Järvinen MJ, Lehto MU. The effects of early mobilisation and immobilisation on the healing process following muscle injuries. Sports Med (Auckland, N.Z.). 1993;15(2):78-89.
- 4. Hernandez AJ. Distensões e rupturas musculares. In: Camanho GL, editor. Patologia do joelho. São Paulo: Sarvier; 1996. p. 132-8.
- 5. Hurme T, Kalimo H, Lehto M, Järvinen M. Healing of skeletal muscle injury: an ultrastructural and immunohistochemical study. Med Sci Sports Exerc. 1991;23(7):801-10.
- 6. Rantanen J, Hurme T, Lukka R, Heino J, Kalimo H. Satellite cell proliferation and the expression of myogenin and desmin in regenerating skeletal muscle: evidence for two different populations of satellite cells. Lab Invest. 1995;72(3):341-7.
- 7. Aärimaa V, Kääriäinen M, Vaittinen S, Tanner J, Järvinen T, Best T, et al Restoration of myofiber continuity after transection injury in the rat soleus. Neuromuscul Disord. 2004;14(7):421-8.
- 8. Cannon JG, St Pierre BA. Cytokines in exertion-induced skeletal muscle injury. Mol Cell Biochem. 1998;179(1-2):159-67.
- 9. Kääriäinen M, Kääriäinen J, Järvinen TL, Sievänen H, Kalimo H, Järvinen M. Correlation between biomechanical and structural changes during the regeneration of skeletal muscle after laceration injury. J Orthop Res. 1998;16(2):197-206.
- 10. Järvinen M. Healing of a crush injury in rat striated muscle. 3. A micro-angiographical study of the effect of early mobilization and immobilization on capillary ingrowth. Acta Pathol Microbiol Scand A. 1976;84(1):85-94.
- 11. Fernandes TL, Pedrinelli A, Hernandez AJ. Dor na coxa e na perna. In: Nobrega A, editor. Manual de medicina do esporte. São Paulo:Atheneu; 2009. p. 140-1.
- 12. Järvinen M. Healing of a crush injury in rat striated muscle. 2. A histological study of the effect of early mobilization and immobilization on the repair processes. Acta Pathol Microbiol Scand A. 1975;83(3):269-82.
- 13. Lehto M, Duance VC, Restall D. Collagen and fibronectin in a healing skeletal muscle injury. An immunohistological study of the effects of physical activity on the repair of injured gastrocnemius muscle in the rat. J Bone Joint Surg Br. 1985;67(5):820-8.
- 14. Hurme T, Rantanen J, Kaliomo H. Effects of early cryotherapy in experimental skeletal muscle injury Scand J Med Sci Sports. 1993;3(1):46-51.
- 15. Thorsson O, Hemdal B, Lilja B, Westlin N. The effect of external pressure on intramuscular blood flow at rest and after running. Med Sci Sports Exerc. 1987;19(5):469-73.
- 16. O'Grady M, Hackney AC, Schneider K, Bossen E, Steinberg K, Douglas JM, et al Diclofenac sodium (Voltaren) reduced exercise-induced injury in human skeletal muscle. Med Sci Sports Exerc. 2000;32(7):1191-6.
- 17. Thorsson O, Rantanen J, Hurme T, Kalimo H. Effects of nonsteroidal antiinflammatory medication on satellite cell proliferation during muscle regeneration. Am J Sports Med. 26(2):172-6.
- 18. Mishra DK, Fridén J, Schmitz MC, Lieber RL. Anti-inflammatory medication after muscle injury. A treatment resulting in short-term improvement but subsequent loss of muscle function. J Bone Joint Surg Am. 1995;77(10):1510-9.
- 19. Beiner JM, Jokl P, Cholewicki J, Panjabi MM. The effect of anabolic steroids and corticosteroids on healing of muscle contusion injury. Am J Sports Med. 27(1):2-9.
- 20. Magnusson SP, Simonsen EB, Aagaard P, Gleim GW, McHugh MP, Kjaer M. Viscoelastic response to repeated static stretching in the human hamstring muscle. Scand J Med Sci Sports. 1995;5(6):342-7.
- 21. Wilkin LD, Merrick MA, Kirby TE, Devor ST. Influence of therapeutic ultrasound on skeletal muscle regeneration following blunt contusion. Int J Sports Med. 2004;25(1):73-7.
- 22. Almekinders LC. Results of surgical repair versus splinting of experimentally transected muscle. J Orthop Trauma. 1991;5(2):173-6.
- 23. Kujala UM, Orava S, Järvinen M. Hamstring injuries. Current trends in treatment and prevention. [Internet]. Sports Med (Auckland, N.Z.). 1997;23(6):397-404.
- 24. Best TM, Shehadeh SE, Leverson G, Michel JT, Corr DT, Aeschlimann D. Analysis of changes in mRNA levels of myoblast- and fibroblast-derived gene products in healing skeletal muscle using quantitative reverse transcription-polymerase chain reaction. J Orthop Res. 2001;19(4):565-72.
- 25. LaBarge MA, Blau HM. Biological progression from adult bone marrow to mononucleate muscle stem cell to multinucleate muscle fiber in response to injury. Cell. 2002;111(4):589-601.
- 26. Siwek CW, Rao JP. Ruptures of the extensor mechanism of the knee joint. J Bone Joint Surg Am. 1981;63(6):932-7.
- 27. Liow RY, Tavares S. Bilateral rupture of the quadriceps tendon associated with anabolic steroids. Br J Sports Med. 1995;29(2):77-9.
- 28. Stephens BO, Anderson GV. Simultaneous bilateral quadriceps tendon rupture: a case report and subject review. J Emerg Med. 5(6):481-5.
- 29. Walker LG, Glick H. Bilateral spontaneous quadriceps tendon ruptures. A case report and review of the literature. Orthop Rev. 1989;18(8):867-71.
- 30. Blasier RB, Morawa LG. Complete rupture of the hamstring origin from a water skiing injury. Am J Sports Med. 18(4):435-7.
- 31. Cunningham PM, Brennan D, O'Connell M, MacMahon P, O'Neill P, Eustace S. Patterns of bone and soft-tissue injury at the symphysis pubis in soccer players: observations at MRI. AJR Am J Roentgenol. 2007;188(3):W291-6.
- 32. Verrall GM, Slavotinek JP, Barnes PG, Esterman A, Oakeshott RD, Spriggins AJ. Hip joint range of motion restriction precedes athletic chronic groin injury. J Sci Med Sport. 2007;10(6):463-6.
- 33. Schilders E, Bismil Q, Robinson P, O'Connor PJ, Gibbon WW, Talbot JC. Adductor-related groin pain in competitive athletes. Role of adductor enthesis, magnetic resonance imaging, and entheseal pubic cleft injections. J Bone Joint Surg Am. 2007;89(10):2173-8.
- 34. Vogt S, Ansah P, Imhoff AB. Complete osseous avulsion of the adductor longus muscle: acute repair with three fiberwire suture anchors. Arch Orthop Trauma Surg. 2007;127(8):613-5.
- 35. Segal RL, Song AW. Nonuniform activity of human calf muscles during an exercise task. Arch Phys Med Rehabil. 2005;86(10):2013-7.
- 36. Bianchi S, Martinoli C, Abdelwahab IF, Derchi LE, Damiani S. Sonographic evaluation of tears of the gastrocnemius medial head ("tennis leg"). J Ultrasound Med. 1998;17(3):157-62.
- 37. McClure JG. Gastrocnemius musculotendinous rupture: a condition confused with thrombophlebitis. South Med J. 1984;77(9):1143-5.
Correspondência:
Datas de Publicação
-
Publicação nesta coleção
08 Set 2011 -
Data do Fascículo
2011
Histórico
-
Recebido
20 Nov 2010 -
Aceito
23 Dez 2010