Resumos
O artigo reporta a obtenção do extrato fluido de Symphytum officinale L., e posterior secagem por nebulização, e a caracterização físico-química por técnicas termogravimétricas, espectroscópicas e cromatográficas. O adjuvante de secagem utilizado foi hidroxietilcelulose na concentração de 1,5%. Foi observado que o processo de secagem por nebulização, nas condições operacionais estabelecidas, não influenciou as características dos constituintes do extrato seco em relação ao extrato fluido pelas técnicas utilizadas.
Symphytum officinale; parâmetros de secagem; hidroxietilcelulose; TGA; IV; CLAE
This work reports the obtaining of the Symphytum officinale L. fluid extract dried by spray-drying and its physicochemical characterization by thermogravimetric analysis, spectroscopic and chromatographic techniques. Hydroxyethylcellulose at 1,5% was used as technological adjuvant. We observed that the drying process by spray-dryer, on the established operational conditions, did not have influence in the characteristics of the dry extract constituents in relation to the fluid extract by the used techniques.
Symphytum officinale; spray drying; hydroxyethylcellulose; TGA; IR; HPLC
ARTIGO
Caracterização físico-química do extrato fluido e seco por nebulização de Symphytum officinale L.
Phisycal chemistry characterization of fluid and dry nebulization extract of Symphytum officinale L.
José Otávio Carréra Silva JúniorI,* * E-mail: carrera@ufpa.br, Tel. + 55-91-32017667 ; José Luiz Fernandes VieiraII; Wagner Luiz Ramos BarbosaIII; Newton Lindolfo PereiraIV
ILaboratório de Farmacotécnica, Departamento de Farmácia, Universidade Federal do Pará, Campus Universitário do Guamá, 66075-110, Guamá, Belém, PA, Brasil
IILaboratório de Toxicologia, Departamento de Deontologia e Medicina Legal, Universidade Federal do Pará, Campus Universitário do Guamá, 66075-110, Guamá, Belém, PA, Brasil
IIILaboratório de Fitoquímica, Departamento de Farmácia, Universidade Federal do Pará, Campus Universitário do Guamá, 66075-110, Guamá, Belém, PA, Brasil
IVLaboratório de Farmacotécnica, Departamento de Ciências Farmacêuticas, Faculdade de Ciências Farmacêuticas de Ribeirão Preto, Av. do Café s/n, Monte Alegre,14040-903, Ribeirão Preto, SP, Brasil
RESUMO
O artigo reporta a obtenção do extrato fluido de Symphytum officinale L., e posterior secagem por nebulização, e a caracterização físico-química por técnicas termogravimétricas, espectroscópicas e cromatográficas. O adjuvante de secagem utilizado foi hidroxietilcelulose na concentração de 1,5%. Foi observado que o processo de secagem por nebulização, nas condições operacionais estabelecidas, não influenciou as características dos constituintes do extrato seco em relação ao extrato fluido pelas técnicas utilizadas.
Unitermos:Symphytum officinale, parâmetros de secagem, hidroxietilcelulose, TGA, IV, CLAE.
ABSTRACT
This work reports the obtaining of the Symphytum officinale L. fluid extract dried by spray-drying and its physicochemical characterization by thermogravimetric analysis, spectroscopic and chromatographic techniques. Hydroxyethylcellulose at 1,5% was used as technological adjuvant. We observed that the drying process by spray-dryer, on the established operational conditions, did not have influence in the characteristics of the dry extract constituents in relation to the fluid extract by the used techniques.
Keywords: Symphytum officinale, spray drying, hydroxyethylcellulose, TGA; IR; HPLC.
INTRODUÇÃO
O uso de plantas medicinais no Brasil vem se consolidando nos últimos tempos em especial com a promulgação da Política Nacional de Plantas Medicinais e Fitoterápicos (Brasil, 2004). Dados da Organização Mundial de Saúde (OMS) mostram que mais da metade dos habitantes da terra especialmente nos países pobres e em desenvolvimento fazem uso de ervas medicinais na busca de alívio de sintomatologia dolorosa ou desagradável, e que desse total pelo menos 30% as utilizam por indicação médica (Estrela, 1995). No mercado brasileiro de medicamentos e cosméticos, 25% dos produtos fabricados contêm princípios ativos naturais.
Symphytum officinale L. (confrei) é uma Boraginaceae de clima temperado que foi introduzido no Brasil e se adaptou facilmente às regiões de clima tropical. Ocorre entre os estados do Paraná e Amazonas, principalmente em São Paulo (Alzugaray; Alzugaray, 1988), onde, entretanto, é encontrada apenas na forma cultivada (Matos, 1994). O estudo morfoanatômico das folhas e raíz desta espécie foi descrito por Toledo et al. (2003; 2006). No extrato etanólico das folhas foram detectadas as seguintes classes de metabólitos secundários: alcalóides, flavonosídeos, esteróides e triterpenóides. Já o extrato aquoso contém: saponosídeos e taninos condensados, principalmente. Compostos fenólicos foram encontrados no rizoma além de amido e lignina (Toledo et al., 2006).
Diversas propriedades terapêuticas, tais como atividade hemostática e antiinflamatória, são atribuídas à planta toda, mas principalmente às raízes e rizomas devido à presença de taninos e mucilagens; já a alta atividade cicatrizante, é atribuída à substância alantoína, que atua como regeneradora, estimulando o crescimento de tecidos novos e sadios (Duarte, 1984; Falcão et al., 2005). Nesse sentido recomenda-se a incorporação do extrato fluido de Symphytum em cremes evanescentes a fim de potencializar a ação umectante e emoliente de tais preparações (Soares et al., 1986). Outras propriedades terapêuticas, descritas para esta espécie são: anticoagulante (Chiryatey; Rusakova, 1994), bactericida, antifúngica e antihipertensiva (Sener; Atta-Ur, 1994). Morrison e West (1982) avaliaram o potencial hipoglicemiante de dezenas de espécies de plantas. O extrato aquoso das folhas de Symphytum officinale estava entre os menos ativos (Barbosa-Filho et al., 2005).
Extratos vegetais secos por aspersão têm sido utilizados como produtos finais e intermediários na obtenção de diferentes formas farmacêuticas (Vasconcelos et al., 2005). Apesar da forma fluida dos extratos ser a mais comumente comercializada, somente após a retirada de parte do liquido extrator é que as formulações sólidas, semi-sólidas ou líquidas podem ser preparadas. Porém, se a eliminação do solvente não for realizada corretamente pode-se provocar a perda de constituintes químicos do extrato.
A padronização de matérias primas, no caso do Symphytum officinale proposta originalmente por Saito e Oliveira (1986), representa um grande desafio, especialmente para reprodução de efeitos biológicos já que apresentam complexos requisitos para a avaliação da composição, constância, estabilidade, contagem microbiológica, etc.
Por fim, a espécie selecionada para a realização do presente trabalho figura como uma das mais utilizadas na forma tópica para o tratamento de afecções da pele de pacientes que buscam a atenção básica à saúde no Distrito Federal Brasil. A garantia da segurança de uso e da qualidade das preparações poderá contribuir para a inserção da espécie na Relação Nacional de Medicamentos Fitoterápicos (Barbosa, 2006).
MATERIAL E MÉTODOS
Material Vegetal
O Symphytum officinale L., foi adquirido diretamente da empresa YOD Comércio de Produtos Naturais LTDA, na condição de planta seca e pulverizada, com certificado garantia.
Preparação do extrato fluido
A extração do material foi realizada de acordo com o método preconizado pela Farmacopéia Brasileira II edição (1959), em processo geral A para a obtenção de extrato fluido.
Análise preliminar das características de secagem do extrato fluido
As características de secagem do extrato fluido de Symphytum officinale puro e adicionado com diferentes concentrações do adjuvante de secagem escolhido (hidroxietilcelulose - HEC), foram avaliadas pelo espalhamento de 5g de cada amostra em uma placa de vidro. Em seguida a placa foi submetida à secagem em estufa de ar circulante por 1 hora a 95 °C.
A Adição de HEC no extrato se deu nas concentrações de 0,5, 0,75 e 1,5% (p/v) sob constante agitação em agitador magnético a 400 rpm. A formulação contendo 1,5% de HEC foi preparada pela adição do adjuvante após a diluição do extrato com água destilada na proporção de 1:1.
Secagem da formulação selecionada pelo método de spray drying
Para a etapa de secagem do extrato seco de S. officinale foi empregado um spray dryier. A atomização do material dentro da câmara foi realizada pelo emprego de uma bomba peristáltica e de um bico atomizador tipo duplo fluido com diâmetro de saída de 2 mm. As condições operacionais empregadas nesse trabalho estão descritas na Tabela 1.
A vazão do ar de secagem empregada durante o processamento foi calculada através da utilização de um tubo de Pitot acoplado a um manômetro de água, através da equação:
Obtenção dos perfis termogravimétrico, espectroscópico e cromatográfico
Perfil termogravimétrico
O extrato fluido seco por nebulização de S. officinale foram analisado e as curvas termogravimétricas foram obtidas em um analisador térmico Shymadzu nas seguintes condições: Razão de aquecimento - 5°C/min.; Peso da amostra - aproximadamente 8 mg; Atmosfera nitrogênio; Fluxo 25,00 mL/min; Material da célula platina.
Perfil espectroscópico
Os extratos fluido liofilizado e seco por nebulização de S. officinale foram analisados e os espectros foram obtidos com o uso de um aparelho de infravermelho com transformador de Fourrier (FTIR) da marca Nicolet, modelo Proteje 460. As leituras foram realizadas em comprimento de onda na faixa de 400 a 4000 cm-1. Quantidades apropriadas da droga vegetal foram comprimidas com KBr.
Perfil cromatográfico
Os perfis cromatográficos dos extratos fluido liofilizado e seco por nebulização foram obtidos em cromatógrafo da Marca Varian Pro-star, detetor UV-visível, com operação em 218 nm, injeção manual em um loop de 20 mL, sobre uma coluna analítica Merck ® ODS (4,6 mm x 250 mm). O processo de desenvolvimento foi realizado utilizando como fase móvel tampão fosfato de sódio 10 mM, pH 4,0, com um fluxo de 0,5 mL/m-1.
RESULTADOS E DISCUSSÃO
A análise do teor de etanol no extrato fluido de S. officinale por picnometria mostrou um teor médio de 26,83 % (v/v) ± 1,04.
A Figura 1 mostra os produtos da secagem do extrato fluido, com e sem a adição do adjuvante de secagem escolhido, a hidroxietilcelulose. O rendimento médio da operação de secagem por spray drying foi de 20%.
A determinação de etanol nas amostras destiladas do extrato fluido de S. officinale, além da importância para a caracterização da preparação, visa também garantir condições seguras durante a operação de secagem do material.
Na Figura 1A observa-se o aspecto de "melaço" apresentado pelo extrato seco sem o acréscimo de adjuvantes de secagem. A elevada viscosidade do material se deve provavelmente à presença de uma quantidade considerável de açúcares de baixo peso molecular na preparação o que constitui característica comum nesse tipo de preparação. As Figuras 1B, 1C e 1D mostram o extrato fluido de S. officinale seco com a adição de hidroxietilcelulose em concentrações de 0,5, 1,0 e 1,5%, respectivamente. Nota-se claramente que, com o aumento da concentração do adjuvante de secagem há uma diminuição da viscosidade do material sem que, no entanto, se observe o desprendimento do material da superfície do vidro. Esse é, provavelmente, efeito do polímero sobre a temperatura de transição vítrea da mistura dos constituintes químicos do extrato (em especial açúcares). A formulação contendo 1,5 % de HEC (Figura 1D), apresenta aspecto visual mais fosco e uma reduzida viscosidade em relação às outras formulações, e por isso foi escolhida para a secagem em spray drying, possibilitando uma melhor recuperação do produto durante seu processamento.
Dessa forma, e direcionado pelas características desejadas para o produto final, optou-se por não adicionar quantidades superiores do referido adjuvante ou mesmo qualquer quantidade de outro adjuvante de secagem à preparação.
A otimização dos parâmetros de secagem como temperaturas de entrada e saída, velocidade de fluxo de alimentação, concentração e tipo de adjuvante tecnológico, assim como os teores de resíduo seco do extrato fluido a nebulizar são fatores indispensáveis para obtenção de extratos secos com melhores características físico-químicas e aumento do rendimento da operação (Gaudy et al., 1991; Paula et al., 1998, Vasconcelos et al., 2005).
Os cálculos referentes ao teor de etanol na preparação vegetal foram empregados juntamente com o valor encontrado para a vazão de ar no spray drier (Tabela 1), no intuito de determinar uma vazão de extrato segura para a secagem do extrato fluido hidroetanólico de S. officinale. Segundo List & Schmidt (1989), a faixa de inflamabilidade do etanol no ar sob pressão atmosférica é de 3,0 a 15 %. Se a concentração do referido solvente estiver dentro dessa faixa durante a secagem do material, a operação é revestida de um alto risco de explosão. Com base nessa assertiva programou-se uma vazão de 4,0 mL de extrato por minuto (Tabela 1), o que garantiu a manutenção de uma concentração de etanol dentro da câmara de secagem sempre muito abaixo do limite inferior de inflamabilidade do solvente (Kirk, 1994).
De acordo com a curva termogravimétrica do extrato fluido liofilizado observa-se até 145 °C uma perda de massa de 1,400%, no intervalo de 150 °C a 350 °C ocorre uma perda acumulada de 41,695%, que atinge 54,540% até 600 °C (Figura 2).
O resultado obtido no ensaio gravimétrico de perda por dessecação para o extrato fluido de S. officinale no valor de 8,83% está entre os valores observados pelas curvas TGA no intervalo de temperatura de interesse, mostrando que a termogravimetria pode fornecer uma estimativa do conteúdo de água residual presente no material após seu preparo.
A decomposição térmica do extrato seco se inicia por volta de 120 °C com um percentual de perda de massa de 58% ao final a uma temperatura de 600 °C. Observou-se também uma série de eventos na região de 120 °C a 320 °C que podem ser atribuídos a decomposição de matéria orgânica (Figura 3).
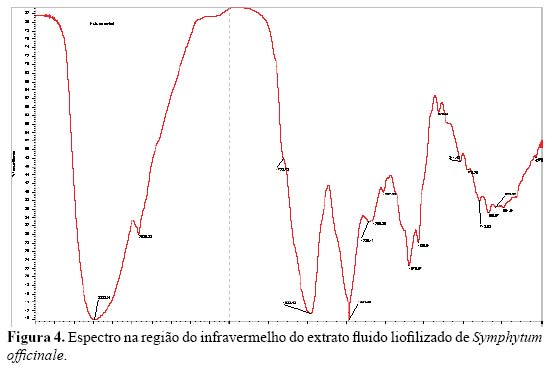
Os espectros dos extratos fluido e seco (Figuras 4 e 5) apresentaram fortes absorções na região de 3500-3200 cm-1 sugerindo a presença de hidroxilas. Absorções na região de 1700-1600 cm-1 sugerem também a presença de carbonilas. A faixa compreendida de 1100 1331 cm-1 (éteres), sugerem a presença de uma ampla classe de metabólitos secundários (flavonóides, cumarinas, antraquinonas, alcalóides quinolínicos e quinolônicos e outros fenil propanóides).
Conforme cromatograma apresentado na Figura 6, podemos observar que os extratos fluido e seco apresentaram um perfil químico semelhantes sugerindo que provavelmente o procedimento de secagem não tenha interferido na integridade de seus constituintes, entre eles a alantoina.
Nos extratos fluido e seco de S. officinale analisados por cromatografia líquida de alta eficiência detectou-se a alantoína, com tempo de retenção de 4,518 min. (Figura 6). Nas condições analíticas empregadas, a substância pura apresentou um tempo de retenção em torno de 4,32 min. Conforme demonstrou o valor da regressão da curva obtida para alantoína, existe linearidade no intervalo de concentração analisado, permitindo assim, o doseamento desta substância por CLAE.
CONCLUSÃO
O procedimento de secagem do extrato fluido de Symphytum officinale por nebulização mostrou que a utilização de hidroxietilcelulose como adjuvante de secagem, na concentração de 1,5%, propicia uma melhor recuperação do produto seco durante seu processamento. Os perfis térmicos, espectrais por ultravioleta e cromatográfico por cromatografia líquida de alta eficiência apresentaram-se semelhantes para o extrato fluido liofilizado e para o seco por nebulização sugerindo que o procedimento de secagem não tenha interferido na integridade de seus constituintes, entre eles a alantoina.
AGRADECIMENTOS
Ao Centro Universitário do Pará CESUPA, pelo auxílio na forma de bolsa concedida.
Recebido em 21/04/06
Aceito em 06/10/06
- Alzugaray D, Alzugaray K 1988. Enciclopédia de Plantas Brasileiras, São Paulo: Editora três.
- Barbosa WLR 2006. Comunicação pessoal.
- Barbosa-Filho JM, Vasconcelos THC, Alencar AA, Batista LM, Oliveira RAG, Guedes DN, Falcão HS, Moura MD, Diniz MFFM, Modesto-Filho J 2005. Plants and their active constituents from South, Central, and North America with hypoglycemic activity. Rev Bras Farmacogn 15: 392-413.
- Brasil 2004. Ministério da Saúde, Agencia Nacional de Vigilância Sanitária. Resolução Diretora Colegiada n° 48 de 16 de março de 2004. Aprova o regulamento técnico sobre registro de medicamentos fitoterápicos. Diário Oficial da Republica Federativa do Brasil, Brasília/DF.
- ChiryatEv EA, Rusakova OA 1994. Species of the Siberian flora as sources of direct action antcoagulants. Rastitel´nye Resursy 30: 21-28.
- Duarte FR 1984. Influência de dois tipos de solos sobre o teor total de alcalóides do confrei. Dissertação de Mestrado, UNESP, Piracicaba.
- Estrela E 1995. Tratado de Cooperaçion Amazonica Secretaria Protempore, Plantas medicinales Amazônicas: Realidad y Perspectivas, Lima: TCA.
- Falcão HS, Lima IO, Santos VL, Dantas HF, Diniz MFFM, Barbosa-Filho JM, Batista LM 2005. Review of the plants with anti-inflammatory activity studied in Brazil. Rev Bras Farmacogn 15: 381-391.
- Farmacopéia Brasileira 1959. 2.ed. São Paulo: Indústria Gráfica Siqueira.
- Gaudy D, Puech A, Jacob M 1991. Rôle de ladjuvant dans loptimization de la production dun extrait sec vegetal nébulisé: "cas de lextrait de Noix vomique". Acta Pharm Helv 66: 5-10.
- Kirk O 1994. Encyclopedia of Chemical Technology Vol. 9, pp.812, 4 edição: John Wiley and Sons.
- List PH, Schmidt, PC 1989. Phytopharmaceutical Technology. CRC Press, Florida.
- Matos FJA 1994. Farmácias vivas: sistema de utilização de plantas medicinais projetado para pequenas comunidades, 2. Ed., Fortaleza: UFC.
- Morrison EY, West ME 1982. A preliminary study of the effects of some West Indian medicinal plants on blood sugar levels in the dog. West Indian Med J 31: 194-197.
- Paula IC, Ortega GG, Bassani VL, Petrovick PR 1998. Development of ointment formulations prepared with Achyrocline satureoides spray-dried extracts. Drug Dev Ind Pharm 24: 235-241.
- Saito ML, Oliveira F 1986. Confrei - virtudes e problemas. Rev Bras Farmacogn 1: 74-85.
- Sener B, Atta-Ur R 1994. Recent results in the search of bioactive compounds from turkish medicinal plants. Pure Appl Chem 66: 2295-2288.
- Soares IC, Nicoletti MA, Conciglieri VO 1986. Incorporação de extrato fluído de Symphytum officinale L. em cremes evanescentes. Rev Bras farmacogn 1(Supl.): 42.
- Toledo ACO, Duarte MR, Nakashima T 2003. Análise farmacognóstica da droga e do extrato flúido das folhas de Symphytum officinale L. (Boraginaceae). Rev Bras Farmacogn 13(Supl. 2): 1-2.
- Toledo ACO, Duarte MR, Nakashima T 2006. Caracterização morfoanatômica de raízes e rizomas de Symphytum officinale L. (Boraginacea). Rev Bras Farmacogn 16: 185-191.
- Vasconcelos EAF, Medeiros MGF, Raffin FN, Moura TFAL 2005. Influência da temperatura de secagem e da concentração de Aerosil® 200 nas características dos extratos secos por aspersão da Schinus terebinthifolius Raddi (Anacardiaceae), Rev Bras Farmacogn 15: 243-249.
Datas de Publicação
-
Publicação nesta coleção
24 Mar 2008 -
Data do Fascículo
Dez 2006
Histórico
-
Recebido
21 Abr 2006 -
Aceito
06 Out 2006