Resumos
OBJETIVO: Analisar a alteração da função pulmonar e dor em pacientes submetidos à cirurgia de revascularização do miocárdio (RM) com enxerto da artéria torácica interna esquerda (ATIE), sem circulação extracorpórea (CEC), comparando a inserção do dreno pleural nas regiões intercostal e subxifóide. MÉTODO: Vinte e oito pacientes (média de idade 57,4 ± 8,4 anos) foram alocados em dois grupos, de acordo com a posição do dreno pleural. Grupo IL (n=15) com inserção do dreno no sexto espaço intercostal esquerdo na linha axilar média; e grupo IM (n =13) inserção do dreno na região subxifóide. Todos os pacientes foram submetidos à avaliação da função pulmonar. Registros espirométricos da capacidade vital forçada (CVF) e do volume expiratório forçado no primeiro segundo (VEF1) foram obtidos no pré, primeiro, terceiro e quinto dia dias pós-operatório (PO) e a gasometria arterial em ar ambiente no pré e primeiro dia de pós-operatório. A sensação de dor foi quantificada por um escore padrão (0 a 10) no primeiro dia de pós-operatório. RESULTADOS: Em ambos os grupos houve queda significativa da CVF e do VEF1 até o quinto pós-operatório (p<0,001). Quando comparados, a diferença entre os grupos se manteve significativa, com maior queda dos valores de CVF e VEF1 no grupo IL (p<0,05). A pressão parcial de oxigênio arterial apresentou queda significativa no primeiro dia de pós-operatório em ambos os grupos, porém com maior decréscimo no grupo IL (p=0,021). A dor referida foi maior no grupo IL (p=0,002). CONCLUSÃO: A cirurgia de RM sem CEC, utilizando a ATIE com pleurotomia esquerda, independente da posição do dreno pleural causa dor e queda significativa na função pulmonar no PO. Porém, a inserção do dreno pleural na região subxifóide demonstrou menor dor subjetiva com melhor preservação da função pulmonar quando comparada à inserção intercostal.
Revascularização miocárdica; Drenagem pleural; Função pulmonar
OBJECTIVE: To analyze the pulmonary function changes and pain in patients undergoing off-pump coronary artery bypass grafting utilizing a left internal thoracic artery graft, comparing the pleural drain insertion through the intercostal space and subxyphoid approach. METHODS: Twenty eight patients (mean age 57.4 ± 8.4 years) were divided into two groups, according to the pleural drain site. Group IL (n=15) had the pleural drain inserted through the sixth left intercostal space at the mid-axillary line and in the IM group (n=13) the drain was placed through the subxyphoid region. All the patients underwent pre- and post-operative evaluation of pulmonary function tests as well as arterial blood gas analysis. Forced vital capacity (FVC) and forced expiratory volume in 1 second (FEV1) were recorded in the preoperative period, and in the first, third and fifth postoperative days. The pain sensation was evaluated using a standard score from 0 to 10. RESULTS: In both groups falls in FVC and FEV1 were noted, up to the fifth postoperative day (P<0.001). However, the decrease was higher in the IL group, when compared to the IM group (p<0.05). Also arterial blood gas analysis showed a decline of the partial oxygen pressure in both groups on the fist postoperative day, but more significantly in the IL group (p=0.021). The pain sensation was higher in the IL group (p=0.002). CONCLUSION: Off-pump coronary artery bypass grafting with using of left internal thoracic artery, disregarding the pleural drain site, leads to a significant decrease of postoperative pulmonary function. However, the subxyphoid technique of drain insertion has shown a better preservation of the lung function when compared to the intercostal drain site.
Coronary artery bypass surgery; Pleural drain; Pulmonary function
ARTIGO ORIGINAL
Efeitos do local de inserção do dreno pleural na função pulmonar no pós-operatório de cirurgia de revascularização do miocárdio
Solange Guizilini; Walter J. Gomes; Sonia M. Faresin; Antonio Carlos C. Carvalho; Jaime I. Jaramillo; Francisco A. Alves; Roberto Catani; Enio Buffolo
Endereço para correspondência Endereço para correspondência Rua Pedro Inácio de Araújo, 202 Ap. 13 A - Vila São Francisco 05386-330 - São Paulo Fone: (011) 37635387 Celular: (011) 81419978 E-mail: sguizilini@uol.com.br
RESUMO
OBJETIVO: Analisar a alteração da função pulmonar e dor em pacientes submetidos à cirurgia de revascularização do miocárdio (RM) com enxerto da artéria torácica interna esquerda (ATIE), sem circulação extracorpórea (CEC), comparando a inserção do dreno pleural nas regiões intercostal e subxifóide.
MÉTODO: Vinte e oito pacientes (média de idade 57,4 ± 8,4 anos) foram alocados em dois grupos, de acordo com a posição do dreno pleural. Grupo IL (n=15) com inserção do dreno no sexto espaço intercostal esquerdo na linha axilar média; e grupo IM (n =13) inserção do dreno na região subxifóide. Todos os pacientes foram submetidos à avaliação da função pulmonar. Registros espirométricos da capacidade vital forçada (CVF) e do volume expiratório forçado no primeiro segundo (VEF1) foram obtidos no pré, primeiro, terceiro e quinto dia dias pós-operatório (PO) e a gasometria arterial em ar ambiente no pré e primeiro dia de pós-operatório. A sensação de dor foi quantificada por um escore padrão (0 a 10) no primeiro dia de pós-operatório.
RESULTADOS: Em ambos os grupos houve queda significativa da CVF e do VEF1 até o quinto pós-operatório (p<0,001). Quando comparados, a diferença entre os grupos se manteve significativa, com maior queda dos valores de CVF e VEF1 no grupo IL (p<0,05). A pressão parcial de oxigênio arterial apresentou queda significativa no primeiro dia de pós-operatório em ambos os grupos, porém com maior decréscimo no grupo IL (p=0,021). A dor referida foi maior no grupo IL (p=0,002).
CONCLUSÃO: A cirurgia de RM sem CEC, utilizando a ATIE com pleurotomia esquerda, independente da posição do dreno pleural causa dor e queda significativa na função pulmonar no PO. Porém, a inserção do dreno pleural na região subxifóide demonstrou menor dor subjetiva com melhor preservação da função pulmonar quando comparada à inserção intercostal.
Descritores: Revascularização miocárdica. Drenagem pleural. Função pulmonar.
INTRODUÇÃO
A cirurgia de revascularização miocárdica (RM) utilizando enxertos de artéria torácica interna esquerda (ATIE) tem demonstrado proporcionar a remissão dos sintomas anginosos e contribuir para prolongar e melhorar a qualidade de vida de pacientes portadores de doença coronariana [1]. Entretanto, na maior parte dos procedimentos, a obtenção do pedículo da ATIE envolve a abertura da cavidade pleural esquerda, que necessita subseqüentemente ser drenada. Essa pleurotomia, associada à presença do dreno pleural, contribui para maior desconforto ao paciente, funcionando como um fator adicional de deterioração da mecânica respiratória [2,3].
A inserção do dreno pleural intercostal adiciona trauma ao tórax, torna necessário perfurar músculos intercostais e a pleura parietal, interferindo nos movimentos respiratórios [4,5]. Conseqüentemente, a localização do dreno pleural poderia ter influência no desconforto do paciente e no grau de alteração da função pulmonar.
Neste trabalho foram estudados os efeitos do local de inserção do dreno pleural, na função pulmonar e na dor, comparando a inserção intercostal com a subxifóide no pós-operatório de pacientes submetidos à cirurgia de revascularização do miocárdio sem uso de circulação extracorpórea (CEC).
MÉTODO
Este estudo foi realizado nos Hospitais Pirajussara e São Paulo, ambos da Universidade Federal de São Paulo, tendo sido previamente aprovado pelo Comitê de Controle Ético de Pesquisas Clinicas da referida Universidade, e obtido termo de consentimento por escrito dos pacientes para realização do estudo.
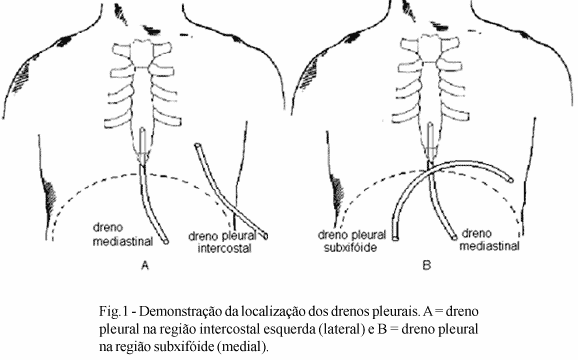
Foram incluídos 28 pacientes com idade média de 57,4 ± 8,4 anos, variando de 46 a 74 anos, sendo 5 (17,8%) do sexo feminino e 23 (82,14%) do sexo masculino. Todos apresentavam insuficiência coronariana comprovada por estudo cinecoronariográfico, fração de ejeção ventricular esquerda maior que 50% e ausência de doença pulmonar aguda ou crônica, sendo submetidos à cirurgia eletiva de RM sem CEC com uso de ATIE e pleurotomia esquerda. Os pacientes foram alocados em dois grupos de acordo com a posição do dreno pleural: 1) Grupo (IL) ou inserção lateral (n=15), cujo dreno encontrava-se na intersecção do sexto espaço intercostal esquerdo com a linha axilar média; 2) Grupo (IM) ou inserção medial (n=13), em que o dreno encontrava-se na região subxifóide (Figura 1).
As características clínicas e demográficas dos grupos IL e IM são apresentadas na Tabela 1.
Pré-operatório
Os dados da história e exame clínico foram registrados em uma ficha de avaliação detalhada contendo diagnósticos, fatores de risco para doença coronariana (hipertensão arterial sistêmica, diabetes mellitus, dislipidemia e hábito tabagístico) e doenças associadas. Também foram avaliados o estado nutricional e a função pulmonar por meio da espirometria e gasometria arterial.
O estado nutricional foi determinado pela análise do índice de massa corpórea (IMC), calculado pela relação peso/altura². Para pacientes até 60 anos foi utilizada a classificação preconizada pela Organização Mundial da Saúde [6]: IMC menor que 18,5 Kg/m2 refere-se aos distróficos ou desnutridos, entre 18,5 e 24,9 Kg/m2 aos eutróficos, entre 24,9 e 29,9 Kg/m2 aos sobrepesos e acima de 29,9 Kg/m2 aos obesos. Após os 60 anos foi utilizada a classificação de LIPSCHITZ [7], onde valor menor que 22 Kg/m2 classifica o paciente como desnutrido, entre 22 e 27 Kg/m2 eutrófico e maior que 27 Kg/m2 obeso. A avaliação espirométrica consistiu na determinação dos valores da capacidade vital forçada (CVF) e volume expiratório forçado no primeiro segundo (VEF1), de acordo com os padrões da American Thoracic Society (ATS) [8].
Os registros da CVF e VEF1 foram obtidos no pré e pós-operatórios (1º, 3° e 5° dias), sendo utilizado o espirômetro portátil Spirobank G da marca Medgraph Ltda. A Pressão parcial de oxigênio no sangue arterial (PaO2) foi determinada no pré e primeiro dia de pós-operatório, em ar ambiente, sempre antes da realização da espirometria.
Todos pacientes foram submetidos à radiografia simples de tórax em incidência póstero-anterior e perfil. No final da avaliação pré-operatória, os pacientes receberam orientação sobre a cirurgia, o pós-operatório imediato e a importância dos exercícios respiratórios e deambulação precoce a serem realizados.
Intra-operatório
A cirurgia de RM foi realizada por meio de esternotomia mediana, sem CEC, com enxerto de ATIE e pleurotomia esquerda, complementada com pontes adicionais de veia safena. Antes do tórax ser fechado, a critério de escolha dos cirurgiões, um dreno pleural foi inserido e exteriorizado na intersecção do sexto espaço intercostal esquerdo com a linha axilar média; ou na região subxifóide. A extremidade do dreno subxifóide foi locada no seio costo frênico esquerdo.
Foram utilizados para ambos os grupos dreno pleural tubular de PVC, sendo o da região subxifóide curvo de ¼ de polegada e o intercostal reto. Em todos os pacientes também foi deixado um dreno subesternal tubular localizado no mediastino e exteriorizado por via subxifóide.
Pós-operatório
Os dois grupos foram reavaliados em relação à função pulmonar no primeiro, terceiro e quinto dias de pós-operatório.
No primeiro dia de PO a sensação subjetiva da dor foi quantificada por meio de um escore padrão modificado com escala de zero a dez, onde zero indicava ausência de dor e dez presença de dor insuportável [9]. Esta avaliação foi efetuada inicialmente em repouso antes da realização da espirometria.
Todos pacientes realizaram diariamente radiografia simples de tórax em incidência antero-posterior para verificar a presença de coleção pleural residual e foram submetidos a um programa de fisioterapia diário até a alta hospitalar. As avaliações acima descritas foram realizadas sempre pelo mesmo profissional tanto no pré quanto no pós-operatório.
Análise Estatística
Para verificar se as amostras eram homogêneas foram aplicados o teste exato de Fisher e o teste de Mann-Whitney. Os parâmetros de função pulmonar foram analisados por testes não-paramétricos: o teste de Friedman comparou as tendências ao longo do tempo, conjuntamente em cada grupo; o teste de Wilcoxon comparou valores intragrupo dois a dois e o teste de Mann-Whitney comparou os grupos entre si. Para todos os testes estatísticos, o nível de significância adotado foi de alfa < 0,05 ou 5%.
RESULTADOS
Os grupos não apresentaram diferenças estatísticamente significantes em relação à idade, sexo,índice de massa corpórea, fatores de risco para doença coronariana, função pulmonar pré-operatória, tempo de cirurgia e tempo de intubação orotraqueal (Tabela 1).
Em relação à função pulmonar, em ambos os grupos houve queda significante da CVF até o quinto dia de pós-operatório (p<0,001). Quando comparados os grupos entre si, a diferença se mantém significante, sempre com maior queda para o grupo IL.
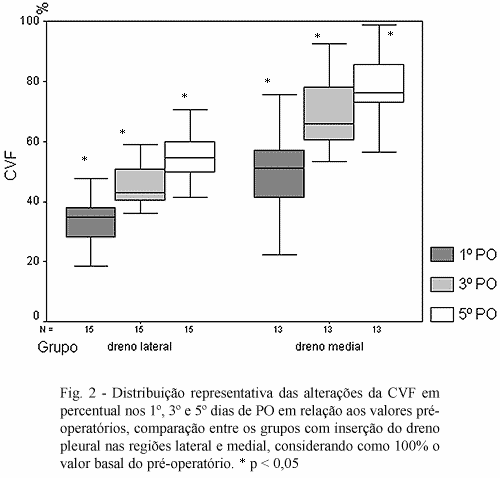
A porcentagem da CVF no 1º dia de PO em relação aos valores do pré-operatório nos grupos IL e IM foi respectivamente: 33,36 ± 8,34% e 50,09 ± 14,35%, mostrando diminuição de 66,64% da CVF no grupo lateral, perda que foi significantemente maior quando comparada a 49,1% no grupo medial (P=0,001).
No 3º dia de PO a porcentagem de queda da CVF no grupo IL e IM foi respectivamente: 45,42 ± 7,06% e 67,00 ± 15,88%, mostrando perda de 57,58% da CVF no grupo lateral, enquanto o medial apresentou menor decréscimo, de 33% (P<0,001).
A porcentagem da CVF no 5º dia de PO no grupo IL e IM foi respectivamente: 55,13 ± 8,30% e 78,22 ± 11,90%, mostrando que a diferença se mantém significante, com diminuição de 44,87% no grupo lateral e 21% no medial (P< 0,001) (Figura 2).
Em relação ao VEF1, em ambos os grupos também houve decréscimo significante até o quinto dia de pós-operatório (p<0,001). Quando comparados entre si, a diferença se mantém, sempre com maior perda para o grupo lateral.
A porcentagem da VEF1 no 1º dia de PO em relação aos valores do pré-operatório nos grupos IL e IM foi respectivamente: 35,70 ± 8,66% e 50,44 ± 13,18%, mostrando diminuição de 64,30% no grupo lateral, perda significantemente maior quando comparada a 49,56% do grupo medial (P=0,003).
No 3º dia de PO a porcentagem de queda no grupo IL e IM foi respectivamente: 48,04 ± 7,22% e 67,09 ± 15,12%, mostrando perda de 51,96% da VEF1 no grupo IL, enquanto o medial apresentou menor decréscimo, 32,91% (P<0,001).
A porcentagem da VEF1 no 5º dia de PO no grupo IL e IM foi respectivamente: 58,80 ± 8,51% e 79,56 ± 11,52%, mostrando que a diferença se mantém significante com perda de 41,2% no grupo lateral e 21% no medial (P<0,001) (Figura 3).
Com relação à PaO2, houve queda significante no primeiro dia de PO para ambos os grupos (p=0,001), mas o grupo IL manteve valores inferiores ao do grupo IM. O percentual da PaO2 no 1º dia de PO em relação ao pré-operatório nos grupos IL e IM foi respectivamente: 76,54 ± 9,11% e 84,90 ± 7,79%, mostrando diminuição de 23,46% no grupo lateral e 15,1% no grupo medial (P = 0,021) (Figura 4).
Em relação a dor, todos os pacientes apresentaram dor no PO, mas a intensidade da dor no grupo com dreno lateral foi maior, diferença que foi estatisticamente significante. As distribuições do escore de dor foram distintas, com média de 7,20 ± 1,52 para grupo IL e de 5,00 ± 1,58 para grupo IM (p=0,002) (Figura 5).
As radiografias seriadas pós-operatórias, em ambos os grupos, não demonstraram presença de coleções pleurais. Todos os drenos foram retirados no 2o dia de PO.
DISCUSSÃO
Confirmando achados anteriores, o presente estudo demonstrou que há deterioração da função pulmonar no PO de cirurgia de revascularização do miocárdio com uso de ATIE e pleurotomia esquerda [3]. A redução da função pulmonar é o resultado da combinação de diversos fatores, como a anestesia geral, esternotomia mediana, CEC [2]e disfunção diafragmática [10]. Além desses, há o fator adicional da drenagem pleural devido ao uso da ATIE com pleurotomia [3,11]. Estudos prévios mostraram que, independente da técnica cirúrgica utilizada, a CEC adiciona lesão pulmonar e atraso na recuperação da função respiratória [12]. Daí a importância deste trabalho original na literatura, estudando pacientes submetidos à cirurgia de RM sem CEC, comparando os efeitos da localização do dreno pleural, intercostal e subxifóide, na função pulmonar, onde os efeitos deletérios e variáveis relacionados com a CEC foram eliminados.
Em relação à função pulmonar, este estudo mostrou mesmo sem CEC, queda significante da função pulmonar até o 5º dia de PO em ambos os grupos, com deterioração dos valores de CVF e VEF1. Entretanto, o grupo com dreno medial apresentou menor queda desses parâmetros, quando comparado ao grupo com dreno lateral. Resultado semelhante foi encontrado por HAGL et al. [13], em estudo de pacientes submetidos à RM e uso de ATIE com CEC, onde os drenos foram inseridos na região intercostal ou na região subxifóide.
No presente estudo, apesar das diferenças se manterem significantes, quando comparados os valores do 5o dia de PO, o grupo IM apresentou média da CVF de 78,22% em relação ao pré-operatório, mas o limite superior da distribuição chegou aos 100%, enquanto o grupo lateral, mostrou limite superior de 70%. Podemos observar que a CVF não voltou totalmente ao normal no 5º dia de PO, mas os valores do grupo medial, quando comparados ao lateral, se aproximaram mais dos valores pré-operatórios.
Segundo OIKKONEN et al. [14], a diminuição da CVF pode determinar queda do pico de fluxo expiratório (PFE), que imediatamente após a cirurgia também se encontra diminuído. Essa queda tem importância clínica na medida em que reflete a capacidade de tossir, debilita a tosse e o transporte de secreções. O fechamento precoce e a obstrução das pequenas vias aéreas predispõem a microatelectasias e conseqüentemente a redução de pressão parcial de oxigênio no sangue arterial (PaO2) [15].
Neste estudo, apesar de não ter sido mensurado o PFE, a diminuição da CVF pode ter provocado sua queda, principalmente no grupo intercostal, onde o decréscimo da CVF foi maior, predispondo o paciente a maiores riscos de desenvolver complicações pulmonares.
As trocas gasosas mostraram-se alteradas neste estudo. YAMAGISHI et al. [16] monstraram que a hipoxemia arterial ocorre normalmente após cirurgia de RM e persiste até algumas semanas. Alguns autores têm mostrado maior queda da PaO2 com uso de ATIE secundário ao efeito da pleurotomia com drenagem pleural [17]. Comentam ainda que a recuperação é mais lenta devido à presença do dreno de tórax, ou seja, ao traumatismo adicional imposto a parede torácica [11,18].
No presente estudo, mesmo não tendo havido circulação extracorpórea, observamos queda significante da PaO2 no 1º dia de PO, em ambos os grupos, mas o grupo intercostal apresentou diminuição de 23,46%, ao passo que menor queda de 15,10% ocorreu no grupo medial. Portanto, a posição do dreno pleural parece ter sido fator importante de deterioração da oxigenação após a cirurgia.
No estudo de HAGL et al. [13] não houve diferença na PaO2 entre os grupos estudados, provavelmente devido à suplementação individual de oxigênio que foi realizada. Contudo, mostraram que a necessidade de oxigênio suplementar foi menor nos pacientes com localização subxifóide.
Vários mecanismos podem contribuir para o aparecimento da hipoxemia: hipoventilação alveolar, alteração da relação ventilação-perfusão, diminuição da difusão e shunt, sendo este último o mais freqüente [17,18]. Um dos mecanismos proposto para o aparecimento do shunt é a diminuição da CVF [17]. Segundo ALI et al. [19], a diminuição da CVF conduz à queda da PaO2 por dois mecanismos: primeiro pela formação de microatelectasias ou colapso alveolar periférico e segundo pelo fechamento precoce das pequenas vias aéreas. Com a CVF diminuída, o volume pulmonar torna-se muito próximo ao volume de fechamento durante a ventilação em repouso, levando alguns segmentos alveolares a ficarem permanentemente fechados [20]. Estes fatos podem justificar, no nosso estudo, a maior queda de oxigenação no grupo intercostal, devido à maior diminuição da CVF.
Em relação à dor e a posição do dreno pleural, este estudo mostrou que pacientes com localização do dreno subxifóide referiram menos dor que os pacientes com inserção intercostal. Resultados semelhantes foram descritos por RIEBMAN et al. [21], que descreveram a técnica de inserção do dreno pleural na região subxifóde, com objetivo de diminuir o desconforto no PO, causado pela fricção do dreno no espaço intercostal. HAGL et al. [13] também mostraram que a dor em pacientes com implantação subxifóide do dreno pleural foi menor, quando comparada a intercostal.
PICK et al. [22] mostraram que essa dor devida à drenagem intercostal é capaz de adicionar disfunção pulmonar no PO, o que podemos comprovar com este estudo. Essa maior queda da função pulmonar observada na inserção intercostal do dreno pleural ocorre porque adiciona maior trauma ao tórax, perfura a pleura parietal e músculos intercostais [3,5].
JAKOB et al. [4] mostraram que a alta sensibilidade da pleura e a fricção produzida durante o movimento respiratório provocam sofrimento ao paciente, por irritação constante dos nervos intercostais e do periósteo. Em contrapartida, o paciente defende-se com a imobilização do tórax e movimentos respiratórios superficiais, ficando restrita a respiração profunda até a retirada do dreno.
Como resultado final, com a inserção de um dreno entre os espaços intercostais intensifica-se a diminuição da capacidade residual funcional, CVF e VEF1 [23]. Estas alterações, associadas à diminuição da complacência pulmonar, aumentam o trabalho respiratório. Neste caso, para haver menor gasto de energia, o volume corrente diminui, levando os alvéolos ao progressivo colapso, resultando em shunt com conseqüente hipoxemia [20].
Estudos mostraram que quanto maior a diminuição da CVF e VEF1, maiores as possibilidades do paciente desenvolver complicações respiratórias. Neste estudo, apesar de não ter sido avaliado, o grupo intercostal por apresentar maior redução destes parâmetros espirométricos poderia estar sujeito a maior ocorrência de complicações no pós-operatório [23,24]. A redução dos volumes pulmonares pode conduzir ao acúmulo de secreção nas vias aéreas, com possibilidades maiores de obstrução ao fluxo aéreo, podendo predispor a ocorrência de atelectasias e pneumonias [19,24].
Em relação à drenagem pleural tem sido argumentado com freqüência que a localização intercostal é mais eficaz para o esvaziamento de coleções sangüíneas pós-operatórias. Neste estudo em discussão, os drenos pleurais dos pacientes, independente de sua posição, foram retirados no 2º dia após a cirurgia, e não houve necessidade de toracocentese adicional, havendo, portanto, drenagem eficaz. Esse resultado é justificado pelo correto posicionamento da extremidade do dreno curvo subxifóide no seio costo-frênico esquerdo [4,13,21], como demonstrado pelas radiografias torácicas pós-operatórias.
Pacientes deste estudo, com dreno localizado na região subxifóide foram mais tolerantes, aceitando melhor as medidas espirométricas, em relação aqueles com dreno intercostal. Resultado semelhante foi relatado por SOFIA & ALMEIDA [25], cujos pacientes portadores de dreno implantado na posição subxifóide apresentavam maior tolerância e disposição ao trabalho do fisioterapeuta.
Como citado anteriormente, devido à queda da função pulmonar no pós-operatório de cirurgia de revascularização do miocárdio, o paciente fica vulnerável a complicações pulmonares neste período de restabelecimento.
Estudos mostraram que a fisioterapia desde do pré até o pós-operatório é capaz de manter boas condições pulmonares, diminuindo as repercussões do prejuízo da função pulmonar. Essa também é nossa opinião, com base não apenas nos resultados deste estudo, mas também na experiência vivida com pacientes submetidos a revascularização do miocárdio, independente da presença ou da posição do dreno pleural. Este estudo mostrou também que merecem cuidado especial aqueles pacientes com localização intercostal do dreno pleural, onde as complicações podem ocorrer com maior frequência devido ao maior grau de comprometimento da função pulmonar.
Evitar a secção dos espaços intercostais na inserção do dreno pleural seria a melhor conduta. Com o acesso subxifóide, evitando os espaços intercostais, atenuar-se-ia a dor, evitar-se-ia o maior prejuízo na função pulmonar e o paciente teria melhor condição de cooperar com o importante papel do fisioterapeuta no pós-operatório.
CONCLUSÃO
Em conclusão, este estudo demonstrou que na cirurgia de RM, sem CEC, com enxerto de ATIE e pleurotomia esquerda, independente da posição do dreno pleural, há dor e prejuízo na função pulmonar. Entretanto, a inserção do dreno na região subxifóide demonstrou melhor preservação da função pulmonar e menor dor subjetiva, quando comparado à localização intercostal.
Artigo recebido em novembro de 2003
Artigo aprovado em fevereiro de 2004
Trabalho realizado nos Hospitais Pirajussara e São Paulo.
Disciplinas de Cirurgia Cardiovascular e Cardiologia, Escola Paulista de Medicina - Universidade Federal de São Paulo. Rua Botucatu 740 - 04023-900 São Paulo - SP
Este artigo é parte da tese de mestrado da Fisioterapeuta Solange Guizilini (Orientador: Prof. Dr. Walter J. Gomes).
- 1. Cameron A, Davis KB, Green G, Schaff HV. Coronary bypass surgery with internal thoracic artery grafts. Effects on survival over a 15-year period. N Engl J Med 1996;334:216-9.
- 2. Berrizbeitia LD, Tessler S, Jacobowitz IJ, Kaplan P, Budzilowicz L, Cunningham JN. Effect of sternotomy and coronary bypass surgery on postoperative pulmonary mechanics. Chest 1989;96:873-76.
- 3. Peng MJ, Vargas FS, Cukier A, Filho MT, Teixeira LR, Light RW. Postoperative pleural changes after coronary revascularization. Chest 1992;101:327-30.
- 4. Jakob H, Kamler M, Hagl S. Doubly angled pleural drain circumventing the transcostal route relieves pain after cardiac surgery. Thorac Cardiovasc Surg 1997;45:263-4.
- 5. Lancey RA, Gaca C, Salm TJV. The use of smaller, more flexible chest drains following open heart surgery. Chest 2001;119:19-24.
-
6WHO Physical Status: the use and interpretation of anthropometry. Report of a WHO Expert Committee. Geneve, World Health Organization, 1995;854:368-9.
- 7. Lipschitz DA. Screening for nutritional status in the elderly. Nutritional in old age. Am J Clin Nutr 1994;21:55-67.
- 8. American Thoracic Society. Standardization of spirometry. 1994 Update. Am J Respir Crit Care Med 1995; 1107-36.
- 9. Symreng T, Gomes MN, Rossi N. Intrapleural bupivacaine versus saline after thoracotomy on pain and lung function: a double-blind study. J Cardiothorac Anesth 1989;3:144-9.
- 10. Dureuil B, Cantineau JP, Desmonts. Effects of upper or lower abdominal surgery on diaphragmatic function. Br J Anesth 1987;59:1230-5.
- 11. Vargas FS, Cukier A, Filho MT, Hueb W, Teixeira LR, Light RW. Relationship between pleural changes after myocardial revascularization and pulmonary mechanics. Chest 1992;102:1333-6.
- 12. Calvin SH, Wan S Yim APC, Arifi AA. Pulmonary dysfunction after cardiac surgery. Chest 2002;121:1269-77.
- 13. Hagl C, Harringer W, Gohrbandt, Haverich A. Site of pleural drain insertion and early postoperative pulmonary function following coronary internal mammary artery. Chest 1999;115:757-61.
- 14. Oiokkonen M, Karjalainen K, Karara V, Kuosa R, Schavikin L. Comparison of incentive spirometry and intermittent positive pressure breathing after coronary artery bypass graft. Chest 1991;99:60-5.
- 15. Quadrelli SA, Montiel G, Roncoroni AJ, Raimondi A. Complicaciones respiratorias en el postoperatorio inmediato de la cirugia coronaria. Medicina (Buenos Aires) 1997;57:742-54.
- 16. Yamagishi T, Ishikawa S, Ohtaki A, Takahashi T, KoyanoT, Ohki S et al. Postoperative oxygenation following coronary artery bypass grafting. J Cardiovasc Surg 2000;41:221-5.
- 17. Quadrelli AS, Brandani LM. Alteraciones del intercambio gaseoso em post-operatorio de cirugia cardíaca. Medicina (Buenos Aires) 1995;55:300-6.
- 18. Singh PN, Vargas FS, Cukier A, Filho MT, Teixeira LR, Light RW. Arterial blood gases after coronary artery bypass surgery. Chest 1992;102:1337-41.
- 19. Ali J, Weisel R, Layung A, Kripke B, Hechtman H. Consequences of postoperative alterations in respiratory mechanics. Am J Surg 1974;128:376-82.
- 20. Fernandes CR, Neto PPR. O sistema respiratório e o idoso: implicações anestésicas. Rev Bras Anestesiol 2002;52:461-9.
- 21. Riebman JB, Yurvati AHO, Laub GW. Improved technique for pleural drain insertion in cardiovascular surgery. J Cardiovasc Surg 1994;35:503-5.
- 22. Pick A, Dearani J, Odell J. Effect of sternotomy direction on the incidence of inadvertent pleurotomy. J Cardiovasc Surg 1998;39:673-6.
- 23. Greinecker GW, Hakimi MY, Rinne T, Buhl R, Matheis G, Martens S et al. Effect of internal thoracic artery preparation on blood loss, lung function, and pain. Ann Thorac Surg 1999;67:1078-82.
- 24. Craig DB. Postoperative recovery of pulmonary function. Anesth Analg 1981;60:46-52
- 25. Sofia RR, Almeida LG. Complicações pulmonares no pós-operatório de cirurgia cardíaca. In: Regenga MM (ed). Fisioterapia em cardiologia da UTI à reabilitação. 1º ed. São Paulo:Roca; 2000. p. 31-43.
Endereço para correspondência
Datas de Publicação
-
Publicação nesta coleção
10 Set 2007 -
Data do Fascículo
Mar 2004
Histórico
-
Recebido
Nov 2003 -
Aceito
Fev 2004