ARTIGO DE REVISÃO
Desenvolvimento tecnológico dos oxigenadores de membrana
Mário Drummond* * Os autores declaram conflito de interesse ; Domingo M. Braile* * Os autores declaram conflito de interesse ; Ana Paula M. Lima-Oliveira* * Os autores declaram conflito de interesse ; Adalberto S. Camim* * Os autores declaram conflito de interesse ; Rosa S. Kawasaki Oyama* * Os autores declaram conflito de interesse ; Geraldo Hebert Sandoval* * Os autores declaram conflito de interesse
Endereço para correspondência Endereço para correspondência: Adalberto Camim Av. Juscelino K. de Oliveira, 1505 São José do Rio Preto SP CEP 15091-450 E-mail: camim@braile.com.br
Descritores: Oxigenadores de membrana. Circulação extracorpórea.
INTRODUÇÃO
As primeiras tentativas de oxigenar o sangue fora do organismo devem-se aos fisiologistas do século XIX, em seus estudos para a perfusão de órgãos isolados de animais.
Os primeiros estudos modernos dedicados à oxigenação artificial do sangue, com o objetivo de sustentar a vida de um organismo intacto, datam de 1937 e devem-se a John Gibbon [1]. Nos anos seguintes, esse mesmo pesquisador dedicou-se ao aperfeiçoamento dessa técnica revolucionária [2-4]. Estimulados pela perspectiva de construir aparelhos capazes de substituir as funções cardiopulmonares, vários pesquisadores se lançaram à construção de diferentes oxigenadores [5-7].
Os oxigenadores devem ser capazes de promover a oxigenação de cerca de cinco litros de sangue por minuto e remover o dióxido de carbono (CO2), para manutenção artificial da vida em um indivíduo adulto. Além disso, as trocas térmicas devem ser otimizadas na menor superfície possível, enquanto o trauma imposto aos elementos do sangue deve ser mínimo. O priming necessário à operação do aparelho também deve ser pequeno, a fim de permitir o seu uso com soluções acelulares, evitando a hemodiluição excessiva e as transfusões desnecessárias de sangue ou seus derivados [8].
Diversas maneiras de oferecer oxigênio (O2) ao sangue foram tentadas, com maior ou menor sucesso, e permitiram o desenvolvimento de inúmeros modelos de oxigenadores, dos quais apenas alguns encontraram aplicação clínica.
Segundo Gibbon [4], o oxigenador deveria produzir uma fina camada de sangue que ficasse em contato com O2. Isso poderia ser conseguido utilizando a força centrífuga ou formando bolhas de sangue ou fluindo o sangue sobre uma tela. Ele descreveu também vários problemas da oxigenação artificial, incluindo formação de espuma, hemólise e produção de substâncias vasoativas.
Os estudos iniciais com membranas para as trocas gasosas mostravam a relativa ineficiência da oxigenação para fluxos de sangue suficientes para manter pacientes em parada cardiocirculatória [8]. Quando se tornou patente que a circulação extracorpórea poderia ser conduzida com fluxos baixos, de acordo com o "princípio ázigos" popularizado pelo grupo de Lillehei, os pesquisadores voltaram a estudar as membranas, como forma de produzir uma oxigenação artificial mais fisiológica, por sua maior semelhança com a oxigenação realizada nos pulmões [9]. Estes estudos originaram os primeiros oxigenadores de membranas [10].
ORIGEM DOS OXIGENADORES DE MEMBRANAS
Os primeiros estudos para a oxigenação artificial do sangue esbarravam na formação de bolhas e espuma, de difícil remoção. Alguns pesquisadores procuraram utilizar membranas permeáveis aos gases, para fazer a separação física entre o sangue e o gás. Desse modo, evitava-se a formação de bolhas e tornava a oxigenação artificial mais semelhante à que ocorre nos pulmões [8].
Kolff e Berk [11], em 1944, observaram a arterialização do sangue ao atravessar as câmaras de celofane do seu primeiro rim artificial e iniciaram uma série de estudos, visando a utilização daquele material como membrana para trocas gasosas. Barrer [12] e Van Amerongen [13], em 1948, demonstraram que alguns elastômeros, naturais ou sintéticos, também eram permeáveis aos gases.
Os estudos iniciais demonstraram que a escolha do material da membrana é muito crítica, pois eles devem ser compatíveis com o sangue, permeáveis ao O2 e CO2, ter espessuras muito finas, com mínima resistência ao fluxo do sangue e dos gases respiratórios. Esses fatores dificultaram o desenvolvimento dos oxigenadores de membrana. Kolff [14], em 1955, construiu o primeiro protótipo de oxigenador de membranas a partir de lâminas de polietileno, que foi usado com sucesso, no laboratório experimental. As membranas eram enroladas em torno de um eixo central, conferindo ao oxigenador o formato de uma bobina.
Outros materiais, como celofane, celulose, silicone e teflon, foram utilizados na confecção de diferentes modelos de oxigenadores de membranas. Clowes e Neville [15] foram os pioneiros no uso de oxigenador de membranas em cirurgia cardíaca clínica e, em 1958, publicaram uma série de casos operados com o seu aparelho. As membranas eram planas, construídas de teflon e dispostas em camadas superpostas. O oxigenador era grande, difícil de montar e, freqüentemente, apresentava vazamentos. Posteriormente, outros oxigenadores de membranas com configurações semelhantes ao projeto original de Clowes e Neville [16] foram colocados em uso [5,17,18].
Kolobow et al. [19], baseando-se no modelo de Kolff, projetaram um oxigenador composto de longas tiras de silicone sustentadas por um envelope com espaçadores para impedir o colabamento das membranas. Nesse modelo, o sangue flui no interior das tiras e o O2 circula na direção do eixo central que sustenta a bobina de membranas. Como esse modelo funcionava adequadamente por longos períodos, foi utilizado em procedimentos de assistência ventilatória prolongada. O oxigenador de Kolobow foi continuamente aperfeiçoado e, atualmente, é produzido e comercializado pela empresa americana Avecor. É o único oxigenador do mercado recomendado para uso prolongado.
Os oxigenadores de membranas da primeira geração ofereciam grande resistência à passagem do sangue pelo trajeto das membranas, sendo impossível vencê-la pela simples sifonagem. Alguns aparelhos eram montados no lado de pressão positiva da bomba peristáltica, enquanto outros requeriam uma bomba adicional para circular o sangue no compartimento das membranas. Em função das dificuldades com as trocas gasosas e em virtude da complexidade de construção e uso, a primeira geração de oxigenadores de membrana não foi muito aceita. O desenvolvimento da tecnologia para a produção de membranas expandidas e capilares permitiu o surgimento de oxigenadores da atual geração. Nesses oxigenadores de membrana, as trocas gasosas ocorrem por difusão dos gases respiratórios através de uma membrana permeável aos gases, situada entre os fluxos de sangue e de gás do oxigenador, sem contato direto entre o sangue e o gás [8].
Os oxigenadores de membrana permitem o controle independente da transferência de O2 e CO2, pelo uso de um misturador de gases. A transferência de O2 é controlada pela porcentagem desse gás instilado no oxigenador. Quanto maior a fração de O2 no gás, maior será sua transferência para o sangue. A transferência do CO2 é controlada pelas variações do fluxo do gás que ventila o oxigenador. Quanto maior o fluxo de gás, maior será a remoção de CO2 do sangue.
O primeiro oxigenador de membrana reutilizável surgiu em 1956, baseado em princípios de trocas de gases observados nos hemodializadores em uso na época. Os primeiros oxigenadores de membranas descartáveis surgiram nos anos sessenta. Eram complicados para montar e operar; requeriam uma bomba adicional, para recircular o sangue no oxigenador, com a finalidade de melhorar a oxigenação. Essa geração de oxigenadores, conforme já assinalado, não desfrutou de muita popularidade [8].
PRINCÍPIOS DAS TROCAS GASOSAS
A transferência de gases para o sangue ou para o gás que ventila o oxigenador ocorre devido à difusão, que compreende a capacidade das moléculas do gás moverem-se das áreas de menor concentração para as áreas de maior concentração, buscando sempre o equilíbrio. A difusibilidade, ou a capacidade de um gás difundir-se, é constante para cada gás, material a ser atravessado e pela temperatura. A teoria cinética dos gases demonstra que a difusão depende da velocidade do movimento das moléculas do gás e, de acordo com a lei de Graham, é inversamente proporcional à raiz quadrada do peso molecular do gás. Assim, quanto menor o peso molecular do gás, maior é a sua difusibilidade. A velocidade da difusão de um gás também aumenta proporcionalmente a sua solubilidade.
A difusão e a transferência de gases nos oxigenadores de membrana são mais complexas do que as leis dos gases demonstram, porque há diversas barreiras a vencer. O O2 deve atravessar a membrana dos oxigenadores, dissolver-se no plasma do sangue, transpor a membrana das hemácias, difundir-se no citoplasma das hemácias para combinar-se com a hemoglobina. A difusão do CO2 no sangue é mais simples que a do O2 porque o CO2 é cerca de vinte vezes mais solúvel que o oxigênio e pode ser eliminado com grande facilidade, pela simples diferença de pressão parcial, através de qualquer tipo de membrana [8].
A difusão desses gases no interior do oxigenador depende do tipo de material da membrana, de sua espessura e porosidade, mas também é influenciada pela espessura da lâmina de sangue em contato com a membrana e pelas características do fluxo de sangue. A força que impulsiona o gás através da membrana é denominada pressão parcial. Quanto maior a diferença entre a pressão parcial, maior a força que impulsiona o gás. A velocidade da difusão também pode ser aumentada diminuindo-se a distância percorrida pelo gás. No caso dos oxigenadores, esse aumento pode ser conseguido reduzindo a espessura da membrana.
Outros fatores, como o tipo de fluxo de sangue, podem acentuar a difusão dos gases através das membranas. Um recurso bastante usado na construção dos oxigenadores é a produção de correntes secundárias ou "marginais". Estas correntes correspondem a um certo turbilhonamento na superfície de contato da membrana com o sangue favorecendo as trocas gasosas. A existência dessa turbulência pode compensar a relativa espessura da lâmina de sangue que atravessa o oxigenador.
Em uma mistura de gases ocupando um determinado volume, cada gás se comporta como se ocupasse sozinho todo o volume da mistura, independente dos demais gases. Este, em essência, constitui o enunciado da lei de Dalton que rege o comportamento dos gases. A soma da pressão parcial de cada gás de uma mistura gasosa corresponde à pressão total exercida pela mistura. Estas regras aplicam-se aos gases ocupando um espaço ou mesmo em solução, como é o caso dos gases dissolvidos no sangue. Assim, quando o sangue está em equilíbrio com a pressão atmosférica, a soma das pressões parciais dos gases dissolvidos no sangue será de 760mmHg, ao nível do mar. Em uma fase gasosa, a pressão parcial, a concentração e a fração de moléculas são grandezas equivalentes.
No sangue, o O2 e o CO2 não se comportam linearmente, como seria de esperar. Isso se deve à não linearidade da dissociação da oxi-hemoglobina. Este fenômeno é representado por uma curva sinusoidal. Do mesmo modo, o CO2 é combinado com diversas substâncias do plasma e da hemácia para formar bicarbonato. Tudo isso contribui para que O2 e o CO2 ocorram em concentrações maiores do que seria esperado pela simples dissolução física. Isto faz com que a análise da transferência de gases nos oxigenadores seja mais complexa.
MEMBRANAS VERDADEIRAS E MICROPOROSAS
Os princípios gerais acima enunciados aplicam-se aos oxigenadores de membrana de todos os tipos. Nas membranas microporosas, os gases não se dissolvem no material da membrana, ao contrário, atravessam os poros microscópicos existentes na membrana para essa finalidade. Todas as demais variáveis que influenciam as trocas gasosas também se aplicam às membranas microporosas.
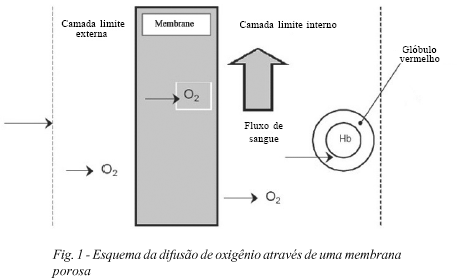
Os oxigenadores de membrana foram concebidos para trabalhar sem a interface gás-sangue existente nas demais modalidades de oxigenadores. As membranas consideradas "verdadeiras" constituem uma barreira entre o sangue e o gás, de modo que a transferência de gases depende da difusão deste no material de que a membrana é constituída. O gás, na realidade, dissolve-se na membrana e é liberado na face oposta, conforme o gradiente de pressão parcial existente entre os dois lados da membrana (Figura 1).
Os oxigenadores de membranas verdadeiras são de alto custo, difíceis de produzir, freqüentemente requerem grandes áreas de membrana e têm um grande volume de priming. Estes oxigenadores podem manter trocas gasosas de O2 e CO2, em condições satisfatórias, por longos períodos (até semanas), sem perda da eficácia. Estes aparelhos são utilizados nos procedimentos de longa duração, como assistência ventilatória ou circulatória prolongadas (ECMO/ELSO).
As membranas microporosas, pelo menos nos primeiros momentos da perfusão, permitem uma interface transitória entre gás-sangue. Após algum tempo ocorre o revestimento protéico das membranas que isola as duas fases, sangue e gás, mas permite a difusão pelos microporos. A tensão superficial do sangue impede que haja extravasamento pelos minúsculos poros da membrana capilar. Os microporos, na realidade, funcionam como condutos através da membrana de polipropileno, conferindo suficiente capacidade de difusão a ambos os gases, oxigênio e dióxido de carbono.
Após algumas horas de uso, a capacidade funcional dos oxigenadores de membrana microporosa se reduz, em virtude da evaporação e subseqüente condensação de soro que extravasa pelos microporos. Há evidências de que o aquecimento das membranas e do gás pode retardar esse fenômeno e aumentar a durabilidade do aparelho.
O diâmetro dos poros das membranas microporosas é inferior a 1micron, embora as dimensões exatas dependam do processo de fabricação. Mas é sempre necessário que os microporos tenham menos de 1 mícron de diâmetro para inibir o extravasamento de líquido ou gás pela superfície das membranas. Tipicamente, durante a fabricação, as fibras ocas de polipropileno são extrusadas, aneladas e alongadas, para produzir os microporos. Após atingir as dimensões desejadas, as fibras são aquecidas, para estabilizar a estrutura do polímero.
TIPOS DE OXIGENADORES DE MEMBRANAS
Os oxigenadores de membranas em uso corrente utilizam membranas de polipropileno microporoso ou silicone. Os demais materiais, como o teflon, polietileno e outros, foram abandonados. Os oxigenadores de membrana podem ser agrupados em três tipos principais:
1. Oxigenadores de placas São construídos com membranas microporosas de polipropileno expandidas, dobradas em Z como o fole de uma sanfona. Nesses equipamentos, o sangue e o gás fluem em lados opostos da membrana. Os principais exemplos são: Cobe Excel, Cobe VPCML, Shiley M-2000.
2. Oxigenadores em espiral São derivados do antigo modelo de oxigenador de Kolobov, que utilizam membranas de silicone. A membrana é enrolada em torno de um eixo central, como em um novelo, ligeiramente espiralado. Existe um único representante desse tipo de oxigenador, produzido pela empresa Avecor.
3. Oxigenadores de fibras ocas São confeccionados com membranas de polipropileno microporosas, constituídas de finos capilares dispostos em feixes paralelos ou em novelos, formando fibras ocas, fibras capilares ou membranas capilares. São os oxigenadores mais usados na atualidade. Esses oxigenadores são divididos em dois subgrupos, de acordo com o tipo de circulação do sangue:
A. O sangue flui no interior do capilar - Nesse modelo, o sangue circula no interior do feixe de fibras capilares e o gás circula no seu exterior, em sentidos opostos. Há um gradiente de pressão, produzido pela resistência das fibras à passagem do sangue e, ocasionalmente, podem apresentar trombose de um grande número de fibras, com comprometimento da função. Os principais exemplos são Bentley CM40 e Terumo Capiox Série 300.
B. O gás flui no interior do capilar Nesse modelo, o feixe de fibras capilares é percorrido pelo gás e fica imerso no fluxo de sangue. Essa configuração reduz o gradiente entre sangue e gás e, por conseguinte, diminui acentuadamente o trauma produzido pela passagem do sangue no interior dos capilares. Essa modalidade permite também reduzir a área de membranas necessária, otimizando o aproveitamento das características dinâmicas dos aparelhos. Esses são modelos mais modernos que acabaram por substituir os anteriores.
Nesses oxigenadores, o sangue venoso pode ser recolhido em um reservatório flácido, colapsável, como uma bolsa plástica, levando ao conceito de circuito dito "fechado". Esses reservatórios freqüentemente requerem a adição de um reservatório para receber o sangue dos aspiradores, chamado de reservatório de cardiotomia para completar o circuito da perfusão. Os modelos mais antigos usavam reservatórios flácidos, que têm sido substituídos pelos rígidos que assumem a função de reservatório venoso e de cardiotomia. Muitos deles incorporam um trocador de calor e o circuito resultante é dito "aberto", muito semelhante ao tradicional circuito dos oxigenadores de bolhas. Essa configuração desfruta da preferência da maioria das equipes cirúrgicas e de perfusão.
Muitos oxigenadores disponíveis no mercado oferecem as duas opções de reservatório, rígido ou colapsável. A última geração de aparelhos é composta de reservatório rígido acoplado ao módulo das membranas e o permutador de calor, em uma peça única. Estes aparelhos são denominados "integrados". Em todos os modelos descritos, o sangue do paciente é recolhido no reservatório venoso, passa para a bomba arterial, que impulsiona para o compartimento das membranas do oxigenador. Após a troca de gases, o sangue segue pela linha arterial, para o sistema arterial do paciente.
OXIGENADORES NEONATOS
A cirurgia cardíaca em neonatos vem aumentando progressivamente nos últimos anos. São realizadas, a cada ano, no Brasil, cerca de 500 cirurgias para correção de cardiopatias congênitas complexas [20]. Como o coração do neonato apresenta diferenças estruturais, funcionais e metabólicas em relação ao coração do adulto, uma nova geração de equipamentos passou a ser desenvolvida. Estes novos equipamentos contribuíram para a significativa redução da morbidade associada ao emprego da circulação extracorpórea (CEC) na idade neonatal. A alta incidência de morbidade se deve às dificuldades técnicas impostas pela correção de algumas cardiopatias e, principalmente, pelo manuseio da CEC com pequenos volumes de enchimento do circuito [21]. Os procedimentos da CEC para o neonato requerem equipamentos especiais, devido à estreita margem de tolerância desses pacientes aos desvios da fisiologia que afetam as funções cardiovasculares, pulmonares, neurológicas, renais e hepáticas [22]. A maioria dos oxigenadores e demais aparelhos destinados à perfusão infantil corresponde a miniaturas dos aparelhos desenvolvidos para adultos. Poucos são os produtos desenvolvidos para atender, especificamente, às necessidades dos neonatos. Uma das dificuldades que isso acarreta é a utilização de volumes de perfusato que correspondem a cerca de três vezes a volemia do paciente (em média, a volemia do neonato é de 250 ml). A nova geração de oxigenadores de membrana, construídos especialmente para a perfusão neonatal, permitiu a drástica redução dos volumes do perfusato. Braile et al. têm se dedicado ao desenvolvimento e aplicação de equipamentos utilizados em cirurgia cardíaca com CEC e, especialmente, oxigenadores de membrana [23-26].
REFERÊNCIAS BIBLIOGRAFICAS
1. Gibbon Jr. JH. Artificial maintenance of circulation during experimental occlusion of pulmonary artery. Arch Surg. 1937;34:1105.
2. Gibbon Jr. JH. The maintenance of life during experimental occlusion of the pulmonary artery followed by survival. Surg Gynecol Obstet. 1939;69:602.
3. Gibbon Jr. JH. An oxygenator with a large surface-volume ratio. J Lab Clin Med. 1939;24:1192.
4. Gibbon Jr. JH. Application of a mechanical heart and lung apparatus to cardiac surgery. Minn Med. 1954;37:171.
5. Bramson ML, Osborn JJ, Gerbode F. The membrane lung. In: Ionescu MI, ed. Techniques in extracorporeal circulation. 2nd ed. London:Butterworth;1981.
6. Bramson ML, Hill JD, Osborn JJ, Gerbode F. Partial veno-arterial perfusion with membrane oxygenation and diastolic augmentation. Trans Am Soc Artif Intern Organs. 1969;15:412-6.
7. Gerbode F, Osborn JJ, Bramson ML. Experiences in the development of a membrane heart-lung machine. Am J Surg. 1967;114(1):16-23.
8. Souza MHL, Elias DO. Circulação extracorpórea: histórico e desenvolvimento. In: Fundamentos da circulação extracorpórea. vol. I. Rio de Janeiro:Centro Editorial Alfa Rio; 1995. p.3-33.
9. Braile DM, Godoy MF. História da cirurgia cardíaca. Arq Bras Cardiol. 1996;66(6):329_37.
10. Taylor KM. Cardiopulmonary bypass: principles and management. London:Chapman and Hall;1986. p.986.
11. Kolff WJ, Berk TJ. Artificial kidney: dialyzer with great area. Acta Med Scand. 1944;117:121-34.
12. Barrer RM, Skirrow G. Transport and equilibrium phenomena in gas-elastomer systems. I. Kinetic phenomena. J Polimer Sc. 1948;3:549-63.
13. Van Amerongen CJ. Influence of structures of elastomers on their permeability to gases. J Polymer Sc. 1950;5:307-32.
14. Kolff WJ, Effler DB, Groves LK, Peereboom G, Moraca PP. Disposable membrane oxygenator (heart-lung machine) and its use in experimental surgery. Cleve Clin Q. 1956;23(2):69-97.
15. Clowes Jr. GHA, Neville WE. Further development of a blood oxygenator dependent upon the diffusion of gases through plastic membranes. Trans Am Soc Artif Intern Organs. 1957;3:52-8.
16. Clowes Jr. GHA, Neville WE. The membrane oxygenator. In: Extracorporeal circulation. Springfield: Thomas;1958. p.81-100.
17. Peirce EC II, Rogers WK, Dabbs CH, Rawson FL. Clinical experience with the membrane lung used in conjunction with hypothermia. J Tn State Med Assoc. 1961;54(1):39-43.
18. Landé AJ, Edwards L, Bloch JH, Carlson RG, Subramanian V, Ascheim R et al. Prolonged cardiopulmonary support with a practical membrane oxygenator. Trans Am Soc Artif Intern Organs. 1970;16:352-6.
19. Kolobow T, Spragg RC, Pierce JE, Zapol WM. Extended term (to 16 days) partial extracorporeal blood gas exchange with the spiral membrane lung in unanesthetized lambs. Trans Am Soc Artif Intern Organs. 1971;17:350-4.
20. DATASUS, 2004.
21. Garcia AM. Circulação extracorpórea em crianças. Acesso em 11/09/2002. Disponível em: www.perfiline.com/artigos/artigos98/ceccrian.htm.
22. Souza MHL, Elias DO. Curso de perfusão neonatal. Acesso em 25/07/2005. Disponível em: www.perfiline.com
23. Gandolfi JF, Braile DM. Perspectivas de aplicação clínica da oxigenação extracorpórea por membrana (ECMO) sem auxílio circulatório em recém-nascidos. Rev Bras Cir Cardiovasc. 2003;18(4):359-63.
24. Moscardini AC, Godoy MF, Braile DM, Godoy JMP, Soares MJ, Brandi AC et al. Oxigenação extracorpórea por membrana e alterações hematológicas em estudo experimental. Rev Bras Hematol Hemoter. 2002;24(2):97-104.
25. Novello WP, Dias FT, Bergamasco N, Braile DM. Clinical evaluation of oximaster i membrane oxygenator. Proceeding of the European Medical & Biological Engineering Conference. 1999;37(2):66-7.
26. Novello WP, Braile DM. Avaliação da tendência ao vazamento de plasma em membranas utilizadas em circulação extracorpórea. In: Congresso Brasileiro de Engenharia Mecânica; 1999; Águas de Lindóia. Anais/CD Rom. Águas de Lindóia:Associação Brasileira de Ciências Mecânicas;1999.
Artigo recebido em setembro de 2005
Artigo aprovado em dezembro de 2005
Trabalho realizado na Braile Biomédica. São José do Rio Preto, SP, Brasil.
Datas de Publicação
-
Publicação nesta coleção
11 Set 2007 -
Data do Fascículo
Dez 2005