Resumos
OBJETIVO: As células progenitoras endoteliais (CPE), caracterizadas pelo marcador CD133+, contribuem para a neovascularização, e o aumento no número dessas células pode ser uma ferramenta terapêutica promissora. O sangue de cordão umbilical humano contém um número significante de CPE, sugerindo a possibilidade do uso destas células para a revascularização de tecidos isquêmicos. O objetivo desse trabalho foi analisar a funcionalidade das células CD133+ diferenciadas in vitro. MÉTODOS: As células diferenciadas foram caracterizadas por citometria de fluxo; a expressão do mRNA de VEGF foi avaliada por RT-PCR e a funcionalidade, por meio de ensaios de formação de túbulos capilares. RESULTADOS: As células diferenciadas perderam os marcadores de CPE, mantiveram em níveis baixos os marcadores das linhagens hematopoética e monocíticas e aumentaram a expressão dos marcadores de células endoteliais adultas. As células diferenciadas apresentaram transcritos no mRNA de VEGF e mostraram-se capazes de formar túbulos capilares in vitro. CONCLUSÃO: As células CD133+ diferenciadas in vitro em células endoteliais demonstraram serem funcionalmente ativas, abrindo perspectiva para seu uso futuro em aplicações terapêuticas.
Células endoteliais; Proliferação de células; Transplante de células-tronco de sangue do cordão umbilical; Neovascularização Fisiológica
OBJECTIVE: Endothelial progenitor cells (EPC) caracterized by the CD133+ marker, contribute to the neovascularization. Increasing EPC number in vitro could be a promising therapeutic tool. Human umbilical cord blood maintains a significant number of EPC, suggesting the possibility to use these cells to induce the revascularization of ischemic tissues. The aim of this study was to analize the in vitro function of differentiated CD133+ cells. METHODS: Cells were characterized by flow cytometry, VEGF mRNA expression was evaluated by the RT-PCR analysis and the functionally by essays of capillary tubes formation. RESULTS: Differentiated cells lost EPC markers, maintained low levels of markers for hematopoietic and monocytic cell lines and increased the expression of adult endothelial cell markers. Differentiated cells expressed VEGF mRNA and were capable to induce in vitro capillary tubules formation. CONCLUSION: CD133+ cells differentiated into endothelial cells in vitro are functionally active initiating the possibility of their use in future therapeutic applications.
Endothelial cells; Cell proliferation; Cord blood stem cell transplantation; Neovascularization, physiologic
ARTIGO ORIGINAL
Formação in vitro de túbulos capilares a partir de células de sangue de cordão umbilical humano com perspectivas para aplicação terapêutica
Alexandra Cristina SenegagliaI; Paulo Roberto Slud BrofmanI; Carlos Alberto Mayora AitaI; Bruno DallagiovannaII; Carmen Lúcia Kuniyoshi RebelattoI; Paula HansenIII; Fabiane BarchikiIV; Marco Aurélio KriegerII
IPhD - Núcleo de Cardiomioplastia Celular - Pontifícia Universidade Católica do Paraná
IIPhD - Instituto Carlos Chagas - FIOCRUZ
IIIGraduada em Biologia, Doutoranda em Ciências da Saúde - Núcleo de Cardiomioplastia Celular - Pontifícia Universidade Católica do Paraná
IVGraduada em Biologia - Núcleo de Cardiomioplastia Celular - Pontifícia Universidade Católica do Paraná
Endereço para correspondência Endereço para correspondência: Paulo Roberto Slud Brofman Rua Gumercindo Mares, 150 - casa 12 - Vista Alegre Curitiba, PR - Brasil - CEP 80810-220 E-mail: paulo.brofman@pucpr.br
RESUMO
OBJETIVO: As células progenitoras endoteliais (CPE), caracterizadas pelo marcador CD133+, contribuem para a neovascularização, e o aumento no número dessas células pode ser uma ferramenta terapêutica promissora. O sangue de cordão umbilical humano contém um número significante de CPE, sugerindo a possibilidade do uso destas células para a revascularização de tecidos isquêmicos. O objetivo desse trabalho foi analisar a funcionalidade das células CD133+ diferenciadas in vitro.
MÉTODOS: As células diferenciadas foram caracterizadas por citometria de fluxo; a expressão do mRNA de VEGF foi avaliada por RT-PCR e a funcionalidade, por meio de ensaios de formação de túbulos capilares.
RESULTADOS: As células diferenciadas perderam os marcadores de CPE, mantiveram em níveis baixos os marcadores das linhagens hematopoética e monocíticas e aumentaram a expressão dos marcadores de células endoteliais adultas. As células diferenciadas apresentaram transcritos no mRNA de VEGF e mostraram-se capazes de formar túbulos capilares in vitro.
CONCLUSÃO: As células CD133+ diferenciadas in vitro em células endoteliais demonstraram serem funcionalmente ativas, abrindo perspectiva para seu uso futuro em aplicações terapêuticas.
Descritores: Células endoteliais. Proliferação de células. Transplante de células-tronco de sangue do cordão umbilical. Neovascularização Fisiológica
INTRODUÇÃO
As investigações envolvendo células-tronco (CT) têm aumentado e apresentam resultados promissores para recuperar tecidos lesados, incluindo os cardíacos [1,2]. Porém, a falta de vasculatura suficiente que possibilite suprir rápida e adequadamente as células infundidas, com oxigênio e nutrientes, ainda é fator limitante para o sucesso da implantação da engenharia de tecidos e para o tratamento da isquemia tecidual [3].
Atualmente, há três tipos de estado-clínico que poderiam ser beneficiados pelo transplante das células progenitoras endoteliais (CPE): isquemia de membro inferior, isquemia do miocárdio e cicatriz pós-infarto. Estudos indicaram que a terapia celular, utilizando células expandidas in vitro, poderia promover a neovascularização de tecidos isquêmicos, mesmo quando aplicada como terapia única; isto é, sem a administração de fatores de crescimento [4-6].
Uma limitação crítica para a aplicação terapêutica das CPE, pós-natal, é seu baixo número na circulação. Foram realizadas várias pesquisas, com o intuito de otimizar a quantidade e a qualidade dessas células para poderem ser usadas clinicamente [4]. Devido às pequenas quantidades de CPE encontradas no sangue periférico, essas não estão disponíveis prontamente para utilização em ensaios clínicos. Experimentos que aumentem a quantidade de CPE funcionais, viabilizando esta terapia, podem se tornar importantes.
Após o infarto do miocárdio, a angiogênese natural é normalmente insuficiente para a grande demanda por oxigênio e nutrientes, bem como para prevenir a apoptose dos cardiomiócitos hipertrofiados e o remodelamento ventricular. Sendo assim, o aumento da perfusão do miocárdio infartado, para melhorar a circulação de oxigênio e de nutrientes, por meio da formação de novos vasos sangüíneos, tem o potencial de melhorar a função cardíaca [7].
Os mecanismos potenciais para as CPE induzirem a neovascularização incluem aumento do fornecimento das células endoteliais (CE) pela proliferação e diferenciação das CPE ou em um aumento no fornecimento de fatores de crescimento para ativar as CE residentes maduras. As CPE são CD133+ e, a maioria, co-expressam o CD34+, somente uma pequena porcentagem é CD34-. Assim, as células CD133+ representam um subgrupo das CT CD34+, e são uma população ideal para gerar CE [8]. Sant'anna et al. [9] relataram que o aumento de capilares pela terapia gênica, utilizando injeção transmural de plasmídeo VEGF 165, tem presumível efeito benéfico na redução e na recuperação da área isquêmica.
Já foi demonstrado que o sangue de cordão umbilical humano (SCUH) contém células tronco mesenquimais [10] e um grande número de CPE [11], sugerindo a possibilidade de usar estas células para a revascularização de doenças isquêmicas. Até o presente, o transplante das CPE derivadas do SCUH ainda está em fase de experimentos com animais. A população exata de CPE específica (isoladas, expandidas ou diferenciadas), que deveria ser utilizada para transplante ainda não está claramente definida [12].
Nosso grupo implementou metodologias para diferenciar in vitro células CD133+, provenientes do SCUH, originando uma população de células semelhantes às endoteliais que foram avaliadas para comprovar se eram funcionalmente ativas e assim tornarem possível seu uso futuro para aplicações clínicas.
MÉTODOS
Os experimentos foram realizados no Laboratório Experimental de Cultivo Celular da PUCPR e no Instituto de Biologia Molecular do Paraná, com cinco amostras de sangue de cordão umbilical humano (SCUH), obtidas no Hospital e Maternidade Víctor Ferreira do Amaral - Curitiba/PR, de cinco parturientes que, após receberem todas as informações necessárias, assinaram o termo de consentimento livre e esclarecido e concordaram em participar do estudo. O Comitê de Ética em Pesquisa da Pontifícia Universidade Católica do Paraná aprovou este estudo sob nº 1366, e está registrado na Comissão Nacionalde Ética em Pesquisa (CONEP) sob nº FR - 105806.
Critérios de Inclusão de Parturientes Doadoras de SCUH
idade: 18 a 36 anos;
pré-natal documentado com pelo menos duas consultas;
parto normal ou cesáreo;
tempo de bolsa rota no máximo até 18 horas;
partos com pelo menos 32 semanas;
peso fetal do recém-nascido acima de 1.500 gramas;
parturientes sem comportamento de risco - uso de drogas,
promiscuidade sexual, doenças infectocontagiosas como: hepatite, doenças sexualmente transmissíveis, doença de Chagas e malária;
parturientes sem doenças que possam interferir na vitalidade da placenta, como: diabetes mellitus e hipertensão arterial;
parturientes que não façam uso de medicamentos antidepressivos, corticóides, ansiolíticos e hormônios de modo geral.
Purificação e expansão das células CD133+
As células CD133+ foram purificadas utilizando-se o conjunto de micropérolas acopladas ao anticorpo antiCD133 (Miltenyi Biotec®), de acordo com as instruções do fabricante. Resumidamente, a suspensão de células mononucleares (CM) foi centrifugada e ressuspendida em solução salina tamponada com fosfato (PBS) (Invitrogen Life Technologies®) suplementada com 5% de soro bovino fetal e 2 mM de ácido etilenodiamino tetra-acético (EDTA). As células foram então filtradas em um filtro com porosidade de 40 µm e centrifugadas por 10 minutos a 450 g e a concentração de células foi ajustada para, no máximo, 1 x 108 células em 300 µL de PBS suplementado. Foram adicionados 100 µL de solução bloqueadora (Miltenyi Biotec®) e 100 µL do anticorpo anti-CD133 puro ligado às micropérolas magnéticas (Miltenyi Biotec®); o material foi homogeneizado e incubado por 30 minutos a 4º C.
As CPE resultantes da purificação das CM do SCUH foram plaqueadas em placas de 12 poços recobertos com fibronectina (BD - Bioscience®) com meio IMDM suplementado e fatores de crescimento beta-FGF (Invitrogen Life Technologies®), IGF-I (Sigma-Aldrich®) e VEGF (Sigma-Aldrich®). Após cinco dias de cultivo, trocou-se o meio pela primeira vez e, depois, a cada dois dias. Os cultivos foram mantidos em estufa, com 5% de tensão de CO2 em atmosfera úmida. As células foram observadas diariamente em microscópio óptico invertido (Olympux IX70®) com relação a sua morfologia e proliferação. Quando as células alcançavam confluência de aproximadamente 80%, procediase à dissociação celular, utilizando a enzima Acutase. Primeiramente as células foram dissociadas das placas e replaqueadas em frascos de cultivo de 25 cm2 (TPP®) e, posteriormente, de um frasco para dois, seguindo em progressão geométrica até 30 dias de cultivo.
Caracterização celular por citometria de fluxo
A caracterização, a quantificação e a análise da viabilidade das células CD133+ purificadas e diferenciadas foram realizadas pela técnica da citometria de fluxo com anticorpos específicos. As células purificadas foram analisadas logo após seu isolamento, enquanto que as células diferenciadas foram analisadas ao final de 30 dias, após a dissociação celular. A técnica utilizada foi realizada de acordo com Owens e Loken [13].
Resumidamente, a marcação foi realizada com 2 x 105 células que foram incubadas com vários anticorpos conjugados a fluorocromos humanos. Isotipos idênticos aos anticorpos foram usados como controle. A aquisição das amostras foi realizada utilizando o citômetro de fluxo FACSCalibur (BD, EUA) e para as análises foi utilizado o programa FlowJo (FlowJo, EUA).
Ensaios para avaliação da funcionalidade das células expandidas e diferenciadas
Análise da expressão de transcritos do VEGF no mRNA por RT-PCR
O ácido ribonucléico (RNA) celular total das células CD133+ purificadas e das diferenciadas foi extraído utilizando o conjunto de reagentes RNeasy (Qiagen), de acordo com as recomendações do fabricante e, em seguida, foi realizada a síntese do ácido desoxirribonucléico complementar (cDNA).
Os transcritos que codificam para o VEGF foram amplificados pela reação em cadeia da polimerase, com transcrição reversa (RT-PCR) utilizando-se o cDNA e o par de primers VEGF (F1 5CTACCTCCACCATGCCAAGTG3 R1 5TGCGCTGATAGAACATCCATGA3). O gliceraldeído-3Fosfato-Desidrogenase (GAPDH) é um gene constitutivo e estável, expresso em altos níveis em quase todos os tecidos e células, e foi utilizado como controle interno. Os produtos de amplificação foram corados e analisados por eletroforese em gel de agarose a 2% e utilizou-se o marcador de peso molecular 1Kb Plus (Invitrogen Life Technologies®). As imagens foram capturadas pelo UV with darkroom (UVP Bioimaging Systems®), com o programa de análise da Labworks.
Ensaio de formação de túbulos capilares in vitro
Ao final de 30 dias de cultivo, as células CD133+ diferenciadas foram dissociadas e semeadas em placas de cultura de 24 poços, recobertas com 250 µL de MatrigelTM (BD-Biosciences®). A densidade celular foi de 20.000 células em 250 µL, de IMDM suplementado mais os fatores de crescimento. As células foram incubadas em estufa umidificada com tensão de 5%, de CO2, e observadas com duas, seis, doze e vinte e quatro horas em microscópio invertido (Olympus IX 70), para verificar a formação de túbulos capilares, e, assim, comprovar sua capacidade funcional in vitro. Durante a análise das células ao microscópio, as imagens foram obtidas por meio do sistema de captura de imagens spot insight (Diagnostic).
RESULTADOS
Caracterização celular por citometria de fluxo
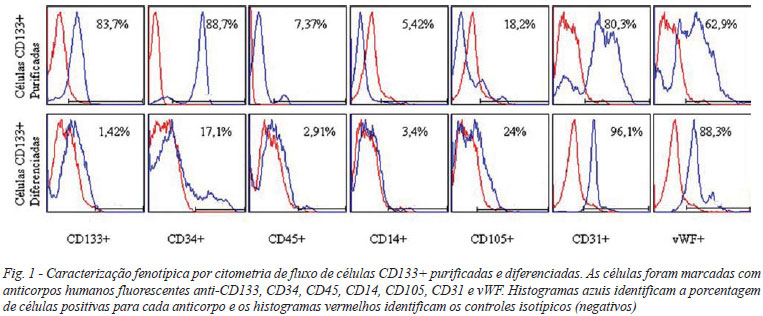
As células CD133+ purificadas foram avaliadas imunofenotipicamente depois do isolamento com as micropérolas imunomagnéticas acopladas ao anticorpo anti-CD133 e as células diferenciadas após dissociação enzimática ao final do cultivo de 30 dias (resultados representados na Figura 1). Desta forma, foi possível caracterizar cada um desses tipos celulares independentemente.
Análise da expressão de transcritos do VEGF no mRNA por RT-PCR
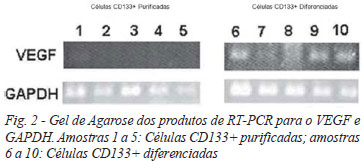
A análise da expressão no mRNA do VEGF foi realizada nas células CD133+ purificadas e diferenciadas, por RTPCR, em cinco amostras. Avaliou-se, como controle interno, a expressão de GAPDH, o qual apresentou bandas para as dez amostras analisadas. Nas células purificadas, não foi verificada a presença de transcritos no mRNA do VEGF. Observaram-se transcritos para o VEGF em todas as células diferenciadas testadas (Figura 2). Foi demonstrado que apenas as células após indução de diferenciação passaram a expressar transcritos no mRNA de VEGF.
Ensaio de formação de túbulos capilares in vitro
Para avaliar a função das células CD133+ diferenciadas foi testada a capacidade, in vitro, dessas células formarem túbulos capilares quando plaqueadas sobre o MatrigelTM. As células foram analisadas e fotografadas com duas, seis, doze e vinte e quatro horas após o plaqueamento. A análise das células demonstrou que, imediatamente após o plaqueamento, as células apresentavam morfologia arredondada e encontravam-se espalhadas pela superfície aleatoriamente, sem a formação de túbulos capilares (Figura 3A). E, após 24 horas, formaram estruturas semelhantes a túbulos capilares bem formadas (Figura 3B). Em todos os cinco experimentos, independentemente realizados, após 24 horas, as células diferenciadas formaram túbulos capilares in vitro.
DISCUSSÃO
Independentemente da fonte, CPE são difíceis de isolar porque representam uma população muito pequena, quando comparadas às células hematopoéticas. No sangue periférico, apenas 0,01% das CM são CPE [14]. Na MO, menos que 0,05% das células são CPE [15]. Em estudos prévios dos autores desse trabalho [16], conseguiu-se obter 0,64%, de CPE isoladas, a partir de CMS de SCUH, demonstrando que o SCUH pode ser uma melhor opção, como fonte de CPE, semelhante ao encontrado por Eggerman et al. [15], que demonstraram que o número de CPE de SCUH é superior ao encontrado no sangue periférico de adultos. O número exato de células necessário para induzir a neovascularização com sucesso ainda é uma incógnita [17]. A possibilidade de obter um número maior de células poderá abrir a perspectiva de que novos testes sejam realizados, para definir o número de células mais adequado para esse tipo de terapia.
As células tiveram seu fenótipo caracterizado por citometria de fluxo. Em torno de quatro semanas, quando as células alcançaram a confluência, as células CD133+ apresentaram-se semelhantes ao fenótipo típico de CE, tendo aumentada a positividade para marcadores característicos destas células, como o CD31 e o vWF [18]. Observou-se o decréscimo das células CD34+, porém algumas ainda continuaram presentes, em concordância com estudos de Gross e Herbrig [14], o mesmo aconteceu com o CD105. Verificou-se uma grande diminuição das células CD133, como descrito por Shmelkov et al. [19]. O número de células CD45 e CD14, respectivamente das linhagens hematopoéticas e monocíticas, não foi representativo.
A técnica da RT-PCR demonstrou claramente a presença de transcritos do VEGF no RNA mensageiro em todos os cinco experimentos independentemente realizados com células CD133+ diferenciadas. Sabe-se que o VEGF tem função determinante na neovascularização por ser um potente mitógeno para as CE, promove a proliferação e migração destas células, participa do remodelamento da matriz extracelular, formação de túbulos capilares e rede vascular [20]. A verificação da presença de transcritos no mRNA do VEGF é um fator importante para confirmar que apenas as CPE diferenciadas in vitro possuem características que permitem afirmar que são células semelhantes às CE adultas.
O ensaio funcional, por meio da formação tubular em MatrigelTM mostrou que as células CD133+ diferenciadas apresentaram in vitro a formação de estruturas semelhantes a capilares, fornecendo evidências adicionais de que as células proliferaram e originaram células semelhantes às células endoteliais. A capacidade de migração celular é fundamental para formar novos vasos e capilares e é uma característica das CE que são capazes de uma organização que resultam na formação de estruturas tubulares tridimensionais in vitro [21].
Os resultados obtidos, a respeito da funcionalidade das células CD133+ diferenciadas, parecem estar em concordância com um estudo pré-clínico de Kawamoto et al. [22]. Nesse estudo, as CPE diferenciadas in vitro e infundidas na área isquêmica de ratos com infarto agudo do miocárdio foram detectadas, em estudos histológicos, pós-eutanásia, na área de neovascularização. Demonstrouse que essas células não participam apenas da indução de fatores parácrinos, os quais estimulariam a proliferação de células presentes in situ, mas, sim, fisicamente da reconstituição da área lesada. Outro estudo, de Mukai et al. [23], que corrobora com os achados deste trabalho comprova que CPE cultivadas poderiam formar vasos sanguíneos. Diferente das CPE sem cultivo que promoveriam a angiogênese por meio da migração e proliferação de CE maduras; sugerindo assim que estas duas populações celulares teriam um papel diferente na neovascularização in vivo.
Segundo Rocha et al. [24], as células derivadas de SCUH são pouco imunogênicas, o que possibilitaria sua utilização em transplantes alogênicos. Há necessidade de estudos mais aprofundados para confirmar se as CPE diferenciadas in vitro possuem expressão de antígenos HLA ou não e qual a sua intensidade de expressão. Mesmo que essas células não apresentem antígenos HLA, outros testes na área da histocompatibilidade deverão ser realizados, com o objetivo de comprovar se as CPE diferenciadas in vitro despertam, ou não, a resposta imunológica alogênica. Em um estudo envolvendo células mesenquimais, Cho et al. [25] descrevem que as células mesenquimais alogênicas não desencadeiam uma resposta imunológica no tecido normal, porém em regiões de inflamação, na presença de citocinas como o IFN-γ pode haver rejeição. A partir dessas informações, será possível ter uma base mais sólida para viabilizar a possível utilização de CPE diferenciadas do SCUH em ensaios clínicos.
O uso de CPE derivadas de SCUH pode servir como uma estratégia útil para estudar a natureza dessas células, antes de usá-las em ensaios clínicos. As CPE podem ser obtidas e expandidas do SCUH e, também, utilizadas para várias propostas, como a expansão ex vivo de células semelhantes às CE, para terapia celular e gênica ou, de acordo com Quirici et al. [26], em co-cultivos in vitro, abrindo novas perspectivas para o tratamento da cardiomiopatia isquêmica. Os resultados obtidos por Melero-Martin et al. [27] reafirmam o potencial terapêutico in vivo das CPE para formar redes vasculares que permitam a vascularização de órgãos e tecidos isquêmicos.
Com base nos ensaios realizados ficou demonstrado que as células CD133+ diferenciadas in vitro têm função semelhante à das CE, abrindo perspectiva para seu uso futuro em aplicações terapêuticas.
AGRADECIMENTOS
À Alessandra Melo Aguiar e a Patrícia Shigunov, pela realização das técnicas de biologia molecular; à Dra. Vivian Ferreira do Amaral, pela coordenação das coletas do sangue de cordão umbilical humano; à Márcia Olandoski, pela análise estatística; e ao Dr. Alejandro Correa, pela análise crítica do trabalho.
Esse trabalho foi financiado pelo Ministério de Saúde e Conselho Nacional de Ensino e Pesquisa (CNPq) - 552233/2005-06.
Artigo recebido em 30 de janeiro de 2008
Artigo aprovado em 23 de setembro de 2008
Trabalho realizado na Pontifícia Universidade Católica do Paraná, Curitiba, PR, Brasil.
- 1. Schwartz Y, Kornowski R. Progenitor and embryonic stem cell transplantation for myocardial angiogenesis and functional restoration. Eur Heart J. 2003;24(5):404-11.
- 2. Scorsin M, Guarita-Souza LC. O transplante celular no tratamento da insuficiência cardíaca. Rev Bras Cir Cardiovasc. 2001;16(3):183-6.
- 3. Fuchs S, Hermanns MI, Kirkpatrick CJ. Retention of a differentiated endothelial phenotype by outgrowth endothelial cells isolated from human peripheral blood and expanded in long-term cultures. Cell Tissue Res. 2006;326(1):79-92.
- 4. Iwami Y, Masuda H, Asahara T. Endothelial progenitor cells: past, state of the art, and future. J Cell Mol Med. 2004;8(4):488-97.
- 5. Dallan LAO, Gowdak LH, Lisboa LAF, Schettert I, Krieger JE, Cesar LAM, et al. Terapia celular associada à revascularização transmiocárdica laser como proposta no tratamento da angina refratária. Rev Bras Cir Cardiovasc. 2008;23(1):43-52.
- 6. Almeida RMS. Carta ao editor: Terapia celular associada à revascularização transmiocárdica a laser: uma nova proposta no tratamento da angina refratária aos métodos terapêuticos. Rev Bras Cir Cardiovasc. 2008;23(2):292-4.
- 7. Lee MS, Lill M, Makkar RR. Stem cell transplantation in myocardial infarction. Rev Cardiovasc Med. 2004;5(2):82-98.
- 8. Chachques JC, Duarte F, Herreros J, Prosper F, Giambroni R, Julia P, et al. Cellular myogenic and angiogenic therapy for patients with cardiac or limb ischemia. Basic Appl Myol. 2003;13(1):29-37.
- 9. Sant'Anna RT, Kalil RAK, Moreno P, Anflor LC, Correa DLC, Ludwig R, et al. Gene therapy with VEGF 165 for angiogenesis in experimental acute myocardial infarction. Rev Bras Cir Cardiovasc. 2003;18(2):142-7.
- 10. Kawasaki-Oyama RS, Braile DM, Caldas HC, Leal JCF, Goloni-Bertollo EM, Pavarino-Bertelli EC, et al. Cultivo de células mesenquimais do sangue de cordão umbilical com e sem uso do gradiente de densidade Ficoll-Paque. Rev Bras Cir Cardiovasc. 2008; 23(1):29-34.
- 11. Nieda M, Nicol A, Denning-Kendall P, Sweetenham J, Bradley B, Hows J. Endothelial cell precursors are normal components of human umbilical cord blood. Br J Haematol. 1997;98(3):775-7.
- 12. Zhang L, Yang R, Han ZC. Transplantation of umbilical cord blood-derived endothelial progenitor cells: a promising method of therapeutic revascularisation. Eur J Haematol. 2006;76(1):1-8.
- 13. Owens M, Loken M. Flow citometry principles for clinical laboratory practice. Quality assurance for quantitative immunophenotyping. New York:Wiley-Liss;1995.
- 14. Gross P, Herbrig K. Role of endothelial progenitor cells in cardiovascular pathology. Rocz Akad Med Bialymst. 2004;49:174-7.
- 15. Eggermann J, Kliche S, Jarmy G, Hoffmann K, Mayr-Beyrle U, Debatin KM, et al. Endothelial progenitor cell culture and differentiation in vitro: a methodological comparison using human umbilical cord blood. Cardiov Res 2003;58(2):478-86.
- 16. Senegaglia AC, Brofman PRS, Aita CAM. Células progenitoras endoteliais de sangue de cordão umbilical humano: purificação, expansão e diferenciação [Tese de doutorado]. Curitiba:Pontifícia Universidade Católica do Paraná;2007. 125p.
- 17. Zammaretti P, Zisch AH. Adult 'endothelial progenitor cells'. Renewing vasculature. Int J Biochem Cell Biol. 2005;37(3):493-503.
- 18. Hoyer LW. The factor VIII complex: structure and function. Blood. 1981;58(1):1-13.
- 19. Shmelkov SV, Jun L, St Clair R, McGarrigle D, Derderian CA, Usenko JK, et al. Alternative promoters regulate transcription of the gene that encodes stem cell surface protein AC133. Blood. 2004;103(6):2055-61.
- 20. Shen BQ, Lee DY, Cortopassi KM, Damico LA, Zioncheck TF. Vascular endothelial growth factor KDR receptor signaling potentiates tumor necrosis factor-induced tissue factor expression in endothelial cells. J Biol Chem. 2001;276(7):5281-6.
- 21. Terranova VP, DiFlorio R, Lyall RM, Hic S, Friesel R, Maciag T. Human endothelial cells are chemotactic to endothelial cell growth factor and heparin. J Cell Biol. 1985;101(6):2330-4.
- 22. Kawamoto A, Gwon HC, Iwaguro H, Yamaguchi JI, Uchida S, Masuda H, et al. Therapeutic potential of ex vivo expanded endothelial progenitor cells for myocardial ischemia. Circulation. 2001;103(5):634-47.
- 23. Mukai N, Akahori T, Komaki M, Li Q, Kanayasu-Toyoda T, Ishii-Watabe A, et al. A comparison of the tube forming potentials of early and late endothelial progenitor cells. Exp Cell Res. 2008;314(3):430-40.
- 24. Rocha V, Wagner JE Jr, Sobocinski KA, Klein JP, Zhang MJ, Horowitz MM, et al. Graft-versus-host disease in children who have received a cord-blood or bone marrow transplant from an HLA-identical sibling. Eurocord and International Bone Marrow Transplant Registry Working Committee on Alternative Donor and Stem Cell Sources. N Engl J Med. 2000;342(25):1846-54.
- 25. Cho PS, Messina DJ, Hirsh EL, Chi N, Goldman SN, Lo DP, et al. Immunogenicity of umbilical cord tissue derived cells. Blood. 2008;111(1):430-8.
- 26. Quirici N, Soligo D, Caneva L, Servida F, Bossolasco P, Deliliers GL. Differentiation and expansion of endothelial cells from human bone marrow CD133(+) cells. Br J Haematol. 2001;115(1):186-94.
- 27. Melero-Martin JM, Khan ZA, Picard A, Wu X, Paruchuri S, Bischoff J. In vivo vasculogenic potential of human blood-derived endothelial progenitor cells. Blood. 2007; 109(11):4761-8.
Endereço para correspondência:
Datas de Publicação
-
Publicação nesta coleção
17 Fev 2009 -
Data do Fascículo
Dez 2008
Histórico
-
Recebido
30 Jan 2008 -
Aceito
23 Set 2008