Resumos
OBJETIVO: A troca valvar aórtica é procedimento rotineiro, envolve substituição da valva nativa/prótese. Na maioria destes pacientes o risco é aceitável, porém, em alguns casos, o risco predito pode justificar contra-indicação. O implante de valva aórtica minimamente invasivo transcateter e sem circulação extracorpórea (CEC) tem se mostrado viável, com menor morbi-mortalidade. O objetivo deste trabalho foi desenvolver bioprótese aórtica, montada em cateter, para implante sem CEC. MÉTODOS: Após desenvolvimento em animais, três pacientes com EuroSCORE elevado foram submetidos ao implante. Caso 1: portador de bioprótese com disfunção; Caso 2: estenose aórtica grave; Caso 3: disfunção de bioprótese aórtica. Após minitoracotomia e sob controle ecocardiográfico e fluoroscópico, cateter-balão foi posicionado sobre posição aórtica e insuflado. Após, segundo cateter-balão, com endoprótese valvada, foi posicionado e liberado sob alta frequência ventricular. Controles angiográficos e ecocardiográficos foram realizados e pacientes encaminhados para UTI. RESULTADOS: No primeiro caso foi possível implante sem CEC com resultados adequados. Evoluiu com melhora da função ventricular. Cursou com broncopneumonia, fístula traqueo-esofágica e óbito por mediastinite. Necropsia confirmou bom posicionamento valvar e preservação dos folhetos. O segundo caso apresentou migração do dispositivo após insuflação do balão, necessidade de esternotomia mediana de urgência, CEC e troca valvar convencional. O paciente evoluiu bem, recebendo alta da UTI 14 dias após procedimento e sem complicações. Cursou com infecção respiratória, choque séptico e óbito no 60º pós-operatório. O terceiro caso foi submetido a implante com sucesso. CONCLUSÃO: O implante de bioprótese transapical montada em cateter sem CEC mostrou ser procedimento factível. Detalhes técnicos e a curva de aprendizado demandam discussão.
Valva aórtica; Ponte cardiopulmonar; Cateterismo cardíaco
OBJECTIVE: The aortic valve replacement is a routine procedure, and involves replacement of the native valve/prosthesis. In most of the patients who undergo such procedure the risk is acceptable, but in some cases, such risk can justify contraindication. The minimally invasive transcatheter aortic valve implantation without cardiopulmonary bypass (CPB) has been shown to be viable, with lower morbidity and mortality. The aim of this study was to develop a catheter-mounted aortic bioprosthesis for implantation without CPB. METHODS: After developing in animals, three patients with high EuroSCORE underwent implantation. Case 1: patients with bioprosthesis dysfunction; Case 2: severe aortic stenosis; Case 3: dysfunction of aortic bioprosthesis. After minithoracotomy and under echocardiographic and fluoroscopic control, a balloon catheter was placed on aortic position and inflated. After, a second balloon with valved endoprosthesis was positioned and released under high ventricular rate. Echocardiographic and angiographic controls were performed and the patients were referred to ICU. RESULTS: In the first case, implantation without CPB was possible with appropriate results. The patient evolved with improvement of ventricular function. After, this patient developed bronchopneumonia, tracheoesophageal fistula and died due to mediastinitis. Autopsy confirmed proper valve positioning and leaflets preservation. The second case showed the device migration after inflation of the balloon, with the need for urgent median sternotomy, CPB and conventional valve replacement. This patient evolved well and was discharged from the ICU on the 14th postoperative day without complications. This patient developed respiratory infection, septic shock and died on the 60th postoperative day. The patient from the third case underwent successful implantation. CONCLUSION: The off-pump transapical implantation of catheter-mounted bioprosthesis was shown to be a feasible procedure. Technical details and learning curve require further discussion.
Aortic valve; Cardiopulmonary bypass; Heart catheterization
COMUNICAÇÃO BREVE
Implante transapical de endoprótese valvada balão-expansível em posição aórtica sem circulação extracorpórea
Diego Felipe GaiaI; José Honório PalmaII; José Augusto Marcondes de SouzaIII; José Cícero Stocco GuilhenIV; Andre TelisV; Claudio Henrique FischerVI; Carolina Baeta Neves Duarte FerreiraVII; Enio BuffoloVIII
IMestrado (Médico Disciplina de Cirurgia Cardiovascular)
IIProfessor Livre Docente (Chefe da Disciplina de Cirurgia Cardiovascular - UNIFESP)
IIIDoutor em Medicina (Hemodinamicista da UNIFESP)
IVCirurgião Cardiovascular (Médico Residente UNIFESP)
VCirurgião Cardiovascular (Médico Residente - UNIFESP)
VIDoutor em Medicina (Ecocardiografista UNIFESP)
VIIMestrado. Médica Anestesiologista. Disciplina de Anestesia, dor e terapia intensiva - (UNIFESP )
VIIIProfessor Titular de Cirurgia Cardiovascular (UNIFESP)
Endereço para correspondência Endereço para correspondência: Diego Felipe Gaia Rua Napoleão de Barros, 715, 3º Andar Cirurgia Cardiovascular - Vila Clementino São Paulo, SP, Brasil E-mail: drgaia@uol.com.br
RESUMO
OBJETIVO: A troca valvar aórtica é procedimento rotineiro, envolve substituição da valva nativa/prótese. Na maioria destes pacientes o risco é aceitável, porém, em alguns casos, o risco predito pode justificar contra-indicação. O implante de valva aórtica minimamente invasivo transcateter e sem circulação extracorpórea (CEC) tem se mostrado viável, com menor morbi-mortalidade. O objetivo deste trabalho foi desenvolver bioprótese aórtica, montada em cateter, para implante sem CEC.
MÉTODOS: Após desenvolvimento em animais, três pacientes com EuroSCORE elevado foram submetidos ao implante. Caso 1: portador de bioprótese com disfunção; Caso 2: estenose aórtica grave; Caso 3: disfunção de bioprótese aórtica. Após minitoracotomia e sob controle ecocardiográfico e fluoroscópico, cateter-balão foi posicionado sobre posição aórtica e insuflado. Após, segundo cateter-balão, com endoprótese valvada, foi posicionado e liberado sob alta frequência ventricular. Controles angiográficos e ecocardiográficos foram realizados e pacientes encaminhados para UTI.
RESULTADOS: No primeiro caso foi possível implante sem CEC com resultados adequados. Evoluiu com melhora da função ventricular. Cursou com broncopneumonia, fístula traqueo-esofágica e óbito por mediastinite. Necropsia confirmou bom posicionamento valvar e preservação dos folhetos. O segundo caso apresentou migração do dispositivo após insuflação do balão, necessidade de esternotomia mediana de urgência, CEC e troca valvar convencional. O paciente evoluiu bem, recebendo alta da UTI 14 dias após procedimento e sem complicações. Cursou com infecção respiratória, choque séptico e óbito no 60º pós-operatório. O terceiro caso foi submetido a implante com sucesso.
CONCLUSÃO: O implante de bioprótese transapical montada em cateter sem CEC mostrou ser procedimento factível. Detalhes técnicos e a curva de aprendizado demandam discussão.
Descritores: Valva aórtica. Ponte cardiopulmonar. Cateterismo cardíaco.
INTRODUÇÃO
A troca valvar aórtica em pacientes idosos é um procedimento rotineiro que envolve a substituição da valva nativa danificada ou de seu substituto protético com disfunção por, normalmente, uma bioprótese biológica de diferentes performances e modelos. Na maioria destes pacientes, o risco cirúrgico associado ao procedimento é aceitável e o resultado de longo prazo adequado é bem estabelecido [1].
O resultado esperado ainda pode ser bastante aceitável mesmo em octogenários [2]. Porém, em alguns casos e especialmente nas reoperações, o risco predito por diversos escores pode alcançar patamares que justifiquem a contra-indicação do procedimento, podendo atingir 6%-15% [3].
Na busca de alternativas para este grupo de pacientes de alto risco, o implante minimamente invasivo transcateter e sem o uso de circulação extracorpórea tem se mostrado, em séries experimentais e clínicas, uma alternativa viável e de menor morbidade e mortalidade para doentes de alto risco cirúrgico, com possibilidade de realização inclusive em reoperações [4].
Alguns dispositivos como a CoreValve (CoreValve, Paris, France) e a Edwards Sapiens (Edwards Lifescience Inc, Irvine, CA, USA) estão em pesquisa, porém nenhum disponível amplamente em nosso meio e com custos elevados de utilização.
Assim, tornou-se necessário o desenvolvimento de tecnologia nacional neste campo, com o intuito de viabilizar a produção e a utilização deste novo conhecimento. Após fase experimental de desenvolvimento e treinamento em animais de experimentação, foi possível obter um dispositivo seguro, de fácil implante e com performance semelhante à encontrada nas biopróteses porcinas atualmente disponíveis em nosso mercado (Figura 1).
Com base nestes resultados, foi possível realizar o implante transapical de uma prótese biológica montada em uma endoprótese balão-expansível sem circulação extracorpórea, em três doentes de alto risco cirúrgico.
RELATO DOS CASOS
Caso 1
Paciente do sexo masculino, 64 anos, hipertenso e portador de prótese biológica em posição aórtica (segunda prótese: primeira há 30 anos e segunda há 20 anos, sem seguimento ambulatorial) foi admitido em nosso serviço de emergência com flutter atrial de alta resposta ventricular. Após controle e reversão da arritmia, o paciente permaneceu em observação na unidade de dor torácica. Apresentou após algumas horas choque cardiogênico, evoluindo para tipo funcional IV (New York Heart Association) e propedêutica compatível com insuficiência aórtica grave.
O ecocardiograma transesofágico demonstrou insuficiência aórtica grave por rotura do folheto da bioprótese, hipertensão pulmonar moderada, insuficiência mitral leve a moderada e disfunção ventricular moderada do ventrículo esquerdo e grave do ventrículo direito.
Em poucas horas, o paciente evoluiu com refratariedade ao uso de drogas vasoativas, congestão pulmonar, oligúria, piora da função renal e necessidade de ventilação mecânica invasiva.
O risco operatório estimado pelo EuroSCORE logístico era de 54%.
Optou-se pela realização do implante válvula-em-válvula transapical transcateter sem circulação extracorpórea, baseado na experiência adquirida em centros já realizadores do procedimento e no desenvolvimento experimental satisfatório de um dispositivo nacional testado em animais de experimentação. Além disso, foi realizada reunião de consenso entre as especialidades envolvidas e obtido consentimento dos responsáveis pelo paciente e aprovação do comitê de ética em pesquisa institucional.
O implante foi realizado em sala cirúrgica híbrida de alta tecnologia, com presença de diversos dispositivos (hemodinâmica, ecocardiografia, suporte de circulação extracorpórea, além dos materiais e equipamentos cirúrgicos e anestésicos habituais).
Após indução anestésica, uma pequena toracotomia ântero-lateral esquerda no quinto espaço intercostal foi confeccionada para expor o ápice ventricular esquerdo. A seguir, foi realizada uma sutura em bolsa dupla apoiada em almofadas de teflon. Um introdutor vascular 6F foi posicionado com auxílio de um fio-guia através de punção no centro da bolsa sob visão ecocardiográfica e fluoroscópica.
Com auxílio de um fio-guia hidrofílico e de um cateter de pigtail, foi possível avançar através da valva aórtica em direção à aorta torácica descendente.
A aortografia inicial confirmou a insuficiência aórtica e auxiliou a identificação do anel valvar aórtico protético e a posição dos óstios coronarianos.
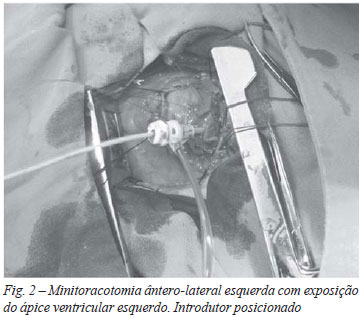
O anel valvar aórtico foi medido pelo ecocardiograma transesofágico, com diâmetro interno de 19 mm. Uma prótese biológica balão-expansível montada em stent de aço inoxidável com "oversize" de 20% foi selecionada e posicionada sobre o anel da bioprótese com disfunção, através de um introdutor 24F (Figura 2).
O débito cardíaco foi reduzido com auxílio de marcapasso epimiocárdico temporário e, em seguida, insuflado o balão com pressão máxima de 5 atmosferas (atm) e liberação da prótese (Figura 3).
Após a recuperação dos batimentos cardíacos e da pressão arterial, o ecocardiograma confirmou ausência de insuficiência aórtica significativa e a aortografia de controle, boa aposição protética e óstios coronarianos livres (Figura 3).
O paciente evoluiu com melhora da função ventricular e possibilidade de retirada de ventilação mecânica no 2º dia de pós-operatório. No 30º dia de pós-operatório, cursou com broncopneumonia, necessidade de traqueostomia, fístula traqueo-esofágica e óbito por mediastinite. O achado necroscópico confirmou bom posicionamento valvar e preservação dos folhetos (Figura 4).
Ecocardiograma realizado no 30º dia de pós-operatório não evidenciou disfunção ou vazamento, com gradiente máximo aórtico de 39 mmHg.
Caso 2
Paciente do sexo feminino, 81 anos, portadora de estenose aórtica grave com gradiente aórtico máximo de 72 mmHg e fração de ejeção de 42%, foi admitida na unidade de emergência com insuficiência cardíaca descompensada e necessidade de introdução de drogas vasoativas.
A doente permaneceu em insuficiência cardíaca, com grave congestão pulmonar e necessidade de ventilação mecânica não-invasiva apesar da terapêutica clínica otimizada.
O EuroSCORE logístico era de 60%. Após obtenção do termo de consentimento informado, a paciente foi submetida ao implante transapical de valva aórtica balão-expansível.
Utilizando a mesma técnica descrita no caso 1, um cateterbalão foi insuflado até o seu limite pressórico (5 atm) com o objetivo de aliviar a estenose aórtica. Uma prótese de 22 mm de diâmetro foi expandida até o seu limiar sobre o anel nativo sob redução do débito cardíaco com marca-passo.
Após a expansão, foi possível notar através da visão fluoroscópica a migração do dispositivo em direção ao arco da aorta. Optado a seguir por esternotomia mediana e conversão para procedimento convencional com circulação extracorpórea para resgate da prótese e substituição valvar aórtica.
A doente evoluiu satisfatoriamente, recebeu alta da unidade de terapia intensiva no 14º dia de pós-operatório. No entanto, no 20º dia de pós-operatório, cursou com infecção respiratória, insuficiência renal, choque séptico e óbito no 60º dia de pós-operatório.
Caso 3
Paciente do sexo masculino, 84 anos, portador de bioprótese aórtica há 16 anos, hipertenso e com insuficiência renal crônica não-dialítica, admitido no setor de emergência com insuficiência cardíaca congestiva em tipo funcional IV (New York Heart Association). O ecocardiograma transtorácico evidenciou rotura dos folhetos da bioprótese com insuficiência aórtica grave e disfunção ventricular esquerda (fração de ejeção de 42%).
A cineangiocoronariografia não demonstrou lesões coronarianas e a aortografia confirmou a insuficiência aórtica.
O EuroSCORE logístico era de 64%. Após obtenção do termo de consentimento informado foi indicada intervenção transapical.
Utilizando-se da técnica descrita no caso 1, sob controle ecocardiográfico transesofágico e fluoroscópico, uma bioprótese montada sobre balão foi posicionada sobre a bioprótese com disfunção e, durante redução do débito cardíaco, expandida por balão sobre a anterior.
Após a recuperação do débito cardíaco, o ecocardiograma demonstrou correta aposição da prótese sem gradiente sistólico significativo (25 mmHg) ou insuficiência aórtica central ou perivalvar. A aortografia confirmou os achados e a ausência de interferência com os óstios coronarianos.
O paciente foi retirado de ventilação mecânica na sala cirúrgica e encaminhado para a unidade de terapia intensiva. No pós-operatório imediato, a insuficiência renal tornou-se mais aguda, com necessidade de terapia dialítica transitória.
O paciente encontra-se atualmente estável em unidade de enfermaria. Ecocardiograma de controle sem disfunção, fração de ejeção do ventrículo esquerdo de 57%, pressão de artéria pulmonar de 40 mmHg, gradiente transvalvar aórtico de 16 mmHg e sem vazamento central ou periprotético. Programação de alta no 10º dia de pós-operatório.
DISCUSSÃO
O implante valvar aórtico transcateter é uma técnica nova e sob pesquisa em diversos centros ao redor do mundo [4-6]. O principal objetivo do procedimento é oferecer uma qualidade técnica satisfatória com menor morbidade e mortalidade quando comparada ao procedimento convencional, especialmente por evitar o uso da circulação extracopórea, esternotomia mediana e pinçamento aórtico.
Resultados preliminares têm sido encorajadores, com mortalidade em 30 dias ao redor de 8% [4]. Além dos implantes sobre valvas nativas, implantes sobre biopróteses com disfunção também são relatados [7].
Diversos dispositivos protéticos têm sido testados em diferentes centros, porém a maior experiência mundial concentra-se na prótese da Edwards Lifesciences, a qual se encontra sob investigação em estudo multicêntrico (Partner trial- Placement of AoRTic traNscathetER valve).
O presente estudo pode demonstrar o desenvolvimento de um dispositivo protético de tecnologia nacional, da mesma maneira que outras experiências nacionais prévias, como os circuitos de circulação extracorpórea, as próteses valvares biológicas e as endopróteses de aorta, frutos da interação entre a indústria e o meio acadêmico.
O desenvolvimento local destas tecnologias torna viável a expansão de procedimentos de alta tecnologia em nosso ambiente, viabilizando inclusive seu acesso pelo Sistema Único de Saúde.
Os três casos relatados ressaltam pontos importantes relacionados ao procedimento: sua aplicabilidade e possibilidade de realização, com sucesso imediato no implante válvula-sobre-válvula e falha no implante sobre prótese nativa.
A falha no implante sobre prótese nativa se deu por provável curva de aprendizado na expansão do balão, o qual se encontrava parcialmente dentro do introdutor, ejetando assim a prótese em direção à aorta ascendente.
A experiência demonstra ser fundamental a interação entre diversas especialidades, demandando cirurgião cardiovascular, hemodinamicista, ecocardiografista e anestesista especialmente treinados e envolvidos no procedimento. Também é necessário um ambiente cirúrgico híbrido capaz de integrar tecnologias cirúrgicas e endovasculares com a presença de dispositivo de aquisição de imagens fluoroscópicas (com capacidade de reprodução de imagens em tempo real), ecocardiograma transesofágico, além de material cirúrgico adaptado ao uso radioscópico [8].
A via transapical foi selecionada em detrimento da transfemoral frente aos relatos de maior mortalidade em 30 dias e maior ocorrência de acidente vascular cerebral por esta via [9].
Não ocorreram complicações vasculares relacionadas ao acesso, uma preocupação presente na manipulação do ápice ventricular em idosos, nem acidentes vasculares cerebrais ou bloqueio atrioventricular, complicação relatada especialmente com os dispositivos auto-expansíveis [10].
Esta pequena experiência inicial não nos permite inferir resultados de sobrevida ou complicações de modo confiável, por se tratar de procedimento inicial e considerando-se a curva de aprendizado do procedimento.
A avaliação de cada um dos dispositivos, inclusive o aqui relatado, é imperativa no intuito de determinar o correto perfil dos pacientes candidatos ao procedimento. A análise da manutenção dos resultados, muitas vezes considerados subótimos, especialmente se comparados à troca valvar convencional também é fundamental.
Outro ponto de discussão são os critérios utilizados para definir a gravidade do paciente selecionado, como o EuroSCORE e o STS Score. Alguns autores relatam índices de complicação e mortalidade na troca valvar aórtica em pacientes de alto risco inferiores aos preditos [2].
CONCLUSÃO
O implante transapical minimamente invasivo de bioprótese aórtica montada em cateter balão-expansível é uma técnica viável. Existe relevante curva de aprendizado e a necessidade de uma equipe de múltiplas especialidades no intuito de viabilizar o procedimento. O resultado em longo prazo, bem como a correta seleção de pacientes, permanecem não resolvidos.
Artigo recebido em 20 de janeiro de 2009
Artigo aprovado em 11 de maio de 2009
Trabalho realizado na Universidade Federal de São Paulo - UNIFESP, São Paulo, SP, Brasil.
Comentário
Eu gostaria de agradecer a oportunidade de comentar este trabalho e cumprimentar o Dr. Diego e o grupo de cirurgia cardiovascular da UNIFESP por mais esta iniciativa pioneira no nosso meio.
O trabalho, além de relatar os primeiros três casos de implante transapical de valva aórtica no Brasil, têm o mérito de desenvolver conjuntamente com uma empresa nacional um dispositivo, que, a exemplo de muitos outros, pode possibilitar e expandir seu uso em nosso país. Atualmente a CoreValve(que é auto expansível), recentemente adquirida pela Medtronic está disponível para uso clínico no Brasil e aprovada pela ANVISA, e provavelmente à época da submissão do artigo ainda não havia sido liberada. A outra disponível (Edwards Sapien) ainda não foi liberada pela ANVISA. Ambas podem ser implantadas tanto por via transfemoral como transapical.
O estudo, apesar de relatar apenas três casos, demonstra a viabilidade do uso do dispositivo e sua aplicação clínica.O implante por cateter de valva aórtica é um procedimento novo e foi introduzido na prática clínica há poucos anos.
Como bem ressaltado no trabalho para o sucesso destes procedimentos, além da curva de aprendizagem, a interação entre o cirurgião cardiovascular, o cardiologista intervencionista, o ecocardiografista e o anestesista é fundamental. Idealmente o procedimento deve ser realizado em uma sala cirúrgica híbrida que conte com todas as facilidades cirúrgicas como iluminação, instrumental, máquina de circulação extracorpórea e facilidades de imagem como ecocardiograma transesofágico, aparelho de hemodinâmica com fluoroscopia de alta qualidade e mesa de fibra de carbono. Como este é um procedimento no início da sua experiência clínica e em evolução o aperfeiçoamento dos dispositivos pela indústria deverá conferir melhor condições de posicionamento e até reposicionamento da prótese, com consequente maior segurança a estes pacientes de alto risco para a cirurgia convencional.
Acredito que na discussão a comparação entre as vias transapical e transfemoral poderia ser mais explorada. As principais vantagens da abordagem transapical são: inserção anterógrada, associada com mínima manipulação da aorta ascendente e arco e menor incidência de AVC quando comparada com a via transfemoral. Além disso não há problema de acesso vascular e o posicionamento é mais preciso. Por outro lado a via transapical requer uma mini-toracotomia que pode ser uma desvantagem, especialmente em pacientes com doença pulmonar grave e naqueles muito debilitados.
Após estas colocações gostaria de fazer quatro perguntas:
1) Qual a opinião do grupo sobre a colocação de um fio guia na veia femoral, além do acesso à artéria femoral (que já e utilizada para a colocação do pigtail para controle angiográfico). De acordo com o grupo de Leipzig, Mohr et al., que recentemente publicaram a experiência de 1 ano em 50 pacientes, esta estratégia permite estabelecer a circulação extracorpórea em 2 a 3 minutos, já tendo sido utilizada com sucesso em uma paciente com oclusão do tronco da coronária esquerda pela prótese (estratégia chamada de "safety net").
2) Com relação ao tipo de dispositivo utlizado. Vocês empregaram a endoprótese valvada expansível por balão. Quais as vantagens e desvantagens em relação à autoexpansível?
3) Se sabe que a ocorrência de insuficiência aórtica após estes procedimentos valvares por cateter é alta. Qual a impressão de vocês sobre o resultado a médio prazo como a possibilidade de insuficiência cardíaca, hemólise e endocardite?
E por fim:
4) Em casos em que há contraindicação para a cirurgia convencional na estenose aórtica, quando se deve indicar a via transfemoral ao invés da transapical?
Agradeço mais uma vez a oportunidade de comentar este trabalho.
Eduardo Keller Saadi
Respostas dos autores
1 - Por tratar-se de experiência inicial do grupo e por julgarmos fundamental a presença da estratégia de "safety net" com o objetivo de aumentar a segurança do procedimento em eventualidades e conversões de urgência para um procedimento convencional ou de resgate de acidentes, utilizamos em todos os casos o circuito de circulação extracorpórea montado e pronto, além das artéria e veia femorais canuladas e preparadas para entrada em perfusão sob heparinização plena.
Provavelmente, com o avançar da experiência poderemos permitir apenas o posicionamento dos fios guia, sem a canulação efetiva.
2) - O desenvolvimento em animais de experimentação do nosso dispositivo passou, inicialmente, por um dispositivo auto-expansível. A manipulação e abertura mostram-se mais complexos quando comparados à balão-expansível. Além disso, a literatura demonstra que os dispositivos auto-expansíveis podem apresentar maior incidência de bloqueios de condução, além de não permitirem a estratégia "valvein-valve" utilizado em alguns casos. Assim, selecionamos o dispositivo balão expansível para nossa experiência inicial, certamente estudos comparativos de maior duração possam esclarecer melhor qual dispositivo apresenta maior segurança e melhor perfil.
3) O procedimentos transcateter definitivamente apresentam um resultado sub-ótimo quando comparados à intervenção convencional. A maioria destes vazamentos é decorrente da incompleta coaptação do dispositivo ao anel valvar. Não existem ainda dados de seguimento em longo prazo capazes de predizer o desfecho comparativo destas insuficiências. Podemos supor que dada a gravidade dos casos selecionados possam ser toleradas insuficiências leves ou leve-moderadas com repercussão
4) Ainda não existe um consenso acerca da melhor via de acesso, é claro que a via transfemoral nos parece menos agressiva e menos invasiva do que a manipulação ventricular apical.
Na disponibilidade de dispositivos de baixo perfil, com introdutores menores que 22F ou 20F, sistema ilíaco femoral favorável, ou seja, sem grande quantidade de ateroscleose/tortuosidades e na ausência de placas/úlceras no arco da aorta, a via transfemoral nos parece mais adequada. Porém, o perfil destes pacientes é exatamente o oposto desta situação. Desta maneira, poderíamos dizer que a via transapical é favorável a grande maioria e a tranfemoral para casos selecionados no atual momento dos dispositivos. clinica existente, porém pouco significativas em médio prazo.
É razoável acreditar que da mesma maneira que observamos clinicamente pacientes com tal insuficiência em valvas nativas possamos agir da mesma maneira neste grupo selecionado. A presença de hemólise severa, insuficiência cardíaca refratária ou endocardite certamente precisarão serem tratadas de maneira convencional mesmo diante do elevado risco predito para tais intervenções.
- 1. Blackstone EH, Cosgrove DM, Jamieson WR, Birkmeyer NJ, Lemmer JH Jr, Miller DC, et al. Prosthesis size and long-term survival after aortic valve replacement. J Thorac Cardiovasc Surg. 2003;126(3):783-96.
- 2. Grossi EA, Schwartz CF, Yu PJ, Jorde UP, Crooke GA, Grau JB, et al. High-risk aortic valve replacement: are the outcomes as bad as predicted? Ann Thorac Surg. 2008;85(1):102-6.
- 3. Iung B, Baron G, Butchart EG, Delahaye F, Gohlke-Bärwolf C, Levang OW, et al. A prospective survey of patients with valvular heart disease in Europe: the Euro Heart Survey on Valvular Heart Disease. Eur Heart J. 2003;24(13):1231-43.
- 4. Walther T, Falk V, Kempfert J, Borger MA, Fassl J, Chu MW, et al. Transapical minimally invasive aortic valve implantation: the initial 50 patients. Eur J Cardiothorac Surg. 2008;33(6):983-8.
- 5. Walther T, Simon P, Dewey T, Wimmer-Greinecker G, Falk V, Kasimir MT, et al. Transapical minimally invasive aortic valve implantation: multicenter experience. Circulation. 2007;116(11 Suppl):I240-5.
- 6. Svensson LG, Dewey T, Kapadia S, Roselli EE, Stewart A, Williams M, et al. United States feasibility study of transcatheter insertion of a stented aortic valve by the left ventricular apex. Ann Thorac Surg. 2008;86(1):46-54.
- 7. Walther T, Kempfert J, Borger MA, Fassl J, Falk V, Blumenstein J, et al. Human minimally invasive off-pump valve-in-a-valve implantation. Ann Thorac Surg. 2008;85(3):1072-3.
- 8. Walther T, Dewey T, Borger MA, Kempfert J, Linke A, Becht R, et al. Transapical aortic valve implantation: step by step. Ann Thorac Surg. 2009;87(1):276-83.
- 9. Webb JG, Pasupati S, Humphries K, Thompson C, Altwegg L, Moss R, et al. Percutaneous transarterial aortic valve replacement in selected high-risk patients with aortic stenosis. Circulation. 2007;116(7):755-63.
- 10. Piazza N, Grube E, Gerckens U, den Heijer P, Linke A, Luha O, et al. Procedural and 30-day outcomes following transcatheter aortic valve implantation using the third generation (18 Fr) corevalve revalving system: results from the multicentre, expanded evaluation registry 1-year following CE mark approval. EuroIntervention. 2008;4(2):242-9.
Endereço para correspondência:
Datas de Publicação
-
Publicação nesta coleção
14 Set 2009 -
Data do Fascículo
Jun 2009
Histórico
-
Aceito
11 Maio 2009 -
Recebido
20 Jan 2009