Resumos
OBJETIVO: Avaliar a descelularização com SDS como tratamento anticalcificante em pericárdio bovino fixado em glutaraldeído. MÉTODOS: Peças de 0,5 cm² foram implantadas em modelo subcutâneo de 18 ratos por até 90 dias. Foram formados quatro grupos: grupo GDA: pericárdio fixado em glutaraldeído 0,5% (GDA), grupo GDA-GL: pericárdio fixado em GDA + ácido glutâmico (GL) 0,2%, grupo D-GDA: pericárdio descelularizado (D) com SDS 0,1% e fixado em GDA e grupo D-GDA-GL: pericárdio descelularizado + GDA + ácido glutâmico 0,2%. Cada animal recebeu enxertos dos quatro grupos. Os explantes foram realizados com 45 e 90 dias. As avaliações foram: análise histológica com as colorações hematoxilina-eosina e alizarina-red, análise morfométrica e quantificação de cálcio por espectrometria de absorção atômica. RESULTADOS: O padrão de infiltrado inflamatório foi o mesmo nos quatro grupos, sendo mais intenso nos grupos GDA e GDA-GL aos 45 dias, ficando mais evidente aos 90 dias. O conteúdo de cálcio aos 45 dias foi de 32,52 ± 3,19 µg/ mg no grupo GDA; 22,12 ± 3,87 µg/mg no grupo GDA-GL; 1,06 ± 0,38 µg/mg no grupo D-GDA e 3,99 ± 5,78 µg/mg no grupo D-GDA-GL (P< 0,001). Aos 90 dias, foi de 65,91 ± 24,67 µg/mg no grupo GDA; 38,37 ± 13,79 µg/mg no grupo GDA-GL; 1,24 ± 0,99 µg/mg no grupo D-GDA e 30,54 ± 8,21 µg/mg no grupo D-GDA-GL (P< 0,001). O grupo D-GDA foi o único que não apresentou progressão da calcificação de 45 para 90 dias (P=0,314). CONCLUSÃO: A descelularização com SDS reduziu o processo inflamatório e inibiu a calcificação em pericárdio bovino implantado em modelo subcutâneo de ratos até 90 dias.
bioprótese; pericárdio; engenharia tecidual; cálcio
OBJECTIVE: The aim of study was to investigate the SDS-based decellularization process as an anticalcification method in glutaraldehyde-preserved bovine pericardium in subcutaneous rat model. METHODS: Pericardium samples with 0.5 cm² area were divide in four groups: group GDA: 0.5% glutaraldehydepreserved pericardium (GDA); group GDA-GL: GDA + 0.2% glutamic acid (GL); group D-GDA: decellularized (D) pericardium with 0.1% SDS + GDA and group D-GDA-GL: decellularized pericardium + GDA + 0.2% glutamic acid. After this samples were implanted in 18 rats in subcutaneous position till 90 days. Each animal received samples of the four groups. The explants were performed at 45 and 90 days. The explants were subjected to histology in glass slides stained with hematoxilin-eosin and alizarin red, morphometry evaluation and the calcium content was measured by flame atomic absorption spectrometry. RESULTS: The inflammatory infiltrate was the same in all groups, however more intense in GDA and GDA-GL groups in 45 days, increasing at 90 days. The calcium contents for 45 days were: 32.52 ± 3.19 µg/mg in GDA group; 22.12 ± 3.87 µg/ mg in GDA-GL group; 1.06 ± 0.38 µg/mg in D-GDA group and 3.99 ± 5.78 µg/mg in D-GDA-GL (P< 0.001). For 90 days were 65.91 ± 24.67 µg/mg in GDA group; 38.37 ± 13.79 µg/mg in GDA-GL group; 1.24 ± 0.99 µg/mg in D-GDA group and 30.54 ± 8.21 µg/mg in D-GDA-GL (P< 0.001). Only D-GDA did not show increase rates of calcium at 45 to 90 days (P=0.314). CONCLUSION: SDS-based decellularization process reduced the inflammatory intensity and calcification in bovine pericardium in subcutaneous rat model for 90 days.
bioprosthesis; pericardium; tissue engineering; calcium
ARTIGO ORIGINAL
Efeito da descelularização com SDS na prevenção da calcificação em pericárdio bovino fixado em glutaraldeído. Studo em ratos
Claudinei CollatussoI; João Gabriel RoderjanII; Eduardo Discher VieiraIII; Francisco Diniz Affonso da CostaIV; Lucia de NoronhaV; Daniele de Fátima FornazariVI
IMestre em cirurgia; Cirurgião cardíaco da Santa Casa de Misericórdia de Curitiba, Curitiba, PR, Brasil
IIMestre em Ciêcias da Saúde; Especialista em Cultivo Celular do Nuìcleo de Enxertos Cardiovasculares, Curitiba, PR, Brasil
IIIBioìlogo; Especialista em Cultivo Celular do Nuìcleo de Enxertos Cardiovasculares, Curitiba, PR, Brasil
IVLivre Docente; Chefe do Serviço de Cirurgia Cardíaca da Santa Casa de Curitiba e Hospital Ecoville, Curitiba, PR, Brasil
VPhD em Patologia; Meìdica patologista do Laboratório de Patologia Experimental do CCBS PUCPR, Curitiba, PR, Brasil
VICirurgiã Cardíaca da Santa Casa de Misericórdia de Curitiba
Endereço para correspondência Endereço para correspondência: Claudinei Collatusso Rua Schiller, 143 - ap. 1301 - Cristo Rei Curitiba, PR, Brasil - CEP: 80050-260 E-mail: claudineicl@yahoo.com.br
RESUMO
OBJETIVO: Avaliar a descelularização com SDS como tratamento anticalcificante em pericárdio bovino fixado em glutaraldeído.
MÉTODOS: Peças de 0,5 cm2 foram implantadas em modelo subcutâneo de 18 ratos por até 90 dias. Foram formados quatro grupos: grupo GDA: pericárdio fixado em glutaraldeído 0,5% (GDA), grupo GDA-GL: pericárdio fixado em GDA + ácido glutâmico (GL) 0,2%, grupo D-GDA: pericárdio descelularizado (D) com SDS 0,1% e fixado em GDA e grupo D-GDA-GL: pericárdio descelularizado + GDA + ácido glutâmico 0,2%. Cada animal recebeu enxertos dos quatro grupos. Os explantes foram realizados com 45 e 90 dias. As avaliações foram: análise histológica com as colorações hematoxilina-eosina e alizarina-red, análise morfométrica e quantificação de cálcio por espectrometria de absorção atômica.
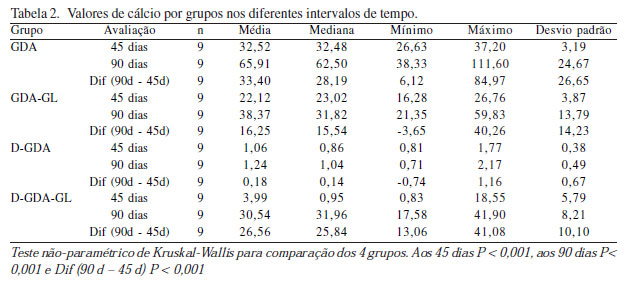
RESULTADOS: O padrão de infiltrado inflamatório foi o mesmo nos quatro grupos, sendo mais intenso nos grupos GDA e GDA-GL aos 45 dias, ficando mais evidente aos 90 dias. O conteúdo de cálcio aos 45 dias foi de 32,52 ± 3,19 µg/ mg no grupo GDA; 22,12 ± 3,87 µg/mg no grupo GDA-GL; 1,06 ± 0,38 µg/mg no grupo D-GDA e 3,99 ± 5,78 µg/mg no grupo D-GDA-GL (P< 0,001). Aos 90 dias, foi de 65,91 ± 24,67 µg/mg no grupo GDA; 38,37 ± 13,79 µg/mg no grupo GDA-GL; 1,24 ± 0,99 µg/mg no grupo D-GDA e 30,54 ± 8,21 µg/mg no grupo D-GDA-GL (P< 0,001). O grupo D-GDA foi o único que não apresentou progressão da calcificação de 45 para 90 dias (P=0,314).
CONCLUSÃO: A descelularização com SDS reduziu o processo inflamatório e inibiu a calcificação em pericárdio bovino implantado em modelo subcutâneo de ratos até 90 dias.
Descritores: bioprótese. pericárdio. engenharia tecidual. cálcio.
INTRODUÇÃO
O emprego do glutaraldeído (GDA) como agente de fixação tecidual [1] possibilitou que próteses valvares cardíacas construídas com tecidos heterólogos pudessem ser utilizadas clinicamente com resultados bastante satisfatórios. Além de ser efetivo na esterilização e na redução antigenicidade tecidual por mascaramento de antígenos celulares, o GDA aumenta a resistência biomecânica dos tecidos, o que pode se traduzir em melhor durabilidade das biopróteses. Entretanto, a degeneração tecidual por calcificação distrófica ainda é problemática, especialmente em crianças e adultos jovens [2].
Os fatores que influenciam a calcificação são multifatoriais incluindo a composição fosfolipídica da matriz extracelular, a intensidade das reações inflamatória e imunológica ao tecido heterólogo e o estresse mecânico provocado pelo movimento de abertura e fechamento das cúspides valvares. Além disso, existem evidências de que a própria fixação pelo GDA também favoreça o processo de calcificação distrófica [3,4]. Na tentativa de eliminar ou retardar essa complicação, diversos métodos anticalcificantes foram testados, com graus variados de sucesso [5]. Esses métodos visam, principalmente, remover os componentes calcificáveis do tecido ou neutralizar os efeitos tóxicos dos aldeídos residuais [6-12].
É bem estabelecido que as células e debris celulares presentes no tecido fixado se constituem em focos iniciais de cristalização. Por estarem desvitalizadas, ocorre um desequilíbrio no processo de transporte de cálcio nessas células que leva ao aumento do cálcio intracelular, o qual se liga aos fosfolipideos da membrana celular, com consequente formação de cristais de fosfato de cálcio. Assim sendo, as tecnologias de descelularização tecidual permitem a obtenção de matrizes acelulares que, ao menos em teoria, são menos imunogênicas e com potencial reduzido de calcificação [13-17].
Nosso grupo de pesquisa na Pontifícia Universidade Católica do Paraná (PUCPR) desenvolveu tecnologia de descelularização de homoenxertos valvares baseada em solução de dodecil sulfato de sódio (SDS). Os resultados experimentais e clínicos demonstraram que homoenxertos aórticos e pulmonares descelularizados são menos imunogênicos e capazes de serem repovoados "in vivo" após o implante. Além disso, houve ausência de calcificação tanto das cúspides como na parede arterial dos enxertos, mesmo em enxertos implantados em crianças e adolescentes com até 6 anos de evolução clínica [18,19].
Este estudo pretende verificar, experimentalmente em ratos, se a descelularização com SDS aplicada ao pericárdio bovino fixado em GDA de próteses comercialmente disponíveis, também é efetiva para reduzir a calcificação nesta situação.
MÉTODOS
Os pericárdios bovinos foram obtidos em abatedouros locais e imediatamente enviados ao laboratório, onde foi realizada limpeza mecânica da gordura da superfície pericárdica, seccionados em porções de 10 cm2 e, então, armazenados em solução de tampão fosfato (PBS 0,1M pH 7,4 - Sigma, IL) a 4ºC. Os pericárdios foram divididos em quatro grupos, de acordo com o método de tratamento tecidual:
Grupo 1 (GDA - Grupo Controle) - pericárdios frescos fixados em GDA 0,5% (glutaraldeído purificado em carvão mineral por filtração - Merck, Alemanha) em tampão fosfato (PBS 0,1M pH 7,4 - Sigma, IL, Estados Unidos) (v/ v) por 72 horas a 20ºC;
Grupo 2 (GDA-GL) - GDA 0,5% (glutaraldeído purificado em carvão mineral por filtração - Merck, Alemanha) em tampão fosfato (PBS 0,1M pH 7,4 - Sigma, IL, Estados Unidos) (v/v) por 72 horas a 20ºC e, subsequentemente, tratados com ácido glutâmico 0,2% (Sigma, IL, Estados Unidos) (m/v) em tampão fosfato (PBS 0,1M pH 3,5 - Sigma, IL) por 24 horas a 20ºC;
Grupo 3 (D-GDA) - pericárdios descelularizados em SDS 0,1% (Patente brasileira PI 800603-2) e, subsequentemente, fixados em GDA 0,5% (Merck, Alemanha) por 72 horas;
Grupo 4 (D-GDA-GL) - pericárdios descelularizados em SDS 0,1%, sendo em seguida fixados em GDA 0,5% (glutaraldeído purificado em carvão mineral por filtração -Merck, Alemanha) por 72 horas a 20ºC e, subsequentemente, tratados com ácido glutâmico 0,2% (Sigma, IL, Estados Unidos) (m/v) em tampão fosfato (PBS 0,1M pH 3,5 - Sigma, IL, Estados Unidos) por 24 horas a 20ºC.
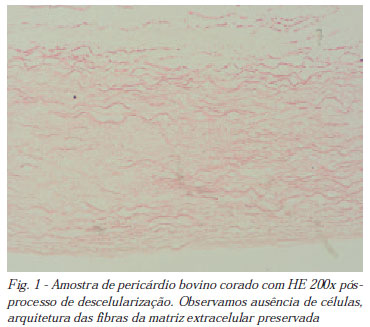
Todos os procedimentos de preparo dos pericárdios foram realizados em fluxo laminar, utilizando-se instrumentos e soluções estéreis, seguindo as normas das Boas Práticas de Fabricação. Os fragmentos de pericárdios dos grupos que envolveram a descelularização foram analisados pela coloração hematoxilina-eosina (HE) para confirmação da retirada completa das células (Figura 1).
As amostras para implante foram preparadas cortando-se os quatro segmentos de pericárdios, de cada grupo de tratamento, em 18 corpos de prova de 0,5 cm2 cada, os quais mantidos em solução salina estéril até o momento do implante no subcutâneo dos ratos.
Implante no subcutâneo de ratos
Para realização dos ensaios de calcificação foi utilizado o modelo experimental em subcutâneo de ratos jovens [18].
Todos os procedimentos foram realizados em acordo com "Guide for Care and Use of Laboratory Animals" publicados no U.S. National Institute Health (NIH publication 85-23, revised in 1996).
Esse estudo foi aprovado pelo Comitê de Ética no Uso de Animais - CEUA PUC-PR, nº 620.
Foram utilizados ratos da linhagem Sprague-Dawley (CEMIB - Unicamp, SP, Brasil), de 4 semanas de idade, pesando entre 70 e 90 g, sendo implantado um segmento de pericárdio de cada grupo em cada animal. No total, foram empregados 18 ratos, os quais foram anestesiados com 10 mg/g de quetamina (Crystália, Brasil) e 3 mg/g de xilasina (Bayer, Brasil) por injeção intraperitonial. Os animais foram colocados em decúbito ventral, realizada tricotomia da região dorsal e, em seguida, feita assepsia com iodopovidona (PVPI - Segmenta, Brasil). Os segmentos de pericárdio foram implantados em quatro áreas distintas: região escapular esquerda - grupo GDA; região escapular direita - grupo GDA-GL; região lombar esquerda - grupo D-GDA; e região lombar direita - grupo D-GDA-GL. Após o procedimento cirúrgico, os animais receberam antibiótico - cefazolina sódica 4 mg/kg (ABL, Brasil) e analgésico - dipirona sódica 10 mg/g (Bayer, Brasil), administrados por 3 dias. Os animais foram acondicionados em gaiolas com sepilho controlado e receberam água e comida ad libitum.
Os animais foram divididos em dois grupos de nove ratos cada, de acordo com o tempo do explante. O primeiro grupo incluiu nove animais que tiveram os pericárdios explantados com 45 dias e o segundo grupo envolveu os demais nove ratos que tiveram os pericárdios explantados com 90 dias de evolução. Para o explante, os animais foram anestesiados com o mesmo protocolo anestésico e, em seguida, foram eutanasiados em câmara de CO2. As amostras foram retiradas do subcutâneo por incisão da pele e remoção das aderências, sendo lavadas em solução salina isotônica e cortadas em duas partes iguais. A primeira metade foi utilizada para análise histomorfológica e a outra para dosagem da concentração de cálcio por espectrometria de absorção atômica.
Espectrometria de absorção atômica
As amostras destinadas à espectrometria de absorção atômica, para quantificação do cálcio, foram secas a 200ºC em uma mufla, por 2 horas, pesadas em sua totalidade e hidrolizadas em tubos de vidro contendo 1 ml de ácido clorídrico 6M. Os tubos foram aquecidos a 92º C em banhomaria. Após o processo, as amostras hidrolisadas foram encaminhadas à análise utilizando o instrumento PERKIN ELMER 4100 (LACTEC - PR, Brasil), sendo os resultados expressos em µg de cálcio por mg de tecido - pericárdio bovino.
Avaliação histomorfológica
Os explantes foram fixados em formalina tamponada a 10%, montados em blocos de parafina e cortados em micrótomo a 5 µm. Os cortes foram montados em lâminas de vidro e corados HE e alizarina Red pH 4,2 e 7,0 (Sigma, IL, Estados Unidos). O estudo histomorfológico visou, fundamentalmente, avaliar a intensidade e as características do infiltrado inflamatório e da calcificação.
As características histopatológicas do infiltrado inflamatório foram feitas de acordo com metodologia descrita por Maizato et al. [20], que incluem a análise da presença de reação granulomatosa, infiltrado mononuclear, tecido granulomatoso, necrose tecidual e presença de bactérias. A quantificação foi baseada na extensão do percentil observado nos campos microscópicos e graduada entre 0 e 4 como se segue:
0: ausência de alterações no tecido examinado;
1: alterações presentes entre 1-25% da área do tecido analisado;
2: alterações presentes entre 26-56% da área do tecido analisado;
3: alterações presentes entre 51-75% da área do tecido analisado;
4: alterações presentes entre 76-100% da área do tecido analisado.
A análise da calcificação foi realizada pela medida morfométrica da área calcificada comparada à área nãocalcificada, medida nos cortes histológicos corados pela alizarina-red em dois pH's: pH 4,2 para fosfato de cálcio e pH 7,0 para oxalato de cálcio e outros sais de cálcio, resultando em uma porcentagem de tecido calcificado [10]. As análises morfométricas foram realizadas sob imagens capturadas em microscópio ótico Olympus DX-40, acoplado em sistema de captura de imagens, no aumento de 100x. As medidas foram realizadas utilizando a ferramenta de comparação de porcentagem do software ImagePro Plus 6, sendo repetidas duas vezes por observadores diferentes em teste cego. Os resultados das medidas foram registrados em planilha e submetidos a análise estatística.
Análise estatística
Os resultados foram expressos por médias, medianas, valores mínimos, valores máximos e desvios padrões. Para a comparação de dois grupos em relação a variáveis quantitativas, foi considerado o teste não-paramétrico de Mann-Whitney. Comparações entre mais de dois grupos foram feitas usando-se o teste não-paramétrico de Kruskal-Wallis. Para a comparação dos momentos de avaliação dentro de cada grupo, foi usado o teste não-paramétrico de Wilcoxon. Valores de P<0,05 indicaram significância estatística. Os dados foram organizados em planilha Excel e analisados com o programa computacional Statistica v.8.0.
RESULTADOS
Análise histomorfométrica
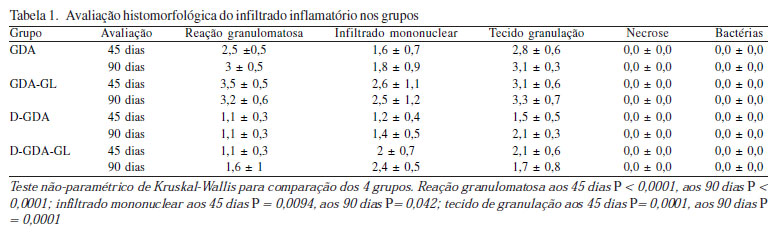
Houve presença de infiltrado inflamatório com as mesmas características nos quatro grupos estudados (Figura 2). Entretanto, pudemos observar que a descelularização diminuiu a intensidade dessa reação, visto que os grupos D-GDA e D-GDA-GL foram os que apresentaram os menores percentis de células inflamatórias, tanto aos 45 como com 90 dias de evolução (P< 0,001). Os pericárdios do grupo GDA-GL foram os que apresentaram reações inflamatórias mais acentuadas quando comparado aos demais grupos (Tabela 1). Não foram observadas áreas de necrose ou presença de bactérias em nenhum grupo.
Com as colorações de alizarina nos pHs 4,2 e 7, ficou evidenciada a presença de calcificação progressiva, especialmente nos grupos GDA e GDA-GL, com grandes quantidades de cristais de cálcio visíveis na região central dos pericárdios explantados. Os melhores resultados foram obtidos com o grupo D-GDA, onde a calcificação foi inexistente ou mínima em ambos os períodos. Os pericárdios do grupo D-GDA-GL tiveram aspecto histológico semelhantes aos do grupo D-GDA, aos 45 dias de evolução, entretanto, aos 90 dias, já era possível evidenciar alguns pequenos grânulos focais de calcificação. A Figura 3 ilustra os aspectos histológicos com coloração alizarina-red pH 4,2 que evidenciam a calcificação em decorrência do depósito de cristais de fosfato de cálcio aos 45 e 90 dias de evolução.
A morfometria da quantidade de cálcio pela coloração de alizarina nos pHs 4,2 e 7, confirmaram a interpretação visual das imagens histológicas (Figura 4). Estatisticamente, todos os grupos tiveram calcificação significativamente menor do que o grupo controle. Entretanto, quando comparados grupo a grupo, o grupo D-GDA foi o que estatisticamente teve os menores índices de calcificação, tanto aos 45 como aos 90 dias de evolução (P<0,0001) em relação aos demais grupos. A única exceção foi o grupo DGDA-GL aos 45 dias, onde a calcificação pela alizarina-red pH 7 foi semelhante ao do grupo 3.
Quantificação do cálcio
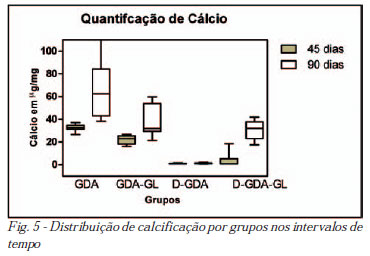
Os valores da quantidade de cálcio em µg de cálcio/mg de tecido obtidos por espectrofotometria por absorção atômica estão demonstrados na Tabela 2 e Figura 5.
Pode-se observar que a quantidade aumentou progressivamente nos grupos GDA, GDA-GL e D-GDA-GL. Da mesma forma com o que foi observado pela morfometria, todos os grupos tiveram calcificação significativamente menor do que os do grupo controle. O grupo D-GDA, além de ser o que teve os menores valores para a quantidade de cálcio, foi o único que não apresentou calcificação progressiva, com valores semelhantes tanto aos 45 como aos 90 dias de evolução (P=0,314). A comparação dos grupos dois a dois nos intervalos de tempo pode ser observada na Tabela 3.
DISCUSSÃO
Os mecanismos de calcificação de próteses valvares biológicas são complexos e multifatoriais, envolvendo aspectos bioquímicos, imunológicos e biomecânicos, dentre outros3. Além disso, a interação de fatores biológicos relacionados aos pacientes com o tecido heterólogo após o implante são importantes na ocorrência da degeneração tecidual e calcificação distrófica progressiva [1-3].
É bem determinado que as membranas e debris celulares, ricos em fosfolipídeos, são focos de deposição inicial dos cristais de cálcio. A fusão desses cristais leva à formação de nódulos, com consequente espessamento e enfraquecimento do tecido, aumentando a quantidade de calcificação distrófica. Além disso, a reação inflamatória causada pelo tecido fixado e a presença dos aldeídos residuais do processo de fixação, ávidos por cálcio, favorecem a deposição progressiva de cristais [3-5].
Diversas abordagens terapêuticas têm sido testadas com o objetivo de evitar ou retardar a degeneração tecidual, prolongando assim a durabilidade das próteses biológicas. Essas abordagens visam, preferencialmente, interferir em dois mecanismos principais da calcificação: remover os elementos teciduais capazes de iniciar a calcificação ou neutralizar os aldeídos residuais tóxicos decorrentes da solução de fixação tecidual [9].
A tecnologia de descelularização tecidual, por do emprego de soluções detergentes e/ou enzimáticas, vem sendo empregada com o objetivo de remover por completo todas as células e debris celulares, mantendo apenas a matriz extracelular intacta [14]. Essa metodologia pode ter dupla influência na redução da calcificação: além de remover as células como foco inicial de deposição de cálcio, reduz a antigenicidade do tecido, o que possivelmente diminui a reação inflamatória e imunológica por parte do receptor, o que tenderia a diminuir a degeneração tecidual progressiva [16].
Nosso grupo de pesquisa no Núcleo de Enxertos Cardiovasculares da PUCPR desenvolveu solução de descelularização baseada em solução de SDS 0,1%. Esta solução foi inicialmente testada em homoenxertos valvares aórticos e pulmonares, e os resultados, tanto experimentais como clínicos, têm demonstrado redução acentuada da calcificação [18,19]. Assim sendo, nos pareceu apropriado estudar os efeitos dessa solução em tecidos heterólogos fixados em GDA, para verificar sua efetividade como agente anticalcificante em biopróteses valvares de pericárdio bovino e/ou próteses porcinas.
A eficiência do nosso método de descelularização foi comprovada por meio de controles histológicos com HE realizados antes da fixação com GDA (Figura 1), onde observamos a presença de uma matriz extracelular colágena íntegra com ausência completa dos elementos celulares. Trabalho semelhante já havia sido realizado por Oswal et al. [15], demonstrando que a solução de SDS possibilitou a completa descelularização de pericárdios bovinos mantendo a integridade da matriz extracelular.
Optamos pelo modelo de implante em subcutâneo de ratos, por ser um método barato, prático e já bem estabelecido na literatura. Entretanto, estamos cientes de que, uma vez comprovada a eficiência da metodologia, será necessária a sua confirmação em modelos mais sofisticados, tais como o implante na circulação pulmonar ou sistêmica de ovinos.
Estudo preliminar do nosso grupo de pesquisa, empregando o mesmo modelo experimental aqui utilizado, já demonstrou que o ácido glutâmico foi eficiente em reduzir a calcificação de pericárdios bovinos fixados em GDA [12]. Por esse motivo, pericárdios bovinos fixados em GDA formaram nosso grupo controle, enquanto que a adição da descelularização ou do pós-tratamento com ácido glutâmico foram comparadas isoladamente ou em associação para se determinar qual a metodologia mais eficiente para a redução da calcificação.
A correlação entre a intensidade da reação inflamatória e a ocorrência de calcificação foi demonstrada por Manjii et al. [4]. Em nosso estudo, observamos que todos os grupos provocaram algum grau de reação inflamatória, entretanto, o grupo D-GDA foi o que teve a resposta mais atenuada. Resultados semelhantes foram reportados por Gonçalves et al. [16], que demonstraram que a remoção das células elimina antígenos presentes nas membranas, reduzindo a reação inflamatória de corpo estranho do heteroenxerto. Wang et al. [6] utilizaram o ácido tânico, reduzindo a reação inflamatória, com conseqüente redução na calcificação em pericárdios bovinos. Em nossos resultados com o ácido glutâmico, observamos que a reação inflamatória foi semelhante ao do grupo controle. Além disso, a adição do tratamento com ácido glutâmico aos pericárdios descelularizados (D-GDA-GL) desencadeou resposta inflamatória mais acentuada do que nos pericárdios apenas descelularizados (D-GDA). A explicação para esse achado não é aparente, mas postulamos que o pH ácido desse tratamento possa de alguma forma lesar a estrutura das fibras da matriz extracelular, levando a maior intensidade na reação inflamatória.
Pela coloração de alizarina red, nos pHs de 4,2 e 7,0, pudemos observar que a calcificação teve correlação direta com a intensidade da reação inflamatória. Os pericárdios dos grupos GDA e GDA-GL desenvolveram intensa calcificação progressiva que ocupava toda a porção central do tecido, enquanto que os pericárdios descelularizados se mostraram livres de calcificação, mesmo após 90 dias de evolução. Apesar dos resultados no grupo D-GDA-GL serem semelhantes aos do grupo D-GDA aos 45 dias, subsequentemente pudemos observar alguns pontos focais de calcificação aos 90 dias, demonstrando que não houve sinergismo nas ações anticalcificantes da descelularização com o ácido glutâmico.
A mensuração quantitativa da quantidade de cálcio confirmou nossa análise morfométrica. O tratamento com ácido glutâmico reduziu a quantidade de cálcio em relação ao grupo controle, o que já havia sido documentado por Ferreira et al. [12]. Por outro lado, no estudo de Jorge-Herrero et al. [8], o ácido glutâmico não teve a mesma efetividade e, paradoxalmente, os pericárdios tratados tiveram comportamento ainda piores que o grupo controle. Os resultados discrepantes desses estudos podem, pelo menos parcialmente, ser explicados pelas diferentes metodologias no uso do ácido glutâmico, tais como a concentração, pH e temperatura de exposição do tecido.
A efetividade da descelularizacão como método anticalcificante em pericárdios bovinos fixados em GDA pode ser claramente demonstrada pela quantidade insignificante de cálcio encontrada aos 45 dias (1,06 µg/mg de tecido) e que se manteve estável em até 90 dias de evolução (1,24 µg/mg de tecido), sendo esses valores significativamente menores do que os encontrados nos demais grupos. Conforme já evidenciado pelas análises histológicas, o pós-tratamento com ácido glutâmico em pericárdios descelularizados não teve sinergismo como método anticalcificante. Ao contrário, apesar dos valores de cálcio terem sido semelhantes nos grupos D-GDA e DGDA-GL aos 45 dias de evolução, a observação mais prolongada por 90 dias demonstrou aumento significativo de cálcio no grupo D-GDA-GL. Conforme demonstrado por Jorge-Herrero et al. [8], o ácido glutâmico apresenta ligação instável com os aldeídos residuais do GDA, que se desfazem com o decorrer do tempo, o que favoreceria a formação de cristais de cálcio numa fase mais tardia. A explicação pelo eventual efeito deletério do ácido glutâmico nessa situação ainda precisa ser melhor compreendida.
Costa et al. [13] já demonstraram, experimentalmente, a eficiência da descelularização como método anticalcificante em pericárdios bovinos. Neste estudo, a descelularização de pericárdios bovinos com a utilização de uma solução alcalina impediu a calcificação em até 90 dias. Na metodologia de Shen et al. [7] com a associação de etanol, éter e detergente tween 80, os níveis de cálcio foram de 13,1 ìg/mg de tecido em 180 dias em ratos. Em nosso estudo, a quantidade de cálcio encontrada nos pericárdios descelularizados foi baixa, havendo redução de 65 µg/mg de tecido no grupo controle para 1,24 µg/mg de tecido nos pericárdios tratados aos 90 dias de evolução. Apesar dos resultados não poderem ser diretamente comparados em decorrência de diferenças nas metodologias e tempos variados de observação, a redução na quantidade de cálcio tem sido um denominador comum nesses estudos. Além disso, a eficiência do uso de detergentes como o SDS como método anticalcificante em tecido heterólogo já pode ser comprovada clinicamente em explantes realizados de próteses Hancock II. Em estudo de Bottio et al. [17], a remoção de fosfolipídeos pelo SDS resultou em níveis de apenas 14,70 mg de cálcio/g de tecido em próteses sem degeneração estrutural explantadas de humanos versus 99 mg de cálcio/g de tecido em próteses com degeneração calcifica após uma média de 94 meses de implante em humanos.
Outros métodos de anticalcificação, apesar de reduzirem a quantidade de cálcio, não foram tão efetivos quando comparados à descelularização. Wang et al. [6] observaram redução dos níveis de cálcio de 90 mg/g de tecido no grupo controle para 6,4 mg/g de tecido aos 21 dias de evolução com a utilização de ácido tânico. Já Pettenazzo et al. [9] demonstraram a efetividade do uso de octanediol, com redução dos níveis de cálcio de 165 µg/mg para 2,36 µg/mg aos 75 dias. Carpentier et al. [11], com tratamento com calor de 50ºC, reduziram os níveis de cálcio de 108 µg/mg de tecido para 19 µg/mg de tecido em implantes em ratos por 90 dias.
CONCLUSÃO
A descelularização de pericárdios bovinos com a solução de SDS 0,1% (Solução PUCPR) foi efetiva em reduzir a calcificação por até 90 dias em implantes subcutâneos de ratos. Não foi observada redução adicional na quantidade de cálcio pelo tratamento simultâneo com ácido glutâmico. Em decorrência desses resultados, recomendamos a confirmação da sua efetividade em modelo circulatório de grandes animais.
Artigo recebido em 3 de outubro de 2011
Artigo aprovado em 26 de janeiro de 2012
Trabalho realizado na Santa Casa de Misericórdia de Curitiba, Curitiba, PR, Brasil.
- 1. Carpentier A, Lemaigre G, Robert L, Carpentier S, Dubost C. Biological factors affecting long-term results of valvular heterografts. J Thorac Cardiovasc Surg. 1969;58(4):467-83.
- 2. Schoen FJ, Levy RJ, Hilbert SL, Bianco RW. Antimineralization treatments for bioprosthetic heart valves. Assessment of efficacy and safety. J Thorac Cardiovasc Surg. 1992;104(5):1285-8.
- 3. Schoen FJ, Levy RJ. Calcification of tissue heart valve substitutes: progress toward understanding and prevention. Ann Thorac Surg. 2005;79(3):1072-80.
- 4. Manji RA, Zhu LF, Nijjar NK, Rayner DC, Korbut GS, Churchill TA, et al. Glutaraldehyde-fixed bioprosthetic heart valve conduits calcify and fail from xenograft rejection. Circulation. 2006;114(4):318-27.
- 5. Gross JM. Calcification of bioprosthetic heart valves and its assessment. J Thorac Cardiovasc Surg. 2001;121(3):428-30.
- 6. Wang D, Jiang H, Li J, Zhou JY, Hu SS. Mitigated calcification of glutaraldehyde-fixed bovine pericardium by tannic acid in rats. Chin Med J (Engl). 2008;121(17):1675-9.
- 7. Shen M, Kara-Mostefa A, Chen L, Daudon M, Thevenin M, Lacour B, et al. Effect of ethanol and ether in the prevention of calcification of bioprostheses. Ann Thorac Surg. 2001;71(5 Suppl):S413-6.
- 8. Jorge-Herrero E, Fernández P, Escudero C, García-Páez JM, Castillo-Olivares JL. Calcification of pericardial tissue pretreated with different amino acids. Biomaterials. 1996;17(6):571-5.
- 9. Pettenazzo E, Valente M, Thiene G. Octanediol treatment of glutaraldehyde fixed bovine pericardium: evidence of anticalcification efficacy in the subcutaneous rat model. Eur J Cardiothorac Surg. 2008;34(2):418-22.
- 10. Sardeto EA, Costa FDA, Costa ISEA, Roderjan JG, Discher E, Scheneider RA, et al. Eficácia do AlCl3 e etanol na prevenção da calcificação de fragmentos da parede aórtica porcina fixados em GDA. Rev Bras Cir Cardiovasc. 2006;21(4):409-17.
- 11. Carpentier SM, Chen L, Shen M, Fornes P, Martinet B, Quintero LJ, et al. Heat treatment mitigates calcification of valvular bioprosteses. Ann Thorac Surg. 1998;66(6 Suppl):S264-6.
- 12. Ferreira ADA, Costa FDA, Santos EAA, Sardeto EA, Gomes CHGG, Collatusso C, et al. Ácido L-glutâmico na prevenção da calcificação de pericárdio bovino fixado em glutaraldeído: estudo em ratos. Rev Bras Cir Cardiovasc. 2007;22(3):303-9.
- 13. Costa JNL, Pomerantzeff PMA, Braile DM, Ramirez VA, Goissis G, Stolf NAG. Comparação entre o pericárdio bovino decelularizado e o pericárdio bovino convencional utilizado na confecção de biopróteses valvares cardíacas. Rev Bras Cir Cardiovasc. 2005;20(1):14-22.
- 14. Gilbert TW, Sellaro TL, Badylak SF. Decellularization of tissues and organs. Biomaterials. 2006;27(19):3675-83.
- 15. Oswal D, Korossis S, Mirsadraee S, Wilcox H, Watterson K, Fisher J, et al. Biomechanical characterization of decellularized and cross-linked bovine pericardium. J Heart Valve Dis. 2007;16(2):165-74.
- 16. Gonçalves AC, Griffiths LG, Anthony RV, Orton EC. Decellularization of bovine pericardium for tissue-engineering by targeted removal of xenoantigens. J Heart Valve Dis. 2005;14(2):212-7.
- 17. Bottio T, Thiene G, Pettenazzo E, Ius P, Bortolotti U, Rizzoli G, et al. Hancock II bioprosthesis: a glance at the microscope in mild-long-term explants. J Thorac Cardiovasc Surg. 2003;126(1):99-105.
- 18. Costa FDA, Dohmen P, Vieira ED, Lopes SV, Collatusso C, Pereira EWL, et al. Operação de Ross com homoenxertos valvares descelularizados: resultados de médio prazo. Rev Bras Cir Cardiovasc. 2007;22(4):454-62.
- 19. Costa FD, Costa AC, Prestes R, Domanski AC, Balbi EM, Ferreira AD, et al. The early e midterm function of decellularized aortic valve allografts. Ann Thorac Surg. 2010;90(6):1854-60.
- 20. Maizato MJ, Pires MD, Canzian M, Higa OZ, Pitombo RN, Leirner AA. Histological evaluation of biocompatibility of lyophilized bovine pericardium implanted subcutaneously in rats. Artif Organs. 2008;32(4):268-71.
Endereço para correspondência:
Datas de Publicação
-
Publicação nesta coleção
19 Jun 2012 -
Data do Fascículo
Mar 2012
Histórico
-
Recebido
03 Out 2011 -
Aceito
26 Jan 2012