Resumos
O objetivo da pesquisa é a utilização da hidroxiapatita porosa de coral, como um xenoenxerto ósseo. Utilizou-se onze coelhos da raça Nova Zelândia, nos quais fez-se defeito padrão nas metáfises femorais distais. Nesses locais praticou-se o implante de hidroxiapatita porosa de coral ou enxerto ósseo autógeno. Fez-se estudo clínico, macroscópico, exames radiológicos e histológicos em intervalos de duas, quatro e doze semanas. Os resultados comparativos foram similares enter dois tipos de implantes. Concluiu-se que a hidroxiapatita porosa de coral é um substituto adequado para enxertos ósseos autógenos em coelhos.
Osso; Hidroxiapatita; Transplante homógeno; Transplante heterógeno; Coelho
The purpose is to utilize coralline porous hydroxyapatite as osseous xenograft. It was utilized eleven New Zeland rabbits, wich it made pattern defect in the distal femoral mataphise. In this place was used coralline porous hidroxyapatite or autogenous graft. It was made clinical, macroscopic, radiologic and histologic study, with interval of two, four and twelve weeks. The comparatives results was similaries between the two implants types. It was concluded taht coralline porous hidroxyapatite is appropriate replacement for osseos autogenous grafts in rabbits.
Bone; Hydroxyapatites; Homogenous transplantation; Heterogenous transplantation; Rabbits
2 NOTA PRELIMINAR
Comparação entre a hidroxiapatita porosa de coral e o enxerto ósseo autógeno em coelhos1 1 Trabalho realizado na Disciplina de Técnica Operatória e Cirurgia Experimental da Universidade Federal do Mato Gosso do Sul (UFMS). * Goniopora (família); Porites (gênero).
Comparison between coralline porus hidroxyapatite and osseous xenograft in rabbits
Arthur Silveira de FigueiredoI; Luiz Carlos TakitaII; Saul GoldenbergIII
IProfessor Adjunto IV da Disciplina de Ortopedia de Traumatologia da UFMS
IIProfessor Assistente da Disciplina de Patologia da UFMS
IIIProfessor Titular da Disciplina de Técnica Operatória e Cirurgia Experimental da Universidade Federal de São Paulo - Escola Paulista de Medicina
Endereço para correspondência Endereço para correspondência: Arthur Silveira de Figueiredo Avenida Mato Grosso 1022 Fax: (067) 383-1133 ou (067) 383-1662 Telefone: 721-0453 Rua Barão do Rio Branco 2167 (consultório) Campo Grande - MS - CEP-79100
RESUMO
O objetivo da pesquisa é a utilização da hidroxiapatita porosa de coral, como um xenoenxerto ósseo. Utilizou-se onze coelhos da raça Nova Zelândia, nos quais fez-se defeito padrão nas metáfises femorais distais. Nesses locais praticou-se o implante de hidroxiapatita porosa de coral ou enxerto ósseo autógeno. Fez-se estudo clínico, macroscópico, exames radiológicos e histológicos em intervalos de duas, quatro e doze semanas. Os resultados comparativos foram similares enter dois tipos de implantes. Concluiu-se que a hidroxiapatita porosa de coral é um substituto adequado para enxertos ósseos autógenos em coelhos.
Descritores: Osso. Hidroxiapatita. Transplante homógeno. Transplante heterógeno. Coelho.
SUMMARY
The purpose is to utilize coralline porous hydroxyapatite as osseous xenograft. It was utilized eleven New Zeland rabbits, wich it made pattern defect in the distal femoral mataphise. In this place was used coralline porous hidroxyapatite or autogenous graft. It was made clinical, macroscopic, radiologic and histologic study, with interval of two, four and twelve weeks. The comparatives results was similaries between the two implants types. It was concluded taht coralline porous hidroxyapatite is appropriate replacement for osseos autogenous grafts in rabbits.
Subject headings: Bone. Hydroxyapatites. Homogenous transplantation. Heterogenous transplantation. Rabbits.
INTRODUÇÃO
A reparação óssea é um processo fisiológico no qual a regeneração é identica a do tecido primário. Quando essa reparação não se concretiza por alguma razão como, por exemplo, nos tumores, nas fraturas com perda de substância óssea, nas pseudartroses e nos cistos ósseos, utilizam-se recursos para alcançá-lo. NADE12 descreveu os princípios da enxertia óssea nessas lesões. Mostrou osso neoformado pelo crescimento vascular e celular dos músculos circundantes, periósteo e extremidades ósseas.
Transplantes ósseos foram estudados por BUCHOLZ3, URIST e col.20, De BÖER4, DUPOIREUX5 e EGGERS e col.6 confirmando que o osso autógeno permanece como o melhor material para enxertia.
Muitos substitutos ósseos têm sido propostos com a finalidade de diminuir a morbidade do sítio doador e o tempo operatório22.
URIST20 fez relato preliminar sobre a utilização experimental de osso desmineralizado como substituto do enxerto ósseo autógeno. FRIEDLANDER8 popularizou a idéia do banco de ossos para se manter armazenados ossos em estado de conservação. Introduziu também a nova técnica de enxerto fibular livre com a conservação de seu pedículo vascular, cujos vasos são anastomosados aos vasos do sítio receptor, mediante microcirurgia.
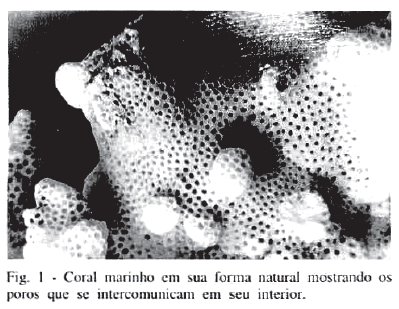
A escleratina do exoesqueleto de corais marinhos (Fig. 1) Porites e Goniopora* 1 Trabalho realizado na Disciplina de Técnica Operatória e Cirurgia Experimental da Universidade Federal do Mato Gosso do Sul (UFMS). * Goniopora (família); Porites (gênero). , possui uma microestrutura tridimensional semelhante à do osso esponjoso humano, e foi convertida por métodos hidrotérmicos17 em hidroxiapatita pura, e proposta como uma alternativa à enxertia autógena em defeitos ósseos20. O coral replicado apresenta poros com tamanho médio de 600mm e poros de interconexão com diâmetro médio de 260 mµ9,15,19,21.
A estrutura morfológica dos poro e suas interconexões com tamanho, forma e uniformidade são apropriados para o crescimento e a fixação dos tecidos corporais receptores12.
O tamanho e forma dos implantes de hidroxiapatita porosa de coral foram estudados e avaliados radiologicamente por SARAF e Col.17, mostrando que os mesmos não influem significantemente no resultado final.
Qualitativamente, avaliações radiográficas permitem uma diferenciação significativa entre a hidroxiapatita porosa de coral e os enxertos autógenos. A hidroxiapatita porosa de coral tem persistência indefinida integrada ao osso formado, como que um arcabouço, sem ser reabsorvida significativamente ou sem sofrer remodelação completa dentro do osso neoformado19.
O coral Porites é encontrado na natureza, no Oeste da Índia e costas do Pacífico com recifes que alcançam um metro de diâmetro e por isso com suprimento virtual ilimitado. WHITE e SHORS21 destacaram as vantagens de hidroxiapatita porosa de coral como biocompatível, biodegradável, não alérgena e não tóxica. Possui alta resistência compressiva e contém poros de tamanho adequado para a invasão fibrovascular e neoformação óssea11,13,14.
O objetivo deste estudo experimental é o de verificar a integração da hidroxiapatita porosa de coral como implante ósseo.
MÉTODO
Onze coelhos machos, da raça Nova Zelândia, com peso entre 2.000 e 3.000 gramas (g) tiveram suas metáfises femorais operadas, com uma trefina circular de seis milímetros de diâmetro, para produção de defeito ósseo padrão. Os defeitos ósseos foram aleatoriamente preenchidos com enxerto ósseo autógeno, de um lado, e implante de hidroxiapatita porosa de coral, do outro. A hidroxiapatita porosa de coral utilizada foi o INTERPORE 500â** ** Interpore International, Irvine, CA, USA em blocos retangulares, que foram modelados com cisalha, de acordo com o formato do defeito padrão e esterilizados no óxido de etileno (Fig. 2).
Técnica operatória
Os animais receberam como medicação pré-anestésica 0,1 mililitro (ml) por quilograma (kg) de acepromazina 10 miligramas (mg) por ml e medicação anestésica xilazina 10 mg/kg e quetamina 25 mg/kg, todas por via intramuscular. Os membros inferiores foram depilados e submetidos e anti-sepsia com solução de álcool iodado 2%. Em condições assépticas, foi realizada uma incisão cutânea retilínea na face lateral do terço distal do fêmur, na cabeça pélvica do músculo bíceps femoral longitudinalmente às suas fibras e no periósteo com deslocamento do mesmo, ressecção de um cilindro ósseo com trefina de 6 mm de diâmetro, interessando a cortical externa e a medualr, com 1cm de profundidade. Em um dos lados, o cilindro ósseo foi recolocado e no outro, o defeito criado foi preenchido com hidroxiapatita porosa de coral, impactada digitalmente. Os planos internos foram fechados com fio categute 3 zeros e a pele com fio de mononylon 4 zeros. Antibioticoterapia com tetraciclina, em dose única de 20 mg/kg de peso foi efetuada por via intramuscular, no pós-operatório imediato, em todos os animais.
Após recuperação anestésica os animais foram confinados em gaiolas metálicas, com dieta livre para ração peletizada e água e o apoio dos membros foi imediatamente permitido.
RESULTADOS
Todos os tecidos incisados cicatrizaram e a movimentação dos animais assumiu a aparência habitual em poucos dias. As radiografias pós-operatórias não mostraram deslocamento dos enxertos e um dos animais apresentou fratura femoral distal com duas semanas de evolução.
Observação clínica
O consumo alimentar e a região operada foram observados rotineiramente em intervalos de setenta e duas horas, sem nenhuma alteração significante. Não foram observados sinais clínicos de processo infeccioso.
Observação radiológica
Radiografias em posicionamentos crânio-caudal e látero-lateral dos ossos femorais foram obtidas em intervalos de duas, quatro e doze semanas. Por possuir uma estrutura cálcica-carbonada, a hidroxiapatita porosa de coral tem aspecto radiológico de osso cortical. Com duas semanas havia aumento da linha de interface entre o enxerto e o osso esponjoso, tanto no enxerto autógeno como no implante de hidroxiapatita porosa de coral. Com quatro semanas o enxerto autógeno apresentava densidade semelhante à do osso hospedeiro com diminuição da radiotransparência na interface. Os implantes de hidroxiapatita porosa de coral mantinham sua densidade radiológica inicial. Com doze semanas havia desaparecimento da linha de interface, aspecto homogêneo nos autoenxertos ósseos e ainda, maior densidade radiológica no implante de hidroxiapatita porosa de coral, caracterizando completa integração do enxerto (Figuras 3 e 4).
Eutanásia
Com duas, quatro e doze semanas, os animais receberam anestesia similar à do ato operatório seguida de injeção intravenosa de pentobarbital sódico, na dose de 60mg/kg. Ambos membors inferiores foram desarticulados no quadril, submetidos a avaliação radiológica. O fêmur e a tíbia foram desarticulados por secção dos tecidos moles conectores. Com dissecção cuidadosa, a área enxertada foi exposta e submetida a observação macroscópica, sendo então, imersas em frascos herméticos, individuais, com formol tamponado 10%.
Observação macroscópica
Em nenhuma das observações os enxertos mostraram sinais de infecção ou encapsulação por tecido fibroso. O estudo macroscópico com duas semanas mostrou mobilidade à manipulação tanto no enxerto autógeno como no implante de hidroxiapatita porosa de coral. O animal que tinha fratura da diáfase femoral distal mostrava o enxerto com aspecto compacto, aderido aos fragmentos ósseos metafisários. Com quatro semanas, os enxertos autógenos e os implantes de hidroxiapatita porosa de coral apresentavam resistência à tentativa de mobilização digital na mesma proporção. Com doze semanas, havia fixação tanto dos enxertos autógenos como dos implantes de hidroxiapatita porosa de coral, com incorporação dos mesmos, sendo impossível sua remoção manual.
Observação Microscópica
Foram realizados exames histológicos com duas, quatro e doze semanas comparando os enxertos autógenos e os implantes de hidroxiapatita porosa de coral. Das peças ósseas foram confeccionadas vinte e duas lâmnias, coradas com hematoxilina e eosina. Com duas semanas o tecido mostrava grande quantidade de conjuntivo altamente vascularizado, entremeando a zona de contato do osso receptor e do autoenxerto. Havia invasão praticamente completa dos poros da hidroxiapatita porosa de coral por tecido conjuntivo ricamente vascularizado. Com quatro semanas, o enxerto autógeno, na zona periférica, onde havia maior contato com o osso esponjoso normal, mostrava tecido fibroso e invasão celular no enxerto (Fig. 5). Na lâmnia do implante de hidroxiapatita porosa de coral verificou-se o arcabouço estrutural calcificado, corado em roxo, e os poros em suas várias posições contendo neoformação óssea com presença de colunas de osteoblastos (Fig. 6 e 7). Com doze semanas mantinha-se o arcabouço calcificado da hidroxiapatita porosa de coral, entremeado de osso maduro em quantidade superior ao imaturo, confirmando a cicatrização óssea, tanto nas áreas que receberam como nas áreas de hidroxiapatita porosa de coral.
DISCUSSÃO
Para recuperação das lesões ósseas decorrentes de fraturas, de doenças congênitas ou de tumores ósseos, os transplantes ósseos são realizados em animais como autoenxerto ou xenoenxerto (De BÖER).
Existem numerosos relatos de sucesso na integração de implantes de hidroxiapatita porosa de coral por teciso ósseo normal (ABDELL-FATTAH e col1., ALLEN e col.2, BUCHOLZ e col.3, FINN e col.7, SARAF e col.17) em falhas produzidas experimentalmente. KÜHNE e col.10, determinaram o tamanho médio dos poros da hidroxiapatita, em 500mm produziam uma invasão fibroplástica e vascular mais precoce apesar de sua menor resistência mecânica quando comparada à hidroxiapatita com poros de 200mm de diâmetro. PIECUCH e col.13,14 mostrou que essa resistência diminuída, inicialmente presente no implante, era eliminada quando o arcabouço do mesmo era invadido por tecido ósseo neoformado16.
Este estudo preliminar corrobora a afirmação de HOLMES e col.9 de que uma estrutura biocompatível, com finalidade de arcabouço ao crecimento ósseo e de conformidade morfológica ao defeito ósseo, quando implantada em área esponjosa, pode produzir resultados semelhantes aos obtidos com autoenxertia óssea3.
Apesar dos resultados promissores obtidos neste estudo peliminar, é necessário um estudo experimental com uma amostra mais ampla de animais, para que a utilização de um xenoenxerto, à semelhança de hidroxiapatita porosa de coral, bocompatível, inerte, atóxico, de baixo custo, permeável à antibióticos e que não produza reações imunológicas indesejáveis, possa ser realizada em seres humanos diminuindo a morbidade dos procedimentos operatórios de autoenxertia.
CONCLUSÃO
A hidroxiapatita porosa de coral integra-se ao osso hospedeiro de modo semelhante ao osso autógeno.
Data do recebimento: 02.01.97
Data da revisão:05.02.97
Data da aprovação: 07.03.97
- 1. ABDEL-FATTAH, W.I.; OSIRIS, W.G.; MOHAMED, S.S.; KHALIL, M.R. - Reconstruction of resected mandibles using a hydroxiapatite veterinary bone graft. Biomaterials, 15:609-14, 1994.
- 2. ALLEN, M.; BRETT, F.; MILLETT, P.; RUSHTON, N. - The efects of particulate polyethylene at a weight-bearing bone-implant interface: a study in rats. J. Bone Joint Surg., 78B:32-6, 1996.
- 3. BUCHOLZ, R.W.; CARLTON, A.; HOLMES, R. - Interporus hydroxyapatite as a bone graft substitute in tibial plateau fractures. Clin. Orthop. Rel. Res, 240:53-62, 1980.
- 4. DE BOER, H.H. - The history of bone grafts. Clin. Orthop. Rel. Res, 226:292-8, 1988.
- 5. DUPOIRILEUX, L.; COSTES, V.; JAMMET, P,; SOUYRIS, F. - Experimental study on demineralized bone matrix (DBM) and coral as bone graft substitutes in maxillofacial surgery. Int. J. Oral Maxillofac. Surg., 23:395-8, 1994.
- 6. EGGERS, C.; MEEDER, P.J. - Biological principles of aurogenous bone grafting. Injury, 25 (Sup.1):A17-20, 1994.
- 7. FINN, R.A.; BELL, W.H.; BRAMMER, J.A. - Interpositional "grafting" with autogenous bone and coralline hydroxiapatite. J. Max-Fac. Surg, 8:217-27, 1980.
- 8. FRIEDLAENDER, G.E. - Current concepts review bone-banking. J. Bone Joint Surg, 64-A:307-11, 1982.
- 9. HOLMES, R.E.; BUCHOLZ, R.W.; MOONEY, V. - Porous hydroxyapatite as a bone graft substitute in methaphyseal defects: a histometric study. J. Foot Surg., 30:472-6, 1991.
- 10. KÜHNE, J.H.; BARTL, R.; FRISCH, B.; HAMMER, C.; JANSSON, V.; ZIMMER, M. - Bone formation in coralline hydroxyapatite: effects of pore size studied in rabbits. Acta Orthop. Scand, 65:246-52, 1994.
- 11. LIGHT, M.; KANAT, I.O. - The possible use of coralline hydroxyapatite as a bone implant. J. Foot Surg., 30:472-6, 1991.
- 12. NADE, S. - Stimmulating osteogenesis. Injury, 25:577-583, 1994.
- 13. PIECUCH, J.F.; TOPAZIAN, R.G.; SKOLY, S.; WOLFE, S. - Experimental ridge augmentation with porous hydroxyapatite implants. J. Dent. Res., 62:148-54, 1983.
- 14. PIECUCH, J.F.; GOLDENBERG, J.F.; GOLDENBERG, A.J.; SHASTRY, C.V.; CHRZANOWSKI, R.B. - Compressive strength if implanted porous replamineform hydroxyapatite. J. Biomed. Mater. Res, 18:39-45, 1984.
- 15. RIPAMONTI, U. - The morphogenesis of bone in replicas of porous hydroxyapatite obtained from conversion of calcium carbonate exoeskeletons of coral. J. Bone Joint Surg., 73-A:692-703, 1991.
- 16. ROY, D.M.; LINNEHAN, S.K. - hydroxyapatite formed from coral skeletal carbonate by hydrotermal exchange. Nature, 247:220-1, 1974.
- 17. SARAF, S.K.; KUMAR, A.; TULI, S.M.; KHANNA, S. - Effect of size and shape of the allogeneic bone grafts is bridging experimental ulnar gap in rabbits. Indian J. Exper. Biol, 32:690-3, 1994.
- 18. SARTORIS. D.J.; HOLMES, R.E.; TENCER, A.F.; MOONEY, V.; RESNICK, D. - Coralline hydroxyapatite bone graft substitutes in a canine metaphyseal defect model: radiographic-biomechanical correlation. Skeletal radiol., 15:635-41, 1986.
- 19. SARTORIS, D.J. GERSHUNI, D.H.; AKESON, W.H.; HOLMES, R.E.; RESNICK, D. - Coralline hydroxyapatite bone graft substitutes: preliminary report os radiographic evaluation. Radiology, 159:133-7, 1986.
- 20. URIST, M.R.; STRATES, B.S. - Bone morphogenetic protein. J. Dent. Res., 50 (Supl.6):1392-406, 1971.
- 21. WHITE, R.A.; WHITE, E.W.; HANSON, E.L.; ROHNER, R.F.; WEBB, W.R. - Evaluation of tissue ingrowth into experimental replamineform vascular protheses: preliminary report. Surgery, 79:229-32, 1976.
- 22. YOUNGER, E.M.; CHAPMAN, M.W. - Morbility at bone graft donor sites. J. Orthop. Trauma, 3:192-5, 1989.
Datas de Publicação
-
Publicação nesta coleção
19 Nov 2010 -
Data do Fascículo
Jun 1997
Histórico
-
Aceito
07 Mar 1997 -
Revisado
05 Fev 1997 -
Recebido
02 Jan 1997