Resumos
A transplantação de osso autógeno continua sendo usada com sucesso, apesar das limitações que apresenta, principalmente no que se refere à morbidade aumentada, operações adicionais e aumento do custo. O objetivo desta pesquisa foi verificar a integração da hidroxiapatita porosa de coral como alternativa biológica, em forma de cerâmica, para substituir o enxerto ósseo autógeno. Foram utilizados 42 coelhos albinos (Nova Zelândia), submetidos a defeito padrão em 84 côndilos femorais, e implantação aleatória, em cada lado, de enxerto ósseo autógeno ou hidroxiapatita porosa. Foram avaliados os aspectos da evolução clínica diária dos animais. Após duas, quatro e doze semanas, grupos de 14 animais foram sacrificados e feita a avaliação radiológica e macroscópica da integração dos enxertos. Peças das regiões operadas foram colhidas para estudo histológico dessa integração. Os resultados macroscópicos mostraram que a integridade óssea, coloração, cicatrização da cortical e mobilidade dos implantes não foram estatisticamente significantes para os dois tipos de enxertos, nos diferentes tempos de observação. A diferença de uma progressiva e melhor integração dos enxertos ocorreu apenas quando se compararam os três tempos de observação, e foi considerada como conseqüência direta da evolução natural do processo cicatricial. Os parâmetros radiológicos de integração seguiram o mesmo padrão dos achados macroscópicos. Os achados microscópicos mostraram que o aparecimento de tecido ósseo maduro é retardado nos enxertos de hidroxiapatita com a ocorrência de cavidades císticas. Concluiu-se que a hidroxiapatita porosa de coral foi um substituto adequado ao enxerto ósseo autógeno em coelhos.
Hidroxiapatita; Osso; Transplante autógeno; Coelho
The transplantation of autogenous bone continues being used with success, in spite of the disadvantages that it presents, mainly in what refers the increased morbidity, additional operations and increase of the cost. The objective of this research was to verify the integration of the porous hydroxyapatite of chorale as biological alternative in ceramic form to substitute the autogenous bony graft. Forty-two New Zealand rabbits were submitted to na standard condylar defect witch were randomic implanted by autogenous bony graft as porous hydroxyapatite of chorale. We made clinical, macroscopic, radiographic and histologic study among the time of evolution of two, four and twelve weeks, respectively. The results were similar between the autogenous graft and the porous hydroxyapatite of chorale in the evolution of twelve weeks. It was ended that the porous hydroxyapatite of chorale is a substitute adapted to the autogenous bony graft in rabbits.
Hydroxyapatite; Bone; Autograft; Rabbit
9 - ARTIGO ORIGINAL
COMPARAÇÃO ENTRE HIDROXIAPATITA POROSA DE CORAL E ENXERTO ÓSSEO AUTÓGENO EM COELHOS1 1 Resumo da tese de mestrado apresentado na Disciplina de Técnica Operatória e Cirurgia Experimental da Universidade Federal de São Paulo, São Paulo. 2 Professor Adjunto IV da Disciplina de Ortopedia e Traumatologia da Universidade Federal de Mato Grosso do Sul, Campo Grande. 3 Coordenador do Programa de Pós-Graduação em Técnica Operatória e Cirurgia Experimental da Universidade Federal de São Paulo, São Paulo. 4 Professor Titular da Disciplina de Bioestatística da Universidade Federal de São Paulo, São Paulo. 5 Professor Adjunto da Disciplina de Bioestatística da Universidade Federal de São Paulo São Paulo. 6 Professor Titular do Departamento de Clínica Cirúrgica da Universidade Federal de Mato Grosso do Sul, Campo Grande.
Arthur Silveira de Figueiredo2 1 Resumo da tese de mestrado apresentado na Disciplina de Técnica Operatória e Cirurgia Experimental da Universidade Federal de São Paulo, São Paulo. 2 Professor Adjunto IV da Disciplina de Ortopedia e Traumatologia da Universidade Federal de Mato Grosso do Sul, Campo Grande. 3 Coordenador do Programa de Pós-Graduação em Técnica Operatória e Cirurgia Experimental da Universidade Federal de São Paulo, São Paulo. 4 Professor Titular da Disciplina de Bioestatística da Universidade Federal de São Paulo, São Paulo. 5 Professor Adjunto da Disciplina de Bioestatística da Universidade Federal de São Paulo São Paulo. 6 Professor Titular do Departamento de Clínica Cirúrgica da Universidade Federal de Mato Grosso do Sul, Campo Grande.
Djalma José Fagundes3 1 Resumo da tese de mestrado apresentado na Disciplina de Técnica Operatória e Cirurgia Experimental da Universidade Federal de São Paulo, São Paulo. 2 Professor Adjunto IV da Disciplina de Ortopedia e Traumatologia da Universidade Federal de Mato Grosso do Sul, Campo Grande. 3 Coordenador do Programa de Pós-Graduação em Técnica Operatória e Cirurgia Experimental da Universidade Federal de São Paulo, São Paulo. 4 Professor Titular da Disciplina de Bioestatística da Universidade Federal de São Paulo, São Paulo. 5 Professor Adjunto da Disciplina de Bioestatística da Universidade Federal de São Paulo São Paulo. 6 Professor Titular do Departamento de Clínica Cirúrgica da Universidade Federal de Mato Grosso do Sul, Campo Grande.
Neil Ferreira Novo4 1 Resumo da tese de mestrado apresentado na Disciplina de Técnica Operatória e Cirurgia Experimental da Universidade Federal de São Paulo, São Paulo. 2 Professor Adjunto IV da Disciplina de Ortopedia e Traumatologia da Universidade Federal de Mato Grosso do Sul, Campo Grande. 3 Coordenador do Programa de Pós-Graduação em Técnica Operatória e Cirurgia Experimental da Universidade Federal de São Paulo, São Paulo. 4 Professor Titular da Disciplina de Bioestatística da Universidade Federal de São Paulo, São Paulo. 5 Professor Adjunto da Disciplina de Bioestatística da Universidade Federal de São Paulo São Paulo. 6 Professor Titular do Departamento de Clínica Cirúrgica da Universidade Federal de Mato Grosso do Sul, Campo Grande.
Yara Juliano5 1 Resumo da tese de mestrado apresentado na Disciplina de Técnica Operatória e Cirurgia Experimental da Universidade Federal de São Paulo, São Paulo. 2 Professor Adjunto IV da Disciplina de Ortopedia e Traumatologia da Universidade Federal de Mato Grosso do Sul, Campo Grande. 3 Coordenador do Programa de Pós-Graduação em Técnica Operatória e Cirurgia Experimental da Universidade Federal de São Paulo, São Paulo. 4 Professor Titular da Disciplina de Bioestatística da Universidade Federal de São Paulo, São Paulo. 5 Professor Adjunto da Disciplina de Bioestatística da Universidade Federal de São Paulo São Paulo. 6 Professor Titular do Departamento de Clínica Cirúrgica da Universidade Federal de Mato Grosso do Sul, Campo Grande.
Celso Massaschi Inouye6 1 Resumo da tese de mestrado apresentado na Disciplina de Técnica Operatória e Cirurgia Experimental da Universidade Federal de São Paulo, São Paulo. 2 Professor Adjunto IV da Disciplina de Ortopedia e Traumatologia da Universidade Federal de Mato Grosso do Sul, Campo Grande. 3 Coordenador do Programa de Pós-Graduação em Técnica Operatória e Cirurgia Experimental da Universidade Federal de São Paulo, São Paulo. 4 Professor Titular da Disciplina de Bioestatística da Universidade Federal de São Paulo, São Paulo. 5 Professor Adjunto da Disciplina de Bioestatística da Universidade Federal de São Paulo São Paulo. 6 Professor Titular do Departamento de Clínica Cirúrgica da Universidade Federal de Mato Grosso do Sul, Campo Grande.
Figueiredo AS, Fagundes DJ, Novo NF, Juliano Y, Inouye CM. Comparação entre hidroxiapatita porosa de coral e enxerto ósseo autógeno em coelhos. Acta Cir Bras [serial online] 2001 Jul-Set;16(3). Disponível em: URL: http://www.scielo.br/acb.
RESUMO: A transplantação de osso autógeno continua sendo usada com sucesso, apesar das limitações que apresenta, principalmente no que se refere à morbidade aumentada, operações adicionais e aumento do custo. O objetivo desta pesquisa foi verificar a integração da hidroxiapatita porosa de coral como alternativa biológica, em forma de cerâmica, para substituir o enxerto ósseo autógeno. Foram utilizados 42 coelhos albinos (Nova Zelândia), submetidos a defeito padrão em 84 côndilos femorais, e implantação aleatória, em cada lado, de enxerto ósseo autógeno ou hidroxiapatita porosa. Foram avaliados os aspectos da evolução clínica diária dos animais. Após duas, quatro e doze semanas, grupos de 14 animais foram sacrificados e feita a avaliação radiológica e macroscópica da integração dos enxertos. Peças das regiões operadas foram colhidas para estudo histológico dessa integração. Os resultados macroscópicos mostraram que a integridade óssea, coloração, cicatrização da cortical e mobilidade dos implantes não foram estatisticamente significantes para os dois tipos de enxertos, nos diferentes tempos de observação. A diferença de uma progressiva e melhor integração dos enxertos ocorreu apenas quando se compararam os três tempos de observação, e foi considerada como conseqüência direta da evolução natural do processo cicatricial. Os parâmetros radiológicos de integração seguiram o mesmo padrão dos achados macroscópicos. Os achados microscópicos mostraram que o aparecimento de tecido ósseo maduro é retardado nos enxertos de hidroxiapatita com a ocorrência de cavidades císticas. Concluiu-se que a hidroxiapatita porosa de coral foi um substituto adequado ao enxerto ósseo autógeno em coelhos.
DESCRITORES: Hidroxiapatita. Osso. Transplante autógeno. Coelho.
INTRODUÇÃO
A falta de reserva óssea adequada, como ocorre em pacientes de baixa estatura, de baixo peso e em crianças, constitui-se em grande obstáculo ao tratamento de deficiências ósseas1 .O enxerto ósseo autógeno é uma alternativa para essas situações, e mesmo para a enxertia óssea em pacientes com reserva óssea normal2.
A obtenção de enxerto ósseo autógeno produz morbidade adicional ao tratamento das lesões ósseas. Acrescenta-se ao procedimento principal um segundo procedimento sujeito a várias complicações inerentes à retirada operatória do enxerto3,4.
Tentando superar estes obstáculos, pesquisas foram dirigidas para a obtenção de um substituto adequado para o enxerto ósseo autógeno5. WEBER, WHITE e LEBIEDZIK6 foram os primeiros a usar o exoesqueleto de equinodermas, mantendo suas características estruturais de porosidade interconectada. WHITE, WEBER e WHITE7 descreveram o processo de "Replamineform" - replicação de um organismo vivo, que consiste na conversão química da estrutura mineral do coral marinho, em um biomaterial de implante, do tipo cerâmica, a hidroxiapatita porosa de coral.
UCHIDA, NADE, McCARTNEY e CHING8; SHIMAZAKI e MOONEY9; EGGLI, MÜLLER e SCHENK10, realizaram estudo experimental em coelhos implantando cerâmicas replicadas de coral marinho em defeito ósseo padrão, comprovando a integração óssea do implante.
KÜHNE, BARTL, FRISCH, HAMMER, JANSSON e ZIMMER11 estudaram radiológica e histologicamente os implantes de hidroxiapatita porosa de coral numa amostra de dezesseis coelhos. Os implantes foram realizados nos côndilos femorais e sem comparação com enxerto ósseo autógeno sendo o estudo foi dirigido para a reparação óssea de cavidades vazias, aloenxertos criopreservados, hidroxiapatita porosa de coral com poros de 200 e 500m m de diâmetro. Comprovaram que os poros de 500m m permitiam uma melhor integração óssea que os de 200m m.
WANG, GOODMAN e ASPENBERG12 estudaram experimentalmente se partículas fagocitáveis de hidroxiapatita promoviam efeito adverso no crescimento ósseo, em metáfises tibiais proximais de coelhos. Com seis semanas, partículas de hidroxiapatita estavam incorporadas dentro da nova matriz óssea e não havia nenhuma evidência de formação de granuloma ou inflamação.
A revisão bibliográfica não mostrou nenhum trabalho experimental publicado em nosso País ou na América Latina que comparasse a hidroxiapatita porosa de coral ao enxerto ósseo autógeno, em coelhos.
Considerando os aspectos expostos julgou-se pertinente o estudo comparativo experimental da hidroxiapatita porosa de coral e do enxerto ósseo autógeno em defeito padrão de côndilos femorais em coelhos.
MÉTODOS
Amostra
Quarenta e dois coelhos machos, albinos, da linhagem Nova Zelândia, com idade de 3 a 6 meses, peso entre 2.000 e 3.500g, provenientes do Biotério Central da Universidade Federal de Mato Grosso do Sul, foram distribuídos em três grupos, cada um com quatorze animais: Grupos I, II e III, com seguimentos de duas, quatro e doze semanas, respectivamente.
Procedimentos
Blocos quadrangulares de hidroxiapatita porosa replicada do coral marinho Goniopora, com microestrutura tridimensional semelhante à do osso esponjoso humano, com poros de diâmetro médio de 500mm e interconexão com diâmetro médio de 260mm , foram recortados com broca odontológica em cilindros de 6mm de diâmetro e 10mm de altura. Os cilindros foram vedados em embalagem plástica dupla, consecutivas, individuais, esterilizados por óxido de etileno e armazenados em temperatura ambiente até o momento do procedimento operatório.
Os coelhos foram privados de ração seis horas antes do ato operatório e pesados em balança de precisão. Receberam como medicação pré-anestésica 0,1mL.Kg-1 de acepromazina na concentração de 10mg.mL-1 por via intramuscular. Quinze minutos após, receberam como medicação anestésica 10mg.Kg-1 de xilazina na concentração de 20mg.mL-1 e 25mg.Kg-1 de quetamina na concentração de 50mg.mL-1, pela mesma via e local da medicação pré-anestésica.
Após epilação, os joelhos foram lavados com povidine tópico e solução salina e os coelhos foram instalados na mesa operatória em decúbito dorsal, com rotação cervical lateral para manter livre as vias aéreas. Foi feita anti-sepsia com solução de álcool iodado 2% em ambos membros inferiores e a colocação dos panos esterilizados, isolando-se os joelhos.
Luxação lateral da patela e manutenção da articulação do joelho em flexão pelo auxiliar para palpação da crista lateral da articulação fêmoro-patelar. Incisão da pele com 30mm, em posicionamento parapatelar lateral, distando 10mm da crista lateral previamente palpada. Afastamento da pele e tela subcutânea com dois afastadores em garra e identificação da borda anterior da cabeça pélvica do músculo bíceps femoral. Incisão seguindo o sentido longitudinal de suas fibras, abertura capsular e exposição da face lateral do côndilo femoral. Incisão do periósteo com descolamento delicado usando bisturi.
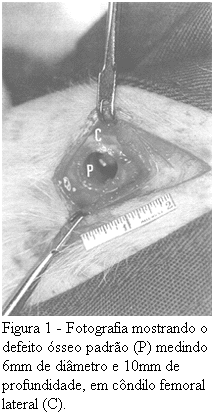
Distando 4mm da crista lateral da articulação fêmoro-patelar, procedeu-se a posição e acionamento de trefina metálica de 6mm de diâmetro interno (foram utilizadas duas trefinas: a primeira de torque manual e corte liso; a segunda com corte serrilhado, instalada em perfurador elétrico de baixa rotação), até que a cortical lateral fosse ultrapassada. Substituição da trefina e ressecção de um cilindro ósseo de 10mm de comprimento, composto da cortical lateral e da medular óssea, criando-se o defeito padrão (Figura 1).
De maneira aleatória, o defeito padrão de um dos lados recebeu o cilindro ósseo resseccionado e o do outro lado recebeu um cilindro de hidroxiapatita porosa de coral. Não foi utilizado nenhum tipo de síntese porque os cilindros possuíam as mesmas dimensões do defeito padrão e impactaram-se firmemente por pressão digital.
A cápsula articular, plano muscular e tela subcutânea foram suturados em plano único com pontos simples, separados, com fio de categute 3.0 e a pele com pontos simples, separados, com fio monofilamentado de náilon 4.0.
As feridas operatórias foram deixadas descobertas e os membros operados não receberam nenhum tipo de imobilização externa. Uma dose única de tetraciclina (0,2g.mL-1) na concentração de 20mg.Kg-1 foi aplicada por via intramuscular, como medicação pós-operatória.
Estando os animais ainda anestesiados, ambos fêmures foram submetidos a exposições radiológicas em posicionamento crânio-caudal e látero-lateral (a distância entre o tubo radiológico e a coxa do coelho foi de 90cm; exposição de 40kV, 12mA, tempo de 0,03s; filme Kodak® para revelador manual).
Para a recuperação anestésica, os coelhos foram devolvidos às suas gaiolas permanecendo envoltos pelos panos operatórios para evitar perda de calor corporal. Foi permitido aos coelhos ração e água à vontade e apoio imediato dos membros operados.
Os coelhos foram observados por um período de duas, quatro e doze semanas, e de acordo com a programação de eutanásia os coelhos receberam anestesia similar à do ato operatório, seguida de injeção intramuscular de pentobarbital sódico, na dose de 60mg.kg-1, promovendo eutanásia.
Ambos membros posteriores foram desarticulados no quadril e os fêmures dissecados. Os tecidos moles conectores com a tíbia seccionados e a área condilar do procedimento operatório foi observada em relação à integridade óssea (a presença de fratura femoral, mesmo consolidada, foi considerada como perda da integridade óssea); cicatrização do acesso operatório (a impossibilidade de identificação do acesso operatório na camada cortical foi considerada como cicatrização completa da camada cortical); coloração (a alteração da coloração nacarada usual do osso, foi considerada como pardacenta); e textura da cortical óssea (qualquer alteração da textura lisa usual da camada cortical foi considerada como rugosa). Por manipulação com pinça de dissecção anatômica, foi observada a presença ou ausência de mobilidade dos enxertos ósseos autógenos e dos implantes de hidroxiapatita porosa de coral.
Todos os fêmures foram submetidos a radiografias em posicionamentos crânio-caudal e látero-lateral.
A seguir, utilizando uma serra óssea, de lâmina oscilatória, os fêmures foram seccionados no plano coronal, em nível médio diafisário, com isolamento da região condilar e no plano sagital, em sentido longitudinal à diáfise óssea, tomando como referência a crista lateral da articulação fêmoro-patelar para observação da continuidade medular e definição da interface do enxerto-implante com o osso receptor. Quando a interface com o osso receptor não foi identificada, o enxerto-implante foi considerado macroscopicamente fixo. A presença de continuidade medular indicava uma integração macroscópica do enxerto-implante pelo osso receptor.
Para a análise radiológica foram realizadas radiografias em posicionamento crânio-caudal (Figura 2) e látero-lateral dos fêmures dos coelhos para observação dos seguintes parâmetros: desvio angular do eixo longitudinal femoral (a alteração do alinhamento femoral natural em varo foi considerado desvio em valgo); reconstituição medular (a continuidade da medular óssea do osso receptor com o enxerto-implante indicava integração radiológica); interface enxerto-implante com o osso receptor (a interface de menor densidade radiológica circundando o enxerto-implante indicava presença de tecido sem calcificação); consolidação óssea (a presença de tecido com densidade radiológica semelhante ao tecido ósseo receptor com desaparecimento parcial ou total da interface).
O processamento histológico foi realizado pelo Departamento de Anatomia Patológica da Universidade Federal de Mato Grosso do Sul segundo metodologia proposta por JUNQUEIRA & JUNQUEIRA13.
Para a análise microscópica foram observados os seguintes parâmetros: cavidades císticas (sua presença correspondia à absorção da matriz mineralizada dos implantes pelos osteoclastos); tecido ósseo maduro (sua presença indicava invasão do tecido ósseo receptor nos poros do implante); tipo de tecido na transição do implante com o osso receptor (a presença de tecido ósseo indicava integração microscópica do implante).
Análise estatística
Para análise estatística dos resultados, realizada pela Disciplina de Bioestatística do Departamento de Medicina Preventiva da Universidade Federal de São Paulo, foram aplicados os seguintes testes: teste da partição do quiquadrado para tabelas 2 x N (COCHRAN, 1954)14 e teste do quiquadrado para tabelas 2 x 2 (SIEGEL, 1988)15. Em alguns casos, levando em conta as restrições de COCHRAN14, aplicou-se o teste exato de FISHER (SIEGEL, 1988)15.Em todos os testes fixou-se em 5% ( a £ 0,05) o nível de rejeição da hipótese de nulidade.
RESULTADOS
Nenhum dos coelhos apresentou sinais macroscópicos ou microscópicos de processo infeccioso. Os pontos operatórios da pele, na maioria das vezes, soltaram-se espontaneamente durante a segunda semana de observação.
Na observação macroscópica, a integridade óssea, a coloração e cicatrização da camada cortical, e a mobilidade dos implantes não apresentaram diferenças significantes (p < 0,05).
A camada cortical apresentou perda significante da textura lisa no grupo da hidroxiapatita porosa de coral com seguimento de duas semanas (· 2 calculado = 21,38*), o que não ocorreu nos grupos de 4 e 12 semanas.
A análise estatística dos resultados da observação macroscópica da interface entre os implantes e o osso receptor, após osteotomia longitudinal mostrou igual comportamento entre os grupos estudados.
A continuidade medular foi significantemente maior (c2 calculado=42,00*) no grupo de doze semanas que nos grupos de duas e quatro semanas, tanto na hidroxiapatita porosa de coral como no enxerto ósseo autógeno.
Pela análise estatística dos resultados da observação radiológica, o grupo de duas semanas foi menor (c2 calculado = 12,88*) que os grupos de quatro e doze semanas; o grupo do enxerto ósseo autógeno foi maior (c2 calculado = 5,14*) que o da hidroxiapatita porosa de coral
A calcificação do tecido circunjacente ao implante que promove o desaparecimento da interface radiotransparente foi significantemente maior com doze semanas no enxerto ósseo autógeno (c2 calculado = 22,74*) e com quatro semanas na hidroxiapatita porosa de coral (c2 calculado = 19,54*). Na comparação entre os grupos de implantes, o do enxerto ósseo autógeno mostrou-se maior (c2 calculado = 28,00*) que o da hidroxiapatita porosa de coral.
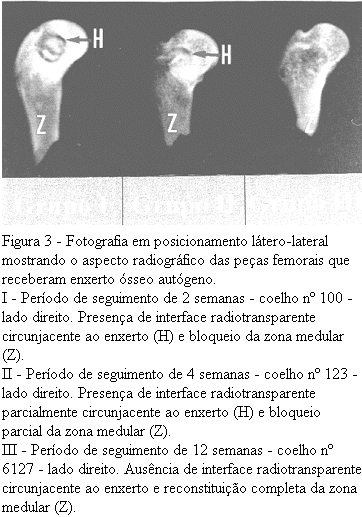
Os resultados da observação radiológica da consolidação óssea foram iguais tanto nos grupos de implantes como nos tempos de seguimento (Figuras 3 e 4).
A análise estatística dos resultados da observação microscópica mostrou a presença de cavidades císticas apenas nos implantes de hidroxiapatita porosa de coral (c2 calculado = 28,00*).
Com doze semanas, a presença de tecido ósseo maduro foi significantemente maior (c2 calculado = 42,00*) que nas duas e quatro semanas; o grupo do enxerto ósseo autógeno mostrou tecido ósseo maduro mais precocemente (c2 calculado = 28,00*) que o grupo da hidroxiapatita porosa de coral (Figuras 5, 6 e 7).
DISCUSSÃO
CHIROFF, WHITE, WEBER e ROY16 ao estudarem experimentalmente o crescimento do tecido ósseo em implantes de hidroxiapatita porosa de coral em cães, relembraram que a capacidade do corpo humano em regenerar tecidos danificados ou perdidos é limitada; tendo o homem que percorrer um longo caminho para encontrar ou desenvolver materiais que poderiam substituir adequada e completamente seus tecidos, especialmente os mineralizados como o osso.
WHITE e SHORS17 (1986) afirmaram ser a hidroxiapatita porosa de coral um biomaterial quimicamente indistinguível dos tecidos ósseos naturais.
SARTORIS, HOLMES, TENCER, MOONEY e RESNICK18 relataram que os implantes de hidroxiapatita porosa de coral implantados em cães, têm uma arquitetura intrínseca facilmente apreciada por métodos radiográficos e que, essa arquitetura é gradualmente perdida em associação com definição marginal pobre, indicando integração desses implantes pelo osso receptor.
BUCHOLZ, CARLTON e HOLMES19 utilizando enxerto ósseo autógeno ou hidroxiapatita porosa de coral no tratamento de fraturas tibiais em humanos, não encontraram diferenças significantes entre os dois grupos.
De acordo com KÜHNE e Col.11 os côndilos femorais de coelhos apresentam tecido ósseo maduro preenchendo os poros da hidroxiapatita porosa de coral em seguimentos de doze semanas.
No presente trabalho estudou-se experimentalmente a integração de biomaterial poroso - a hidroxiapatita porosa de coral - em côndilos femorais de coelhos, comparando-a com a dos enxertos ósseos autógenos.
O fêmur do coelho tem alinhamento natural em varo. Com a epifisiodese provocada pelo procedimento operatório, observou-se desvio em valgo do eixo femoral.
A análise estatística dos resultados da observação macroscópica da continuidade medular e da observação radiológica do desvio femoral em valgo, maiores no grupo de doze semanas, mostrou que esses aspectos são tempo-dependente.
Uma maior calcificação do tecido circunjacente ao implante, que promove o desaparecimento da interface radiotransparente, no grupo do enxerto ósseo autógeno que no da hidroxiapatita porosa de coral, provavelmente decorreu da avascularidade do implante de hidroxiapatita.
A presença de cavidades císticas apenas nos implantes de hidroxiapatita porosa de coral foi, provavelmente, resultante da atividade osteoclástica na zona de transição entre o implante e o osso receptor.
O resultado das observações macroscópica, radiológica e microscópica da integração da hidroxiapatita porosa de coral ao osso de coelhos sugere a possibilidade de seu uso, sem intercorrências, em seres humanos.
CONCLUSÃO
A hidroxiapatita porosa de coral integrou-se ao osso receptor de modo semelhante ao enxerto ósseo autógeno no seguimento de doze semanas.
Figueiredo AS, Fagundes DJ, Novo NF, Juliano Y, Inouye CM. Comparison between porous hydroxyapatite of chorale and autogenous bony graft in rabbits. Acta Cir Bras [serial online] 2001 Jul-Sept;16(3). Available from: URL: http://www.scielo.br/acb.
ABSTRACT: The transplantation of autogenous bone continues being used with success, in spite of the disadvantages that it presents, mainly in what refers the increased morbidity, additional operations and increase of the cost. The objective of this research was to verify the integration of the porous hydroxyapatite of chorale as biological alternative in ceramic form to substitute the autogenous bony graft. Forty-two New Zealand rabbits were submitted to na standard condylar defect witch were randomic implanted by autogenous bony graft as porous hydroxyapatite of chorale. We made clinical, macroscopic, radiographic and histologic study among the time of evolution of two, four and twelve weeks, respectively. The results were similar between the autogenous graft and the porous hydroxyapatite of chorale in the evolution of twelve weeks. It was ended that the porous hydroxyapatite of chorale is a substitute adapted to the autogenous bony graft in rabbits.
KEY WORDS: Hydroxyapatite. Bone. Autograft. Rabbit.
Conflito de interesses: nenhum
Fontes de financiamento: nenhuma
Endereço para correspondência:
Arthur Silveira de Figueiredo
Rua Barão do Rio Branco, 2167
Campo Grande - MS
79008-067
Data do recebimento: 28/03/2001
Data da revisão: 16/04/2001
Data da aprovação: 23/05/2001
- 1. Burchardt H. Biology of bone transplantation. Orthop Clin North Am 1987;18:187-96.
- 2. Nade S. Stimulating osteogenesis. Injury 1994;25(9):577-83.
- 3. De Boer HH. The history of bone grafts. Clin Orthop Rel Res 1988;226:292-8.
- 4. Friedlaender G. Current concepts review bone-banking. J Bone Joint Surg 1982;64-A:307-11.
- 5. Holmes RE, Bucholz RW, Mooney V. Porous hydroxyapatite as a bone-graft substitute in metaphyseal defects: a histometric study. J Bone Joint Surg 1986;68-A:904-11.
- 6. Weber JN, White EW, Lebiedzik J. New porous biomatherials by replication of echinoderm skeletal microstructures. Nature 1971;233:337-9.
- 7. White RA, Weber JN, White EW. Replaminerform: a new process for preparing porous ceramic, metal, and polymer prosthetic materials. Science 1975;176:922-4.
- 8. Uchida A, Nade SML, McCartney ER, Ching W. The use of ceramics for bone replacement: a comparative study of three different porous ceramics. J Bone Joint Surg 1984;66-B:269-75.
- 9. Shimazaki K, Mooney V. Comparative study of porous hydroxyapatite and tricalcium phosphate as bone substitute. J Orthop Res 1985;3(3):301-10.
- 10. Eggli PS, Müller W, schenk RK. Porous hydroxyapatite and tricalcium phosphate cylinders with two different pore size ranges implanted in the cancellous bone of rabbits: a comparative histomorphometric and histologic study of bony ingrowth and implant substitution. Clin Orthop Rel Res 1988;232:127-38.
- 11. Kühne JH, Bartl R, Frisch B, Hammer C, Jansson V, Zimmer M. Bone formation in coralline hydroxyapatite: effects of pore size studied in rabbits. Acta Orthop Scand 1994;65(3):246-52.
- 12. Wang JS, Goodman SE, Aspenberg P. Bone formation in the presence of phagocytosable hydroxyapatite particles. Clin Orthop Rel Res 1994;304:272-9.
- 13. Junqueira LC, Junqueira MMS. Técnicas básicas de citologia e histologia. Săo Paulo: Santos; 1983.
- 14. Cochran WG. Some methods for strenghtering the common c 2 test. Biometrics 1954;10:417-51.
- 15. Siegel S, Castellan Jr NJ. Nonparametrics statistics. New York: McGraw Hill Int Ed; 1988.
- 16. Chiroff RT, White EW, Weber JN, Roy DM. Tissue ingrowth of replamineform implants. J Biomed Mater Res Symp 1975;6:29-45.
- 17. White E, Shors EC. Biomaterial aspects of Interpore-200 porous hydroxyapatite. Dent Clin North Am 1986;30:49-67.
- 18.Sartoris DJ, Holmes RE, Tencer AF, Mooney V, Resnick D. Coralline hydroxyapatite bone graft substitutes in a canine metaphyseal defect model: radiographic-biomechanical correlation. Skeletal Radiol 1986;15(8):635-41.
- 19. Bucholz RW, Carlton A, Holmes R. Interporous hydroxyapatiteas a bone graft substitute in tibial plateau fractures. Clin Orthop Rel Res 1989;240:53-62.
Datas de Publicação
-
Publicação nesta coleção
11 Set 2003 -
Data do Fascículo
Set 2001
Histórico
-
Aceito
23 Maio 2001 -
Revisado
16 Abr 2001 -
Recebido
28 Mar 2001