Resumos
OBJETIVO: Verificar o efeito da solução composta por fenol, ácido acético e glicerina sobre o tumor ascítico de Ehrlich. MÉTODOS: Após a coleta do líquido ascítico de três camundongos procedeu-se a incubação, a 37° C, do mesmo com diferentes doses da solução teste (0,50, 0,25, 0,10 e 0,05 ml) e com solução salina (0,50 ml como controle; estudou-se a viabilidade celular pela técnica de exclusão do azul tripan). RESULTADOS: Observou-se que ao final de 15 minutos todas as células tumorais encontravam-se inviáveis com as diferentes doses da solução teste. CONCLUSÃO: A solução proposta, causa, in vitro, a morte das células tumorais ao foral de 15 minutos.
Carcinoma de Ehrlich; Terapia combinada; In vitro
PURPOSE: To evaluate the effects of phenol, acetic and glycerin solution in Ehrlich ascites tumor. METHODS: After the ascites liquid of three mice was collected, the incubation of these cells took place at 37 degrees Celsius with saline solution (0,50mL) and different solution dosages (0,25mL, 0,10mL e 0,05mL). RESULTS: After 15 minutes all tumors cells were dead regardless of the dosage. Whereas in the control group the tumor cells were alive. CONCLUSION: This solution destroys the tumor cells in vitro after 15 minutes.
Carcinoma; Ehrlich tumor; Combined modality therapy; In vitro
ARTIGO ORIGINAL
Efeito da solução aquosa de fenol, ácido acético e glicerina sobre o tumor ascítico de Ehrlich. Estudo experimental in vitro1 1 Trabalho realizado no Laboratório de Cirurgia e Cirurgia Experimental "William Saad Hossne" - Faculdade de Medicina, Universidade Estadual de São Paulo (UNESP). Botucatu - SP.
Effects of watery solution of phenol, acetic acid and glycerin in Ehrlich mouse ascites tumor: experimental study in vitro
Rogério Saad-HossneI; Willian Saad-HossneII; Renê Gamberini PradoI
IProfessor Doutor do Departamento de Cirurgia e Ortopedia da UNESP
IIProfessor Emérito do Departamento de Cirurgia e Ortopedia da UNESP
Endereço para correspondência Endereço para correspondência Prof. Rogério Saad-Hossne Faculdade de Medicina de Botucatu - UNESP Depto. Cirurgia e Ortopedia 18618-970 Botucatu São Paulo Tel: (14) 6802-6269 cgeral@fmb.unesp.br
RESUMO
OBJETIVO: Verificar o efeito da solução composta por fenol, ácido acético e glicerina sobre o tumor ascítico de Ehrlich.
MÉTODOS: Após a coleta do líquido ascítico de três camundongos procedeu-se a incubação, a 37° C, do mesmo com diferentes doses da solução teste (0,50, 0,25, 0,10 e 0,05 ml) e com solução salina (0,50 ml como controle; estudou-se a viabilidade celular pela técnica de exclusão do azul tripan).
RESULTADOS: Observou-se que ao final de 15 minutos todas as células tumorais encontravam-se inviáveis com as diferentes doses da solução teste.
CONCLUSÃO: A solução proposta, causa, in vitro, a morte das células tumorais ao foral de 15 minutos.
Descritores: Carcinoma de Ehrlich. Terapia combinada. In vitro.
ABSTRACT
PURPOSE: To evaluate the effects of phenol, acetic and glycerin solution in Ehrlich ascites tumor.
METHODS: After the ascites liquid of three mice was collected, the incubation of these cells took place at 37 degrees Celsius with saline solution (0,50mL) and different solution dosages (0,25mL, 0,10mL e 0,05mL).
RESULTS: After 15 minutes all tumors cells were dead regardless of the dosage. Whereas in the control group the tumor cells were alive.
CONCLUSION: This solution destroys the tumor cells in vitro after 15 minutes.
Key words: Carcinoma. Ehrlich tumor. Combined modality therapy. In vitro.
Introdução
O volume de informação a respeito de câncer cresce muito rapidamente em função de alguns fatores: primeiro, o fato do câncer não constituir uma só doença, mas sim um grande conjunto de doenças diferentes, com história natural distinta, multiplicidade de causas e diferentes formas de tratamento; segundo, o progressivo controle das doenças infecto contagiosas (com exceção da AIDS) e o aumento da idade da população, tornaram o câncer um problema mais comum e em evidência, associado também ao aumento progressivo da incidência. Dessa forma, assume papel cada vez mais relevante a pesquisa científica em Oncologia Clínica e/ou experimental.
Paralelamente a isto, o campo da pesquisa terapêutica vem se desenvolvendo no sentido de testar novas formas de tratamento, bem como novas substâncias potencialmente eficazes contra as neoplasias. A pesquisa de teste realizada com novas drogas é um procedimento oneroso e demorado. Como em toda a investigação com drogas ou medicamentos, antes de se iniciar e realizar as fases de farmacologia clínica, impõe-se a execução de estudos pré clínicos em laboratório. Para isto, faz-se necessária a utilização de modelos experimentais em animais para testar novas drogas ; um modelo muito empregado nesta linha de investigação é o tumor de Ehrlich em camundongo.Este tumor tem a capacidade de crescimento em suspensão no líquido ascítico e em tecido celular subcutâneo1,2,3, e após a sua implantação na cavidade peritoneal em camundongos sadios tem como resultado a formação de líquido ascítico tumoral. Em nosso meio , na década de 70, surgiu a idéia do uso de soluções esclerosantes no tratamento da hiperplasia prostática benigna. 4,5 verificou-se a injeção da solução composta por ácido acético, fenol, glicerina e água destilada em próstata de cães, produzia necrose, seguida de fibrose.
Tendo em vista a ação necrotizante da solução pareceu-nos válido pesquisar o efeito de tal solução em células neoplásicas, inicialmente in vitro e, caso comprovada a eficácia, testar posteriormente in vivo.
No presente trabalho tivemos como objetivo responder às seguintes indagações: a) solução in vitro causa "morte" (inviabilidade) das células neoplásicas? b) se positivo, a ação ocorre em quanto tempo? c) se positivo, qual a alteração celular que ocorre?.
Escolhemos como modelo o tumor ascitico de Ehrlich e como métrica, o método de azul de tripan e a microscopia ótica e eletrônica
Métodos
1 - Modelo de tumor -Tumor Ascítico de Ehrlich (T.A.E.)
1.1 - Manutenção do tumor in vivo e obtenção das células tumorais
Utilizou-se como modeloexperimental o tumor ascítico de Erlich em camundongos, proveniente de cepa fornecida em 1990 pelo Laboratório do Departamento de Patologia da Faculdade de Medicina Veterinária da Universidade de São Paulo (U.S.P.). A manutenção do tumor in vivo tem sido feita pela injeção intraperitoneal de 107 células a cada sete dias em camundongos receptores.
Os animais portadores do tumor foram sacrificados por deslocamento da coluna cervical sete dias após a inoculação tumoral e fixados a placa de cortiça. Após a assepsia da parede abdominal com álcool iodado realizou-se laparotomia mediana, com retirada de todo o líquido ascítico possível, por meio de aspiração com seringa de 5 ml, com a transferência do líquido para um tubo de ensaio seco e estéril.
A seguir, o líquido foi centrifugado duas vezes a 1500 rpm durante dez minutos, sendo o sobrenadante descartado e as células tumorais novamente suspensas em solução salina tamponada ao volume original (3 ml a 5 ml). O número total de células na suspensão foi determinado pela contagem de células na câmara de Neubauer, com o emprego de microscópio ótico de campo claro; a concentração desejada (107 células por ml) de células foi obtida mediante a diluição da suspensão em salina tamponada.
1.2. Teste de viabilidade celular pela técnica de exclusão do azul tripan
Com a finalidade de se determinar a viabilidade das células tumorais, à suspensão de células (0,9 ml) foi acrescido azul tripan (0,1 ml a 0,2%). Em seguida, uma gota da suspensão foi colocada entre lâmina e lamínula e realizada a contagem percentual, sendo consideradas mortas (inviáveis) as células que incorporavam o corante e, vivas as que excluiam o azul tripan.No protocolo experimental foram utilizadas para manutenção do tumor, apenas suspensões com viabilidade celular superior a 95%.
2 Solução-teste (S.T.)
A solução testada é composta de fenol (0,6 g), ácido acético (0,6 g), glicerina (1,2 g) e água bidestilada (28,0 ml), preparada no Laboratório de Cirurgia Experimental do Departamento de Cirurgia e Ortopedia (Fac. Med. Botucatu).
3 Protocolo
Procurou-se investigar o efeito in vitro da solução em estudo sobre as células tumorais, tendo sido realizados testes repetidos (três leituras).
Foi coletado o líquido ascítico de três animais com tumor de Ehrlich e feita a diluição para a concentração de 107 células tumorais por ml de líquido ascítico. Foi retirado 1 ml desta diluição (107 células tumorais) e incubado a 37º C com diferentes doses da solução teste (0,50 ml, 0,25 ml, 0,10 ml e 0,05 ml) e com solução salina (SS - 0,50 ml), como controle. Foi estudada a percentagem de células viáveis pelo teste de azul tripan a cada cinco minutos; foi também analisado à microscopia ótica e eletrônica o efeito da solução teste sobre as células tumorais.
Resultados
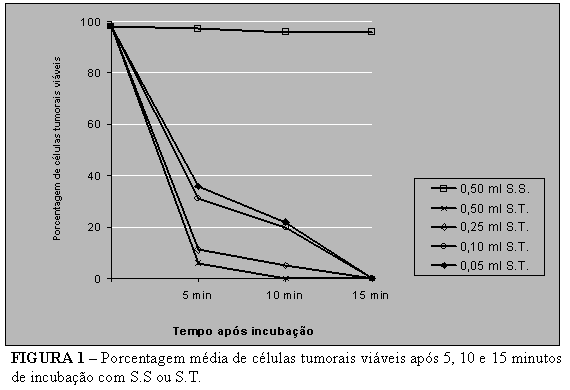
Os resultados (médios) obtidos pelo teste de exclusão do azul tripan estão expostos na Tabela 1 e na Figura 1, onde se verifica o percentual de viabilidade de células tumorais incubadas com diferentes doses da solução-teste ou com solução salina (controle), aos 5, 10 e 15 minutos.
Evidencia-se nitidamente a associação entre a solução-teste e a morte das células tumorais. O efeito aos cinco minutos é maior com a dose mais elevada; aos 15 minutos, porém, todas as células tumorais perderam sua viabilidade, independentemente da dosagem empregada.
As Figuras 2a e 2b mostram o aspecto das células tumorais à microscopia ótica, entre 5 e 10 minutos de incubação com S.S ou S.T. (0,50 ml) respectivamente: na Figura 2a nota-se que as células conservam-se viáveis, não assumindo o corante (células "translúcidas"). Na Figura 2b, pode-se observar que as células coram-se intensamente de azul (células não viáveis).
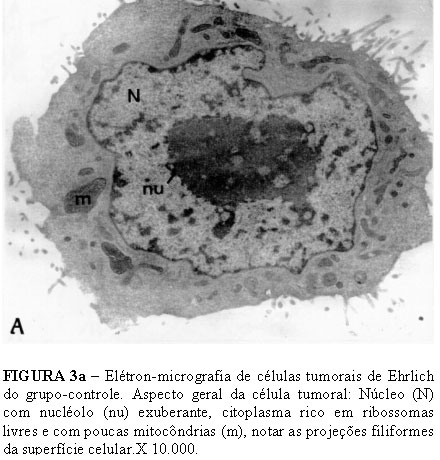
As Figuras 3a e 3b mostram uma célula tumoral, não tratada, à microscopia eletrônica; evidencia-se núcleo volumoso de contorno irregular, com cromatina descondensada e nucléolos exuberantes. A superfície celular é recoberta por grande quantidade de pequenas projeções filiformes. O citoplasma é pobre em organelas, apresenta grande quantidade de ribossomas livres, pequenas mitocôndrias esparsas, gotas lipídicas e complexo de Golgi evidente, além de esparsas cisternas de retículo endoplasmático rugoso. Visualizam-se vacúolos, de conteúdo variado.
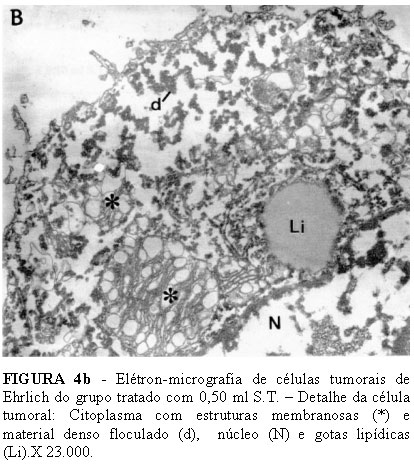
As Figuras 4a e 4b mostram o aspecto da célula tumoral à microscopia eletrônica entre 5 e 10 minutos de incubação com 0,50 ml de S.T.; a célula tumoral não apresenta alteração de forma, quer da superfície (membrana) celular como da nuclear. O núcleo apresenta massas densas e irregulares aderidas à carioteca e em meio a material bastante eletrolucente. No citoplasma, as organelas não são caracterizáveis, exceto as gotas lipídicas. Existem pequenos grumos de material denso floculado, além de estruturas membranosas vesiculares e lamelares, imersas em citosol elétron-transparente. A célula é nitidamente não viável.
Discussão
A solução testada é composta de fenol (0,6 g), ácido acético (0,6 g), glicerina (1,2 g) e água bidestilada (28 ml). O fenol é uma substância que tem poder bacteriostático (solução a 0,02% a 1%) e bactericida para determinados germes; a aplicação na pele tem efeito analgésico, podendo, porém, acarretar irritação e necrose profunda; sua ação germicida e histotóxica ocorre pela desnaturação de proteínas.
O ácido acético glacial, tem efeito bactericida a 5%, e bacteriostático a 1% , além de apresentar capacidade cáustica e antifúngica6.
A glicerina é um álcool triidroxilado, amplamente empregado como veículo para muitas drogas aplicadas na pele. Quando administrada por via oral, pode ser usada no tratamento do edema cerebral e na diminuição da tensão ocular no glaucoma 6.
Em nosso meio,4,5 investigou-se os efeitos da injeção da solução na próstata de cães, tendo observado ocorrência de necrose do tecido, seguida de fibrose; não se observaram alterações clínicas ou bioquímicas no sangue ou na urina.
Revendo a literatura, não encontramos referências ao uso dessa solução no tumor ascítico de Ehrlich ou na ascite neoplásica, justificando-se, assim a nosso ver, a oportunidade da investigação proposta em nosso trabalho.
No presente protocolo experimental (teste in vitro), optamos por utilizar, empiricamente, as doses de 0,50 ml, 0,25 ml, 0,10 ml e 0,05 ml da solução teste, observando resultados efetivos com as mesmas (Tabela 1). Na verdade, partimos da dose de 0,50 ml (1,67 ml/kg peso, em média), por ter sido este o volume injetado na cavidade peritoneal de cobaias normais, em estudo anterior 7, sem a ocorrência de efeitos colaterais, obviamente, o peso da cobaia seja bem maior que o do camundongo. Iniciamos, pois, a pesquisa com doses mais elevadas do que as utilizadas na cobaia normal.
Em nosso estudo, in vitro, mostrou-se que a solução-teste, em todas as doses utilizadas, tem efeito intenso (morte celular) sobre a célula tumoral. Esse efeito é dose-dependente, pois é quase imediato quando se utiliza concentração maior (0,50 ml); ele é também rapidamente progressivo, uma vez que, aos 15 minutos, mesmo com a menor concentração da solução (0,05 ml), todas as células haviam perdido a viabilidade.
À microscopia eletrônica, verificou-se que a solução preserva a membrana celular e a membrana nuclear. A célula tumoral mantém a sua forma. Nota-se, porém, que no citoplasma as organelas não são mais caracterizáveis, pois houve destruição das mesmas; existem pequenos grumos de material denso com aspecto "coagulado", e a célula torna-se não viável, mas a membrana celular não é destruída.
Verifica-se, pelos dados da literatura, que a maior parte das drogas antineoplásicas atualmente em teste têm como objetivo a destruição das células tumorais através de alterações na síntese proteica. Vale referir, porém, que em grande parte desses testes utilizam-se culturas de células do tumor ascítico, incubadas com substâncias citostáticas como: cisplatina, daunomicina, citosina, colchicina e vincristina8, 5-fluorouracil associado a hipertemia9 , bleomicina10, beta-alanil mefalan11, verapamil12 e metrotexate e adriamicina13, nestes ensaios, a ação antineoplásica das drogas não é imediata.
A própria técnica da hipertemia, defendida principalmente pela escola japonesa, demonstrou-se efetiva após a incubação de suspensão de células tumorais por uma hora e meia a 43º C; somente após esse período é que as células perdem sua viabilidade14.
Em nosso caso, pelo contrário, demonstrou-se, in vitro, uma ação imediata e intensa da solução sobre as células. Deve ser referido que esse efeito ocorre sobre todas as células, de qualquer natureza, em suspensão no líquido ascítico, lembrando-se contudo que, por ocasião da feitura dos teste, 95% das células são tumorais15,16.
De qualquer modo, ficou patente que a solução, ao fim de 15 minutos, é efetiva para a morte das células, em doses menores, muito embora haja efeito dose-dependente.
Conclusão
No modelo experimental de tumor ascítico de Ehrlich, a solução aquosa de fenol, ácido acético e glicerina, causa, "in vitro", a morte ( in viabilidade) das células tumorais, por destruição de estruturas citoplasmáticas e nucleares, sem rompimento da membrana celular; a ação é imediata, levando à destruição total ao final de 15 minutos.
Data do recebimento: 18/11/2004
Data da revisão: 12/12/2003
Data da aprovação: 06/01/2004
Conflito de interesse: nenhum
Fonte de financiamento: nenhuma
- 1. Ehrlich P, Apolant H. Beobachtungen über maligne mausetumoren. Berl Klin Wschr 1905;28:871-4.
- 2. Loewenthal H, Jahn G. Ubertraungsversuche mit carcinomatosis mause ascitesflussigkeit und ihr verhalten gegen physikaliche und chemise einwirkungen. Z Krebsforch 1932;37:439-47.
- 3. Klein G, Klein E. The transformation of a solid transplantable mouse carcinoma into a "ascite tumor". Cancer Res 1951;11:466-9.
- 4. Camara FR. Injeção prostática de solução esclerosante. Estudo experimental no cão [Tese Doutorado]. Universidade Estadual Paulista Faculdade de Medicina; 1973.
- 5. Camara FR, Hossne WS, Montenegro MRG. Injeção prostática de solução esclerosante. Estudo experimental no cão. J Bras Urol 1976;2:278-81.
- 6. Goodman LS, Gilman AG. As bases farmacológicas da terapêutica. 7 ed. Rio de Janeiro: Guanabara; 1987.
- 7. Saad-Hossne R. Ação necrotizante da solução de fenol, ácido acético e glicerina. Instilação peritonial. Alterações bioquímicas e anatomopatológicas. In : Resumos do 1. Congresso Médico Acadêmico; 1992. Botucatu.
- 8. Bielka H, Hoinkis G, Oesterreich S, Stahl J, Benndorf R. Induction of small stress protein on Ehrlich ascites carcinoma cells by anticancer drugs. FEBS Lett 1994;343:165-7.
- 9. Tsumura M, Yoshiga K, Takada K. Enhancement of antitumor effect of 5-fluorouracil combined with hypertermia on Ehrlich ascites tumor in vivo. Cancer Res 1988;48:3977-80.
- 10. Kato T. Enhancement of bleomycin activity in vitro on growth of Ehrlich ascite tumor cells [Abstract]. Nippon Igaku Hoshasen Gakkaiu Zasshi 1988;11:1230-7.
- 11. Tsay BL, Wolfenbarger L. Phase I study of beta-alanil-mephalan as a potent anticancer drug. Cancer Chemother Pharmacol 1987;19:190-6.
- 12. Friche E, Skovsgaard T, Nissen NI. Effect of verapamil on daunorubicin acumulation in Ehrlich ascites tumor. Cancer Chemother Pharmacol 1987;19:35.
- 13. Levin E, Chernavsky A. Effect of antineoplasic drugs on Ehrlich tumor cells. Biomed Pharmacother 1989;43:215-7.
- 14. Fung KP, Lam WP, Wen HL, Choy YM, Lee CY. Effect of hyperthermia on growth of Ehrlich ascites tumor cells. Cancer Biochem Biophys 1988;10:117-24.
- 15. Sigiura K. Tumor transplantation. In: Gray WI. Methods of animal experimentation. New York: Academic Press;1965. v.2, p. 171-222.
- 16. Fecchio D. Inflamação e tumor de Ehrlich: efeitos da modulação da resposta inflamatória sobre o crescimento tumoral [Tese - Doutorado]. Universidade de São Paulo Instituto de Ciências Biológicas; 1989.
Datas de Publicação
-
Publicação nesta coleção
07 Abr 2004 -
Data do Fascículo
Jan 2004
Histórico
-
Revisado
12 Dez 2003 -
Recebido
18 Nov 2004 -
Aceito
06 Jan 2004