Resumos
OBJETIVO: Comparar a reação tecidual à inclusão de politetrafluoroetileno-expandido com a reação tecidual ao implante de pericárdio bovino. MÉTODOS: Vinte ratos foram divididos em dois grupos iguais: 7 e 30 dias. Um disco de cada material foi introduzido no dorso de cada animal. As peças e o tecido reacional foram retirados 7 e 30 dias após a introdução, para a realização do estudo morfométrico. Para análise estatística foram aplicados os testes de Mann-Whitney e Wilcoxon. RESULTADOS: No PTFE-E, no grupo 30 dias, houve um aumento significante no número de fibroblastos e uma diminuição significante no número de neutrófilos, linfócitos e apilares. Em relação ao pericárdio bovino, ocorreu uma diminuição significante no número de fibroblastos. Quando os mesmos períodos foram comparados, o número de fibroblastos foi significativamente maior no PTFE-E, aos 30 dias, assim como o número de plasmócitos e linfócitos no grupo 30 dias , no pericárdio bovino. CONCLUSÕES: A reposta inflamatória foi menor e menos durável no PTFE-E; a reparação foi menor no PTFE-E e não houve reação de corpo estranho para ambos os materiais.
Pericárdio; Politetrafluoroetileno; Materiais biocompatíveis; Biopróteses; Inflamação
PURPOSE: It is to compare tissue reactions of the expanded polytetrafluoroethyele (E-PTFE) implantation and the tissue reaction of the bovine pericardium implants. METHODS: Twenty male rats were divided into two equal groups: 7 and 30 days. A disc-shaped specimen of test material was introduced into each animal's paraspinal region. The material and the tissue were resected 7 and 30 days after the introduction, for morphometric analysis. The Mann-Whitney and Wilcoxon tests were applied for statistical analysis of the results. RESULTS: E-PTFE demonstrated a significant increase in the number of fibroblast at 30 days. A significant drop was noted in the number of neutrophils, lymphocytes and porcentage of capilaries within the time periods. Bovine pericadium displayed a strinking drop in the number of fibroblasts. When the same periods were compared, the number of fibrolasts was greater in the E-PTFE at 30 days. The number of plasmocytes and lymphocytes was greater at 30 days compared to bovine pericardium. CONCLUSION: The inflammatory response was minor and less persistant over time in the E-PTFE; repair using the synthetic material was speedier and it did not produce a foreign body reaction.
Pericardial; Politetrafluoroetilen; Biocompatible materials; Bioprothesis; Inflamation
ARTIGO ORIGINAL
Estudo comparativo das reações teciduais ao implante de pericárdio bovino e a inclusão de politetrafluoroetileno expandido em ratos1 1 Trabalho realizado na Disciplina de Técnica Operatória e Cirurgia Experimental da Universidade Federal de São Paulo - Escola Paulista de Medicina (UNIFESP-EPM) e do Serviço de Anatomia Patológica do Hospital Israelita Albert Einstein.
A comparison of tissue reactions to bovine pericardial implants and expanded polytetrafluoroethylene inclusions in a rat model
Douglas Haddad FilhoI; Américo MarquesII; Andréa Paula Kafejian-HaddadIII; Déborah Krutman ZveibelIV
IMestre pelo curso de Pós-Graduação da Disciplina de Técnica Operatória e Cirurgia Experimental da UNIFESP-EPM
IILivre-Docente da Disciplina de Cirurgia Plástica da UNIFESP-EPM
IIIMestra pelo curso de Pós-Graduação da Disciplina de Técnica Operatória e Cirurgia Experimental da UNIFESP-EPM
IVDoutora pelo curso de Pós-Graduação do Departamento de Anatomia Patológica da Faculdade de Medicina da Universidade de São Paulo
Endereço para correspondência Endereço para correspondência Douglas Haddad Filho Rua Bom Pastor, 1238 04203-001 São Paulo - SP
RESUMO
OBJETIVO: Comparar a reação tecidual à inclusão de politetrafluoroetileno-expandido com a reação tecidual ao implante de pericárdio bovino.
MÉTODOS: Vinte ratos foram divididos em dois grupos iguais: 7 e 30 dias. Um disco de cada material foi introduzido no dorso de cada animal. As peças e o tecido reacional foram retirados 7 e 30 dias após a introdução, para a realização do estudo morfométrico. Para análise estatística foram aplicados os testes de Mann-Whitney e Wilcoxon.
RESULTADOS: No PTFE-E, no grupo 30 dias, houve um aumento significante no número de fibroblastos e uma diminuição significante no número de neutrófilos, linfócitos e apilares. Em relação ao pericárdio bovino, ocorreu uma diminuição significante no número de fibroblastos. Quando os mesmos períodos foram comparados, o número de fibroblastos foi significativamente maior no PTFE-E, aos 30 dias, assim como o número de plasmócitos e linfócitos no grupo 30 dias , no pericárdio bovino.
CONCLUSÕES: A reposta inflamatória foi menor e menos durável no PTFE-E; a reparação foi menor no PTFE-E e não houve reação de corpo estranho para ambos os materiais.
Descritores: Pericárdio. Politetrafluoroetileno. Materiais biocompatíveis. Biopróteses. Inflamação.
ABSTRACT
PURPOSE: It is to compare tissue reactions of the expanded polytetrafluoroethyele (E-PTFE) implantation and the tissue reaction of the bovine pericardium implants.
METHODS: Twenty male rats were divided into two equal groups: 7 and 30 days. A disc-shaped specimen of test material was introduced into each animal's paraspinal region. The material and the tissue were resected 7 and 30 days after the introduction, for morphometric analysis. The Mann-Whitney and Wilcoxon tests were applied for statistical analysis of the results.
RESULTS: E-PTFE demonstrated a significant increase in the number of fibroblast at 30 days. A significant drop was noted in the number of neutrophils, lymphocytes and porcentage of capilaries within the time periods. Bovine pericadium displayed a strinking drop in the number of fibroblasts. When the same periods were compared, the number of fibrolasts was greater in the E-PTFE at 30 days. The number of plasmocytes and lymphocytes was greater at 30 days compared to bovine pericardium.
CONCLUSION: The inflammatory response was minor and less persistant over time in the E-PTFE; repair using the synthetic material was speedier and it did not produce a foreign body reaction.
Key words: Pericardial. Politetrafluoroetilen. Biocompatible materials. Bioprothesis. Inflamation.
Introdução
A substituição de tecidos no organismo é um dos principais desafios da cirurgia atual. Essa substituição é necessária nas perdas de estrutura anatômica, seja por defeitos congênitos, seqüelas de trauma ou cirurgia oncológica1.
Muitos materiais foram utilizados para este fim, sejam sintéticos ou biológicos 2.
Em 1937, na Inglaterra, se iniciou o uso das resinas sintéticas, com o polietileno e o matacrilato de metila. Desde então, outros materiais foram desenvolvidos: silicone (Silastic®), politetrafluoroetileno (Teflon® ), polietileno poroso (Plasti-pore®) e poliamida (Supramid® ) 3 .
Scales definiu as características de um implante sintético ideal: não causar modifiação física no tecido horpedeiro, ser quimicamente inerte, não ser carcinogênico, não causar reação alérgica ou de corpo estranho, ter capacidade de resistência a forças mecânicas, poder ser fabricado na forma desejada, poder ser submetido à esterilização, existir em diferentes tamanhos e não necessitar de preparo 4.
Grande estorço se faz em busca de um material que desenvolva uma mínima reação inflamatória no tecido hospedeiro 5.
Foi sugerido em relação aos materiais sintéticos que, as resposta inflamatórias agudas mínimas e a incorporação tecidual fossem denominadas de biocompatibilidade 6. Foram considerados materiais biocompativeis e seguros, aqueles que submetidos a testes biológicos e mecânicos, apresentaram resultados nulos e aceitáveis, respectivamente 7. É referido que a segurança e a efetividade dos materiais incluem o conhecimento histopatológico da interface material-tecido e a possibilidade da ocorrência de inflamação crônica e resposta granulomatosa 8.
Em 1976, o politetrafluoroetileno-expandido (PTFE-E), material microporoso, foi desenvolvido. Este é composto de nódulos sólidos de politetrafluoroetileno interligados com finas fibras flexíveis do mesmo material, formando uma estrutura microporosa variada. Atualmente, é utilizado em várias especialidades cirúrgicas 9.
Quanto aos substitutos biológicos, de procedência animal, muita importância se tem dado ao pericárdio bovino. Esse tecido é utilizado principalmente na cirurgia cardiovascular, inclusive nas construções das próteses valvulares cardíacas, visto sua alta resistência e fácil aquisição10 .
Em ampla revisão da literatura, não foi encontrado trabalho que correlacionasse a reação inflamatória produzida pelo uso do politetrafluoroetileno-expandido com a produzida pelo pericárdio bovino, materiais que podem ser usados em topografias semelhantes nas diversas especialidades cirúrgicas. Desta forma, desenvolveu-se este estudo experimental, comparando as reações inlfamatórias produzidas pelos materiais acima citados, utilizando ratos.
Métodos
Foram utilizados 20 ratos (Rattus norvegicus albinus) da linhagem OUTB EPM 1 (Wistar), adultos, machos, com peso entre 200 e 300 gramas (g).
Estes foram distribuidos em dois grupos de dez animais cada, que diferiram entre si quanto ao dia de reoperação e eutanásia, quais sejam:
Grupo 7 dias (animais de 01 a 10) introdução dos materiais reoperação e eutanásia após sete dias.
Grupo 30 dias (animais de 11 a 20) introdução dos materiais reoperação e eutanásia após trinta dias.
Realizou-se anestesia por inalação com éter sulfúrico. A seguir, a manutenção foi feita por inalação intermitente de éter sulfúrico, com máscara.
Procedeu-se inicialmente à epilação manual do dorso do animal e anti-sepsia com álcool iodado a 2%. Foram colocados panos estéreis para delimitar o campo operatório.
Para a delimitação das incisões e do local de implantação dos materiais, traçou-se uma linha horizontal acompanhando o rebordo costal inferior, a qual interceptava a linha sagital média, perfazendo assim quatro quadrantes. O inicio das incisões era a 1 centímetro (cm) acima da linha subcostal e a 1 cm da linha sagital média, no quadrante superior direito e esquerdo, com extensão de 1 cm em direção caudal.
As incisões interessavam a pele e o tecido celular subcutãneo, abaixo do músculo Panniculus carnosus (panículo carnoso).
Os materiais introduzidos eram de formato discóide, com diâmetro de 6 milímetros (mm), sendo a espessura do pericárdio bovino de 0,2 a 0,3 mm e a do PTFE-E de 0,68 mm, com distância internodal de 25 micrômetros (µm).
Desta forma, os materiais foram introduzidos em túneis, nos quadrantes superiores direito e esquerdo, realizados por divulsão no plano subcutâneo, em um ponto a 2 cm do início da incisão e a 45 graus, em direção lateral.
O fechamento da pele foi realizado com pontos separados de fio de nailon monofilamentado 4-0.
Quanto ao método de esterelização dos materiais, o PTFE-E foi submetido à ação da autoclave (121 graus centígrados por 30 minutos) e o pericárdio bovino à ação do glutaraldeido e preservação em formaldeido.
O pericárdio foi banhado oito vezes com soro fisiológico, com duração de dois minutos cada banho, antes de sua utilização, para se retirar o material conservante. Padronizou-se a face lisa do pericárdio bovino voltada para a musculatura profunda do animal e a face rugosa para a pele.
Foi convencionado o lado de introdução de cada um dos materiais:
- animal de número par: PTFE-E à esquerda; pericárdio bovino à direita
- animal de número impar: PTFE-E à direita; pericárdio bovino à esquerda
A ferida operatória foi mantida exposta.
Após o tempo de observação pré-determinado de cada grupo, os animais foram reoperados com anestesia similar à do primeiro ato operatório. Foram retirados os materiais, com as margens teciduais de 0,5 cm de cada lado dos mesmos, desde a pele até o tecido celular subcutâneo. A seguir, os animais foram submetidos a eutanásia.
Procedimentos histológicos
As peças retiradas foram fixadas por imersão em formol a 10%. Após secção de cada material na porção mediana, o mesmo era incluído em parafina e seccionado em cortes de 6 µm. Os cortes foram corados pelas técnicas da hematoxilina-eosina (H.E.), para os elementos celulares e capilares, e pela técnica do tricrômico de Masson com azul do Nilo, para as fibras colágenas.
Para o exame microscópico foi utilizada uma ocular de 10 X, focalizável, dotada de placa integradora com quadrícula de 25 pontos e objetiva de 40 X.
Para a leitura, foram contados oito campos no tecido reacional periférico ao material, contendo 25 pontos cada, sendo três campos em cada face do material e um em cada extremidade, totalizando 200 pontos contados em cada lâmina. Todos os campos tangenciavam o material.
Quanto aos elementos celulares: foi anotado para cada tipo celular (neutrófilos, linfócitos, plasmócitos, fibroblastos e células gigantes), o número de células encontradas nos pontos de intersecção da quadrícula. Esse número foi dividido pelo total de células nos 200 pontos lidos, obtendo-se assim, o número proporcional de cada elemento celular em relação ao total.
Quanto aos capilares e fibras colágenas: foram anotados os pontos de intersecção com os espaços correspondentes aos capilares e fibras colágenas, obtendo-se uma razão representativa do volume vascular e de fibras colágenas, respectivamente 11.
Estudo estatístico
Os dados obtidos por estas análises foram submetidos a estudo estatístico. Dada a natureza das variáveis, foram utilizados os seguintes testes não-paramétricos: testes de Mann-Whitney e de Wilcoxon.
Em ambos os testes, fixou-se 0,05 ou 5% o nível rejeição da hipótese de nulidade.
Resultados
Quando aplicado o teste de Wilcoxon aos resultados obtidos nos grupos 7 dias, em relação aos elementos histológicos neutrófilos, linfócitos, plasmócitos, fibroblastos, capilares, fibras colágenas e células gigantes, assim como, quando aplicado aos resultados obtidos nos grupos 30 dias, em relação aos neutrófilos, fibras colágenas, células gigantes e capilares, não se mostraram significantes.
Quando aplicado o teste de Mann-Whitney aos resultados obtidos do PTFE-E, em relação aos elementos histológicos plasmócitos, fibras colágenas e células gigantes, assim como, quando aplicado aos resultados obtidos do pericárdio bovino, em relação aos neutrófilos, linfócitos, plasmócitos, capilares, fibras colágenas e células gigantes, não se mostraram significantes.
Os resultados estatisticamente significantes foram distribuídos em gráficos e assinalados com asterisco (Figuras 1, 2 e 3).
Discussão
As várias origens dos substitutos anatômicos, com diferentes respostas inflamatórias dos hospedeiros, motivam diversos e complexos estudos, relacionados diretamente com a segurança desses materiais e com a previsibilidade das reações ao longo do tempo. Essas reações ocorrem em função não somente da natureza química e-ou biológica do material e de sua configuração, mas também da área receptora 8,12. Na compilação ampla da literatura não encontramos estudos comparativos entre o PTFE-E e pericárdio bovino.
Os materiais foram introduzidos no dorso do animal, por meio de duas incisões paralelas que distavam 2cm uma da outra, para que não houvesse comunicação entre elas.
Os períodos de sete e 30 dias para análise do tecido reacional foram escolhidos com o objetivo de avaliar a resposta inflamatória precoce e tardia.
Estudo semelhante feito por Pinto e col.13, avaliou-se e comparou-se a biocompatibilidade do dacron e do pericárdio bovino, em diversos preparados, introduzidos em subcutâneo de ratos. Os autores observaram no grupo de 30 dias, onde o pericárdio bovino foi preparado com solução salina, glutaraldeído, formol e lavagens com solução fisiológica, um comportamento inócuo, com encapsulamento, contrastando com reação intensa, envolvendo leucócitos, neutrófilos e fibroblastos. Em nosso estudo, onde o pericárdio bovino recebeu preparo semelhante, no mesmo período de 30 dias, também observamos histologicamente uma tendência ao encapsulamento do material, bem como a presença de processo inflamatório-reparacional, com neutrófilos, linfócitos, plasmócitos e fibroblastos, responsáveis por tal evolução, além da permeação destas células entre as fibras pericárdicas. Acreditamos não poder denominar esse processo de inócuo, mesmo que a longo prazo este seja resolvido e o material fique circunscrito.
Em relação aos neutrófilos, seu acúmulo constitui uma das principais características da reação inflamatória aguda. Com o decorrer do processo inflamatório-reaparacional, o número dessas células tende a diminuir, cedendo lugar a outros componentes que caracterizam mais a fase crônica ou reparadora. Em nosso estudo, em relação ao pericárdio bovino, observou-se uma tendência de aumento destas células, no decorrer dos períodos de sete e 30 dias. Contudo em um dos ratos, notou-se a manutenção do processo inflamatório agudo, o qual acreditamos ter sido devido à contaminação. Tal dado, estatisticamente analisado, nos cálculos das médias, acabou por mostrar uma contradição na análise do processo. Porém, isolado este dado, com o uso da mediana, observamos o esperado, ou seja, uma tendência real a uma diminuição do número dessas células, consoânte à resolução do processo inflamatório.
A principal célula produtora de colágeno, o fibroblasto, dentro do processo inflamatório, é responsável pela produção de material orgânico a ser utilizado pelo organismo, para a reparação. Com estas características, é esperado que o número destes aumente no início da reparação e depois diminua, seja pela sua própria maturação, ou por estar finalmente entre as fibras colágenas que produziu. Nossos achados em relação ao pericárdio bovino, no decorrer dos períodos de sete e 30 dias, houve uma diminuição significante dessas células ao redor do material biológico (Figura 1).
Em relação ao PTFE-E, Kafejian-Haddad e col.14compararam a reação inflamatória provocada por este material em relação à provocada pelo silicone, utilizando modelo experimental em ratos com técnica similar à do nosso estudo. Observaram a reação inflamatória desses materiais nos períodos de três, sete e 30 dias, por meio de análises morfológica e morfométrica.
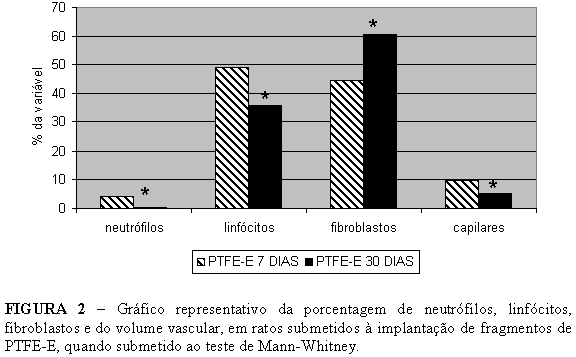
Quanto aos neutrófilos, em relação ao PTFE-E, os autores citados referiam que estas células foram raramente observados no período de 30 dias. Em nosso estudo, em relação ao PTFE-E, houve uma diminuição significante de neutrófilos, quando comparados os período de sete e 30 dias (Figura 2). Concordamos com a afirmativa de Kafejian-Haddad e col.14 em relação a essas células, quando relataram que em geral elas são observadas nas fases iniciais do processo inflamatório-reparacional.
No que concerne ao número de linfócitos, quanto ao PTFE-E, houve uma diminuição significante, quando comparados os períodos de sete e 30 dias, indicando uma não persistência de componente crônico de inflamação (Figura 2).
Em relação ao número de fibroblastos, no PTFE-E, Kafejian-Haddad e col.14 observaram, no trabalho referido, um aumento destes no transcorrer dos períodos, porém sem diferença significante. Em nosso estudo, em relação ao mesmo material, houve também um aumento, porém significante em relação a estas células, quando comparados os períodos de sete e 30 dias (Figura 2). Este fato nos parece caracterizar a evolução natural da inflamação-reparação, correspondendo à tendência de aumento das fibras colágenas no decorrer dos períodos.
Quanto à porcentagem de capilares, em relação ao PTFE-E, em nosso estudo houve uma diminuição significante, em relação aos períodos de sete e 30 dias, tendo ocorrido o fato possivelmente pela resolução do processo inflamatório (Figura 2).
Nell (1983) 6, trabalhando com PTFE-E de porosidade de 10 a 30 µm, descreveu a penetração do tecido conjuntivo no material de espaço internodal de 30 µm, não sendo esta observada no material de porosidade de 10µm. Segundo o autor, a dimensão da porosidade tem relação com a possiblidade de penetração do tecido. Acredita-se que o grande espaço internodal permite a anexação do implante e o englobamento do mesmo pelo tecido conjuntivo. A este fenômeno, o autor denominou de biocompatibilidade, pois mínimas quantidade de histíocitos e células gigantes tipo corpo estranho foram observadas. Da mesma forma, estas últimas também observadas raramente em nosso estudo, assim como no pericárdio bovino, citado acima.
Segundo Kafejian-Haddad e col.14, a maior penetração de tecido conjuntivo no interior de PTFE-E com porosidade de 25µm, quando comparado ao material com porosidade de 22µm do estudo de Mass et al. (1993)15, explica-se pela variação da microporosidade do material utilizado. Em nosso estudo, onde também utilizamos PTFE-E de 25µm, observamos permeação por células do tecido conjuntivo, principalmente após 30 dias, o que ao nosso ver sugere a incorporação do material pelos tecidos adjacentes.
Após avaliarmos o proceso inflamatório-reparacional que envolveu cada um dos materiais, demos ênfase ao estudo comparativo deste processo, comparando os materiais entre si, PTFE-E e pericárdio bovino, no mesmo período. Quanto ao número de linfócitos e plasmócitos, no período de 30 dias, houve uma maior quantidade dessas células estatisticamente significante , em relação ao pericárdio bovino, o que caracterizou uma cronificação da reação inflamatória no material biológico (Figura 3). Quanto ao número de fibroblastos, houve um maior número estatisticamente significate desta variável no tecido reacional ao PTFE-E, no período de 30 dias (Figura 3), caracterizando períodos de tempo diferentes para o processo inflamatório-reparacional, para diferentes materiais.
Conclusões
1 - O processo inflamatório oriundo da inclusão de PTFE-E foi quantitativamente menor e menos durável ao longo do tempo do que o do implante de pericárdio bovino.
2 - O processo reparacional oriundo da inclusão de PTFE-E foi mais rápida que o oriundo do implante de pericárdio bovino.
3 - Não houve reação de corpo estranho significativa, induzida pela inclusão de PTFE-E ou pelo implante de pericárdio bovino.
Data do recebimento: 18/12/2003
Data da revisão: 07/01/2004
Data da aprovação: 25/01/2004
Conflito de interesse: nenhum
Fonte de financiamento: nenhuma
- 1. Andrews JM. Biomateriais em cirurgia plástica. In: Mélega JM, Zanini AS, Psillakis JM. Cirurgia plástica reparadora e estética. 3ed. Rio de Janeiro: Medsi Editora médica Científica; 1988. p.111-8.
- 2. Marques AF. Pericárdio bovino na reparação da parede abdominal de cães [Tese - Mestrado]. Universidade Federal de São Paulo Escola Paulista de Medicina; 1984.
- 3. Marques AF, Smialovski EB, Andrews JM. Biomateriais na substituição de tecidos moles. Acta Cir Bras 1989; 4:158-67.
- 4. Scales J. Tissue reaction to suybthetic materials. Proc R Soc Med 1953;46: 647.
- 5. Antell DE, Smith JW. Implantation materials. In: Smith JW, Aston S. Grabb and Smith's plastic surgery. 4 ed. Boston: Litle Brown; 1991. p.107-25.
- 6. Nell B. Implants of gore-tex. Arch Otolaryngol 1983;109:427-33.
- 7. Holmes RE. Alloplastic implants. In: McCarthy JC. Plastic surgery. 4ed. Philadelphia: W.B. Saunders; 1990. p.698-731.
- 8. Silver FH, Mass CS. Biology of synthetic facial implant materials. Facial Plast Surg Clin North Am 1994; 2:241-53.
- 9. Gore RW. Process for producing porous produts. EUA pat. 3.9553.566, 27 ap. 1976. Newark, WI. Gore and Associates, Inc.
- 10. Bartek IT, Holden, MP, Ionescu MI. Frame-mounted tissue heart valves techniques of construction. Thorax 1974;.29:51-5.
- 11. Chalkley HW. Method for quantitative morphologic analysis os tissue. J Natl Cancer Inst 1943;4:934-54.
- 12. Taylor SR, Gibons DF. Effects of surface texture on the soft tissue response to polymer implants. J Biomed Mater Res 1983;17:205-9.
- 13. Pinto TJA, Saito T, Glerean A. Biocompatibilidade de materiais empregados na confecção de próteses cardiovasculares: comparação entre pericárdio bovino e dacron. Rev Saúde Pública 1993; 27:185-9.
- 14. Kafejian-Haddad AP, Haddad-Filho D, Guidugli-Neto J, Goldenberg S. Estudo comparativo das reações teciduais de silicone e politetrafluoroetileno expandido no dorso de ratos. Acta Cir Bras 1997;12:182-8.
- 15. Mass CS, Gnepp DR, Bumpous J. Expanded politetrafluoroethylene (Gore-tex soft tissue patch) in facial augmentation. Arch Otolaryngol Head Neck Surg 1993;119:109-14.
Datas de Publicação
-
Publicação nesta coleção
20 Mar 2006 -
Data do Fascículo
Abr 2004
Histórico
-
Aceito
25 Jan 2004 -
Revisado
07 Jan 2004 -
Recebido
18 Dez 2003