RESUMO
Objetivo:
Validar a quantificação de T-cell receptor excision circles (TRECs) e kappa-deleting recombination circles (KRECs) por reação em cadeia de polimerase (polymerase chain reaction, PCR) em tempo real (qRT-PCR), para triagem neonatal de imunodeficiências primárias que cursam com defeitos nas células T e/ou B no Brasil.
Métodos:
Amostras de sangue de recém-nascidos (RN) e controles foram coletadas em papel-filtro. O DNA foi extraído e os TRECs e KRECs foram quantificados por reação duplex de qRT-PCR. O valor de corte foi determinado pela análise de Receiver Operating Characteristics Curve, utilizando-se o programa Statistical Package for the Social Sciences (SSPS) (IBM®, Armonk, NY, EUA).
Resultados:
6.881 amostras de RN foram analisadas quanto à concentração de TRECs e KRECs. Os valores de TRECs variaram entre 1 e 1.006 TRECs/µL, com média e mediana de 160 e 139 TRECs/µL, respectivamente. Três amostras de pacientes diagnosticados com imunodeficiência grave combinada (severe combined immunodeficiency, SCID) apresentaram valores de TRECs abaixo de 4/µL e um paciente com Síndrome de DiGeorge apresentou TRECs indetectáveis. Os valores de KRECs encontraram-se entre 10 e 1.097 KRECs/µL, com média e mediana de 130 e 108 KRECs/µL, e quatro pacientes com diagnóstico de agamaglobulinemia tiveram resultados abaixo de 4 KRECs/µL. Os valores de corte encontrados foram 15 TRECs/µL e 14 KRECs/µL, e foram estabelecidos de acordo com a análise da Receiver Operating Characteristics Curve, com sensibilidade de 100% para detecção de SCID e agamaglobulinemia, respectivamente.
Conclusões:
A quantificação de TRECs e KRECs foi capaz de diagnosticar crianças com linfopenias T e/ou B em nosso estudo, validando a técnica e dando o primeiro passo para a implementação da triagem neonatal em grande escala no Brasil.
Palavras-chave:
Imunodeficiência combinada grave (SCID); Agamaglobulinemia; Triagem neonatal; Síndromes de imunodeficiência; Criança
ABSTRACT
Objective:
To validate the quantification of T-cell receptor excision circles (TRECs) and kappa-deleting recombination excision circles (KRECs) by real-time polymerase chain reaction (qRT-PCR) for newborn screening of primary immunodeficiencies with defects in T and/or B cells in Brazil.
Methods:
Blood samples from newborns and controls were collected on filter paper. DNA was extracted and TRECs, and KRECs were quantified by a duplex real-time PCR. The cutoff values were determined by receiver operating characteristic curve analysis using SPSS software (IBM®, Armonk, NY, USA).
Results:
Around 6,881 samples from newborns were collected and TRECs and KRECs were quantified. The TRECs values ranged between 1 and 1,006 TRECs/µL, with mean and median of 160 and 139 TRECs/µL, respectively. Three samples from patients with severe combined immunodeficiency (SCID) showed TRECs below 4/µL and a patient with DiGeorge syndrome showed undetectable TRECs. KRECs values ranged from 10 to 1,097 KRECs/µL, with mean and median of 130 and 108 KRECs/µL. Four patients with agammaglobulinemia had results below 4 KRECs/µL. The cutoff values were 15 TRECs/µL and 14 KRECs/µL and were established according to the receiver operating characteristic curve analysis, with 100% sensitivity for SCID and agammaglobulinemia detection, respectively.
Conclusions:
Quantification of TRECs and KRECs was able to diagnose children with T- and/or B-cell lymphopenia in our study, which validated the technique in Brazil and enabled us to implement the newborn screening program for SCID and agammaglobulinemia.
Keywords:
Severe combined immunodeficiency (SCID); Agammaglobulinemia; Newborn screening; Immunologic deficiency syndromes; Child
INTRODUÇÃO
A imunodeficiência grave combinada (SCID - do inglês severe combined immunodeficiency) é formada por um grupo heterogêneo de doenças e caracteriza-se pelo baixo número ou ausência de linfócitos T. Um defeito na produção de anticorpos, que pode ser resultante de defeitos intrínsecos dos linfócitos B ou da atividade inadequada das células T, geralmente está presente.11. Dvorak CC, Cowan MJ, Logan BR, Notarangelo LD, Griffith LM, Puck JM, et al. The natural history of children with severe combined immunodeficiency: baseline features of the first fifty patients of the primary immune deficiency treatment consortium prospective study 6901. J Clin Immunol. 2013;33:1156-64. Os pacientes com SCID são saudáveis ao nascimento; no entanto, desenvolvem infecções bacterianas, virais ou fúngicas nos primeiros meses de vida e, quando não tratados adequadamente, vão a óbito antes de completarem um ano de idade.22. Puck JM. Laboratory technology for population based screening for severe combined immunodeficiency in neonates: the winner is T cell receptor excision circles. J Allergy Clin Immunol. 2012;129:607-16.,33. Somech R, Lev A, Simon AJ, Korn D, Garty BZ, Amariglio N, et al. Newborn screening for severe T and B cell immunodeficiency in Israel: a pilot study. Isr Med Assoc J. 2013;15:404-9. O tratamento curativo é o transplante de células-tronco hematopoiéticas (TCTH) ou, em alguns casos, a terapia gênica. Quanto mais precocemente o TCTH for realizado, melhor o prognóstico desses pacientes.44. Spek J, Groenwold RH, Burg M, Montfrans JM. TREC Based Newborn Screening for Severe Combined Immunodeficiency Disease: A Systematic Review. J Clin Immunol. 2015;35:416-30.
Desde 2008, está disponível nos EUA a triagem neonatal para SCID. A metodologia consiste na quantificação de T-cell receptor excision circles (TRECs), que são pequenos marcadores produzidos durante o desenvolvimento dos linfócitos T no timo. Durante a recombinação dos genes do receptor da célula T, segmentos de DNA são excisados, formando pequenos círculos denominados TRECs, que podem ser amplificados por reação em cadeia da polimerase (polymerase chain reaction - PCR), e sua quantidade no sangue periférico reflete diretamente a atividade tímica.33. Somech R, Lev A, Simon AJ, Korn D, Garty BZ, Amariglio N, et al. Newborn screening for severe T and B cell immunodeficiency in Israel: a pilot study. Isr Med Assoc J. 2013;15:404-9.,55. Baker MW, Grossman WJ, Laessig RH, Hoffman GL, Brokopp CD, Kurtycz DF, et al. Development of a routine newborn screening protocol for severe combined immunodeficiency. J Allergy Clin Immunol. 2009;124:522-7.
Recentemente, Borte et al.66. Borte S, Döbeln U, Fasth A, Wang N, Janzi M, Winiarski J, et al. Neonatal screening for severe primary immunodeficiency diseases using high throughput triplex real time PCR. Blood. 2012;119:2552-5. descreveram um ensaio multiplex capaz de detectar TRECs e kappa-deleting excision circles (KRECs) em uma mesma reação para triagem neonatal de imunodeficiências primárias. Os KRECs são formados de maneira semelhante aos TRECs durante o desenvolvimento de linfócitos B e sua quantificação permite o diagnóstico precoce de defeitos nas células B, como a agamaglobulinemia ligada ao X (XLA, do inglês X-linked agammaglobulinemia) ou a autossômica recessiva, doenças caracterizadas pela deficiência de células B causadas por mutações nos genes que codificam componentes do receptor de célula B (BCR) ou seu precursor (pré-BCR), levando à redução dos níveis séricos de imunoglobulinas. O defeito predominante é a XLA, correspondendo a 85% dos casos. Os portadores dessa patologia são suscetíveis a infecções virais e bacterianas, sendo as bactérias encapsuladas - Haemophilus influenza e Streptococcus pneumonia - as causas mais comuns de infecções. Os sintomas da agamaglobulinemia começam a aparecer entre três e seis meses de idade, quando caem os níveis de imunoglobulinas maternas; quando não há antecedentes familiares, o diagnóstico geralmente é realizado tardiamente.77. Bestas B, Turunen JJ, Blomberg KE, Wang Q, Mansson R, El Andaloussi S, et al. Splice correction strategies for treatment of X linked agammaglobulinemia. Curr Allergy Asthma Rep. 2015;15:510.,88. Fernandes A, Guedes M, Vasconcelos J, Neves E, Fernandes S, Marques L. X linked agammaglobulinemia: experience in a Portuguese hospital. An Pediatr (Barc). 2015;82:166-71. A identificação precoce de portadores de agamaglobulinemias é muito vantajosa, uma vez que essas crianças são propensas ao desenvolvimento de infecções respiratórias crônicas e debilitantes.33. Somech R, Lev A, Simon AJ, Korn D, Garty BZ, Amariglio N, et al. Newborn screening for severe T and B cell immunodeficiency in Israel: a pilot study. Isr Med Assoc J. 2013;15:404-9.,66. Borte S, Döbeln U, Fasth A, Wang N, Janzi M, Winiarski J, et al. Neonatal screening for severe primary immunodeficiency diseases using high throughput triplex real time PCR. Blood. 2012;119:2552-5.
Um trabalho anterior de nosso grupo, pioneiro no país, validou a metodologia de quantificação de TRECs para triagem neonatal de SCID.99. Kanegae MP, Barreiros LA, Mazzucchelli JT, Hadachi SM, Guilhoto LM, Acquesta AL, et al. Neonatal screening for severe combined immunodeficiency in Brazil. J Pediatr (Rio J). 2016;92:374-80. O presente trabalho teve como objetivo validar a quantificação de TRECs e KRECs em uma mesma reação por PCR quantitativa em tempo real (qRT-PCR), para triagem neonatal de imunodeficiências primárias que cursam com defeitos nas células T e/ou B, ampliando, assim, a gama de doenças triadas.
MÉTODO
Este estudo transversal incluiu amostras de recém-nascidos (RN) cujos pais/responsáveis aceitaram participar do projeto de pesquisa. As amostras de sangue foram coletadas em papel-filtro a partir de punção no calcâneo do RN seguindo-se as normas éticas vigentes (CAAE: 36364214.8.0000.5467), entre setembro de 2014 e julho de 2015. Foram coletadas e analisadas amostras provenientes de três hospitais da Região Metropolitana de São Paulo (Amparo Maternal, Hospital Geral de Carapicuíba e Hospital Municipal São Luiz Gonzaga), uma clínica de Belém (PA - CLIMEP), um hospital de São José dos Campos (SP - Hospital Municipal Dr. José de Carvalho Florence) e um hospital de Porto Alegre (RS - Hospital Nossa Senhora da Conceição). Vinte e três amostras de pacientes com suspeita diagnóstica de imunodeficiência primária (Quadro 1)1010. BRAGID [homepage on the Internet]. BRAGID Brazilian Group for Immunodeficiencies [cited 2016 Jul 11]. Available from: http://www.imunopediatria.org.br
http://www.imunopediatria.org.br...
foram encaminhadas para investigação por pediatras imunologistas de todo o país. Como controles positivos para a validação do teste foram utilizadas amostras de três pacientes previamente diagnosticados com SCID e quatro com agamaglobulinemia.
Para a PCR, realizamos a eluição do DNA a partir de discos de 3,2 mm de diâmetro provenientes das amostras coletadas em papel-filtro.1111. Heath EM, O'Brien DP, Banas R, Naylor EW, Dobrowolski S. Optimization of an automated DNA purification protocol for neonatal screening. Arch Pathol Lab Med. 1999;123:1154-60. O DNA foi então amplificado em uma duplex de qRT-PCR para TRECs e KRECs em volume final de 20 µL, contendo 10 µL de Taqman Gene Expression Master Mix, 8 µL da solução de DNA, 0,8 µL de albumina sérica bovina 10 mg/mL e primers e sondas descritos por Sottini et al.1212. Sottini A, Ghidini C, Zanotti C, Chiarini M, Caimi L, Lanfranchi A, et al. Simultaneous quantification of recent thymic T cell and bone marrow B cell emigrants in patients with primary immunodeficiency undergone to stem cell transplantation. Clin Immunol. 2010;136:217-27. As concentrações finais dos primers para TRECs e KRECs foi, respectivamente, de 300 e 600 nM e as sondas foram utilizadas na concentração de 200 nM. A amplificação de beta-actina foi realizada na mesma placa, somente para amostras que apresentaram TRECs e/ou KRECs abaixo do valor de corte, com primers e sonda descritos por Baker et al.,55. Baker MW, Grossman WJ, Laessig RH, Hoffman GL, Brokopp CD, Kurtycz DF, et al. Development of a routine newborn screening protocol for severe combined immunodeficiency. J Allergy Clin Immunol. 2009;124:522-7. nas concentrações finais de 250 e 150 nM, respectivamente. As concentrações das moléculas de TREC, KREC e beta-actina (controle endógeno) foram calculadas utilizando-se uma curva-padrão construída por meio da diluição de plasmídeos contendo as sequências específicas descritas por Sottini et al.1212. Sottini A, Ghidini C, Zanotti C, Chiarini M, Caimi L, Lanfranchi A, et al. Simultaneous quantification of recent thymic T cell and bone marrow B cell emigrants in patients with primary immunodeficiency undergone to stem cell transplantation. Clin Immunol. 2010;136:217-27.
Para determinar se uma amostra se encontrava dentro dos parâmetros normais, utilizamos um valor de corte inicial para TRECs e KRECs de 25 cópias/µL, baseando-nos em trabalho de Baker et al.55. Baker MW, Grossman WJ, Laessig RH, Hoffman GL, Brokopp CD, Kurtycz DF, et al. Development of a routine newborn screening protocol for severe combined immunodeficiency. J Allergy Clin Immunol. 2009;124:522-7. Quando a amostra apresentou valores abaixo dessa concentração na primeira análise, repetimos todo o processo de extração e amplificação, juntamente com a quantificação de beta-actina. Após essa segunda etapa, nos casos em que TRECs e/ou KRECs se mantiveram abaixo do normal, com beta-actina acima de 8.000 cópias/µL, os pacientes foram contatados e encaminhados para imunologista pediátrico para avaliação e realização de exames confirmatórios (imunofenotipagem de linfócitos e subpopulações).
A análise final dos dados foi realizada utilizando-se estatística descritiva. Por meio do teste de Kolmogorov-Smirnov, determinamos a distribuição não Gaussiana da amostra e os dados foram então apresentados segundo mediana e valores interquartis. As concentrações de TRECs e KRECs em RN a termo e pré-termo foram analisadas utilizando-se o teste de Mann-Whitney no programa GraphPad Prism 5.0 (San Diego, CA, EUA). Por fim, realizamos a análise da Receiver Operating Characteristics Curve (área sob a curva) para determinar um valor de corte final, com 100% de sensibilidade para detecção de SCID e agamaglobulinemia, utilizando o Statistical Package for the Social Sciences (SSPS) (IBM®, Armonk, NY, EUA).
RESULTADOS
Foram coletadas 6.881 amostras de RN, que foram analisadas quanto à concentração de TRECs e KRECs. Do total de amostras, 1.853 (26,90%) foram provenientes da CLIMEP (Belém/PA), 146 (2,10%) do Hospital Municipal Dr. José de Carvalho Florence (São José dos Campos/SP) e 40 (0,58%) do Hospital Nossa Senhora da Conceição (Porto Alegre/RS); o restante veio dos hospitais localizados na Região Metropolitana de São Paulo.
Os valores de TRECs variaram entre 1 e 1.006 moléculas/microlitro, com média e mediana de 160 e 139 moléculas/microlitro, respectivamente. Três amostras de pacientes diagnosticados com SCID apresentaram valores de TRECs abaixo de 4/µL, e um paciente com Síndrome de DiGeorge apresentou TRECs indetectáveis apesar da amplificação normal de beta-actina (Tabela 1).1313. Baker MW, Laessig RH, Katcher ML, Routes JM, Grossman WJ, Verbsky J, et al. Implementing routine testing for severe combined immunodeficiency within Wisconsin's newborn screening program. Public Health Rep. 2010;125 Suppl 2:88-95. Os valores de KRECs encontraram-se entre 10 e 1.097 moléculas/microlitro, com média e mediana de 130 e 108 moléculas/microlitro, e quatro pacientes com diagnóstico de agamaglobulinemia tiveram resultados abaixo de 4 moléculas/microlitro.
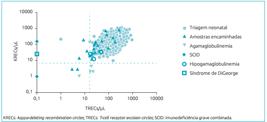
Os valores de corte encontrados foram 15 TRECs/µL e 14 KRECs/µL, e foram estabelecidos de acordo com a análise da Receiver Operating Characteristics Curve, com sensibilidade de 100% para detecção de SCID e agamaglobulinemia, respectivamente (Fig. 1). As amostras com resultados abaixo dos valores de corte, descritos anteriormente, foram submetidas a nova extração de DNA e reanalisadas adicionando-se a análise de beta-actina para controle de qualidade da extração. Somente duas amostras provenientes da triagem neonatal mantiveram valores baixos de TRECs e/ou KRECs, conforme mostra a Fig. 2. Esses pacientes foram contatados para que fossem encaminhados ao pediatra imunologista, colaborador do trabalho. O primeiro paciente, cujos resultados foram 1 TREC/µL e 211 KRECs/µL, faleceu no sexto dia após o nascimento em decorrência de um derrame pleural ocorrido aos seis meses de gestação e, por esse motivo, os pais receberam aconselhamento genético e amostra de sangue seguiu para sequenciamento genético. O segundo paciente (157 TRECs/µL e 10 KRECs/µL) compareceu à primeira consulta, quando não se constatou história prévia relacionada a imunodeficiências primárias ou consanguinidade, porém não retornou para coleta de exames específicos. Vinte e três amostras de pacientes com suspeita diagnóstica de imunodeficiências primárias (triângulos pretos na Fig. 2) foram encaminhadas por pediatras imunologistas de todo o Brasil. Dessas, cinco resultaram em valores de TRECs e/ou KRECs abaixo do valor de corte, resultado que corroborou a suspeita clínica. Um desses pacientes é portador da trissomia do cromossomo 21 e apresentou valores de 6 TRECs/µL e 14 KRECs/µL.
(A) Receiver Operating Characteristics Curve para valor de corte de T-cell receptor excision circles de 15/µL, com área sob a curva de 1,00. (B) Receiver Operating Characteristics Curve para valor de corte de kappa-deleting recombination circles de 14/µL, com área sob a curva de 1,00.
Concentração de T-cell receptor excision circles e kappa-deleting recombination circles de 6.881 amostras de triagem neonatal e de 23 amostras de pacientes encaminhados por imunologistas pediátricos por suspeita de imunodeficiência primária. T-cell receptor excision circles e kappa-deleting recombination circles foram quantificados por reação em cadeia da polimerase quantitativa em tempo real. Amostras de portadores já diagnosticados com imunodeficiência grave combinada, agamaglobulinemia, hipogamaglobulinemia e Síndrome de DiGeorge foram analisadas como controles para validação do método. As linhas tracejadas representam os valores de corte resultantes da análise da Receiver Operating Characteristics Curve.
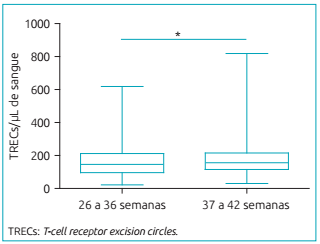
Um total de 1.548 amostras provenientes de Belém (PA) foi analisado quanto à idade gestacional e aos valores de TRECs e KRECs, pois há relatos na literatura de que prematuros possuem valores de TRECs mais baixos,1313. Baker MW, Laessig RH, Katcher ML, Routes JM, Grossman WJ, Verbsky J, et al. Implementing routine testing for severe combined immunodeficiency within Wisconsin's newborn screening program. Public Health Rep. 2010;125 Suppl 2:88-95.,1515. Ward CE, Baptist AP. Challenges of newborn severe combined immunodeficiency screening among premature infants. Pediatrics. 2013;131:e1298-302. o que representaria um risco de falsos-positivos. A Fig. 3 mostra que os valores de TRECs foram significativamente menores nos prematuros (p<0,05). Esses apresentaram mediana de 146 TRECs/µL, enquanto os nascidos a termo obtiveram mediana de 156 TRECs/µL. Os valores de KRECs não apresentaram variações em relação à idade gestacional.
Concentração de TRECs/µL em 180 recém-nascidos prematuros (26 a 36 semanas) e 1.368 nascidos a termo (37 a 42 semanas), quantificados por reação em cadeia da polimerase em tempo real. As crianças prematuras apresentaram concentrações de T-cell receptor excision circles mais baixas que os nascidos a termo (146 versus 156 TRECs/µL, respectivamente; *p<0,05, teste de Mann-Whitney). A concentração de T-cell receptor excision circles está representada em box plot mostrando mediana, 25° e 75° percentis e mínimos e máximos.
DISCUSSÃO
Foram analisadas 6.881 amostras de diferentes Estados do Brasil, juntamente com controles positivos de SCID e agamaglobulinemia, que validaram o ensaio para quantificar a concentração de TRECs e KRECs.
Para as primeiras 1.000 amostras analisadas, utilizaram-se inicialmente os valores de corte de 25 TRECs/µL e 25 KRECs/µL, resultando em um alto índice de repetição - 2,5% das amostras tiveram concentrações abaixo dos valores de corte em uma primeira análise -, comparado a trabalho anterior de nosso grupo,99. Kanegae MP, Barreiros LA, Mazzucchelli JT, Hadachi SM, Guilhoto LM, Acquesta AL, et al. Neonatal screening for severe combined immunodeficiency in Brazil. J Pediatr (Rio J). 2016;92:374-80. mas ainda dentro dos valores relatados por outros autores (0,20-3,26%).44. Spek J, Groenwold RH, Burg M, Montfrans JM. TREC Based Newborn Screening for Severe Combined Immunodeficiency Disease: A Systematic Review. J Clin Immunol. 2015;35:416-30. Uma possibilidade para esse alto índice de repetição foi a utilização de um plasmídeo diferente do anteriormente empregado - continha somente a sequência de TRECs. Desse modo, decidiu-se pela análise de um maior número de amostras, juntamente com controles positivos das doenças em estudo, para que se estabelecesse um valor de corte adequado. Assim, após a quantificação de quase 7.000 amostras, realizou-se a análise da Receiver Operating Characteristics Curve e chegou-se a um valor de corte de 15 TRECs/µL e 14 KRECs/µL, com sensibilidade de 100% para detecção de SCID e agamaglobulinemia, respectivamente. Esses valores estão muito próximos dos relatados por Borte et al.88. Fernandes A, Guedes M, Vasconcelos J, Neves E, Fernandes S, Marques L. X linked agammaglobulinemia: experience in a Portuguese hospital. An Pediatr (Barc). 2015;82:166-71. (15 TRECs/µL e 10 KRECs/µL) e resultaram em uma taxa de repetição de 0,49% (34 amostras), valor muito próximo ao encontrado em nosso trabalho anterior.99. Kanegae MP, Barreiros LA, Mazzucchelli JT, Hadachi SM, Guilhoto LM, Acquesta AL, et al. Neonatal screening for severe combined immunodeficiency in Brazil. J Pediatr (Rio J). 2016;92:374-80. Após a reanálise dessas 34 amostras que ficaram abaixo dos novos valores de corte, somente duas (0,03%) mantiveram seus valores alterados. A confirmação de diagnóstico desses dois indivíduos não foi possível devido à impossibilidade de seguimento.
O índice de repetição da metodologia aplicada, ou seja, a percentagem de amostras a serem reanalisadas, está diretamente relacionado à restrição imposta pelo valor de corte utilizado, sendo que quanto mais baixo for esse valor, menor será o número de amostras a terem todo o procedimento repetido. Ademais, outro fator importante a ser considerado na determinação dos valores de corte são as patologias que se deseja detectar por meio da triagem neonatal. Uma revisão recente sobre o rastreio neonatal para SCID/linfopenias T mostrou que várias outras doenças que cursam com linfopenia T podem ser detectadas pela quantificação de TRECs; no entanto, alguns desses casos não apresentam TRECs indetectáveis ou muito baixos, como no caso da SCID clássica.1616. Kwan A, Abraham RS, Currier R, Brower A, Andruszewski K, Abbott JK, et al. Newborn screening for severe combined immunodeficiency in 11 screening programs in the United States. JAMA. 2014;312:729-38.
Outro trabalho interessante quantificou TRECs em portadores da deleção 22q11 e mostrou que a variação no valor de corte leva a diferentes taxas de sucesso no diagnóstico neonatal de portadores dessa síndrome, sendo que quanto menor o valor de corte, menor o número de portadores identificados.1717. Framme J, Borte S, Döbeln U, Hammarström L, Oskarsdottir S. Retrospective analysis of TREC based newborn screening results and clinical phenotypes in infants with the 22q11 deletion syndrome. J Clin Immunol. 2014;34:514-9. Em nosso estudo, um paciente com tetralogia de Fallot, hipocalcemia e linfopenia (CD3+:994/mm3) foi encaminhado por suspeita de Síndrome de DiGeorge, mais tarde confirmada pela detecção da deleção do 22q11. Os TRECs desse paciente foram indetectáveis, resultado compatível com o número de células T, comprovando, portanto, a utilidade do ensaio na detecção não só de SCID, mas de outras patologias que cursam com baixo número de linfócitos T.
De modo similar aos TRECs, a quantificação dos KRECs permite a detecção precoce de imunodeficiências com defeitos no desenvolvimento de linfócitos B. A metodologia descrita neste trabalho permite não só a identificação de pacientes portadores de agamaglobulinemia, como também auxilia na classificação do tipo de SCID (T-B+; T-B-).66. Borte S, Döbeln U, Fasth A, Wang N, Janzi M, Winiarski J, et al. Neonatal screening for severe primary immunodeficiency diseases using high throughput triplex real time PCR. Blood. 2012;119:2552-5. Com o advento da triagem neonatal para linfopenias T e B, essas crianças podem ser diagnosticadas logo após o nascimento, como comprovaram nossos resultados.
Dos três pacientes controles com SCID participantes do estudo, dois apresentaram ausência ou número muito reduzido de TRECs e KRECs (SCID T-B-) e o terceiro apresentou fenótipo T-B+, de acordo com o ensaio de qRT-PCR e compatível com imunofenotipagem de linfócitos prévia. O paciente com Síndrome de DiGeorge, como esperado, apresentou valor normal de KRECs.
Médicos colaboradores da rede BRAGID (Grupo Brasileiro de Imunodeficiências Primárias, www.bragid.org.br) foram responsáveis pelo encaminhamento de 23 amostras suspeitas de imunodeficiência primária. Do total de amostras recebidas, cinco apresentaram valores de TRECs e/ou KRECs abaixo do valor de corte, confirmando, portanto, a suspeita médica. Um desses, paciente, portador da trissomia do cromossomo 21, apresentou valores de TRECs abaixo do valor de corte, compatíveis com relatos norte-americanos anteriores da triagem neonatal para SCID;1616. Kwan A, Abraham RS, Currier R, Brower A, Andruszewski K, Abbott JK, et al. Newborn screening for severe combined immunodeficiency in 11 screening programs in the United States. JAMA. 2014;312:729-38. foi verificada, também nesse paciente, a presença de imunodeficiência associada, alertando médicos e cuidadores quanto aos cuidados adicionais a serem tomados.
A análise de amostras de RN prematuros e a termo comprovou dados já relatados anteriormente de que prematuros possuem valores de TRECs mais baixos (146 versus 156 TRECs/µL).1313. Baker MW, Laessig RH, Katcher ML, Routes JM, Grossman WJ, Verbsky J, et al. Implementing routine testing for severe combined immunodeficiency within Wisconsin's newborn screening program. Public Health Rep. 2010;125 Suppl 2:88-95.,1515. Ward CE, Baptist AP. Challenges of newborn severe combined immunodeficiency screening among premature infants. Pediatrics. 2013;131:e1298-302. Desse modo, estabelecemos que as crianças prematuras com valores de TRECs alterados ao nascimento devem ter sua triagem neonatal para linfopenias T repetida quando completarem a idade gestacional ajustada de 37 semanas. Quanto aos KRECs, os valores não diferiram estatisticamente entre prematuros e a termo, conforme relato anterior.1818. Olbrich P, Felipe B, Delgado Pecellin C, Rodero R, Rojas P, Aguayo J, et al. A first pilot study on the neonatal screening of primary immunodeficiencies in Spain: TRECS and KRECS identify severe T and B cell lymphopenia. An Pediatr (Barc). 2014;81:310-7.
A incidência das imunodeficiências primárias é desconhecida no Brasil. Acredita-se que muitas crianças sucumbem antes que o diagnóstico seja realizado e, por esse motivo, como ocorria nos EUA antes da triagem neonatal, a incidência provavelmente está subestimada.1919. Kwan A, Puck JM. History and current status of newborn screening for severe combined immunodeficiency. Semin Perinatol. 2015;39:194-205. No Brasil, somente os pacientes com história familiar positiva para imunodeficiências primárias têm a possibilidade de se beneficiar do diagnóstico precoce. O início da triagem neonatal universal para essas patologias possibilitará o diagnóstico e tratamento precoce para todas as crianças. Com o advento do TREC na triagem neonatal, foi possível estabelecer a incidência de SCID nos EUA em 1:58.000.1616. Kwan A, Abraham RS, Currier R, Brower A, Andruszewski K, Abbott JK, et al. Newborn screening for severe combined immunodeficiency in 11 screening programs in the United States. JAMA. 2014;312:729-38. Considerando que no Brasil temos 2,9 milhões nascimentos/ano, deveríamos diagnosticar aproximadamente 50 pacientes ao ano. Uma investigação recente constatou um número reduzido de casos de SCID diagnosticados no Brasil e alta taxa de mortalidade.2020. Mazzucchelli JT, Bonfim C, Castro GG, Condino Neto AA, Costa NM, Cunha L, et al. Severe combined immunodeficiency in Brazil: management, prognosis, and BCG associated complications. J Investig Allergol Clin Immunol. 2014;24:184-91. A incorporação da quantificação de TRECs à triagem neonatal de nosso país beneficiaria um número expressivo de pacientes com SCID.
A SCID se encaixa perfeitamente nos critérios formulados por Wilson e Jungner para que seja incluída na triagem neonatal: inexistência de sinais e sintomas clínicos ao exame físico, grande prejuízo ao portador se a doença não for tratada, tratamento disponível, melhora da sobrevida e teste de triagem disponível a um custo razoável.2121. Wilson JM, Jungner YG. Principles and practice of mass screening for disease. Bol Oficina Sanit Panam. 1968;65:281-393. Sem diagnóstico e tratamento adequados, as crianças com SCID evoluem para o óbito nos dois primeiros anos de vida.11. Dvorak CC, Cowan MJ, Logan BR, Notarangelo LD, Griffith LM, Puck JM, et al. The natural history of children with severe combined immunodeficiency: baseline features of the first fifty patients of the primary immune deficiency treatment consortium prospective study 6901. J Clin Immunol. 2013;33:1156-64. Estudos mostraram que a sobrevida em longo prazo, quando o RN é submetido ao TCTH até os três meses e meio de vida, é de 94%. Quando o transplante ocorre após essa idade, com infecções ativas, a sobrevida diminui para somente 50%.44. Spek J, Groenwold RH, Burg M, Montfrans JM. TREC Based Newborn Screening for Severe Combined Immunodeficiency Disease: A Systematic Review. J Clin Immunol. 2015;35:416-30. Analisando-se esses números, chega-se à conclusão de que o diagnóstico precoce pode salvar a vida das crianças portadoras de SCID. A adição da quantificação dos KRECs à PCR a um custo ínfimo permite o diagnóstico de imunodeficiências primárias de células B e se mostrou capaz de detectar pacientes portadores de SCID T-B- e portadores de agamaglobulinemia.
Atualmente, o acesso a exames que quantifiquem linfócitos e suas subpopulações é restrito a grandes centros e laboratórios de pesquisa. A quantificação de TRECs e KRECs em amostras de sangue seco em papel-filtro permite uma triagem dessas amostras vindas de quaisquer áreas geográficas e um direcionamento a exames específicos, poupando tempo e recursos. No Brasil não existem estudos sobre o custo ao sistema público de saúde de pacientes com imunodeficiências primárias, mas, nos EUA, estudos já comprovaram o custo-benefício da inclusão da triagem neonatal para linfopenias T, mostrando que o tratamento dos pacientes diagnosticados previamente ao aparecimento das infecções e consequentes internações custa até quatro vezes menos que dos pacientes diagnosticados tardiamente.2222. Kubiak C, Jyonouchi S, Kuo C, Garcia Lloret M, Dorsey MJ, Sleasman J, et al. Fiscal implications of newborn screening in the diagnosis of severe combined immunodeficiency. J Allergy Clin Immunol Pract. 2014;2:697-702.
Por fim, concluímos que a quantificação de TRECs e KRECs detectou crianças com linfopenias T e/ou B em nosso estudo. A técnica está validada e pode ser implantada em grande escala no Brasil, sem a necessidade de coleta adicional, uma vez que a coleta usual do teste do pezinho é a utilizada nesse ensaio. Assim, damos o primeiro passo em direção à inclusão da triagem neonatal para linfopenias T e B em nosso país, facilitando o rastreamento, o diagnóstico precoce e o tratamento de indivíduos com imunodeficiências primárias no Brasil.
REFERÊNCIAS
-
1Dvorak CC, Cowan MJ, Logan BR, Notarangelo LD, Griffith LM, Puck JM, et al. The natural history of children with severe combined immunodeficiency: baseline features of the first fifty patients of the primary immune deficiency treatment consortium prospective study 6901. J Clin Immunol. 2013;33:1156-64.
-
2Puck JM. Laboratory technology for population based screening for severe combined immunodeficiency in neonates: the winner is T cell receptor excision circles. J Allergy Clin Immunol. 2012;129:607-16.
-
3Somech R, Lev A, Simon AJ, Korn D, Garty BZ, Amariglio N, et al. Newborn screening for severe T and B cell immunodeficiency in Israel: a pilot study. Isr Med Assoc J. 2013;15:404-9.
-
4Spek J, Groenwold RH, Burg M, Montfrans JM. TREC Based Newborn Screening for Severe Combined Immunodeficiency Disease: A Systematic Review. J Clin Immunol. 2015;35:416-30.
-
5Baker MW, Grossman WJ, Laessig RH, Hoffman GL, Brokopp CD, Kurtycz DF, et al. Development of a routine newborn screening protocol for severe combined immunodeficiency. J Allergy Clin Immunol. 2009;124:522-7.
-
6Borte S, Döbeln U, Fasth A, Wang N, Janzi M, Winiarski J, et al. Neonatal screening for severe primary immunodeficiency diseases using high throughput triplex real time PCR. Blood. 2012;119:2552-5.
-
7Bestas B, Turunen JJ, Blomberg KE, Wang Q, Mansson R, El Andaloussi S, et al. Splice correction strategies for treatment of X linked agammaglobulinemia. Curr Allergy Asthma Rep. 2015;15:510.
-
8Fernandes A, Guedes M, Vasconcelos J, Neves E, Fernandes S, Marques L. X linked agammaglobulinemia: experience in a Portuguese hospital. An Pediatr (Barc). 2015;82:166-71.
-
9Kanegae MP, Barreiros LA, Mazzucchelli JT, Hadachi SM, Guilhoto LM, Acquesta AL, et al. Neonatal screening for severe combined immunodeficiency in Brazil. J Pediatr (Rio J). 2016;92:374-80.
-
10BRAGID [homepage on the Internet]. BRAGID Brazilian Group for Immunodeficiencies [cited 2016 Jul 11]. Available from: http://www.imunopediatria.org.br
» http://www.imunopediatria.org.br -
11Heath EM, O'Brien DP, Banas R, Naylor EW, Dobrowolski S. Optimization of an automated DNA purification protocol for neonatal screening. Arch Pathol Lab Med. 1999;123:1154-60.
-
12Sottini A, Ghidini C, Zanotti C, Chiarini M, Caimi L, Lanfranchi A, et al. Simultaneous quantification of recent thymic T cell and bone marrow B cell emigrants in patients with primary immunodeficiency undergone to stem cell transplantation. Clin Immunol. 2010;136:217-27.
-
13Baker MW, Laessig RH, Katcher ML, Routes JM, Grossman WJ, Verbsky J, et al. Implementing routine testing for severe combined immunodeficiency within Wisconsin's newborn screening program. Public Health Rep. 2010;125 Suppl 2:88-95.
-
14Moraes Pinto MI, Ono E, Santos Valente EC, Almeida LC, Andrade PR, Dinelli MI, et al. Lymphocyte subsets in human immunodeficiency virus unexposed Brazilian individuals from birth to adulthood. Mem Inst Oswaldo Cruz. 2014;109:989-98.
-
15Ward CE, Baptist AP. Challenges of newborn severe combined immunodeficiency screening among premature infants. Pediatrics. 2013;131:e1298-302.
-
16Kwan A, Abraham RS, Currier R, Brower A, Andruszewski K, Abbott JK, et al. Newborn screening for severe combined immunodeficiency in 11 screening programs in the United States. JAMA. 2014;312:729-38.
-
17Framme J, Borte S, Döbeln U, Hammarström L, Oskarsdottir S. Retrospective analysis of TREC based newborn screening results and clinical phenotypes in infants with the 22q11 deletion syndrome. J Clin Immunol. 2014;34:514-9.
-
18Olbrich P, Felipe B, Delgado Pecellin C, Rodero R, Rojas P, Aguayo J, et al. A first pilot study on the neonatal screening of primary immunodeficiencies in Spain: TRECS and KRECS identify severe T and B cell lymphopenia. An Pediatr (Barc). 2014;81:310-7.
-
19Kwan A, Puck JM. History and current status of newborn screening for severe combined immunodeficiency. Semin Perinatol. 2015;39:194-205.
-
20Mazzucchelli JT, Bonfim C, Castro GG, Condino Neto AA, Costa NM, Cunha L, et al. Severe combined immunodeficiency in Brazil: management, prognosis, and BCG associated complications. J Investig Allergol Clin Immunol. 2014;24:184-91.
-
21Wilson JM, Jungner YG. Principles and practice of mass screening for disease. Bol Oficina Sanit Panam. 1968;65:281-393.
-
22Kubiak C, Jyonouchi S, Kuo C, Garcia Lloret M, Dorsey MJ, Sleasman J, et al. Fiscal implications of newborn screening in the diagnosis of severe combined immunodeficiency. J Allergy Clin Immunol Pract. 2014;2:697-702.
-
Financiamento Fundação de Amparo à Pesquisa do Estado de São Paulo (FAPESP), Conselho Nacional de Desenvolvimento Técnico Científico (CNPq), Departamento de Ciência e Tecnologia/Secretaria de Ciência, Tecnologia e Insumos Estratégicos do Ministério da Saúde/Ministério da Saúde (DECIT/SCTIE/MS) e Secretaria da Saúde do Estado de São Paulo (2012/51233-2).
Datas de Publicação
-
Publicação nesta coleção
Jan-Mar 2017
Histórico
-
Recebido
12 Maio 2016 -
Aceito
02 Out 2016





 Fonte: Grupo Brasileiro de Imunodeficiência Primária (BRAGID).
Fonte: Grupo Brasileiro de Imunodeficiência Primária (BRAGID).