Resumos
No período de 1978 a 1996, de um total de 3.259 cães necropsiados, 16 (0,49%) apresentaram parasitismo por Dioctophyma renale. Desses, 12 (75%) eram cães de rua. Em 13 cães (81, 2%), um ou vários parasitas localizavam-se no rim direito. Em 3 casos (18,7%), o parasita foi observado na cavidade abdominal. Nos casos de parasitismo renal, observou-se acentuada atrofia do parênquima, transformando o rim numa bolsa fibrosa contendo o parasita em meio a exsudato necro-hemorrágico semilíquido. Foi observada hipertrofia renal compensatória contralateral em 5 casos. O ciclo evolutivo de D. renale é complexo e incompletamente entendido. Envolve um hospedeiro intermediário e hospedeiros paratênicos. A alta ocorrência da doença em cães de rua sugere que a infecção seja relacionada aos hábitos alimentares pouco seletivos desses animais.
Dioctophyma renale; parasitas; doenças de cães; patologia
From 1978 to 1996, out of a total of 3,259 dogs necropsied, sixteen (0.49%) were parasitized by Dioctophyma renale. Twelve of those (75%) were stray dogs. Thirteen dogs (81.2%) presented one or more specimens of D. renale in the right kidney. In three dogs (18.7%), the parasite was observed in the abdominal cavity. In those cases of renal parasitism, there was marked atrophy of the kidney which became a fibrous-walled bag within which the parasite was found imersed in a semiliquid necro-hemorrhagic exudate. In five cases, compensatory hypertrophy of the contralateral kidney was observed. The life cycle of D. renale is complex and not fully understood. It envolves intermediate and parathenic hosts. The high incidence of the disease in stray dog suggests that the infection is related to the poor selective feeding habits of this kind of dog.
Dioctophyma renale; parasites; diseases of dogs; pathology
DIOCTOFIMOSE EM CÃES: 16 CASOS
DIOCTOPHYMOSIS IN DOGS: 16 CASES
Glaucia Denise Kommers1 1 Médico Veterinário, Professor Assistente, Mestre, Departamento de Patologia, Centro de Ciências da Saúde (CCS), Universidade Federal de Santa Maria (UFSM). Márcia Regina da Silva Ilha2 1 Médico Veterinário, Professor Assistente, Mestre, Departamento de Patologia, Centro de Ciências da Saúde (CCS), Universidade Federal de Santa Maria (UFSM). Claudio Severo Lombardo de Barros3 1 Médico Veterinário, Professor Assistente, Mestre, Departamento de Patologia, Centro de Ciências da Saúde (CCS), Universidade Federal de Santa Maria (UFSM).
RESUMO
No período de 1978 a 1996, de um total de 3.259 cães necropsiados, 16 (0,49%) apresentaram parasitismo por Dioctophyma renale. Desses, 12 (75%) eram cães de rua. Em 13 cães (81, 2%), um ou vários parasitas localizavam-se no rim direito. Em 3 casos (18,7%), o parasita foi observado na cavidade abdominal. Nos casos de parasitismo renal, observou-se acentuada atrofia do parênquima, transformando o rim numa bolsa fibrosa contendo o parasita em meio a exsudato necro-hemorrágico semilíquido. Foi observada hipertrofia renal compensatória contralateral em 5 casos. O ciclo evolutivo de D. renale é complexo e incompletamente entendido. Envolve um hospedeiro intermediário e hospedeiros paratênicos. A alta ocorrência da doença em cães de rua sugere que a infecção seja relacionada aos hábitos alimentares pouco seletivos desses animais.
Palavras-chave:Dioctophyma renale, parasitas, doenças de cães, patologia.
SUMMARY
From 1978 to 1996, out of a total of 3,259 dogs necropsied, sixteen (0.49%) were parasitized by Dioctophyma renale. Twelve of those (75%) were stray dogs. Thirteen dogs (81.2%) presented one or more specimens of D. renale in the right kidney. In three dogs (18.7%), the parasite was observed in the abdominal cavity. In those cases of renal parasitism, there was marked atrophy of the kidney which became a fibrous-walled bag within which the parasite was found imersed in a semiliquid necro-hemorrhagic exudate. In five cases, compensatory hypertrophy of the contralateral kidney was observed. The life cycle of D. renale is complex and not fully understood. It envolves intermediate and parathenic hosts. The high incidence of the disease in stray dog suggests that the infection is related to the poor selective feeding habits of this kind of dog.
Key words:Dioctophyma renale, parasites, diseases of dogs, pathology.
INTRODUÇÃO
O parasitismo pelo nematódeo D. renale (sinônimos: Ascaris renalis, A. visceralis, Strongylus gigas, Eustrongylus gigas), conhecido como verme gigante renal, tem sido descrito em várias espécies animais e no homem (BARRIGA, 1982). Dentre as espécies domésticas, afeta principalmente cães, mas já foi observado em felinos, suínos (OSBORNE et al., 1969), eqüinos e bovinos (BARRIGA, 1982; SOULSBY, 1982). Visons (Mustela vison) são considerados como hospedeiros definitivos (OSBORNE et al., 1969). A doença foi relatada em outras espécies silvestres incluindo martas americanas (Martes americana), coiotes (Canis latrans), raposas (Canis vulpes), lobos (Canis lupus), chacais (Canis mesomelas), doninhas (Mustela nivalis), lontras (Lutra longicaudis), ratos almiscarados (Ondatra zibethica), quatis (Nasua nasua, Procyon lotor), furões (Galictis cuja, Mustela putorius), preguiças (Choloepus didactylus), cachorros do mato (Speothos venaticus), ursos (Ursus ursus) e focas (Arctocephalus australis) (OSBORNE et al., 1969; BARRIGA, 1982; SOULSBY, 1982; LOW, 1995).
No Brasil, o parasitismo pelo D. renale foi descrito no cão, quati (Nasua nasua), furão (Galictis cuja), lontra (Lutra longicaudis), preguiça (Choloepus didactylus) e no lobo guará (Chrysocyon brachiurus) e atinge animais em vários estados brasileiros, dentre eles, São Paulo (PACHECO et al., 1965; ALVARENGA et al., 1984), Rio de Janeiro (MATTOS JÚNIOR & PINHEIRO,1994), Espírito Santo (BARROS, 1971; COSTA et al., 1990), Minas Gerais (COSTA & FREITAS, 1967; FERREIRA NETOet al., 1971; COSTA & LIMA, 1987), Paraná (BARROS et al., 1990), Santa Catarina (NEVES et al., 1983), Rio Grande do Sul (CORREA & BAUER, 1967; GONÇALVES et al., 1961; AMATO et al., 1976; GRAÇA et al., 1980; LARA et al., 1981), Pará (FREIRE, 1979; MIRANDA et al., 1992) e Amazonas (ROCHA et al., 1965).
A epidemiologia do parasitismo pelo D. renale envolve um ciclo evolutivo complexo. Ovos contendo larvas de primeiro estágio devem ser ingeridos por um anelídeo oligoqueta aquático (Lumbriculus variegatus), que é o único hospedeiro intermediário essencial para a continuação do ciclo (BARRIGA, 1982; ANDERSON, 1992). Vários autores citam que oligoquetas branquiobdelídeos (Cambarinocola chirocephala), ectoparasitas de camarões de água doce (lagostim) são também hospedeiros intermediários de larvas de D. renale (OSBORNE et al., 1969). Entretanto, as larvas encontradas nos branquiobdelídeos não são de D. renale (ANDERSON, 1992). Geralmente, o hospedeiro definitivo infecta-se ingerindo anelídeos oligoquetas ou hospedeiros paratênicos (peixes e rãs) infectados (OSBORNE et al., 1969; BARRIGA, 1982; ANDERSON, 1992).
Este trabalho descreve os casos de parasitismo por Dioctophyma renale, diagnosticados no Setor de Patologia Veterinária da Universidade Federal de Santa Maria, discute a epidemiologia e patogenia da infecção, a morfologia e o ciclo do parasita.
MATERIAL E MÉTODOS
Numa revisão dos arquivos do Setor de Patologia Veterinária da Universidade Federal de Santa Maria, no período de 1978 a 1996 (incluindo 4 casos já publicados por GRAÇA et al, 1980) verificou-se o número de cães necropsiados e o número de cães parasitados pelo nematódeo Dioctophyma renale. Nos animais parasitados, foram relacionados a idade, o sexo, a raça, o número de espécimes encontrados, o sexo e localização dos parasitas e o tipo de criação dos cães.
RESULTADOS
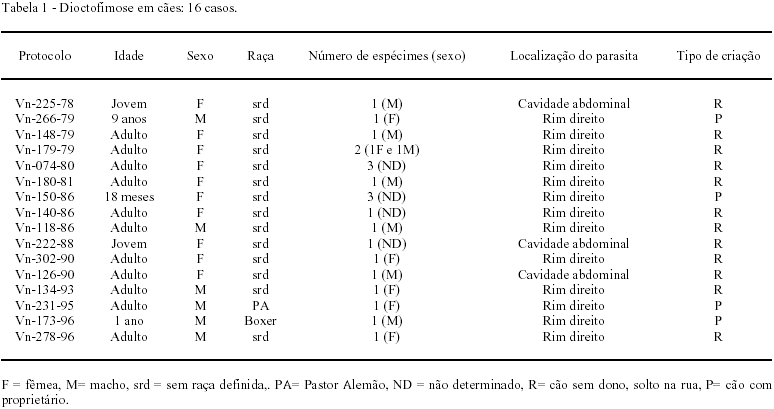
No período estudado, foram necropsiados 3.259 cães, dos quais 16 (0,49%) estavam parasitados por D. renale. A idade dos cães afetados variou entre 1 e 9 anos. Seis cães eram machos e 10 eram fêmeas. Quatorze animais não tinham raça definida, um era Boxer e um outro Pastor Alemão. Parasitismo único foi observado em 12 cães e 4 apresentaram 2 ou 3 parasitas. D. renale foi encontrado na cavidade abdominal em 3 casos e no rim direito em 13. Apenas 4 animais tinham proprietário e 12 eram cães de rua. A distribuição das informações referentes a idade, sexo, raça, tipo de criação e procedência dos cães, bem como número e localização dos parasitas encontram-se na tabela 1.
Quinze cães não apresentaram sinais clínicos sugestivos do parasitismo por D. renale. Nesses casos, os parasitas consistiram de achados incidentais em procedimentos cirúrgicos experimentais ou de necropsia. Um cão (Vn-140-86) apresentou hematúria e emagrecimento progressivo.
As lesões macroscópicas, nos casos de parasitismo renal, eram de atrofia moderada ou acentuada do parênquima, associada à presença de 1 a 3 parasitas adultos. Na maioria dos casos, havia exsudato necro-hemorrágico na pelve, que se encontrava dilatada. Nos casos de atrofia acentuada do parênquima renal, o rim era visto como uma saculação formada por parede lisa, delgada e fibrosa contendo os parasitas (figura 1). No cão Vn-231-95, a pelve do rim direito encontrava-se discretamente dilatada e apresentava uma perfuração com 0,5cm de diâmetro que se estendia até o espaço subcapsular, onde se alojava um parasita adulto. Em 5 cães, com parasitismo no rim direito, observou-se hipertrofia do rim esquerdo. Somente em um caso (Vn-225-78) de parasitismo da cavidade abdominal havia peritonite, diagnosticada durante laparotomia exploratória e confirmada posteriormente na necropsia. Os parasitas apresentavam coloração avermelhada (figura 1). Os machos mediram entre 11 e 26cm de comprimento e tinham uma bolsa copuladora e um espículo. As fêmeas mediram entre 30 e 73cm de comprimento.
Histologicamente, o parênquima renal era delgado e obliterado por tecido conjuntivo fibroso associado a infiltrado inflamatório mononuclear intersticial, atrofia acentuada e perda de glomérulos e túbulos. Em alguns casos, observou-se hiperplasia do epitélio de transição da pelve.
DISCUSSÃO
Nos 16 cães parasitados por D. renale no período estudado (1978-1996), o parasitismo foi um achado de necropsia. Apenas um cão apresentou hematúria e emagrecimento progressivo. Como esses sinais não são exclusivos dessa doença, não foi estabelecido o diagnóstico clínico. De fato, cães afetados geralmente são assintomáticos (OSBORNE et al., 1969; BARRIGA, 1982; COPPO & BREM, 1983; LOW, 1995), porém alguns animais apresentam manifestações clínicas relacionadas com peritonite ou com uremia devido à insuficiência renal (OSBORNE et al., 1969). Andar vacilante, arqueamento do dorso, hematúria, aumento de volume palpável na região renal e emagrecimento são, também, sinais descritos em alguns casos (BARRIGA, 1982). No parasitismo renal por fêmeas do nematódeo, é possível estabelecer o diagnóstico clínico pela presença de ovos na urina dos animais afetados (FERREIRA NETO et al., 1971). A urografia excretora não revela o parasita, mas indica a ausência de função renal no lado atingido (FERREIRA NETO et al., 1971; ALVARENGA et al., 1984). A laparotomia exploratória pode também ser utilizada para o diagnóstico (ANDERSON, 1986).
Observou-se o predomínio do parasitismo renal (lado direito) em relação ao parasitismo na cavidade abdominal. Parasitas adultos têm sido encontrados principalmente nesses locais (OSBORNE et al., 1969; AMATO et al., 1976; HODESSON et al., 1980; BARRIGA, 1982; NEVES et al., 1983), entretanto, há divergência entre os autores quanto ao predomínio de um ou de outro local. A localização dos parasitas adultos no hospedeiro definitivo parece estar relacionada com o local de penetração das larvas infectantes no trato alimentar. Se as larvas atravessam a parede gástrica na curvatura menor, podem desenvolver-se entre os lobos do fígado. Quando penetram na curvatura maior, vão para o rim esquerdo. Se penetram na parede duodenal, os parasitas adultos desenvolvem-se no rim direito (OSBORNE et al., 1969), sendo essa, possivelmente, a rota mais utilizada nos casos estudados.
Outras localizações pouco freqüentes do D. renale adulto são rim esquerdo, bexiga, uretra, bolsa escrotal, tecido subcutâneo inguinal, útero, ovário, linfonodo mesentérico, glândula mamária, cavidade torácica e pericárdio (OSBORNE et al., 1969; BARROS, 1971; FREIRE, 1979; BARRIGA, 1982; NEVES et al., 1983; ALVARENGA et al., 1984; MIRANDA et al., 1992; MATTOS JÚNIOR & PINHEIRO, 1994). O parasita pode, também, penetrar no ureter e sair para o exterior através da uretra, perfurar a cápsula renal e cair na cavidade abdominal (ANDERSON, 1986) ou atravessar a parede abdominal (BARRIGA, 1982).
As lesões macroscópicas dependem da localização dos parasitas. No parasitismo renal, nos casos estudados, o parênquima encontrava-se destruído e atrofiado, associado à acentuada dilatação da pelve. Enzimas proteolíticas e lipolíticas liberadas pelas glândulas esofágicas do parasita (OSBORNE et al., 1969) possibilitam a penetração e a destruição do parênquima renal. Um fluido necro-hemorrágico acumula-se na pelve renal, podendo ser rico em ovos se o rim estiver parasitado por fêmeas do nematódeo (ANDERSON, 1992; LOW, 1995). Pode ocorrer hidronefrose devido à obstrução do ureter (BARRIGA, 1982). Nos casos em que o rim direito ficou reduzido a uma cápsula fibrosa contendo os parasitas, o rim esquerdo apresentou hipertrofia compensatória. Os achados macroscópicos no parasitismo renal desse estudo são semelhantes aos de outros autores (PACHECO et al., 1965; BARRIGA, 1982; NEVESet al., 1983). Na cavidade abdominal, geralmente os parasitas são achados acidentais em cirurgias ou necropsias. Em apenas um cão desse estudo, observou-se peritonite, que ocorre nos casos em que há ruptura de órgãos por ação de enzimas liberadas pelo nematódeo (OSBORNE et al., 1969). A presença de fêmeas de D. renale na cavidade abdominal é acompanhada pela presença de grande quantidade de ovos, os quais também contribuem para a peritonite (ANDERSON, 1992).
A identificação do parasita foi baseada em suas características morfológicas, destacando-se o tamanho, a coloração e a presença da bolsa copuladora nos machos. O D. renale adulto apresenta-se avermelhado, medindo, os machos, entre 14 e 45cm de comprimento por 3 a 4mm de diâmetro e as fêmeas, com 20 a 100cm de comprimento por 5 a 12mm de diâmetro. Os machos possuem uma bolsa copuladora na extremidade posterior em forma de sino, não sustentada por raios, e um espículo com 0,5 a 0,6cm de comprimento. As fêmeas apresentam a extremidade posterior romba, ânus terminal, um ovário e a vulva distando de 5 a 7cm da extremidade anterior. Os ovos, encontrados na urina dos animais parasitados, são elípticos, castanhos, medem 60-80x 39-46mm, têm uma casca espessa e com depressões, exceto nos pólos (BARRIGA, 1982).
As lesões histológicas no parênquima renal caracterizaram-se por necrose, reação inflamatória mononuclear, atrofia e fibrose. Metaplasia óssea, como observada na parede dorsal dos rins afetados em furões (Mustela putorius) e em visons (M. vison) (MACE, 1975), não foi vista nos cães desse estudo. Hiperplasia do epitélio de revestimento da pelve do rim parasitado, como observada em alguns dos cães estudados, foi, também, observada em visons (KUMAR et al., 1972). Em muitos casos de parasitismo por D. renale, o rim atingido fica completamente destruído e a sobrevivência dos animais afetados depende da integridade e da hipertrofia do rim contralateral. (OSBORNE et al., 1969).
O predomínio do parasitismo único visto neste estudo, também foi observado por outros, sendo o cão considerado um hospedeiro definitivo anormal e terminal, uma vez que o ciclo de vida do parasita é interrompido. Os visons são considerados hospedeiros definitivos e reservatórios de D. renale na natureza, devido à presença de grande número de parasitas de ambos os sexos e por esses localizarem-se, geralmente, nos rins, favorecendo a liberação de ovos férteis para o meio ambiente, perpetuando o ciclo (OSBORNE et al., 1969; BARRIGA, 1982).
Observou-se que 12 cães (75%) eram animais de rua. O parasitismo mais freqüente em cães de rua, os quais têm hábitos alimentares pouco seletivos, foi observado, também, no Irã (ZAKARIAN & SHAFAII-TONKABONI, 1972). Pode-se supor, então, que esses animais tenham se infectado ingerindo diretamente o hospedeiro intermediário (anelídeo oligoqueta) ou hospedeiros paratênicos como peixes (ou suas vísceras) e rãs. Os mustelídeos, principalmente os visons, normalmente alimentam-se de peixes e rãs, o que favorece a manutenção do ciclo do parasita. Outra possibilidade considerada, nos casos de parasitismo em visons, é que as larvas infectantes possam ser transmitidas ao longo da cadeia alimentar dos hospedeiros paratênicos e definitivos, visto que foram encontradas em ratos almiscarados (hospedeiros definitivos) que infectaram visons e em peixes predadores que ingeriram peixes infectados (BARRIGA, 1982). A possibilidade de transmissão ao longo da cadeia alimentar dos hospedeiros paratênicos e definitivos permite que se questione outras fontes de infecção para cães, principalmente para os animais que perambulam pelas ruas alimentando-se do que estiver disponível nos locais por onde passam. Dentre essas fontes de infecção alternativas, deve-se considerar que roedores domésticos fazem parte dos hábitos alimentares de cães de rua e que estudos realizados no Japão revelaram o parasitismo por D. renale em ratazanas (Rattus norvegicus) (TANIGUCHI et al., 1976; TANIGUCHIet al., 1977). Esses roedores vivem em locais próximos à água, sendo que os esgotos constituem um ambiente onde as ratazanas vivem e se reproduzem com êxito (SILVA, 1994). O regime alimentar amplo e a proximidade com a água devem favorecer a infecção de ratazanas, que podem estar envolvidas na rota de infecção de cães de rua, uma vez que são abundantes nos centros habitacionais.
Dentre as espécies silvestres em que já foi verificada dioctofimose, no Brasil e em outros países, várias delas, como o lobo-guará (COSTA & FREITAS, 1967; PALLARES & VALESE, 1970; KUMAR et al., 1972), alimentam-se com freqüência de roedores (SILVA,1994). Entretanto, não há estudos sobre a possibilidade de envolvimento desses roedores na rota do parasitismo pelo D. renale. A infecção de herbívoros parece dever-se à ingestão acidental de anelídeos oligoquetas infectados e no homem está associada à ingestão de peixes ou rãs mal cozidos (BARRIGA, 1982).
Em cães, as tentativas de reproduzir reinfecção em animais ainda parasitados falharam (OSBORNE et al., 1969; BARRIGA, 1982), parecendo que os animais infectados desenvolvem certo grau de imunidade ao parasita. O único tratamento eficaz é a remoção cirúrgica do parasita e, em alguns casos, do rim afetado (OSBORNE et al., 1969; FERREIRA NETO, 1971; ANDERSON, 1986).
2 Aluno de Curso de Medicina Veterinária, UFSM. Bolsista de IC (CNPq) no Departamento de Patologia.
3 Médico Veterinário, Professor Titular, PhD., Departamento de Patologia, CCS, UFSM, Santa Maria, RS, 97105-900. E-mail: cslb@sm.conex.com.br. Autor para correspondência.
Recebido para publicação em 24.08.98. Aprovado em 04.11.98
- ALVARENGA, J., MATERA, J.M., BARROS, P.S.M. et al. Dioctophyma renale in a dog. Mod Vet Pract, v. 65, n. 2, p. 125, 1984.
- AMATO, J.F.R., GRISI, L., ROSA, V.L.M. Reuniăo dos casos brasileiros dedioctofimose canina, com o registro do caso de mais alta intensidade de infecçăo por Dioctophyma renale (GOEZE, 1782). Rev Bras Biol, v. 36, n. 1, p. 117-122, 1976.
- ANDERSON, H.M. Giant kidney worm infection in a dog. Mod Vet Pract, v. 67, n. 2, p. 153-154, 1986.
- ANDERSON, R.C. Nematode parasites of vertebrates - their development and transmission. Cambridge: CAB International, 1992, p. 533-539.
- BARRIGA, O.O. Dioctophymosis. In: SCHULTZ, M.G. CRC Handbook series in zoonoses Florida: CRC, 1982. p. 83-92.
- BARROS, D.M., LORINI, M.L., PERSSON, V.G. Dioctophymosis in the little Grison (Galictis cuja). J Wildlife Dis, v. 26, n. 4, p. 538-539, 1990.
- BARROS, G.C. Dioctophyme renale (GOEZE,1782) em căo no Estado do Espírito Santo. Arq Esc Vet, v. 23, p. 195-196, 1971.
- COPPO, J.A., BREM, J.J. Canine dioctophymosis in the north east of Argentine. Rev Inst Med Trop Săo Paulo, v. 25, n. 5, p. 259-262, 1983.
- CORREA, O., BAUER, A. Dioctofimose canina. Rev Fac Agron Vet UFRGS, v. 5, p. 37-41, 1967.
- COSTA, H.M.A., FREITAS, M.G. Alguns helmintos parasitos do guará [Chrysocyon brachiurus (Illiger)], com a descriçăo de Molineus brachiurus N. sp. (Nematoda - trichostrongylidae). Arq Esc Vet, v. 14, p. 25-29, 1967.
- COSTA, H.M.A., LIMA, W.S. Dioctophyme renale (GOEZE, 1782): ocorręncia em Minas Gerais. Arq Bras Med Vet Zoot, v. 39, n. 6, p. 959-962,1987.
- COSTA, J.O., GUIMARĂES, M.P., LIMA, W.S. et al.Freqüęncia de endo e ectoparasitos de căes capturados nas ruas de Vitória - ES - Brasil. Arq Bras Med Vet Zoot, v. 42, n. 5, p. 451-452, 1990.
- FERREIRA NETO, J.M., NUNES, L.P., BERNIS, W.O. et al. Observaçőes clínicas da dioctofimose em um căo e transplantaçăo do parasito. Arq Esc Vet, v. 23, p. 29-35, 1971.
- FREIRE, N.M.S. Ocorręncia de Dioctophyma renale (Goeze, 1782) parasitando Canis familiaris L. em Belém do Pará. Atas Soc Biol Rio de Janeiro, v. 20, p. 31-32, 1979.
- GONÇALVES, P.C., BARROS, S.S., SIQUEIRA, C.S. Sobre a presença de Dioctophyme renale (Goeze, 1782) no Rio Grande do Sul (Nematoda, Dioctophymoidea). Rev Fac Agron Vet Porto Alegre, v.4, p. 44-49, 1961.
- GRAÇA, D.L., COPELLO, R.A., SANTOS, M.N. Dioctofimose canina no Rio Grande do Sul. Descriçăo de 4 casos. Rev Centro Cięncias Rurais, v. 10, n. 3, p. 231-233, 1980.
- HODESSON, D.L., DANIELS, R.B., RICHARDS, B. Dioctophyma renale in a dog (a case report). Vet Med Small Anim Clin, v. 75, n. 5, p. 825, 1980.
- KUMAR, V., VERCRUYSSE, J., VANDESTEENE, R. Studies on two cases of Dioctophyma renale (Goeze, 1782) infection in Chrysocyon brachyurus (Illiger). Acta Zool Patol Antverpiensia, v. 56, p. 83-98, 1972.
- LARA, S.I.M., TAROUCO, M.R.R., RIBEIRO, P.B. Helmintos parasitos de Canis familiaris de Pelotas - Rio Grande do Sul. Arq Esc Vet UFMG, v. 33, n. 2, p. 293-297, 1981.
- LOW, D.G. Parasites of the upper and lower urinary tract of the dogs and cats. In: OSBORNE, C.A., FINCO, D.R. Canine and feline nephrology and urology. Baltimore: William & Wilkins, 1995. p. 917-921.
- MACE, T.F.A. Studies on the biology of the giant kidney worm, Dioctophyma renale (Goeze,1782) (Nematoda - Dioctophymoidea). Dissertation Abstracts International, v. 36 B: n. 1, p. 126-127, 1975.
- MATTOS JÚNIOR, D.G., PINHEIRO, J. Dioctophyma renale (Goeze, 1782) no tecido subcutâneo da regiăo inguinal de um căo. Arq Bras Med Vet Zoot, v. 46, p. 301-302, 1994.
- MIRANDA, M.A., BENIGNO, R.N.M., GALVĂO, G.R. et al. Dioctophyma renale (Goeze, 1782): localizaçăo ectópica e alta intensidade parasitária em Canis familiaris do Pará - Brasil. Arq Bras Med Vet Zoot, v. 44, n. 2, p. 151-153, 1992.
- NEVES, D.S., MORAIS, A.N., NOGUEIRA, R.H.G. et al.Ocorręncia de Dioctophyme renale (Goeze, 1782) em căes da regiăo de Lages, Estado de Santa Catarina, Arq Bras Med Vet Zoot, v. 35, n. 5, p. 665-673, 1983.
- OSBORNE, C.A., STEVENS, J.B., HANLON, G.F. et al. Dioctophyma renale in a dog. J Am Vet Med Assoc, v. 155, n. 4, p. 605-620, 1969.
- PACHECO, A.C., CIRNE, B.R., CORRĘA, W.M. Dioctofimíase em căes na regiăo de Botucatu - Săo Paulo. Arq Inst Biol, v. 32, n. 1, p. 1-7, 1965.
- PALLARES, R.M., VALESE, S. Multiple parasitación por Dioctophyma renale en un rińón de un Chrysocyon brachyurus Rev Parag Microb, v. 51, n. 1, p. 82-83, 1970.
- ROCHA, U.F., SERRA, R.G., GRECHI, R. Parasitismo por Dioctophyme renale (Goeze, 1782) em preguiça, Choloepus didactylus Linnaeus, 1758. Rev Fac Farm Bioq Săo Paulo, v. 3, n. 2, p. 325-334, 1965.
- SILVA, F. Mamíferos silvestres -Rio Grande do Sul. 2 ed. Porto Alegre: Fundaçăo Zoobotânica do Rio Grande do Sul, 1994, p. 184-185.
- SOULSBY, E.J. L. Helminths, arthropods and protozoa of domesticated animals 7 ed. London: Bailličre Tindall, 1982. p. 343-344.
- TANIGUCHI, M., IKENOUE, S., SUMITA, N. et al. Discovery of Dioctophyma renale (Goeze, 1782) from a brown rat. Bull Coll Agric Vet Med Nihon Univ, v. 33, p. 300-305, 1976.
- TANIGUCHI, M., MATSUI, K., SUMITA, N. et al. A survey of parasitic helminths from house rodents in the area of Setagaya-Ku, Tokyo. Bull Coll Agric Vet Med Nihon Univ, n. 34, p. 202-217, 1977.
- ZAKARIAN, B., SHAFAII-TONKABONI, J. Dioctophymosis in Iran. Br Vet J, v. 128, p. 446-451, 1972.
Datas de Publicação
-
Publicação nesta coleção
11 Dez 2006 -
Data do Fascículo
Set 1999
Histórico
-
Aceito
04 Nov 1998 -
Recebido
24 Ago 1998