Resumos
O Trypanosoma evansi é um protozoário hemoflagelado que causa, em várias espécies, uma doença caracterizada por altos níveis de parasitemia, com rápido desenvolvimento de anemia. Este trabalho teve como objetivo investigar a relação entre o grau de parasitemia e a alteração na eritropoese de ratos (Rattus norvegicus) da linhagem Wistar infectados experimentalmente com T. evansi. Foram utilizados 42 ratos, dos quais 36 foram inoculados pela via intraperitoneal com 0,2ml de sangue, contendo 2,5 x 104 parasitas. Seis ratos não-inoculados foram utilizados como controles. Após inoculação, a parasitemia foi avaliada a cada 12h. Os grupos para análise foram estipulados de acordo com a média de tripanossomas em 10 campos homogêneos focados aleatoriamente, sendo: A, controle; B, animais que apresentaram um grau de parasitemia entre 1-10 tripanossomas/campo; C, ratos com 11-20 tripanossomas/campo; D, ratos com 21-30 tripanossomas/campo; E, ratos com 31-40 tripanossomas/campo; F, 41-50 tripanossomas/campo; e G, ratos com mais de 51 tripanossomas/campo. Quando os animais apresentaram o número de protozoários equivalente ao grupo, foram coletadas amostras de sangue para realização de hemograma e dosagem de ferro, e foi realizada citologia de medula óssea para avaliação da relação mielóide:eritróide. A análise estatística mostrou redução significativa das hemácias e do hematócrito a partir de 31 tripanossomas/campo (grupos E, F e G; P<0,005) e a redução de hemoglobina ocorreu a partir de 41 tripanossomas/campo (grupos F e G; P<0,005). A relação mielóide:eritróide foi reduzida de 0,7 para 0,6 a partir de 41 tripanossomas/campo (grupos F e G; P<0,005). Não foram detectadas variações na concentração de ferro. Os dados obtidos demonstraram que ratos com parasitemia acima de 31 tripanossomas por campo desenvolvem uma anemia aguda, com um aumento compensatório na atividade hematopoética.
Tripanossomíase; hematologia; atividade hematopoética; ferro sérico; medula óssea; Rattus norvegicus
Trypanosoma evansi is a flagellate protozoan that causes a disease characterized by high parasitemia and acute anemia in various species. This study was aimed at evaluating and establishing a relationship between different parasitemia levels and eritropoyesis in Wistar rats (Rattus norvegicus) experimentally infected by T. evansi. Forty two animals were used. In 36 animals parasites were inoculated by intraperitoneal blood injection of 0.2ml containing 2.5x104 parasites. Six non-inoculated animals were used as controls. Parasitemia was evaluated every 12 hours and the animals were allocated in groups according to parasitemia levels. Then they were classified according to average number of parasites in 10 random homogeneous fields, Group A: control (not-inoculated); B: rats with 1-10 trypanosomes/field; C: 11-20 trypanosomes/field; D: 21-30 trypanosomes/field; E: 31-40 trypanosomes/field; F: 41-50 trypanosomes/field; G: more then 51. Blood samples were taken when the animals reached the correspondent group number of parasites. Hemogram and iron levels were evaluated and a bone marrow cytology was performed to detect the myeloid:erythroid ratio. Statistical analysis showed a significant reduction on red blood cells count and hematocrit from group E on and also hemoglobin on groups F and G. The myeloid:erythroid ratio reduced from 0.7 to 0.6 on groups F and G (P<0.005). Iron levels alterations were not detected. These data showed that Wistar rats with parasitemia higher then 31 parasites per field have an acute anemia associated to a compensatory hematopoietic activity.
Trypanosomiasis; hematology; hematopoietic activity; seric iron; bone marrow; Rattus norvegicus
ARTIGOS CIENTÍFICOS
CLÍNICA E CIRURGIA
Resposta eritropoética de ratos em diferentes graus de parasitemia por Trypanosoma evansi
Erithropoietic response in Trypanosoma evansi infected rats with different parasitaemia intensity
Patrícia WolkmerI,1 1 Autor para correspondência. ; Aleksandro Schafer da SilvaII; Juliana Felipetto CargneluttiI; Márcio Machado CostaII; Carolina Kist TraeselI; Sonia Terezinha dos Anjos LopesIII; Sílvia Gonzalez MonteiroIV
IPrograma de Pós-graduação em Medicina Veterinária, Universidade Federal de Santa Maria (UFSM). Avenida Roraima, n. 1000, Hospital Veterinário, sala 107, 97105-900, Santa Maria, RS, Brasil. E-mail: patiwol@hotmail.com
IICurso de Medicina Veterinária, UFSM, Santa Maria, RS, Brasil
IIIDepartamento de Clínica de Pequenos Animais, UFSM, Santa Maria, RS, Brasil
IVDepartamento de Microbiologia e Parasitologia, UFSM, Santa Maria, RS, Brasil
RESUMO
O Trypanosoma evansi é um protozoário hemoflagelado que causa, em várias espécies, uma doença caracterizada por altos níveis de parasitemia, com rápido desenvolvimento de anemia. Este trabalho teve como objetivo investigar a relação entre o grau de parasitemia e a alteração na eritropoese de ratos (Rattus norvegicus) da linhagem Wistar infectados experimentalmente com T. evansi. Foram utilizados 42 ratos, dos quais 36 foram inoculados pela via intraperitoneal com 0,2ml de sangue, contendo 2,5 x 104 parasitas. Seis ratos não-inoculados foram utilizados como controles. Após inoculação, a parasitemia foi avaliada a cada 12h. Os grupos para análise foram estipulados de acordo com a média de tripanossomas em 10 campos homogêneos focados aleatoriamente, sendo: A, controle; B, animais que apresentaram um grau de parasitemia entre 1-10 tripanossomas/campo; C, ratos com 11-20 tripanossomas/campo; D, ratos com 21-30 tripanossomas/campo; E, ratos com 31-40 tripanossomas/campo; F, 41-50 tripanossomas/campo; e G, ratos com mais de 51 tripanossomas/campo. Quando os animais apresentaram o número de protozoários equivalente ao grupo, foram coletadas amostras de sangue para realização de hemograma e dosagem de ferro, e foi realizada citologia de medula óssea para avaliação da relação mielóide:eritróide. A análise estatística mostrou redução significativa das hemácias e do hematócrito a partir de 31 tripanossomas/campo (grupos E, F e G; P<0,005) e a redução de hemoglobina ocorreu a partir de 41 tripanossomas/campo (grupos F e G; P<0,005). A relação mielóide:eritróide foi reduzida de 0,7 para 0,6 a partir de 41 tripanossomas/campo (grupos F e G; P<0,005). Não foram detectadas variações na concentração de ferro. Os dados obtidos demonstraram que ratos com parasitemia acima de 31 tripanossomas por campo desenvolvem uma anemia aguda, com um aumento compensatório na atividade hematopoética.
Palavras-chave: Tripanossomíase, hematologia, atividade hematopoética, ferro sérico, medula óssea, Rattus norvegicus.
ABSTRACT
Trypanosoma evansi is a flagellate protozoan that causes a disease characterized by high parasitemia and acute anemia in various species. This study was aimed at evaluating and establishing a relationship between different parasitemia levels and eritropoyesis in Wistar rats (Rattus norvegicus) experimentally infected by T. evansi. Forty two animals were used. In 36 animals parasites were inoculated by intraperitoneal blood injection of 0.2ml containing 2.5x104 parasites. Six non-inoculated animals were used as controls. Parasitemia was evaluated every 12 hours and the animals were allocated in groups according to parasitemia levels. Then they were classified according to average number of parasites in 10 random homogeneous fields, Group A: control (not-inoculated); B: rats with 1-10 trypanosomes/field; C: 11-20 trypanosomes/field; D: 21-30 trypanosomes/field; E: 31-40 trypanosomes/field; F: 41-50 trypanosomes/field; G: more then 51. Blood samples were taken when the animals reached the correspondent group number of parasites. Hemogram and iron levels were evaluated and a bone marrow cytology was performed to detect the myeloid:erythroid ratio. Statistical analysis showed a significant reduction on red blood cells count and hematocrit from group E on and also hemoglobin on groups F and G. The myeloid:erythroid ratio reduced from 0.7 to 0.6 on groups F and G (P<0.005). Iron levels alterations were not detected. These data showed that Wistar rats with parasitemia higher then 31 parasites per field have an acute anemia associated to a compensatory hematopoietic activity.
Key words: Trypanosomiasis, hematology, hematopoietic activity, seric iron, bone marrow, Rattus norvegicus.
INTRODUÇÃO
As tripanossomíases são causadas por espécies do gênero Trypanosoma, que pertencem ao filo Euglenozoa, da classe Mastigophora, ordem Kinetoplastida, subordem Trypanosomatina. A característica principal desses protozoários é a presença de um cinetoplasto localizado na base do flagelo, que contém o DNA mitocondrial (VICKERMAN, 1976). A subordem Trypanosomatina contém uma única família, Trypanosomatidae, que, por sua vez, contém oito gêneros (Trypanosoma, Leishmania, Endotrypanum, Crithidia, Blastocrithidia, Leptomonas, Herpetomonas e Phytomonas). Os tripanossomas patogênicos de importância na pecuária estão classificados na seção Salivaria, dos quais apenas o Trypanosoma vivax, Trypanosoma equiperdum e Trypanosoma evansi foram encontrados na América do Sul (SILVA et al., 2002).
T. evansi afeta muitas espécies de animais domésticos e selvagens (FRANKE et al., 1994). Sua transmissão é essencialmente mecânica. O protozoário é transferido de um hospedeiro mamífero a outro por insetos picadores, principalmente tabanídeos e Stomoxys sp., e por morcegos hematófagos (HOARE, 1972). Existe também a possibilidade de transmissão por carrapatos (CAMARGO et al., 2004).
T. evansi pode ser observado intercelularmente em tecidos, no plasma sangüíneo e em fluidos das cavidades corporais dos animais infectados (SHARMA et al., 2000). As alterações causadas pela infecção do T. evansi são multifatoriais e vários sinais clínicos são descritos nos hospedeiros, incluindo a elevação da temperatura corporal, a perda da condição física, a fraqueza e alterações neurológicas (NGERANWA et al., 1993). A anemia é comumente descrita e caracterizada por redução nos valores de eritrócitos, hemoglobina e hematócrito. Contudo, as causas da anemia não estão completamente esclarecidas (SILVA et al., 1995; MARQUES et al., 2000; AQUINO et al., 2002) e os mecanismos propostos são eritrofagocitose, destruição dos eritrócitos pelo sistema imune, fragilidade osmótica dos eritrócitos, hemodiluição e depressão da eritropoese (CLARKSON, 1968; JATKAR & PUROHIT, 1971; ASSOKU, 1975; JENKINS & FACER 1985; SHARMA et al., 2000; AQUINO et al., 2002).
Embora existam vários trabalhos que descrevam a tripanossomíase, ainda há lacunas no conhecimento a respeito das alterações patológicas e da eritropoese dos animais infectados por diferentes espécies de tripanossomas, incluindo o T. evansi (SILVA et al., 1995; SHARMA et al. 2000; AQUINO et al., 2002). O objetivo deste trabalho é investigar a relação entre o grau de parasitemia e a alteração na eritropoese, através da análise citológica da medula óssea, do hemograma e da determinação da concentração de ferro sérico de ratos (Rattus norvegicus) da linhagem Wistar experimentalmente infectados com T. evansi.
MATERIAL E MÉTODOS
Foram utilizados 42 ratos da espécie Rattus norvegicus, da linhagem Wistar, sendo 21 machos com 70 dias (250 a 300g) e 21 fêmeas com 75 dias (100 a 180g). Os animais eram mantidos em gaiolas, separados por sexo, com temperatura e umidade controlada (25°C e 80% UR). Os animais tiveram livre acesso à água e ao alimento (ração comercial para roedores) durante todo o experimento, sendo previamente avaliados quanto à ausência de hemoparasitos, endoparasitos e ectoparasitos. O isolado do Trypanosoma evansi foi proveniente de cães infectados naturalmente do município de Uruguaiana, RS (COLPO et al., 2005), e mantido em laboratório sob cultura viva em ratos Wistar.
Trinta e seis ratos foram inoculados pela via intraperitoneal com 0,2ml de sangue, proveniente de um rato infectado experimentalmente, contendo 2,5 x 104 parasitas, segundo metodologia descrita por ASSOKU (1975). Seis ratos, utilizados como controle, receberam 0,2ml de solução fisiológica pela mesma via. A parasitemia foi avaliada a cada 12h após inoculação, através da pesquisa microscópica do esfregaço de sangue periférico, conforme SILVA et al. (2006). As lâminas foram coradas por panótico rápidoa e observadas em microscópio óptico de luz no aumento de 1.000 vezes, estipulando-se a média de tripanossomas em dez campos homogêneos (considerando as hemácias), focados aleatoriamente. Foram constituídos sete grupos com seis animais, de ambos os sexos, uniformizados, sendo Grupo A, controle (não-inoculado); Grupo B, animais que apresentaram um grau de parasitemia entre 1-10 tripanossomas/campo; Grupo C, ratos com 11-20 tripanossomas/campo; Grupo D, ratos com 21-30 tripanossomas/campo; Grupo E, ratos com 31-40 tripanossomas/campo; Grupo F, 41-50 tripanossomas/campo; e Grupo G, ratos com mais de 51 tripanossomas/campo.
Quando os animais apresentavam o número de protozoários por campo equivalente ao grupo, eram anestesiados, em câmara éter etílico, para coleta de sangue por punção cardíaca, realizada eutanásia e necropsiados. O sangue foi armazenado em tubos com e sem anticoagulante, ácido etilenodiaminotetracético (EDTA) a 10%, para análise hematológica e dosagem de ferro sérico, respectivamente. Imediatamente após a coleta, as amostras sem anticoagulante foram centrifugadas e o soro congelado a -20°C. Para dosagem de ferro sérico, foi utilizado kit comercialb.
Os parâmetros hematológicos analisados neste trabalho foram o número de hemácias, o hematócrito (Ht), o volume corpuscular médio (VCM), a concentração de hemoglobina (Hb), a concentração de hemoglobina corpuscular média (CHCM) e os reticulócitos. Os esfregaços sanguíneos foram corados por panótico rápido para a avaliação citológica. Para a contagem de reticulócitos, foi utilizado corante supravital azul de metileno e contracorado com panótico rápido. As determinações do hematócrito, a contagem de reticulócitos e o cálculo dos índices hematimétricos foram efetuados de acordo com a técnica descrita por FELDMAN et al. (2000). A contagem de hemácias e a determinação da concentração de hemoglobina foram realizadas em aparelho de contagem celular eletrônico, da marca CELM - modelo CC 550.
A coleta da medula óssea foi realizada por secção da epífise proximal do fêmur direito, curetagem e impressão do tecido em lâminas, sendo estas coradas com panótico rápido. As amostras foram obtidas em até 30 min após o sacrifício dos animais. A atividade hematopoética foi avaliada em todos os animais pela relação mielóide:eritróide (M:E), segundo TYLER & COWELL (1989).
As variáveis dependentes dos diferentes grupos foram comparadas por análise de variância, utilizando o programa Proc GLM do pacote estatístico SAS (Statistical Analisis System, versão 9.1 para Windows; SAS Institute, Cary, NC, USA). Os resultados estão expressos na forma de médias, que foram comparadas por Lsmeans. Diferenças entre grupos foram consideradas significativas quando P<0,005.
RESULTADOS E DISCUSSÃO
Ratos Wistar são considerados modelos apropriados para estudos com Trypanosoma evansi por apresentarem a parasitemia típica dos tripanossomas (QUEIROZ et al., 2000). O T. evansi foi detectado no sangue periférico de todos os ratos 24h após a inoculação intraperitoneal do parasito. O grau de parasitemia aumentou progressivamente e 5 dias após a inoculação todos os grupos já haviam sido constituídos (Figura 1). Sinais clínicos, como apatia, fraqueza e anorexia, foram observados nos grupos a partir de 41 tripanossomas/campo (F e G), demonstrando que esta linhagem de ratos possui extrema suscetibilidade a infecções por T. evansi, que produz uma síndrome aguda. Resultados semelhantes, também em ratos, foram relatados por ASSOKU (1975), QUEIROZ et al. (2000, 2001) e AL-MOHAMMED (2006).
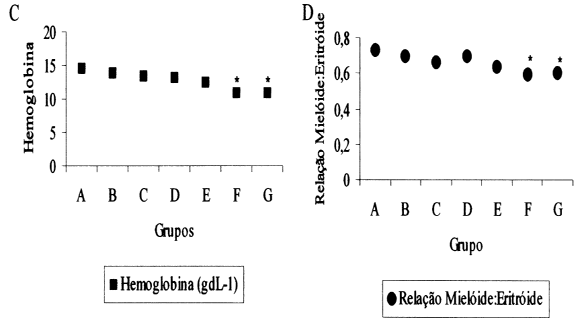
A alteração hematológica mais marcante que ocorreu durante a infecção foi a redução na contagem de eritrócitos (Figura 2A), no Ht (Figura 2B) e na Hb (Figura 2C) dos animais infectados. Observou-se uma redução das hemácias e do Ht a partir de 31 tripanossomas/campo (grupos E, F e G; P<0,005) e redução da Hb a partir de 41 tripanossomas/campo (grupos F e G; P<0,005), indicando anemia nos animais infectados. A anemia é a característica mais comum em infecções por tripanossomas e já foi descrita em ovelhas, cabras, cães, coatis (Nasua nasua), camelos e búfalos (ONAH et al., 1996; SHARMA et al., 2000; AQUINO et al., 2002, HERRERA et al., 2002; ATARHOUCH et al., 2003; HILALI et al., 2006).
As médias do VCM e da CHCM não variaram entre os grupos de animais infectados e não infectados, caracterizando uma anemia normocítica normocrômica. Esses dados são semelhantes aos encontrados por MENEZES et al. (2004), em camundongos, e diferem dos de ASSOKU (1975), que observou anemia macrocítica hipocrômica em ratos. Contudo, reticulócitos foram observados em todos os grupos, ocorrendo um aumento progressivo a partir de 31 tripanossomas/campo (grupos E, F e G; P<0,005; Figura 2E), indicando anemia regenerativa. Além disso, foi evidenciada policromasia em alguns animais dos grupos F e G. A reticulocitose geralmente ocorre 3 ou 4 dias após hemólise aguda ou episódio de hemorragia, e uma resposta máxima pode levar uma a duas semanas (JAIN, 1993). A anemia nos ratos infectados com T. evansi tem caráter agudo, sendo que o grupo com maior parasitemia foi formado em até cinco dias após a infecção. Sendo assim, os animais ainda não haviam atingido o pico de produção de reticulócitos, mantendo os cálculos do VCM e da CHCM dentro da normalidade (normocítica e normocrômica).
A citologia da medula óssea revelou um aumento compensatório na atividade hematopoética nos grupos com maior grau de parasitemia (F e G). A relação M:E (Figura 2D) foi reduzida de 0,7 para 0,6 a partir de 41 tripanossomas/campo (grupos F e G; P<0,005), indicando que ocorreu resposta medular à anemia. A hiperplasia da medula óssea em ratos infectados por T. evansi foi reportada por SEN et al. (1959) e ASSOKU (1975), que demonstraram a ocorrência de aumento da produção de eritrócitos e, conseqüentemente, aumento de reticulócitos no sangue periférico. Essa anemia pode ser causada por injúria dos eritrócitos sob o efeito da hemolisina secretada por Trypanosoma sp. (FIENNES et al., 1946). NADIUM & SOLIMAN (1967) e WALIA et al. (1996) relataram que a enzima sialidase do tripanossoma é a principal causadora de injúria celular, resultando em destruição dos eritrócitos no fígado, no baço, nos pulmões, nos linfonodos e na medula óssea. Outra possibilidade seria uma alteração na produção de eritrócitos por seqüestro de ferro por macrófagos, acarretando uma anemia (DARGIE et al., 1979). Porém, neste experimento, não foram observadas variações na concentração de ferro nos animais estudados.
CONCLUSÕES
Este estudo demonstra que ratos da espécie Rattus norvegicus da linhagem Wistar apresentam uma correlação positiva entre o grau de parasitemia de Trypanosoma evansi e alterações na eritropoese. Os animais desenvolvem uma anemia aguda, a partir de 31 tripanossomas por campo, e a severidade da anemia está correlacionada ao grau de parasitas no sangue, sendo que, quanto maior o grau de parasitemia, maior a anemia nos ratos desta linhagem. Foi demonstrado também um aumento compensatório na atividade hematopoética em animais com maior grau de parasitemia, sem redução nos valores séricos de ferro.
APROVAÇÃO DO BEM ESTAR ANIMAL
O presente experimento foi aprovado pelo Comitê de Ética e Bem-Estar Animal do Centro de Ciências Rurais da Universidade Federal de Santa Maria (CCR/UFSM), n°23081.002689/2006-53, de acordo com legislação vigente e os Princípios Éticos publicados pelo Colégio Brasileiro de Experimentação Animal (COBEA).
FONTES DE AQUISIÇÃO
aLaborclin, Pinhais - PR bLabtest Diagnóstico S.A., Lagoa Santa MG.
Recebido para publicação 17.11.06
Aprovado em 07.03.07
- AQUINO, L.P.C.T. et al. Hematological, biochemical and anatomopathological aspects of the experimental infection with Trypanosoma evansi in dogs. Arquivo Brasileiro de Medicina Veterinária e Zootecnia, v.54, n.1, p.8-18, 2002.
- ASSOKU, R.K. Immunological studies of the mechanism of anaemia in experimental Trypanosoma evansi infection in rats. International Journal for Parasitology, v.5, n.2, p.137-145, 1975.
- AL-MOHAMMED H.I. Parasitological and immunological studies on rats experimental infected with Saudi Arabian strain of Typanosoma evansi Journal of the Egyptian Society of Parasitology, v.36, n.2, p.363-371, 2006.
- ATARHOUCH T. et al. Camel trypanosomosis in Marocco 1: results of a first epidemiological survey. Veterinary Parasitology, v.111, n.4, p.277286, 2003.
- CAMARGO, R.E. et al. Isolation of two antigens from Trypanosoma evansi that are partially responsible for its cross-reactivity with Trypanosoma vivax Veterinary Parasitology, v.123, n.1, p.67-81, 2004.
- CLARKSON, M.J. Blood and plasma volumes in sheep infected with T. vivex Journal of Comparative Pathology, v.78, p.189-193, 1968.
- COLPO, C.B. et al. Infecção Natural por Trypanosoma evansi em cão no Rio Grande do Sul. Ciência Rural, v.35, n.3, p.717-719, 2005.
- DARGIE, J.D. et al. Bovine trypanosomiasis: the red kinetics of N'dama and zebu cattle infected with Trypanosoma congolense Patasitology, v.78, p.271-286, 1979.
- FELDMAN, B.V. et al. Schalm's veterinary hematology 5.ed. Philadelphia: Lippincott Williams & Wilkins, 2000. p.1344.
- FIENNES, R.N.T.W. et al. The course and pathology of Trypanosoma congolense (Borden) disease of cattle. Journal of Comparative Pathology, v.56, p.1-27, 1946.
- FRANKE, C.R. et al. Investigations on naturally occurring Trypanosoma evansi infections in horses, cattle, dogs and capybaras (Hydrochaeris hydrochaeris) in Pantanal de Poconé (Mato Grosso, Brazil). Acta Tropica, v.58, p.159-169, 1994.
- HERRERA, H.M. et al. Experimental Trypanosoma evansi infection in the South American coati (Nasua nasua): hematological, biochemical and histopathological changes. Acta Tropica, v.81, n.3, p.203-210, 2002.
- HILALI M. et al. Hematological and biochemical changes in water buffalo calves (Bubalus bubalis) infected with Trypanosoma evansi Veterinary Parasitology, v.139, p.237243, 2006.
- HOARE, C.A. The Trypanosomes of mammals: a zoological monograph Oxford: Blackwell Scientific Publications, 1972. 749p.
- JAIN, N.C. Evaluation of anemias and polycythemias. In:______. Essentials of veterinary hematology Philadelphia: Lea & Febiger, 1993. Cap.8, p.159-168.
- JATKAR, P.R.; PUROHIT M.S. Pathogenesis of anaemia in Trypanosoma evansi infection. I. Haematology. Indian Veterinary Journal, v.48, n.3, p.239-244, 1971.
- JENKINS, G.C.; FACER C.A. Hematology of African trypanosomiasis. In: TIZARD I. Immunology and pathogenesis of Trypanosomiasis Boca Raton, Florida: CRC, 1985. p.13-44.
- MARQUES, L.C. et al. Experimental infection with Trypanosoma evansi in horses: clinical and haematological observations. Revista Brasileira de Parasitologia Veterinária, v.9, p.11-15, 2000.
- MENEZES V.T. et al. Trypanosoma evansi in inbred and Swiss-Webster mice: distinct aspects of pathogenesis. Parasitology Research, v.94, n.3, p.193-200, 2004.
- NADIUM, M.A.; SOLIMAN, M.K. Prognostic value of blood picture in animals affected with trypanosomiasis (El Dabab). Indian Journal of Veterinary Science, v.44, p.566571, 1967.
- NGERANWA J.J et al. Pathogenesis of Trypanosoma evansi in small east African goats. Research Veterinary Science, v.54, n.3, p.283289, 1993
- ONAH D.N. et al. Haematological changes in sheep experimentally infected with Trypanosoma evansi Parasitology Research, v.84, p.659-663, 1996.
- QUEIROZ A.O. et al. Biological and biochemical characterization of isolates of Tripanosoma evansi from Pantanal of Matogrosso Brazil. Veterinary Parasitology, v.92, p.107-118, 2000.
- QUEIROZ A.O. et al. Specific antibody levels and antigenic recognition of Wistar rats inoculated with distinct isolates of Trypanosoma evansi Memorial Instituto Oswaldo Cruz, v.97, n.7, p.965-972, 2001.
- SEN, H.G. et al. Pathology of T. evansi infection in rats. Indian Journal of Veterinary Science, v.29, p.108-112, 1959.
- SHARMA, D.K. et al. Haematological changes in experimental trypanosomiasis in Barbari goats. Small Ruminant Research, v.38, n.2, p.145-149, 2000.
- SILVA, R.A.M.S. et al. Pathogenesis of Trypanosoma evansi infection in dogs and horses: hematological and clinical aspects. Ciência Rural, v.25, p.233-238, 1995.
- SILVA, R.A.M.S et al. Trypanosoma evansi e Trypanosoma vivax: biologia, diagnóstico e controle Corumbá: Embrapa Pantanal, 2002. 137p.
- SILVA, A.S. et al. Métodos de contenção e confecção de esfregaço sanguíneo para pesquisa de hemoparasitas em ratos e camundongos. Revista da Faculdade de Zootecnia, Veterinária e Agronomia, v.13, n.2, p.83-87, 2006.
- TYLER, R.D.; COWELL R.L. Bone marrow. In: COWELL R.L.; TYLER R.D. Diagnostic cytology of dog and cat California: American Veterinary Publications, 1989. Cap.9, p.99-119.
- WALIA, P.S. et al. Role of activity of Trypanosoma evansi in inducing anemia and immunomodulation in buffalo calves. Journal Veterinary Parasitology, v.10, n.1, p.1-9, 1996.
- VICKERMAN, K. The diversity of the kinetoplastid flagellates. In: LUMSDEN, W.H.R.; EVANS, D.A. Biology of the kinetoplastida London/New York/San Francisco: Academic, 1976. p.1-34.
Datas de Publicação
-
Publicação nesta coleção
05 Out 2007 -
Data do Fascículo
Dez 2007
Histórico
-
Recebido
17 Nov 2006 -
Aceito
07 Mar 2007