Resumos
A análise comparativa das glândulas armazenadoras de espermatozóides das junções infundíbulo-magno e útero-vagina do oviduto da codorna Nothura maculosa foi realizada durante a fase reprodutiva. As aves foram eutanasiadas por inalação com éter etílico, após a pesagem. Após a laparotomia e o deslocamento cranial do esterno, foram coletadas amostras de dois centímetros da junção infundíbulo-magno e útero-vagina. Os fragmentos foram fixados em solução de Bouin por 24 horas e, posteriormente, banhos sucessivos de álcool 70% foram aplicados sobre as amostras. Em seguida, as amostras foram desidratadas em uma série de concentração crescente de alcoóis (80, 90, 95 e 3x100%), diafanizadas em xilol e incluídas em parafina. Cortes histológicos de sete micrômetros de espessura foram obtidos e corados pela técnica da Hematoxilina-eosina (HE), que foram analisados e fotomicrografados em um fotomicroscópio Olympus BX-50. Para a análise morfométrica, foram capturadas imagens das glândulas armazenadoras de espermatozóides da junção infundíbulo-magno e útero-vagina mediante o programa computacional "Image Pro Plus 4.1" da Cibernetics do Brasil, tornando-se possível a quantificação das mesmas. A mucosa da junção infundíbulo-magno apresentou pregas estreitas no infundíbulo e largas no magno, enquanto na junção útero-vagina mostrou-se amplamente pregueada na vagina e mais lisa na porção uterina. O número médio de glândulas armazenadoras de espermatozóides na junção infundíbulo-magno foi maior (11,7 glândulas) (P<0,01) que na junção útero-vagina (7,5 glândulas). Supõe-se que a abundância de glândulas armazenadoras de espermatozóides na junção infundíbulo-magno permite acesso mais rápido do ovócito, após a oocitação, ao espermatozóide armazenado, garantindo a fertilização.
histologia; morfometria; oviduto; glândulas armazenadoras de espermatozóides; codorna
The comparative analysis of sperm-host glands of infundibulum-magnum and uterus-vagina junctions of Nothura maculosa quail oviduct was done during the reproductive phase. The birds were euthanized with ethyl ether after weight data were taken. After abdominal laparotomy and cranial displacement of the breastbone, two centimeters samples of infundibulum-magnum and uterus-vagina junctions were collected. The samples were fixed in Bouin's solution for twenty four hours and later, successive baths of alcohol 70% were applied on samples and soon afterwards dehydrated in a series of grow concentration alcohols (80, 90, 95 and 3x100%), diaphanized in xylol and included on paraffin. Histological sections with seven micrometers thickness were obtained and stained on Haematoxylin-Eosin (HE) technique, then they were analyzed and photomicrographed in a photomicroscope Olympus BX-50. For the morphometry analysis, infundibulum-magnum junctions and uterus-vagina sperm host gland images were captured through a computacional program Image Pro Plus 4.1", Cibernetics Brazil, making it possible to quantify them. The mucosa of the infundibulum-magnum junction presented very narrow folds in the infundibulum and too large in the magnum, while in the uterus-vagina junction was observed widely folds mucous in the vagina and smoother in the uterine portion. The average of sperm host gland in the infundibulum-magnum junction was higher (11.7 glands) (P<0.01) compared to the uterus-vagina junction (7.5 glands). It is supposed that the abundance number of sperm host glands in infundibulum-magnum junction allows faster access of the oocyte, after the ovulation of the host spermatozoid ensuring the fertilization.
histology; morphometry; oviduct; sperm-host glands; quail
ARTIGOS CIENTÍFICOS
CLÍNICA E CIRURGIA
Histologia e morfometria das glândulas das junções infundíbulo-magno e útero-vagina de codorna doméstica
Histology and morphometry of the infundibulum-magnum and uterus-vaginal junctions of spotted quails
Carime MoraesI; Silvana Martinez Baraldi-ArtoniI,1 1 Autor para correspondência. ; Maria Rita PachecoI; Daniela OliveiraI; Lizandra AmorosoI; Alex Luís SagulaI
IDepartamento de Morfologia e Fisiologia Animal, Laboratório de Anatomia Animal, Universidade Estadual Paulista (UNESP), Faculdade de Ciências Agrárias e Veterinárias de Jaboticabal (FCAVJ). Rod. Acesso Paulo Donato Castellane, s/n, km 5, 14884-900, Jaboticabal, SP, Brasil. Fone: (16) 3209-2654, r. 239. E-mail: smbart@fcav.unesp.br
RESUMO
A análise comparativa das glândulas armazenadoras de espermatozóides das junções infundíbulo-magno e útero-vagina do oviduto da codorna Nothura maculosa foi realizada durante a fase reprodutiva. As aves foram eutanasiadas por inalação com éter etílico, após a pesagem. Após a laparotomia e o deslocamento cranial do esterno, foram coletadas amostras de dois centímetros da junção infundíbulo-magno e útero-vagina. Os fragmentos foram fixados em solução de Bouin por 24 horas e, posteriormente, banhos sucessivos de álcool 70% foram aplicados sobre as amostras. Em seguida, as amostras foram desidratadas em uma série de concentração crescente de alcoóis (80, 90, 95 e 3x100%), diafanizadas em xilol e incluídas em parafina. Cortes histológicos de sete micrômetros de espessura foram obtidos e corados pela técnica da Hematoxilina-eosina (HE), que foram analisados e fotomicrografados em um fotomicroscópio Olympus BX-50. Para a análise morfométrica, foram capturadas imagens das glândulas armazenadoras de espermatozóides da junção infundíbulo-magno e útero-vagina mediante o programa computacional Image Pro Plus 4.1 da Cibernetics do Brasil, tornando-se possível a quantificação das mesmas. A mucosa da junção infundíbulo-magno apresentou pregas estreitas no infundíbulo e largas no magno, enquanto na junção útero-vagina mostrou-se amplamente pregueada na vagina e mais lisa na porção uterina. O número médio de glândulas armazenadoras de espermatozóides na junção infundíbulo-magno foi maior (11,7 glândulas) (P<0,01) que na junção útero-vagina (7,5 glândulas). Supõe-se que a abundância de glândulas armazenadoras de espermatozóides na junção infundíbulo-magno permite acesso mais rápido do ovócito, após a oocitação, ao espermatozóide armazenado, garantindo a fertilização.
Palavras-chave: histologia, morfometria, oviduto, glândulas armazenadoras de espermatozóides, codorna.
ABSTRACT
The comparative analysis of sperm-host glands of infundibulum-magnum and uterus-vagina junctions of Nothura maculosa quail oviduct was done during the reproductive phase. The birds were euthanized with ethyl ether after weight data were taken. After abdominal laparotomy and cranial displacement of the breastbone, two centimeters samples of infundibulum-magnum and uterus-vagina junctions were collected. The samples were fixed in Bouin's solution for twenty four hours and later, successive baths of alcohol 70% were applied on samples and soon afterwards dehydrated in a series of grow concentration alcohols (80, 90, 95 and 3x100%), diaphanized in xylol and included on paraffin. Histological sections with seven micrometers thickness were obtained and stained on Haematoxylin-Eosin (HE) technique, then they were analyzed and photomicrographed in a photomicroscope Olympus BX-50. For the morphometry analysis, infundibulum-magnum junctions and uterus-vagina sperm host gland images were captured through a computacional program Image Pro Plus 4.1, Cibernetics Brazil, making it possible to quantify them. The mucosa of the infundibulum-magnum junction presented very narrow folds in the infundibulum and too large in the magnum, while in the uterus-vagina junction was observed widely folds mucous in the vagina and smoother in the uterine portion. The average of sperm host gland in the infundibulum-magnum junction was higher (11.7 glands) (P<0.01) compared to the uterus-vagina junction (7.5 glands). It is supposed that the abundance number of sperm host glands in infundibulum-magnum junction allows faster access of the oocyte, after the ovulation of the host spermatozoid ensuring the fertilization.
Key words: histology, morphometry, oviduct, sperm-host glands, quail.
INTRODUÇÃO
Em suas pesquisas com aves, SISSON & GROSSMAN (1986) e DYCE et al. (1996) relataram que os órgãos reprodutores de fêmeas são constituídos pelo ovário e pelo oviduto, os quais são bilateralmente simétricos na fase embrionária. Em aves domésticas, normalmente o ovário e o oviduto esquerdos são funcionais, enquanto os direitos são rudimentares. Além disso, o oviduto das aves está dividido anatomicamente em cinco regiões distintas e com funções fisiológicas específicas: infundíbulo, magno (região secretora de albúmen), istmo, útero (glândula da casca) e vagina (RIBEIRO et al. 1995; DYCE et al. 1996 ; SULTANA et al. 2003).
BACHA & BACHA (2000) relataram que o oviduto de aves histologicamente está constituído por uma camada mucosa revestida por epitélio simples cilíndrico ciliado, apoiado em uma lâmina própria de tecido conjuntivo frouxo, uma camada muscular de músculo liso circular interna e longitudinal externa e uma serosa formada por tecido conjuntivo frouxo e mesotélio.
A junção do útero à vagina foi demarcada por um forte esfíncter, segundo as descrições de FUJII & TAMURA (1963) e BOBR et al. (1964). Os autores verificaram que o esfíncter está localizado na vagina, próximo ao útero. As pregas delicadas da mucosa são longitudinais ao invés de espiraladas, bem mais delgadas e baixas do que em qualquer outra parte do oviduto, exceto no funil do infundíbulo. Na região do esfíncter da vagina, as pregas são especialmente modificadas, tornando-se menos uniformes e apresentando superfícies rugosas. Na região em que o esfíncter estreita o lúmen, verificou-se que as pregas estão intimamente juntas e, desse modo, potencializam a redução do lúmen a um estreito anel (BOBR et al.,1964). Estas pregas especiais sustentam glândulas tubulares que FUJII & TAMURA (1963) denominaram glândulas vaginais, enquanto que BOBR et al. (1964) denominaram glândulas útero-vaginais. No principal segmento vaginal de peruas, não existem glândulas tubulares, sendo observadas na junção útero-vagina, caracterizadas como principal área de estocagem espermática (VERMA & CHERMS, 1964). Além da espécie Gallus gallus, as glândulas útero-vaginais foram observadas também em muitas outras aves, tais como a perua (VERMA & CHERMS, 1964), a pata doméstica (PAL, 1977), a codorna (FRIEB et al, 1978) e o falcão americano (BAKST, 1987), sendo que tais glândulas foram estudadas histológica e funcionalmente.
Embora alguns espermatozóides provavelmente sejam armazenados nos sulcos glandulares e nas glândulas tubulares do colo do infundíbulo (VAN DRIMMELEN, 1946; FUJII & TAMURA, 1963; VAN KREY et al., 1964), as glândulas vaginais (glândulas útero-vaginais) são geralmente consideradas como sendo os locais principais de armazenamento (BOBR et al. 1962, 1964; FUJII & TAMURA, 1963). KING et al. (1999) determinaram que espermatozóides viáveis são passíveis de serem isolados desses túbulos de estocagem de esperma na mucosa da junção útero-vagina de peruas. O desenvolvimento desses túbulos de estocagem foi estudado em codornas durante a maturação sexual utilizando microscopia óptica e analisador de imagens por HOLM & RIDDERSTRALE (2002).
A capacidade das fêmeas armazenarem espermatozóides por períodos prolongados é uma característica importante da reprodução em aves e ocorre em túbulos armazenadores de espermatozóide, caracterizados como invaginações localizadas principalmente na junção útero-vagina do oviduto e em pequenas quantidades no infundíbulo (VAN KREY et al., 1964). Os espermatozóides são transferidos para a vagina por meio da copulação ou da inseminação artificial e ascendem para os túbulos da junção útero-vagina. Nesta junção, os espermatozóides permanecem por tempo variável, dependendo das espécies, do estado reprodutivo e da idade da fêmea (KING et al., 2002).
Além de a função de armazenar espermatozóides, a junção útero-vagina age como uma barreira seletiva no transporte, sendo que apenas espermatozóides móveis podem passar nesta região (FRIEB et al., 1978). FROMAN (2003) cita que somente espermatozóides móveis se elevam para a vagina e penetram nesses túbulos e emergem deles. O autor explica vários fatores que interferem nesse fenômeno, os quais estão relacionados à motilidade do espermatozóide. Os espermatozóides mortos não penetram no interior do útero (FUJII & TAMURA, 1963) e são possivelmente reabsorvidos na região útero-vagina.
KING et al. (2002) relataram que os espermatozóides do último macho que copulou fecundam a maioria dos ovos durante os cinco primeiros dias após a última inseminação. Muitos autores sugerem que os espermatozóides do último macho são os mais atuantes por serem resultado da última estratificação no interior dos túbulos (BURKE & OGASAWARA, 1969; COMPTON et al., 1978; CHRISTENSEN, 1981).
Um estudo conduzido por DEGEN & HAVENS (1972) revela que o armazenamento pode, em certos casos, ter lugar na região infundibular. SCHINDLER et al. (1967) verificaram que as glândulas infundibulares são capazes de armazenar espermatozóides por mais tempo que as glândulas útero-vaginais.
Diante de todas essas informações, os objetivos deste trabalho são realizar estudo histológico e avaliar a morfometria das glândulas armazenadoras de espermatozóides situadas nas junções infundíbulo-magno e útero-vagina. Tais informações poderão contribuir, sobremaneira, com a técnica de inseminação artificial e, conseqüentemente, com a reprodução dessas aves, que, por sua vez, têm grande valor econômico em termos de carne e ovos.
MATERIAL E MÉTODOS
Foram utilizadas 10 codornas Nothura maculosa, fêmeas, em fase reprodutiva, pesando em média 155±20,11g, as quais foram eutanasiadas por inalação com éter etílico. Após a laparotomia e o deslocamento cranial do plastão esternal, os ovidutos foram retirados e foram coletadas amostras de dois centímetros da junção infundíbulo-magno e útero-vagina. Os fragmentos foram fixados em solução de Bouin por 24 horas. Posteriormente, banhos sucessivos de álcool 70% foram aplicados sobre as amostras para a retirada do fixador. Em seguida, as amostras foram desidratadas em uma série de concentração crescente de alcoóis (80,90,95 e 3x 100%). Após a desidratação do material, as amostras foram recortadas em fragmentos de 0,5cm de comprimento, diafanizadas em xilol e incluídas em parafina. Foram preparadas lâminas das junções infundíbulo-magno e útero-vagina e em cada lâmina foram colocados cinco fragmentos histológicos com 7µm de espessura e posteriormente foram corados com hematoxilina-eosina (HE), analisados e fotomicrografados com o auxílio de um fotomicroscópio Olympus BX-50.
Para o estudo morfométrico, foram capturadas 15 imagens das glândulas armazenadoras de espermatozóides por lâmina, totalizando 150 imagens para cada junção, as quais foram retidas em um cartão de memória smartmídia e, posteriormente, descarregadas em um programa computacional acoplado a um analisador de imagens Image Pro Plus versão 4.1, da Media Cybernetics do Brasil para a quantificação das mesmas. Após a obtenção dos dados científicos, estes foram analisados estatisticamente por meio da análise de variância, sendo que as médias foram comparadas pelo teste de Tukey a 5% de probabilidade.
RESULTADOS E DISCUSSÃO
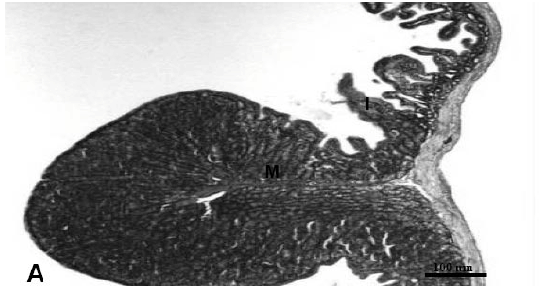
Histologicamente, o infundíbulo mostrou-se constituído por duas regiões: cranial (aglandular) e caudal (glandular). A junção infundíbulo-magno apresentou a mucosa com pregas muito estreitas no infundíbulo e muito largas no magno (Figura. 1A). A junção útero-vagina exibiu mucosa amplamente pregueada no segmento vaginal e discretamente mais lisa na porção uterina (Figura. 2A). Ambas as regiões apresentaram na lâmina própria numerosas glândulas simples tubulares, revestidas por epitélio cúbico a cilíndrico, com luz ampla e nítida (Figura 1B-C e 2A-B). Foram observados alguns espermatozóides no seu lúmen (Figura 2B). Estas evidências histológicas confirmam as descrições de BACHA & BACHA (2000) em galinhas domésticas.
Morfometricamente, verificou-se que a junção infundíbulo-magno apresentou uma média significativamente maior (11,7±1,48) em relação às glândulas útero-vagina (7,5±1,36) (Figura 3). Esses resultados provavelmente estão relacionados com a topografia do ovário e do infundíbulo, uma vez que o ovócito, ao sofrer oocitação, entra em contato o mais rápido possível com os espermatozóides, armazenados nas glândulas infundibulares quando comparados aos espermatozóides armazenados nas glândulas da junção útero-vagina. Vale destacar que os espermatozóides da junção útero-vagina levam muito mais tempo para chegar ao infundíbulo, sendo que alguns podem vira morrer durante os seus trajetos. Entretanto, os resultados observados neste estudo contradizem as descrições de VAN KREY et al. (1964) em relação às glândulas armazenadoras de espermatozóide, ao mencionarem que estas se encontravam em menor concentração na junção infundíbulo-magno e em maior quantidade na junção útero-vagina.
A quantificação de glândulas na junção infundíbulo-magno obtida em codorna Nothura maculosa diferiu das afirmações feitas em galinhas domésticas por BOBR et al. (1962, 1964) e FUJII & TAMURA (1963) ao constatarem nesta região uma menor quantidade dessas glândulas. Além disso, estes mesmos autores consideraram as glândulas útero-vaginais os principais locais de armazenamento de espermatozóides.
Levando-se em conta um giro de 180° no momento da postura, a distensão do tecido e, conseqüentemente, das glândulas, e a passagem do ovo pela região útero-vaginal, estes resultados levam a acreditar que o armazenamento dos espermatozóides é mais efetivo nas glândulas da junção infundíbulo-magno, onde existe somente a dinâmica correspondente à passagem do ovócito por esta região, em comparação com aquelas da região útero-vagina. Ressalta-se ainda que a fertilização será facilitada pela maior quantidade de glândulas na junção infundíbulo-magno, de acordo com OLSEN (1942), ao relatar que a penetração de espermatozóides no oócito ocorre aproximadamente 15 minutos após a ovulação, ponderando-se que este é o tempo de permanência do oócito no infundíbulo.
CONCLUSÕES
Histologicamente o oviduto da codorna apresentou resultados semelhantes a outros galiniformes, tais como a galinha e a perua. Morfometricamente a junção infundíbulo-magno se destacou em relação à junção útero-vagina na quantificação de glândulas armazenadoras de espermatozóides, provavelmente, por ser uma região mais próxima do ovário e apresentar um acesso mais rápido do espermatozóide ao ovócito em relação aos espermatozóides armazenados na junção útero-vagina, favorecendo, assim, a fertilização dos oócitos.
AGRADECIMENTO
A Fundação de Amparo à Pesquisa do Estado de São Paulo (FAPESP), pelo auxílio financeiro fornecido para o desenvolvimento deste Projeto de Pesquisa.
COMITÊ DE ÉTICA E BIOSSEGURANÇA
Este Projeto de Pesquisa foi autorizado pelo Comitê de Ética e Bem Estar Animal (CEBEA) da Faculdade de Ciências Agrárias e Veterinárias, Campus de Jaboticabal. Protocolo n° 015862.
Recebido para publicação 13.02.08
Aprovado em 25.07.08
- BACHA, W.J.; BACHA, L.M. Color atlas of veterinary histology 2.ed. Philadelphia: Lippincott Williams & Wilkins. 2000. 318p.
- BAKST, M.R. Anatomical basis of sperm storage in the avian oviduct. Scanning. Electron Microscopy, Chicago, v.1, p.1257-1266, 1987.
- BOBR, L.W. et al. The role of the uterovaginal junction in storage of cock spermatozoa. Poultry Science, Champaign, v.41, p.1628, 1962.
- BOBR, L.W. et al. Distribution of spermatozoa in the oviduct and fertility in domestic birds.1. Residence sites of spermatozoa in fowl oviducts. Journal of Reproduction and Fertility, Cambridge, v.8, p.39-47, 1964.
- BURKE, W.H.; OGASAWARA, F.X Presence of spermatozoa in uterovaginal fluids of the hen at various stages of the ovulatory cycle. Poultry Science, Champaign, v.48, p.408-413, 1969.
- CHRISTENSEN, V.L. Effect of insemination intervals on oviductal sperm storage in turkeys. Poultry Science, Champaign, v.60, p.2150-2156, 1981.
- COMPTON, M.M. et al. The filling and emptying of the uterovaginal sperm-host glands in the domestic hen. Poultry Science, Champaign, v.57, p.1696-1700, 1978.
- DEGEN, A.A.; HAVENS, R.O. Fertility in the domestic hen following the surgical removal of the utero-vaginal junction. Poultry Science, Champaign, v.51, p.464-470, 1972.
- DRIMMELEN, G.C. VAN. Sperm nests in the oviduct of the domestic hen. Journal of Soulth African Veterinary Association v.17, p.42-52, 1946.
- DYCE, K.M. et al. Anatomia das aves. In: DYCE, K.M.et al. Tratado de anatomia veterinária 2.ed. Rio de Janeiro: Guanabara Koogan, 1996. p.631-650.
- FRIEB, A.E. et al. The utero-vaginal sperm host glands of the quail (Cortunix cortunix japonica). Cell Tissue Research, Heidelberg,v.1 p.115-119, 1978.
- FROMAN, D. Deduction of a model for sperm storage in the oviduct of the domestic fowl (Gallus domesticus). Biology of Reproduction, Champaign, v.69, n.1, p.248-253, 2003.
- FUJII, S.; TAMURA, T. Location of sperms in the oviduct of the domestic fowl with special reference to storage of sperms in the vaginal gland. Journal of the Faculty Fisheries and Animal Husbandry Hiroshima, Fukuyama, v.5, p.145-163, 1963.
- HOLM, L.; RIDDERSTRALE, Y. Development of sperm storage tubules in the quail during sexual maturation. Journal of Experimental Zoology, New York, v.292, n.2, p.200-205, 2002.
- KING, L.M.et al. Isolation of sperma storage tubules from the uterovaginal junction mucosa of the turkey. Poultry Science, Champaign, v.78, n.7, p.1044-1047, 1999.
- KING, L.M. et al. Segregation of spermatozoa within sperm storage tubules of fowl and turkey hens. Reproduction, Cambridge, v.123, n.1, p.79-86, 2002.
- OLSEN, M.W. Maturation, fertilization, and early cleavage in the hens egg. Journal of Morphology, New York, v.70, p.513-533, 1942.
- PAL, D. Histochemistry of the utero-vaginal junction with special reference to the sperm host glands in the oviduct of the domestic duck. Folia Histochemica Cytochemica, Warsaw, v.15, p.235-242, 1977.
- RIBEIRO, M.G. et al Estudo histológico do oviduto de Numida meleagris (Linné, 1758), com referência especial ao útero. Bios, Unadilla, v.2, n.3, p.43-48, 1995.
- SCHINDLER, H. et al. The relation of spermatozoa to the glandular tissue in the storage sites in the hen oviduct. Poultry Science, Champaign, v.46, p.1462-1471, 1967.
- SISSON, S.; GROSSMAN, J.D. Anatomia dos animais domésticos 5.ed. Rio de Janeiro: Guanabara Koogan,1986. 2000p.
- SULTANA, F. et al. The peri-albumen layer: a novel structure in the envelopes of avian egg. Journal Anatomy, London, v.203, n.1, p.115-122, 2003.
- VAN KREY, H.P. et al. Relative storage potential of the uterovaginal and infundibular sperm glands. Poultry Science, Savoy, v.43, p.1373, 1964.
- VERMA, O.P.; CHERMS, F.L. Observations on the oviduct of the turkeys. Avian Diseases, Vennete Square, v.8, p.19-26, 1964.
Datas de Publicação
-
Publicação nesta coleção
08 Out 2008 -
Data do Fascículo
Abr 2009
Histórico
-
Aceito
25 Jul 2008 -
Recebido
13 Fev 2008