Resumos
Indução de calogênese eficiente e multiplicação celular rápida são pré-requisitos fundamentais em biotecnologia de plantas. Sucesso na calogênese é dependente dos componentes do meio de cultura e da qualidade dos explantes. Neste trabalho é relatada a influência do tratamento de matrizes de Dianthus caryophyllus L. com nitrogênio na indução de calogênese in vitro. Mudas de cravo cultivadas em vasos contendo areia foram tratadas com soluções nutritivas contendo 5 níveis de nitrogênio. Explantes folha, entrenós e nó foram coletados aos 30, 45 e 60 dias após início dos tratamentos e inoculados em meio de cultura contendo os sais básicos e vitaminas de Murashige & Skoog (1962), suplementado com 1 g L-1 de caseína hidrolizada, 2 mimol L-1 de cinetina e 3 mimol L-1 de 2,4-D para indução da calogênese. Ao longo dos 60 dias de tratamento com as soluções nutritivas, as matrizes de cravo não apresentaram sintomas visíveis de deficiência ou de excesso do nutriente nitrogênio. O tratamento com nitrogênio afetou a calogênese avaliada em massa de matéria fresca e seca. A produção da massa de matéria fresca de calos foi proporcional ao tratamento com nitrogênio até concentração de 267 mg L-1 para explantes folha por durante 30 dias. Tratamentos mais prolongados (45 e 60 dias) afetaram negativamente a calogênese e foram inversamente proporcionais a concentração de nitrogênio na solução nutritiva.
nutrição mineral; cultura de tecido
Efficient calogenesis induction and rapid cell multiplication are fundamental requirements in plant biotechnology. The success of calogenesis is dependent on the growth medium components and the quality of explants. This work is referred to the influence of Dianthus caryophyllus L. nitrogen treatment on calogenesis induction in vitro. Carnation cuts rooted in sand pots were treated with nutrient solutions containing 5 nitrogen levels. Leaves, internodes and node explants were collected and inoculated on callus induction culture media containing Murashige & Skoog (1962) salts and vitamins, supplemented with 1 g L-1 hidrolysed casein, 2 mumol L-1 kinetin and 3 mumol L-1 2,4-D. No plant deficiency and toxicity symptoms were apparent on the treated plants during the 60 day treatment. The nitrogen treatment affected calogenesis in relation to calli fresh and dry weights. Callus fresh weigth yield was proportional to nitrogen concentration up to 267 mg L-1 for leaf explant during 30 days. Longer treatments (45 and 60 days) affected calogenesis negatively which were inversely proportional to the nitrogen concentration of the nutrient solution.
mineral nutrition; tissue culture
TRATAMENTO DE MATRIZES DE CRAVO (Dianthus caryophyllus L., CARYOPHYLLACEAE) COM NITROGÊNIO E CALOGÊNESE in vitro
Telma Kazumi Hayashi1,4; Adônis Moreira2,5; Antônio Francisco de Campos Amaral3; Murilo Melo3*
12Embrapa Amazônia Ocidental, C.P. 319 - CEP: 69011-970 - Manaus, AM.
3Depto. de Ciências Biológicas - USP/ESALQ, C.P. 9 - CEP: 13418-900 - Piracicaba, SP.
4Bolsista CAPES.
5Bolsista DCR/CNPq.
*Autor correspondente <mmelo@carpa.ciagri.usp.br>
RESUMO: Indução de calogênese eficiente e multiplicação celular rápida são pré-requisitos fundamentais em biotecnologia de plantas. Sucesso na calogênese é dependente dos componentes do meio de cultura e da qualidade dos explantes. Neste trabalho é relatada a influência do tratamento de matrizes de Dianthus caryophyllus L. com nitrogênio na indução de calogênese in vitro. Mudas de cravo cultivadas em vasos contendo areia foram tratadas com soluções nutritivas contendo 5 níveis de nitrogênio. Explantes folha, entrenós e nó foram coletados aos 30, 45 e 60 dias após início dos tratamentos e inoculados em meio de cultura contendo os sais básicos e vitaminas de Murashige & Skoog (1962), suplementado com 1 g L-1 de caseína hidrolizada, 2 mmol L-1 de cinetina e 3 mmol L-1 de 2,4-D para indução da calogênese. Ao longo dos 60 dias de tratamento com as soluções nutritivas, as matrizes de cravo não apresentaram sintomas visíveis de deficiência ou de excesso do nutriente nitrogênio. O tratamento com nitrogênio afetou a calogênese avaliada em massa de matéria fresca e seca. A produção da massa de matéria fresca de calos foi proporcional ao tratamento com nitrogênio até concentração de 267 mg L-1 para explantes folha por durante 30 dias. Tratamentos mais prolongados (45 e 60 dias) afetaram negativamente a calogênese e foram inversamente proporcionais a concentração de nitrogênio na solução nutritiva.
Palavras-chave: nutrição mineral, cultura de tecido
NITROGEN TREATMENT OF CARNATION (Dianthus caryophyllus L., CARYOPHYLLACEAE) AND in vitro CALOGENESIS
ABSTRACT: Efficient calogenesis induction and rapid cell multiplication are fundamental requirements in plant biotechnology. The success of calogenesis is dependent on the growth medium components and the quality of explants. This work is referred to the influence of Dianthus caryophyllus L. nitrogen treatment on calogenesis induction in vitro. Carnation cuts rooted in sand pots were treated with nutrient solutions containing 5 nitrogen levels. Leaves, internodes and node explants were collected and inoculated on callus induction culture media containing Murashige & Skoog (1962) salts and vitamins, supplemented with 1 g L-1 hidrolysed casein, 2 mmol L-1 kinetin and 3 mmol L-1 2,4-D. No plant deficiency and toxicity symptoms were apparent on the treated plants during the 60 day treatment. The nitrogen treatment affected calogenesis in relation to calli fresh and dry weights. Callus fresh weigth yield was proportional to nitrogen concentration up to 267 mg L-1 for leaf explant during 30 days. Longer treatments (45 and 60 days) affected calogenesis negatively which were inversely proportional to the nitrogen concentration of the nutrient solution.
Key words: mineral nutrition, tissue culture
INTRODUÇÃO
A cultura de tecidos de plantas é a expressão utilizada para designar a cultura in vitro de células, tecidos e órgãos de plantas, que além de proporcionar variação genética, condição essencial para a seleção de genótipos superiores, amplia os conhecimentos para a compreensão dos fenômenos bioquímicos e fisiológicos responsáveis pelo crescimento e desenvolvimento das plantas (Gallo & Crocomo, 1995).
Cultura de calos, suspensões celulares e cultura de protoplastos são de relevante importância nas investigações de diferenciação celular e de biologia molecular (Veasey et al., 1991). Através da cultura de células; linhas de células mutantes com resistência a antibióticos, herbicidas, aminoácidos e seus análogos, toxinas fúngicas e tolerância a estresse ambiental têm sido selecionadas (Bhojwani & Razdam, 1996). Outra aplicação da cultura de células está relacionada com a produção de metabólitos secundários na área industrial. Células vegetais mantidas em suspensão líquida em biorreatores produzem produtos de seu metabolismo, entre eles alcalóides, corantes, antioxidantes e taninos (Crocomo, 1988).
Quando um explante é excisado da planta doadora e inoculado em meio de cultura , um dos eventos mais comuns é a formação de uma massa de células não diferenciadas, com proliferação contínua e desordenada, denominada calo (Handro & Floh, 1990). De acordo com Stafford & Warren (1991), o estabelecimento da cultura de calos a partir de explantes (raiz, caule, folha, flor, etc.) é dividido em três etapas: (1) indução (ativação do metabolismo para a desdiferenciação e divisão celular); (2) divisão (as células dividem-se ativamente em células de tamanho menor); e (3) diferenciação (as células tornam-se maiores, vacuolizadas e a taxa de divisão diminui, e então ocorre o equilíbrio entre a divisão e a expansão celular).
Muitos são os fatores que influenciam o comportamento do explante no meio de cultura, incluindo o órgão que serve como fonte de tecido, a idade fisiológica e ontogenética do órgão, o tamanho do explante e acima de tudo a qualidade da planta doadora (Thorpe & Patel, 1984).
O controle da qualidade do material vegetal em si e a manipulação deste antes de se isolar o explante são aspectos importantes na cultura de tecidos. Esta manipulação inclui o manejo cultural e ambiental da planta matriz, pois o estado nutricional, fisiológico e fitossanitário desta tem grande influência no posterior comportamento do explante e da cultura. Plantas bem nutridas, sem sintomas de deficiência nutricional ou hídrica, em geral fornecem explantes de melhores qualidades (Grattapaglia & Machado, 1990).
Em estudos feitos com Chrysanthemum morifolium verificou-se que o tratamento de plantas matrizes com nitrogênio afeta a calogênese in vitro, evidenciando a importância do estado nutricional das plantas matrizes fornecedoras dos explantes (Borgatto, 2000).
O metabolismo do nitrogênio está envolvido nos processos fisiológicos e bioquímicos associados ao controle de crescimento, diferenciação e morfogênese. Durante o crescimento celular, a assimilação do nitrogênio contribui para o aumento de macromoléculas e componentes celulares, importantes para a regulação dos processos metabólicos do crescimento celular, implicando no aumento de tamanho e número de células (Durzan, 1985).
Apesar da história da cultura de tecidos de plantas ornamentais ser recente, muitos trabalhos têm sido realizados neste espaço de tempo. Entre os trabalhos referentes à cultura de tecidos de Dianthus caryophyllus L., bem como outras culturas são raros na literatura estudos relacionando o estado nutricional da planta matriz com o processo de calogênese, diferenciação celular e micropropagação do explante in vitro.
Este trabalho teve como objetivo avaliar a influência do tratamento de matrizes de Dianthus caryophyllus L. com nitrogênio no processo de calogênese in vitro.
MATERIAL E MÉTODOS
O trabalho foi realizado nos Laboratórios do Centro de Biotecnologia Agrícola (CEBTEC), Departamento de Ciências Biológicas da Escola Superior de Agricultura "Luiz de Queiroz"/USP, em Piracicaba/SP.
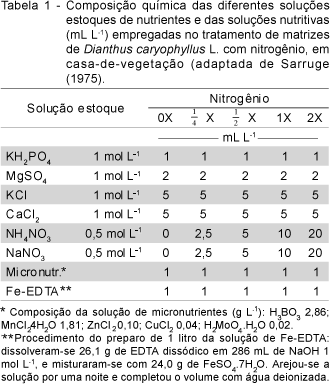
Mudas de Dianthus caryophyllus L. cv. Delphi foram plantadas em vaso contendo areia lavada e mantidas em casa-de-vegetação, com a finalidade de servirem como matrizes para o fornecimento de explantes para indução de calogênese. Em cada vaso foram plantadas duas mudas de cravo, com aproximadamente 15 cm de comprimento e 6 pares de folhas. Durante o período de pegamento e aclimatação (15 dias) em casa-de-vegetação as mudas foram irrigadas somente com água. Após este período as mudas foram tratadas com soluções nutritivas contendo 0X, , 1X e 2X (Tabela 1) da concentração da solução completa de Sarruge (1975) em nitrogênio (210 mg L-1). As soluções nutritivas foram aplicadas de acordo com as necessidades das plantas, de modo geral a cada 3 dias.
, 1X e 2X (Tabela 1) da concentração da solução completa de Sarruge (1975) em nitrogênio (210 mg L-1). As soluções nutritivas foram aplicadas de acordo com as necessidades das plantas, de modo geral a cada 3 dias.
Sob delineamento experimental inteiramente ao acaso, cada nível do nutriente representou um tratamento, sendo que cada tratamento foi constituído por 20 vasos contendo 2 mudas de cravo cada um, perfazendo um total de 100 vasos (5 tratamentos X 20 repetições).
A retirada dos explantes (folha, segmento nó e entrenós) foi efetuada aos 30, 45 e 60 dias após início do tratamento com solução nutritiva durante a fase de crescimento vegetativo das plantas. Ápices contendo até 4 pares de folhas expandidas, utilizados como fonte de explantes, foram imersos em solução de água destilada autoclavada contendo detergente neutro TWEEN-20 a 0,1% (v/v) e agitados por 5 minutos. Sob condições assépticas na câmara de fluxo laminar, o material vegetal foi transferido para solução comercial de hipoclorito de sódio (Q-Boa) a 20% (v/v) e TWEEN-20 a 0,1% (v/v), mantido por 20 minutos em agitação e posteriormente lavado quatro vezes em água destilada autoclavada.
Com o auxílio de pinças e bisturis assépticos foram retirados as bases das folhas, segmentos nodais e entrenodais da região do segundo e terceiro par de folhas expandidas, os quais foram utilizados como explantes. Estes explantes foram pesados em balança analítica e inoculados em meio de cultura contendo os sais básicos e vitaminas de Murashige & Skoog (1962), suplementado com 87,6 mmol L-1 de sacarose, 1 g L-1 de caseína hidrolisada, 2 mmol L-1 de cinetina e 3 mmol L-1 de 2,4-D (Frey et al.,1992), solidificado com 2,3 g L-1 de Phytagel (Sigma), e pH ajustado a 5,8 com KOH 1 mol L-1, antes da autoclavagem a 120°C por 40 minutos. Os frascos de inoculação utilizados foram vidros contendo 20 mL do meio de cultura e vedados com tampa plástica. O delineamento experimental utilizado para inoculação foi inteiramente ao acaso, com 20 repetições para cada explante de cada tratamento. Os valores médios da massa de matéria fresca dos explantes, em gramas, foram: folha 0,019 ± 0,004, entrenós 0,058 ± 0,06 e nó 0,076 ± 0,06.
Aos 30 dias após a inoculação foi realizada a transferência dos calos para meio novo de cultura de mesma composição química. A incubação do material inoculado foi feita em sala de crescimento com intensidade luminosa de 2000 lux, sob condições de fotoperíodo de 16/8 horas (claro/escuro) e temperatura de 26 ± 2°C.
Aos 60 dias após a inoculação foi efetuada a avaliação de massa de matéria fresca pesando-se os calos e calculado o índice de multiplicação celular (IMC) dividindo-se a massa de matéria fresca dos calos pela massa de matéria fresca de seu respectivo explante. Após a pesagem os calos foram acondicionados em sacos de papel e mantidos em estufa com circulação forçada de ar a 60°C até atingirem massa constante. Após a secagem os calos foram novamente pesados para a obtenção de massa de matéria seca.
Na análise estatística dos dados usou-se os valores do índice de multiplicação celular e a massa de matéria seca formada. Os dados em gramas de massa de matéria seca de calos e o IMC foram transformados pela equação  e submetidos a análise de variância e regressão, conforme as metodologias descritas por Pimentel-Gomes (1990).
e submetidos a análise de variância e regressão, conforme as metodologias descritas por Pimentel-Gomes (1990).
RESULTADOS E DISCUSSÃO
Ao longo do período de tratamento com as diferentes soluções nutritivas (60 dias), os cravos não apresentaram sintomas visíveis de deficiência ou de excesso de nitrogênio. De acordo com Winsor & Adams (1987), o cravo é tolerante quanto à nutrição mineral, portanto não sendo os sintomas, tanto de deficiência como de excesso mineral, evidentes quando comparados a outras culturas em casa-de-vegetação. Estas condições são altamente desejáveis aos objetivos desta pesquisa, pois é de interesse testar plantas com deficiências ou toxidez capazes de causar apenas imperfeições metabólicas, antes que os sintomas de deficiências e toxidez morfológicas sejam manifestadas.
Os resultados obtidos para a calogênese induzida em diferentes explantes (folha, entrenós e nó) oriundos de matrizes de Dianthus caryophyllus L. tratadas por 30, 45 e 60 dias com soluções nutritivas contendo diferentes níveis de nitrogênio são mostrados nas Figuras 1, 2 e 3. Níveis crescentes de nitrogênio apresentaram efeito significativo (p£0,05) na produção de massa de matéria fresca de calos medida pelo IMC somente na calogênese induzida nos explantes folha coletados aos 30 dias após o início dos tratamento (Figura 1). Este efeito seguiu um modelo de equação de regressão quadrática (Y= 7,895 + 0,016X - 0,00003X2; R2= 0,49), que representa o índice de multiplicação celular (produção de massa de matéria fresca de calos) em função das concentrações de nitrogênio na solução nutritiva, sendo que o índice de multiplicação celular máximo de 10,03 ocorreu na dose estimada de 267 mg L-1 de N. O aumento dos níveis de nitrogênio na solução nutritiva até concentração por volta de 267 mg L-1 de N causou portanto acréscimo na calogênese pelo explante folha coletado aos 30 dias e decréscimo para concentrações de nitrogênio acima deste valor. Esta dose estimada foi superior àquela encontrada por Frett & Dirr (1986), que estudando o efeito do nitrogênio e do cálcio em calogênese de petúnia, obtiveram maior produção de massa de matéria fresca de calos em explantes folha provenientes de plantas tratadas com 100 mg L-1 de N.
Os resultados obtidos com o explante folha são diferentes daqueles observados por Borgatto (2000), que trabalhando com calogênese em Chrysanthemum morifolium observou maior ganho de massa de matéria fresca de calos em tratamento com nitrogênio de mais longa duração (60 dias).
Nenhum efeito significativo do tratamento com nitrogênio na calogênese (índice de multiplicação celular e massa de matéria seca de calos) foi observado para os explantes entrenós e nó (Figuras 2 e 3) quando avaliados nas três épocas de coleta (30, 45 e 60 dias), embora tratamentos mais prolongados (45 e 60 dias) afetaram negativamente a calogênese sendo a mesma portanto inversamente proporcional a concentração de nitrogênio na solução nutritiva. No entanto, estudos feitos por Borgatto (2000) relatam maior calogênese em explante entrenós de Chrysanthemum morifolium quando submetido a tratamento de longa duração (60 dias).
De acordo com Marschner (1995), o aumento da concentração de um nutriente estimula o crescimento, porém pode induzir deficiência de outro nutriente pelo efeito diluição, que deve ser considerado na interpretação dos conteúdos de nutrientes em termos de antagonismo durante a absorção. Também o ponto de inversão em qualquer curva de resposta de produção pode ser causado por fatores como toxicidade e/ou deficiência de um nutriente, bem como deficiência induzida competitivamente por um outro nutriente devido a um desbalanço iônico, como por exemplo, a indução de deficiência de potássio, cálcio e magnésio pelo amônio.
O nitrogênio está envolvido nos processos fisiológicos e bioquímicos associados ao controle de crescimento, diferenciação e morfogênese, sendo necessário para a síntese de macromoléculas e componentes celulares (Durzan, 1985), estando portanto associado às características químicas das matrizes e conseqüentemente dos explantes.
O nitrogênio é transportado no xilema e redistribuído no floema em processos relativamente rápidos. A redistribuição do nitrogênio pelo floema é de alta mobilidade, sendo portanto redistribuído das folhas e órgãos mais velhos para os mais novos (Malavolta et al., 1997). Isto está certamente relacionado com a ausência do efeito do tratamento com nitrogênio para os tratamentos de longa duração (Figura 1) em que pela translocabilidade do nitrogênio a concentração satisfatória ou excessiva do nutriente na planta é atingida.
De acordo com Raven et al. (1992), as duas principais funções associadas ao caule, do qual entrenós e nó fazem parte, são condução e sustentação, sendo as funções metabólicas das células do caule bastante modestas. Através do caule são transportados os nutrientes minerais, água e substâncias sintetizadas nas folhas, por intermédio do xilema e floema, para os locais de utilização, incluindo folhas, raízes e frutos, enquanto que a folha é considerada o principal órgão fotossintético e de biossíntese celular da planta. Portanto a concentração de nitrogênio nos tecidos do caule é relativamente baixa o que proporcionaria, com referência ao explante folha, baixa calogênese e ausência do efeito do tratamento com nitrogênio pelos explantes entrenós e nó.
Aparentemente, a duração do tratamento foi um fator importante para todos os níveis de nitrogênio testados. Entretanto estes resultados devem ser avaliados com alguma ressalva pois explantes retirados de plantas matrizes no período inicial de tratamento (30 dias) além de ter sido submetidos a escassez de nutrientes durante a aclimatação, quando as matrizes foram irrigadas somente com água por durante 15 dias, podem ainda estar sob efeito dos níveis de nutrientes minerais aplicados durante a fase de produção das mudas e ao reduzido desenvolvimento das raízes, podendo assim mascarar ou acentuar o efeito do tratamento com nitrogênio na calogênese pelos explantes coletados nesta época. Quanto a influência da idade fenológica dos explantes, este efeito pode ser desconsiderado pois os explantes foram sempre coletados na mesma posição da planta (segundo e terceiro par de folhas expandidas a partir do ápice), entretanto o efeito diluição deve ser considerado principalmente para os tratamentos de longa duração com baixos níveis de nitrogênio.
Recebido em 02.10.00
- BHOJWANI, S.S.; RAZDAN, M.K. Plant tissue culture: theory and practice. Amsterdam: Elsevier, 1996. 767p.
- BORGATTO, F. Tratamento de plantas matrizes de Chrysanthemum morifolium Ramat cv. "Bi Time" com N, P, K+, Ca2+ e Mg2+ e calogênese in vitro Piracicaba, 2000. 61p. Dissertação (Mestrado) - Escola Superior de Agricultura "Luiz de Queiroz", Universidade de São Paulo.
- CROCOMO, O.J. Biotecnologia de plantas: aplicações da engenharia celular. Biotecnologia: Agropecuária, Energia e Saúde, n.17, p.1-4, 1988.
- DURZAN, D.J. Nitrogen metabolism and vegetative propagation of forest trees. In: BONGA, J.M.; DURZAN, D.J. (Ed.) Tissue culture in forestry Dordrecht: Martinus Nijhoff, 1985. cap.10, p.256-324.
- FRETT, J.J.; DIRR, M.A. Effect of nitrogen and calcium stock plant nutrition on Petunia X Hybrida leaf and anther explant growth in vitro Scientia Horticulturae, v.28, p.289-298, 1986.
- FREY, L.; SARANGA, Y.; JANICK, J. Somatic embryogenesis in carnation. HortScience, v.27, p.63-65, 1992.
- GALLO, L.A.; CROCOMO, O.J. A cultura de tecidos em fitopatologia. In: BERGAMIN FILHO, A.; KIMATI, H.; AMORIN, L. (Ed.) Manual de fitopatologia: princípios e conceitos. São Paulo: Agronômica Ceres, 1995. v.1, cap.25, p.494-506.
- GRATTAPAGLIA, D.; MACHADO, M.A. Micropropagação. In: TORRES, A.C.; CALDAS, L.S. Técnicas e aplicações da cultura de tecidos de plantas Brasília: EMBRAPA, CNPH, 1990. p.99-169.
- HANDRO, W.; FLOH, E.I.S. Aspectos básicos do controle da morfogênese in vitro In: TORRES, A.C.; CALDAS, L.S. Técnicas e aplicações da cultura de tecidos de plantas Brasília: EMBRAPA, CNPH, 1990. p.204-212.
- MALAVOLTA, E.; VITTI, G.C.; OLIVEIRA, S.A. Avaliação do estado nutricional das plantas: princípios e aplicações. 2.ed. Piracicaba: Potafos, 1997. 319p.
- MARSCHNER, H. Mineral nutrition of higher plants 2.ed. London: Academic Press, 1995. 889p.
- MURASHIGE, T.; SKOOG, F. A revised medium for rapid growth and bioassays with tobaco tissue cultures. Physiologia Plantarum, v.15, p.473-497, 1962.
- PIMENTEL-GOMES, F. Curso de estatística experimental Piracicaba: Nobel, 1990. 468p.
- RAVEN, P.H.; EVERT, R.F.; EICHHORN, S.E. Biology of plants 5.ed. New York: Worth Publishers, 1992. 791p.
- SARRUGE, J.R. Soluções nutritivas. Summa Phytopatologica, v.1, p.231-233, 1975.
- STAFFORD, A.; WARREN, G. Plant cell and tissue culture Melksham: Red Wood Press, 1991. 251p.
- THORPE, T.A.; PATEL, K.R. Clonal propagation: adventitious buds. In: VASIL, I. (Ed.) Cell culture and somatic cell genetics of plants: laboratory procedures and their applications. Orlando: Academic Press, 1984. v.1, cap.7, p.49-60.
- VEASEY, E.A.; VIEIRA, M.L.; BANDEL, G. Tissue culture in Gramineae, with emphasis on forage grasses. Ciência e Cultura, v.43, p.36-43, 1991.
- WINSOR, G; ADAMS, P. Glasshouse crops: diagnosis of mineral disorders in plants. London: Her Majesty's Stationery Office, 1987. 168p.
Datas de Publicação
-
Publicação nesta coleção
27 Set 2002 -
Data do Fascículo
Mar 2002
Histórico
-
Recebido
10 Fev 2000