Resumos
Neste trabalho foi utilizado um sistema catalítico composto por hidreto de diisobutilalumínio (DIBAH), versatato de neodímio (NdV) e um agente de cloração para avaliar a influência da fonte de cloro e da razão molar Cl:Nd nas características da reação de polimerização (conversão e constante de velocidade de propagação) e do polibutadieno (massa molecular e microestrutura). Os agentes de cloração estudados foram cloreto de t-butila (t-BuCl), sesquicloreto de etilalumínio (EASC) e cloreto de dietilalumínio (DEAC). As razões molares Cl:Nd utilizadas foram: 1:1, 3:1 e 5:1 para o t-BuCl; 0,5:1, 1:1 e 3:1 para o EASC e 1:1, 1,5:1, 3:1 e 5:1 para o DEAC. Foi observada a existência, para cada agente de cloração, de um valor ótimo de razão molar Cl:Nd para o qual a conversão foi máxima. O DEAC apresentou uma maior conversão em relação aos outros agentes de cloração; em contrapartida, o t-BuCl produziu polibutadienos com maior teor de unidades 1,4-cis e maior massa molecular (<img border=0 width=32 height=32 src="../../../../../../../img/revistas/po/v19n2/a11ent02.gif" align=absmiddle>n e <img border=0 width=32 height=32 src="../../../../../../../img/revistas/po/v19n2/a11ent02.gif" align=absmiddle>w)
Catalisador Ziegler-Natta; neodímio; agente de cloração; polibutadieno 1,4-cis
In this work catalyst systems consisting of diisobutylaluminium hydride (DIBAH), neodymium versatate (NdV) and a chlorinating agent were employed to study the influence of the chloride source and Cl:Nd molar ratio on 1,3-butadiene polymerization and polybutadiene's characteristics (molecular weight and microstructure). The chloride sources studied were t-butyl chloride, ethylaluminium sesquichloride (EASC) and diethylaluminium chloride (DEAC). The Cl:Nd molar ratios used were 1:1, 3:1 e 5:1 for t-butyl chloride; 0.5:1, 1:1 and 3:1 for EASC and 1:1, 1.5:1, 3:1 and 5:1 for DEAC. A maximum value of Cl:Nd molar ratio exists. Moreover, DEAC showed to be more reactive than EASC and t-BuCl but t-BuCl produced higher molecular weight and cis-1,4 units contents.
Ziegler-Natta catalysts; neodymium; chlorinating agent; high cis-polybutadiene
ARTIGO TÉCNICO CIENTÍFICO
Influência do agente de cloração do catalisador à base de veodímio e da razão molar Cl:Nd na polimerização do butadieno
Influence of the chlorinating agent of neodymium based catalysts and Cl:Nd molar ratio on butadiene polymerization
Cintia N. Ferreira; Ivana L. Mello; Fernanda M. B. Coutinho
Instituto de Química, UERJ
Autor para correspondência Autor para correspondência: Fernanda M. B. Coutinho Instituto de Química, UERJ Rua São Francisco Xavier 524, PHLC - 3º andar - sala 310 - Maracanã CEP: 20550-900, Rio de Janeiro, RJ, Brasil E-mail: fern@ajato.com.br
RESUMO
Neste trabalho foi utilizado um sistema catalítico composto por hidreto de diisobutilalumínio (DIBAH), versatato de neodímio (NdV) e um agente de cloração para avaliar a influência da fonte de cloro e da razão molar Cl:Nd nas características da reação de polimerização (conversão e constante de velocidade de propagação) e do polibutadieno (massa molecular e microestrutura). Os agentes de cloração estudados foram cloreto de t-butila (t-BuCl), sesquicloreto de etilalumínio (EASC) e cloreto de dietilalumínio (DEAC). As razões molares Cl:Nd utilizadas foram: 1:1, 3:1 e 5:1 para o t-BuCl; 0,5:1, 1:1 e 3:1 para o EASC e 1:1, 1,5:1, 3:1 e 5:1 para o DEAC. Foi observada a existência, para cada agente de cloração, de um valor ótimo de razão molar Cl:Nd para o qual a conversão foi máxima. O DEAC apresentou uma maior conversão em relação aos outros agentes de cloração; em contrapartida, o t-BuCl produziu polibutadienos com maior teor de unidades 1,4-cis e maior massa molecular ( n e
n e  w)
w)
Palavras-chave: Catalisador Ziegler-Natta, neodímio, agente de cloração, polibutadieno 1,4-cis.
ABSTRACT
In this work catalyst systems consisting of diisobutylaluminium hydride (DIBAH), neodymium versatate (NdV) and a chlorinating agent were employed to study the influence of the chloride source and Cl:Nd molar ratio on 1,3-butadiene polymerization and polybutadiene's characteristics (molecular weight and microstructure). The chloride sources studied were t-butyl chloride, ethylaluminium sesquichloride (EASC) and diethylaluminium chloride (DEAC). The Cl:Nd molar ratios used were 1:1, 3:1 e 5:1 for t-butyl chloride; 0.5:1, 1:1 and 3:1 for EASC and 1:1, 1.5:1, 3:1 and 5:1 for DEAC. A maximum value of Cl:Nd molar ratio exists. Moreover, DEAC showed to be more reactive than EASC and t-BuCl but t-BuCl produced higher molecular weight and cis-1,4 units contents.
Keywords: Ziegler-Natta catalysts, neodymium, chlorinating agent, high cis-polybutadiene.
Introdução
Dentre os possíveis isômeros do polibutadieno, o de maior interesse industrial é o polibutadieno com alto teor de unidades 1,4-cis (polibutadieno alto-cis)[1]. Entretanto, para que sejam obtidos valores elevados de unidades 1,4-cis, é necessária a presença de um agente de halogenação no sistema catalítico[2]. O controle estereoquímico da polimerização de dienos conjugados só se tornou possível a partir do desenvolvimento dos catalisadores Ziegler-Natta[3]. A produção de polidienos estereorregulares depende tanto de fatores relacionados ao sistema catalítico quanto aos parâmetros da polimerização[4]. Há vários estudos na literatura[3-8,11,12] sobre sistemas catalíticos ternários, constituídos por um sal de neodímio, um agente de alquilação e um agente de halogenação. Assim, este trabalho tem por objetivo avaliar a influência do agente de halogenação (cloração) e da razão molar Cl:Nd na polimerização, na massa molecular e na microestrutura do polibutadieno.
Experimental
Materiais
Cloreto de t-butila - procedência: Aldrich Chemical Company, Inc.; usado como recebido; cloreto de dietilalumínio (DEAC) - procedência: Akzo Nobel; usado como recebido; sesquicloreto de etilalumínio (EASC) - procedência: Akzo Nobel; usado como recebido; hidreto de diisobutilalumínio (DIBAH) - procedência: Akzo Nobel; usado como recebido; versatato de Neodímio (NdV) - procedência: Rhodia-Rare Earths and Gallium, cedido pela Petroflex Indústria e Comércio S.A.; usado como recebido; hexano - procedência: cedido pela Petroflex Indústria e Comércio S.A, usado como recebido; 3,5-di-t-butil-4-hidroxi-tolueno (BHT) - procedência: Shell Brasil S.A., cedido pela Petroflex Indústria e Comércio S.A.; usado como recebido; irganox 1076 - procedência: Ciba Geigy Química S/A, cedido pela Petroflex Indústria e Comércio S.A.; usado como recebido; fosfito de trinofenilfenila (TNPP) - procedência: GE Specialty Chemicals cedido pela Petroflex Indústria e Comércio S.A.; usado como recebido; blend B (solução de butadieno em hexano) - procedência: cedido pela Petroflex Indústria e Comércio S.A.; usado como recebido; nitrogênio - Procedência: White Martins S.A; passado através de coluna recheada com peneira molecular de 3 Å e coluna com pentóxido de fósforo; nitrogênio super seco - Procedência: White Martins S.A; passado através de coluna recheada com peneira molecular de 3 Å.
Métodos
Preparo do catalisador
A primeira etapa consistiu no preparo das soluções de DIBAH e do agente de cloração, utilizadas logo em seguida. Transferiu-se determinado volume da solução de DIBAH para uma garrafa com capacidade de 300 mL, previamente lacrada com uma gaxeta de borracha e tampa de alumínio, contendo em seu interior uma barra magnética revestida de teflon. Em seguida a garrafa foi colocada sob agitação magnética e resfriada a uma temperatura de 10 ºC. Sob agitação, adicionou-se à garrafa um determinado volume de uma solução de versatato de neodímio. Após aproximadamente 10 minutos transferiu-se para a garrafa um determinado volume da solução do agente de halogenação. Feito isso, manteve-se o sistema sob agitação por uma hora. Decorrido esse tempo, o catalisador foi levado para envelhecer por 24 horas a 5 ºC.
Reação de polimerização
O volume total da solução de monômero e parte do volume de solvente utilizado ao longo da reação foi transferido, por diferença de pressão, para o reator de polimerização, nessa ordem. Em seguida admitiu-se nitrogênio para remover algum resíduo porventura retido ao longo da linha de transferência. Após a temperatura ter atingido 70 ºC, adicionou-se um determinado volume do catalisador, sob fluxo de nitrogênio, e em seguida, transferiu-se o volume restante do solvente seguido de nitrogênio para garantir a transferência total do catalisador para o reator de polimerização.
Durante a reação foram retiradas amostras de 15 em 15 minutos na primeira hora de reação, e de 30 em 30 minutos na segunda hora para que se acompanhar a conversão ao longo da reação. Após duas horas, o polímero obtido foi transferido para um segundo reator, contendo um determinado volume de solvente e de uma solução de BHT em hexano. Em seguida foi transferido um determinado volume de solvente e de nitrogênio para garantir a remoção total da solução de polímero. Após 15 minutos, adicionou-se um volume determinado da solução de antioxidante. A solução polimérica obtida foi coagulada em um reator de vidro encamisado contento água destilada a 80 ºC, sob agitação intensa. Finalmente, o polímero coagulado foi seco em estufa a 60 ºC.
Caracterização do polibutadieno
A microestrutura dos polímeros foi caracterizada por espectroscopia na região do infravermelho em um espectrômetro Perkin-Elmer, modelo Spectrum One, como filmes de polibutadieno, formados sobre célula de KBr, por vazamento de uma solução a 2% (p/v) de polibutadieno em clorofórmio O teor de cada unidade repetitiva isomérica foi obtido a partir das absorbâncias em 725 cm-1 (1,4-cis), 910 cm-1 (1,2-vinila) e 965 cm-1 (1,4-trans) de acordo com o método de Kimmer[3]. Esse método considera que a soma das proporções das unidades isoméricas corresponde ao total das ligações duplas (100%).
A determinação das massas molares médias foi realizada por cromatografia de exclusão por tamanho (SEC), utilizando cromatógrafo de permeação em gel (GPC) Waters 600, equipado com injetor automático Waters 717 Autosampler, detector de índice de refração 2410 e colunas de Styragel com limites de exclusão entre 50 e 1 × 106 Å, calibradas com padrões monodispersos de poliestireno. As medidas foram feitas a 30 ºC e as amostras injetadas automaticamente, sob um fluxo de 1 mL/min como soluções a 0,15% (m/v) em tetra-hidrofurano.
Resultados e Discussão
Inicialmente, pretendia-se testar as três razões molares Cl:Nd (1:1, 3:1 e 5:1) para todos os agentes de halogenação. Entretanto, ao se testar o EASC na razão molar Cl:Nd = 3:1, a conversão da reação de polimerização foi muito baixa, por isso a razão molar Cl:Nd = 5:1 para este agente de halogenação não foi estudada. Devido ao fato de o EASC conter três átomos de cloro em sua estrutura, decidiu-se testar este agente de halogenação na razão molar Cl:Nd = 0,5:1. Os catalisadores em que se utilizou DEAC como agente de halogenação na razão molar Cl:Nd = 5:1 não foram testados pois a sua solução se apresentou turva e muito viscosa.
A Figura 1 mostra o comportamento da conversão com o tempo de polimerização para os diferentes agentes de halogenação utilizados em diferentes razões molares Cl:Nd.
Quando se comparam os valores de conversão encontrados para os três agentes de halogenação ao final da reação, pode-se observar que há um "valor ótimo" para a razão molar Cl:Nd para o qual, após duas horas de reação, a conversão encontrada é máxima. Esse valor é igual a 3:1, 0,5:1 e 1:1 quando se utiliza como agente de halogenação o t-BuCl, o EASC e o DEAC, respectivamente.
A utilização de valores de razão molar Cl:Nd abaixo do "valor ótimo" resulta em uma menor conversão. Isso se deve, ou à menor quantidades de sítios catalíticos, conseqüência da menor quantidade de átomos de cloro, ou à formação de sítios menos ativos. A diminuição da conversão também ocorre quando são utilizados valores de razão molar Cl:Nd acima do "valor ótimo". Nesse caso, devido à aglomeração de partículas de NdCl3, insolúveis, resultantes de uma "supercloração"[2,5-7].
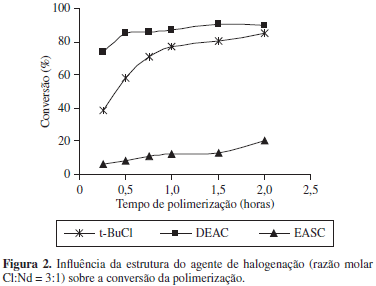
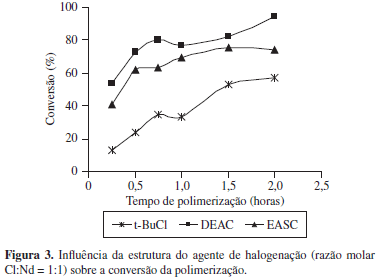
As Figuras 2 e 3 mostram a influência da estrutura do agente de halogenação sobre a conversão, quando são utilizadas as mesmas razões molares Cl:Nd (1:1 e 3:1).
Os resultados obtidos indicam que, em ambas as razões molares, o DEAC foi o agente de halogenação que apresentou a maior atividade catalítica, seguido pelo t-BuCl e pelo EASC, nessa ordem, quando se utilizou a razão molar Cl:Nd 3:1. Quando a razão molar Cl:Nd = 1:1 foi utilizada, os resultados obtidos seguiram a ordem: DEAC > EASC > t-BuCl. Esses resultados não estão em concordância com os resultados encontrados na literatura[8], porém as condições utilizadas foram diferentes das empregadas neste trabalho. Quirk[8], em seu trabalho, utilizou um sistema catalítico constituído por NdV e DIBAH, e estudou a influência do agente de halogenação na atividade catalítica na massa molar, na polidispersão e no teor de unidades 1,4-cis do polibutadieno. Os agentes de halogenação utilizados foram EASC, DEAC e t-BuCl, a razão molar Nd:Cl:Al utilizada foi 1:3:25. O catalisador no qual foi utilizado o t-BuCl foi envelhecido a 20 ºC por 24 horas e os catalisadores nos quais foram utilizados o DEAC e o EASC foram ativados in situ, a reação de polimerização ocorreu por 1 hora a 70 ºC. A ordem encontrada para a atividade catalítica foi: EASC = DEAC > t-BuCl.
Não foi encontrado na literatura nenhum estudo comparando diferentes agentes de halogenação, utilizando a razão molar Cl:Nd = 1:1.
A Tabela 1 mostra a influência do agente de halogenação e da razão molar Cl:Nd sobre a massa molecular numérica média ( n), a massa molecular ponderal média (
n), a massa molecular ponderal média ( w) e a microestrutura do polibutadieno
w) e a microestrutura do polibutadieno
Ao se analisar os resultados obtidos, comparando-se o mesmo agente de halogenação em diferentes razões molares Cl:Nd, concluiu-se que usando o t-BuCl e com o DEAC como agentes de halogenação, houve uma tendência ao aumento da massa molecular ( w) com o aumento da razão molar Cl:Nd. Esse comportamento deve-se ao aumento de sítios ativos insolúveis com o aumento da razão molar Cl:Nd. Sendo assim, conclui-se que quando são utilizados baixos valores de razão molar Cl:Nd, tem-se a formação de sítios menos ativos e não de menos sítios ativos, pois, se assim fosse, ao serem utilizados baixos valores de razão molar Cl:Nd, seriam obtidos os maiores valores de massa molecular[5]. Quando se utilizou o EASC como agente de halogenação, a maior massa molecular (
w) com o aumento da razão molar Cl:Nd. Esse comportamento deve-se ao aumento de sítios ativos insolúveis com o aumento da razão molar Cl:Nd. Sendo assim, conclui-se que quando são utilizados baixos valores de razão molar Cl:Nd, tem-se a formação de sítios menos ativos e não de menos sítios ativos, pois, se assim fosse, ao serem utilizados baixos valores de razão molar Cl:Nd, seriam obtidos os maiores valores de massa molecular[5]. Quando se utilizou o EASC como agente de halogenação, a maior massa molecular ( w) foi encontrada com o catalisador no qual a razão molar Cl:Nd utilizada foi 0,5:1, devido à menor concentração de sítios ativos formados em função da menor quantidade de átomos de cloro presentes no sistema[7].
w) foi encontrada com o catalisador no qual a razão molar Cl:Nd utilizada foi 0,5:1, devido à menor concentração de sítios ativos formados em função da menor quantidade de átomos de cloro presentes no sistema[7].
Com relação à microestrutura do polibutadieno obtido, pode-se concluir que, quando se utilizou o t-BuCl como agente de halogenação, o teor de unidades 1,4-cis aumentou com o aumento da razão molar Cl:Nd até a razão molar Cl:Nd = 3:1, em seguida apresentou uma tendência ao declínio.
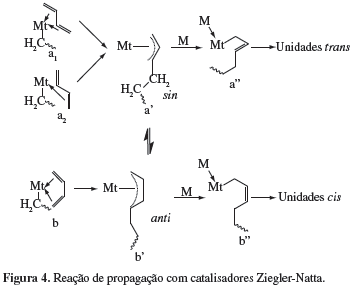
Na etapa de propagação da polimerização do 1,3-butadieno, a inserção da nova molécula de monômero na ligação carbono-metal (C-Mt) ocorre em duas etapas i) coordenação do monômero com o metal; e ii) insersão do monômero em uma ligação metal-carbono, que pode ocorrer em C(3), originando nesse caso unidades 1,2-vinila, ou em C(1) originando unidades 1,4-cis ou 1,4-trans (Figura 4). O predomínio de uma delas é determinado pelas velocidades relativas do processo de inserção e de isomerização anti-sin. Essas duas formas estão em equilíbrio, e este, à temperatura ambiente é deslocado em direção à forma sin que é termodinamicamente mais estável. Sendo assim, as unidades 1,4-trans podem ser formadas via a1 ou a2  a'
a'  a'' ou via b
a'' ou via b  b'
b'  a'
a'  a'', e as unidades 1,4-cis são formadas via b
a'', e as unidades 1,4-cis são formadas via b  b'
b' b''. Se o processo de inserção for mais rápido que o de isomerização, a formação de unidades 1,4-cis será favorecida, porém se o processo de isomerização for mais rápido haverá a formação de unidades 1,4-trans[5,9-10].
b''. Se o processo de inserção for mais rápido que o de isomerização, a formação de unidades 1,4-cis será favorecida, porém se o processo de isomerização for mais rápido haverá a formação de unidades 1,4-trans[5,9-10].
Quando se utilizou o t-BuCl na razão molar Cl:Nd = 1:1 foi encontrado o menor valor de unidades 1,4-cis devido à menor velocidade que a reação apresentou nesse caso (Figura 5). Isso fez com que houvesse tempo para que ocorresse a isomerização da configuração anti para a configuração sin. Quando se utilizou valores mais elevados de razão molar Cl:Nd, devido ao aumento da velocidade, não houve tempo para que ocorresse a isomerização, resultando em um aumento no teor de unidades 1,4-cis. Quando se utilizou o DEAC, levando-se em consideração os valores de k ao longo de toda a polimerização (Figura 5), ao se aumentar a razão molar Cl:Nd de 1:1 para 1,5:1, houve um aumento no valor de k, o que favoreceu a reação de inserção em relação à reação de isomerização, ocasionando assim, um aumento no teor de unidades 1,4-cis. Quando se utilizou a razão molar Cl:Nd = 1:1 foram obtidos os maiores valores de velocidade de polimerização durante todo o período de reação, o que fez com que se obtivesse, utilizando essa razão molar, o maior teor de unidades 1,4-cis.
Quando se utilizou o EASC, observou-se a diminuição do teor de unidades 1,4-cis com o aumento da razão molar Cl:Nd até a razão molar Cl:Nd = 1:1, devido à queda da velocidade (Figura 5). Isso fez com que houvesse tempo suficiente para que ocorresse a isomerização, e conseqüentemente um aumento no teor de unidades 1,4-trans. Em seguida, observou-se o aumento do teor de unidades 1,4-cis com o aumento da razão molar Cl:Nd, apesar da queda de velocidade (Figura 5). Possivelmente, a partir da razão molar Cl:Nd = 1:1 o equilíbrio entre as formas anti e sin passou a ser deslocado para a forma menos estereoimpedida (anti) e não para a termodinamicamente mais estável (sin). Sendo assim, a queda na velocidade ocasionou uma diminuição no teor de unidades 1,4-trans e um aumento no teor de unidades 1,4-cis[11].
Ao se analisar os diferentes agentes de halogenação nas razões molares 3:1 e 1:1, o t-BuCl foi o que apresentou o maior valor de massa molecular ( w). Isso sugere que um menor número de sítios ativos é gerado quando se utiliza esse agente de halogenação[8]. Com relação à microestrutura, o t-BuCl, forneceu um maior teor de unidades 1,4-cis, seguido pelo EASC e pelo DEAC, respectivamente. Esses resultados não estão de acordo com a literatura[8,12], segundo a qual o agente de halogenação não altera a microestrutura do polibutadieno. Entretanto, cloretos de alquilalumínio do tipo RxAlyClz, atuam tanto como agentes de alquilação como agentes de halogenação, sendo assim, o DEAC por ter um maior poder de alquilação em relação ao EASC concorre de maneira mas eficaz pela vacância do átomo de neodímio, favorecendo a inserção 1,4-trans e, conseqüentemente, diminuindo o teor de unidades 1,4-cis[2].
w). Isso sugere que um menor número de sítios ativos é gerado quando se utiliza esse agente de halogenação[8]. Com relação à microestrutura, o t-BuCl, forneceu um maior teor de unidades 1,4-cis, seguido pelo EASC e pelo DEAC, respectivamente. Esses resultados não estão de acordo com a literatura[8,12], segundo a qual o agente de halogenação não altera a microestrutura do polibutadieno. Entretanto, cloretos de alquilalumínio do tipo RxAlyClz, atuam tanto como agentes de alquilação como agentes de halogenação, sendo assim, o DEAC por ter um maior poder de alquilação em relação ao EASC concorre de maneira mas eficaz pela vacância do átomo de neodímio, favorecendo a inserção 1,4-trans e, conseqüentemente, diminuindo o teor de unidades 1,4-cis[2].
Conclusões
A variação tanto do agente de halogenação quanto da razão molar Cl:Nd utilizada provocou variações significativas tanto na conversão e na constante de velocidade de propagação da polimerização quanto na massa molecular e na microestrutura do polibutadieno obtido. Sendo assim, é possível otimizar as características da polimerização e do polibutadieno através da escolha do agente de halogenação e da razão molar Cl:Nd.
Agradecimentos
As autoras agradecem ao Conselho Nacional de Desenvolvimento Científico e Tecnológico (CNPq), à Fundação de Amparo à Pesquisa do Estado do Rio de Janeiro (FAPERJ), à Coordenação de Aperfeiçoamento de Pessoal de Nível Superior (Capes) e à Petroflex Indústria e Comércio S.A.
Enviado: 24/08/08
Reenviado: 26/01/09
Aceito: 09/02/09
- 1. Macedo, M. M. - "Polibutadieno 1,4-cis", Dissertação de Mestrado, Universidade do Estado do Rio de Janeiro, Brasil (2001).
- 2. Friebe, L.; Nuyken, O. & Obrecht, W. - Polym. Sci., 204, p.1 (2006).
- 3. Mello, I. L. - "Efeito do solvente na polimerização 1,4-cis de 1,3-butadieno com catalisador à base de neodímio", Dissertação de Mestrado, Universidade Federal do Rio de Janeiro, Brasil (2003).
- 4. Nunes, D. S. S.; Coutinho, F. M. B. & Mello, I. L. - Polímeros, 15, p.296 (2005).
- 5. Pires, N. M. T. - "Estudo de sistemas catalíticos à base de neodímio para a produção de polibutadieno alto-cis", Tese de Doutorado, Universidade Federal do Rio de Janeiro, Brasil (2004).
- 6. Mello, I. L. - "Estudo do envelhecimento de sistemas catalíticos Ziegler-Natta à base de neodímio para a polimerização de 1,3-butadieno", Tese de Doutorado, Universidade Federal do Rio de Janeiro, Brasil (2007).
- 7. Quirk, R. P.; Kells, A. M.; Yunlu, K. & Cuif, J. C. - Polymer, 41, p.5903 (2000).
- 8. Quirk, R. P. & Kells, A. M. - Polym. Int., 49, p.751 (2000).
- 9. Costabile, C.; Milano, G.; Cavallo, L. & Guerra, G. - Macromolecules, 34, p.7952 (2001).
- 10. Tobish, S. - J. Macromol. Struct.: TEOCHEM, 771, p.171 (2006).
- 11. Ferreira, C. N. - "Influência do agente de halogenação e da razão molar Cl: Nd na polimerização e nas características do polibutadieno obtido com catalisador Ziegler-Natta à base de neodímio", Dissertação de Mestrado, Universidade do Estado do Rio de Janeiro, Brasil (2008).
- 12. Wilson, D. J. - J. Polym. Sci. Part A: Polym. Chem., 33, p.2505 (1995).
Autor para correspondência:
Datas de Publicação
-
Publicação nesta coleção
13 Ago 2009 -
Data do Fascículo
Jun 2009
Histórico
-
Aceito
09 Fev 2009 -
Recebido
24 Ago 2008