Resumos
O presente manuscrito descreve o desenvolvimento de um sensor descartável sensível e seletivo baseado em filmes de polipirrol dopados (PPy) para determinação íons fluoreto. Os íons fluoretos foram incorporados na matriz PPy durante a polimerização eletroquímica realizada em condições galvanostáticas em um eletrodo compósito etileno vinil acetato e negro de fumo. Parâmetros experimentais envolvidos na preparação de película PPy tais como densidade de corrente elétrica, carga elétrica, o pH e a concentração de eletrólito foram otimizados de forma a maximizar a resposta potenciométrica. A resposta do sensor para íons de flúor foi linear no intervalo de concentração de 1,00 × 10- 5 a 1,08 × 10- 2 mol L- 1, com uma inclinação de ~ 40 mV / pF e foi estável suficiente para várias determinações. O método foi aplicado com sucesso na determinação de íons fluoreto em amostras comerciais farmacêuticas. Os resultados demonstraram que o sensor proposto pode ser utilizado como uma alternativa interessante aos métodos analíticos tradicionais para determinação de íons fluoreto.
Filmes de polipirrol; íons fluoreto; eletrodos íon-seletivo; eletrodo compósito
This manuscript describes the development of a sensitive and selective disposable potentiometric sensor based on doped polypyrrole films (PPy) for fluoride ions determination. The fluoride ions were incorporated in the PPy matrix during electrochemical polymerization under galvanostatic conditions on a composite electrode of ethylene vinyl acetate and black carbon. Experimental parameters involved in PPy film preparation, such as electric current densities, electric charge, pH and electrolyte concentration, were optimized in order to maximize the potentiometric response. The sensor response for fluoride ions was linear in the concentration range of 1.00 × 10- 5 to 1.08 × 10- 2 mol L- 1, with a slope of ~40 mV/pF, and it was sufficiently stable for several determinations. The method was successfully applied in the determination of fluoride ions in pharmaceutical commercial samples. Results demonstrated that the proposed sensor can be used as an interesting alternative to traditional analytical methods for fluoride ions.
Polypyrrole films; fluoride ions; ions-selective electrode; composite electrode
ARTIGO TÉCNICO CIENTÍFICO
Filmes de polipirrol aplicados no desenvolvimento de eletrodos descartáveis seletivos a íons fluoreto
Polypyrrole films applied to development of disposable ion-selective electrode for fluoride ions determination
Alyne Cristina Lamy-Mendes; Eduardo Henrique Bindewald; Maurício Alberto Poletti Papi; Luiz Humberto Marcolino-Jr; Márcio Fernando Bergamini
Laboratório de Sensores Eletroquímicos - LabSensE, Departamento de Química, Universidade Federal do Paraná - UFPR
Endereço para correspondência Endereço para correspondência: Márcio Fernando Bergamini Laboratório de Sensores Eletroquímicos - LabSensE Departamento de Química, Centro Politécnico Universidade Federal do Paraná - UFPR Av. Cel. Francisco H. dos Santos, 210, Jardim das Américas, CP 19081 CEP 81531-990, Curitiba, Paraná, Brasil e-mail: bergamini@ufpr.br
RESUMO
O presente manuscrito descreve o desenvolvimento de um sensor descartável sensível e seletivo baseado em filmes de polipirrol dopados (PPy) para determinação íons fluoreto. Os íons fluoretos foram incorporados na matriz PPy durante a polimerização eletroquímica realizada em condições galvanostáticas em um eletrodo compósito etileno vinil acetato e negro de fumo. Parâmetros experimentais envolvidos na preparação de película PPy tais como densidade de corrente elétrica, carga elétrica, o pH e a concentração de eletrólito foram otimizados de forma a maximizar a resposta potenciométrica. A resposta do sensor para íons de flúor foi linear no intervalo de concentração de 1,00 × 10 - 5 a 1,08 × 10 - 2 mol L - 1, com uma inclinação de ~ 40 mV / pF e foi estável suficiente para várias determinações. O método foi aplicado com sucesso na determinação de íons fluoreto em amostras comerciais farmacêuticas. Os resultados demonstraram que o sensor proposto pode ser utilizado como uma alternativa interessante aos métodos analíticos tradicionais para determinação de íons fluoreto.
Palavras-chave: Filmes de polipirrol, íons fluoreto, eletrodos íon-seletivo, eletrodo compósito.
ABSTRACT
This manuscript describes the development of a sensitive and selective disposable potentiometric sensor based on doped polypyrrole films (PPy) for fluoride ions determination. The fluoride ions were incorporated in the PPy matrix during electrochemical polymerization under galvanostatic conditions on a composite electrode of ethylene vinyl acetate and black carbon. Experimental parameters involved in PPy film preparation, such as electric current densities, electric charge, pH and electrolyte concentration, were optimized in order to maximize the potentiometric response. The sensor response for fluoride ions was linear in the concentration range of 1.00 × 10 - 5 to 1.08 × 10 - 2 mol L - 1, with a slope of ~40 mV/pF, and it was sufficiently stable for several determinations. The method was successfully applied in the determination of fluoride ions in pharmaceutical commercial samples. Results demonstrated that the proposed sensor can be used as an interesting alternative to traditional analytical methods for fluoride ions.
Keywords: Polypyrrole films, fluoride ions, ions-selective electrode, composite electrode.
Introdução
O desenvolvimento de sensores eletroquímicos vem sendo amplamente explorado nos últimos anos, devido a características apresentadas por estes dispositivos tais como: baixos limites de detecção, alta seletividade e estabilidade[1]. Dentre as diversas possibilidades de resposta dos sensores eletroquímicos, podemos destacar os potenciométricos devido à simplicidade operacional e o baixo custo. Destaque para os eletrodos íon-seletivo (ISE) de membrana que permitem a determinação dos mais diversos analitos com alta seletividade, baixos limites de detecção e poucos efeitos de interferência da matriz[2].
O uso de polímeros condutores, como o polipirrol (PPy), para a fabricação de ISE tem se destacado por exibir características como: alta condutividade, estabilidade química e síntese relativamente simples, além da possibilidade de ser empregado em diversos solventes[3]. O aspecto mais interessante envolvido na síntese do polipirrol é que em sua forma oxidada o filme incorpora ânions como contra-íons, para manter a eletroneutralidade do sistema[4]. A capacidade de incorporação de diferentes ânions na estrutura polimérica durante o processo de polimerização afeta diretamente propriedades como adesão, condutividade, morfologia, resistência mecânica e atividade química[5] e também confere seletividade ao íon dopante o que possibilita o uso deste material para a construção de eletrodos íon-seletivos as espécies incorporadas. Na literatura são verificados relatos do uso do polipirrol para a determinação de diversas espécies de interesse, como por exemplo, nitrato[6], cloreto[7], perclorato[8], dipirona[9] e sacarina[10].
A preparação dos filmes de polipirrol dopados pode ser realizada sobre as mais diversas superfícies eletródicas, como cobre[11] e platina[12], empregando diferentes métodos eletroquímicos como, por exemplo, procedimentos potenciodinâmico, potenciostático e galvanostático[13]. Visando o desenvolvimento de um dispositivo de menor custo, que envolva materiais de baixo custo e procedimentos mais simples e menos onerosos, os eletrodos a base de carbono se tornam uma opção atraente. Dentro deste contexto, diversos trabalhos encontrados na literatura descrevem o uso de eletrodos compósitos de carbono ou grafite escolar como materiais base para a construção de ISE, resultando em um dispositivo final de baixo custo de produção e versáteis, que em muitos casos, pode ser utilizado como um eletrodo descartável[9,13-15].
Os íons fluoreto são utilizados com frequência como um eficiente redutor na incidência de cáries dentárias[16-18] sendo inclusive comum a fluoração de águas de abastecimento das cidades[19,20] tornando-o assim uma espécie cujo interesse está intimamente ligada a saúde pública. Apesar disso, essa medida muitas vezes ainda não é suficiente para a promover o efeito desejado sendo complementada pela presença destes íons em cremes dentais e antissépticos bucais. Além da determinação de fluoreto em amostras comerciais o desenvolvimento de procedimentos com precisão e seletividade, permite também a prevenção com relação ao uso, uma vez que a dose letal para o organismo humano é por volta de 5 mg de fluoreto/kg de peso corporal[21].
Considerando os fenômenos de incorporação envolvendo filmes de polipirrol e a potencialidade desse material na construção de ISE, a proposta deste estudo foi construir e avaliar o desempenho de um sensor potenciométrico para íons fluoreto como uma alternativa de baixo custo para sua determinação.
Experimental
Materiais
Os reagentes empregados foram: Pirrol (Acros Organics) previamente destilado, Sulfato de Amônio (Sigma-Aldrich) e Fluoreto de Potássio (Sigma-Aldrich). As soluções foram preparadas com água destilada, e quando necessário o ajuste de pH foi realizado pela adição de solução estoque de NaOH ou HCl.
Para as medidas eletroquímicas, potenciométricas e demais procedimentos foram utilizados: Potenciostato/Galvanostato μAutolab Type III, multímetro (ICEL Manaus MD-6115), agitador magnético (Synth), kit de destilação, eletrodo de referência Ag/AgCl 3,0 mol L - 1 de KCl, eletrodo de placa de platina (Metrohm) como contra-eletrodo.
Procedimento experimental
A metodologia utilizada para a construção dos ISE foi constituída em quatro etapas básicas: i) preparação do material eletródico, ii) preparação dos eletrodos, iii) eletropolimerização do pirrol e iv) medidas potenciométricas. O material eletródico utilizado no presente trabalho foi composto de 40% (m/m) de aglutinante EVA (Etileno Vinil Acetato) e 60% de Negro de Fumo como condutor. Este material foi conectado a um fio de cobre para o contato elétrico e fixado a um suporte plástico.
Polimerização do pirrol
A polimerização do pirrol sobre o eletrodo compósito foi realizada utilizando o método galvanostático[9,22] em uma solução contendo fluoreto de potássio 0,1 mol L - 1 e 1,0 mol L - 1 de pirrol. Foram utilizadas diferentes densidades de correntes e cargas na formação do filme de polipirrol dopado com íons fluoreto para avaliar a influência desses parâmetros na resposta potenciométrica.
Medidas potenciométricas
As medidas potenciométricas realizadas para a avaliação da resposta do eletrodo indicador (ISE) foram feitas sob agitação constante em uma célula contendo dois eletrodos, o referência de Ag/AgCl 3,0 mol L - 1 de KCl (ânodo) e o eletrodo íon-seletivo (cátodo), em uma solução de (NH4)2SO4 1,0 × 10 - 2 mol L - 1. Foram realizadas adições sucessivas da solução estoque do padrão de íons fluoreto.
Com o auxílio de um multímetro, acompanhou-se a variação de potencial desenvolvida na interface eletrodo-solução. Parâmetros como o pH do eletrólito suporte, tempo de resposta do eletrodo e efeito de interferentes foram avaliados.
Preparo da amostra comercial
Para a determinação de fluoreto em amostras comerciais de enxaguante bucal, foi empregado o método de adição padrão. Um volume de 1,0 mL da amostra foi adicionado em um balão volumétrico de 10 mL e seu volume completado com eletrólito suporte ((NH4)2SO4 1,0 × 10 - 2 mol L - 1), obtendo-se uma concentração de referência de 1,08 × 10 - 3 mol L - 1 de F - .
Resultados e Discussão
Comportamento potenciométrico do dispositivo
A formação do filme de polipirrol foi realizada utilizando uma corrente positiva sobre a superfície do eletrodo compósito em solução contendo pirrol e íons fluoreto. A polimerização do pirrol se inicia através da oxidação do monômero, o que leva à formação de um intermediário cátion-radical pirrol. O cátion-radical se associa a outros monômeros do pirrol e, sucessivamente, vão sendo formadas cadeias de oligômeros que por sua vez levam à formação do polipirrol. O processo de dopagem ocorre com a oxidação da cadeia polimérica, o que leva à formação de um policátion carregado que é balanceado pela entrada de um contra íon dopante (fluoreto neste caso), formando assim filmes de polipirrol dopados com íons fluoreto (PPy-F - ).
Um estudo comparativo para avaliar o comportamento da resposta potenciométrica para íons F- entre os eletrodos, modificado com filmes de PPy-F - e sem modificação, é apresentado na Figura 1.
Observa-se na Figura 1 que para o eletrodo modificado (A) há uma variação no potencial a medida que a concentração de fluoreto aumenta na solução, o que não ocorre para o eletrodo não modificado (B). Através da regressão linear da curva se obtém a equação da reta para o eletrodo modificado: E (mV) = 86,45 + 21,43 pF, revelando uma adequada sensibilidade. Eletrodos modificados com filmes de polipirrol preparados em solução contendo outros ânions, como cloreto e nitrato, não exibiram resposta potenciométrica significava para os íons fluoreto. Esses resultados confirmam a incorporação de íons F - no filme de polipirrol conferindo uma seletividade na resposta potenciométrica para o ânion dopante. A resposta potenciométrica observada é atribuída ao equilíbrio formado entre a interface da membrana dopada e os ânions presentes em solução, sendo dada por: E (mV) = constante + (59,16*β) pA[6]. O coeficiente de variação potenciométrica depende do parâmetro β, chamado de eficiência eletromotriz, que está relacionado a características estruturais da membrana e com a mobilidade do ânion no interior do filme. Espécies com maior mobilidade e pouca interação com a rede polimérica apresentam valores de β próximo a 1. Uma vez demonstrada que a modificação do eletrodo promove sensibilidade ao dispositivo, torna-se necessário o estudo dos parâmetros experimentais envolvidos buscando as melhores condições de preparação do filme.
Otimização da densidade de corrente e carga elétrica
Os parâmetros envolvidos na formação do filme de polipirrol, como carga elétrica e densidade de corrente, foram estudados a fim de obter a melhor sensibilidade para o ISE. Primeiramente foi investigado o efeito da carga elétrica total aplicada ao eletrodo durante a formação do filme de polipirrol, a variação da sensibilidade (slope) em função da carga utilizada está apresentada na Figura 2.
Os valores aplicados variaram de 0,5 mC a 75 mC e verificou-se um aumento da sensibilidade em função do aumento da carga aplicada até o valor de 50 mC (Figura 2). Esses resultados sugerem que a quantidade de carga aplicada é proporcional à quantidade de filme de polipirrol formado na superfície do substrato. Filmes formados por valores abaixo de 50 mC não exibem uma resposta adequada, já valores de cargas mais elevadas tornam o filme muito espesso, e, como consequência, apresentam uma maior resistividade ocorrendo um decréscimo da sensibilidade[9,22]. Entre os valores avaliados determinou-se então que a carga de 50 mC apresentou a melhor resposta em função da maior sensibilidade obtida.
Depois de estudado o efeito da carga elétrica sobre a resposta potenciométrica do ISE foi avaliada a densidade de corrente aplicada, variando de 0,2 a 2,2 mA cm - 2. A densidade de corrente é importante para uma estruturação adequada do filme de polipirrol, pois, segundo DePaoli et al.[22], altas densidades de corrente podem acarretar na formação de um filme irregular enquanto valores baixos desse parâmetro podem não ser suficientes para a reação de polimerização efetiva. A Figura 3 apresenta os resultados obtidos.
Os resultados obtidos nesse estudo mostraram que a melhor sensibilidade do eletrodo foi observada para o filme polimerizado sob uma densidade de corrente igual a 1,4 mA cm - 2, sendo esse valor então fixado para os estudos posteriores.
Influência do pH sobre a resposta potenciométrica do eletrodo
Avaliou-se o efeito do pH sobre a resposta potenciométrica do eletrodo para valores entre 4,5 e 6,5. Os resultados obtidos demonstraram uma melhor resposta do eletrodo em uma solução de 1,0 × 10 - 2 mol L - 1 de (NH4)2SO4 pH 6, assim esse foi o valor escolhido para a solução de sulfato de amônio utilizada como eletrólito suporte. Para valores de pH menores que 5,5 observa-se uma diminuição gradual da resposta que pode ser atribuída a protonação parcial dos ânions fluoreto podendo haver a formação de ácido fluorídrico (HF), pois o pKa do HF é 3,17[23]. Valores mais elevados de pH podem promover a reação entre os íons hidroxila e a rede polimérica presente na superfície eletródica, como sugerido por Maksymiuk[24], que em valores de pH próximos a neutralidade os íons OH- podem atuar como nucleófilos se ligando à cadeia polimérica, essa reação leva a perda do ânion dopante e consequentemente perda da seletividade da resposta potenciométrica.
Efeito do tempo de condicionamento
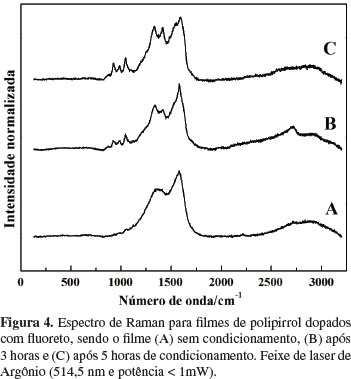
Em geral, a reposta potenciométrica de eletrodos íon-seletivos de membrana pode apresentar uma melhora quando o dispositivo é mantido em solução contendo o analito, a fim de verificar esse efeito foi estudado o tempo de condicionamento em uma solução de fluoreto de potássio 1,0 × 10 - 2 mol L - 1 no intervalo de zero hora (sem condicionamento) a 48h. Foi verificada a melhor resposta logo após a preparação do filme e um decréscimo acentuado com tempo de condicionamento. Esse comportamento pode ser atribuído a uma possível reação entre a rede polimérica e os íons F-, em um mecanismo semelhante ao efeito dos íons OH-. Com o intuito de verificar a ocorrência desta reação entre os íons fluoreto e a rede polimérica foram realizadas medidas de espectroscopia Raman para diferentes tempos de condicionamento do eletrodo (0h, 2h e 5h). Os espectros obtidos estão representados na Figura 4.
As bandas entre 1580 cm - 1 e 1592 cm - 1 podem ser atribuídas à banda de estiramento C=C. Os picos próximos de 1410 cm - 1 são característicos do estiramento C-N, enquanto os próximos de 1330 cm - 1 são do estiramento do anel. Os picos próximos de 920 cm - 1 são atribuídos à ligação C-H fora do plano de deformação, e os entorno de 1040 cm - 1 ao plano de deformação. Já os picos em 990 cm - 1 são característicos da deformação do anel[25].
Os resultados obtidos mostram que com o aumento do tempo de condicionamento as bandas referentes à ligação C-H fora e no plano de deformação e à deformação do anel são evidenciadas, sugerindo que há uma interação dos íons fluoreto com o anel pirrólico. Através desses estudos comprova-se que não há necessidade de condicionamento do eletrodo modificado com filme de PPy-F - e que tempos longos de exposição podem degradar a membrana e comprometer o desempenho do eletrodo. Nesse aspecto cabe salientar que o uso de um substrato base de baixo custo, como um compósito de carbono, permite que esses dispositivos, se necessário, sejam utilizados como eletrodos descartáveis.
Estudos de repetibilidade e reprodutibilidade do processo de construção do filme
O estudo de repetibilidade consistiu em modificar um eletrodo compósito com o filme de PPy-F - e realizar quatro curvas analíticas consecutivas para o mesmo eletrodo. Este estudo teve como objetivo avaliar a variação da sensibilidade para um mesmo eletrodo durante as sucessivas análises.
Os resultados apresentaram um desvio de 10,8% nos valores de sensibilidade entre as replicatas, havendo uma queda brusca a partir da segunda medida e decrescendo nas medidas subsequentes, porém tendendo à estabilização. Esse decréscimo de sensibilidade pode ser atribuído a possível reação entre a rede polimérica e os íons fluoreto durante as medidas, o que gera uma desativação do filme, reduzindo a sensibilidade do eletrodo. Tendo em vista isso, uma alternativa pode ser a utilização deste dispositivo como descartável, uma vez que sua construção e modificação são simples e de baixo custo.
A fim de verificar a viabilidade da utilização deste sensor como um dispositivo descartável, um estudo de reprodutibilidade foi realizado, no qual cinco diferentes eletrodos foram construídos e submetidos à modificação através do crescimento do filme de PPy-F - .
Os valores de sensibilidade obtidos para os diferentes eletrodos modificados apresentaram concordância entre eles, com um desvio padrão relativo da ordem de 0,67%, o que confere uma boa reprodutibilidade da construção e modificação do eletrodo proposto, viabilizando seu uso de forma descartável.
Curva analítica e determinação de íons fluoreto em amostras comerciais
Depois de investigados os parâmetros envolvidos na etapa de crescimento do filme e de leitura de potencial, foi construída uma curva analítica para diferentes concentrações de íons fluoreto. As condições utilizadas para a preparação do eletrodo estão, apresentadas na Tabela 1 e a curva analítica na Figura 5.
Através da curva analítica obtida pode-se observar um intervalo de resposta linear para valores de concentração variando entre 1,00 × 10 - 5 e 1,08 × 10 - 2 mol L - 1 de íons fluoreto segundo a equação: E (mV) = 18,95 + 40,36 pF (R = 0,995, n = 7). As determinações das diferentes concentrações de fluoreto se mostram concordantes e representativas, uma vez que a curva apresenta uma boa linearidade. Quanto à sensibilidade do eletrodo, foi observada uma melhora significativa no valor da inclinação se comparado a análises realizadas sem a otimização dos parâmetros de modificação do eletrodo.
O dispositivo proposto foi aplicado na determinação de íons fluoreto em uma amostra de enxaguante bucal e os resultados comparados com o valor rotulado pelo fabricante. Foi utilizado o método da adição padrão a partir de adições sucessivas de íons fluoreto (solução padrão) em diferentes concentrações à matriz da amostra diluída (razão1:10). Os resultados obtidos nestas determinações demonstraram que o procedimento proposto possui boa precisão sendo encontrados valores em concordância com os dados rotulados para a um nível de confiança de 95% (tcalc = 2,30 e tcrítico = 6,31).
Conclusões
A preparação de um eletrodo íon-seletivo baseada em filmes de polipirrol dopado com íons fluoreto se mostrou viável e com resultados adequados. O procedimento galvanostático utilizado na construção é simples e a resposta potenciométrica fortemente dependente dos parâmetros: densidade de corrente e carga elétrica. Embora tenha sido verificada uma interação entre o analito e o filme polimérico para longos períodos de uso, o eletrodo compósito empregado como substrato base permite a construção de sensores de baixo custo que podem ser utilizados como dispositivos descartáveis, se necessário. A determinação de íons fluoreto apresentou resultados satisfatórios em termos de sensibilidade e seletividade, sendo o eletrodo aplicado na determinação do analito em amostra de enxaguante bucal sem nenhum tipo de tratamento da amostra.
Agradecimentos
Os autores agradecem a CAPES, CNPq e Fundação Araucária pelo incentivo concedido na forma de recursos financeiros para projetos e bolsas.
Enviado: Set. 4, 2013
Reenviado: Mar. 14, 2014
Aceito: Abr. 6, 2014
- 1.Lowinsihn, D. & Bertotti, M. - Quím. Nova, 29, p.1818 (2006).
- 2.Bühlmann, P.; Pretsch, E. & Bakker, E. - Chem. Rev., 98, p.1593 (1998). PMid:11848943. http://dx.doi.org/10.1021/cr970113+
- 3.Torres, K. Y. C.; Calvo-Marzal, P.; Kubota, L. T. & Bakker, E. - Quím. Nova, 29, p.1094 (2006). http://dx.doi.org/10.1590/S0100-40422006000500033
- 4.Arantes, C.; Rocco, M. L. M.; Cruz, A. G. B. & Rocco, A. M. - Quím. Nova, 31, p.61 (2008). http://dx.doi.org/10.1590/S0100-40422008000100013
- 5.Rover Júnior, L.; Oliveira Neto, G. & Kubota, L. T. - Quím. Nova, 20, p.519 (1997). http://dx.doi.org/10.1590/S0100-40421997000500012
- 6.Bendikov, T. A. & Harmon, T. C. J. - Chem. Educ., 82, p.439 (2005). http://dx.doi.org/10.1021/ed082p439
- 7.Dong, S.; Sun, Z. & Lu, Z. - Analyst, 113, p.1525 (1988). http://dx.doi.org/10.1039/an9881301525
- 8.Lu, Z.; Sun, Z. & Dong, S. - Electroanal., 1, p.271 (1989). http://dx.doi.org/10.1002/elan.1140010313
- 9.Bindewald, E. H.; Bergamini, M. F. & Marcolino Júnior, L. H. - Electroanal., 25, p.1535 (2013). http://dx.doi.org/10.1002/elan.201300098
- 10.Álvarez-Romero, G. A.; Lozada-Ascencio, S. M.; Rodríguez-Ávila, J. A.; Galán-Vidal, C. A. & Páez-Hernández, M. E. - Food Chem., 120, p.1250 (2010). http://dx.doi.org/10.1016/j.foodchem.2009.11.072
- 11.Sharifiriad, M.; Omrani, A.; Rostami, A. A. & Khoshroo, M. - J. Electroanal. Chem., 645, p.149 (2010). http://dx.doi.org/10.1016/j.jelechem.2010.05.005
- 12.Adeloju, S. & Sohail, M. - Biosens. Bioelectron., 26, p.4270 (2011). PMid:21592768. http://dx.doi.org/10.1016/j.bios.2011.04.002
- 13.Oliveira, P. R.; Oliveira, M. M.; Zarbin, A. J. G.; Marcolino Junior, L. H. & Bergamini, M. F. - Sensor. Actuat. B, 171-172, p.795 (2012). http://dx.doi.org/10.1016/j.snb.2012.05.073
- 14.Souza, M. D. F. B. - Quím. Nova, 20, p.191 (1997). http://dx.doi.org/10.1590/S0100-40421997000200011
- 15.Stradiotto, N. R.; Yamanaka, H. & Zanoni. - J. Braz. Chem. Soc., 14, p.159 (2003). http://dx.doi.org/10.1590/S0103-50532003000200003
- 16.Cate, J. M. & Featherstone, J. D. B. - Crit Rev Oral Biol Med., 2, p.283 (1991). PMid:1892991.
- 17.Castioni, N. V.; Baehni, P. C. & Gurny, R. - Eur. J. Pharm. Biopharm., 45, p.101 (1998). http://dx.doi.org/10.1016/S0939-6411(97)00083-0
- 18.Ingram, G. S.; Agalamanyi, E. A. & Higham, S. M. - J. Dent., 33, p.187 (2005). PMid:15725519. http://dx.doi.org/10.1016/j.jdent.2004.10.004
- 19.Browne, D.; Whelton, H. & O'Mullane. - J. Dent., 33, p.177 (2005). PMid:15725518. http://dx.doi.org/10.1016/j.jdent.2004.10.003
- 20.Harrison, P. T. C. - J. Fluorine Chem., 126, p.1448 (2005). http://dx.doi.org/10.1016/j.jfluchem.2005.09.009
- 21.Whitford, G. M. - J. Dent. Res., 69, p.539 (1990).
- 22.DePaoli, M. A.; Peres, R. C. D.; Panero, S. & Scrosati, B. - Electrochim. Acta, 37, p.1173 (1992).
- 23.Harris, D. C. - "Quantitative Chemical Analysis", W. H. Freeman and Company, New York (2010).
- 24.Maksymiuk, K. - Electroanal., 18, p.1537 (2006). http://dx.doi.org/10.1002/elan.200603573
- 25.Chen, F.; Shi, G.; Fu, M.; Qu, L. & Hong, X. - Synt. Met., 132, p.125 (2003). http://dx.doi.org/10.1016/S0379-6779(02)00197-2
Datas de Publicação
-
Publicação nesta coleção
10 Set 2014 -
Data do Fascículo
Ago 2014
Histórico
-
Recebido
04 Set 2013 -
Aceito
06 Abr 2014 -
Revisado
14 Mar 2014