Resumos
OBJETIVO: Embora de grande importância para os que lidam com o perioperatório do transplante de fígado, seu comportamento hemodinâmico ainda não encontra uma descrição consensual na literatura. O objetivo deste estudo é descrever o comportamento hemodinâmico durante as primeiras 48 horas do transplante de fígado. MÉTODOS: Foram estudados prospectiva e consecutivamente 61 pacientes, sendo 50 homens, com idade média de 49 anos (18-70 anos). As medidas hemodinâmicas foram realizadas no início da cirurgia, 30 minutos após a revascularização do enxerto e, a partir de então, a cada 6 horas até 48 horas após a revascularização. O peso foi obtido no momento da internação e no primeiro e segundo dias de pós-operatório às 6h. RESULTADOS: A pressão arterial média começa a apresentar aumento nas primeiras horas de pós-operatório com valores significativamente mais elevados 24 horas após a revascularização. O índice cardíaco apresenta um aumento significativo logo após a revascularização, voltando progressivamente aos valores pré-operatórios. Da mesma forma, a resistência vascular sistêmica apresenta uma queda significativa imediatamente após a revascularização, voltando a atingir valores próximos aos pré-transplante após 24 horas da revascularização. A pressão de capilar pulmonar começa a apresentar valores significativamente mais elevados já com 6 horas após a revascularização e o peso aumenta significativamente já no primeiro pós-operatório. CONCLUSÃO: Nas primeiras horas após o transplante de fígado, há uma intensa variação hemodinâmica, com aumento progressivo das pressões arterial sistêmica e de capilar pulmonar, além de variações significativas, porém transitórias, do índice cardíaco e da resistência vascular sistêmica, exigindo uma vigilância contínua para minimizar suas conseqüências.
Transplante de fígado; Fenômenos hemodinâmicos; Cuidados intensivos
OBJECTIVES: Although of great importance for all those involved in liver transplant, in literature there is no consensual description on its hemodynamic behavior. This study intends to describe the hemodynamic behavior during and in the first 48h after liver transplant . METHODS: A prospective and consecutive study of 61 patients was carried out; 50 were male, with average age of 49 years (18-70 years). Hemodynamic measurements were followed up at the beginning of the surgery, 30 minutes after revascularization of the graft and afterwards 6 hours up to 48h post revascularization. Weight was obtained upon hospital admission and at 6 o'clock on the first and second postoperative days. RESULTS: mean arterial pressure starts to increase soon after surgery, reaching significantly higher values 24h after revascularization. Cardiac index increases significantly soon after revascularization, progressively returning to preoperative values. Likewise the systemic vascular resistance falls significantly immediately after revascularization, reaching values similar to the preoperative ones 24h after revascularization. The pulmonary wedge pressure rises significantly 6 hours after revascularization and there is a significant weight increase at the end of the first postoperative day. CONCLUSIONS: During the first hours after liver transplant an intense hemodynamic variation is noted with progressive increase in the systemic arterial pressures and in the pulmonary wedge pressure. Furthermore, significant although transitory variations of the cardiac index and of the systemic vascular resistance demand continuous surveillance to minimize their consequences.
Liver transplantation; Hemodynamic phenomena; Intensive care
ARTIGOS ORIGINAL
A instabilidade hemodinâmica no transplante de fígado: um desafio para o intensivista
Hemodynamic instability in liver transplant: a challenge for the intensivist
Dirk Schreen* * Correspondência: Rua Mucuripe, 103 Alphaville Fortaleza, Cep: 61760-000, Eusébio, CE, e-mail: dirksch@uol.com.br ; Bruno Caramelli
RESUMO
OBJETIVO: Embora de grande importância para os que lidam com o perioperatório do transplante de fígado, seu comportamento hemodinâmico ainda não encontra uma descrição consensual na literatura. O objetivo deste estudo é descrever o comportamento hemodinâmico durante as primeiras 48 horas do transplante de fígado.
MÉTODOS: Foram estudados prospectiva e consecutivamente 61 pacientes, sendo 50 homens, com idade média de 49 anos (18-70 anos). As medidas hemodinâmicas foram realizadas no início da cirurgia, 30 minutos após a revascularização do enxerto e, a partir de então, a cada 6 horas até 48 horas após a revascularização. O peso foi obtido no momento da internação e no primeiro e segundo dias de pós-operatório às 6h.
RESULTADOS: A pressão arterial média começa a apresentar aumento nas primeiras horas de pós-operatório com valores significativamente mais elevados 24 horas após a revascularização. O índice cardíaco apresenta um aumento significativo logo após a revascularização, voltando progressivamente aos valores pré-operatórios. Da mesma forma, a resistência vascular sistêmica apresenta uma queda significativa imediatamente após a revascularização, voltando a atingir valores próximos aos pré-transplante após 24 horas da revascularização. A pressão de capilar pulmonar começa a apresentar valores significativamente mais elevados já com 6 horas após a revascularização e o peso aumenta significativamente já no primeiro pós-operatório.
CONCLUSÃO: Nas primeiras horas após o transplante de fígado, há uma intensa variação hemodinâmica, com aumento progressivo das pressões arterial sistêmica e de capilar pulmonar, além de variações significativas, porém transitórias, do índice cardíaco e da resistência vascular sistêmica, exigindo uma vigilância contínua para minimizar suas conseqüências.
Unitermos: Transplante de fígado. Fenômenos hemodinâmicos. Cuidados intensivos.
SUMMARY
OBJECTIVES: Although of great importance for all those involved in liver transplant, in literature there is no consensual description on its hemodynamic behavior. This study intends to describe the hemodynamic behavior during and in the first 48h after liver transplant .
METHODS: A prospective and consecutive study of 61 patients was carried out; 50 were male, with average age of 49 years (18-70 years). Hemodynamic measurements were followed up at the beginning of the surgery, 30 minutes after revascularization of the graft and afterwards 6 hours up to 48h post revascularization. Weight was obtained upon hospital admission and at 6 o'clock on the first and second postoperative days.
RESULTS: mean arterial pressure starts to increase soon after surgery, reaching significantly higher values 24h after revascularization. Cardiac index increases significantly soon after revascularization, progressively returning to preoperative values. Likewise the systemic vascular resistance falls significantly immediately after revascularization, reaching values similar to the preoperative ones 24h after revascularization. The pulmonary wedge pressure rises significantly 6 hours after revascularization and there is a significant weight increase at the end of the first postoperative day.
CONCLUSIONS: During the first hours after liver transplant an intense hemodynamic variation is noted with progressive increase in the systemic arterial pressures and in the pulmonary wedge pressure. Furthermore, significant although transitory variations of the cardiac index and of the systemic vascular resistance demand continuous surveillance to minimize their consequences.
Key words: Liver transplantation. Hemodynamic phenomena. Intensive care.
INTRODUÇÃO
O transplante de fígado se consolidou, nas últimas décadas, como o único tratamento eficaz para a doença hepática terminal, seja ela crônica, subaguda ou aguda. Isto se deveu não só pelo fato de as técnicas relativas a esse transplante e a imunossupressão terem se aprimorado mas, também, porque, nesse meio tempo, não se desenvolveu nenhuma tecnologia ou terapia que pudesse substituir as múltiplas funções exercidas pelo fígado. É a multiplicidade dessas funções que torna as doenças que acometem o fígado tão complexas, com repercussões hemodinâmicas importantes1-5. São também essas funções que tornam o transplante e o perioperatório desses pacientes extremamente conturbado. Basta lembrar o tão temido, pelos anestesistas, período pós-reperfusão do enxerto. Ou, ainda, a instabilidade hemodinâmica do pós-operatório, desta vez temida pelos intensivistas, e a congestão pulmonar descrita em até 40% dos casos6-8. Outra alteração freqüentemente observada é a hipertensão arterial, muitas vezes de difícil controle9,10.
Existem poucos trabalhos na literatura que descrevem adequadamente o comportamento hemodinâmico do perioperatório do transplante de fígado; alguns, até mesmo, com resultados conflitantes entre si. O conhecimento adequado desse comportamento torna-se, no entanto, fundamental para todos os que estão envolvidos no cuidado desses pacientes, para que as condutas tomadas sejam as mais adequadas e embasadas do ponto de vista científico.
O objetivo deste estudo é descrever as alterações hemodinâmicas no período entre o pré-operatório imediato até 48 horas após a revascularização do enxerto, em pacientes submetidos a transplante de fígado.
MÉTODOS
Pacientes
Foram estudados, prospectiva e consecutivamente, 61 pacientes, (50 homens e 11 mulheres), com idade média de 49 anos (18 a 70 anos), transplantados no período entre 5 de setembro de 1998 e 14 de agosto de 2000. Não foram incluídos pacientes com menos de 18 anos, aqueles transplantados por hepatite fulminante ou retransplantados, receptores de transplante intervivos, bem como pacientes que já tivessem doença cardiológica ou pulmonar grave prévia. Foram excluídos pacientes que evoluíram a óbito durante a cirurgia ou nas 24 primeiras horas após o transplante (cinco pacientes). Adicionalmente, dez pacientes transplantados por PAF (polineuropatia amilodótica familiar) e seis pacientes com medidas hemodinâmicas insuficientes (menos que 60% das medidas preconizadas) também não foram considerados para este estudo.
O estudo foi aprovado pelo comitê de ética da instituição, e estava de acordo com a Declaração de Helsinki. Consentimento informado foi obtido de cada paciente previamente à inclusão no estudo.
Trinta e cinco pacientes foram operados por hepatite crônica viral, sendo 30 por vírus C, três por vírus B e dois por associação dos dois vírus. Em 13 pacientes a indicação do transplante foi por doença alcoólica. As demais indicações do transplante foram: colangite esclerosante primária em dois, cirrose biliar primária em dois, cirrose criptogênica em três, doença ductopênica em dois, hepatite autoimune em dois e doença policística em dois.
A caracterização dos pacientes estudados, conforme a classificação de Child-Pugh, está demonstrada na Figura 1. Quarenta e quatro pacientes foram operados pelo método de piggyback e 17 pelo método convencional.
Anestesia e imunossupressão
Todos os pacientes foram anestesiados com isofluorane e fentanil. A administração de hemoderivados foi realizada a critério da equipe, com o fim de manter o hematócrito sérico acima de 30%, tempo de protrombina (INR) < 2 e plaquetas acima de 30.000/mm3. A administração de cristalóides ou colóides seguiu os parâmetros habituais de ressuscitação, procurando-se manter pressão arterial média acima de 60 mmHg, diurese acima de 0,5 ml/Kg/h e pressão venosa central e/ou pressão de capilar pulmonar acima de 10 mmHg.
Todos os pacientes receberam infusão contínua de dopamina em dose de ~2,5 pg/Kg/min, que foi mantida até o fim do protocolo na quase totalidade dos pacientes.
O tratamento imunossupressor padrão consistiu em 1g de metilprednisolona endovenosa concomitante à revascularização do enxerto, com doses decrescentes de corticóide, variáveis conforme o inibidor de calcineurina utilizado. Pacientes submetidos a imunossupressão com ciclosporina, receberam 200 mg de metilprednisolona no primeiro, 160 mg no segundo e 120 mg no terceiro pós-operatórios, divididos em quatro doses. Concomitantemente, receberam 10 mg de ciclosporina/Kg/dia em duas doses associadas a azatioprina 1 a 1,5 mg por Kg a partir do primeiro pós-operatório. A partir do segundo pós-operatório, as doses de ciclosporina foram reajustadas a fim de manter o nível sérico entre 300 e 350 mg/ml. Pacientes submetidos a imunossupressão com FK506 receberam 100 mg de metilprednisolona divididos em quatro doses no primeiro, 80 mg no segundo e 60 mg no terceiro pós-operatórios. FK506 foi administrado na dose inicial de 0,1mg/Kg/dia em duas doses a partir do primeiro pós-operatório; as doses foram reajustadas a partir do segundo pós-operatório, a fim de manter níveis séricos de 8 a 15 ng/ml.
Medidas hemodinâmicas
Após a indução anestésica e intubação orotraqueal, os pacientes foram monitorados por meio de cateter de artéria pulmonar (Swan-Ganz - Baxter Healthcare, Deerfield, IL) e cateterização de artéria radial. Registrou-se assim, por medida direta, a pressão arterial média (PAM), a pressão média de artéria pulmonar (PAPM), a pressão de átrio direito (PAD) e a pressão de capilar pulmonar (PCP). O débito cardíaco (DC) foi obtido utilizando-se a técnica de termodiluição e o índice cardíaco (IC), dividindo-se o débito cardíaco pela superfície corpórea. A monitorização foi realizada por monitor multicanal (Hewlett-Packard modelos M1106B ou Viridia, Hewlett-Packard, Waltham, MA).
Para se calcular a resistência vascular sistêmica (RVS) e pulmonar (RVP), foram utilizadas as seguintes fórmulas:
RVS = PAM PAD x 80/DC e
RVP = PAPM PCP x 80/DC
Os parâmetros hemodinâmicos foram obtidos no início da cirurgia, cerca de 30 minutos após a revascularização e, a partir de então, a intervalos de 6 horas até se completarem 48 horas pós-revascularização.
O peso foi obtido em cama-balança Hill-Rom (Hillenbrand Industries, Inc., Batesville, IN), no momento da internação do paciente e no primeiro e segundo dias de pós-operatório às 6h.
Análise estatística
Os valores pré-operatórios de cada parâmetro estudado (IC, PAM, PCP, PAPM, RVS e RVP) foram comparados com os valores 48 horas após a revascularização do enxerto por meio do teste t pareado, considerando-se um nível de significância de 5%. Além disso, cada valor obtido ao longo das medidas seriadas foi comparado com o valor pré-operatório, utilizando-se o mesmo teste e nível de significância. O peso, refletindo o ganho volêmico total, foi comparado entre o pré-operatório e o segundo dia de pós-operatório, também utilizando-se o teste t pareado (a = 0.05).
A seguir, a análise foi repetida considerando-se a influência das covariáveis etiologia e método operatório sobre o comportamento hemodinâmico dos pacientes.
RESULTADOS
Os dados comparativos entre o pré e o pós-transplante estão expressos na Tabela 1. O comportamento de cada parâmetro hemodinâmico está descrito a seguir.
Pressão arterial média (PAM): a pressão arterial média, com valores iniciais de 79 mmHg, começou a apresentar aumento progressivo a partir das primeiras horas após o transplante, porém só atingiu e manteve valores significativamente mais elevados a partir de 24 horas pós-reperfusão, como demonstrado no Gráfico 1. A partir das 24 horas, o aumento da PAM ainda se manteve até ao fim das 48 horas do acompanhamento, atingindo 95 mmHg.
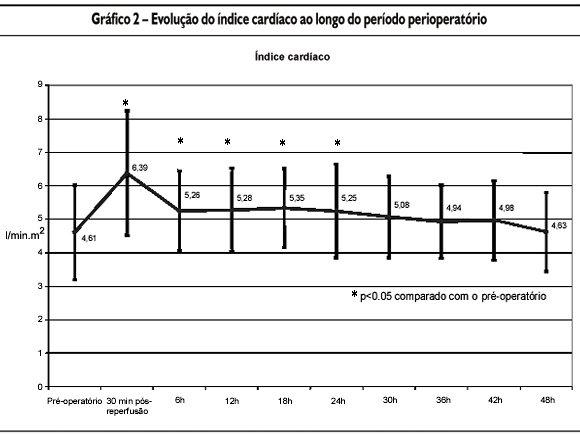
Índice cardíaco (IC): o IC no início da cirurgia era de 4,4 ± 1,5 l/min/m2 e, ao final das 48 horas, 4,6 ± 1,2 l/min/m2, não havendo diferença estatisticamente significante (p=0,458). Imediatamente após a reperfusão, no entanto, e até as primeiras 24 horas após o procedimento, o índice cardíaco se elevou significa-tivamente, decrescendo progressivamente até atingir valores próximos aos do pré-operatório. Seu comportamento está demonstrado no Gráfico 2.
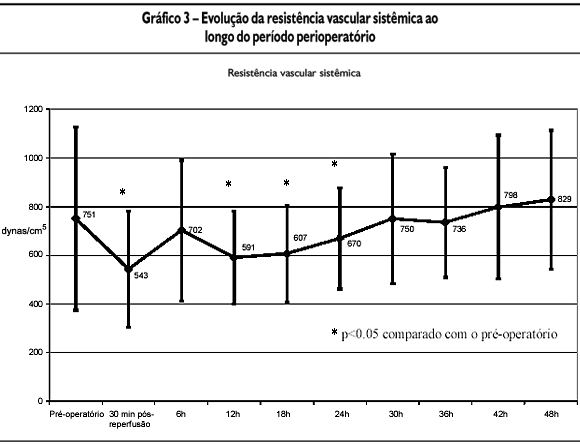
Resistência vascular sistêmica (RVS): a resistência vascular sistêmica apresentou uma redução significativa durante as primeiras 24 horas do pós-transplante, com aumento progressivo durante esse período, voltando a atingir valores próximos aos do pré-transplante após esse período. Os valores de resistência vascular sistêmica mais baixos encontrados foram 30 minutos após a reperfusão do enxerto. O Gráfico 3 mostra o comportamento da RVS.
Pressão de artéria pulmonar média (PAPM): a pressão arterial pulmonar começou a se elevar significativamente imediatamente após a reperfusão (p<0,05), passando a apresentar um comportamento estável após 12 horas da reperfusão.
Resistência vascular pulmonar (RVP): a resistência vascular pulmonar apresentou um incremento progressivo após o transplante, porém somente passou a apresentar diferença significativa 48 horas após a reperfusão do enxerto (p=0,047).
Pressão de capilar pulmonar (PCP): no gráfico 4, está demonstrado o comportamento da pressão de capilar pulmonar. No início da cirurgia, seu valor era de 12 ± 4 mmHg e, ao final do estudo, 18 ± 4 mmHg (p<0,001), sendo que ela passou a ser significativamente diferente dos valores pré-operatórios já com 6 horas da fase de reperfusão.
O peso dos pacientes teve um incremento médio de 3 Kg. Inferindo-se com isso um ganho volêmico, esses pacientes tiveram um balanço hídrico positivo de aproximadamente 3 litros. Os pacientes receberam, em média, 12 concentrados de hemácias e 30 plasmas no perioperatório, significando um aporte médio de 8 litros de hemoderivados.
A análise da influência das covariáveis no comportamento hemodinâmico após o transplante demonstrou não haver influência das etiologias da doença hepática. Por outro lado, pacientes operados pelo método de piggyback apresentaram pressão de capilar pulmonar em média 1,5 mmHg mais elevada que os operados pelo método convencional (p < 0,008).
DISCUSSÃO
No pré-operatório do transplante, existe a condição hemodinâmica característica do hepatopata: débito cardíaco aumentado, resistência vascular sistêmica reduzida, taquicardia, pressão arterial normal ou tendendo a baixa e volume sangüíneo aumentado. Tal padrão já vem sendo descrito desde a década de 50, e é observado também no nosso estudo1-3. A grande controvérsia no que se refere à hemodinâmica no pós-transplante de fígado é se existe a persistência do estado hemodinâmico característico do pré-transplante nesses pacientes e em quanto tempo ele se normalizaria.
Alguns autores defendem uma rápida elevação da resistência vascular sistêmica e redução do índice cardíaco, iniciando-se já no pós-operatório imediato11-14,18-20. Tal elevação na resistência vascular sistêmica e normalização do estado hiperdinâmico não é, porém, encontrada por outros autores. Segundo estes, há persistência do padrão hiperdinâmico até meses ou anos após o transplante15-17 .
Nosso estudo demonstrou que existe um aumento significativo da pressão arterial quando se comparam os níveis prévios ao transplante com 48 horas após o procedimento. Esse aumento na pressão arterial se manifesta mais intensamente com 24 horas de transplante. Tal aumento, no entanto, não pode ser creditado somente ao aumento da resistência vascular sistêmica nem ao aumento no débito cardíaco. O aumento na resistência vascular sistêmica, observado por diversos autores18-20, não parece ser, isoladamente, o fator causal da elevação pressórica em nosso e em outros estudos. Glauser, por exemplo, demonstra redução significativa do índice cardíaco e aumento na resistência vascular sistêmica somente após 48 horas do transplante. A pressão arterial, no entanto, segundo este autor, começa a se elevar precocemente19. Mesmo se questionarmos o fato de, no início do estudo, os pacientes se encontrarem sob efeito de sedação e no final não, não se justifica o aumento da pressão arterial, pois esperaríamos um aumento mais significativo na resistência vascular sistêmica. Fatores como ansiedade ou dor também não podem ser diretamente implicados, pois de igual modo esperaríamos aumento na liberação de catecolaminas endógenas, o que resultaria em aumento na resistência periférica.
Foi demonstrado, em nosso estudo, aumento significativo e precoce na pressão de capilar pulmonar e no peso no período pós-transplante. A interação entre um aumento, mesmo que não significativo, da resistência vascular sistêmica associado a aumento na volemia poderia explicar o aumento precoce da pressão arterial no pós-transplante. Outros fatores, como a nefrotoxicidade dos inibidores da calcineurina e o uso de corticóides para a imunossupressão também poderiam estar implicados9,21.
Da mesma forma, o aumento da pressão de artéria pulmonar também poderia ser explicado por uma sobrecarga volêmica. O significado clínico e a fisiopatologia do aumento da resistência vascular pulmonar necessitam de explicação adicional, eventualmente decorrente do edema intersticial conseqüente à congestão pulmonar ou vasoconstricção provocada por hipóxia regional.
O resultado deste estudo sugere que, apesar de grande parte dos hemoderivados e do volume administrado no perioperatório passar para o interstício sob forma de edema, parte desse volume administrado aumenta significativamente a volemia desses pacientes, podendo ser um dos responsáveis pelo aumento da pressão no período precoce do pós-transplante. A administração de corticóides em altas doses e dos inibidores da calcineurina, com seus efeitos nefrotóxicos, também poderia contribuir para esse fenômeno. Além disso há, provavelmente, alterações na permeabilidade vascular e no poder coloidosmótico do plasma após o transplante, pois, mesmo após a estabilização volêmica desses pacientes, observa-se muitas vezes um incremento adicional da pressão de capilar pulmonar, levando à necessidade freqüente de diuréticos em pacientes que há pouco necessitavam de volume.
Por fim, fica evidenciado um período logo após a reperfusão do enxerto em que há uma redução significativa da resistência vascular sistêmica e aumento no índice cardíaco que tendem a se normalizar rapidamente no pós-transplante.
CONCLUSÃO
Após o transplante de fígado, há um progressivo aumento da pressão arterial sistêmica e pulmonar, bem como da pressão de capilar pulmonar. Esse aumento não se acompanha, necessariamente, de alterações significativas da resistência vascular sistêmica e do índice cardíaco, embora alterações não significativas nesses últimos possam levar a aumentos significativos da pressão arterial.
Conflito de interesse: não há.
Artigo recebido: 04/11/04
Aceito para publicação: 28/06/05
Trabalho realizado no Hospital das Clínicas da Faculdade de Medicina da Universidade de São Paulo, São Paulo, SP.
- 1. Kowalski HJ, Abelmann WH. The cardiac output at rest in Laennec's cirrhosis. J Clin Invest 1953;32:1025-33.
- 2. Murray JF, Dawson AM, Sherlock S. Circulatory changes in chronic liver disease. Am J Med 1958;24:358-67.
- 3. Lee SS. Cardiac abnormalities in liver cirrhosis. West J Med 1989;151:530-53.
- 4. Kontos HÁ, Shapiro W, Mauck HP, Patterson JL. General and regional circulatory alterations in cirrhosis of the liver. Am J Med 1964;37:526-35.
- 5. Schlant RC. Cardiovascular effects of hepatic cirrhosis. In: Hurst JW, editor. Update III: the heart. New York: McGraw-Hill; 1980. p.129-38.
- 6. Golfieri R, Giampalma E, Morselli Labate AM, D'Arienzo P, Jovine E, et al. Pulmonary complications of liver transplantation: radiological appearance and statistical evaluation of risk factors in 300 cases. Eur Radiol 2000; 10:1169-83.
- 7. Snowden CP, Hughes T, Rose J, Roberts DR. Pulmonary edema in patients after liver transplantation. Liver Transpl 2000;6:466-70.
- 8. Singh N, Gayowski T, Wagener MM, Marino IR. Pulmonary infiltrates in liver transplant recipients in the intensive care unit. Transplantation 1999;67:1138-44.
- 9. Scheiner PA, Magliocca JF, Bodian CA, Kim-Schluger L, Altaca G, Guarrera JV, et al. Long-term medical complications in patients surviving > or = 5 years after liver transplant. Transplantation 2000;69:781-9.
- 10. Textor, SC; Canzanello, VJ; Taler SJ; Schwartz, L; Augustine, J. Hypertension after liver transplantation. Liver Transplant Surg 1995;1(5 Suppl 1):20-8.
- 11. Piscaglia F, Zironi G, Gaiani S, Mazziotti A, Cavallari A, Gramatieri L, et al. Systemic and splanchnic hemodynamic changes after liver transplantation for cirrhosis: a long-term prospective study. Hepatology 1999;30:58-64.
- 12. Navasa M, Feu F, Garcia-Pagan JC, Jimenez W, Llach J, Rimola A, et al. Hemodynamic and humoral changes after liver transplantation in patients with cirrhosis. Hepatology 1993;17:355-60.
- 13. Alvarez D, Gerona S, Waisburg Z, Ciardullo M, De Santibanes E, Mastai R. Splanchnic hyperemia after liver transplantation in patients with end-stage liver disease. Liver Transpl Surg 1998;4:300-3.
- 14. Gadano A, Hadengue A, Widmann JJ, Vachiery F, Moreau R, Yang S, et al. Hemodynamic after orthotopic liver transplantation: study of associated factors and long-term effects. Hepatology 1995;22:458-65.
- 15. Henderson JM, MacKay GJ, Hooks M, Chezmar JL, Galloway JR, Dodson TF, et al. High cardiac output of advanced liver disease persists after orthotopic liver transplantation. Hepatology 1992;15:258-62.
- 16. Henderson JM, Gilmore GT, Mackay GJ, Galloway JR, Dodson TF, Kutner MH. Hemodynamics during liver transplantation: the interactions between cardiac output and portal venous and hepatic arterial flows. Hepatology, 1992;16:715-8.
- 17. Hadengue A, Lebrec D, Moreaus R, Sogni P, Durand F, Gaudin C, et al. Persistence of systemic and splanhnic hyperkinetic circulation in liver transplant patients. Hepatology 1993;17:175-8.
- 18. Plevak DJ. Hyperdinamic circulatory state after liver transplantation. Transplant Proc 1993;25:1839.
- 19. Glauser FL. Systemic hemodynamic and cardiac function changes in patients undergoing orthotopic liver transplantation. Chest 1990;98:1210-15.
- 20. Vera SR, Williams JW, Peters TG, Britt LG. Hemodynamic study following liver transplanation. Transplant Proc 1989;21:2302-4.
- 21. De Mattos AM, Olyaei AJ, Bennett WM. Nephrotoxicity of immunosuppressive drugs: long-term consequences and challenges for the future [editorial]. Am J Kidney Dis 2000;35:333-46.
Datas de Publicação
-
Publicação nesta coleção
01 Jun 2006 -
Data do Fascículo
Abr 2006
Histórico
-
Aceito
28 Jun 2005 -
Recebido
04 Nov 2004