Resumos
- O estudo da cicatrização da pele envolve uma enorme gama de eventos e de situações especiais. Exige conhecimentos básicos de anatomia, histologia, bioquímica, imunologia, farmacologia, entre outras ciências. O artigo faz revisão dos conceitos de cicatrização, em seus diversos aspectos, e ressalta a importância da atuação multidisciplinar na abordagem das feridas, bem como a percepção do paciente como um todo. São abordados os aspectos econômicos que representam as feridas agudas e crônicas. Apresenta ainda os recursos que podem auxiliar o processo de cicatrização, bem como os diversos tipos de curativos disponíveis.
Cicatrização de feridas; mecanismos defensivos e curativos
The study of cicatrization of the skin involves an enormous gamut of events and special situations. It requires a basic knowledge of anatomy, histology, biochemistry, immunology, pharmacology and many other sciences. This article offers a revision of the concepts of cicatrization, in its diverse aspects, and underscores the importance of a team with practitioners from various fields for the wound management as well as a global perception of the patient. The economic aspects of acute and chronic wounds are considered. Furthermore, the resources which can be used to aid the healing process and the various types of curatives available are also presented.
Wound healing; defensive and curative mechanisms
EDUCAÇÃO MÉDICA CONTINUADA
Cicatrização: conceitos atuais e recursos auxiliares - Parte I* * Trabalho realizado no Serviço de Dermatologia do Hospital Universitário de Taubaté, na disciplina de Dermatologia do Departamento de Medicina da Universidade de Taubaté - Unitau, em São Paulo
Cicatrization: current concepts and auxiliary resources - Part I* * Trabalho realizado no Serviço de Dermatologia do Hospital Universitário de Taubaté, na disciplina de Dermatologia do Departamento de Medicina da Universidade de Taubaté - Unitau, em São Paulo
Samuel Henrique MandelbaumI; Érico Pampado Di SantisII; Maria Helena Sant'Ana MandelbaumIII
IProfessor assistente responsável pela disciplina de Dermatologia do Departamento de Medicina da Universidade de Taubaté, em São Paulo; chefe do Serviço de Dermatologia do Hospital Universitário de Taubaté - Fust
IIEspecialista em Dermatologia pela SBD e AMB; preceptor do Serviço de Dermatologia do Hospital Universitário de Taubaté - Fust
IIIEnfermeira formada pela Universidade de São Paulo; especialista em Enfermagem em Dermatologia pela Sociedade Brasileira de Enfermagem em Dermatologia - Sobende; supervisora do Projeto Profae - Fundap / Ministério da Saúde
Endereço para correspondência E ndereço para correspondência Samuel Henrique Mandelbaum Av. 9 de julho, 520 - cjs. 3 e 4 São José dos Campos SP 12243-001 Tel/Fax: (12) 3921-5455 / 3942-8549 E-mail: dr_samuel@directnet.com.br
RESUMO
- O estudo da cicatrização da pele envolve uma enorme gama de eventos e de situações especiais. Exige conhecimentos básicos de anatomia, histologia, bioquímica, imunologia, farmacologia, entre outras ciências. O artigo faz revisão dos conceitos de cicatrização, em seus diversos aspectos, e ressalta a importância da atuação multidisciplinar na abordagem das feridas, bem como a percepção do paciente como um todo. São abordados os aspectos econômicos que representam as feridas agudas e crônicas. Apresenta ainda os recursos que podem auxiliar o processo de cicatrização, bem como os diversos tipos de curativos disponíveis.
Palavras-chave: Cicatrização de feridas; mecanismos defensivos e curativos.
SUMMARY
The study of cicatrization of the skin involves an enormous gamut of events and special situations. It requires a basic knowledge of anatomy, histology, biochemistry, immunology, pharmacology and many other sciences. This article offers a revision of the concepts of cicatrization, in its diverse aspects, and underscores the importance of a team with practitioners from various fields for the wound management as well as a global perception of the patient. The economic aspects of acute and chronic wounds are considered. Furthermore, the resources which can be used to aid the healing process and the various types of curatives available are also presented..
Key-words: Wound healing.; defensive and curative mechanisms.
I - INTRODUÇÃO: O PROCESSO DE CICATRIZAÇÃO
A cicatrização de feridas consiste em uma perfeita e coordenada cascata de eventos celulares e moleculares que interagem para que ocorra a repavimentação e a reconstituição do tecido.1 Tal evento é um processo dinâmico que envolve fenômenos bioquímicos e fisiológicos que se comportem de forma harmoniosa a fim de garantir a restauração tissular.
Como desencadeante da cicatrização, ocorre a perda tecidual, a partir da qual o fisiologismo volta-se completamente para o reparo de um evento danoso ao organismo.
A perda tecidual pode atingir a derme completa ou incompletamente, ou mesmo atingir todo o órgão, chegando ao tecido celular subcutâneo. É daí que vem a definição do tipo de ferida.
Ferida de espessura parcial (derme incompleta): ocorre após muitos procedimentos dermatológicos como a dermoabrasão, o resurfacing por laser ou peelings químicos; pode também ser causada por traumatismos. A reparação faz-se pela reepitelização dos anexos epiteliais ou epitélio derivado da pele adjacente não acometida. Como resultado final tem-se uma cicatriz praticamente imperceptível.
Já as feridas de espessura total (derme completa ou estendida ao tecido celular subcutâneo) necessitam da formação de um novo tecido, o tecido de granulação; a epitelização, base da cicatrização nas feridas de espessura parcial, acontece apenas nas margens da ferida. Nesse caso, a cicatriz é totalmente perceptível e, muitas vezes, pronunciada.2
A cicatrização também depende de vários fatores, locais e gerais, como: localização anatômica, tipo da pele, raça, técnica cirúrgica utilizada.
A cicatrização em uma mesma espécie varia se a ferida ocorre no feto, no recém-nascido ou no indivíduo adulto.3
Classificação dos Processos Biológicos da Cicatrização
Diferentes classificações didáticas são utilizadas para facilitar o entendimento de um processo totalmente dinâmico e com fases tão interdependentes como a cicatrização.
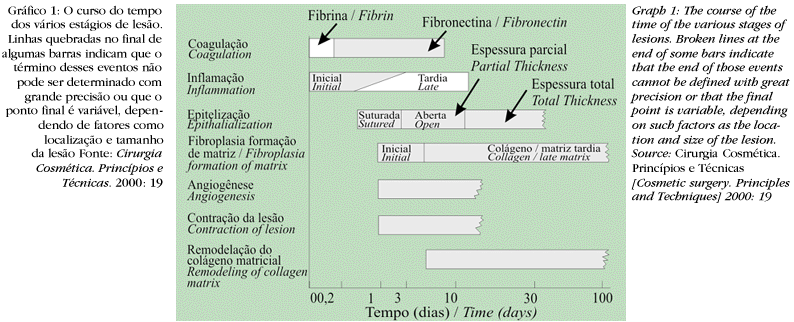
Existem autores que consideram três estágios no processo de cicatrização: inicialmente um estágio inflamatório, seguido por um de proliferação e finalizando com o reparo em um estágio de remodelação.4 Outros autores classificam de uma forma mais completa dividindo o processo em cinco fases principais:
1 - coagulação;
2 - inflamação;
3 - proliferação;
4 - contração da ferida;
5 - remodelação.5
Em um determinado período de tempo as fases coincidem e acontecem simultaneamente, permitindo assim o sucesso da cicatrização (Gráfico 1).
Coagulação
O início é imediato após o surgimento da ferida. Essa fase depende da atividade plaquetária e da cascata de coagulação.6
Ocorre uma complexa liberação de produtos. Substâncias vasoativas, proteínas adesivas, fatores de crescimento e proteases são liberadas e ditam o desencadeamento de outras fases.7
A formação do coágulo serve não apenas para coaptar as bordas das feridas, mas também para cruzar a fibronectina, oferecendo uma matriz provisória, em que os fibroblastos, células endoteliais e queratinócitos possam ingressar na ferida.8,9
Inflamação
Intimamente ligada à fase anterior, a inflamação depende, além de inúmeros mediadores químicos, das células inflamatórias, como os leucócitos polimorfonucleares (PMN), macrófagos e linfócitos.
Os PMN chegam no momento da injúria tissular e ficam por período que varia de três a cinco dias; são eles os responsáveis pela fagocitose das bactérias.
O macrófago é a célula inflamatória mais importante dessa fase.10 Permanece do terceiro ao décimo dia. Fagocita bactérias, desbrida corpos estranhos e direciona o desenvolvimento de tecido de granulação. O uso de laser de baixa energia em pele de ratos favorece a cicatrização. Alta atividade fagocitária dos macrófagos é observada após trauma.11
Os linfócitos aparecem na ferida em aproximadamente uma semana. Seu papel não é bem definido, porém sabe-se que, com suas linfocinas, tem importante influência sobre os macrófagos.
Além das células inflamatórias e dos mediadores químicos, a fase inflamatória conta com o importante papel da fibronectina.12 Sintetizada por uma variedade de células como fibroblastos, queratinócitos e células endoteliais, ela adere, simultaneamente à fibrina, ao colágeno e a outros tipos de células, funcionando assim como cola para consolidar o coágulo de fibrina, as células e os componentes de matriz.13 Além de formar essa base para a matriz extracelular, tem propriedades quimiotáticas e promove a psonização e fagocitose de corpos estranhos e bactérias.
Proliferação
Dividida em três subfases, a proliferação é responsável pelo "fechamento" da lesão propriamente dita.
A primeira das fases da proliferação é a reepitelização. Faz-se a migração de queratinócitos não danificados das bordas da ferida e dos anexos epiteliais, quando a ferida é de espessura parcial, e apenas das margens nas de espessura total. Fatores de crescimento são os prováveis responsáveis pelos aumentos das mitoses e hiperplasia do epitélio.14
Acontecem estudos em várias partes do mundo. Utilização de colágeno e citoquinas são promessas para uma cicatrização mais rápida e eficaz.15
Sabe-se que o plano de movimento dos queratinócitos migrantes é determinado também pelo conteúdo de água no leito da ferida.
Feridas superficiais abertas e ressecadas reepitelizam mais lentamente do que as ocluídas.16,17
A segunda fase da proliferação inclui a fibroplasia e formação da matriz, que é extremamente importante na formação do tecido de granulação (coleção de elementos celulares, incluindo fibroblastos, células inflamatórias e componentes neovasculares e da matriz, como a fibronectina, as glicosaminoglicanas e o colágeno). A formação do tecido de granulação depende do fibroblasto, célula crítica na formação da matriz. Longe de ser apenas produtor de colágeno, o fibroblasto produz elastina, fibronectina, glicosaminoglicana e proteases, estas responsáveis pelo desbridamento e remodelamento fisiológico.18
A última fase da proliferação é a angiogênese, essencial para o suprimento de oxigênio e nutrientes para a cicatrização.
Inicialmente as células endoteliais migram para a área ferida, a seguir ocorre proliferação das células endoteliais, acesso para as células responsáveis pelas próximas fases.
Contração da Ferida
É o movimento centrípeto das bordas da ferida (espessura total). As feridas de espessura parcial não contam com essa fase. Uma ferida de espessura total tem contração mesmo quando há enxertos, que diminuem em 20% o tamanho da ferida.19 Em cicatrizes por segunda intenção a contração pode reduzir 62% da área de superfície do defeito cutâneo.20
Remodelação
Essa é a última das fases; ocorre no colágeno e na matriz; dura meses e é responsável pelo aumento da força de tensão e pela diminuição do tamanho da cicatriz e do eritema. Reformulações dos colágenos, melhoria nos componentes das fibras colágenas, reabsorção de água são eventos que permitem uma conexão que aumenta a força da cicatriz e diminui sua espessura.21
A neovasculatura diminui, e tardiamente a cicatriz é considerada avascular.
Uma cicatrização normal tem aproximadamente 80% da força de tensão da pele normal, não é volumosa e é plana.
Muitas variáveis tanto de ordem geral como de ordem local influenciam esse longo e complexo processo. É fundamental uma completa e minuciosa anamnese, para avaliação de todos os fatores que podem interferir na cicatrização.
Dos fatores gerais, interferem a idade, o estado nutricional do paciente, a existência de doenças de base, como diabetes, alterações cardiocirculatórias e de coagulação, aterosclerose, disfunção renal, quadros infecciosos sistêmicos e uso de drogas sistêmicas.
Dos fatores locais, interferem a técnica cirúrgica, formação de hematomas, infecção, reação de corpo estranho, uso de drogas tópicas, ressecamento durante a cicatrização. Esses fatores devem ser de conhecimento do cirurgião dermatológico e merecem atenção especial. Nas cirurgias dermatológicas, que na maioria das vezes são eletivas, três são os fatores que devem ser destacados:
1- Técnica cirúrgica: respeitando unidades cosméticas e linhas de força; manuseio delicado evitando pinçamento das bordas; uso excessivo e, muitas vezes, desnecessário de eletrocautério; material apropriado e de boa qualidade; suturas subcutâneas para diminuição do espaço morto. Quanto à sutura da pele: promover uma aproximação natural das bordas, sem demasiado aperto, evitando isquemia, necrose e infecção da cicatriz.
2- Uso de drogas sistêmicas e principalmente tópicas. Drogas sistêmicas: especial cuidado com pacientes em uso de anticoagulantes, antiagregantes plaquetários, corticosteróides, antineoplásicos, isotretinoína.22,23 Além dos fármacos, a nicotina deve ser considerada e melhores resultados são conseguidos com a abstinência do cigarro durante 10 dias, pelo menos, antes da cirurgia e três semanas após.24
Drogas tópicas, como o uso desnecessário de associações de antibióticos, corticóides e antifúngicos: vários agentes tópicos atrapalham a migração epidérmica, se comparada ao não-tratamento: acetonido de triancinolona 0,1% diminui 34% a taxa relativa de cura; nitrofurazona diminui 30%. Já o peróxido de benzoíla e coberturas com permeabilidade seletiva melhoram em 14%, a sulfadiazina de prata e pomada neosporina ,em 28%.25
3- Ressecamento das feridas. Popularmente há a crença de que "ferida seca cura mais rápido".
Estudos demonstram que as feridas abertas formam crosta e epitelizam mais lentamente. Inúmeros curativos são então utilizados para produzir umidade local, melhorando de 35% a 45% a taxa de reepitelização de feridas profundas.
II - INTERVINDO NO PROCESSO DE CICATRIZAÇÃO: RECURSOS, TECNOLOGIAS E PROCEDIMENTOS
2.1 Evolução histórica
As tentativas humanas de intervir no processo de cicatrização das feridas, acidentais ou provocadas intencionalmente como parte da realização de procedimentos, remontam à Antigüidade, demonstrando que desde então já se reconhecia a importância de protegê-las de forma a evitar que se complicassem e repercutissem em danos locais ou gerais para o paciente.
Embora tenham sido verificados grandes avanços na compreensão dos processos e fenômenos envolvidos nas diversas fases da reparação tissular e simultaneamente muito se tenha investido em pesquisa e desenvolvimento de recursos e tecnologias com o objetivo de favorecer esses processos, a incidência e prevalência de úlceras crônicas é ainda extremamente alta , repercutindo em elevados custos financeiros e profundas conseqüências sociais sobre os portadores, os quais com freqüência desenvolvem seqüelas que podem levar à perda de membros e de suas funções, com conseqüente afastamento do trabalho e de suas atividades normais, como refere Moryson.26
Embora não haja dados precisos no Brasil, alguns trabalhos demonstram que o impacto psíquico, social e econômico da cronificação de lesões, em especial as úlceras crônicas dos pés e pernas, representa a segunda causa de afastamento do trabalho no Brasil.27
Isso demonstra que, embora se acredite que tudo já foi descoberto e pesquisado no campo da cicatrização e dos curativos e que existem recursos e tecnologias em excesso no mercado, muito há que se pesquisar nesse campo não só para aperfeiçoar tais recursos, como para torná-los acessíveis a maior número de pessoas, mediante o desenvolvimento de tecnologias mais simples e baratas, igualmente eficientes, que se aproveitem de matérias-primas encontradas nessas regiões menos desenvolvidas, pois um dos desafios para o profissional é o elevado custo de tais recursos, em sua maioria importados e cuja tecnologia é patenteada por empresas multinacionais.27
Os registros mais antigos, citados por Zimmerman e Veith28 falam sobre manuscritos egípcios que datam de 3000-2500 a.C, e neles são mencionados curativos à base de mel, graxa, fios de linho e diversos tipos de excrementos, que faziam parte dos princípios da farmacopéia egípcia.
Hipócrates, que lançou as bases da medicina científica, recomendava que as feridas fossem mantidas limpas e secas, e preconizava sua limpeza com água morna, vinho e vinagre. Foi ele também quem criou os conceitos de cicatrização por primeira ou segunda intenção, como refere Trevelyn, citado por Dealey.29
A partir do século XIX, durante a Guerra da Criméia, foram criados vários tipos de curativos, à base de fibras de linho, que, sendo reutilizadas várias vezes, se tornavam gradativamente mais macias, mas eram pouco absorventes.
Por volta de 1860, Gamgee descobre o processo de remoção do óleo da lã de algodão, tornando-o absorvível, e cria o chumaço de algodão envolto em gaze, ainda hoje utilizado.
Entre o final de 1840 e a Segunda Guerra Mundial, o foco para o tratamento de feridas e cicatrização foi a utilização de anti-sépticos e agentes tópicos com ação antimicrobiana e a proteção com coberturas secas, como conseqüência às descobertas de Pasteur sobre a "Teoria dos Germes". Nessa fase, como referem Sinclair e Ryan,30 dá-se o período áureo de utilização de anti-sépticos como o líquido de Dakin, Eusol, derivados de iodo, mercúrio e alumínio.
Até o final da Segunda Guerra Mundial os recursos utilizados para a proteção das lesões baseavam-se na crença de que o ambiente seco proporcionava melhores condições de cicatrização, sendo largamente desenvolvidos e utilizados agentes tópicos que provocavam o dessecamento do leito da ferida, e as coberturas consistiam basicamente de gaze seca, fixada com espessa camada de fitas adesivas.
Em 1945, Bloom relata pela primeira vez a utilização de um filme transparente, permeável ao vapor, em 55 pacientes com queimaduras, e descreve seu efeito benéfico no processo de cicatrização. Posteriormente, em 1950, Schilling apresenta novos estudos com a utilização desse tipo de filme, envolto em moldura adesiva de polivinil, que veio trazer as bases para o desenvolvimento dos futuros recursos, como referido por Field.31
Embora já se aceitasse o pressuposto de que a criação de um ambiente úmido na ferida trazia efeitos extremamente benéficos para o processo cicatricial, bem como reduzia a dor, devido à proteção das terminações nervosas contra o dessecamento, até início da década de 1960 esses recursos ainda não estavam sendo desenvolvidos pela indústria. Só a partir de 1962, quando Winter e Roove16 demonstraram que a taxa de epitelização era 50% mais rápida em um ambiente úmido e que a formação de crostas era minimizada, houve grande interesse pelo desenvolvimento de pesquisas, produção e comercialização desse tipo de recurso, ocorrendo uma verdadeira "revolução no conceito de curativos"
Nos Estados Unidos e Europa, registra-se uma avalancha de novos recursos a partir de 1970, gerando entre os profissionais grande confusão quanto a sua adequada indicação e utilização; em contrapartida, não se tinham evidências sobre os reais benefícios de cada um desses recursos, nem estudos controlados sobre custo/benefício de cada um deles.
Com essa preocupação, diversos órgãos e agências passaram a coordenar estudos que pudessem estabelecer critérios para a avaliação adequada das feridas e, concomitantemente, indicar parâmetros que direcionassem a adequada seleção desses recursos, de acordo com tais critérios, como refere Goldsmith.32
Esses critérios, parâmetros e escalas de avaliação têm sido exaustivamente estudados, e, embora ainda exista muita controvérsia entre os diversos grupos, de forma geral todos eles buscam reunir as melhores evidências sobre as diversas tecnologias, os materiais, recursos e procedimentos, disponibilizando e divulgando o máximo de informações e referências, cujo acesso pode ser facilmente obtido pelos sites dessas agências na internet (www.npuap.org e www.ahcpr.org).
A partir de 1980 passam a ser realizados estudos em larga escala, nos Estados Unidos e em vários países da Europa, visando desenvolver instrumentos mais adequados para a avaliação de feridas e princípios para a reformulação de protocolos e revisão de procedimentos e de técnicas utilizadas para a realização de curativos.33
Em 1982 as coberturas à base de hidrocolóides são lançadas nos Estados Unidos e Europa, passando a ser largamente utilizadas em feridas de espessura parcial. Tais coberturas só foram disponibilizadas no mercado brasileiro a partir da década de 1990, e seu custo elevado foi uma barreira inicial para sua difusão. Também no início dos anos 90 são lançados os hidropolímeros, que, além de manter o meio úmido, agregavam a propriedade de promover a evaporação do exsudato, favorecendo a granulação e diminuindo a maceração de tecidos neoformados.
Nesse período o número de publicações sobre o assunto cresceu vertiginosamente nesses países; no Brasil, só a partir da década de 1990, com a chegada dos primeiros curativos chamados "modernos", é que o assunto passou a ser alvo de estudos e pesquisas, em especial nas universidades.32
Grande parte das publicações sobre recursos, tecnologias e procedimentos para o tratamento de feridas é fragmentada, consistindo em relatos isolados sobre um ou outro tipo de agente tópico ou cobertura em alguns tipos de ferida, mas tais estudos são freqüentemente descontinuados, e os resultados não trazem evidências precisas quanto a custo/benefício de cada um deles, como refere Dantas.33
O impacto social e econômico da cronificação de feridas e suas conseqüências, devido à infecção local ou sistêmica, tem sido alvo de grande preocupação por parte dos profissionais, fazendo com que, na década de 1990 a utilização de anti-sépticos e dos mais variados tipos de agentes antimicrobianos se tornasse uma panacéia com repercussões extremamente danosas. Com o estabelecimento de estudos controlados do efeito desses diversos agentes sobre os tecidos, pôde-se constatar que a maioria provocava mais danos do que benefícios, e sua utilização tem-se tornado cada vez mais restrita, como refere Ribeiro.34
Ayello,35 ao analisar a situação atual em termos de tratamento de feridas crônicas nos Estados Unidos, especialmente devido à grande preocupação das autoridades e seguradoras norte-americanas com relação aos elevados e crescentes custos desses pacientes, chama atenção dos profissionais para vários mitos e crenças que, de forma sutil, se incorporam ao cotidiano e, sem que se perceba, passam a ser vistos como verdades.
Entre eles, alguns devem ser destacados, pois comumente são utilizados como argumentos para manutenção de condutas inadequadas por parte dos profissionais.
"Curativos especiais, industrializados são melhores do que curativos simples."
"O cuidado de feridas é um procedimento estéril."
"O cliente/paciente ou familiar não precisa de orientação."
"Os novos recursos da tecnologia substituirão o cuidado."
"Tudo já foi pesquisado e descoberto sobre tratamento de feridas."
Segundo Ayello,35 o sucesso no tratamento de feridas depende mais da competência e do conhecimento dos profissionais envolvidos, de sua capacidade de avaliar e selecionar adequadamente técnicas e recursos, do que da disponibilidade de recursos e tecnologias sofisticadas. Para uma intervenção efetiva no processo cicatricial, com o objetivo de favorecê-lo, isso implica a necessidade de estabelecer metas realistas, que considerem os diversos fatores, como o diagnóstico preciso do tipo de lesão e seu estágio cicatricial, e critérios clínicos e técnicos (Figura 2.1).
2.2 Componentes do processo de seleção de recursos para otimizar a cicatrização
Pergunta freqüente entre os profissionais é: qual o melhor curativo para tal tipo de ferida?
Essa resposta não existe de forma absoluta, pois, feridas diferentes, em diferentes tipos de pacientes, requerem diferentes formas de tratamento. Como refere Dealey,27não se pode fazer esse tipo de comparação de forma absoluta, pois o tratamento de lesões com o objetivo de favorecer sua cicatrização não se restringe ao estabelecimento de rotinas para troca de curativos ou ao estabelecimento de protocolos sobre o uso de produtos.
As grandes mudanças ocorridas nas últimas décadas nos conceitos referentes à cicatrização têm mobilizado as indústrias a desenvolver e colocar no mercado produtos cada dia mais específicos que sejam eficazes e adequados a cada tipo de ferida em termos de custo/benefício.
Segundo Cuzzell,36 existem hoje no mercado aproximadamente 2.500 itens que se destinam ao tratamento de feridas agudas e crônicas, desde a mais simples cobertura, soluções para higienização e anti-sepsia até os mais complexos tipos de curativos, chamados "curativos inteligentes" ou "bioativos", que interferem de forma ativa nas diversas fases do processo cicatricial, dos vários tipos de feridas. Se por um lado tal diversidade de opções é um fator altamente positivo, por outro, pode tornar extremamente desafiadora a decisão.
Para direcionar esse processo de escolha, Cuzzell36 reforça a idéia de que é fundamental uma acurada avaliação da lesão, identificando-se cuidadosamente o estágio do processo cicatricial e tomando-se a decisão a partir dessa avaliação, que, aliás, deve ser sistemática e periodicamente realizada, com critérios bem estabelecidos e protocolos de avaliação, como refere Marquez.37
Os produtos para tratamentos de feridas podem ser reunidos em dois grandes grupos: agentes tópicos e curativos.
Agentes tópicos são aqueles aplicados diretamente sobre o leito da ferida ou destinados à limpeza ou proteção da área em seu redor. Curativo, também chamado por alguns autores de cobertura, é o recurso que cobre uma ferida, com o objetivo de favorecer o processo de cicatrização e protegê-la contra agressões externas, mantendo-a úmida e preservando a integridade de sua região periférica.29
Normalmente os curativos são divididos em primários, quando usados em contato direto com o tecido lesado, e secundários, quando colocados sobre o curativo primário. Algumas coberturas destinam-se basicamente a atuar como curativo secundário; outros, por sua vez, requerem a utilização de cobertura secundária, como será tratado a seguir.
Com a oferta crescente e diversificada desses recursos, aliada a uma estratégia publicitária intensiva junto aos profissionais, o processo de tomada de decisão pode ficar comprometido se nele prevalecerem fatores como a pressão da mídia ou apenas o custo dos produtos.
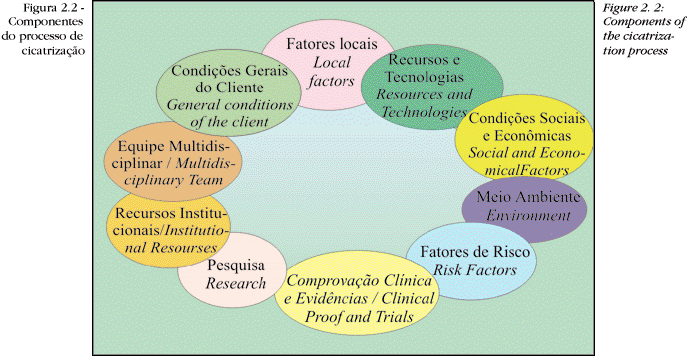
Deve-se considerar que a utilização de recursos para otimizar a cicatrização e reparação tecidual é um processo multifatorial e de caráter multidisciplinar,33 que precisa levar em conta os seguintes parâmetros, como ressalta Hill:38
os clientes portadores de feridas, agudas ou crônicas, lesões primárias ou lesões secundárias, infectadas ou não, com suas necessidades e expectativas de um tratamento eficaz e que lhes ofereça qualidade de vida;
os profissionais de saúde, com seu conhecimento técnico-científico e suas ferramentas para a implementação de medidas preventivas, profiláticas e curativas no tratamento das lesões, e abordagem holística do paciente;
as indústrias, que pesquisam, desenvolvem e produzem materiais e recursos, e esperam ver seus produtos difundidos no mercado, para retorno desse investimento;
as instituições de saúde, públicas e privadas, com seus recursos orçamentários e seus critérios para seleção de recursos. Em grande número de instituições públicas os recursos são exíguos para atender à grande demanda de clientes de baixo poder aquisitivo, que freqüentemente desenvolvem afecções mais graves. Por outro lado, as instituições privadas e as seguradoras estabelecem critérios cada vez mais rígidos para autorizar a utilização de recursos e tecnologias mais sofisticadas, devido à necessidade de controle de custos.
Ao selecionar os recursos que serão utilizados, é fundamental uma análise cuidadosa de cada um desses componentes, pois o sucesso no processo de tomada de decisão para a escolha dos recursos deve ter como objetivo harmonizar esses diversos elementos, tendo-se como base princípios permanentemente revisados sobre a fisiopatologia do processo de reparação tecidual e do tratamento de feridas, como refere Rijiswijk.39
2.3 Fatores que interferem na escolha dos recursos
2.3.1 Necessidades do cliente
A avaliação geral do cliente é um dos fatores mais importantes do processo de tratamento de feridas, como refere Sheridan,40 pois toda e qualquer proposta de intervenção deve levar em conta não só a lesão a ser tratada, mas o portador da mesma, com suas características e necessidades. Nessa avaliação devem ser consideradas algumas ações:
a) diagnosticar os fatores intrínsecos (decorrentes das condições gerais do paciente) e extrínsecos, que possam interferir na evolução do processo cicatricial;
b) identificar as expectativas do cliente e família, suas possibilidades econômico-financeiras de manutenção. Avaliar, quanto ao custo/benefício, a relação entre medidas preventivas mais simples e tratamentos mais complexos;
c) avaliar a disponibilidade do paciente e da família para realizar o curativo e a facilidade de utilização do recurso selecionado;
d) avaliar os fatores que possam interferir na aderência ao tratamento proposto e em sua continuidade;
e) buscar a independência, estabelecendo um planejamento que leve o paciente ao autocuidado. Inúmeros trabalhos têm demonstrado que portadores de feridas crônicas se tornam dependentes de cuidadores familiares ou profissionais, devido a falhas no processo de educação para o autocuidado. Outros autores têm salientado que as lesões da pele, especialmente as crônicas, provocam alterações de auto-imagem, e os indivíduos desenvolvem um processo de negação e resistência em relação a tais lesões, evitando olhá-las, tocá-las e delas cuidar;
f) promover a qualidade de vida além da cicatrização e do fechamento das lesões, pois o processo de tomada de decisão quanto aos procedimentos, recursos e tecnologias que serão utilizados deve buscar a preservação das potencialidades e bem-estar das pessoas que os utilizam, e para isso é fundamental que haja participação, envolvimento e respeito às opiniões do paciente e da família.
2.3.2 Avaliação da Ferida
Bryant,40 entre outros autores, e diversas agências reguladoras norte-americanas, como a AHCPR,41 destacam que a avaliação é uma parte fundamental do processo de tratamento das lesões da pele, pois só o diagnóstico preciso do tipo e estágio da lesão vai permitir a correta tomada de decisão sobre as medidas a serem implementadas e os recursos que serão utilizados. Um roteiro sistemático de avaliação deve incluir:
a) história e exame subjetivo do cliente;
b) dados objetivos do cliente: condições gerais, exames laboratoriais, doenças associadas;
c) avaliação do risco, com base nas condições gerais do cliente e do local da lesão;
d) avaliação e classificação adequada da lesão: localização, tempo de evolução, medida do tamanho, diâmetro, profundidade, vitalidade do leito e dos tecidos circunvizinhos, presença de secreção e necrose, coloração do leito da ferida, sensibilidade cutânea, comprometimentos;
e) diagnóstico adequado do tipo de ferida, suas necessidades e conseqüente planejamento de ações.
Podem ser utilizados diversos sistemas, alguns mais indicados para a avaliação de feridas agudas, outros especialmente desenvolvidos para a avaliação de feridas crônicas. Vários instrumentos têm sido criados para facilitar e direcionar o processo de avaliação, e alguns já estão validados no Brasil.
Nos Estados Unidos têm sido desenvolvidos alguns sistemas que auxiliam os profissionais nesse processo de avaliação e facilitam a tomada de decisão sobre os procedimentos e recursos a serem utilizados. Entre eles, vários trabalhos têm relatado e difundido a utilização do sistema Red/Yellow/Black - RYB,42 proposto por Cuzzel,43 para classificação de feridas que cicatrizam por segunda intenção. Segundo tal sistema, as feridas são classificadas de acordo com a coloração que, afirma a autora, freqüentemente reflete o balanço entre tecidos novos e tecidos necrosados. O sistema RYB assim classifica as feridas:
- as vermelhas incluem sítios doadores de enxertos, feridas pós-desbridamento, feridas crônicas em cicatrização, em que predomina o tecido de granulação e novo epitélio. Nesse tipo de ferida, o objetivo do tratamento é favorecer o ambiente úmido, proteger os tecidos neoformados e prevenir a infecção;
- as amarelas normalmente apresentam exsudato fibroso e seus tecidos são moles, desvitalizados; elas podem estar colonizadas, o que favorece a instalação de infecção. Nesse tipo de ferida o objetivo é identificar adequadamente a presença ou não de infecção e, neste último caso, promover o desbridamento dos tecidos desvitalizados e estancar a infecção, preferencialmente por meio de terapia sistêmica;
- as pretas apresentam necrose tecidual, com desnaturação e aumento de fibras colágenas, e conseqüente formação de escara espessa, cuja coloração pode variar entre castanho, marrom e preto. Nesse tipo de ferida, devido à presença do tecido necrótico, o objetivo é remover o tecido necrosado com a máxima brevidade, por meio do desbridamento.
É evidente que a coloração não constitui um parâmetro preciso de avaliação da ferida e não deve ser o único, pois normalmente as feridas apresentam combinações dessas diversas colorações, de acordo com a profundidade da lesão, das terapias usadas e das condições locais e gerais.
Outro sistema útil para avaliação e estabelecimento de condutas e objetivos, assim como para acompanhamento da evolução do tratamento, é a escala Push Tool, proposta pela NPUAP44 que, partindo dos parâmetros acima, permite a categorização da lesão e auxilia no direcionamento das medidas de intervenção em cada uma das fases do processo cicatricial, permite avaliar eficácia de medidas e recursos utilizados e a evolução do processo cicatricial.
2.3.3 Oferta de produtos
Devido à diversidade de tipos e marcas de produtos, é importante que sejam considerados alguns aspectos quando da análise para sua escolha, aquisição e indicação:
1) documentação técnico-científica do produto fornecida pelos fabricantes; estudos clínicos realizados e metodologia de utilização para avaliação e validação desses recursos;
2) comprovação de resultados, ou seja, evidências clínicas, mediante estudos padronizados, veiculados em publicações científicas reconhecidas;
3) origem dos produtos e das matérias-primas utilizadas, atestando seriedade, experiência, compromisso e registro nos órgãos de fiscalização;
4) custo/benefício - avaliação do custo inicial e de manutenção, e dos investimentos por meio da elaboração de planilhas comparativas entre os diversos recursos, que considere não apenas seu preço inicial, mas se baseie em estudos controlados dos diversos elementos envolvidos;
5) disponibilidade do produto e facilidade de acesso;
6) atendimento ao cliente por parte do fabricante (serviço de atendimento ao consumidor) para orientação e substituição em caso de iatrogenias ou descontinuidade de produção;
7) atendimento à instituição e aos pesquisadores;
8) qualidade de vida - iatrogenias, autocuidado, independência, educação, motivação;
9) pesquisa e avaliação, incluindo ensaios clínicos, testes, grupo piloto;
10) auditoria e serviço de atendimento aos consumidores;
11) controle de qualidade constante;
12) treinamento e reciclagem dos usuários, clientes e profissionais;
13) facilidade de utilização pelos clientes e profissionais;
14) biodegradabilidade/preocupação com meio ambiente;
2.3.4 Recursos da instituição
1) Formação de grupos multiprofissionais nas instituições para definição de procedimentos e seleção de recursos.
2) Participação efetiva de especialistas nos processos de tomada de decisão para compra de materiais.
3) Atualização constante de protocolos e estudos de custo/benefício.
4) Embasamento técnico-científico seguro.
5) Avaliação constante.
6) Qualidade sob todos os ângulos.
7) Custo/benefício.
8) Qualidade de vida.
9) Protocolos atualizados e acessíveis.
10) Pesquisa constante e atualização profissional - reciclagem de conhecimentos X modismos.
11) Decisões em equipe multiprofissional - estudos de casos - publicação de resultados com base em evidências.
12) Metodologia científica rigorosa.
(ver figura 2.2)
2.3.5 Elementos para proposição de um plano de tratamento que favoreça o processo de cicatrização com enfoque multidisciplinar
13) Cuidados de ordem geral: alimentação, nutrição, higiene, deambulação ou mobilização.
14) Cuidados com a ferida: avaliação a cada troca de curativo, por meio de instrumentos e critérios adequados já referidos, e documentação, utilizando escalas de avaliação, também já referidas.
15) Estabelecimento de procedimentos e técnicas, e sua permanente reavaliação e revisão pela equipe multidisciplinar: a equipe deve discutir as diversas etapas do processo de tratamento de lesões, assim como selecionar e indicar o conjunto de recursos que serão utilizados, tanto nos aspectos preventivos como nos de recuperação.
Esse conjunto de recursos e tecnologias deve ser decidido em equipe, por meio do estabelecimento de protocolos básicos, que devem incluir:
- procedimentos para higienização da ferida, com a utilização de técnicas e recursos atualizados constantemente, com base em evidências da literatura;
- procedimentos e recursos para remoção de tecido necrótico desvitalizado, de acordo com o tipo de ferida;
- recursos para proteção da ferida e da área periférica, e prevenção de infecção;
- coberturas adequadas ao tipo de ferida, selecionadas conforme parâmetros relativos a: localização da ferida (saliências ósseas, local anatomico, região de dobras); área (comprimento x largura) e profundidade da lesão; características e quantidade de exsudato; existência de túneis ou cavidades, vitalidade dos tecidos do leito da ferida e condições das bordas, presença de edema, odor, coloração do leito e área próxima.
16) Diagnóstico preciso do tipo de ferida e estágio do processo cicatricial, e estabelecimento de metas e objetivos em função de cada estágio.
17) Treinamento e reciclagem contínua das equipes.
18) Acompanhamento e documentação para controle e avaliação, e estabelecimento de evidências sobre a eficácia dos diversos recursos e reavaliação contínua.
Recebido em 24.06.2003
Aprovado pelo Conselho Editorial e aceito para publicação em 24.06.2003
Questões e Resultados das Questões
1) Assinale a alternativa falsa:
a) A cicatrização é evento complexo e dinâmico.
b) A cicatrização final depende da perda tecidual inicial.
c) Muitos eventos dermatológicos contam com a cica trização em derme incompleta.
d) As fases da cicatrização são bem determinadas e individualizadas.
e) A cicatrização depende de vários fatores como: localização anatômica, tipo da pele, raça, e técnica cirúrgica utilizada.
2) Qual das alternativas abaixo não corresponde à cicatrização em derme completa?
a) A cicatriz é perceptível.
b) Muitas vezes a cicatriz é pronunciada.
c) A reparação se faz basicamente pela reepitelização.
d) Necessita de formação de um novo tecido.
e) Pode se estender até tecido celular subcutâneo.
3) Em relação à coagulação, podemos afirmar:
a) O início é imediato após o surgimento da ferida.
b) Independe de outras atividades como a plaquetária e cascata de coagulação.
c) Inúmeros produtos como substâncias vasoativas são liberadas, e são importantes apenas para esta fase.
d) É a única fase individual, sendo bem particularizada das subseqüentes.
e) O coágulo é imprescindível para coaptar as bordas das feridas, e imediatamente fagocitado por não ter mais nenhum papel relevante nesta fase.
4) As células mais importantes da fase inflamatória são:
a) Leucócitos Polimorfonucleares
b) Eosinófilos
c) Linfócitos
d) Plasmócitos
e) Macrófagos
5) As primeiras células a chegar à ferida são:
a) Macrófagos
b) Plasmócitos
c) Linfócitos
d) Eosinófilos
e) Leucócitos Polimorfonucleares
6) Importante na fase inflamatória, sobre a fibronectina podemos afirmar:
a) Sintetizada por várias células.
b) Funciona como cola para consolidar o colágeno de fibrina, às células e os componentes da matriz.
c) É munida de propriedades quimiotáticas.
d) Promove opsonização e fagocitose de corpos estra nhos e bactérias.
e) Todas as alternativas estão corretas.
7) Para a formação do tecido de granulação, é extremamente importante:
a) Coagulação.
b) Fibroplasia e formação da matriz.
c) Reepitelização.
d) Atividade plasmocitária.
e) Ação quimiotática dos leucócitos.
8) Em relação a contração da ferida, é errado afirmar:
a) Movimento centrípeto das bordas.
b) Ocorre em todas as feridas de espessura parcial.
c) Ocorre mesmo quando há enxertos.
d) Pode passar de 50% em cicatrizes por segunda intenção.
e) Facilita por diminuição da área o reparo do defeito cutâneo.
9) A remodelação ocorre:
a) Rapidamente e logo após a coagulação.
b) Aumentando a quantidade de água, para melhor efeito final da cicatriz.
c) No colágeno e na matriz.
d) Para aumentar a espessura da cicatriz e diminuir a sua força de tensão.
e) Visando aumentar a vascularização da cicatriz.
10) Existem muitas variáveis que podem modificar o efeito final da cicatriz:
a) Uso de drogas sistêmicas.
b) Uso de drogas tópicas
c) Técnica cirúrgica respeitando unidades estéticas, evitando o pinçamento, e promovendo uma aproxi mação natural das bordas.
d) Material cirúrgico utilizado, em feridas provocadas.
e) Todas acima são variáveis importantes e devem ser consideradas em cirurgia dermatológica.
11. O desenvolvimento de recursos e tecnologias para otimizar o processo cicatricial foi especialmente acelerado:
a) logo após a Segunda Guerra Mundial, com o adven to dos antibióticos tópicos
b) na década de 60, com o surgimento dos anti-sépticos e descoberta do papel dos fatores de crescimento na cicatrização
c) a partir de 1970, com a descoberta dos curativos modernos, que minimizaram o fator humano na rea lização dos procedimentos
d) a partir de 1960, com as pesquisas sobre os efeitos do meio úmido no processo de cicatrização
e) a partir da década de 90, com o desenvolvimento da engenharia de tecidos e do Projeto Genoma
12. Dentre os fatores abaixo, identifique aqueles que retardam ou impedem a cicatrização de lesões abertas, de forma mais imperativa:
a) idade e utilização de antibióticos sistêmicos
b) pressão contínua sobre o local e manutenção da lesão em meio seco
c) doenças pré existentes e uso de anti-sépticos
d) estado nutricional e uso de curativos não industria lizados
e) presença de infecção e técnica de limpeza utilizada
13. De acordo com o sistema RYB as feridas são classificadas:
a) pelo grau de lesão tissular, em 4 estágios diferentes
b) pelo tipo e volume de exsudato, em 3 grupos: alta mente ex-sudativas, moderamente exsudativas e não exsudativas
c) pela profundidade, podendo ser superficiais ou pro fundas,
d) pela coloração do leito da ferida
e) pelo tamanho da lesão quanto ao seu diâmetro
14. Considerando-se que a cicatrização é um processo multifatorial, segundo Hill, que parâmetros devem ser avaliados quando se busca otimizar este processo:
a) tipos de curativos, tipos de feridas, tipo de pacientes e profissionais
b) pacientes, produtos, recursos financeiros, tipos de feridas
c) profissionais,clientes,indústrias , instituições
d) recursos humanos,tipos de feridas, pacientes, recursos materiais
e) tipos de feridas, recursos institucionais,pacientes, tipos de curativos
15. Dos elementos abaixo, assinale aqueles que têm influência direta sobre a decisão do tipo de cobertura a ser utilizada em uma lesão:
a) causa, tempo de evolução e localização da lesão
b) tamanho, localização e tipo de exsudato
c) profundidade, causa e coloração da lesão
d) localização, tempo de evolução, presença de odor
e) coloração, presença de infecção, causa da lesão
16. A limpeza das feridas abertas é um assunto controverso, mas alguns consensos recomendam que:
a) para a limpeza de feridas crônicas deve-se utilizar anti-sépticos e a técnica deve ser estéril
b) em todos os tipos de feridas o ideal é que se utilize água e sabão neutro
c) as feridas abertas devem ser limpas através da fricção de gaze embebida em soluções anti-sépticas recomendadas pelos órgãos de controle de infecções, diluí das em solução salina
d) a limpeza da maioria das feridas abertas deve ser feita com o uso de soluções isotônicas através de irrigação sob pressão controlada
e) todas as alternativas estão corretas
17. A prescrição de tratamento baseado em estudos clínicos controlados deve levar em conta:
a) necessidades do paciente, necessidades da ferida, resultados dos estudos clínicos
b) estudos clínicos controlados, evolução do paciente , evolução da ferida
c) evolução da ferida, evolução clínica do paciente, resultados obtidos
d) avaliação do paciente, prescrição do curativo, evolução da ferida
e) avaliação da ferida, tipo de curativo, evolução
18. Das alternativas abaixo, assinale a afirmação correta :
a) O cuidado de feridas é um procedimento estéril
b) Os curativos industrializados substituiram os cura tivos artesanais pois são mais seguros
c) Os recursos hoje disponíveis para auxiliar na cicatrização são suficientes e não são necessários novos processos e pesquisas
d) A competência dos profissionais influe de maneira mais efetiva no processo de cicatrização do que os recursos existentes
e) Com o advento dos curativos modernos a cicatriza ção de feridas deixou de ser um problema
19. Os primeiros registros sobre a utilização de recursos para favorecer o processo de cicatrização são atribuídos a:
a) aos gregos, a partir dos trabalhos de Hipócrates
b) aos fenícios, com o uso de anti-sépticos
c) aos romanos, com a utilização de mel sobre as feridas
d) aos egípcios, com o uso de excrementos de animais
e) aos babilônios, com o uso de plantas medicinais
20. Os recursos disponíveis no mercado para o tratamento de feridas podem ser classificados em dois grandes grupos:
a) anti-sépticos e curativos
b) coberturas primárias e coberturas secundárias
c) agentes tópicos e coberturas
d) curativos oclusivos e não oclusivos
e) curativos úmidos e curativos secos
GABARITO
Vitamina C
2003; 78(3): 265-274
- 1. Ortonne JP, Clévy JP. Physiologie de la cicatrisation cutanée. Ver Prat 1994; 44(13): 1733-4.
- 2. Fazio MJ, Zitelli JA, Goslen JB. Cicatrização de feridas. In: Coleman III WP, Hanke CW, Alt TH, Asken S. Cirurgia Cosmética - Princípios e Técnicas. 2.ed. Rio de Janeiro: Revinter, 2000:18-23.
- 3. Julía V, Albert A, Morales L, Miró D, Bombi J, Sancho A. Características de la cicatrización de las heridas en el período fetal. Cir Pediatr 1992; 5(3): 117-21.
- 4. Ortonne JP, Clévy JP. Physiologie de la cicatrisation cutanée. Rev. Prat 1944; 44(13); 1735-7.
- 5. Fazio MJ, Zitelli JA, Goslen JB. Cicatrização de feridas. In: Coleman III WP, Hanke CW, Alt TH, Asken S. Cirurgia Cosmética - Princípios e Técnicas. 2.ed. Rio de Janeiro: Revinter, 2000:23-28.
- 6. Terkeltaub RA, Ginsberg MH. Platelets and response to injury. In: Clark RAF, Henson PM, editors: The molecular and cellular biology of wound repair. New York: Plenum Press,1998.
- 7. Clark RAF. Cutaneous tissue repair. Basic biologic considerations. J Am Acad Dermatol 1985;13:701.
- 8. Clark RAF, Lanigan JM, Dellapelle P et al Fibronectin and fibrin provide a provisional matrix for epidermal cell migration during wound reepithelization, J Invest Dermatol 1982;(79):264.
- 9. Grinnel F, Billinghiam RE, Burgess L. Distribution of fibronectin during wound healing in vivo. J Invest Dermatol 1981; (76):181.
- 10. Diegelmann RF, Cohen IK, Kaplan AM. The role of macrophages in wound repair: a review. Plast Reconstr Surg 1981; (68):107.
- 11. Petrova MB. Morfofunktsional'nye osobennosti zazhivleniia kozhnoi rany u krys pri vozdeistvii nizkointensivnogo lazernogo izlucheniia. Morfologiia, 1992;102(6):112-21.
- 12. Clark RAR. Potential roles of fibronectin in cutaneous wound repair. Arch Dermatol 1998; 124:201.
- 13. Mosher DF, Furcht LT. Fibronectin: review of its structure and possible functions. J Invest Dermatol 1981; (77):175.
- 14. Christopher E. Kinetic aspects of epidermal healing. In: Maibach H, Rovee D. eds. Epidermal wound healing. St Louis: Mosby., 1972
- 15. Gentilhomme E, Neveux Y, Lebeau J, Desmouliere A, Bergier J, Schmitt D, Haftek M. Modulation of a fibrotic process induced by transforming growth factor beta-1 in dermal equivalents. Cell Biol Toxicol 1999;15(4):229-38.
- 16. Winter GD. Formation of the scab and the rate of epithelization of superficial wounds in the skin of the young domestic pig. Nature 1962;(193):293.
- 17. Hinman CD, Maibach H. Effect of air exposure and occlusion on experimental human skin wounds. Nature 1963;(200):377.
- 18. Van Winkle W. The fibroblast in wound healing. Surg Ginecol Obstet 1967;(124):369.
- 19. Stegman SJ, Tromovitch TA, Glogau RG. Grafts. In: Basics of Dermatological Surgery. St Louis: Mosby, 1982.
- 20. Lawrence CM, Comaish HS, Dahl MGC. Excision of skin tumors without wound closure. Br J Dermatol 1986;(115):563.
- 21. Doillon CJ, Dunn MG, Bender E et al Collagen fiber formation in repair tissue. Development of strength and toughness. Collagen Rel Res 1985;(5):481.
- 22. Marks JG, Cano C, Lietzel K et al Inhibition of wound healing by topical steroids. J Dermatol Surg Oncol 1983;(9):819.
- 23. Rubenstein R, Roenigk Jr HH, Stegman SJ et al. Atypical keloids after dermabrasion of patients taking isotretinoin. J Am Acad Dermatol 1986;(15):280.
- 24. Rees TD, Liverett DM, Guy CL. The effect of cigarette smoking on skin-flap survival in the face lift patient. Plast Reconstr Surg 1984;(73):911.
- 25. Fazio MJ, Zitelli JA, Goslen JB. Cicatrização de feridas. In: Coleman III WP, Hanke CW, Alt TH, Asken S. Cirurgia Cosmética - Princípios e Técnicas. 2.ed. Rio de Janeiro: Revinter, 2000:28-38.
- 26. Moryson M. Leg Ulcers. In: Moryson M. Nursing Management of chronic wounds. Cap. 10, p.177-220. Mosby, London, 2nd edition,1998.
- 27. Ereno D. Curativo de Borracha. Revista Pesquisa Fapesp, número 88, junho de 2003, disponível em http://www.fapesp.org.br/ www.revistapesquisa.fapesp.br
- 28. Zimmerman LM, Veith I. Great ideas in the History. Baltimore, Wilkins & Wilkins Co. 1961.
- 29. Dealey C. Cuidando de Feridas: um guia para as enfermeiras. São Paulo, Atheneu Editora, 2ª edição, 2001, capítulo 3: p. 49-65, capítulo 4: p. 68-89; cap. 9: p. 200-207.
- 30. Sinclair RD, Ryan TJ. A great war for antiseptics. Wound Mangement, 4(1):16-18, 1993.
- 31. Field C, Kerstein M. Overview of wound healing in a moist environment. Am J Surgery, 167:25-65, 1994.
- 32. Goldsmith SP. Wound care: combining three classification systems to select dressings. Home Health Care Mangement and Practice, 8(6):17-26, 1996
- 33. Dantas SRPE. Aspectos históricos do tratamento de feridas. In: Jorge SA. Abordagem Multiprofissional do tratamento de feridas, cap. 1, p. 3-6, São Paulo: Atheneu, 2003.
- 34. Ribeiro SMCP. Soluções anti-sépticas em curativos. In: Jorge SA. Abordagem Multiprofissional do Tratamento de Feridas, cap. 9: p. 101-109. São Paulo: Atheneu, 2003.
- 35. Ayello E, Franz R. Pressure ulcer prevent and treatment: competency-based nursing curricula. Dermatology Nursing, 15(1):44-65, February, 2003.
- 36. Cuzzel J, Krasner D. Curativos. In: Gogia P. Feridas - tratamento e cicatrização. Rio de Janeiro: Livraria Editora Revinter Ltda. cap 9, p. 103-114, 2003.
- 37. Marquez RR. Avaliação da ferida. In: Gogia P. Feridas - tratamento e cicatrização, Rio de Janeiro: Livraria e Editora Revinter Ltda, cap. 2, p. 11-23; 2003.
- 38. Hill MJ. Dermatologic Nursing Essentials: a core curriculum. New Jersey, DNA/ Pitman Editor, 1998. Cap. 18, p. 295-317.
- 39. Rijswijk L V. Princípios gerais do tratamento de feridas. In: Gogia, P. Feridas - tratamento e cicatrização, Rio de Janeiro: Livraria Revinter Ltda. cap. 3, p. 23-37, 2003.
- 40. Bryant RA. Acute and chronic wounds. Saint Louis, Mosby , 2nd edition, 2000.
-
41Agency fo Health Care Policy and Research (AHCPR) - Clinical practice guidelines: pressure ulcer treatment: quick reference guide for clinicians. Dermatology Nursing, 7(2): 87-101.
- 42. _________. Wound Healing: Translating theory into clinical practice. Dermatology Nursing, 14 ( 4 ): 257-261, august 2002
- 43. Cuzzel JZ. The new RYB color code. American Journal of Nursing, 88 (10): 1342-1346, 1988.
- 44. National Pressure Ulcer Advisory Panel . PUSH Tool information and registration form. (2002) In: NPUAP Website http://www.npuap.org
Datas de Publicação
-
Publicação nesta coleção
25 Nov 2003 -
Data do Fascículo
Ago 2003
Histórico
-
Aceito
24 Jun 2003 -
Recebido
24 Jun 2003