Resumos
A imunofluorescência é um valioso instrumento auxiliar no diagnóstico das dermatoses bolhosas autoimunes e desordens inflamatórias, uma vez que seus achados clínicos e histopatológicos podem não ser determinantes. Consiste em um método laboratorial factível, que requer profissionais técnicos experientes, e detecta imunocomplexos in situ e/ou circulantes, que podem estar envolvidos na patogênese de tais enfermidades cutâneas.
Autoimunidade; Imunofluorescência; Membrana basal; Pênfigo
Immunofluorescence is a valuable auxiliary diagnostic tool for autoimmune bullous diseases and inflammatory disorders, since their clinical and histopathologic findings may be inconclusive. It is a feasible laboratory method that requires experienced technicians and detects in situ and circulating immune deposits that may be involved in the pathogenesis of such skin diseases.
Autoimmunity; Basement membrane; Fluorescent antibody technique; Pemphigus
REVISÃO
Imunofluorescência direta e indireta* * Trabalho realizado no Departamento de Dermatologia, Laboratório de Imunopatologia Cutânea, Faculdade de Medicina da Universidade de São Paulo (USP) - São Paulo (SP), Brasil.
Valéria AokiI; Joaquim X. Sousa JrII; Lígia M. I. FukumoriIII; Alexandre M. PérigoIV; Elder L. FreitasV; Zilda N. P. OliveiraVI
IProfessora doutora, Departamento de Dermatologia, Faculdade de Medicina da Universidade de São Paulo (USP) - São Paulo (SP), Brasil
IIDoutorando, Departamento de Dermatologia, Faculdade de Medicina da Universidade de São Paulo (USP) - São Paulo (SP), Brasil
IIIBiologista, Laboratório de Imunopatologia Cutânea, Faculdade de Medicina da Universidade de São Paulo (USP) - São Paulo (SP), Brasil
IVBiologista, Laboratório de Imunopatologia Cutânea, Faculdade de Medicina da Universidade de São Paulo (USP) - São Paulo (SP), Brasil
VBolsista do Programa Integrado de Bolsas de Iniciação Científica (PIBIc), Conselho Nacional de Desenvolvimento Científico e Tecnológico (CNPq); acadêmico da Faculdade de Medicina da Universidade de São Paulo (USP) - São Paulo (SP), Brasil
VIProfessora doutora, Departamento de Dermatologia, Faculdade de Medicina da Universidade de São Paulo (USP) - São Paulo (SP), Brasil
Endereço para correspondência Endereço para correspondência: Valéria Aoki Laboratório de Imunopatologia Cutânea Av. Dr. Enéas de Carvalho Aguiar, 255, 3º andar ICHC, sala 3.016 05403 002 São Paulo - SP, Brasil Tel./fax: 11 3069 8036 E-mail: valaoki@hotmail.com
RESUMO
A imunofluorescência é um valioso instrumento auxiliar no diagnóstico das dermatoses bolhosas autoimunes e desordens inflamatórias, uma vez que seus achados clínicos e histopatológicos podem não ser determinantes. Consiste em um método laboratorial factível, que requer profissionais técnicos experientes, e detecta imunocomplexos in situ e/ou circulantes, que podem estar envolvidos na patogênese de tais enfermidades cutâneas.
Palavras-chave: Autoimunidade; Imunofluorescência; Membrana basal; Pênfigo
INTRODUÇÃO
As reações imunológicas que envolvem a ligação antígeno-anticorpo podem ser visualizadas ou quantificadas por meio de diferentes marcadores para o antígeno ou para o anticorpo. Entre os marcadores mais comumente empregados, podem-se citar os fluorocromos, as enzimas e os compostos radioativos e eletro-opacos.
Os primórdios da imunofluorescência direta (IFD) datam de 1942, quando Albert Coons e col. demonstraram a marcação de anticorpos antipneumococos com fluoresceína no tecido pulmonar.1
Os fluorocromos são corantes que absorvem radiação (luz ultravioleta), são por ela excitados e emitem luz visível. Para que funcionem como marcadores, necessitam possuir grupos químicos capazes de formar ligações covalentes com moléculas protéicas, emitindo alta fluorescência no espectro visível com coloração distinta da emitida pelos tecidos. Devem ter uma conjugação relativamente simples, retenção da atividade do anticorpo na proteína marcada e estabilidade do conjugado fluorescente obtido. Um dos fluorocromos mais utilizados é o isotiocianato de fluoresceína (FITC), de cor verde, que tem um pico de absorção de 490l e de emissão de 520l. A rodamina, outro agente utilizado na IFD, de cor vermelha, possui picos distintos de absorção e de emissão (520l e 610l). O microscópio utilizado para a leitura de IFD pode ser de epiluminescência ou confocal.2
Na leitura das reações de imunofluorescência (IF), devem-se enumerar três formas distintas de fluorescência: específica, não específica e autofluorescência. A fluorescência específica deve-se à reação entre o substrato e a proteína marcada com o fluorocromo (reação antígeno-anticorpo). A fluorescência não específica deve-se à coloração dos tecidos por corante livre ou proteínas fluoresceinadas, ou ambos. A autofluorescência ocorre devido à fluorescência natural dos tecidos (amarela, azul), quando expostos à luz ultravioleta.3
A imunofluorescência foi introduzida na Dermatologia na década de 60, quando Beutner e Jordon, por meio dessa técnica, revelaram anticorpos tanto no tecido como circulantes nas dermatoses vesicobolhosas autoimunes, especialmente, nos pênfigos vulgar (PV) e foliáceo (PF)4-5 e penfigoide bolhoso (PB).6
Atualmente, os estudos de imunofluorescência são determinantes no diagnóstico laboratorial das dermatoses bolhosas autoimunes, mas também desempenham importante papel na investigação de outras enfermidades, como: dermatoses inflamatórias (lúpus eritematoso, líquen plano, porfírias, vasculites).
A - IMUNOFLUORESCÊNCIA DIRETA
O melhor local e o tempo de evolução das lesões cutâneas para realizar biópsia para o exame de imunofluorescência direta (IFD) dependem da enfermidade em investigação. Em termos gerais, a biópsia deve ter uma extensão adequada (punch 4mm), bem como uma profundidade que represente epiderme e derme suficientes. Além disso, quanto menor for o traumatismo realizado durante o procedimento, melhor será a amostra para análise.3
Os seguintes locais para biópsia são recomendados:
Nas dermatoses vesicobolhosas autoimunes, o melhor local é a região perilesional;
Nas colagenoses, deve-se realizar biópsia na lesão ativa em evolução (evitar lesões recentes, com menos de 60 dias);
Nas vasculites, deve-se dar preferência a lesões recentes com até 24 horas de evolução.
Após o procedimento, o material pode ser imediatamente congelado em nitrogênio líquido ou colocado no meio de transporte adequado, o meio de Michel.7 Este é composto de sulfato de amônio, N-etil-maleimida e sulfato de magnésio em um tampão citrato, que permite a conservação do espécime por até duas semanas.8-9
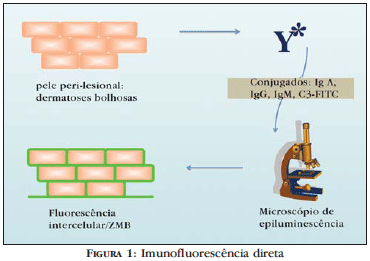
O espécime é, então, seccionado em um criostato, em fragmentos de quatro micra de espessura. A cada secção aplicam-se os anticorpos anti-humanos primários conjugados à fluoresceína FITC (anti-IgA, anti-IgG, anti-IgM e anti-C3) e realiza-se a leitura através do microscópio de fluorescência (Figura 1).3
1. Epitélio
Há dois padrões de fluorescência intraepitelial: a fluorescência intercelular, típica dos pênfigos, e a fluorescência no núcleo dos queratinócitos (FAN in vivo), observada, em geral, nas doenças do tecido conectivo.
1.2 Fluorescência intercelular
Todas as formas de pênfigo caracterizam-se pela perda da adesão celular, levando à acantólise. Essa perda de adesão resulta em formação de bolha intraepidérmica, e o nível de clivagem permite diferenciar as duas formas principais de pênfigo: vulgar e foliáceo. No pênfigo vulgar (PV), a clivagem é suprabasal, enquanto que, no foliáceo (PF), se caracteriza por ser intramalpighiana. A IFD revela fluorescência intercelular, de padrão linear, intraepidérmica.10-11
Pênfigo foliáceo
Os achados de IFD no pênfigo foliáceo clássico (PF) e no endêmico (PFE) apresentam as mesmas características. Autoanticorpos da classe IgG dirigem-se contra a desmogleína 1 (Dsg1), o principal autoantígeno no pênfigo foliáceo.
IFD: Encontram-se depósitos de IgG e C3 intercelulares ao longo de toda a epiderme (Figura 2A) em 100% dos casos na doença ativa.3 Autoanticorpos da classe IgG depositam-se, também, no epitélio escamoso oral, apesar da ausência de lesões clínicas de PFE nas mucosas.3,12 Subclasses de IgG podem ser empregadas, revelando que, em pacientes com lesões de PF ativas, o isótipo de IgG mais predominante é a IgG4, em contraste com a IgG1, mais encontrada nos doentes em remissão.13
Pênfigo vulgar
Autoanticorpos da classe IgG depositam-se na pele e no epitélio escamoso oral. No pênfigo vulgar (PV) com lesões exclusivas de mucosa, os autoanticorpos da classe IgG dirigem-se, geralmente, contra a desmogleína 3 (Dsg3), um autoantígeno de maior expressão nas porções inferiores da epiderme. Quando há lesões mucocutâneas, os doentes de PV podem, também, apresentar anticorpos contra a Dsg1 e indicar pior prognóstico da doença.14 À semelhança do PF, lesões de PV ativas apresentam IgG4, em contraste com os doentes em remissão, nos quais há predomínio de IgG1.15
IFD: Depósitos de IgG e C3 intercelulares, estes últimos com localização predominante nas camadas inferiores dos epitélios (Figura 2B) no PV com envolvimento mucoso, em 100% dos casos de doença ativa.
Pênfigo herpetiforme
O pênfigo herpetiforme (PH) é uma variante do PV ou do PF, em que, clinicamente, se evidenciam pápulas e vesículas agrupadas, pruriginosas, que lembram a dermatite herpetiforme; os achados de IFD são semelhantes ao PF ou PV, ou seja, deposição de IgG intercelular intraepitelial.8,16
Pênfigo paraneoplásico
O pênfigo paraneoplásico (PNP) é uma dermatose bolhosa de prognóstico grave, descrita por Anhalt e col. em 1990. O quadro envolve pele e mucosas e há associação com neoplasias (tumor de Castleman, linfomas, timomas). Exibe muitas semelhanças com o PV, mas apresenta diversidade de autoantígenos (reatividade com a desmogleína 3, desmoplaquinas e antígenos da zona da membrana basal - ZMB).17
IFD: Padrão semelhante ao PV, mas com ocasionais depósitos homogêneos de IgG e C3 na zona de membrana basal (Figura 2C).
Uma das formas de se diferenciar o PNP do PV é a realização da IF indireta (IFI), utilizando-se como substrato o epitélio vesical murino (epitélio não estratificado simples, transicional)18 (V. IFI).
Pênfigo por IgA
O pênfigo por IgA (PIgA) é uma dermatose acantolítica neutrofílica rara. Caracteriza-se por depósitos de IgA intercelulares intraepidérmicos à IFD (Figura 2D) e pode ser classificada em dois tipos: dermatose pustulosa subcórnea (SPD), cujo autoantígeno é a desmocolina 1 (Dsc1), e dermatose neutrofílica intraepidérmica (IEN).19-20
1.3 Fator antinúcleo in vivo
Depósitos de imunoglobulinas, em especial, IgG ou de complemento (C3) nos núcleos de queratinócitos (Figura 3) podem surgir nos quadros autoimunes, tais como no lúpus eritematoso, doença mista do tecido conectivo (DMTC), síndrome overlap e vasculites. Esse fenômeno é denominado fator antinúcleo (FAN) in vivo e apresenta imunopatologia desconhecida. Setenta e um por cento dos pacientes também apresentam anticorpos antinucleares circulantes. Esse padrão de IFD pode ser uma das primeiras evidências de doença autoimune, com valor preditivo positivo para colagenoses variando de 75% a 88%.21-22
2. Zona da membrana basal
A zona da membrana basal (ZMB) ou junção dermoepidérmica apresenta inúmeras proteínas ou glicoproteínas que servem de antígenos-alvo para diversas dermatoses bolhosas autoimunes. Em determinadas dermatoses inflamatórias, tais como lúpus eritematoso, vasculites, líquen plano e porfírias, representa uma região propensa a depósitos de imunocomplexos. Há diferentes padrões de fluorescência da ZMB, sendo os mais frequentes o linear, o homogêneo, o granuloso e o reticulado.
2.1 Depósitos lineares de IgG e/ou C3 na zona da membrana basal
Penfigoide bolhoso
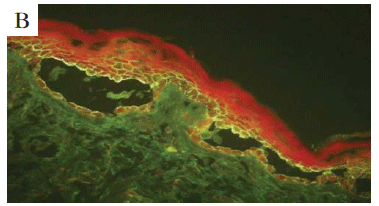
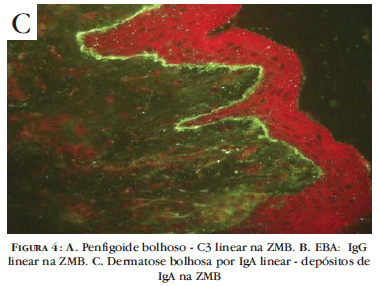
IFD: Depósito linear ou fibrilar ao longo da zona de membrana basal com o conjugado anti-C3 (Figura 4A), em 100% dos espécimes, e de IgG ao redor de 90%; IgA e IgM são raramente evidenciados. Há maior expressão do antígeno do penfigoide bolhoso (PB) nas áreas flexurais, sendo as regiões preferenciais para a biópsia.6,23
Penfigoide gestacional ou herpes gestacional
IFD: Deposição linear de C3 na ZMB em 100% dos casos. Depósitos lineares de IgG na ZMB são encontrados em apenas 30% a 40% dos casos.24-25
Penfigoide das membranas mucosas
IFD: Depósitos de IgG e C3 de padrão linear na ZMB, indistinguível do penfigoide bolhoso. IgA na ZMB ocorre em cerca de 20% dos casos. A positividade da mucosa oral é cerca de 90% a 100%, enquanto que, na conjuntiva, oscila entre 65% e 85%.26-27
2.2 Depósitos lineares múltiplos (IgA, IgG, IgM e/ou C3) na zona da membrana basal
Esses depósitos favorecem o diagnóstico para as dermatoses anticolágeno VII: a epidermólise bolhosa adquirida (EBA) e o lúpus eritematoso sistêmico bolhoso (LESB).3,28-29
Epidermólise bolhosa adquirida e lúpus eritematoso sistêmico bolhoso
IFD: Depósitos lineares ou homogêneos de IgG, IgM, IgA, C3 na ZMB (Figura 4B). Na EBA, depósitos de IgG são mais intensos e presentes em quase 100% dos casos, em comparação com o C3. IgA surge em 67% e IgM em 50% dos espécimes.3,28 No LESB, 60% dos doentes apresentam IFD semelhante à da EBA; nos casos remanescentes, há depósitos que podem ser granulosos, e IgA parece ser a imunoglobulina mais frequente.28
2.3 Depósitos lineares de IgA na zona da membrana basal
Dermatose bolhosa por IgA Linear
A dermatose por IgA linear é uma entidade distinta da dermatite herpetiforme. A IFD é fundamental para que o diagnóstico diferencial entre as duas doenças seja realizado, especialmente, porque na IgA linear (LAD) não há intolerância ao glúten. O autoantígeno é uma glicoproteína de 120kDa e representa uma porção do autoantígeno do penfigoide bolhoso de 180kDa (BP180), que sofreu clivagem enzimática (sheddase).30-31
IFD: Depósito linear ou homogêneo de IgA na ZMB em 80% a 100% dos pacientes (Figura 4C). Eventuais depósitos de C3 e IgG podem ser encontrados na ZMB.3,28
3. Fluorescência na derme
Neste grupo, destacam-se os depósitos granulosos no topo das papilas dérmicas da dermatite herpetiforme (DH), bem como a fluorescência vista na parede dos vasos nas vasculites e porfirias. Por razões didáticas, colocaram-se nesse grupo os achados do líquen plano, que, na maioria das vezes, correspondem a corpos citoides localizados abaixo da ZMB e sem significado clínico aparente.
Dermatite herpetiforme
A IFD representa uma ferramenta diagnóstica de relevância na DH, uma vez que o depósito de imunocomplexos (IgA) nas papilas dérmicas é diagnóstico da enfermidade glúten-sensível.
IFD: Depósitos granulosos, fibrilares ou pontilhados de IgA são encontrados nas papilas dérmicas (Figura 5A). O subtipo de IgA consiste, basicamente, em IgA1; IgA2 ocorre raramente. Outras imunoglobulinas e C3 podem ser encontradas nas papilas dérmicas, mas são raras.32-33
Vasculite
Nas vasculites, os imunodepósitos localizam-se, em geral, nas paredes das vênulas pós-capilares da derme superficial, uma vez que os processos mais frequentes são as vasculites leucocitoclásticas (VLC) e a púrpura de Hennoch-Schönlein (PHS). A coleta deve ser realizada dentro das primeiras 24 horas, visto que os imunocomplexos são rapidamente degradados.
IFD: Na PHS, o depósito predominante é de IgA (75%-100%), de padrão granuloso na parede dos vasos da derme superficial (Figura 5B). Nas vasculites leucocitoclásticas, o depósito nas paredes vasculares consiste, predominantemente, em C3, seguido de IgM e de IgG, e é fibrilar. Nas crioglobulinemias, predominam C3 e, ocasionalmente, IgM e IgA na luz dos vasos. Nas colagenoses, os depósitos mais observados são de IgG, IgM e C3.28,34
Porfiria
A pele lesada na porfiria (cutânea tarda, eritropoiética, variegata, coproporfiria) mostra depósitos homogêneos de IgG, IgM (raro), C3 e IgA na parede de vasos dilatados na derme papilar e ao longo da ZMB. A frequência de tais depósitos nas lesões ativas pode chegar a 100%, enquanto que, na pele normal do doente, a positividade é de 50% (Figura 5C).3,28
Líquen plano
IFD: Presença de corpos citoides fluorescentes com IgM (Figura 5D) e, com menor frequência, IgA e IgG. Depósitos granulosos de IgM na ZMB podem ser encontrados. Todavia, os achados não são diagnósticos de líquen plano, uma vez que podem ser encontrados em outras condições (LE, PB).35-36
4. Imunofluorescência direta no lúpus eritematoso
No lúpus eritematoso (LE), os imunocomplexos dirigem-se contra componentes nucleares dos queratinócitos e de estruturas da zona de membrana basal. A IFD auxilia na confirmação diagnóstica do LE, diferenciando-o de outras doenças. Podem ocorrer depósitos de IgG, IgM, IgA e C3, além de outros imunorreactantes na ZMB. Existem vários padrões de depósitos na ZMB, tais como: o homogêneo, o fibrilar, o linear e o granuloso, que podem ser focais ou contínuos. Na derme, podem ser observados corpos citoides fluorescentes na junção dermoepidérmica com IgM ou IgA. A prevalência das imunoglobulinas na ZMB é determinada, em parte, pela idade, localização e morfologia da lesão, atividade da doença e tratamento.3,28,37
Lúpus eritematoso cutâneo crônico
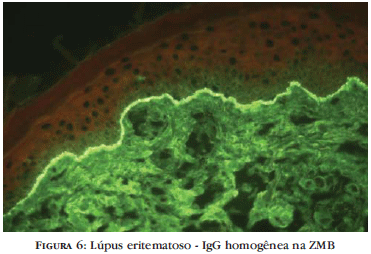
No lúpus eritematoso cutâneo crônico (LECC), a ocorrência dos depósitos de imunorreactantes varia entre 60% e 90%. A positividade da IFD no LECC torna-se, em geral, positiva após o segundo mês de doença. A localização da biópsia é de fundamental importância: as lesões no tronco são, geralmente, negativas, enquanto que as da porção cefálica, pescoço e extremidade superior demonstram mais de 80% de positividade. IgG e IgM, com padrão homogêneo, granuloso ou reticulado (Figura 6), são os mais frequentes, e a maioria dos autores encontra maior positividade de IgM. Na pele não acometida, a IFD é, não raro, negativa.3,28,37
Corpos citoides fluorescentes (IgA e IgM) são encontrados na derme papilar e representam queratinócitos basais degenerados. Não são achados exclusivos do LE, uma vez que são frequentes no líquen plano (LP) e em outras dermatoses inflamatórias.
Lúpus eritematoso cutâneo subagudo
Os achados de IFD são semelhantes aos do LECC, com positividade entre 54% e 100% dos casos. Entretanto, a fluorescência da ZMB, geralmente, é granulosa e ocorre ocasional fluorescência dos núcleos dos queratinócitos, o fenômeno FAN in vivo.3,22,28
Lúpus eritematoso sistêmico
No lúpus eritematoso sistêmico (LES), os depósitos de imunorreactantes (teste da banda lúpica = TBL)37 são de fundamental importância no diagnóstico e prognóstico da doença, quando associados aos achados clínicos e testes sorológicos. Como teste diagnóstico, o TBL apresenta sensibilidade de 60% a 90% na pele normal fotoexposta de doentes com LES, em comparação com as áreas não fotoexpostas (40%-60%). A área recomendada atualmente consiste na área deltoídea ou porção dorsal do antebraço. Como teste prognóstico, o TBL deve ser realizado em área não exposta de pele normal (região glútea ou porção flexora do antebraço).
Num estudo de Gilliam et al.38 envolvendo 42 doentes com LES, 55% deles apresentaram depósitos de imunoglobulinas na pele não envolvida (LBT). LBT foi positiva em 70% dos doentes com LE renal e em 31% dos LEs sem agressão renal.
Os depósitos de imunocomplexos envolvem diversas imunoglobulinas, associadas ou não ao C3. A associação mais frequente é de IgG/IgM. Também pode ocorrer fluorescência na parede dos vasos dérmicos, anexos e presença de fluorescência nos núcleos dos queratinócitos.3,28
B- IMUNOFLUORESCÊNCIA INDIRETA
A imunofluorescência indireta (IFI) apresenta um importante auxílio diagnóstico nas dermatoses vesicobolhosas autoimunes (DVB), como também permite a avaliação de auto-anticorpos circulantes, sendo, muitas vezes, possível a correlação clínico-laboratorial dos doentes.
A técnica de IFI aplicada a estudos de anticorpos circulantes nas DVBs utiliza como substrato o epitélio normal. Os substratos variam de acordo com os protocolos de cada laboratório, mas, em nosso meio, a pele normal humana obtida de prepúcio, mama ou pálpebra é considerada ideal (fácil obtenção, boa antigenicidade), substituindo o esôfago de macaco (Figura 7).
Um exemplo de protocolo de IFI é assim descrito: a pele é criosseccionada a 4m e os fragmentos são colocados em lâminas silanizadas. Após a incubação do soro diluído do doente (a partir de 1:20) com o substrato por 30 minutos, à temperatura ambiente em câmara úmida, segue-se a lavagem com o tampão trizma base/cálcio (TBS Ca2+). A reação é revelada por anticorpos secundários anti-humanos (IgG, IgA, IgM e C3), produzidos em coelhos, murinos ou caprinos, e conjugados ao isotiocianato de fluoresceína (FITC). A leitura da reação é realizada no microscópio de epiluminescência. Em testes quantitativos, o título resultante é aquele onde ainda se detecta a fluorescência no substrato.3,5
Dermatoses bolhosas intraepidérmicas: pênfigos
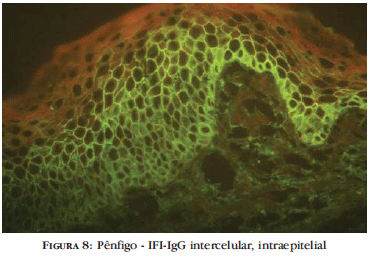
À semelhança da IFD, a IFI nos pênfigos apresenta fluorescência intercelular, de padrão linear, intraepitelial (Figura 8).
Pênfigo foliáceo
IFI: O pênfigo foliáceo (PF) clássico e o endêmico (PFE) revelam o mesmo padrão intercelular de fluorescência, que se apresenta como linear, intercelular, intraepitelial. Os autoanticorpos da classe IgG dirigem-se contra a desmogleína 1 (Dsg1 - glicoproteína de 160kDa), o seu principal autoantígeno.5,38 A sensibilidade da IFI é de 90%-100%.3,5 No PF invasivobolhoso ou eritrodérmico, os títulos de IFI podem ser elevados (>1:5120).
A subclasse dominante de IgG no PFE é a IgG4 . Autoanticorpos das subclasses IgG1 e IgG2 são detectados em baixos títulos nos doentes em remissão e em indivíduos sadios habitantes de áreas endêmicas, enquanto a IgG3 está ausente.5,13,39 A IgG4 é um isótipo patogênico capaz de induzir o PFE em modelo experimental. Estudos demonstraram que a IgG4 em baixos títulos na IFI pode ser encontrada em 56% dos doentes de PFE em remissão clínica, o que pode representar maior possibilidade de reativação da enfermidade, caso esses autoanticorpos estejam se dirigindo contra os epítopos patogênicos extracelulares da Dsg1 (EC 1-2). 40
Pênfigo vulgar
No PV, os autoanticorpos da classe IgG dirigem-se à desmogleína 3 (Dsg3), autoantígeno de maior expressão nos epitélios escamosos. Quando há lesões mucocutâneas, os doentes podem apresentar, também, anticorpos contra a Dsg1.14,41
IFI: Padrão de fluorescência semelhante ao PF. Apresentam de 75% a 100% de positividade para anticorpos antiepiteliais da classe IgG. Também ocorre predomínio de IgG4 na doença ativa.5,14-15,41
Pênfigo paraneoplásico
No pênfigo paraneoplásico (PNP) existe um reconhecimento de autoantígenos do epitélio vesical murino em 83% dos casos (Figura 9). Nos casos suspeitos, com a IFI negativa (epitélio vesical murino), são necessárias outras provas imunológicas, como a imunoprecipitação, para afastar o diagnóstico de PNP. No PF e no PV, a IFI utilizando como substrato o epitélio vesical murino é usualmente negativa, mas existem doentes, especialmente os de PV com predomínio de lesões mucosas, que apresentam reatividade contra a desmoplaquina1.17-18,42
Pênfigo por IgA
IFI: Caracteriza-se por depósitos de IgA intercelulares intraepidérmicos, sendo positiva em cerca de 50% dos casos.19-20
Dermatoses bolhosas subepidérmicas
Penfigoide bolhoso
IFI: Revela anticorpos circulantes da classe IgG anticolágeno XVII (BP180) em 70% dos pacientes. Parece não haver correlação entre o título de anticorpos e a extensão ou atividade da doença.3,28,43
Epidermólise bolhosa adquirida/Lúpus eritematoso sistêmico bolhoso
IFI: Revela anticorpos IgG circulantes anti-ZMB em 25%-50% dos doentes. Não há correlação dos títulos de anticorpos com a extensão ou atividade da doença. O padrão de fluorescência para EBA é similar ao do PB. A técnica de salt-split skin permite diferenciá-las, por meio da localização da fluorescência.
IFI: Salt-split Skin
A técnica de salt-split skin (SS) foi desenvolvida em 198444 e permitiu aumentar a sensibilidade da detecção de anticorpos anti-ZMB nas DVBs subepidérmicas, quando comparada com o substrato (pele) não clivado.
A técnica de SS consiste em incubar a pele normal humana em solução de cloreto de sódio a 1,0M (NaCl 1,0M) por 72 horas, a 4ºC, com uma troca diária da solução durante esse período. Dessa forma, o split, ou separação artificial da pele, é induzido na área da lâmina lúcida da ZMB. O splitting separa os autoantígenos do PB e do EBA. O lado epidérmico contém os antígenos associados ao hemidesmossomo (plectina, antígeno do PB-BP 230) e o lado dérmico consiste em laminina 5 (abaixo da lâmina lúcida) e colágenos tipos IV (lâmina densa) e VII (fibrilas de ancoragem).
Cerca de 85% dos soros de pacientes tipicamente com PB mostram ligação de anticorpos da classe IgG aos antígenos-alvo na área do teto da bolha (lado epidérmico) ou em ambos os lados da clivagem em 15% dos casos (Figura 10A). Isso ocorre devido à localização dos antígenos de PB, que estão presentes no hemidesmossomo (BPGA1) ou na região da lâmina lúcida (BPGA2-BP180 ou colágeno XVIIa).44
Nos doentes com EBA ou LESB, há reatividade no assoalho da bolha (lado dérmico), pois o colágeno tipo VII localiza-se nas fibrilas de ancoragem, na região da sublâmina densa (Figura 10B). EBA apresenta cerca de 50% de positividade no SS.
Penfigoide das membranas mucosas
O autoantígeno principal do penfigoide das membranas mucosas (PMM) é a laminina 5 (calinina), mas o BP180 e a proteína a6b4 também são citados.
IFI: Raramente positiva, em torno de 10% dos pacientes com anti-IgG contra a ZMB. O melhor substrato é a mucosa humana (oral ou vaginal) sadia.3,28
SS: Positividade no lado epidérmico e dérmico da clivagem.27,28
Penfigoide gestacional ou herpes gestacional
O herpes gestacional (HG) é considerado uma forma particular de PB que aparece durante a gestação.
IFI: Anticorpos da subclasse IgG1 circulantes de 10%-20% dos casos. Os soros desses pacientes contêm anticorpos anti-ZMB fixadores de complemento, referido como fator HG. No SS, usualmente, apresentam fluorescência no lado epidérmico da clivagem.28
Fator HG: É uma técnica de IFI amplificada, em que se adiciona uma fonte de complemento (soro humano normal fresco). É utilizado em situações de dúvida diagnóstica e aumenta a sensibilidade da IFI no HG para 50%.28
Dermatose bolhosa por IgA linear
IFI: Anticorpos circulantes da classe IgA são raros (7% a 30% dos casos) e a IFI deve ser realizada para afastar outras dermatoses, como o PB.3,28,30
SS: Positivo no lado epidérmico em 60%-70% dos casos.3,30
Dermatite herpetiforme
IFI: Geralmente, negativa para anticorpos circulantes da classe IgA.
Como conclusão, pode-se considerar a imunofluorescência (direta e indireta) como um método sensível e específico de detecção de autoanticorpos in situ e circulantes nas dermatoses vesicobolhosas autoimunes; nas dermatoses inflamatórias, pode ser um recurso laboratorial auxiliar para o diagnóstico definitivo da enfermidade em investigação. 
Aprovado pelo Conselho Editorial e aceito para publicação em 31.07.2009
Conflito de interesse: Nenhum
Suporte financeiro: CNPq-processo 303493/2008-9 e CNPq-processo 803070/87.0
Este artigo sofreu alterações por solicitação do editor em Nov/2010 conforme ERRATA publicada no Volume 85 Número 6 do periódico. [Link]
- 1. Coons AH, Creech HJ, Jones RN, Berliner E. The Demonstration of Pneumococcal Antigen in Tissues by the Use of Fluorescent Antibody. J Immunol. 1942;45:159-70.
- 2. Beutner EH. The development of immunofluorescence and the immunopathology of the skin. Int J Dermatol. 2003;42:99-109.
- 3. Aoki V. Imunofluorescência, immunoblotting e imunoprecipitação. In: Sampaio SA, Rivitti E, eds. Dermatologia. 3 ed. Sao Paulo: Artes Médicas; 2007. p.127-38.
- 4. Beutner EH, Jordon RE. Demonstration of Skin Antibodies in Sera of Pemphigus Vulgaris Patients by Indirect Immunofluorescent Staining. Proc Soc Exp Biol Med. 1964;117:505-10.
- 5. Aoki V, Huang MH, Perigo AM, Fukumori LM, Maruta CW, Santi CG, et al. Endemic pemphigus foliaceus (fogo selvagem) and pemphigus vulgaris: immunoglobulin G heterogeneity detected by indirect immunofluorescence. Rev Hosp Clin Fac Med Sao Paulo. 2004;59:251-6.
- 6. Jordon RE, Beutner EH, Witebsky E, Blumental G, Hale WL, Lever WF. Basement zone antibodies in bullous pemphigoid. JAMA. 1967;29;200:751-6.
- 7. Mutasim DF, Pelc NJ, Supapannachart N. Established methods in the investigation of bullous diseases. Dermatol Clin. 1993;11:399-418.
- 8. Santi CG, Maruta CW, Aoki V, Sotto MN, Rivitti EA, Diaz LA. Pemphigus herpetiformis is a rare clinical expression of nonendemic pemphigus foliaceus, fogo selvagem, and pemphigus vulgaris. Cooperative Group on Fogo Selvagem Research. J Am Acad Dermatol. 1996;34:40-6.
- 9. Morrison LH. When to request immunofluorescence: practical hints. Semin Cutan Med Surg. 1999;18:36-42.
- 10. Mihai S, Sitaru C. Immunopathology and molecular diagnosis of autoimmune bullous diseases. J Cell Mol Med. 2007;11:462-81.
- 11. Hans-Filho G, dos Santos V, Katayama JH, Aoki V, Rivitti EA, Sampaio SA, et al. An active focus of high prevalence of fogo selvagem on an Amerindian reservation in Brazil. Cooperative Group on Fogo Selvagem Research. J Invest Dermatol. 1996;107:68-75.
- 12. Rivitti EA, Sanches JA, Miyauchi LM, Sampaio SA, Aoki V, Diaz LA. Pemphigus foliaceus autoantibodies bind both epidermis and squamous mucosal epithelium, but tis sue injury is detected only in the epidermis. The Cooperative Group on Fogo Selvagem Research. J Am Acad Dermatol. 1994;31:954-8.
- 13. Warren SJ, Arteaga LA, Rivitti EA, Aoki V, Hans-Filho G, Qaqish BF, et al. The role of subclass switching in the pathogenesis of endemic pemphigus foliaceus. J Invest Dermatol. 2003;120:104-8.
- 14. Ding X, Aoki V, Mascaro JM Jr., Lopez-Swiderski A, Diaz LA, Fairley JA. Mucosal and mucocutaneous (generalized) pemphigus vulgaris show distinct autoantibody profiles. J Invest Dermatol. 1997;109:592-6.
- 15. Bhol K, Natarajan K, Nagarwalla N, Mohimen A, Aoki V, Ahmed AR. Correlation of peptide specificity and IgG subclass with pathogenic and nonpathogenic autoantibodies in pemphigus vulgaris: a model for autoimmunity. Proc Natl Acad Sci U S A. 1995;92:5239-43.
- 16. Jablonska S, Chorzelski TP, Beutner EH, Chorzelska J. Herpetiform pemphigus, a variable pattern of pemphigus. Int J Dermatol. 1975;14:353-9.
- 17. Anhalt GJ, Kim SC, Stanley JR, Korman NJ, Jabs DA, Kory M, et al. Paraneoplastic pemphigus. An autoimmune mucocutaneous disease associated with neoplasia. N Engl J Med. 1990;323:1729-35.
- 18. Hashimoto T. Immunopathology of paraneoplastic pemphigus. Clin Dermatol. 2001;19:675-82.
- 19. Hashimoto T, Kiyokawa C, Mori O, Miyasato M, Chidgey MA, Garrod DR, et al. Human desmocollin 1 (Dsc1) is an autoantigen for the subcorneal pustular dermatosis type of IgA pemphigus. J Invest Dermatol. 1997;109:127-31.
- 20. de Oliveira JP, Gabbi TV, Hashimoto T, Aoki V, Santi CG, Maruta CW, et al. Two Brazilian cases of IgA pemphigus. J Dermatol. 2003;30:886-91.
- 21. Velthuis PJ, Kater L, van der Tweel I, Meyling FG, Derksen RH, Hene RJ, et al. In vivo antinuclear antibody of the skin: diagnostic significance and association with selective antinuclear antibodies. Ann Rheum Dis. 1990;49:163-7.
- 22. Sousa JX Jr, Miyamoto D, Zimbres JM, Costa DV, Aoki V. Clinicopathological evaluation of in vivo epidermal nuclear fluorescence. Clin Exp Dermatol. 2009;34:314-8.
- 23. Giudice GJ, Emery DJ, Zelickson BD, Anhalt GJ, Liu Z, Diaz LA. Bullous pemphigoid and herpes gestationis autoantibodies recognize a common non-collagenous site on the BP180 ectodomain. J Immunol. 1993;151:5742-50.
- 24. Katz SI, Hertz KC, Yaoita H. Herpes gestationis. Immunopathology and characterization of the HG factor. J Clin Invest. 1976;57:1434-41.
- 25. Morrison LH, Labib RS, Zone JJ, Diaz LA, Anhalt GJ. Herpes gestationis autoantibodies recognize a 180-kD human epidermal antigen. J Clin Invest. 1988;81:2023-6.
- 26. Chan LS, Ahmed AR, Anhalt GJ, Bernauer W, Cooper KD, Elder MJ, et al. The first international consensus on mucous membrane pemphigoid: definition, diagnostic criteria, pathogenic factors, medical treatment, and prognostic indicators. Arch Dermatol. 2002;138:370-9.
- 27. Leverkus M, Schmidt E, Lazarova Z, Brocker EB, Yancey KB, Zillikens D. Antiepiligrin cicatricial pemphigoid: an underdiagnosed entity within the spectrum of scarring autoimmune subepidermal bullous diseases? Arch Dermatol. 1999;135:1091-8.
- 28. Mutasim DF, Adams BB. Immunofluorescence in dermatology. J Am Acad Dermatol. 2001; 45:803-22; quiz 22-4.
- 29. Woodley DT, Burgeson RE, Lunstrum G, Bruckner-Tuderman L, Reese MJ, Briggaman RA. Epidermolysis bullosa acquisita antigen is the globular carboxyl terminus of type VII procollagen. J Clin Invest. 1988;81:683-7.
- 30. Wojnarowska F, Marsden RA, Bhogal B, Black MM. Chronic bullous disease of childhood, childhood cicatricial pemphigoid, and linear IgA disease of adults. A comparative study demonstrating clinical and immunopathologic overlap. J Am Acad Dermatol. 1988;19:792-805.
- 31. Marinkovich MP, Taylor TB, Keene DR, Burgeson RE, Zone JJ. LAD-1, the linear IgA bullous dermatosis autoantigen, is a novel 120-kDa anchoring filament protein synthesized by epidermal cells. J Invest Dermatol. 1996;106:734-8.
- 32. Beutner EH, Chorzelski TP, Reunala TL, Kumar V. Immunopathology of dermatitis herpetiformis. Clin Dermatol. 1991;9:295-311.
- 33. Zone JJ. Skin manifestations of celiac disease. Gastroenterology. 2005;128(4 Suppl 1):S87-91.
- 34. Van Hale HM, Gibson LE, Schroeter AL. Henoch-Schonlein vasculitis: direct immunofluorescence study of uninvolved skin. J Am Acad Dermatol. 1986;15(4 Pt 1):665-70.
- 35. de la Faille-Kuyper EH, de la Faille HB. An immunofluorescence study of lichen planus. Br J Dermatol. 1974;90:365-71.
- 36. Kulthanan K, Jiamton S, Varothai S, Pinkaew S, Sutthipinittharm P. Direct immunofluorescence study in patients with lichen planus. Int J Dermatol. 2007;46:1237-41.
- 37. Burnham TK, Neblett TR, Fine G.. Immunofluorescent "band" test for lupus erythematosus. II. Employing skin lesions. Arch Dermatol. 1970;102:42-50.
- 38. Gilliam JN, Cheatum DE, Hurd ER, Stastny P, Ziff M. Immunoglobulin in clinically uninvolved skin in systemic lupus erythematosus: association with renal disease. J Clin Invest. 1974;53:1434-40.
- 39. Aoki V, Rivitti EA, Ito LM, Hans-Filho G, Diaz L. Perfil historico da imunopatogenia do pênfigo foliaceo endemico (fogo selvagem)* Historical profile of the immunopathogenesis of endemic pemphigus foliaceus (fogo selvagem)*. An Bras Dermatol. 2005;80:287-92.
- 40. Li N, Aoki V, Hans-Filho G, Rivitti EA, Diaz LA. The role of intramolecular epitope spreading in the pathogenesis of endemic pemphigus foliaceus (fogo selvagem). J Exp Med. 2003;197:1501-10.
- 41. Ishii K, Amagai M, Hall RP, Hashimoto T, Takayanagi A, Gamou S, et al. Characterization of autoantibodies in pemphigus using antigen-specific enzyme-linked immunosorbent assays with baculovirus-expressed recombinant desmogleins. J Immunol. 1997;159:2010-7.
- 42. Mimouni D, Foedinger D, Kouba DJ, Orlow SJ, Rappersberger K, Sciubba JJ, et al. Mucosal dominant pemphigus vulgaris with anti-desmoplakin autoantibodies. J Am Acad Dermatol. 2004;51:62-7.
- 43. Lessey E, Li N, Diaz L, Liu Z. Complement and cuta neous autoimmune blistering diseases. Immunol Res. 2008;41:223-32.
- 44. Gammon WR, Briggaman RA, Inman AO 3rd, Queen LL, Wheeler CE. Differentiating anti-lamina lucida and antisublamina densa anti-BMZ antibodies by indirect immunofluorescence on 1.0 M sodium chloride-separated skin. J Invest Dermatol. 1984;82:139-44.
Datas de Publicação
-
Publicação nesta coleção
16 Fev 2011 -
Data do Fascículo
Ago 2010
Histórico
-
Recebido
31 Jul 2009