Resumos
O Fator de Proteção Solar (FPS) é o principal dado para quantificação da eficácia fotoprotetora de um filtro solar, sendo universalmente aceito. Seu método é baseado na determinação da Dose Eritematosa Mínima (DEM), definida como sendo a menor quantidade de energia necessária para o desencadeamento de eritema, em áreas de pele protegidas e não protegidas pelo produto em estudo. O valor do FPS é, então, calculado como a razão numérica entre a DEM da pele protegida e a da pele não protegida. A primeira publicação demonstrando um método para determinação do valor do FPS foi apresentada em 1978 pela agência norte-americana FDA, seguida por outras publicações do próprio FDA e de outras agências regulatórias internacionais. Apesar de ser considerado o método referência para quantificação da eficácia fotoprotetora de produtos tópicos, existem controvérsias na literatura acerca do método para determinação do FPS e sobre as implicações das reais condições de uso na proteção atingida na prática pelos usuários
Dermatologia; Queimadura solar; Protetores de raios solares
The Sun Protection Factor (SPF) is the most important data to quantify the effectiveness of a sunscreen, being universally accepted. The method is based on determining the minimum erythematous dose (MED), defined as the smallest amount of energy required for triggering the erythema, in areas of protected and unprotected skin. The SPF value is then calculated as the ratio between the MED of protected and unprotected skin. The first publication of a method for determining the SPF was presented in 1978 by the U.S. FDA agency, followed by other publications of FDA and other international regulatory agencies. Although considered the reference method for quantification of sunscreen efficacy of topical products, there are controversies in literature about the method for determining the SPF and the implications of the real conditions of use in the protection achieved in practice by users
Dermatology; Solar radiation; Sunscreening agents
REVISÃO
Fator de proteção solar: significado e controvérsias* * Trabalho realizado em clínica privada - São Paulo (SP), Brasil.
Sergio SchalkaI; Vitor Manoel Silva dos ReisII
IMestre em Dermatologia - Professor-associado de Dermatologia - Universidade de Santo Amaro (UNISA) - São Paulo (SP), Brasil
IIDoutor em Dermatologia - Professor de Dermatologia da Faculdade de Medicina da Universidade de São Paulo (FMUSP) - São Paulo (SP), Brasil
Endereço para correspondência Endereço para correspondência: Sergio Schalka Av. Dr. Carlos de M. Barros, 304 06023 000 Osasco (SP) - Brasil schalka@terra.com.br
RESUMO
O Fator de Proteção Solar (FPS) é o principal dado para quantificação da eficácia fotoprotetora de um filtro solar, sendo universalmente aceito. Seu método é baseado na determinação da Dose Eritematosa Mínima (DEM), definida como sendo a menor quantidade de energia necessária para o desencadeamento de eritema, em áreas de pele protegidas e não protegidas pelo produto em estudo. O valor do FPS é, então, calculado como a razão numérica entre a DEM da pele protegida e a da pele não protegida. A primeira publicação demonstrando um método para determinação do valor do FPS foi apresentada em 1978 pela agência norte-americana FDA, seguida por outras publicações do próprio FDA e de outras agências regulatórias internacionais. Apesar de ser considerado o método referência para quantificação da eficácia fotoprotetora de produtos tópicos, existem controvérsias na literatura acerca do método para determinação do FPS e sobre as implicações das reais condições de uso na proteção atingida na prática pelos usuários.
Palavras-chave: Dermatologia; Queimadura solar; Protetores de raios solares
INTRODUÇÃO
Sempre fez parte da natureza humana proteger a pele contra a queimadura solar por meio do uso de roupas e acessórios ou pela simples não exposição ao sol. Os primeiros relatos científicos sobre a tentativa do uso de agentes fotoprotetores surgem no final do século XIX, com substâncias de efeito bastante limitado.1
Em 1891, Friedrich Hammer11 publicou a primeira monografia em fotobiologia, em que discutia a fotoproteção e o uso de diferentes produtos na prevenção da queimadura solar (1891 apud Roelandts,1 2007, p.5).
Em 1928, surge o primeiro filtro solar comercialmente disponível, nos Estados Unidos da América, uma emulsão contendo benzil-salicilato e benzil-cinamato.2 Nos anos subsequentes, entretanto, pouca atenção foi dada a agentes fotoprotetores, sendo seu uso bastante restrito.
Durante a segunda guerra mundial, pela necessidade de fotoproteção adequada para os soldados norte-americanos em frentes de batalha nos países tropicais, foi utilizado o petrolatum vermelho como equipamento de proteção padrão.1
Em 1943, o ácido para-aminobenzoico (PABA) foi patenteado como o primeiro filtro solar estabelecido, marcando uma nova etapa da fotoproteção.2
Somente durante a década de 70 do século passado, entretanto, a popularização dos fotoprotetores ocorreu, com a incorporação de diferentes filtros UVB em cremes e loções.3
O uso de filtros UVA iniciou-se efetivamente em 1979, mas somente a introdução das partículas inorgânicas dióxido de titânio, em 1989, e óxido de zinco, em 1992, levou a uma proteção mais efetiva nesta faixa.2
A definição clássica de protetor solar, segundo Pathak,4 é produto destinado a bloquear o sol e a proteger ou abrigar células viáveis da pele contra efeitos potencialmente danosos da radiação ultravioleta, como a queimadura solar e o câncer de pele.
Pelos conceitos atuais, fotoprotetores tópicos, ou protetores solares (ou ainda filtros solares), são substâncias de aplicação cutânea em diferentes apresentações que contenham em sua formulação ingredientes capazes de interferir na radiação solar, reduzindo seus efeitos deletérios.5
Os filtros ultravioleta (filtros UV) são os ingredientes presentes nos fotoprotetores que apresentam a capacidade de interagir com a radiação incidente, através de 3 mecanismos básicos: reflexão, dispersão e absorção, conforme apresentado na figura 1.6
Os filtros UV podem ser divididos em filtros inorgânicos (físicos) ou orgânicos (químicos), dependendo de suas características físico-químicas.7
Os filtros inorgânicos são partículas de óxidos metálicos8 capazes de, por mecanismo óptico, refletir ou dispersar a radiação incidente. Seus principais representantes são o óxido de zinco (ZnO) e o dióxido de titânio (TiO2), utilizados habitualmente em associação com os filtros orgânicos. As principais características dos filtros inorgânicos são sua baixa permeação cutânea e sua elevada fotoestabilidade, ou seja, a capacidade do filtro de manter sua capacidade fotoprotetora mesmo após longos períodos de radiação solar.7
Por outro lado, os filtros orgânicos são moléculas que interferem na radiação incidente por meio do mecanismo de absorção, quando o filtro atua como cromóforo exógeno ao absorver um phóton de energia e evoluir para o estado excitado da molécula. Ao retornar para o estado estável (não excitado), ocorre a liberação de energia em um comprimento de onda mais longo, seja na faixa da luz visível (como fluorescência), seja na faixa da radiação infravermelha (como calor). O processo pode repetir-se inúmeras vezes pelo mecanismo denominado ressonância. Dependendo da capacidade de absorver comprimentos de onda mais curtos ou mais longos, os filtros orgânicos podem ser subclassificados em filtros UVA, filtros UVB e filtros de amplo espectro (UVA e UVB).9
A legislação norte-americana (FDA 99)10 classifica os protetores solares como medicamentos não prescritivos e relaciona 16 substâncias aprovadas como filtros UV, permitidas para uso em fotoprotetores.
No Brasil, a Agência Nacional de Vigilância Sanitária (ANVISA)11 define os protetores solares como produtos cosméticos e apresenta a relação de filtros ultravioleta permitidos, contendo 38 ingredientes ativos.
O desenvolvimento e o uso do fotoprotetor tópico sempre esteve relacionado à prevenção dos efeitos agudos da radiação solar, particularmente a queimadura solar.4
Foi somente depois da década de 80 do século passado, com os estudos demonstrando o papel do ultravioleta no desenvolvimento de neoplasias cutâneas, que o protetor solar passou a ser entendido não somente como agente contra a queimadura solar, mas também como elemento importante na prevenção do dano actínico crônico, particularmente em relação ao desenvolvimento de neoplasias cutâneas.4
Diferentes estudos demonstram que o protetor solar tem efeito protetor contra o dano actínico crônico.
O uso regular de fotoprotetores pode reduzir o número de queratoses actínicas.12,13
Segundo Green,14 somente o carcinoma espinocelular, e não o basocelular, pode ser evitado pelo uso regular de fotoprotetores.
Vainio,15 em publicação recente, conclui que o uso diário de fotoprotetores reduz o risco do desenvolvimento de carcinoma espinocelular.
Fourtanier16 apresentou trabalho realizado em ratos, demonstrando superioridade do uso de protetores solares de amplo espectro em comparação a outros que não são de amplo espectro, na proteção ao dano do DNA e na prevenção da fotocarcinogênese, retardando o desenvolvimento do tumor.
O uso de protetores solares também foi reportado como capaz de prevenir o desenvolvimento do câncer cutâneo desencadeado por UV, por meio do decréscimo da formação dos dímeros da pirimidinaciclobutano, além de prevenir outros efeitos imunológicos induzidos por ultravioleta, como a supressão da hipersensibilidade de contato.7
O estudo apresentado por Hayag,17 em 1997, conclui que a aplicação de protetor solar com FPS 30, antes da exposição solar, pode prevenir o decréscimo de células de Langerhans no sítio irradiado e atenuar a supressão induzida por UV na hipersensibilidade de contato ao dinitroclorobenzeno (DNCB).
Em relação ao uso de protetores solares e o risco de desenvolvimento de melanoma, a literatura ainda apresenta alguma controvérsia.
Huncharek e Kupelnick18 publicaram meta-análise de onze estudos publicados, mostrando que o uso de fotoprotetores apresenta somente pequena vantagem em relação à redução do risco de desenvolvimento de melanoma.
Rigel,19 entretanto, revisando somente os artigos mais recentemente publicados, em que somente protetores solares de alto FPS foram utilizados, conclui que o uso destes produtos parece oferecer um efeito protetor evidente em relação ao risco de melanoma. Diffey20 apresentou em 2005 uma revisão sobre o assunto, em que o autor conclui que a melhora recente na eficácia de protetores solares modernos oferecerá um benefício adicional como agente protetor contra o melanoma, resultado este, entretanto, que não poderá ser visto ainda nas próximas décadas.
Com isso, e também com a percepção do efeito deletério da radiação UVA em diferentes fotodermatoses, no desenvolvimento de neoplasias cutâneas, na fotoimunosupressão e no fotoenvelhecimento, novos filtros ultravioleta foram desenvolvidos, com maior capacidade fotoprotetora na faixa UVB e com amplo espectro de absorção nas faixas UVA e UVB, levando a um salto em termos de eficácia fotoprotetora, particularmente do valor do Fator de Proteção Solar (FPS).20
O valor médio do FPS de produtos utilizados na Europa em 1984 era de 4 a 6, evoluindo para 6 a 10 em 1987 e para cerca de 15 em 1997, demonstrando a recente evolução dos fotoprotetores.20
De acordo com a Agência Internacional para Pesquisa em Câncer (IARC),21 apesar de inadequada evidência de que os fotoprotetores apresentem um papel protetor contra o CBC e o melanoma, e somente limitada evidência de que previna o CEC, o uso de protetor solar deve ser considerado como parte de um programa completo de fotoproteção.
Para uma melhor eficácia fotoprotetora, o protetor solar deve apresentar em sua composição filtros ultravioleta com espectro de absorção na faixa da radiação UVA e UVB e ser fotoestável. Além disso, para o efeito protetor ideal, o produto deve ser capaz de formar um filme homogêneo, capaz de distribuir seus ingredientes de forma regular em toda a superfície cutânea.9
Fator de Proteção Solar - Aspectos Históricos
O primeiro relato acerca da avaliação da eficácia protetora dos protetores solares foi feito por Friedrich Ellinger em 1934,22 em que o autor realizava a determinação da Dose Eritematosa Mínima na pele protegida e não protegida, utilizando ambos os antebraços e lâmpada de mercúrio e propunha um coeficiente de proteção que decrescia em valor na medida em que a proteção aumentava.
Em 1956, Rudolf Schulze23 propôs a avaliação de fotoprotetores comercialmente disponíveis, calculando um fator de proteção, posteriormente denominado de "Fator Schulze", em que o autor dividia o tempo de exposição necessário para a indução de eritema com o protetor pelo tempo necessário para a produção de eritema sem o protetor, utilizando doses de radiação progressivas emitidas por lâmpadas com espectro de radiação mais próximo ao da luz solar. O método Schulze foi utilizado durante décadas em países europeus como referência na avaliação de protetores solares.
Somente em 1974, o termo Fator de Proteção Solar (FPS) foi introduzido por Greiter,24 sendo apenas nova denominação do já conhecido "método Schulze".
O Fator de Proteção Solar, proposto por Greiter, tornou-se rapidamente popular e passou a ser utilizado em todo o mundo. Entretanto, pela falta de padronização do método, os valores numéricos encontrados e utilizados nos fotoprotetores apresentavam grande variação, não conferindo confiabilidade ao método.25
Em 1978, a agência regulatória norte-americana FDA propôs a primeira normatização para a determinação do Fator de Proteção Solar (FPS).26
Fator de Proteção Solar - Conceito e Métodos Internacionais
O Fator de Proteção Solar pode ser definido, conforme proposto pelo FDA em 1978,26 como sendo a razão numérica entre a Dose Eritematosa Mínima (DEM) da pele protegida pelo fotoprotetor em questão, aplicado na quantidade de 2 mg/cm2, e a Dose Eritematosa Mínima da pele não protegida, numa relação matemática que pode ser apresentada conforme equação abaixo:
FPS = DEM (pele protegida) / DEM (pele não protegida)
Para a determinação do valor do FPS, um grupo de 10 a 20 voluntários (conforme o método de referência), de fototipos I a III (classificação de Fitzpatrick27), são selecionados e submetidos a doses progressivas de radiação ultravioleta emitidas por uma fonte artificial de luz, denominada simulador solar, em áreas de pele não protegida e pele protegida pelo protetor solar em estudo, aplicado na quantidade de 2 mg/cm2. Após cerca de 16 a 24 horas da exposição, é realizada a leitura da Dose Eritematosa Mínima nas duas áreas e calculada a sua razão (Figura 2). A média dos valores encontrados no grupo de voluntários é o Fator de Proteção Solar do produto.
Após a publicação do método pelo FDA em 1978, novos métodos foram propostos por agências regulatórias internacionais.
A agência alemã Deutches Institut für Normung (DIN) apresentou nova versão do método, em 1984, denominada norma DIN 67501, então utilizada em toda a Europa.25 As diferenças metodológicas entre ambas eram grandes e se referiam, principalmente, à fonte emissora de ultravioleta (lâmpada de arco xenônio para metodologia FDA e luz natural ou lâmpada de mercúrio para norma DIN) e a quantidade aplicada de protetor solar em estudo (2,0 mg/cm2 para metodologia FDA e 1,5 mg/cm2 para norma DIN).25
Todas as publicações que se seguiram mantive-ram os conceitos metodológicos descritos pela monografia apresentada pelo FDA em 1978, com o uso da lâmpada de arco xenônio como fonte emissora e a quantidade de 2,0 mg/cm2 como quantidade padrão a ser aplicada do produto-teste.
Após a primeira publicação, ocorrida em 1978,26 a agência norte-americana FDA produziu a proposta de monografia final em 199328 e, finalmente, a monografia final, em 1999.10 Atualmente, está em discussão uma nova revisão metodológica, proposta pelo FDA no final de 2007.29
Além da ação do FDA, outras instituições e agências regulatórias internacionais produziram monografias técnicas descrevendo os procedimentos necessários para a realização do estudo clínico para avaliação de eficácia fotoprotetora por meio da determinação do Fator de Proteção Solar.25
A comunidade europeia, por meio da Associação Europeia da Indústria de Cosméticos, Higiene Pessoal e Perfumaria (Comité de Liason des Associations Européenes de lndustrie et de la Parfumerie - COLIPA) desenvolveu sua primeira versão de monografia em 1994.30
Em 2003, o método denominado International Sun Protection Factor Test Method (ISPF) foi apresentado conjuntamente pelas associações Europeia (COLIPA), Japonesa (JCIA) e Sul Africana (CTFA-SA),31 seguido posteriormente por uma revisão em 2006, com a introdução da Associação da Indústria Cosmética Norte-Americana (CTFA-USA).32
As metodologias norte-americana (FDA) e europeia (COLIPA ou Internacional) tornaram-se referência para a determinação do Fator de Proteção Solar (FPS) em diferentes países, dentre os quais o Brasil, que, por meio da resolução RDC 237, editada pela Agência Nacional de Vigilância Sanitária (ANVISA) em 2002,11 determina que todo produto denominado protetor solar deva apresentar estudos comprobatórios de sua eficácia fotoprotetora (teste para determinação de FPS) por meio de uma das duas metodologias internacionais: Metodologia FDA 199328 ou Metodologia COLIPA 199430 ou ainda de suas respectivas atualizações.
A tabela 1 apresenta todas as publicações sobre métodos para determinação do FPS apresentados pelas autoridades desde 1978.25
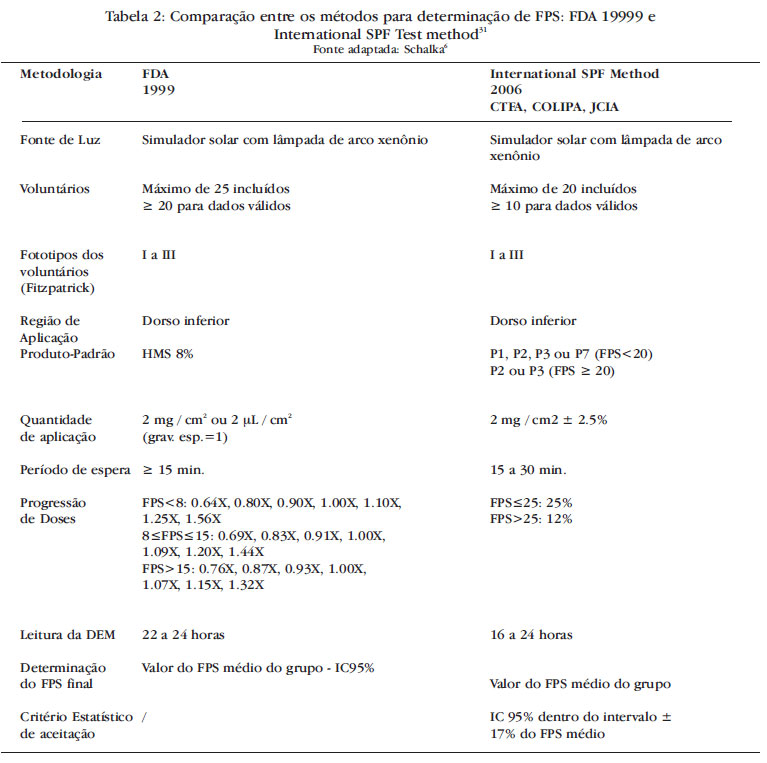
Por serem os métodos mais realizados atualmente no Brasil e nos demais países do mundo, a tabela 2 apresenta as principais características metodológicas e as principais diferenças dos métodos para determinação do FPS publicado pelo FDA 199910 (método padrão na América do Norte) e o método International Sun Protection Fator Method (ISPF) 200632 (Método-padrão na Comunidade Europeia e no Japão).
Apesar das diferenças metodológicas demonstradas na tabela 2, os estudos de FPS realizados pelos dois diferentes métodos citados (método FDA e método Internacional) produzem resultados próximos entre si. Na prática, podemos entender que os dois métodos produzem valores de FPS equivalentes.
FPS - Controvérsias
O Fator de Proteção Solar quantifica a proteção que um determinado produto é capaz de oferecer, em termos de tempo de exposição, contra a queimadura solar se comparado à exposição desprotegida.10 Assim, se um determinado protetor apresenta o valor de FPS 30, isso significa, na prática, que é necessária uma exposição solar 30 vezes maior para produzir eritema, se comparada à situação em que este usuário não estaria usando aquele protetor.
Para que pudéssemos calcular o tempo de proteção com o uso do protetor solar, teríamos de saber o tempo para produção de eritema sem o referido protetor para aquele indivíduo. Esse tempo, entretanto, sofre uma forte influência de fatores pessoais e ambientais, como a resposta eritematogênica individual (na qual o fototipo é uma tentativa de classificação), o índice ultravioleta (IUV) daquele específico dia (lembrando que o IUV é uma estimativa para o meiodia solar), o horário do dia, o índice de exposição daquela região do corpo (por exemplo, a face tem índice de 0,3, ou seja, recebe somente cerca de 30% do total da radiação) e o tipo de solo onde está o indivíduo (considerando que o índice de reflexão é variável de solo para solo e não está estimado no IUV). Por estes motivos, a tendência é não utilizar o valor do FPS para determinar tempo de exposição ao sol, mas sim, nível de proteção.
Desenvolvido há mais de trinta anos, o Fator de Proteção Solar (FPS) é o método mais aceito para avaliação da eficácia fotoprotetora dos filtros solares, sendo consagrado universalmente como a principal informação na rotulagem dos fotoprotetores. Mesmo assim, existem controvérsias em relação ao método e sua aplicabilidade nas condições reais de uso.
Por utilizar um marcador biológico com resposta individual variável, como é o eritema, o FPS é um método que pode sofrer variações em seus resultados.
Segundo Sayre,33 os pontos críticos para que o método de FPS seja repetitível e reprodutível, essenciais para a confiabilidade dos resultados, são a fonte artificial emissora de radiação ultravioleta (atualmente padronizada pelo uso da lâmpada de arco xenônio) e a quantidade de aplicação do produto no dorso do voluntário.
A COLIPA reuniu em 1992 uma força-tarefa composta por cientistas da área de fotoproteção e organizou uma validação interlaboratorial para avaliação do Fator de Proteção Solar.30 A avaliação foi realizada em diferentes etapas: em um primeiro momento, 6 laboratórios europeus receberam quatro diferentes protetores solares para determinação de seus FPS. Os resultados apresentaram uma variação no valor de FPS entre 18,2% a 37%, este último relacionado a um fotoprotetor composto somente por filtros inorgânicos. Foram identificados os seguintes pontos críticos do método:
 Quantidade e forma de aplicação do protetor solar
Quantidade e forma de aplicação do protetor solar
 Espectro e fluxo de radiação UV da fonte emissora
Espectro e fluxo de radiação UV da fonte emissora
 Leitura da Dose Eritematosa Mínima
Leitura da Dose Eritematosa Mínima
Outras duas avaliações interlaboratoriais foram realizadas na sequência,30 a fim de produzir um controle maior dos parâmetros acima descritos. Ao final, segundo conclusão do estudo, os parâmetros-chave do método, que devem ser idealmente controlados, são a quantidade e a forma de aplicação do produto.
A definição da quantidade de 2 mg/cm2 de aplicação do produto, apresentada pelo FDA em 1978, e posteriormente mantida pelas revisões do FDA, da COLIPA e do Método Internacional, baseia-se na observação de que quantidades inferiores reduzem a homogeneidade do filme protetor na pele como decorrência das irregularidades da superfície cutânea.
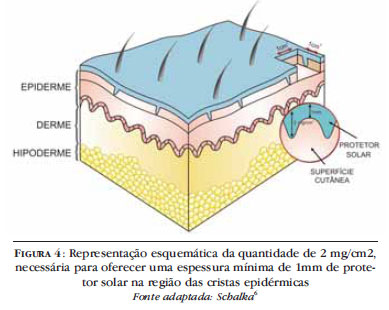
A superfície cutânea é irregular, composta por sulcos e saliências que podem apresentar maior ou menor amplitude dependendo da região do corpo.35
De forma esquemática observamos na figura 3 como se apresenta a superfície da pele.36
Segundo Brown e Diffey,34 apesar de haver uma grande variação entre os indivíduos, o volume médio necessário para um determinado produto cobrir todos os "sulcos" presentes na superfície cutânea, correspondente a 1 cm2, seria entre 1 a 2 μl. Neste caso, qualquer produto tópico, assumindo-se a densidade de 1 g/cm3, não cobriria o "topo" das cristas epidérmicas até o mínimo de 1 mg/cm2. Assim, segundo concluem os autores, seria necessária a quantidade de 2 mg/cm2 para que o protetor solar oferecesse o mínimo de 1 mm de cobertura na região dos topos das cristas epidérmicas (Figura 4).6
Apesar de recomendável, entretanto, os usuários de protetores solares não utilizam a quantidade de 2 mg/cm2 quando expostos ao sol em atividades de trabalho ou lazer.
Diferentes trabalhos publicados na literatura36-41 demonstram que a quantidade de protetor solar aplicada pelos usuários varia de 0,39 a 1,3 mg /cm2, muito inferior à aplicada no teste laboratorial para determinação do FPS, conforme recomendam os métodos internacionalmente aceitos.10,32
A interferência da quantidade aplicada no nível de proteção oferecido pelos fotoprotetores foi avaliada por diferentes autores.36,38,42,43 As conclusões destes estudos, principalmente na avaliação do padrão de interferência da quantidade aplicada na determinação do valor do FPS, são contraditórias.
Estudo recentemente publicado por Schalka S, Reis VMS e Cuce LC44 avaliou a interferência da quantidade aplicada de dois fotoprotetores (com valores de FPS 15 e 30, respectivamente) na determinação do valor do FPS, de acordo com a metodologia proposta pelo FDA em 1999,10 e concluíram que existe uma relação exponencial entre a quantidade aplicada e a variação do valor do FPS.
Os autores foram capazes de desenvolver uma equação matemática para estimar a proteção atingida pelo voluntário na prática, baseada nos dados de FPS de rotulagem e a quantidade aplicada.
A principal controvérsia, entretanto, refere-se à limitação do valor do FPS em 30, conforme sugestão do FDA publicada em 1993.28
Tal proposta fora baseada em estudo previamente publicado por Groves,45 em que os autores demonstraram, por meio de espectrofotometria e análises matemáticas, que o valor da absorbância de um determinado protetor solar pode ser relacionado ao inverso do valor do FPS, conforme equação abaixo:
A = 1 - 1/FPS
Onde A = Absorbância do produto
Aplicada tal equação, podemos desenvolver uma curva de relação entre absorbância e FPS, conforme apresentada no gráfico 1.
Como podemos observar, o ganho proporcional de absorbância em relação ao aumento do valor do FPS é reduzido drasticamente quando o valor de FPS fica acima de 30.
Esta justificativa levou o FDA a publicar, em sua proposta de monografia final em 1993,28 a limitação do FPS em 30, conceito esse que foi amplamente difundido.
Entretanto, o assunto é bastante controverso na literatura.
Osterwalder e Herzog,46 em recente artigo publicado, mostram que o raciocínio matemático proposto poderia ser realizado de forma inversa, ao se analisar o quanto de energia passa pelo protetor (transmitância) ao invés de o quanto de energia é absorvida pelo protetor (absorbância), em que:
T = 1 - A
Ao aplicar este raciocínio, percebemos que a quantidade de energia que passa através do protetor solar de FPS 60 (portanto, que atinge a pele) seria a metade daquela transmitida pelo protetor de FPS 30. Assim, a proteção oferecida pelo produto de FPS 60 seria o dobro daquela oferecida pelo produto com FPS 30, conforme vemos no gráfico 2.
Outro ponto a ser considerado é em relação ao marcador biológico relacionado ao efeito de proteção. Sabemos que o FPS quantifica a proteção contra a queimadura solar. Assim, o efeito da proteção (em termos de percentual de absorção ou transmissão), conforme descrito acima, refere-se exclusivamente à proteção quanto à produção de eritema. Não podemos afirmar, por este raciocínio, qual é o percentual de proteção contra o desenvolvimento de neoplasias cutâneas ou mesmo em relação aos efeitos da radiação UVA.
Por fim, devemos considerar a relação entre a quantidade aplicada do fotoprotetor e o FPS. Conforme já discutido acima, a quantidade aplicada é o principal fator de interferência no FPS de um determinado fotoprotetor.44 Portanto, se a aplicação do fotoprotetor for insuficiente, como ocorre na maioria dos casos, a proteção atingida pelos usuários é menor do que a apresentada no rótulo do produto e a relação entre absorbância e FPS, como proposto por Groves,45 não é mais válida.
Todos esses fatores foram considerados pelo FDA em sua proposta para emenda à monografia final de fotoprotetores, apresentada em 2007,29 e ainda não finalizada até o presente momento. Neste documento, a agência regulatória norte-americana recomenda a elevação do limite do valor do FPS para 50+, reconsiderando as observações apresentadas em 1993.
As questões relativas ao uso correto dos protetores solares, como fator essencial na efetividade do produto, têm sido destacadas na literatura internacional. Publicações recentes46,47 reforçam a necessidade de maior atenção em relação à adesão do usuário para o uso mais adequado do fotoprotetor, incluindo a aplicação da quantidade correta e a reaplicação periódica.
Segundo comentam Osterwalder e Herzog46 em seu artigo de revisão sobre o assunto: "O melhor fotoprotetor pode só oferecer proteção insuficiente se não aplicado uniformemente, em quantidade insuficiente ou se simplesmente não for aplicado".
Assim, como dito anteriormente, o valor do FPS não deve ser mais considerado em termos absolutos como o tempo de exposição adicional que o usuário poderia ser exposto ao sol antes da formação de eritema.
O conceito mais atualizado em termos de fotoproteção é considerar o valor do FPS dentro de uma faixa de proteção, como proposto pelo FDA em 200729 e apresentado na tabela 3.
A interpretação mais adequada é a de que o valor do FPS, em termos numéricos, deve ser relativa em decorrência das condições reais de uso do produto. Desta forma, não faz diferença, na prática, o uso de um protetor solar de FPS 30 ou 35, por exemplo, se de fato a aplicação não for feita de forma adequada.
CONCLUSÃO
O Fator de Proteção Solar é ainda a principal informação acerca da eficácia fotoprotetora de um filtro solar, mas a sua interpretação não deve ser baseada somente no valor numérico em si, devendo-se também considerar a adequada forma de uso do produto, em termos de quantidade aplicada e regularidade na reaplicação.
Por fim, na escolha de um agente fotoprotetor, além do FPS, os dados relativos à substantividade (resistência à água), proteção UVA e fotoestabilidade devem ser considerados para uma correta fotoproteção.
Aprovado pelo Conselho Editorial e aceito para publicação em 12.05.2010.
Conflito de interesse: Nenhum
Suporte financeiro: Nenhum
- 1. Roelandts R. History of human photobiology In: Lim HW, Hönigsmann H, Hawk JLM. Photodermatology. New York: Informa Healthcare USA; 2007. p 1-13.
- 2. Giacomoni PU. Sunprotection: Historical perspective In: Shaath NA. Sunscreens: Regulation and commercial development. 3rd ed. Boca Raton: T&F Informa; 2005. p 71-85.
- 3. Urbach F, Forbes PD, Davies RE, Berger D. Cutaneous photobiology: past, present, and future. J Invest Dermatol. 1976;67:209-24.
- 4. Pathak MA. Photoprotection against harmful effects of Solar UVB and UVA radiation: An Update. In: Lowe NJ, Shaath NA, Pathak MA. Sunscreens: Development, evaluation, and regulatory aspects, 2nd ed. New York: Marcel Dekker; 1997. p 59-79.
- 5. Osterwalder U, Lim HW. Novel developments in photoprotection: Part I. In: Lim HW, Hönigsmann H, Hawk JLM. Photodermatology. New York: Informa Healthcare USA; 2007. p 279-95.
- 6. Schalka S. Influência da quantidade aplicada de protetores solares no fator de proteção solar (FPS): avaliação de dois protetores solares com os mesmos ingredientes em diferentes concentrações [Dissertação]. São Paulo (SP): Universidade de São Paulo; 2009. 152 p.
- 7. Kullavanijaya P, Lim HW. Photoprotection. J Am Acad Dermatol. 2005;52:937-58.
- 8. Tuchinda C, Lim HW, Osterwalder U, Rougier A. Novel emerging sunscreen technologies. Dermatol Clin. 2006;24:105-17.
- 9. Forestier S. Rationale for sunscreen development. J Am Acad Dermatol. 2008;58:S133-8.
- 10. Food and Drug Administration [Internet]. Department of Health and Human Services. FDA, USA. Sunscreen Drug Product for Over-The-Counter Human Use, Final Monograph. Federal Register. 1999;64(98):27689-93. [cited 2011 Apr 28]. Avaiable from: www.fda.gov/downloads/Drugs/DevelopmentApprovalProcess/DevelopmentResources/Over-the-CounterOTCDrugs/StatusofOTCRulemakings/ucm090244.pdf
- 11. Agência Nacional de Vigilância Sanitária (ANVISA) [Internet]. 2002. Regulamento Técnico Sobre Protetores Solares em Cosméticos, Resolução RDC 237. [acesso 28 Mar 2011]. Disponível em: http://e-legis.anvisa.gov.br/leisref/public/showAct.php?id=18298&word=
- 12. Naylor MF, Boyd A, Smith DW, Cameron GS, Hubbard D, Neldner KH. High sun protection factor sunscreens in the suppression of actinic neoplasia. Arch Dermatol. 1995;131:170-5.
- 13. Thompson SC, Jolley D, Marks R. Reduction of solar keratoses by regular sunscreen use. N Engl J Med. 1993;329:1147-51.
- 14. Green A, Williams G, Neale R, Hart V, Leslie D, Parsons P, et al. Daily sunscreen application and betacarotene supplementation in prevention of basal-cell and squamous-cell carcinomas of the skin: a randomized controlled trial. Lancet. 1999;354:723-9.
- 15. Vainio H, Miller AB, Bianchini F. An international evaluation of the cancer-preventive potential of sunscreens. Int J Cancer. 2000;88:838-42.
- 16. Fourtanier A. Mexoryl SX protects against solar-simulated UVR-induced photocarcinogenesis in mice. Photochem Photobiol. 1996;64:688-93.
- 17. Hayag MV, Chartier T, DeVoursney J, Tie C, Machler B, Taylor JR. A high SPF sunscreen's effects on UVB-induced immunosuppression of DNCB contact hypersensitivity. J Dermatol Sci. 1997;16:31-7.
- 18. Huncharek M, Kupelnick B. Use of topical sunscreens and the risk of malignant melanoma: a meta-analysis of 9067 patients from 11 case-control studies. Am J Public Health. 2002;92:1173-7.
- 19. Rigel DS. The effect of sunscreen on melanoma risk. Dermatol Clin. 2002;20:601-6.
- 20. Diffey BL. Sunscreen and melanoma: The future looks bright. Br J Dermatol. 2005;153:378-81.
- 21. IARC Handbooks of Cancer Prevention. World Health Organization. Lyon, France: International Agency for Research on Cancer; 2001. p. 62. (Sunscreens; vol. 5).
- 22. Henne W. In vivo determination of the sunscreen factor of cosmetic preparations, history and the present state of art. Parf Kosm. 1983;64:415-423.
- 23. Schulze R, Einige Versuche und Bemerkungen zum Problem der handelsüblichen Lichtschutzmittel. Praf u Kosm. 1956;37: 310-5.
- 24. Greiter F. Sun protection factor-development methods. Parf Kosm. 1974;55:70-75.
- 25. Brown M. SPF testing in Europe: The International SPF Test Method. In: Shaath NA. Sunscreens: Regulation and Commercial Development. 3rd ed. Boca Raton: T&F Informa; 2005. p 779-806.
- 26. Food and Drug Administration (FDA). Department of Health, Education and Welfare. USA: Sunscreen drug products for over-the-counter drugs: proposed safety, effective and labeling conditions. Federal register. 43/166. 1978;38206-69.
- 27. Fitzpatrick TB. The validity and practicability of sun-reactive skin types I through VI. Arch Dermatol. 1988;124:869-71.
- 28. Food and Drug Administration, Department of Health and Human Services, FDA. USA: Sunscreen Drug Product for Over-The-Counter Human Use, Tentative Final Monograph. Federal Register. 1993;58(90):27693-28194.
- 29. Food and Drug Administration (FDA). Department of Health and Human Services. USA: Sunscreen Drug Product for Over-The-Counter Human Use, Proposed Amendment of Final Monograph, Propose Rule, Federal Register. 2007:72(165):49070-122.
- 30. COLIPA. Sun protection factor test method. COLIPA Publication. Ref 94/289. October 1994.
- 31. COLIPA [Internet]. International Sun Protection Factor Test Method, February 2003. [cited 2011 May 05]. Avaiable from: http://www.ncv-cosmetica.nl/upload/File/20030201_Colipa_SPF_methode.pdf
-
32COLIPA [Internet].Guidelines. The European Cosmetics Association. International Sun Protector Factor Test Method, May 2006. [cited 2011 Apr 29]. Avaiable from: http://www.colipa.eu/publications-colipa-the-european-cosmetic-cosmeticsassociation/guidelines.html?view=item&id=21
- 33. Sayre RM, Agin PP, LeVee GJ, Marlowe E. A comparison of In Vivo and in Vitro testing of sunscreening formulas. Photochem photobiol. 1979; 29:559-66.
- 34. Brown S, Diffey BL. The effect of applied thichness on sunscreen protection: In vivo and in vitro studies. Photochem Photobiol. 1986;44:509-13.
- 35. Freeberg IM, Eisen AZ, Wolff K, Auster KF, Goldsmith LA, Katz SI. Fitzpatrick's Dermatology in General Medicine. 6th ed. New York: Mc Graw-Hill; 2003. p.58-88.
- 36. Stenberg C, Larko O. Sunscreen application and its importance for the sun protection factor. Arch Dermatol. 1985;121:1400-2.
- 37. Bech-Thomsen N, Wulf HC. Sunbather's application of sunscreen is probably inadequate to obtain the sun protection factor assigned to the preparation. Photodermatol Photoimmunol Photomed. 1992;9:242-4.
- 38. Gottieb A, Bourget TD, Lowe NJ. Effects of amounts of application of sun protection factor. In: Lowe NJ, Shaath NA, Pathak MA. Sunscreens: Development, evaluation, and regulatory aspects. 2nd ed. New York: Marcel Dekker; 1997. p 583-9.
- 39. Azurdia RM, Pagliaro JA, Diffey BL, Rhodes LE. Sunscreen application by photosensitive patients is inadequate for protection. Br J Dermatol. 1999;140:255-8.
- 40. Autier P, Boniol M, Severi G, Dore JF. European Organization for Research and Treatment of Cancer Melanoma Co-operative Group. Quantity of sunscreen used by European students. Br J Dermatol. 2001;144:288-91.
- 41. Neale R, Williams G, Green A. Application patterns among participants randomized to daily sunscreen use in a skin cancer prevention trial. Arch Dermatol. 2002;138:1319-25.
- 42. Faurschou A, Wulf HC. The relation between sun protection factor and amount applied in vivo. Br J Dermatol. 2007;156: 716-9.
- 43. Bimczok R, Gers-Barlag H, Mundt C, Klette E, Bielfeldt S, Rudolph T, et al. Influence of applied quantity of sunscreen products on Sun Protection Factor - A multicenter study organized by the DGK Task force Sun Protection. Skin Pharmacol Physiol. 2007;20:57-64.
- 44. Schalka S, dos Reis VM, Cucé LC. The influence of the amount of sunscreen applied and its sun protection factor (SPF): Evaluation of two sunscreens including the same ingredients at different concentrations. Photodermatol Photoimmunol Photomed. 2009;25:175-80.
- 45. Groves GA, Agin PP, Sayre PM. In vitro and In vivo methods to define sunscreen protection. Australas J Dermatol. 1979;20:112-9.
- 46. Osterwalder U, Herzog B. SPF: World Wide Confusion. Br J Dermatol. 2009;161(Suppl. 3):13-24.
- 47. Diffey B. Sunscreens: Expectation and Realizations. Photodermatol Photoimmunol Photomed. 2009;25:233-6.
Datas de Publicação
-
Publicação nesta coleção
21 Jun 2011 -
Data do Fascículo
Jun 2011
Histórico
-
Recebido
12 Maio 2010