Resumos
Este trabalho visa a preparação, caracterização e estudo da adsorção de íons sulfato em óxido de zircônio hidratado preparado pelos métodos da precipitação convencional e da precipitação em solução homogênea. Os materiais obtidos foram caracterizados por difração de raios X, análise termogravimétrica, microscopia eletrônica de varredura e análise de área superficial específica pelo método BET. Através da constante Q0, relacionada com a capacidade de adsorção máxima, observou-se que o ZrO2.nH2O/PSH possui maior capacidade de adsorção para íons sulfato que o ZrO2.nH2O/PC. Pelos resultados de ΔG, observou-se que os íons sulfato foram adsorvidos através de reações energeticamente favoráveis para toda a faixa de concentração estudada.
óxido de zircônio hidratado; adsorção; isoterma de Langmuir
This work reports the preparation, characterization and adsorption study of sulfate on hydrous zirconium oxides prepared by conventional and homogeneous solution precipitation methods. The materials prepared were characterized by X-ray diffraction, thermogravimetric analysis, scanning electron microscopy and surface area measurements. Through the Q0 constant, related with the capacity of maximum adsorption, it was observed that the ZrO2.nH2O/PSH presented better adsorption capacity than ZrO2.nH2O/PC. By results of ΔG, it was observed that sulfate ions had been adsorbed through favorable reactions for all studied concentration ranges.
hydrous zirconium oxide; adsorption; Langmuir isotherm
Adsorção de íons sulfato em ZrO2.nH2O preparado pelo método da precipitação convencional e da precipitação em solução homogênea
Adsorption of sulfate ions in ZrO2.nH2O prepared by conventional precipitation and homogeneous solution methods
L. A. Rodrigues; D. R. Mulinari; M. L. C. P. Silva
Departamento de Engenharia Química, Escola de Engenharia de Lorena - EEL/USP, CP 116, Lorena, SP 12600-000. mlcaetano@dequi.eel.usp.br
RESUMO
Este trabalho visa a preparação, caracterização e estudo da adsorção de íons sulfato em óxido de zircônio hidratado preparado pelos métodos da precipitação convencional e da precipitação em solução homogênea. Os materiais obtidos foram caracterizados por difração de raios X, análise termogravimétrica, microscopia eletrônica de varredura e análise de área superficial específica pelo método BET. Através da constante Q0, relacionada com a capacidade de adsorção máxima, observou-se que o ZrO2.nH2O/PSH possui maior capacidade de adsorção para íons sulfato que o ZrO2.nH2O/PC. Pelos resultados de ΔG, observou-se que os íons sulfato foram adsorvidos através de reações energeticamente favoráveis para toda a faixa de concentração estudada.
Palavras-chave: óxido de zircônio hidratado, adsorção, isoterma de Langmuir.
ABSTRACT
This work reports the preparation, characterization and adsorption study of sulfate on hydrous zirconium oxides prepared by conventional and homogeneous solution precipitation methods. The materials prepared were characterized by X-ray diffraction, thermogravimetric analysis, scanning electron microscopy and surface area measurements. Through the Q0 constant, related with the capacity of maximum adsorption, it was observed that the ZrO2.nH2O/PSH presented better adsorption capacity than ZrO2.nH2O/PC. By results of ΔG, it was observed that sulfate ions had been adsorbed through favorable reactions for all studied concentration ranges.
Keywords: hydrous zirconium oxide, adsorption, Langmuir isotherm.
INTRODUÇÃO
Os íons sulfato são despejados no ambiente aquático pela lixiviação de minerais, produção de tintas, de plástico e de borracha. Quando em concentrações elevadas estes íons podem provocar desidratação e irritação gastrointestinal tanto ao homem quanto aos animais [1]. O excesso desse ânion em efluentes também leva à acidificação dos corpos de água, se transformando na principal causa da corrosão de tubulações [2, 3].
A remoção de íons sulfato de águas é um problema complexo devido à alta solubilidade e estabilidade desses ânions em soluções aquosas. Entre as diversas técnicas de tratamento disponíveis para remoção de sulfato está a adsorção, osmose reversa, eletrodiálise e precipitação química [1]. Atualmente, a maior parte dos tratamentos de efluentes são realizados pela técnica da precipitação química [4]. Porém, esta técnica é ineficiente quando os íons estão na concentração de traços [5], estando então sujeitos a custos e problemas de manipulação do precipitado, sua eliminação e neutralização do efluente [6]. Alguns métodos físicos têm provado serem muito caros, como no caso da osmose reversa e eletrodiálise [7]. A vantagem da adsorção sobre as outras técnicas é a baixa formação de resíduos, a possibilidade de regeneração dos adsorventes [4] e a aplicação de materiais de baixo custo no tratamento de efluentes [8, 9].
Nos últimos anos, vários adsorventes têm sido desenvolvidos para a remoção de íons sulfato, tais como: óxidos metálicos [10-14], quitosana [3-15], óxidos metálicos hidratados [2, 16], zeólita [17], goethite [18-23] e alguns tipos de solo [24-25]. Dentre estes materiais, os óxidos metálicos são materiais promissores para a remoção desse íon por possuírem elevada afinidade pelos mesmos [19].
Neste contexto, o óxido de zircônio hidratado é um material promissor para a remoção de íons sulfato de efluentes por apresentar os requisitos de seletividade e estabilidade necessários ao processo de adsorção, bem como ser de fácil preparação. Este óxido metálico hidratado é praticamente insolúvel em água e na maioria dos ácidos, apresenta estrutura rígida, sofrendo pouca dilatação ou compressão quando imerso em solução aquosa, características estas necessárias para um bom desempenho como adsorvente [26].
O objetivo deste trabalho foi estudar a preparação, a caracterização e o estudo dos parâmetros termodinâmicos da reação de adsorção de íons sulfato em óxido de zircônio hidratado preparado pelos métodos da precipitação convencional (PC) e da precipitação em solução homogênea (PSH).
EXPERIMENTAL
O óxido de zircônio hidratado (PC) foi preparado pela dissolução de 5 g de oxicloreto de zircônio em 100 mL de HCl 0,5 mol.L-1. Após total solubilização do material adicionou-se solução NH4OH (3:1, 30 mL de água deionizada/10 mL NH4OH) até pH 10. Filtrou-se a vácuo, lavou-se com água deionizada até ausência de íons cloreto. Secou-se em estufa a 50 °C até peso constante. O óxido de zircônio hidratado (PSH) foi preparado pela dissolução de 5 g de oxicloreto de zircônio em 100 mL de HCl 0,5 mol.L-1. Após total solubilização do material, adicionou-se 20 g de uréia como agente precipitante. Aqueceu-se a solução a 90 °C para que houvesse decomposição, lenta e gradual da uréia, gerando "in situ" as hidroxilas necessárias para a precipitação do óxido de zircônio (IV) hidratado. O aquecimento foi mantido por 5 h para digestão do precipitado. O material foi então filtrado, lavado com água deionizada até ausência de íons cloreto e seco em estufa a 50 °C até peso constante.
Os difratogramas foram obtidos em um difratômetro de raios X Rich Seifert, com fonte de radiação Cukα, 30 kV, 40 mA, varredura 0,05 ( 2θ/5 s) para valores de 2θ entre 10 e 70°.
A análise termogravimétrica foi realizada em uma termobalança Shimadzu TG-50, com razão de aquecimento 20°C min-1 em fluxo de nitrogênio, no intervalo de temperatura de 25 a 900 °C.
As micrografias foram obtidas em um microscópio eletrônico de varredura LEO1450 VP a baixo vácuo.
A medida de área de superfície específica foi realizada em um Analisador de Adsorção Gasosa (Gas Sorption Analyzer, Quantachrome), sob atmosfera de nitrogênio com fluxo de 30 mL.min-1. Para a determinação da área superficial específica usou-se o método BET [28]. As condições de pré-tratamento foram 50 °C sob vácuo por 16 h.
A adsorção de íons sulfato sobre o óxido de zircônio hidratado foi feita em processo batelada à temperatura ambiente e pH= 5. Amostras de 0,2 g do óxido foram agitadas com soluções de Na2SO4 de diferentes concentrações durante 5 min. Após o período de agitação, a solução foi filtrada. Em seguida, alíquotas da solução foram utilizadas para a determinação de íons sulfato pelo método turbidimétrico [29]. Os dados da adsorção foram ajustados pelo modelo linear de Langmuir. A expressão linear de Langmuir é dada pela equação 1:
sendo Ce a concentração de íons fosfato no equilíbrio (mg.L-1), qe a quantidade adsorvida no equilíbrio (mg.g-1), Qo a constante relacionada com a capacidade de adsorção máxima (mg.g-1) e b a constante relacionada com a energia de adsorção (L.mg-1). A característica essencial da isoterma pode ser expressa pela constante adimensional chamada parâmetro de equilíbrio (RL):
sendo Co a concentração inicial mais alta (mg.L-1) e b a constante de Langmuir. Se 0 < RL < 1 a adsorção é favorável.
O estudo da energia livre de Gibbs foi realizado para uma análise da extensão e espontaneidade da reação de adsorção SO42- estudada.
RESULTADOS E DISCUSSÃO
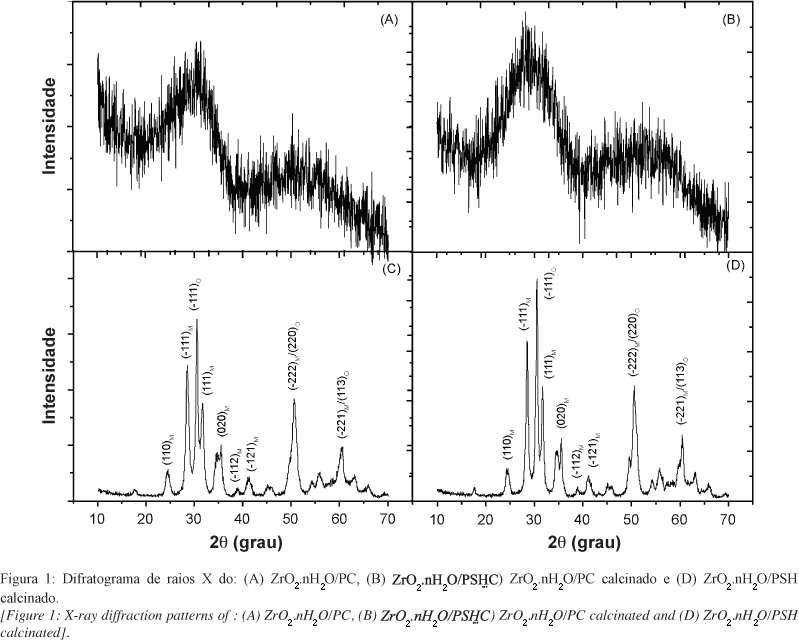
A Fig. 1 mostra os difratogramas de raios X dos óxidos de zircônio hidratados obtidos pelo método PC e PSH. Observa-se que o ZrO2.nH2O obtido pelos 2 métodos, apresenta-se amorfo com um ombro característico em torno de 2θ=30 [30-32]. Comparou-se os difratogramas obtidos com o padrão JCPDS. Como não foram encontradas fichas para o óxido de zircônio hidratado, realizou-se um tratamento térmico nos materiais a 550 °C por 6 h, para eliminação de toda água de hidratação. Os difratogramas do óxido metálico anidro (ZrO2) (Fig. 1) apresentam reflexões correspondentes às fases monoclínica (M) (ficha JCPDS n° 37-1484) e ortorrômbica (O) (ficha JCPDS n° 37-1413) da zircônia, como observado em trabalho anterior [33].
Pela curva termogravimétrica (TG) do ZrO2.nH2O/PC (Fig. 2) e do ZrO2.nH2O/PSH (Fig. 3) observou-se uma perda de massa ocorrendo em uma única etapa na faixa de temperatura de 25 a 800 °C. Para o ZrO2.nH2O/PC observou-se uma perda de massa de 29% entre as temperaturas de 25 a 800 °C, decorrente da eliminação das moléculas de água ligadas à matriz [26]. A curva DTG (derivada primeira da TG) mostra que água é eliminada em 115 °C. Porém a curva termogravimétrica do ZrO2.nH2O/PSH apresentou uma maior perda de massa em relação ao ZrO2.nH2O/PC, no intervalo de temperatura entre 25 a 800 °C. Pode-se observar que cerca de 31% dessa água foi eliminada. A curva DTG mostra que água é eliminada a 123 °C, 8 °C acima da temperatura observada para o material preparado pelo método PC. Com esses dados pode-se calcular o grau de hidratação (n) e, consequentemente a fórmula estequiométrica de cada material preparado. A Tabela I mostra os resultados obtidos pelas curvas termogravimétricas. Pode-se observar através das micrografias apresentadas nas Figs. 4 e 5, que os materiais preparados são pouco porosos e que estes não possuem homogeneidade quanto à forma e o tamanho de partículas.
A área superficial específica está diretamente relacionada ao sítio ativo da superfície do substrato, que no caso dos óxidos metálicos hidratados, são as hidroxilas. Desta forma, a área superficial também influencia na capacidade de adsorção do material, pois quanto maior a área superficial específica, maior a quantidade de sítios na superfície do material e, consequentemente, maior a capacidade de adsorção do mesmo [32]. A área superficial específica do óxido de zircônio hidratado preparado pelo método PC e PSH medida pelo método BET foi de 253,7 m2.g-1 e 248,9 m2.g-1, respectivamente.
Os dados de adsorção foram ajustados pelo modelo de Langmuir. Este modelo de isoterma considera que o adsorvente possui um número definido de sítios ativos idênticos, onde cada sítio retém apenas uma molécula do adsorvato, que a energia de adsorção não depende da quantidade de material adsorvido e que as espécies adsorvidas não reagem com o meio e nem entre si, sendo a adsorção restrita a uma monocamada [34-39]. As isotermas de Langmuir do ZrO2.nH2O/PC e são mostradas nas Figs. 6 e 7, respectivamente.
As constantes de Langmuir foram determinadas pela regressão linear das equações linearizadas e estão listadas na Tabela II. Os valores dos coeficientes de correlação das retas mostram que o modelo de Langmuir descreve adequadamente os dados da adsorção e os valores de RL indicam que a adsorção é um processo favorável na faixa de concentração estudada para os dois materiais preparados. Através da constante Q0, relacionada com a capacidade de adsorção máxima, observou-se que o ZrO2.nH2O/PSH possui maior capacidade de adsorção para íons sulfato que o ZrO2.nH2O/PC. A maior capacidade de adsorção do ZrO2.nH2O/PSH pode ser atribuída ao seu maior grau de hidratação, já que o grau de hidratação dos óxidos hidratados corresponde aos sítios ativos de troca iônica e teoricamente quanto maior o grau de hidratação, maior a quantidade de sítios ativos de adsorção e, consequentemente, maior a capacidade de adsorção. O mesmo foi observado no estudo da adsorção de PO43- em óxido de tungstênio hidratado, o material com maior grau de hidratação também apresentou maior capacidade de adsorção [39].
A distribuição íons sulfato entre as fases líquida e sólida é uma medida da posição de equilíbrio no processo de adsorção e o estado deste sistema pode ser definido por um conjunto de propriedades termodinâmicas, tais como as variações da energia livre de Gibbs (ΔG), que podem servir como medidas da extensão da reação de adsorção [40].
A partir dos de adsorção de SO42-, foram calculados os respectivos valores de energia livre das reações por meio da equação: ΔG = RT (log Ce - log C0), sendo ΔG a variação da energia livre (J.mol-1), R a constante universal dos gases (8,314 J.mol-1K-1) e T a temperatura (K) [40]. Os dados obtidos revelam que para todas as amostras e concentrações estudadas, os valores de ΔG foram negativos (Tabela III) indicando a espontaneidade da reação. O aumento da concentração de íons sulfato leva à um decréscimo da variação de energia livre da reação de adsorção na matriz, indicando que quanto mais concentrada a solução, menos fortemente esse ânion é adsorvido.
CONCLUSÃO
O ZrO2,nH2O/PSH apresentou maior capacidade de adsorção do que o ZrO2.nH2O/PC, evidenciando o efeito positivo do grau de hidratação para o estudo da adsorção de íons sulfato. Os íons sulfato foram adsorvidos nas matrizes por reações energeticamente favoráveis e espontâneas em toda a faixa de concentração estudada. Com o decréscimo da concentração dos íons presentes na solução inicial, a ΔG tornou-se mais negativa como resultado do aumento da força motriz para a ocorrência da reação de adsorção.
(Rec. 04/03/2008, Rev. 08/08/2008, Ac. 15/08/2008)
- [1] C. Namasivayam, D. Sangeetha, Desalination 219 (2008) 1.
- [2] C. Boukhalfa, A. Mennour, L. Reinert, H. Fuzellier, Desalination 214 (2007) 38.
- [3] A. Moret, J. Rubio, Minerals Eng. 16 (2003) 715.
- [4] V. A. Spinelli, M. C. M. Laranjeira, V. T. Favere, Polímeros 15, 3 (2005) 218.
- [5] R. Chitrakar, S. Tezuka, A. Sonoda, K. Sakane, K. Ooi, T. Hirotsu, J. Colloid Interface Sci. 290 (2005) 45.
- [6] M. Ozacar, Chemosphere 51 (2003) 321.
- [7] S. Karaca, A. Gürses, M. Ejder, M. Aç1ky1ld1z, J. Colloid Interface Sci. 277 (2004) 257.
- [8] H. Ye, F. Chen, Y. Sheng, G. Sheng, G. Fu, Separation Purification Technology 50 (2006) 283.
- [9] M. Özacar, J. Hazardous Mater. 137 (2006) 218.
- [10] G. Horányi, P. Joó, J. Colloid Interface Sci. 243 (2001) 46.
- [11] A. Kolics, J. C. Polkinghorne, A. Wieckowski, Electrochim. Acta 43 (1998) 2605.
- [12] H. Wijnja, C. P. Schulthess, Soil Sci. Soc. Am. J. 64 (2000) 898.
- [13] G. Horányi, J. Colloid Interface Sci. 261 (2003) 580.
- [14] C. H. Wu, S. L. Lo, C. F. Lin, C. Y. Kuo, J. Colloid Interface Sci. 233 (2001) 259.
- [15] F. C. Wu, R. L. TSENG, R. S. Juang, Watter Res. 35 (2001) 613.
- [16] K. W. Paul, J. D. Kubicki, D. L. Sparks, Environmental Sci. & Technology 40 (2006), 7717.
- [17] A. D. Vujakovic, M. R. T. Canovic, A. S. Dakovic, V. T. Dondur, Appl. Clay Sci. 17 (2000), 265.
- [18] S. Shahsavani, M. Ardalan, K. R. Sistani, Communications Soil Sci. Plant Analysis 37 (2006) 1587.
- [19] M. Ishiguro, T. Makino, Y. Hattori, J. Colloid Interface Sci. 300 (2006) 504.
- [20] J. S. Geelhoed, T. Hiemstra, W. H. Van Riemsdijk, Geochimica Cosmochimica Acta 61 (1997) 2389.
- [21] R. P. J. J. Rietra, T. Hiemstra, W. H. van Riemsdijk, J. Colloid Interface Sci. 240 (2001) 384.
- [22] R. P. J. J. Rietra, T. Hiemstra, W. H. van Riemsdijk, J. Colloid Interface Sci. 229 (2000) 199.
- [23] R. P. J. J. Rietra, T. Hiemstra, W. H. van Riemsdijk, J. Colloid Interface Sci. 218 (1999) 511.
- [24] M. E. Alves, A. Lavorenti, Geoderma 118 (2004), 89.
- [25] M. Pigna, A. Violante, Communications Soil Sci. Plant Analysis 34 (2003) 2099.
- [26] G. V. Tagliaferro, G. L. J. P. Silva, M. L. C. P. Silva, Quimica Nova 28 (2005) 250.
- [27] G. L. J. P. Silva, M. L. C. P. Silva, T. Caetano, Mater. Res. 5 (2002) 149.
- [28] S. Brunauer, P. H. Emmett, E. Teller, J. Am. Chem. Soc. 60 (1938) 309.
- [29] M. Radojevic, V. N. Bashkin, Pratical Enviromental Analysis, MPG Books Ltd, Cornwal (1999).
- [30] D. Tichit, D. El Alami, F. Figueiras, Applied Catalysis A. General 145 (1996) 195.
- [31] D. R. Mulinari, G. L. J. P. Silva, M. L. C. P. Silva, Quimica Nova 29 (2006) 496.
- [32] D. R. Mulinari, G. L. J. P. Silva, L. A. Rodrigues, M. L. C. P. Silva, Cerâmica 53, 328 (2007) 345.
- [33] A. L. C. Peixoto, G. L. J. P. Silva, M. L. C. P. Silva, Cerâmica 52, 324 (2006) 249.
- [34] F. F. Sodré, E. Lenzi, A. C. S. Costa, Quimica Nova 24, 3 (2001) 324.
- [35] E. A. Deliyanni, E. N. Peleka, N. K. Lazaridis, Separation Purification Technology/ 52 (2007) 478.
- [36] S. Gomri, J.-L Seguin, J. Guerin, A. Aguir, Sensors & Actuators B: Chemical/ 114 (2006) 451.
- [37] G. Limousin, J.-P. Gaudet, L. Charlet, S. Szenknect, V. Barthès, M. Krimissa, Appl. Geochem. 22 (2007) 249.
- [38] N. Ortiz, C. Susca, K. M. R. Oliveira, J. C. Bressiani, Cerâmica/ 49, 312 (2003) 216.
- [39] L. A. Rodrigues, M. L. C. P. Silva, Cerâmica 54, 329 (2008) 92.
- [40] M. R. Soares, L. R. F. Alleoni, J. C. Casagrande, Química Nova 28, 6 (2005) 1014.
Datas de Publicação
-
Publicação nesta coleção
12 Maio 2009 -
Data do Fascículo
Mar 2009
Histórico
-
Aceito
15 Ago 2008 -
Revisado
08 Ago 2008 -
Recebido
04 Mar 2008