Resumos
A prolactina (PRL) é um hormônio fundamental para a galactopoiese, porém, desempenha também outras diversas funções no papel de citocina, como a imunomodulação. A PRL é secretada pela maioria das células do sistema imunológico, estimulando a proliferação, diferenciação e maturação de linfócitos T e B, amplificando a ação de IL-2 e promovendo a inibição da apoptose dessas células. Há diversas evidências da participação da PRL na fisiopatologia das doenças autoimunes, especialmente do lúpus eritematoso sistêmico (LES), epidemiológicas e provenientes de estudos em modelos animais, in vitro e in vivo. A presença da PRL monomérica, biologicamente ativa, correlaciona-se com a atividade lúpica, enquanto que a macroprolactinemia, caraterizada pela presença de um anticorpo anti-PRL, se correlaciona negativamente. Há ainda pontos que merecem melhor esclarecimento: Qual a origem da PRL nos pacientes com hiperprolactinemia (hipofisária versus extra-hipofisária)? Há aumento da bioatividade da PRL? Há mutações ou polimorfismos no gene da PRL ou de seu receptor? O tratamento da hiperprolactinemia ou o uso de agonistas da PRL podem mudar a história natural do LES?
prolactina; hiperprolactinemia; lúpus eritematoso sistêmico; citocina; autoimunidade
Prolactin (PRL) is a fundamental hormone to galactopoiesis. Nevertheless, it has many other actions, including a cytokine that modulates immune system. Most of immune cells secretes PRL, which stimulates proliferation, differentiation and maturation of T and B lymphocytes, amplifies IL-2 action and inhibits lymphocytes apoptosis. There are many evidences of the role of PRL in physiopathology of autoimmune diseases, especially systemic lupus erythematosus (SLE), as shown by data from epidemiologic and animal models studies, in vitro and in vivo. Monomeric PRL, the biologic active isoform, correlates positively to lupus activity, while macroprolactinemia, characterized by an autoantibody anti-PRL, correlates negatively. There are still some issues that deserve more studies: which is the PRL origin in hyperprolactinemic patients (pituitary versus extrapituitary)?; is PRL bioactivity increased?; is there any mutations or polymorphisms in PRL gene and PRL receptor gene?, can hyperprolactinemia treatment or PRL antagonist change SLE natural history?
prolactin; hyperprolactinemia; systemic lupus erythematosus; cytokine; autoimmunity
ARTIGO DE REVISÃO
O papel da prolactina no lúpus eritematoso sistêmico: onde estamos
Andrea GlezerI; Diane Belchior ParaibaI; Jozélio Freire de CarvalhoII
IDoutora em Endocrinologia e Médica do Ambulatório de Neuro-endocrinologia do Hospital das Clínicas da Faculdade de Medicina da Universidade de São Paulo
IIProfessor Colaborador e Médico Assistente doutor do serviço de Reumatologia do Hospital das Clínicas da Faculdade de Medicina da Universidade de São Paulo
Endereço para correspondência Endereço para correspondência: Dr. Jozélio Freire de Carvalho Av. Dr. Arnaldo, 455, 3 andar, sala 3190, São Paulo - SP CEP: 01246-903. Tel./Fax: (11) 30617490 E-mail: reumato@usp.br
RESUMO
A prolactina (PRL) é um hormônio fundamental para a galactopoiese, porém, desempenha também outras diversas funções no papel de citocina, como a imunomodulação. A PRL é secretada pela maioria das células do sistema imunológico, estimulando a proliferação, diferenciação e maturação de linfócitos T e B, amplificando a ação de IL-2 e promovendo a inibição da apoptose dessas células. Há diversas evidências da participação da PRL na fisiopatologia das doenças autoimunes, especialmente do lúpus eritematoso sistêmico (LES), epidemiológicas e provenientes de estudos em modelos animais, in vitro e in vivo. A presença da PRL monomérica, biologicamente ativa, correlaciona-se com a atividade lúpica, enquanto que a macroprolactinemia, caraterizada pela presença de um anticorpo anti-PRL, se correlaciona negativamente. Há ainda pontos que merecem melhor esclarecimento: Qual a origem da PRL nos pacientes com hiperprolactinemia (hipofisária versus extra-hipofisária)? Há aumento da bioatividade da PRL? Há mutações ou polimorfismos no gene da PRL ou de seu receptor? O tratamento da hiperprolactinemia ou o uso de agonistas da PRL podem mudar a história natural do LES?
Palavras-chave: prolactina, hiperprolactinemia, lúpus eritematoso sistêmico, citocina, autoimunidade.
INTRODUÇÃO
A prolactina (PRL) é uma proteína que desempenha dupla ação: como hormônio, devido à produção hipofisária, e como citocina, secundária à produção extra-hipofisária.1 Nos seres humanos, a função mais conhecida da PRL é a ação hormonal que estimula o desenvolvimento final mamário e garante a galactopoiese.
A PRL, no papel de citocina, apresenta ações autócrinas e parácrinas em diversos órgãos e tecidos, participando de funções ligadas à reprodução, metabolismo, controle de água e eletrólitos, crescimento e desenvolvimento, modulação do sistema imunológico.1
A PRL é considerada uma citocina por vários motivos: ser secretada por células imunológicas; seu receptor pertencer à família de receptores de citocinas tipo 1 (interleucinas, eritropoetina, trombopoetina, leptina, granulocyte macrophage-colony stimulating factor, granulocyte-colony stimulating factor); compartilhar a via de sinalização intracelular com a de outras citocinas; e o gene que a codifica estar localizado no cromossomo seis, próximo ao complexo HLA.2
Apesar de haver muitas evidências sobre a participação da PRL no sistema imunonológico, o seu exato papel na fisiologia e fisiopatologia das doenças autoimunes ainda não foi totalmente esclarecido. Dentre os estudos sobre PRL e doenças autoimunes, o paradigma é o lúpus eritematoso sistêmico (LES).
PRL EXTRA-HIPOFISÁRIA
A expressão do gene da PRL, assim como a do seu receptor, tem sido registrada em vários outros sítios além da hipófise, tais como cérebro, miométrio, glândula lacrimal, timo, baço, células epiteliais mamárias, fibroblastos, linfócitos circulantes e células linfoides da medula óssea, entre outros. A PRL pode ser encontrada também nos mais diversos compartimentos fluídos além do sangue, como líquor, leite materno, suor e líquido amniótico1 (Figura1).
A PRL hipofisária é sempre tomada como modelo quando se discute mecanismo de ação, regulação gênica, heterogeneidade molecular e estrutura de receptores. A PRL hipofisária age como um hormônio clássico, secretado pela glândula, transportado via circulação, agindo nas células-alvo através de receptores de membrana e desencadeando uma série de eventos próprios, como a lactação.
Além dessa ação hormonal clássica, a PRL extra-hipofisária apresenta ação sob as células adjacentes (ação parácrina) e sob as próprias células que a produzem (ação autócrina). A secreção da PRL extra-hipofisária, no entanto, não parece interferir na concentração sérica da PRL. Por isso, a dosagem sérica de PRL não se correlaciona linearmente com suas ações autócrinas e parácrinas.3
A composição da proteína final da PRL extra-hipofisária é idêntica à da hipofisária e ambas compartilham um mesmo gene, porém, os RNAs mensageiros e as regiões promotoras são distintos, assim como o controle de sua transcrição.4
A PRL hipofisária é transcrita a partir da ativação de um promotor proximal, cujo principal ativador é o estrógeno e o principal inibidor é a dopamina. Já a transcrição da PRL extra-hipofisária é controlada por um promotor superdistal. A expressão da PRL extra-hipofisária é célula-específica e independente de Pit-1,2 um importante fator de transcrição dos genes de PRL, hormônio de crescimento e hormônio tireosestimulante.
PRL E O SISTEMA IMUNOLÓGICO
Muitos estudos sugerem o papel da PRL5,6 como um fator importante na imunomodulação, mas ainda não se sabe a real implicação desse "hormônio-citocina" no complexo sistema imunológico.
Em 1991, Nagy e Berczi7 relataram que ratas hipofisectomizadas permaneciam com 10% a 20% da atividade lactogênica. Dentro de dois meses, essa atividade gradualmente aumentava para 50%. Nos animais submetidos à imunoneutralização da PRL houve redução importante da atividade lactogênica, causando deficiências imunológicas múltiplas e morte. Esses achados não ocorreram no grupo de ratas hipofisectomizadas sem imunoneutralização. Por esses resultados, os autores sugerem que a PRL esteja envolvida em funções vitais, provavelmente mantidas pela sua produção extra-hipofisária.
Em contrapartida, o papel fundamental da PRL no sistema imunológico não foi confirmado nos estudos com camundongos knockout para o receptor de PRL,8 nos quais não houve qualquer imunodeficiência.
Entretanto, a produção, a distribuição, as funções fisiológicas e fisiopatológicas e a regulação da PRL podem diferir entre as espécies, demonstrando-se diferenças entre ratos e camundongos, devendo a extrapolação para humanos ser feita com cuidadosa avaliação.9
A observação de que a maioria das doenças autoimunes humanas incide sobre o sexo feminino e de que pode haver piora da atividade dessas doenças na gestação e no período periparto sugere que o estrógeno e a PRL possam modular a atividade imunológica.10 Há diversas evidências da inter-relação entre os hormônios, especialmente a PRL, e o sistema imunológico: citocinas como a interleucinas (IL) 1 e 2 influenciam a secreção de hormônios hipofisários, como a PRL;11,12 as células do sistema imune expressam receptores para PRL, dentre outros hormônios;13 a PRL ativa a proteína quinase C, essencial para a proliferação de células T, induz a expressão do receptor de IL-2 e estimula a produção de INF gama através do fator de regulação do INF 1 (IRF-1), que por sua vez regula a maturação e diferenciação das células B e T.14
Esses dados apontam para um papel imunomodulador da PRL, justificando que em animais knockout a ausência da PRL não comprometa por completo a imunidade.
A PRL tem também papel regulatório no processo de linfopoiese. A curto prazo, estimula a proliferação de linfócitos T, a expressão de IL-2 e de seus receptores, tendo um efeito comitogênico com a IL-2.15 Cronicamente, estimula a ativação de mononucleares, a diferenciação e maturação das células B e T; aumenta a apresentação de antígenos e de autoantígenos;16 e aumenta a produção de imunoglobulinas.17
A PRL, tanto de origem hipofisária quanto extra-hipofisária, ativa a via de sinalização intracelular JAK2/STAT, incrementando a expressão do IRF1, que, por sua vez, estimula a transcrição do INF gama. O IRF1 é um fator de transcrição envolvido na resposta Th1, antiviral e antibacteriana, na qual também participam macrófagos, células dendríticas e células NK (natural killers).
Em resumo, o espectro completo das funções imunológicas da PRL ainda é muito controverso. No entanto, existem evidências de que níveis fisiológicos de PRL circulante são necessários para manter a competência imunológica, estando tanto a hipoprolactinemia como a hiperprolactinemia implicadas em danos imunológicos, podendo ocorrer imunossupressão ou desenvolvimento de autoimunidade, respectivamente.18
HIPERPROLACTINEMIA E LÚPUS ERITEMATOSO SISTÊMICO
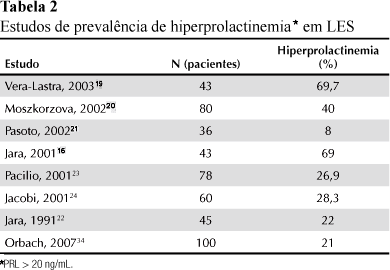
A prevalência de hiperprolactinemia na população geral é menor que 5%, estando as principais causas detalhadas na Tabela 1. No entanto, a média de prevalência de hiperprolactinemia nos pacientes lúpicos é de 20% a 30%, variando de 8% a 69,7%,19-24 em geral com níveis apenas discretamente elevados (Tabela 2).
Os estudos in vitro demonstram alterações no sistema imunológico de pacientes lúpicos, com relação à PRL: as células mononucleares são mais sensíveis à ação da PRL para produção de imunoglobulinas, mesmo em concentrações fisiológicas;25 a PRL in vitro é capaz de induzir a síntese de imunoglobulinas e de anti-DNA.26
Em contrapartida, uma publicação sugere que não há alteração na secreção de PRL hipofisária em pacientes com LES.27 Os autores avaliaram a função da hipófise anterior, por meio de dosagens hormonais basais e de testes estimulatórios, em 11 pacientes com LES e nove indivíduos controles. Não houve diferença quanto às dosagens de PRL nos dois grupos. Esses dados reforçam a hipótese de que o aumento da PRL em alguns pacientes se deva à produção local por células imunológicas.
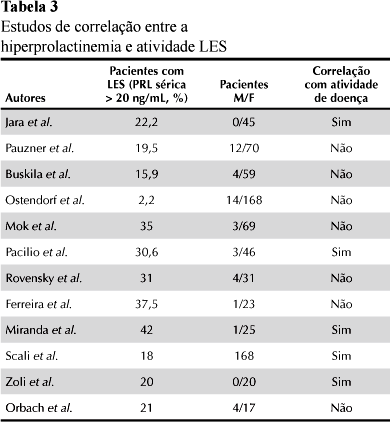
Uma vez demonstrado que existe uma correlação entre LES e hiperprolactinemia, cabe a indagação sobre a correlação entre PRL e atividade do LES.27-29 Os dados na literatura são conflitantes (Tabela 3); no entanto, muitos dos trabalhos apontam para uma correlação presente,21,23,25,30-33 inclusive com algumas lesões orgão-específicas, como acometimento cutâneo, articular, renal e de sistema nervoso central.17
Os resultados discordantes sobre a correlação entre PRL e atividade do LES podem ser explicados pela heterogeneidade dos grupos de pacientes estudados, pela utilização de diferentes índices para medir atividade do LES, pela inclusão de pacientes com duração de doença variável e pelas diversas metodologias usadas para a dosagem de PRL. A presença da hiperprolactinemia associa-se à de diversos autoanticorpos, como anti-núcleo, anti-dsDNA, anticardiolipina e antimicrossomal.17
A alta prevalência de hiperprolactinemia em pacientes com LES e em várias outras doenças autoimunes (Tabela 4) reforçam o envolvimento da PRL.34,35 Em 1.029 soros de pacientes com diversas doenças autoimunes, Orbach et al. confirmaram a pesença de hiperprolactinemia no lúpus e observaram pela primeira vez esse achado em 24% dos pacientes com polimiosite.34
BIOATIVIDADE DA PRL NO LES
Como nem todos os indivíduos com LES apresentam hiperprolactinemia e, na maior parte dos casos, a hiperprolactinemia encontrada é discreta, cabe o questionamento sobre a atividade biológica da PRL desses pacientes.
Um modelo muito utilizado na literatura para a avaliação da bioatividade da PRL é o bioensaio com células Nb2, derivadas de linfoma de rato castrado da linhagem Noble. Essa metodologia é muito sensível, porém pouco específica, uma vez que essas células expressam receptor de PRL murino e mutado. Essas diferenças em relação às células imunes humanas podem justificar os diferentes resultados encontrados.36 Alguns autores encontraram bioatividade maior em pacientes,23,38 enquanto outros não encontraram diferenças.38,39
ISOFORMAS DE PRL
Em 1992, Hattori et al.40 descreveram a presença de uma imunoglobulina específica anti-PRL que, por causar redução da depuração renal, da degradação e da alça de retroalimentação negativa no hipotálamo, explicaria a hiperprolactinemia na presença desse autoanticorpo. A forma agregada de PRL e autoanticorpo apresenta peso molecular de mais de 100 kDa e é chamada de macroprolactina. Na maioria dos indivíduos normo e hiperprolactinêmicos, a principal isoforma circulante é a PRL monomérica, com 23 kDa; no entanto, em média 25% dos indivíduos com hiperprolactinemia podem apresentar como isoforma principal circulante a macroprolactina, situação denominada de macroprolactinemia.
A presença do anticorpo anti-PRL é encontrada com maior frequência em pacientes com LES. Sua presença foi associada à maior prevalência de macroprolactina. Por sua vez, a macroprolactinemia parece conferir proteção à atividade lúpica, provavelmente porque a macroprolactina é uma isoforma biologicamente pouco ativa, sendo encontrada mais frequentemente em pacientes com LES em inatividade de doença, enquanto que a PRL monomérica, biologicamente ativa, se correlaciona com a atividade da doença. Esses dados podem explicar em parte os resultados conflitantes e reforçam o fato de que a PRL monomérica esteja envolvida na fisiopatologia da autoimunidade.39,41-43
POLIMORFISMO DE PRL E R-PRL
Nos pacientes com LES ativo, a presença de mutações ou de polimorfismos da PRL ou de seu receptor poderia justificar a maior ação da PRL sob o sistema imune, sem que houvesse hiperprolactinemia. No entanto, Mellai et al.44 não encontraram polimorfismo da PRL e de seu receptor em 217 pacientes com LES e 707 controles. Stevens et al.45 associaram SNP (single nucleotide polymorphism) na região promotora distal de linfócitos à presença de LES (PRL1149-G). O tema ainda merece novos estudos.
TRATAMENTO DA HIPERPROLACTINEMIA NO LES
A literatura descreve estudos em animais e alguns protocolos clínicos com uso de bromocriptina em indivíduos com LES.
Os camundongos NZB/NZW representam um excelente modelo para o estudo do LES, e nele o estrógeno é um importante fator acelerador e a bromocriptina, um agonista dopaminérgico, um dos principais fatores inibidores da evolução da doença. A bromocriptina é capaz de suprimir a doença renal e aumentar a sobrevida dos animais tratados.46
Há séries de casos relatados nas quais houve melhora da atividade lúpica em pacientes que utilizaram a bromocriptina, incluindo portadores ou não de prolactinoma.47 Um recente estudo piloto aberto com gestantes lúpicas, divididas em dois grupos, um em uso de bromocriptina (2,5 mg/dia) e prednisona (10 mg/dia), e outro apenas com prednisona (10 mg/dia), mostrou que o primeiro teve menos complicações materno-fetais (abortamento, descolamento prematuro de placenta, pré-eclâmpsia, entre outros) do que o grupo sem a bromocriptina.48 No entanto, considerando-se que a transcrição de PRL extra-hipofisária independe da ação dopaminérgica, o mecanismo terapêutico permanece desconhecido. Publicações demonstraram que pacientes lúpicos tratados com a bromocriptina apresentaram menor atividade da doença.46,49 Alguns autores sugerem que a bromocriptina ativa de forma não específica as células T supressoras CD8+ em modelos experimentais.50
Há evidências da presença de receptores dopaminérgicos em linfóctios murinos. No entanto, esse efeito in vitro ocorreu com doses cerca de 50 vezes maiores que a utilizada in vivo em camundongos NZB/NZW.46
Vale ressaltar que o tratamento convencional para o LES também promoveu redução dos valores de PRL em pacientes com hiperprolactinemia leve (20 a 40 ng/mL).47
A bromocriptina ainda não é autorizada para uso rotineiro em pacientes com LES, o que significa que novos dados precisam ser publicados para recomendar o uso dessa medicação em tais pacientes.
CONCLUSÕES
A PRL é uma citocina que apresenta algumas funções definidas na imunomodulação, especialmente em relação à resposta Th1.
Há diversas evidências correlacionando PRL e atividade do LES. A literatura sugere a hipótese de que a produção de PRL pelos linfócitos seja a principal implicada. Portanto, devido tanto à morbidade do LES, como também aos efeitos colaterais relevantes das drogas atualmente disponíveis para seu tratamento, tornam-se importantes novos estudos para avaliação do real papel da PRL na sua etiopatogenia, visando o potencial emprego de drogas agonistas dopaminérgicas. Adicionalmente, o detalhamento das isoformas mais prevalentes e a verificação da origem desta PRL (hipofisária versus linfocitária) podem trazer novos dados para o uso terapêutico dessas drogas e ainda abrir caminhos para o desenvolvimento de outros medicamentos para tratamento específico, tais como um antagonista do receptor da PRL.
Apesar de as evidências mostrarem claramente o papel da PRL na imunomodulação, ainda não está definido se a presença da hiperprolactinemia é causa, efeito ou apenas um epifenômeno na atividade lúpica. Portanto, até o presente momento, a dosagem de PRL em pacientes lúpicos não deve ser realizada rotineiramente, somente em centros de pesquisa. A indicação da dosagem de PRL sérica em pacientes lúpicos é a presença de hipogonadismo (infertilidade, irregularidade menstrual), com ou sem galactorreia, como se procede em qualquer situação clínica. O uso de bromocriptina na atividade lúpica é ainda experimental.
Recebido em 15/07/2008.
Aprovado, após revisão, em 10/01/09.
A Glezer e JF Carvalho receberam auxílio da Fundação Frederico.
Serviços de Endocrinologia e Reumatologia do Hospital das Clínicas da Faculdade de Medicina da Universidade de São Paulo
-
1Ben-Jonathan N, Mershon JL, Allen DL, Steinmetz RW. Extrapituitary Prolactin: Distribution, Regulation, Functions, and Clinical Aspects. Endocrine Reviews 1996;17:639-69.
-
2Freeman ME, Kanyicska B, Lerant A, Nagy G. Prolactin: Structure, Function, and Regulation of Secretion. Physiological Reviews 2000;80(4):1523-631.
-
3Bole-Feysot C, Goffin V, Edery M, Binart N, Kelly PA. Prolactin and its receptor: actions signal transduction pathways and phenotypes observed in prolactin receptor knockout mice. Endocr Rev 1998;19:225-68.
-
4Berwaer M, Martial JA, Davis JR. Characterization of an up-stream promoter directing extrapituitary expression of the human prolactin gene. Mol Endocrinol 1994;8(5):635-42.
-
5Peeva E, Zouali M. Spotlight on the role of hormone factors in the emergence of autoreactive B-lymphocytes. Immunol Lett 2005;101:123-43.
-
6Peeva E, Michael D, Cleary J, Rice J, Chen X, Diamond B. Prolactin modulates the naïve B cell repertoire. J Clin Invest 2003;111:275-83.
-
7Nagy E, Berczi I: Hypophysectomized rats depend on residual prolactin for survival. Endocrinology. 1991;128: 2776-84.
-
8Bouchard B, Ormandy C, Di Santo J, Kelly P. Immune system development and function in prolactin receptor-deficient mice. J Immunol 1999;163:576-82.
-
9Ben-Jonathan N, LaPensee CR, LaPensee EW. What can we learn from rodents about prolactin in humans? Endoc Rev 2008;29(1):1-41.
-
10Cooper GS, Dooley MA, Treadwell EL, St Clair EW, Parks CG, Gilkeson GS. Hormonal, environmental, and infectious risk factors for developing systemic lupus erythematosus. Arthritis Rheum 1998;41(10):1714-24.
-
11Karanth S, McCann SM. Anterior pituitary hormone control by interleukin 2. Proc Natl Acad Sci U S A 1991;88(7):2961-5.
-
12Rotiroti D, Ciriaco E, Germanà GP, Naccari F, Gratteri S, Laurà R et al Stimulatory effects on lactotrophs and crop-sac of interleukin-1 and interleukin-2 in pigeons (Columba livia). Funct Neurol 1993;8(3):205-10.
-
13Russell DH, Kibler R, Matrisian L, Larson DF, Poulos B, Magun BE. Prolactin receptors on human T and B lymphocytes: antagonism of prolactin binding by cyclosporin. J Immunol.;1985;134:3027-3031.
-
14Yu-Lee L. Stimulation of interferon regulatory factor-1 by prolactin. Lupus 2001;10(10):691-9.
-
15Cesario TC, Yousefi S, Carandang G. Enhanced yields of gamma interferon in prolactin treated human prepheral blood mononucelar cells. Proc Soc Exp Biol Med 1994;205:89-95.
-
16Jara LJ, Benitez G, Medina G. Prolactin, dendritic cells, and systemic lupus erythematosus. Autoimmun Rev 2008;7(3):251-5.
-
17Vera-Lastra O, Jara LJ, Espinoza LR. Prolactin and autoimmunity. Autoimmun Rev 2002;1(6):360-4.
-
18Chuang E, Molitch ME. Prolactin and autoimmune diseases in humans. Acta Biomed 2007;8(Suppl 1):255-61.
-
19Vera-Lastra O, Mendez C, Jara LJ, Cisneros M, Medina G, Ariza R, Espinoza LR. Correlation of prolactin serum concentrations with clinical activity and remission in patients with systemic lupus erythematosus. Effect of conventional treatment. J Rheumatol 2003;30(10):2140-6.
-
20Moszkorzová L, Lacinová Z, Marek J, Musilová L, Dohnalová A, Dostál C. Hyperprolactinaemia in patients with systemic lupus erythematosus. Clin Exp Rheumatol 2002;20(6):807-12.
-
21Pasoto SG, Mendonça BB, Bonfá E. Menstrual disturbances in patients with systemic lupus erythematosus without alkylating therapy: clinical, hormonal and therapeutic associations. Lupus 2002;11(3):175-80.
-
22Jara LJ, Vera-Lastra O, Miranda JM, Alcala M, Alvarez-Nemegyei J. Prolactin in human systemic lupus erythematosus. Lupus 2001;10:748-56.
-
23Pacilio M, Migliaresi S, Meli R, Ambrosone L, Bigliardo B, Di Carlo R. Elevated bioactive prolactin levels in systemic lupus erythematosus—association with disease activity. J Rheumatol 2001;28(10):2216-21.
-
24Jacobi AM, Rohde W, Ventz M, Riemekasten G, Burmester GR, Hiepe F. Enhanced serum prolactin (PRL) in patients with systemic lupus erythematosus: PRL levels are related to the disease activity. Lupus 2001;10(8):554-61.
-
25Jacobi AM, Rohde W, Volk HD, Dörner T, Burmester GR, Hiepe F. Prolactin enhances the in vitro production of IgG in peripheral blood mononuclear cells from patients with systemic lupus erythematosus but not from healthy controls. Ann Rheum Dis 2001;60(3):242-7.
-
26Gutiérrez MA, Molina JF, Jara LJ, García C, Gutiérrez-Ureña S, Cuéllar ML, et al Prolactin-induced immunoglobulin and autoantibody production by peripheral blood mononuclear cells from systemic lupus erythematosus and normal individuals. Int Arch Allergy Immunol 1996;109(3):229-35.
-
27Köller MD, Templ E, Riedl M, Clodi M, Wagner O, Smolen JS, et al Pituitary function in patients with newly diagnosed untreated systemic lupus erythematosus. Ann Rheum Dis 2004;63:1677-80.
-
28Buskila D, Lorber M, Neumann L, Flusser D, Shoenfeld Y. No correlation between prolactin levels and clinical activity in patients with systemic lupus erythematosus. J Rheumatol 1996; 23(4):629-32.
-
29Jimena P, Aguirre MA, López-Curbelo A, de Andrés M, Garcia-Courtay C, Cuadrado MJ. Prolactin levels in patients with systemic lupus erythematosus: a case controlled study. Lupus 1998;7(6):383-6.
-
30McMurray RW, Allen SH, Braun AL, Rodriguez F, Walker SE. Longstanding hyperprolactinemia associated with systemic lupus erythematosus: possible hormonal stimulation of an autoimmune disease. J Rheumatol 1994;21(5):843-50.
-
31Petri M. Clinical features of systemic lupus erythematosus. Curr Opin Rheumatol 1995;7(5):395-401.
-
32Neidhart M. Elevated serum prolactin or elevated prolactin/cortisol ratio are associated with autoimmune processes in systemic lupus erythematosus and other connective tissue diseases. J Rheumatol 1996;23(3):476-81.
-
33Rovenský J, Juránková E, Rauová L, Blazícková S, Lukác J, Veselková Z, et al Relationship between endocrine, immune, and clinical variables in patients with systemic lupus erythematosus. J Rheumatol 1997;24(12):2330-4.
-
34Orbach H, Zandman-Goddard G, Amital H, Barak V, Szekanecz Z, Szucs G, et al Novel biomarkers in autoimmune diseases: prolactin, ferritin, vitamin D, and TPA levels in autoimmune diseases. Ann N Y Acad Sci 2007;1109:385-400.
-
35De Bellis A, Bizzarro A, Pivonello R, Lombardi G, Bellastella A. Prolactin and autoimmunity. Pituitary 2005;8:25-30.
-
36Glezer A, Soares CR, Vieira JG, Giannella-Neto D, Ribela MT, Goffin V, et al Human macroprolactin displays low biological activity via its homologous receptor in a new sensitive bioassay. J Clin Endocrinol Metab 2006;91(3):1048-55.
-
37Méndez I, Alcocer-Varela J, Parra A, Lava-Zavala A, de la Cruz DA, Alarcón-Segovia D, et al Neuroendocrine dopaminergic regulation of prolactin release in systemic lupus erythematosus: a possible role of lymphocyte-derived prolactin. Lupus 2004;13(1):45-53.
-
38Cruz J, Aviña-Zubieta A, Martínez de la Escalera G, Clapp C, Lavalle C. Molecular heterogeneity of prolactin in the plasma of patients with systemic lupus erythematosus. Arthritis Rheum 2001 44(6):1331-5.
-
39Leaños-Miranda A, Chávez-Rueda KA, Blanco-Favela F. Biologic activity and plasma clearance of prolactin-IgG complex in patients with systemic lupus erythematosus. Arthritis Rheum 2001;44(4):866-75.
-
40Hattori N, Ishihara T, Ikekubo K, Moridera K, Hino M, Kurahachi H. Autoantibody to human prolactin in patients with idiopathic hyperprolactinemia. J Clin Endocrinol Metab 1992;75(5):1226-9.
-
41Leaños-Miranda A, Pascoe-Lira D, Chávez-Rueda KA, Blanco-Favela F. Antiprolactin autoantibodies in systemic lupus erythematosus: frequency and correlation with prolactinemia and disease activity. J Rheumatol 2001;28(7):1546-53.
-
42Blanco-Favela F, Chavez-Rueda K, Leaños-Miranda A. Analysis of anti-prolactin autoantibodies in systemic lupus erythematosus. Lupus 2001;10(10):757-6.
-
43Leaños-Miranda A, Cárdenas-Mondragón G, Ulloa-Aguirre A, Isordia-Salas I, Parra A, Ramírez-Peredo J. Anti-prolactin autoantibodies in pregnant women with systemic lupus erythematosus: maternal and fetal outcome. Lupus 2007;16(5):342-9.
-
44Mellai M, Giordano M, D'Alfonso S, Marchini M, Scorza R, Giovanna Danieli M, et al Prolactin and prolactin receptor gene polymorphisms in multiple sclerosis and systemic lupus erythematosus. Hum Immunol 2003;64(2):274-84.
-
45Stevens A, Ray DW, Worthington J, Davis JR. Polymorphisms of the human prolactin gene—implications for production of lymphocyte prolactin and systemic lupus erythematosus. Lupus 2001;10(10):676-83.
-
46Walker SE. Treatment of systemic lupus erythematosus with bromocriptine. Lupus 2001;10:197.
-
47Orbach H, Shoenfeld Y. Hyperprolactinemia and autoimmune diseases. Autoimmun 2007; 6:537-42.
-
48Jara LJ, Cruz-Cruz P, Saavedra MA, Medina G, García-Flores A, Angeles U, et al Bromocriptine during pregnancy in systemic lupus erythematosus: a pilot clinical trial. Ann N Y Acad Sci 2007;1110:297-304.
-
49McMurray RW, Weidensaul D, Allen SH, Walker SE. Efficacy of bromocriptine in an open label therapeutic trial for systemic lupus erythematosus. J Rheumatol 1995;22(11):2084-91.
-
50Blank M, Krause I, Buskila D, Teitelbaum D, Kopolovic J, Afek A et al Bromocriptine immunomodulation of experimental SLE and primary antiphospholipid syndrome via induction of nonspecific T suppressor cells. Cell Immunol 1995;162(1):114-22.
Endereço para correspondência:
Datas de Publicação
-
Publicação nesta coleção
07 Abr 2009 -
Data do Fascículo
Abr 2009
Histórico
-
Aceito
10 Jan 2009 -
Recebido
15 Jul 2008