Resumos
O sistema imunológico é constituído por uma intrincada rede de órgãos, células e moléculas, e tem por finalidade manter a homeostase do organismo, combatendo as agressões em geral. A imunidade inata atua em conjunto com a imunidade adaptativa e caracteriza-se pela rápida resposta à agressão, independentemente de estímulo prévio, sendo a primeira linha de defesa do organismo. Seus mecanismos compreendem barreiras físicas, químicas e biológicas, componentes celulares e moléculas solúveis. A primeira defesa do organismo frente a um dano tecidual envolve diversas etapas intimamente integradas e constituídas pelos diferentes componentes desse sistema. A presente revisão tem como objetivo resgatar os fundamentos dessa resposta, que apresenta elevada complexidade e é constituída por diversos componentes articulados que convergem para a elaboração da resposta imune adaptativa. Destacamos algumas etapas: reconhecimento molecular dos agentes agressores; ativação de vias bioquímicas intracelulares que resultam em modificações vasculares e teciduais; produção de uma miríade de mediadores com efeitos locais e sistêmicos no âmbito da ativação e proliferação celulares, síntese de novos produtos envolvidos na quimioatração e migração de células especializadas na destruição e remoção do agente agressor, e finalmente a recuperação tecidual com o restabelecimento funcional do tecido ou órgão.
imunidade inata; inflamação; autoimunidade; PAMPs; receptores toll-like
The immune system consists of an intricate network of organs, cells, and molecules responsible for maintaining the body's homeostasis and responding to aggression in general. Innate immunity operates in conjunction with adaptive immunity and is characterized by rapid response to aggression, regardless of previous stimulus, being the organism first line of defense. Its mechanisms include physical, chemical and biological barriers, cellular components, as well as soluble molecules. The organism first line of defense against tissue damage involves several steps closely integrated and constituted by different components of this system. The aim of this review is to restore the foundations of this response, which has high complexity and consists of several components that converge to articulate the development of adaptive immune response. We selected some of the following steps to review: perception and molecular recognition of aggressive agents; activation of intracellular pathways, which result in vascular and tissue changes; production of a myriad of mediators with local and systemic effects on cell activation and proliferation, synthesis of new products involved in the chemoattraction and migration of cells specialized in destruction and removal of offending agent; and finally, tissue recovery with restoration of functional tissue or organ.
innate immunity; inflammation; autoimmunity; PAMPs; Toll-like receptors
ARTIGO DE REVISÃO
Sistema imunitário - parte II. fundamentos da resposta imunológica mediada por linfócitos T e B
Danilo Mesquita JúniorI; Júlio Antônio Pereira AraújoII; Tânia Tieko Takao CatelanIII; Alexandre Wagner Silva de SouzaIV; Wilson de Melo CruvinelI; Luís Eduardo Coelho AndradeVI; Neusa Pereira da SilvaVI
IDoutorando em Reumatologia da Universidade Federal de São Paulo - UNIFESP
IIMestre em Reumatologia pela Universidade Federal de São Paulo - UNIFESP
IIIMestrando em Reumatologia da Universidade Federal de São Paulo - UNIFESP
IVMédico Assistente da Disciplina de Reumatologia da Universidade Federal de São Paulo - UNIFESP
VDoutorando em Reumatologia da Universidade Federal de São Paulo - UNIFESP e Professor-assistente de imunologia dos cursos de Medicina e Biomedicina da Pontifícia Universidade Católica de Goiás - PUC-Goiás
VIProfessor Adjunto da Disciplina de Reumatologia da Universidade Federal de São Paulo (UNIFESP)
Endereço para correspondência Endereço para correspondência: Neusa Pereira da Silva Rua Botucatu, 740, 3º andar CEP: 04023-900, São Paulo, Brasil Tel/fax: 55 (11) 5576-4239 Email: npsilva@unifesp.br
RESUMO
O sistema imunológico é constituído por uma intrincada rede de órgãos, células e moléculas, e tem por finalidade manter a homeostase do organismo, combatendo as agressões em geral. A imunidade inata atua em conjunto com a imunidade adaptativa e caracteriza-se pela rápida resposta à agressão, independentemente de estímulo prévio, sendo a primeira linha de defesa do organismo. Seus mecanismos compreendem barreiras físicas, químicas e biológicas, componentes celulares e moléculas solúveis. A primeira defesa do organismo frente a um dano tecidual envolve diversas etapas intimamente integradas e constituídas pelos diferentes componentes desse sistema. A presente revisão tem como objetivo resgatar os fundamentos dessa resposta, que apresenta elevada complexidade e é constituída por diversos componentes articulados que convergem para a elaboração da resposta imune adaptativa. Destacamos algumas etapas: reconhecimento molecular dos agentes agressores; ativação de vias bioquímicas intracelulares que resultam em modificações vasculares e teciduais; produção de uma miríade de mediadores com efeitos locais e sistêmicos no âmbito da ativação e proliferação celulares, síntese de novos produtos envolvidos na quimioatração e migração de células especializadas na destruição e remoção do agente agressor, e finalmente a recuperação tecidual com o restabelecimento funcional do tecido ou órgão.
Palavras-chave: imunidade inata, inflamação, autoimunidade, PAMPs, receptores toll-like.
ORIGEM
Células tronco pluripotentes da medula óssea dão origem às células progenitoras mieloides e linfoides. Os progenitores linfoides, por sua vez, dão origem aos linfócitos T, B e células NK. As células que vão se diferenciar em linfócitos T (LT) deixam a medula óssea e migram para o timo, onde ocorre todo o processo de seleção e maturação. Apenas os linfócitos T maduros deixam o timo e caem na circulação. As células, que vão se diferenciar em linfócitos B (LB), permanecem na medula óssea e, ao final de sua maturação, deixam a medula e entram na circulação, migrando para os órgãos linfoides secundários (Figura 1).
LINFÓCITOS B
Os LB são inicialmente produzidos no saco vitelino, posteriormente, durante a vida fetal, no fígado e finalmente na medula óssea. As células que vão se diferenciar em LB permanecem na medula óssea durante sua maturação e os LB maduros deixam a medula e entram na circulação, migrando para os órgãos linfoides secundários1,2,3 (Figura 1).
As moléculas responsáveis pelo reconhecimento de antígenos nos LB são as imunoglobulinas de membrana, IgM e IgD. Estas são a contrapartida dos receptores de linfócitos T (TCR) e por analogia são denominadas receptores de linfócitos B (BCR) em alguns contextos.
CARACTERÍSTICAS DAS IMUNOGLOBULINAS
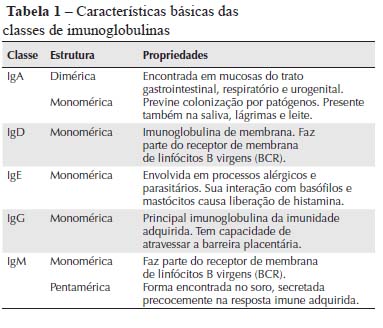
Cada molécula de imunoglobulina (Ig) é constituída por duas cadeias pesadas e duas cadeias leves ligadas por pontes dissulfeto. Existem cinco tipos de cadeias pesadas denominadas α, γ, δ, ε e µ, que definem as classes de imunoglobulina IgA, IgG, IgD, IgE e IgM. As cadeias leves são de dois tipos, κappa (κ) e lambda (λ). A especificidade de ligação ao antígeno é definida pela porção variável (Fab) da molécula, constituída pela união das regiões variáveis das cadeias leve e pesada da imunoglobulina. As propriedades características de cada classe de Ig podem ser vistas na Tabela 1.1,3
ORGANIZAÇÃO DOS GENES DAS IMUNOGLOBULINAS
Cada cadeia de imunoglobulina é formada a partir de segmentos gênicos que se rearranjam em uma sequência específica para constituir a cadeia completa (Figura 1). A porção variável da cadeia pesada das imunoglobulinas é codificada pelos segmentos VH, DH e JH. Há mais de 50 genes VH, ~25 DH e 6 JH dispostos sequencialmente no cromossomo, seguidos das regiões constantes Cµ, Cδ, Cγ3, Cγ1, Cα1, Cγ4, Cγ2, Cε1 e Cα2. Nas cadeias leves os segmentos são: ~35 Vκ, 5 Jκ e um só segmento Cκ; ~30 Vλ e 4 conjuntos JλCλ.2
MATURAÇÃO DOS LINFÓCITOS B
A maturação dos linfócitos B tem início a partir das células pró-B que expressam três genes, TdT, RAG1 e RAG2, que comandam a recombinação gênica necessária para a produção de imunoglobulinas. A montagem da cadeia pesada se inicia com a combinação aleatória de um segmento D e um J, que a seguir se unem a um segmento V, definindo a especificidade de reconhecimento do anticorpo que será formado, independentemente da porção constante que fará parte da cadeia completa. Essa cadeia pesada se associa a uma cadeia invariável e é expressa na superfície como um pré-BCR, juntamente com as moléculas assessórias Igα e Igβ. Em seguida ocorre o rearranjo da cadeia leve k e, na falha desta, da cadeia λ. Cada LB apresenta, portanto, um único tipo de cadeia leve associado à cadeia pesada. O sucesso na expressão de uma IgM completa na superfície do LB leva à progressão da maturação com subsequente produção de IgD de membrana.3
É importante ressaltar que todo rearranjo gênico ocorre no início da maturação do LB, no estágio pré-B, ainda na medula óssea, e de modo totalmente independente de qualquer contato com antígeno.2
O processo combinatório dos diferentes segmentos que compõem as porções variáveis das cadeias pesadas e leves e as diferentes possibilidades de associação entre elas resultam em cerca de 1011 especificidades diferentes de reconhecimento pelas imunoglobulinas.1
A fim de restringir esse repertório, mecanismos de seleção positiva e negativa atuam durante a maturação dos LB. Na seleção positiva, os LB imaturos expressando moléculas funcionais de Ig de membrana recebem sinais de sobrevivência para prosseguir a maturação. No processo de seleção negativa, os LB imaturos, ainda na medula óssea, que reconhecem antígenos próprios com alta afinidade sofrem apoptose ou entram em um processo denominado edição de receptor, no qual os genes RAG são novamente ativados e outra combinação V-J de cadeia leve é gerada em substituição à anterior, auto-reativa.1,2,3 Alguns detalhes da dinâmica de maturação das células B estão apresentados na Figura 1.
CARACTERIZAÇÃO IMUNOFENOTÍPICA
Os estágios de maturação dos LB são caracterizados por um padrão específico de expressão de genes de imunoglobulinas e de outras proteínas de membrana que servem como marcadores fenotípicos desses estágios de desenvolvimento (Figura 2). Essas moléculas de superfície cumprem funções específicas importantes nas diferentes fases de maturação do LB. A existência de anticorpos monoclonais específicos para cada um desses marcadores permite que sejam feitos estudos sobre a distribuição e a dinâmica da linhagem de LB. Ademais, monoclonais contra algumas dessas moléculas de superfície também podem ser utilizados com finalidade terapêutica, atingindo determinadas subpopulações de células da linhagem B.
ATIVAÇÃO DOS LINFÓCITOS B
Os LB são responsáveis pela imunidade humoral que se caracteriza pela produção e liberação de anticorpos capazes de neutralizar, ou até mesmo destruir, os antígenos (Ag) contra os quais foram gerados. Para tal, os LB devem ser ativados, o que acarreta um processo de proliferação e diferenciação, que culmina na geração de plasmócitos com produção de imunoglobulinas com alta afinidade para o epítopo antigênico que originou a resposta. Para ativação, é preciso que o BCR ligue-se a um epítopo antigênico, o que desencadeia uma sequência de eventos intracelulares. Além do reconhecimento do antígeno, a ativação dos LB depende também de um segundo sinal ativador.1,2
O complexo do receptor de LB (BCR) inclui, além da imunoglobulina de membrana, duas cadeias peptídicas, Igα e Igβ, que têm função de dar início à sinalização intracelular após o encontro com o antígeno.1,2 As moléculas Igα e Igβ contêm motivos de ativação (ITAMs) que são fosforilados após ligação do antígeno ao complexo BCR, e ativam fatores que promovem a transcrição de genes envolvidos na proliferação e diferenciação dos LB (Figura 3-A).2,7
Os LB funcionam também como células apresentadoras de antígeno, após interiorizarem e processarem o Ag ligado ao receptor de superfície (BCR). Os peptídeos gerados pelo processamento são expressos na membrana dos LB ligados às moléculas do complexo maior de histocompatibilidade (MHC) classe II, para apresentação aos LTCD4+ (auxiliares). A interação do complexo peptídeo/MHC classe II com o receptor de LT (TCR) inicia uma cadeia de eventos que levam os LT auxiliares à expansão clonal e produção de citocinas que estimulam a proliferação e diferenciação dos LB (Figura 3-B).1,2,7
Proteínas do complemento também fornecem sinais secundários para ativação por meio do receptor para o fragmento C3d, denominado CR2 ou CD21, expresso na superfície dos LB. O CD21 forma um complexo com outras duas proteínas de membrana, CD19 e CD81, permitindo o reconhecimento simultâneo do C3d e do antígeno pelo BCR. Esta ligação promove o início da cascata de sinalização de ambos os receptores, gerando uma resposta muito maior se comparada à resposta do antígeno não ligado à molécula C3d.1,2 A possibilidade da ligação C3d/CR2 atuar como o segundo sinal para a ativação dos LB garante o desencadeamento da resposta frente a microorganismos e antígenos que ativam o complemento. Esse é também um mecanismo de amplificação da resposta imune humoral, uma vez que anticorpos capazes de ativar o complemento vão resultar em maior estímulo dos LB.1,8
Recentemente tem sido destacado o potencial dos LB em desempenhar suas funções após ativação de outros receptores relacionados à resposta imune inata, tais como os Toll-Like Receptors (TLRs). Foi demonstrado que os LB expressam a maioria dos TLRs, tais como TLR-2, TLR-3, TLR-5 TLR-7 e TLR-9, respondendo a uma enorme variedade de ligantes que podem ser proteicos, polissacarídicos, lipídicos e outros.8
A resposta dos LB a antígenos peptídicos requer a ajuda dos LT auxiliares e esses antígenos são, por isso, denominados "antígenos T dependentes". Muitos antígenos não proteicos, com epítopos repetitivos, não necessitam da cooperação dos LT e são denominados "antígenos T independentes".1
CARACTERÍSTICAS DA RESPOSTA T DEPENDENTE
A resposta humoral frente a Ag proteicos requer o reconhecimento do antígeno pelos LT auxiliares e sua cooperação com os LB antígeno-específicos, estimulando a expansão clonal dos LB, a mudança de classe, a maturação de afinidade e a diferenciação em LB de memória.1
Os LT expressam na sua superfície moléculas CD40L, que interagem com seu ligante, CD40, presente na superfície de LB, e expressam também CD28 que se liga às moléculas B7-1 (CD80) e B7-2 (CD86), cuja expressão na membrana dos LB ativados é significantemente aumentada. Esses dois pares de moléculas, CD40/CD40-L e CD28/B7, permitem a transmissão dos sinais de estímulo e induzem a produção de enorme variedade de citocinas (Figura 3-B).1,2
MUDANÇA DE CLASSE DE IMUNOGLOBULINAS
A etapa de diferenciação caracteriza-se por alterações significativas na morfologia dos LB e também pela troca da porção constante da cadeia pesada de IgM ou IgD para IgG, IgA ou IgE, processo conhecido como mudança de classe. Esta etapa envolve eventos moleculares complexos como rearranjo ao nível do DNA genômico e splicing alternativo ao nível do RNA mensageiro. Neste processo as porções variáveis das cadeias pesada e leve permanecem as mesmas e consequentemente a especificidade antigênica do anticorpo não é alterada, mas a resposta imune torna-se mais diversificada, uma vez que as diferentes classes de Ig apresentam diferentes características funcionais.1,2
O sinal gerado pela interação CD40/CD40L parece atuar de forma global no início do processo de mudança de classe. Pacientes com um tipo de deficiência de imunoglobulinas ligada ao X apresentam baixa expressão de CD40L em LT ativados, consequentemente os LB apresentam um defeito no processo de mudança de classe de imunoglobulinas com aumento nos níveis séricos de IgM mas não de IgG, IgA ou IgE, tornando o paciente mais susceptível a infecções piogênicas e ao desenvolvimento de doenças autoimunes e linfoma.1,2
MATURAÇÃO DA AFINIDADE
No início da resposta, há Ag suficiente para interagir com LB tanto de alta quanto de baixa afinidade e os anticorpos produzidos são heterogêneos. No decorrer da resposta, quantidades maiores de anticorpos se ligam ao Ag diminuindo sua disponibilidade. Nessa fase, os LB com Ig de maior afinidade, que interagem melhor com o determinante antigênico, são preferencialmente estimulados. Esse processo é denominado maturação da afinidade. O aumento da afinidade de anticorpos para um dado Ag, durante a progressão da resposta humoral T dependente, é resultado de mutação somática nos genes de Ig durante a expansão clonal. Algumas destas mutações vão gerar células capazes de produzir anticorpos de alta afinidade, contudo, outras podem resultar na diminuição ou mesmo na perda da capacidade de ligação com o antígeno. A seleção positiva garante a sobrevivência seletiva de LB produtores de anticorpos de afinidade progressivamente maior. Nesse processo é fundamental a interação CD40/CD40L bem como a presença de fatores solúveis derivados dos linfócitos T e por isso a maturação de afinidade ocorre somente na resposta aos antígenos T dependentes.1,2,3
Pelo fato de que persistem LB de memória após uma exposição a antígenos T dependentes, os anticorpos produzidos numa resposta secundária apresentam afinidade média mais alta que os produzidos na primária. Esse processo é importante na eliminação de antígenos persistentes ou recorrentes.1,2
CARACTERÍSTICAS DAS RESPOSTAS PRIMÁRIAS E SECUNDÁRIAS DE ANTICORPOS
As respostas primárias e secundárias dos anticorpos para os antígenos proteicos diferem qualitativa e quantitativamente.
Resposta Primária
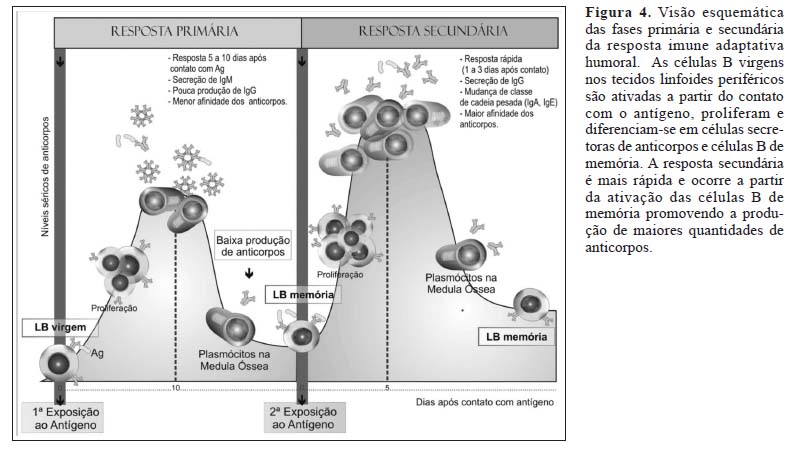
O primeiro contato com um antígeno, por exposição natural ou vacinação, leva à ativação de LB virgens, que se diferenciam em plasmócitos produtores de anticorpos e em células de memória, resultando na produção de anticorpos específicos contra o antígeno indutor. Após o início da resposta, observa-se uma fase de aumento exponencial dos níveis de anticorpos, seguida por uma fase denominada platô, na qual os níveis não se alteram. Segue-se a última fase da resposta primária, a fase de declínio, na qual ocorre uma diminuição progressiva dos anticorpos específicos circulantes.1,2
Resposta Secundária
Ao entrar em contato com o antígeno pela segunda vez, já existe uma população de LB capazes de reconhecer esse antígeno devido à expansão clonal e células de memória geradas na resposta primária. A resposta secundária difere da primária nos seguintes aspectos: a dose de antígeno necessária para induzir a resposta é menor; a fase de latência é mais curta e a fase exponencial é mais acentuada; a produção de anticorpos é mais rápida e são atingidos níveis mais elevados; a fase de platô é alcançada mais rapidamente e é mais duradoura e a fase de declínio é mais lenta e persistente (Figura 4).1,2,3
A magnitude da resposta secundária depende também do intervalo de tempo desde o contato inicial com o antígeno. A resposta será menor se o intervalo for muito curto ou muito longo. Se for muito curto, os anticorpos ainda presentes formam complexos Ag/Ac que são rapidamente eliminados; se for muito longo, é possível que as células de memória tenham diminuído gradualmente com o tempo, embora a capacidade para deflagrar uma resposta secundária possa persistir por meses ou anos. O período ótimo para a indução de resposta secundária é logo após a queda do nível de anticorpos da resposta primária abaixo dos limites de detecção.1,2
Nos dois tipos de resposta, primária e secundária, há a produção dos isótipos IgM e IgG, porém, na resposta primária IgM é a principal Ig e a produção de IgG é menor e mais tardia. Na resposta secundária, a IgG é a imunoglobulina predominante. Nas duas respostas, a concentração de IgM sérica diminui rapidamente de maneira que, após uma ou duas semanas, observa-se queda acentuada enquanto a produção de IgG é persistente.1,2 Vale a pena enfatizar que os testes imunoenzimáticos muito sensíveis podem registrar níveis baixos ou residuais de IgM por meses em alguns casos.
CARACTERÍSTICAS DA RESPOSTA T INDEPENDENTE
Antígenos T independentes podem estimular a produção de anticorpos na ausência total ou relativa de LT. Esses antígenos são usualmente moléculas não proteicas, poliméricas, que estimulam a produção de Ig de baixa afinidade pertencentes, na sua maioria, à classe IgM. Como, geralmente, não há ativação de LT, não serão geradas as citocinas necessárias para a mudança de classe, maturação de afinidade ou formação de LB de memória. Raramente na resposta a antígenos T independentes ocorre mudança para outros isótipos.1,2,3
Um exemplo da importância da resposta a antígenos T independentes é a imunidade humoral frente a polissacarídeos bacterianos, um mecanismo decisivo na defesa do hospedeiro contra infecções por bactérias encapsuladas. Por essa razão, indivíduos com deficiências congênitas ou adquiridas que prejudiquem a resposta humoral são especialmente suscetíveis a infecções, muitas vezes fatais, por bactérias encapsuladas. Outro exemplo de resposta aos antígenos T independentes são os anticorpos naturais, presentes na circulação de indivíduos normais e produzidos aparentemente sem exposição antigênica. Muitos destes anticorpos naturais reconhecem carboidratos com baixa afinidade e acredita-se que sejam produzidos por LB peritoneais, isto é, células B1, estimuladas por bactérias que colonizam o trato gastrointestinal, e por LB da zona marginal dos órgãos linfoides. Anticorpos contra antígenos glicolipídicos A e B do grupo sanguíneo são outro exemplo de anticorpos naturais.1,3
CÉLULAS B REGULADORAS (BREGS)
O conceito de LB reguladores (BREGS) foi introduzido por Bhan e Mizoguchi11 a partir de estudo com camundongos LB deficientes (B-) cruzados com camundongos que não expressavam TCRα (TCRα-/-) e desenvolviam espontaneamente colite crônica. Os camundongos duplamente afetados (B-/TCRα-/-) apresentaram doença mais precocemente e inflamação mais exacerbada do que animais TCRα-/-, mas que tinham LB. De modo surpreendente foi comprovado que, naquele modelo experimental, era possível minimizar o efeito da colite no grupo B-/TCRα-/-, pela administração de imunoglobulinas purificadas e de autoanticorpos anticélulas epiteliais colônicas. A melhora observada foi acompanhada de aumento no clearance de células apoptóticas favorecido pelos autoanticorpos produzidos pelos LBREGS.
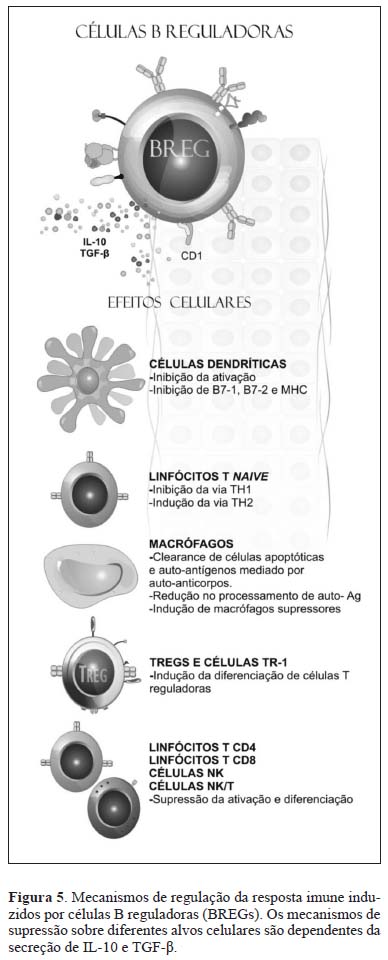
Outros estudos em modelos experimentais comprovaram a existência de células com capacidade imunomoduladora no pool de LB que, em um ambiente cronicamente inflamado, se diferenciam em um fenótipo com alta expressão de CD1d, capacidade de produção de IL-10 e habilidade para suprimir a resposta inflamatória. Os LBREGS dependem de interação antigênica e estimulação via molécula CD40L e B7, mas, uma vez ativadas, produzem IL-10 e TGF-β suprimindo a ativação e diferenciação de LTCD4+, LTCD8+ e células NK/T, inibem a ativação de células dendríticas e estimulam a diferenciação de LT reguladores. Mediante contato dos LBREGS com LT virgens há inibição da ativação do LT e da diferenciação em TH1 (Figura 5).12,13
O estudo dos LBREGS em modelos animais deixa claro o papel regulador dessas células nas diferentes enfermidades. A comprovação da existência dessas células no homem será de grande relevância para a compreensão das doenças autoimunes. Mais do que entender a diversidade de efeitos das citocinas anti-inflamatórias que asseguram as funções dos LBREGS, o seu estudo reforça as evidências da produção de autoanticorpos de modo fisiológico com finalidade protetora.11,12,13
SUBTIPOS ESPECIAIS DE LINFÓCITOS B EFETORES
Além do LB convencional (B2) existem outros subtipos de LB como os B1 e os LB da zona marginal (MZ-B) do baço, que atuam como verdadeiras sentinelas em sítios anatômicos específicos como: cavidade peritoneal, cavidade pleural e zona periférica do baço, respectivamente. Estes subtipos assemelham-se muito aos linfócitos Tγδ e aos linfócitos NK/T por sua localização em regiões específicas e função efetora com a utilização de receptores altamente conservados, mas capazes de reconhecer uma variedade limitada de patógenos. Ambos os subtipos exercem tanto as funções de células da imunidade inata como da resposta adaptativa. Por pertenceram aos dois tipos de resposta, provavelmente essas células representam uma forma primitiva e conservada de imunidade.1,2,14
LINFÓCITOS B1
Os LB1 constituem uma subpopulação distinta dos LB convencionais (B2). Possuem forte capacidade autorrenovadora e são encontrados principalmente na cavidade pleural, peritoneal e em menor quantidade no baço. São responsáveis pela produção da maior parte das IgM naturais e também da maioria dos anticorpos de classe IgM, incluindo anticorpos contra LT, dsDNA, eritrócitos e anticorpos que reconhecem constituintes bacterianos comuns. Tem sido sugerido que os LB1 representam uma relíquia evolutiva originada de uma linhagem primitiva da imunidade inata que se tornou uma célula linfoide do sistema adaptativo, mas ainda mantém muitas características de uma célula do sistema inato. Os LB1 parecem representar a primeira linha de defesa contra infecções sistêmicas por vírus e bactérias e são de fundamental importância para o equilíbrio homeostático do organismo. Produzem anticorpos polirreativos e de baixa afinidade, importantes para remoção de células envelhecidas e/ou que sofreram estresse celular e proteção contra o desenvolvimento de doenças autoimunes e arterosclerose.15,16
Os LB1 expressam baixos níveis dos marcadores B220/ CD45R, CD19, Mac-1 e IgD de superfície, altos níveis de IgM de superfície e são subdivididos em 2 grupos principais: B1a e B1b. Os LB1a expressam a molécula CD5 de superfície em níveis intermediários, enquanto os LB1b são CD5- e capazes de diferenciação em células com características mielomonocíticas com função e morfologia semelhante ao macrófago. Foi verificado que a secreção de IL-10 pelos LB1 modula a atividade fagocítica do macrófago in vitro, e a apresentação de antígenos na presença de IL-10 induz à tolerância ou diferenciação de LT em células supressoras, indicando um possível papel imunomodulador dessa população celular.
Linfócitos B da zona marginal
As principais populações de LB efetoras do baço são os LB da zona marginal (MZ-B) e os LB foliculares (FC-B). Os MZ-B são populações especializadas de LB localizadas na região periférica ou marginal do baço, região denominada sinusoide esplênico. Neste sítio estão localizados também os macrófagos da zona marginal que junto com os MZ-B representam a primeira linha de defesa rápida, contra antígenos particulados da corrente sanguínea. No entanto, fenotipicamente, estes linfócitos são muito semelhantes aos LB convencionais, sendo classificadas também no grupo LB2.14
Os FC-B, localizados nos folículos linfoides, atuam em um estágio mais avançado da resposta adquirida, gerando LB de memória e plasmócitos por meio da resposta humoral T dependente comentada anteriormente nesta revisão.14
Os MZ-B, assim como os LB1, possuem um repertório de reconhecimento antigênico limitado, normalmente autorreativo. Mas, ainda que autorreativos, eles são também polirreativos, com especificidade importante tanto para remoção de restos celulares, como para o reconhecimento de antígenos bacterianos e virais. Outra característica importante destas células é a propriedade que elas têm de gerar as chamadas respostas humorais T independentes, ou seja, podem responder avidamente a estímulos antigênicos e se diferenciarem em células secretoras de anticorpos sem a necessidade de auxilio de LT. Juntos, MZ-B e LB1 fazem parte das chamadas repostas de memória natural, pois geram rapidamente células efetoras nos estágios iniciais da resposta imune.14
LINFÓCITOS T
As células pré-T entram no córtex tímico pelas artérias e durante o processo de seleção e maturação migram em direção à medula, de onde saem para a circulação. O processo de maturação dos LT envolve a expressão de um receptor de células T (TCR) funcional e dos co-receptores CD4 e/ou CD8.1
Os LT só reconhecem antígenos processados, apresentados por moléculas de MHC na superfície de uma célula apresentadora de antígeno. O TCR é expresso na membrana dos LT em associação com um complexo denominado CD3, composto por cinco diferentes proteínas da família das imunoglobulinas. O TCR é responsável pelo reconhecimento do complexo peptídeo-molécula de MHC, e o CD3, pela sinalização celular subsequente.1
RECEPTOR DE CÉLULAS T (TCR)
O TCR é formado por duas cadeias peptídicas da superfamília das imunoglobulinas, com uma região variável e uma região constante, formadas a partir de segmentos gênicos que durante a maturação dos LT sofrem recombinação de forma semelhante à do BCR. Em cerca de 95% dos LT circulantes o TCR é formado pelas cadeias α e β. Uma pequena porcentagem de LT apresenta TCR composto por cadeias γ e δ. As cadeias α e δ são formadas pela combinação de três tipos de segmentos (V, J e C) e as cadeias β e γ, quatro tipos (V, D, J e C). Há ~70 diferentes segmentos Vα, 60 Jα e 1 único Cα. Para a cadeia β, há ~50 Vβ seguidos de dois conjuntos compostos de 1 Dβ, 6-7 jβ e 1 Cβ. Nas cadeias γ e δ a variabilidade é menor.17
A grande diversidade de repertório dos LT maduros é gerada pelo processo de recombinação somática na qual um dado gene V, entre os diversos possíveis, liga-se a um dado gene J ou combinação DJ. A diversidade de repertório potencial dos LT é algo em torno de 1016. A recombinação entre os diferentes segmentos é mediada por enzimas expressas apenas durante a fase de maturação dos linfócitos.1,17
MATURAÇÃO DOS LINFÓCITOS T
O processo de maturação dos LT ocorre em etapas sequenciais que envolvem a recombinação somática e expressão do TCR, proliferação das células, expressão dos co-receptores CD4 e CD8 e seleção positiva e negativa induzida por apresentação de antígenos próprios por células do estroma tímico.17
Inicialmente ocorre o rearranjo dos genes da cadeia β do TCR e, em seguida, da cadeia α. Os timócitos, ou linfócitos imaturos, começam a expressar baixos níveis de CD4 e CD8 na superfície, sendo, portanto, duplo-positivos. Nesta fase, os timócitos migram em direção à medula tímica e entram em contato com Ag próprios apresentados pelas células epiteliais do estroma tímico. Apenas aqueles que se ligam ao complexo MHC/Ag com afinidade adequada recebem estímulo para sobreviver (seleção positiva). Os timócitos cujo TCR não apresenta afinidade pelo MHC próprio sofrem apoptose pela falta de estímulo (morte por negligência).17 A interação com moléculas MHC de classe I ou II determina a diferenciação do timócito em LT CD8+ ou CD4+, respectivamente. Continuando a maturação, os timócitos αβ que sobreviveram à seleção positiva e expressam apenas CD4 ou CD8 entram em contato na medula com células dendríticas e macrófagos, células apresentadoras de antígenos (APCs) extremamente eficientes, que apresentam Ag próprios associados ao MHC. Os timócitos imaturos que interagem com muita afinidade com esses complexos morrem por apoptose (seleção negativa). As células que sobrevivem tornam-se LT maduros, prontos para deixarem o timo e exercerem suas funções na periferia. Apenas cerca de 5% das células que entram no timo tornam-se LT maduros17 (Figura 1).
Este processo de educação tímica visa garantir que os LT circulantes sejam tolerantes aos Ag próprios, mas capazes de reconhecer Ag estranhos ao organismo quando apresentados pelo MHC próprio. Entretanto, os mecanismos centrais de tolerância não são absolutos uma vez que LT autorreativos podem ser encontrados na periferia. Entre outros mecanismos de regulação periférica, destacam-se diferentes populações de LT reguladores que atuam na periferia impedindo o desenvolvimento de autoimunidade.17
LT EFETORES
Existem diversos subtipos de LT efetores. Classicamente os dois principais subtipos são os auxiliares (Th) e os citotóxicos, que apresentam um receptor TCR αβ e as moléculas correceptoras, CD4 ou CD8, respectivamente. Os LT CD4 (Th) são responsáveis por orquestrar outras células da resposta imune na erradicação patógenos e são também muito importantes na ativação dos LB, macrófagos ou mesmo LT CD8. Os LT CD8 estão envolvidos principalmente nas respostas antivirais e possuem também atividade antitumoral. Ambos os subtipos apresentam papel muito importante no controle de patógenos intracelulares. Outros subtipos de LT efetores, encontrados especialmente nas barreiras de mucosa e na pele, são os LT γδ. Essas células são importantes nas respostas imunes contra antígenos comumente encontrados nesses sítios anatômicos e representam um elo entre a resposta imune inata e adaptativa (Figura 6).18
Linfócitos T CD4 Auxiliares (Th)
Os LTh são subdivididos funcionalmente pelo padrão de citocinas que produzem. Durante o estímulo fornecido por uma APC, um linfócito precursor Th0 pode se tornar um linfócito Th1, Th2 ou Th17, na dependência do ambiente de citocinas presente. Embora morfologicamente indistinguíveis essas células apresentam distintos padrões de citocinas secretadas e, consequentemente, diferentes respostas efetoras19 (Figura 6).
Linfócitos Th1
Os LTh1 produzem grandes quantidades de IL-2, que induz proliferação de LT (incluindo os próprios LTCD4 de maneira autócrina) e também induz a proliferação e aumenta a capacidade citotóxica dos LT CD8. A outra citocina produzida em grandes quantidades pelos LTh1 é o INF-γ, uma citocina muito importante na ativação de macrófagos infectados com patógenos intracelulares como micobactérias, protozoários e fungos, que apresenta também um papel relevante na ativação de LT CD8.18 Os pacientes com síndrome de imunodeficiência em que o receptor de INF-γ está ausente sofrem de infecções graves por micobactérias.20 Existe um ciclo de retroalimentação positiva na ação do INF-γ sobre outros LThO, induzindo sua polarização para a via de diferenciação Th1 e inibindo a via Th2.19 A resposta Th1 é essencial para o controle de patógenos intracelulares, sendo possível que contribua para a patogênese de doenças reumáticas autoimunes como artrite reumatoide (AR) e esclerose múltipla (EM). Entretanto, nos últimos anos, uma nova subpopulação de LT, os LTh17, tem sido responsabilizada pelo processo fisiopatológico dessas enfermidades.21
Linfócitos Th2
A segunda população Th muito importante nas respostas imunes humorais é o LTh2, que produz IL-4, IL-5, IL-6 e IL-10, favorecendo a produção de anticorpos.18 As respostas Th2 estão associadas com as doenças alérgicas e infecções por helmintos, uma vez que a IL-4 induz a troca de classe de imunoglobulinas nos linfócitos B para IgE e a IL-5 induz a produção e ativação de eosinófilos. De forma análoga ao INF-γ, a IL-4 também promove retroalimentação positiva para a via Th2 e suprime a via Th1. Em situações de hipersensibilidade imediata, como nas doenças alérgicas, a terapia visa a dessensibilização imune Th2 e indução de respostas Th1 alérgeno-específicas.18,19 Já em doenças sabidamente causadas por LTh1, as citocinas Th2 têm sido consideradas protetoras, portanto a busca pela alteração no padrão de resposta imune de Th1 para Th2 tem sido muito estudada, visando a melhora ou o restabelecimento da tolerância imunológica. Entretanto, este paradigma bipolar tem sido reformulado recentemente em função do reconhecimento de novos subtipos de LT, principalmente as células Th17.18,19
Linfócitos Th17
Os LTh17 representam um novo subtipo de LT efetores importantes na proteção contra infecção por microorganismos extracelulares. Foram originalmente descritos em modelos experimentais de doenças autoimunes como encefalite autoimune e artrite induzida por colágeno, que antes se acreditava serem mediadas predominantemente por células Th1. Esta nova via de diferenciação Th começou a ser elucidada com a descoberta da citocina IL-23 que, juntamente com IL-1 e IL-6, pode levar ao desenvolvimento de doenças autoimunes em modelos murinos por seu importante papel pró-inflamatório e indutor da diferenciação e ativação de LTh17.21 Os LTh17 produzem citocinas IL-22, IL-26 e citocinas da família IL-17. As citocinas da família IL-17 são potentes indutoras da inflamação, induzindo à infiltração celular e produção de outras citocinas pró-inflamatórias.21,22
A produção desregulada de IL-17 está associada a várias condições autoimunes, como: esclerose múltipla, doença intestinal inflamatória, psoríase e lúpus. Em pacientes com artrite reumatoide, níveis aumentados de IL-17 foram encontrados na sinóvia, onde atua como um importante fator na ativação dos osteoclastos e reabsorção óssea.21,22
A via de diferenciação Th17 é antagonizada pelas citocinas Th1 e Th2 e, em alguns modelos experimentais de autoimunidade causada por LTh17, as citocinas Th1 e Th2 têm se mostrado protetoras. A exata compreensão dos mecanismos de polarização Th em humanos é fundamental para um melhor entendimento dos mecanismos fisiopatológicos das doenças inflamatórias crônicas e para o possível desenvolvimento de formas mais eficazes de imunoterapia.21
LT CITOTÓXICOS (CD8)
Os LT CD8 reconhecem antígenos intracitoplasmáticos apresentados por moléculas MHC de classe I, que são expressas por praticamente todas as células nucleadas. Células infectadas por vírus e células tumorais normalmente são reconhecidas pelos LT CD8.18 Após adesão às células alvo apresentando um antígeno associado ao MHC e coestímulo adequado, os LT CD8 proliferam e, em um encontro subsequente, podem eliminar por citotoxicidade qualquer célula que apresente esse antígeno especifico, independente da presença de moléculas coestimulatórias. Os LT CD8 induzem a via de morte celular programada (apoptose) na célula alvo pela ação de perforinas e granzimas e também podem levar à apoptose pela expressão do receptor Fas L (CD95) que interage com a molécula Fas nas células alvo.18
LT γδ
Uma pequena população de LT periféricos possui TCR com diversidade limitada, composto por cadeias γδ. Essas células são comumente encontradas nas primeiras linhas de defesa do organismo, como as barreiras mucosas e a pele, onde atuam como verdadeiras sentinelas de reconhecimento de padrões moleculares, reconhecendo e apresentando antígenos, respondendo a eles e contribuindo também para ativação e proliferação de células do sistema imune.23 Essas células diferem dos LT αβ, pois seu TCR pode reconhecer antígenos mesmo na ausência de apresentação pela molécula de MHC, sendo então consideradas verdadeiras sentinelas do organismo.23,24 Os LT γδ apresentam também memória imunológica, respondendo mais vigorosamente em um segundo encontro antigênico. Os LT γδ exercem suas funções efetoras de maneiras variadas, podendo, por exemplo, apresentar citotoxicidade (característica primária de LTCD8). Estudos terapêuticos têm explorado esta característica citotóxica contra antígenos tumorais. Os LTγδ exercem também função auxiliadora liberando citocinas como INF-γ (Th1) ou IL-4 (Th2), podendo inclusive atuar como APCs eficientes, pois possuem alta capacidade de apresentar antígenos aos LTαβ, mediando sua ativação e proliferação. Os LTγδ são também capazes de ativar células dendríticas e LB, ampliando assim tanto a resposta imune celular como humoral.
Os LTγδ trazem à tona a discussão de um dos dogmas contemporâneos da imunologia, a divisão do sistema imune em sistema inato e adaptativo. O sistema imune inato responde rapidamente ao reconhecer padrões moleculares derivados de patógenos e é capaz de induzir repostas imunes adaptativas pela liberação de citocinas e apresentação de antígenos. Em contraste, a reposta adaptativa age lentamente em um encontro antigênico inicial, mas desenvolve memória imunológica e responde rápida e vigorosamente em um encontro subsequente (Figura 4). Os LTγδ podem ser incluídos em ambos os braços da resposta imune, uma vez que exercem tanto as funções de células da imunidade inata como da resposta adaptativa. Sua participação nos dois tipos de resposta sugere que essas células representam uma forma primitiva e conservada de imunidade.23
LT REGULADORES
Várias evidências demonstram a importância das diferentes populações de LT reguladores na manutenção da autotolerância imunológica e no controle das respostas autoimunes. Assim, há grande interesse no estudo dessas células e de sua potencial aplicação no tratamento das doenças autoimunes.25
As células com função imunorreguladora apresentam como característica básica a capacidade de produção de citocinas imunossupressoras, como IL-4, IL-10 e TGF-β. Atuam em uma complexa rede de mecanismos reguladores destinados a assegurar a modulação das respostas imunológicas frente aos diversos antígenos provenientes de agentes infecciosos, tumores, aloantígenos, autoantígenos e alérgenos. Entre os LT com função reguladora estão os LT reguladores de ocorrência natural (TREGS CD4+CD25+), descritos por Sakaguchi et al (1995),26 os LTR1 que produzem IL-10 e suprimem o desenvolvimento de algumas respostas de LT in vivo, e os LTh3, capazes de impedir o desenvolvimento de enfermidades autoimunes mediante a produção de TGF-β (Figura 6)(27). Outros LT com função reguladora são os LT γδ, células CD8+Qa-1+, os LT CD8+CD28- (CD8+TR), as células NK/T e os LT duplo-negativos.23,28,29
LT REGULADORES DE OCORRÊNCIA NATURAL - TREGs
As células TREGS representam 5 a 10% do total de LT CD4+ no sangue periférico, podendo também ser isoladas diretamente do timo. As TREGS presentes no timo são células naive que, quando saem para a periferia, se tornam ativadas, adquirindo fenótipo de memória.25
As TREGS apresentam altos níveis de CD25 (CD25HIGH ou CD25BRIGHT) e expressam CD45RO, CD62L, CD122, HLA-DR, CD69, CD71 e o receptor para TNF α induzido por glicocorticoides (GITR) entre outros. Expressam também o fator de transcrição Foxp3, encontrado predominantemente nas TREGS tímicas e periféricas, que parece ter grande importância no desenvolvimento e função das TREGS tanto em camundongos quanto em humanos.25 Pacientes com mutação no gene FOXP3 apresentam a síndrome denominada IPEX (Desregulação imune, Poliendocrinopatia, Enteropatia, Síndrome ligada ao X), um distúrbio autoimune que afeta múltiplos órgãos com desenvolvimento de alergia e doença inflamatória intestinal. Aparentemente esses pacientes têm comprometimento no desenvolvimento das TREGS e consequente defeito na função supressora, levando a um estado de hiperativação de LT, que se tornam reativos contra autoantígenos, bactérias comensais do intestino ou antígenos ambientais inócuos, desenvolvendo poliendocrinopatia autoimune, doença inflamatória intestinal ou alergia, respectivamente.30
Há interesse no estudo dos LT reguladores por sua função chave na manutenção dos mecanismos de autotolerância e regulação da resposta imune. Além dos distúrbios autoimunes associados à ausência/deficiência de sua função, existe interesse no seu estudo em situações de exacerbação da resposta imunitária como nos transplantes, na doença do enxerto versus hospedeiro (GVHD), nos processos alérgicos e outras condições. Nessas situações, uma abordagem terapêutica seria estimular o número e a função dessas células a partir da administração de fármacos, citocinas, moléculas coestimulatórias ou outros elementos que potencialmente atinjam esta finalidade.25
Linfócitos T Reguladores Duplo Negativos
A maioria dos LTCD3+ TCRαβ expressam também moléculas CD4 ou CD8. Entretanto, uma nova subpopulação de LT reguladores com receptor TCRαβ mas CD4-CD8- foi descrita por Strober et al, em 1989.29 Os LT duplo-negativos naturais periféricos com atividade supressora, denominados células TREG DN constituem uma subpopulação de células presentes em tecidos linfoides e não linfoides. Existem em pequeno número, representando 1% - 2% dos LT periféricos em humanos, podendo estar aumentados em algumas doenças autoimunes. As TREG DN produzem predominantemente INF-γ, TNF-α e pequena quantidade de TGF-β e são capazes de suprimir a reposta imune alogênica e xenogênica mediada por LT CD4+ e CD8+, assim como a resposta a antígenos próprios.29,31
O estímulo dos LTREG DN por antígenos específicos através do TCR é importante para o desenvolvimento da atividade reguladora. Os LTREG DN são capazes de adquirir alopeptídeos a partir de complexos peptídeo-MHC de APCs e apresentar esses peptídeos na sua superfície. Essa apresentação permite a interação específica dos LTREG DN com LT efetores reativos ao aloantígeno, que após esse contato progridem para morte celular.32 Similarmente aos LTREGs CD4+CD25+, a supressão pelos LTREG DN também requer o contato célula-célula.
Na síndrome linfoproliferativa autoimune (ALPS) tipo Ia, os pacientes têm um acúmulo de LT CD3+TCRαβ+ DN na periferia como resultado de um defeito de apoptose. Acredita-se que o aumento do número de células DN nesses casos se deva à perda das moléculas CD4 e CD8 pelos LT senescentes que falham em morrer por apoptose.32 Neste caso específico não há evidência de que essas células tenham atividade reguladora.
Dados recentes indicam que os LTREG DN podem estar aumentados em algumas doenças autoimunes, talvez como uma tentativa de controlar as células efetoras. A completa caracterização dos LTREG DN humanos poderá ter implicações importantes no entendimento e tratamento de doenças autoimunes e na rejeição de transplantes.32
Linfócitos T Reguladores CD8+CD28-
As células caracterizadas imunofenotipicamente como CD8+CD28- reconhecem especificamente antígenos expressos principalmente por APCs em associação ao MHC de classe I, mas não são ativadas por carecerem do receptor CD28. Ao invés, suprimem a resposta proliferativa de LTCD4+ aloreativas nas imediações. Este efeito supressor não é mediado por citocinas, mas requer a interação célula-célula entre LTh CD4+, LT supressores CD8+CD28- e APCs apresentando antígenos alogeneicos.33
O mecanismo de ação das células reguladoras CD8+CD28- não está completamente esclarecido e poucos estudos têm caracterizado a função dessas células regulatórias in vitro.
Células NK/T
Praticamente todas as células que expressam TCRαβ são restritas ao MHC, ou seja, reconhecem o antígeno apenas em associação a moléculas do MHC próprio, e expressam co-receptores CD4 ou CD8. Uma pequena população de LT expressa marcadores encontrados em células NK e são conhecidas como células NK/T, que parecem também ter papel importante na regulação da resposta imune. As células NK/T apresentam expressão de TCR com cadeias α de diversidade limitada. Esse TCR reconhece lipídeos ligados a moléculas não-polimórficas, denominadas CD1 e semelhantes ao MHC da classe I.34
As células NK/T parecem surgir do mesmo precursor que origina LT convencionais, mas são selecionadas positivamente após interações de alta avidez com glicolipídeos associados a moléculas CD1d expressas por células epiteliais ou medulares do tecido tímico.35
Apesar do repertório limitado, as células NK/T apresentam duas estratégias diferentes no reconhecimento de patógenos. A primeira, observada no reconhecimento de bactérias Gram-negativas, ocorre pela sinalização de receptores do tipo Toll (TLR) pelo LPS. A segunda ocorre pelo reconhecimento específico de glicosilceramidas presentes na parede celular bacteriana, apresentadas por CD1d. Essa última via de sinalização assegura o reconhecimento de patógenos que não apresentam ligantes para TLRs em sua parede celular.36
Devido ao reconhecimento de glicolipídios conservados, tanto endógenos (iGbeta3) quanto exógenos, essas células estão envolvidas em respostas alérgicas, inflamatórias, tumorais e na autoimunidade, além de participarem da regulação da resposta imune.36
APRESENTAÇÃO DE ANTÍGENOS E ATIVAÇÃO DE LT
A apresentação de antígenos aos LT inicia-se com o processamento antigênico pelas APCs. O processamento consiste na captura do antígeno, sua degradação proteolítica a fragmentos menores, transporte e acomodação dos peptídeos antigênicos na fenda das moléculas do MHC e finalmente na transposição do complexo MHC-peptídeo para a superfície celular para reconhecimento pelo TCR. Os LT reconhecem o complexo MHC-peptídeo via TCR, independente do compartimento celular onde esse antígeno foi captado.37
Normalmente os antígenos exógenos, fagocitados ou endocitados, são acomodados em moléculas de MHC classe II, que interagem com o TCR e o co-receptor CD4 na superfície celular de LT.1
No processamento de antígenos intracelulares, moléculas proteicas do citosol, como por exemplo os antígenos virais, são integradas à proteína ubiquitina e direcionadas para o proteassomo, uma unidade catalítica capaz de converter os antígenos citosólicos em peptídeos. Os peptídos assim produzidos são conduzidos para o retículo endoplasmático e associados às moléculas de MHC I. Os complexos MHC I e peptídeo são transportados para a superfície celular para posterior apresentação aos LT CD8+38.
Para que ocorra a ativação dos LT, após o reconhecimento do peptídeo pelo TCR, há necessidade de um segundo sinal, que é mediado pela interação de várias outras moléculas coestimulatórias presentes na superfície do LT e da APC. Por sua importância na regulação da resposta imune, destacamos as moléculas coestimuladoras participantes da interação CD28-CD80 ou CD28-CD86, que resulta em sinais estimuladores, e da interação CD28-CTLA4, que promove sinalização inibitória.(39,40)
CONSIDERAÇÕES FINAIS
Existem diferentes populações de células B maduras, que podem ser encontradas em diferentes sítios anatômicos, com funções muitas vezes diversificadas. As células B-1 e MZ-B parecem ser pré-selecionadas para reagirem a antígenos capazes de gerar respostas T independentes, atuando como células B de memória inata. As células B foliculares atuam como percussoras das repostas imunes T dependentes e podem sofrer adaptações celulares e moleculares em resposta ao estímulo antigênico. Como resultado, temos as repostas mediadas por plasmócitos maduros de vida longa capazes de sintetizar uma quantidade substancial de anticorpos de alta avidez por vários anos. Estas respostas T dependentes também elaboram um compartimento de células B de memória não secretoras de anticorpos, que responde vigorosamente à reexposição antigênica.
As células T têm como uma de suas principais características a atividade efetora auxiliar na ativação de outros subtipos celulares, principalmente via secreção de citocinas e ação efetora direta sobre células alvo, cujos exemplos emblemáticos são os LT CD8 citotóxicos. Várias subpopulações de LT, classificadas principalmente pelo padrão de citocinas secretado, vêm sendo descritas. Os principais subtipos efetores são os LTh1 (secretor de INF-γ e IL-2), LTh2 (secretor de IL-4,IL-10 e IL-13) e LTh17 (secretor de IL-17, IL-21 e IL-22). Outras subpopulações como os linfócitos NKT e LTγδ representam populações muito heterogêneas quanto a sua capacidade funcional, atuando ora como efetoras, ora como reguladoras. LT reguladores são fundamentais no controle de praticamente todas as respostas imunes, atuando sobre todos os subtipos celulares da imunidade inata e adaptativa. As TREGS naturais originadas no timo e as populações de LT reguladoras induzidas na periferia, incluindo as células CD8+Qa-1+, LT CD8+CD28- e LT duplo-negativas, fazem parte deste diverso pool de linfócitos imunomoduladores.
Não somente os LT podem exercer imunoregulação, mas muitas vezes durante uma reposta efetora as células B podem se comportar tanto como células efetoras ativas quanto como células imunomoduladoras, denominadas BREGS. Estas últimas são capazes de controlar a magnitude da resposta humoral e celular, trazendo de volta a homeostase imune e auxiliando na manutenção da tolerância periférica.
Assim, compartimentos distintos de células T e B antígeno-específicas podem ser recrutados na resposta efetora após um estímulo local ou sistêmico. Os eventos moleculares necessários para seu desenvolvimento, seleção, migração e ativação ainda estão sendo investigados e a compreensão destas vias permitirá no futuro a manipulação específica de vias efetoras celulares e humorais, facilitando a imunidade a microorganismos e prevenindo doenças.
Recebido em 27/08/2010.
Aprovado, após revisão, em 23/09/2010.
Declaramos a inexistência de conflitos de interesse.
Universidade Federal de São Paulo - UNIFESP.
-
1Abbas AK, Lichtman AH, Pillai S. Cellular and Molecular Immunology, 6ª ed, Editora Saunders 2007.
-
2Janeway CA, Travers P, Walport Mark, Shlomchik M. Imunobiologia - O sistema imune na saúde e na doença, 5ª ed, Editora Artmed, 2002.
-
3Rudin CM, Thompson CB. B-Cell Development and Maturation. Seminar in Oncology 1998; 25(4):435-46.
-
4Van Zelm M, Reisli I, Van der Burg M, Castaño D, Van Noesel CJM, Van Tol MJD et al An antibody deficiency syndrome due to mutations in the CD19 gene. N. England J Med 2006; 354:1901-12.
-
5László M, Notarangelo LD. Immunological and genetic bases of new primary immunodeficiencies. Nature Rev Immunology 2007; 7:851-61.
-
6Van Lochem EG, Van der Velden VHJ, Wind HK, Te Marvelde JG, Westerdaal NAC, Van Dongen JJM. Immunophenotypic Differentiation Patterns of Normal Hematopoiesis in Human Bone Marrow: Reference Patterns for Age-Related Changes And Disease-Induced Shifts. Cytometry - Part B (Clinical Cytometry) 2004; 60B:1-13.
-
7McHeyzer-Williams MG: B cells as effectors. Curr Opin Immunol 2003; 15(3):354-61.
-
8Gray D, Gray M, Barr T. Innate responses of B cells. Eur J Immunol 2007; 37(12):3304-10.
-
9Wen L, Roberts SJ, Viney JL, Wong FS, Mallick C, Findly RC. Immunoglobulin synthesis and generalized autoimmunity in mice congenitally deficient in alpha beta(+) T cells. Nature 1994; 369:654-8.
-
10Peng SL, Madaio MP, Hughes DP, Crispe IN, Owen MJ, Wen L. Murine lupus in the absence of alpha beta T cells. J Immunol 1996; 156:4041-9.
-
11Mizoguchi A, Bhan AK. A case for regulatory B cells. J Immunol 2006; 176(2):705-10.
-
12Mauri C, Ehrenstein MR. The 'short' history of regulatory B cells. Trends Immunol 2008; 29(1):34-40.
-
13Mizoguchi A, Mizoguchi E, Smith RN, Preffer FI, Bhan AK. Suppressive role of B cells in chronic colitis of T cell receptor alpha mutant mice. J Exp Med 1997; 186(10):1749-56.
-
14Allman D, Pillai S. Peripheral B cell subsets. Curr Opin Immunol 2008; 20(2):149-57.
-
15Hardy RR: B-1 B cell development. J Immunol 2006; 177(5):2749-54.
-
16Duan B, Morel L. Role of B-1a cells in autoimmunity. Autoimmun Rev 2006; 5(6):403-8.
-
17Stutman O. Intrathymic and extrathymic T cell maturation. Immunol Rev 1978; 42:138-84.
-
18Parkin J, Cohen B. An overview of the immune system. Lancet 2001; 357: 1777-89.
-
19Bradley LM. Migration and T-lymphocyte effector function. Curr Opin Immunol 2003; 15(3):343-8.
-
20Tuerlinckx D, Vermylen C, Brichard B, Ninane J, Cornu G. Disseminated Mycobacterium avium infection in a child with decreased tumour necrosis factor production. Eur J Pediatr 1997; 156(3):204-6.
-
21Mesquita Jr. D, Cruvinel WM, Câmara NOS, Kállas EG, Andrade LEC. Autoimmune diseases in the TH17 era. Braz J Med Biol Res 2009; 42(6):476-486.
-
22Chen Z, Tato CM, Muul L, Laurence A, O'Shea JJ. Distinct Regulation of Interleukin-17 in Human T Helper Lymphocytes. Arthritis & Rheumatism 2007; 56(9):2936-46.
-
23Modlin RL, Sieling PA. Now Presenting: T γδ Cells. Science 2005; 309:252-3.
-
24Holtmeier W, Kabelitz D. Gammadelta T cells link innate and adaptive immune responses. Chem Immunol Allergy 2005; 86:151-83.
-
25Cruvinel WM, Mesquita Jr. D, Araujo JAP, Salmazi KC, Kállas EG, Andrade LEC. Natural Regulatory T cells in Rheumatic Diseases. Rev Bras Reumatol 2008; 48(6):342-355.
-
26Sakaguchi S, Sakaguchi N, Asano M, Itoh M, Toda M. Immunologic self-tolerance maintained by activated T cells expressing IL-2 receptor alpha-chains (CD25). Breakdown of a single mechanism of self-tolerance causes various autoimmune diseases. J Immunol 1995; 155(3):1151-64.
-
27Jiang H, Chess L. An integrated view of suppressor T cell subsets in immunoregulation. J Clin Invest 2004; 114(9):1198-208.
-
2828. Lu L, Werneck MBF, Cantor H. The immunoregulatory effects of Qa-1 Immunological Reviews 2006; 212:51-9.
-
29Sttrober S, Dejbachsh-Jones S, Van Vlasselaer P, Duwe G, Salimi S, Allison JP . Cloned natural supressor cell lines express CD3+ CD4-CD8- surface phenotype and the alpha, beta heterodimer of the T cell antigen receptor. J Immunol 1989; 143:1118-22.
-
30Levings MK, Sangregorio R, Sartirana C, Moschin AL, Battaglia M, Orban PC et al Human CD25+CD4+ T suppressor cell clones produce transforming growth factor beta, but not interleukin 10, and are distinct from type 1 T regulatory cells. J Exp Med 2002; 196(10):1335-46.
-
31Murison JG, Quaratino S, Londei M. Phenotypic and functional heterogeneity of double negative (CD4-CD8-) alpha beta TcR+ T cell clones. Curr Top Microbiol Immunol 1991; 173:215-20.
-
32Wang R, Wang-Zhu Y, Grey H. Interactions between double positive thymocytes and high affinity ligands presented by cortical epithelial cells generate double negative thymocytes with T cell regulatory activity. Proc Natl Acad Sci USA 2002; 99:2181-6.
-
33Ben-David H, Sharabi A, Dayan M, Sela M, Mozes E. The role of CD8+CD28- regulatory cells in suppressing myasthenia gravis - associated responses by dual altered peptide ligand PNAS 2007; 104(44):17459-64.
-
34Godfrey DI, Berzins SP. Control points in NKT-cell development. Nature Rev. Immunol 2007; 7:505-18.
-
35MacDonald HR. Development and function of natural killer 1+ T-cells. Biochem Soc Trans 1997; 25(2):696-9.
-
36Yokoyama WM. Betting on NKT and NK cells. Immunity 2004; 20(4):363-5.
-
37Granucci F, Zanoni I, Ricciardi-Castagnoli P. Central role of dendritic cells in the regulation and deregulation of immune responses. Cell Mol Life Sci 2008; 65:1683-97.
-
38Cruz PD Jr, Bergstresser PR. Antigen processing and presentation by epidermal Langerhans cells. Induction of immunity or unresponsiveness. Dermatol Clin 1990; 8(4):633-47.
-
39Shortman K, Wu L, Süss G, Kronin V, Winkel K, Saunders D et al Dendritic cells and T lymphocytes: developmental and functional interactions. Ciba Found Symp 1997; 204:130-8.
-
40Banchereau J, Briere F, Caux C, Davoust J, Lebecque S, Liu YJ et al Immunobiology of dendritic cells. Annu Rev Immunol 2000; 18:767-811.
Endereço para correspondência:
Datas de Publicação
-
Publicação nesta coleção
12 Nov 2010 -
Data do Fascículo
Out 2010
Histórico
-
Aceito
23 Set 2010 -
Recebido
27 Ago 2010