Resumos
OBJETIVO: Elaborar recomendações para o tratamento da artrite reumatoide no Brasil. MÉTODO: Revisão da literatura com seleção de artigos baseados em evidência e opinião de especialistas da Comissão de Artrite Reumatoide da Sociedade Brasileira de Reumatologia. RESULTADOS E CONCLUSÕES: 1) A decisão terapêutica deve ser compartilhada com o paciente; 2) imediatamente após o diagnóstico, uma droga modificadora do curso da doença (DMCD) deve ser prescrita e o tratamento ajustado para atingir remissão; 3) o tratamento deverá ser conduzido por reumatologista; 4) o tratamento inicial inclui DMCD sintéticas; 5) o metotrexato é a droga de escolha; 6) pacientes que não alcançaram resposta após a utilização de dois esquemas de DMCD sintéticas devem ser avaliados para DMCD biológicas; 7) excepcionalmente, DMCD biológicas poderão ser consideradas mais precocemente; 8) recomenda-se preferencialmente o uso de agentes anti-TNF como terapia biológica inicial; 9) após falha terapêutica a uma primeira DMCD biológica, outros biológicos poderão ser utilizados; 10) ciclofosfamida e azatioprina podem ser consideradas em manifestações extra-articulares graves; 11) recomenda-se a utilização de corticoide oral em baixas doses e por curtos períodos; 12) os anti-inflamatórios não hormonais devem sempre ser prescritos em associação à DMCD; 13) avaliações clínicas devem ser mensais no início do tratamento; 14) terapia física, reabilitação e terapia ocupacional são indicadas; 15) deve-se recomendar tratamento cirúrgico para correção de sequelas; 16) métodos de terapia alternativa não substituem a terapia tradicional; 17) deve-se orientar planejamento familiar; 18) orienta-se a busca ativa e o manejo de comorbidades; 19) atualizar e documentar a vacinação do paciente; 20) doenças transmissíveis endêmico-epidêmicas devem ser investigadas e tratadas.
artrite reumatoide; terapêutica; Brasil; antirreumáticos; consenso
OBJECTIVE: To elaborate recommendations for the treatment of rheumatoid arthritis in Brazil. METHOD: Literature review with articles' selection based on evidence and the expert opinion of the Rheumatoid Arthritis Committee of the Brazilian Society of Rheumatology. RESULTS AND CONCLUSIONS: 1) The therapeutic decision should be shared with the patient; 2) immediately after the diagnosis, a disease-modifying antirheumatic drug (DMARD) should be prescribed, and the treatment adjusted to achieve remission; 3) treatment should be conducted by a rheumatologist; 4) the initial treatment includes synthetic DMARDs; 5) methotrexate is the drug of choice; 6) patients who fail to respond after two schedules of synthetic DMARDs should be assessed for the use of biologic DMARDs; 7) exceptionally, biologic DMARDs can be considered earlier; 8) anti-TNF agents are preferentially recommended as the initial biologic therapy; 9) after therapeutic failure of a first biologic DMARD, other biologics can be used; 10) cyclophosphamide and azathioprine can be used in severe extra-articular manifestations; 11) oral corticoid is recommended at low doses and for short periods of time; 12) non-steroidal anti-inflammatory drugs should always be prescribed in association with a DMARD; 13) clinical assessments should be performed on a monthly basis at the beginning of treatment; 14) physical therapy, rehabilitation, and occupational therapy are indicated; 15) surgical treatment is recommended to correct sequelae; 16) alternative therapy does not replace traditional therapy; 17) family planning is recommended; 18) the active search and management of comorbidities are recommended; 19) the patient's vaccination status should be recorded and updated; 20) endemic-epidemic transmissible diseases should be investigated and treated
rheumatoid arthritis; therapy; Brazil; antirheumatic agents; consensus
ARTIGO ORIGINAL
Consenso 2012 da Sociedade Brasileira de Reumatologia para o tratamento da artrite reumatoide
Licia Maria Henrique da MotaI; Boris Afonso CruzII; Claiton Viegas BrenolIII; Ivanio Alves PereiraIV; Lucila Stange Rezende-FronzaV; Manoel Barros BertoloVI; Max Victor Carioca de FreitasVII; Nilzio Antonio da SilvaVIII; Paulo Louzada-JúniorIV; Rina Dalva Neubarth GiorgiX; Rodrigo Aires Corrêa LimaXI; Geraldo da Rocha Castelar PinheiroXII
IDoutora em Ciências Médicas, Faculdade de Medicina, Universidade de Brasília - FM-UnB; Orientadora do Programa de Pós-graduação em Ciências Médicas, UnB
IIMédico Reumatologista do Biocor Instituto, Belo Horizonte
IIIProfessor Adjunto do Departamento de Medicina Interna, Faculdade de Medicina, Universidade Federal do Rio Grande do Sul - UFRGS; Coordenador do Centro de Referência de Artrite Reumatoide, Hospital de Clínicas de Porto Alegre/SES-RS
IVDoutor em Reumatologia, Faculdade de Medicina, Universidade de São Paulo - FMUSP; Chefe do Núcleo de Reumatologia, Hospital Universitário, Universidade Federal de Santa Catarina - UFSC
VMédica Reumatologista, Hospital de Clínicas, Universidade Federal do Paraná - HC-UFPR; Ex-fellow do Serviço de Reumatologia, Hospital Geral AKH, Áustria; Médica Investigadora do Centro de Estudos em Terapias Inovadoras - CETI
VIProfessor-Associado e Coordenador da Disciplina de Reumatologia, Faculdade de Ciências Médicas, Universidade Estadual de Campinas - Unicamp; Superintendente do Hospital de Clínicas, Unicamp
VIIProfessor Adjunto, Faculdade de Medicina, Universidade Federal do Ceará - UFCE
VIIIProfessor Titular de Reumatologia, Faculdade de Medicina, Universidade Federal de Goiás - UFG
IXProfessor-Associado, Faculdade de Medicina de Ribeirão Preto, Universidade de São Paulo - FMUSP
XMédica Reumatologista, Chefe da Seção de Diagnóstico e Terapêutica do Serviço de Reumatologia, Hospital do Servidor Público Estadual de São Paulo - HSPE-FMO
XIMédico Reumatologista, Chefe do Serviço de Reumatologia do HUB e preceptor da Residência médica do HBDF
XIIProfessor Adjunto e Coordenador da Disciplina de Reumatologia, Faculdade de Ciências Médicas, Universidade do Estado do Rio de Janeiro - UERJ
Correspondência para Correspondência para: Licia Maria Henrique da Mota Av. Brigadeiro Luís Antônio, 2466 - Jardim Paulista CEP: 01402-000. São Paulo, SP, Brasil E-mail: liciamhmota@yahoo.com.br
RESUMO
OBJETIVO: Elaborar recomendações para o tratamento da artrite reumatoide no Brasil.
MÉTODO: Revisão da literatura com seleção de artigos baseados em evidência e opinião de especialistas da Comissão de Artrite Reumatoide da Sociedade Brasileira de Reumatologia.
RESULTADOS E CONCLUSÕES: 1) A decisão terapêutica deve ser compartilhada com o paciente; 2) imediatamente após o diagnóstico, uma droga modificadora do curso da doença (DMCD) deve ser prescrita e o tratamento ajustado para atingir remissão; 3) o tratamento deverá ser conduzido por reumatologista; 4) o tratamento inicial inclui DMCD sintéticas; 5) o metotrexato é a droga de escolha; 6) pacientes que não alcançaram resposta após a utilização de dois esquemas de DMCD sintéticas devem ser avaliados para DMCD biológicas; 7) excepcionalmente, DMCD biológicas poderão ser consideradas mais precocemente; 8) recomenda-se preferencialmente o uso de agentes anti-TNF como terapia biológica inicial; 9) após falha terapêutica a uma primeira DMCD biológica, outros biológicos poderão ser utilizados; 10) ciclofosfamida e azatioprina podem ser consideradas em manifestações extra-articulares graves; 11) recomenda-se a utilização de corticoide oral em baixas doses e por curtos períodos; 12) os anti-inflamatórios não hormonais devem sempre ser prescritos em associação à DMCD; 13) avaliações clínicas devem ser mensais no início do tratamento; 14) terapia física, reabilitação e terapia ocupacional são indicadas; 15) deve-se recomendar tratamento cirúrgico para correção de sequelas; 16) métodos de terapia alternativa não substituem a terapia tradicional; 17) deve-se orientar planejamento familiar; 18) orienta-se a busca ativa e o manejo de comorbidades; 19) atualizar e documentar a vacinação do paciente; 20) doenças transmissíveis endêmico-epidêmicas devem ser investigadas e tratadas.
Palavras-chave: artrite reumatoide, terapêutica, Brasil, antirreumáticos, consenso.
INTRODUÇÃO
A artrite reumatoide (AR) é uma doença autoimune inflamatória sistêmica caracterizada pelo comprometimento da membrana sinovial das articulações periféricas. A prevalência da AR é estimada em 0,5%-1% da população, com predomínio em mulheres e maior incidência na faixa etária de 30-50 anos.1,2
A característica principal da AR é o acometimento simétrico das pequenas e das grandes articulações, com maior frequência de envolvimento das mãos e dos pés. O caráter crônico e destrutivo da doença pode levar a importante limitação funcional, com perda de capacidade laboral e de qualidade de vida, a menos que o diagnóstico seja feito em fase inicial da doença e o tratamento determine melhora clínica.3 Além de deformidade irreversível e de limitação funcional, pacientes com AR e doença avançada podem apresentar menor sobrevida, o que confirma a gravidade dessa doença.4,5
Os custos relacionados à AR são elevados, o que decorre tanto de fatores diretos (gastos com diversos medicamentos, alguns deles de alto custo, como as drogas biológicas, além de despesas médicas e hospitalares) quanto indiretos (perda da produtividade pessoal, absenteísmo e pagamento de aposentadorias por invalidez, para aqueles com perda total da capacidade laboral).6
Nos últimos 10 anos houve grande avanço no conhecimento dos mecanismos fisiopatológicos da AR, com o desenvolvimento de novas classes terapêuticas e a implementação de diferentes estratégias de tratamento e de acompanhamento dos pacientes, como controle intensivo da doença e intervenção na fase inicial dos sintomas.7 O período inicial da doença, em especial seus 12 primeiros meses (AR inicial),5 é considerado uma janela de oportunidade terapêutica, ou seja, um momento em que a intervenção farmacológica rápida e efetiva pode mudar o curso da doença em longo prazo. Esses fatores resultaram em melhor controle clínico da doença, com a possibilidade de remissão sustentada da AR.7,8
O presente consenso tem o objetivo de elaborar recomendações para o manejo da AR, com enfoque no tratamento da doença, levando em consideração aspectos peculiares da realidade socioeconômica brasileira. A finalidade deste documento é sintetizar a posição atual da Sociedade Brasileira de Reumatologia (SBR) sobre o tema, objetivando orientar os médicos brasileiros, em especial os reumatologistas, sobre o manejo terapêutico racional da AR no Brasil.
MÉTODO DE ELABORAÇÃO DO CONSENSO
O método de elaboração do consenso para o desenvolvimento das recomendações incluiu revisão da literatura e opinião de especialistas membros da Comissão de Artrite Reumatoide da SBR. O levantamento bibliográfico abrangeu publicações existentes nas bases MEDLINE, SciELO, PubMed e EMBASE até novembro de 2011. As recomendações foram escritas e reavaliadas por todos os participantes durante cinco reuniões presenciais, ocorridas em outubro e dezembro de 2010, e fevereiro, julho e outubro de 2011, além de múltiplas rodadas de questionamentos e correções realizadas via internet.
TRATAMENTO DA ARTRITE REUMATOIDE
O tratamento da AR inclui educação do paciente e de sua família, terapia medicamentosa, fisioterapia, apoio psicossocial, terapia ocupacional e abordagens cirúrgicas. As terapias medicamentosas incluem uso de anti-inflamatórios não hormonais (AINH), corticoides, drogas modificadoras do curso da doença (DMCD) sintéticas e biológicas e drogas imunossupressoras.
Medidas educativas
Antes de iniciar qualquer forma de tratamento, o paciente deve ser esclarecido sobre sua enfermidade e, particularmente, quanto às possibilidades evolutivas, terapêuticas e de prognóstico. É preciso alertar sobre informações inadequadas veiculadas pelos meios de comunicação, em especial a internet. A educação deve ser iniciada desde o primeiro atendimento e deve incluir os familiares, para que todos compartilhem das informações sobre a doença, o que resulta em melhor manejo dos tratamentos medicamentosos e não medicamentosos.9,10
Atividades educativas são essenciais para que se obtenha a colaboração do paciente. Ele tem o direito de saber sobre suas condições e sobre as opções terapêuticas disponíveis, e de participar ativamente das escolhas. O paciente que entende sua condição e compreende a ação dos medicamentos, os métodos de prevenção de deformidades e o processo de reabilitação apresenta melhor evolução clínica.11
O paciente deve ser informado sobre o papel dos exercícios e da proteção articular e as técnicas específicas de fisioterapia e de reabilitação, para que possa dedicar-se às atividades de prevenção de deformidades articulares. Além disso, deve ser orientado sobre as possibilidades de ajuste de equipamentos domésticos e de modificação do ambiente de trabalho.12
Como o paciente é muitas vezes acompanhado por uma equipe multidisciplinar, é necessário que todos tenham os mesmos objetivos e trabalhem em conjunto e em harmonia.13
Tratamento medicamentoso
Anti-inflamatórios não hormonais - AINH
Os AINH são úteis para diminuir o processo inflamatório e a dor, principalmente no início da doença, pois as DMCD não têm ação imediata. Podem ser empregados, também, quando não se obtém controle completo da atividade e em reagudizações da AR.14,15
A escolha dos AINH deve ser individualizada, pois não há superioridade conhecida de qualquer fármaco dessa classe. Maior controle, substituição, suspensão, diminuição do tempo de utilização e redução das doses devem ser os cuidados se houver condições clínicas que possam ser agravadas pelos AINH, como, por exemplo, hipersensibilidade prévia a AINH, hipertensão arterial sistêmica (HAS), insuficiência cardíaca, insuficiência renal, doença gastrintestinal, insuficiência arterial, hepatopatia e distúrbios de coagulação.16
Para os pacientes com história prévia de doença gastrintestinal, os inibidores seletivos de ciclo-oxigenase 2 apresentam menor risco em relação aos demais AINH.17 Para pacientes com maior risco de doença cardiovascular, o uso de anti-inflamatórios, em geral, deve ser cauteloso.18
Corticoides
O efeito mais conhecido e esperado dos corticoides na AR é a melhora do processo inflamatório e da dor. Contudo, atualmente há evidência para indicá-los como participantes na modificação do curso da doença, em associação com as DMCD.19,20
A maioria dos estudos sobre o uso de corticoides no tratamento da AR sugere a utilização da prednisona ou prednisolona em doses baixas (< 15 mg/dia). Não há estudos comparativos que permitam indicar preferencialmente doses mais altas no início do tratamento.19,20
Como os corticoides podem causar vários efeitos colaterais, seu tempo de uso deve ser abreviado ao mínimo possível. Se a previsão for de três ou mais meses de uso, deve-se fazer suplementação de cálcio e de vitamina D. Dependendo do resultado de densitometria óssea, e em pacientes com fatores de risco para fraturas, a utilização de drogas antirreabsortivas, como os bisfosfonatos, pode ser considerada.21 Em pacientes que mantêm a doença ativa em poucas articulações pode-se usar o corticoide intra-articular a qualquer momento do tratamento22 - porém, uma mesma articulação não deve ser infiltrada mais de três a quatro vezes ao ano. Para pacientes em uso concomitante de corticoide e AINH, recomenda-se proteção gástrica com inibidor de bomba de próton.22
Drogas modificadoras do curso da doença - DMCD
As DMCD devem ser indicadas ao paciente a partir da definição do diagnóstico de AR.23A utilização de DMCD em pacientes com artrite indiferenciada e biomarcadores preditores de AR, como positividade dos anticorpos antipeptídeos citrulinados cíclicos (anti-CCP) e/ou fator reumatoide (FR), pode ser considerada.24
A Tabela 1 resume as principais DMCD utilizadas no Brasil, sua apresentação, dose e considerações sobre monitoração.20,25-94
DMCD sintéticas
a) Metotrexato - MTX
O MTX é um agente imunomodulador cuja ação consiste na inibição da síntese de DNA, RNA, timidinato e proteínas. Os efeitos anti-inflamatórios do MTX na AR parecem estar relacionados, pelo menos em parte, com a modulação do metabolismo da adenosina e com os efeitos possíveis nas vias do fator de necrose tumoral (TNF, do inglês, tumor necrosis factor). Os efeitos imunossupressivos e tóxicos do MTX são devido à inibição do diidrofolato redutase, enzima envolvida no metabolismo do ácido fólico, o que evita a redução do diidrofolato a tetraidrofolato ativo. O tempo até a concentração máxima é de 1-5 horas por via oral (VO) e de 30-60 minutos por via intramuscular (IM) ou subcutânea (SC). Elimina-se por via renal entre 40% e 90% de forma inalterada.25
O MTX é atualmente considerado o fármaco padrão no tratamento da AR.26 Sua capacidade de reduzir sinais e sintomas de atividade da AR e de melhorar o estado funcional do paciente foi demonstrada.27 Ele também reduz a progressão das lesões radiográficas.
Recomenda-se dose inicial de 10-15 mg/semana, VO ou parenteral (IM ou SC). Caso não se observe melhora ou controle da doença com a dose inicial, deve-se aumentar progressivamente a cada 2-4 semanas até alcançar a dose de 20-30 mg/semana, preferencialmente nas primeiras 12 semanas. A apresentação parenteral pode ser indicada em pacientes com intolerância gastrintestinal ou com resposta inadequada à forma oral.28
Os efeitos adversos mais frequentemente observados são anemia, neutropenia, náuseas e vômitos, mucosite e elevação de enzimas hepáticas. A pneumonia intersticial é uma manifestação menos frequente. Sugere-se a associação do MTX ao ácido fólico na dose de 5-10 mg/semana, 24-48 horas após o MTX, a fim de minimizar efeitos adversos.28 O MTX está contraindicado em pacientes com insuficiência renal, hepatopatias, etilismo, supressão da medula óssea e em mulheres em idade fértil que não estejam utilizando métodos anticoncepcionais. A gestação e a amamentação estão formalmente contraindicadas nas pacientes em uso do MTX. O medicamento deve ser usado com cautela em pacientes com pneumopatias leves, e deve ser evitado em indivíduos com comprometimento pulmonar moderado ou grave.28
b) Sulfassalazina - SSZ
A SSZ pertence ao grupo dos salicilatos e sulfamidas, e é desdobrada pelas bactérias intestinais na sulfapiridina e no ácido 5-aminosalicílico. A sulfapiridina tem vários efeitos imunomodulatórios, como inibição da produção de prostaglandinas, de diversas funções neutrofílicas e linfocitárias e da quimiotaxia. É também um inibidor de enzimas folato-dependentes. O pico de concentração sérica da SSZ é de aproximadamente 1,5-6 horas, e sua meia-vida de eliminação é de 5-10 horas. O metabolismo ocorre no trato gastrintestinal (via flora intestinal), e a excreção é renal (75%-91%).29
A SSZ é considerada mais efetiva que o placebo na redução da atividade da doença, no controle da dor e na avaliação clínica global. Sua eficácia clínica e a interferência sobre a progressão radiográfica estão confirmadas.29 Usualmente, é prescrita na dose de 1-3 g/dia (VO).29,30
Os efeitos colaterais incluem intolerância gastrintestinal (anorexia, náuseas, vômitos), exantema cutâneo, elevação de enzimas hepáticas, úlceras orais e mielossupressão (leucopenia com neutropenia). Raramente observam-se pneumonia de hipersensibilidade, manifestações neurológicas ou alterações da fertilidade masculina. A maioria dos efeitos é de caráter benigno, reversível com a retirada da droga.30
A SSZ está contraindicada em pacientes com história de hipersensibilidade a sulfas, salicilatos ou a qualquer componente da fórmula, e em indivíduos com porfiria.29,30
c) Leflunomida - LEF
A LEF é um agente imunomodulador com atividade antiproliferativa que inibe a enzima diidroorotato desidrogenase, envolvida na síntese da pirimidina. É absorvida no trato gastrintestinal, e a biotransformação ocorre provavelmente no fígado e na parede gastrintestinal, onde a LEF é transformada principalmente em M1, o metabólito ativo responsável por todas as ações da medicação. O tempo para a concentração máxima (pico) da M1 é de 6-12 horas, e a eliminação é renal e intestinal.31
A LEF melhora a atividade da doença e a qualidade de vida e reduz a progressão radiográfica.32,33 É prescrita na dose de 20 mg/dia (VO),31-33 mas pode-se prescrever dose de 20 mg em dias alternados.
Os efeitos adversos incluem náuseas, vômitos, dor abdominal e diarreia, alterações das enzimas hepáticas, exantema cutâneo e HAS.31 Está contraindicada em mulheres em idade fértil que não estejam utilizando métodos anticoncepcionais, e em pacientes com insuficiência renal e hepatopatias. A gestação e a amamentação estão formalmente contraindicadas nas pacientes em uso da LEF. Sua suspensão é recomendada até dois anos antes de uma possível gravidez. Em casos de intercorrências, em especial na gravidez, a LEF pode ser eliminada com a utilização de colestiramina na dosagem de 8 g três vezes ao dia, por 11 dias.31
d) Antimaláricos (difosfato de cloroquina - DCQ e sulfato de hidroxicloroquina - HCQ)
Os antimaláricos vêm sendo usados no tratamento da AR há mais de 50 anos. São medicamentos seguros e eficazes, sobretudo para formas iniciais e leves. Seu mecanismo de ação ainda é pouco conhecido, mas parece envolver múltiplos fatores: atividade anti-inflamatória (estabilização das membranas lisossomais, inibição de enzimas lisossômicas e da quimiotaxia e fagocitose de polimorfonucleares), interferência na produção de prostaglandinas, entre outros.34,35
As duas formas disponíveis dos antimaláricos são o DCQ e o HCQ, das quais a última é preferível por seu melhor perfil de segurança, sobretudo oftalmológico. A dose máxima diária do DCQ é de 4 mg/kg/dia, e a do HCQ é de 6 mg/kg/dia VO. O início de ação é lento, levando de 3-4 meses para atingir o pico de eficácia em cerca de 50% dos pacientes.
Os efeitos colaterais são diversos e incluem, entre outros, intolerância gastrintestinal (náuseas, vômitos, dor abdominal), hiperpigmentação da pele, cefaleia, tontura, miopatia e retinopatia. Este último é infrequente, mas indica-se monitoração oftalmológica regular (avaliação inicial e anual após cinco anos, ou anual desde o princípio, se houver fatores de risco: pacientes com disfunção renal ou hepática, com maculopatia, idosos ou dose cumulativa superior a 1000 g para o HCQ ou 460 g para o DCQ).36
O HCQ é eficaz em comparação ao placebo, reduzindo os parâmetros clínicos e laboratoriais (velocidade de hemosedimentação, VHS) analisados, embora isoladamente não tenha alterado a progressão radiográfica.34,35,37 Resultados similares foram observados com o DCQ, que tem menor custo. Ambos são contraindicadas em pacientes com alterações retinianas e de campo visual.36,37
Embora seu uso seja tradicional no Brasil, muitas vezes em associação a outras DMCD, os antimaláricos atualmente são considerados drogas menos potentes, devendo ser usados em casos iniciais de AR ou artrite indiferenciada, com baixo potencial erosivo.
e) Sais de ouro
Os sais de ouro, especificamente sob as formas injetáveis (aurotioglicose e aurotiomalato) são capazes tanto de reduzir os sintomas constitucionais e articulares quanto de retardar a evolução radiográfica da AR.38 Podem ser usados em monoterapia ou em combinação com outros agentes.39
A dose habitual é de 50 mg/semana, iniciando-se geralmente com 25 mg/semana, com possibilidade de aumento dos intervalos de aplicações para doses quinzenais e mensais após controle do quadro. A dose cumulativa não deve ultrapassar 3 g.38,39 Seu perfil de toxicidade inclui mielotoxicidade (marcadamente trombocitopenia), úlceras orais, reações cutâneas (dermatite esfoliativa), nefropatia (podendo haver proteinúria nefrótica) e doença intersticial pulmonar.38,39
Embora tenham sido citados em recentes recomendações internacionais,20 atualmente os sais de ouro são bem pouco utilizados no Brasil, dados seus efeitos adversos e a dificuldade de aquisição da droga em nosso meio.
DMCD biológicas
Um dos mais relevantes avanços na terapia da AR foi o desenvolvimento das DMCD biológicas.40 Embora essas medicações sejam eficazes no controle da AR, sua segurança a longo prazo ainda não está estabelecida.41
Encontram-se aprovadas pela Agência Nacional de Vigilância Sanitária (ANVISA) para uso no Brasil as seguintes DMCD biológicas:42
Anti-TNF: adalimumabe, certolizumabe, etanercepte, infliximabe e golimumabe;
Depletor de linfócito B: rituximabe;
Bloqueador da coestimulação do linfócito T: abatacepte;
Bloqueador do receptor de interleucina-6 (IL-6): tocilizumabe.
As DMCD biológicas estão indicadas para os pacientes que persistam com atividade da doença, apesar do tratamento com pelo me nos dois esquemas de DMCD sintéticas, dos quais pelo menos um deles é combinação de DMCD. O uso de agentes biológicos deve ser feito associado a uma DMCD, preferencialmente MTX. Excepcionalmente, como discutido a seguir, uma DMCD biológica pode ser prescrita mais precocemente no curso do tratamento da AR, sobretudo em casos de doença com combinação de sinais de pior prognóstico (elevado número de articulações acometidas, erosões radiográficas na fase inicial da doença, FR e/ou anti-CCP presentes em altos títulos).13,20,43-46
Características sociais/educacionais/demográficas das diferentes macrorregiões brasileiras, como a dificuldade de aplicação de medicação SC por alguns pacientes e seus familiares, bem como a inexistência de centros de infusão para aplicação de medicação intravenosa (IV) em certos locais, podem determinar a escolha de uma ou outra DMCD biológica. Os centros de dispensação/infusão das drogas, públicos ou privados, devem informar aos pacientes e aos seus familiares o adequado acondicionamento de cada medicação, ou enviá-las diretamente para o local de infusão, para evitar perda de eficácia do tratamento. Recomenda-se que o uso desses fárma cos seja indicado e monitorado por um reumatologista.47
A associação de DMCD biológicas não deve ser utilizada, devido ao potencial risco de infecções graves.48,49Atualmente, as DMCD biológicas mais utilizadas são os anti-TNF, mas há evidências de que as demais DMCD biológicas também promovam o controle de sinais e sintomas da AR e a inibição da progressão radiográfica.
a) Anti-TNF
O TNF é uma potente citocina inflamatória expressa em grandes quantidades no soro e no líquido sinovial de indivíduos com AR. Ele promove a liberação de outras citocinas inflamatórias, particularmente as interleucinas IL-1, IL-6 e IL-8, e estimula a produção de proteases. A inibição do TNF demonstrou ser uma forma efetiva e rápida de controlar a atividade da doença.50
Em termos de eficácia, não há dados que permitam afirmar a superioridade de qualquer um dos cinco agentes anti-TNF aprovados no Brasil para tratamento da AR.51,52
Os anti-TNF devem ser utilizados em associação ao MTX ou a outras DMCD, pois o uso combinado mostrou-se seguro e propiciou rápido benefício no controle da atividade da doença, comparado ao uso do anti-TNF como monoterapia. Em pacientes que apresentem contraindicações ao uso de DMCD sintéticas, os anti-TNF podem eventualmente ser prescritos em monoterapia.46,53-63
Adalimumabe - ADA
O ADA é um anticorpo humano contra o TNF, prescrito para aplicação SC na dose de 40 mg uma vez a cada duas semanas.55,56,64-68
Certolizumabe - CERT
O CERT pegol é um fragmento Fab de um anticorpo anti-TNF humanizado, com alta afinidade ao TNF, conjugado com duas moléculas de polietilenoglicol. É prescrito para aplicação SC na dose de 400 mg a cada duas semanas, nas semanas 0, 2 e 4, e, após isso, na dose de 200 mg a cada duas semanas ou 400 mg a cada quatro semanas.61,62,69
Etanercepte - ETN
O ETN é uma proteína de fusão composta pelo receptor solúvel do TNF mais a região Fc da IgG, prescrita em dose única semanal de 50 mg por via SC.57,58,68,70
Infliximabe - IFX
O IFX é um anticorpo monoclonal anti-TNF quimérico humano-murino, prescrito na dose inicial de 3 mg/kg IV, seguida da mesma dose nas segunda e sexta semanas e, depois, a cada oito semanas. Em pacientes com resposta insuficiente, a dose pode ser elevada para 5 mg/kg por infusão, ou o intervalo entre as doses pode ser reduzido. Doses mais altas trazem pouco benefício terapêutico e maior risco de complicações infecciosas, portanto devem ser evitadas no tratamento da AR.54,59,63,68,71
Golimumabe - GOL
O GOL é um anticorpo monoclonal humano anti-TNF administrado mensalmente na dose de 50 mg por via SC.60,72
Efeitos adversos e contraindicações dos anti-TNF
Os efeitos adversos incluem reações infusionais para as drogas IV (febre, calafrios, dor torácica, oscilação de pressão arterial, dispneia, prurido e/ou urticária) e manifestações nos locais de injeção para as drogas SC (eritema, prurido, dor local e/ou urticária). Essas drogas aumentam a chance de infecções, especialmente no primeiro ano de uso, incluindo infecções graves e aquelas causadas por patógenos intracelulares (como bacilo da tuberculose, listeria, histoplasma, micobacterias atípicas e legionella), além de disfunção cardíaca, doenças desmielinizantes, fenômenos autoimunes (produção de autoanticorpos), vasculites cutâneas, doença pulmonar intersticial e eventual aumento do risco de linfoma.68,73-75 Anticorpos antiquiméricos humanos podem ocorrer com todas as drogas da classe, mas seu efeito sobre a eficácia da terapia é incerto.76,77
As medicações anti-TNF são contraindicadas em mulheres grávidas ou que estejam amamentando e em pacientes com insuficiência cardíaca congestiva classe III e IV (segundo a classificação da New York Heart Association), em vigência de infecção ativa ou com elevado risco para o desenvolvimento de infecções (úlcera crônica de membros inferiores, artrite séptica nos últimos 12 meses), com infecções pulmonares recorrentes, esclerose múltipla e diagnóstico atual ou pregresso de neoplasias (menos de cinco anos). Deve-se acompanhar o paciente de maneira cuidadosa, avaliando o possível surgimento de sinais de infecção, que deve ser tratada de forma pronta e imediata.73-75
b) Modulador da coestimulação
Abatacepte - ABAT
O ABAT é uma proteína de fusão CTLA-4-IgG que atua como inibidor de moléculas de coestimulação dos linfócitos T. É indicado para pacientes com AR ativa que tenham apresentado falha terapêutica à DMCD ou aos agentes anti-TNF. Pode ser utilizado associado às DMCD ou em monoterapia. O ABAT deve ser administrado como infusão IV, durante 30 min, na dose de 500 mg nos pacientes com menos de 60 kg, 750 mg nos pacientes entre 60-100 kg e 1.000 mg naqueles com mais de 100 kg de peso corporal. A dose seguinte deve ser administrada duas e quatro semanas após a dose inicial, e depois a cada quatro semanas.78-80
O uso do ABAT está associado à maior ocorrência de complicações infecciosas quando comparado ao placebo, assim como observado com outras DMCD biológicas. As reações infusionais com o ABAT são pouco frequentes e são, principalmente, reações de hipersensibilidade que se manifestam por exantema ou broncoespasmo. Está contraindicado em pacientes com quadro de doença pulmonar obstrutiva crônica, por exacerbação do quadro de dispneia e maior ocorrência de infecções.78,81
c) Depletor de linfócitos B
Rituximabe - RTX
O RTX é um anticorpo monoclonal quimérico dirigido contra o linfócito CD20+, indicado em pacientes com AR em atividade moderada a grave com falha terapêutica ao agente anti-TNF. É administrado na dose de 1.000 mg em duas infusões IV em um intervalo de 14 dias. Cada infusão é precedida de 100 mg de metilprednisolona IV 60 min antes e de 1 g de paracetamol e anti-histamínico, para diminuir a gravidade e a frequência das reações infusionais.82-85
O RTX é utilizado preferencialmente em associação com o MTX, podendo ser prescrito em associação com outras DMCD. É importante ressaltar que pode haver retardo em três a quatro meses para que se observe o início da melhora sintomática.82-84 Indivíduos com sorologia positiva para FR e/ou anti-CCP apresentam melhor resposta terapêutica.86 Os pacientes com boa resposta ao tratamento podem ser submetidos a novo curso de RTX, caso reativem a doença, em intervalo de tempo não inferior a seis meses.82-85
Os eventos adversos mais frequentes são as reações infusionais, que acometem 35% dos pacientes na primeira infusão e cerca de 10% na segunda infusão. Complicações infecciosas podem ocorrer, bem como pneumonia intersticial, neutropenia e trombocitopenia.82-85
d) Bloqueador do receptor de IL-6
Tocilizumabe - TOCI
O TOCI é um anticorpo monoclonal humanizado que se liga ao receptor de IL-6, inibindo o efeito biológico da IL-6. Pode ser usado em monoterapia, associado ao MTX ou a outras DMCD. A incidência de infecções e de infecções graves é equivalente aos outros agentes biológicos. É prescrito na dose de 8 mg/kg por via IV, a cada quatro semanas.87-89
O uso de TOCI pode ocasionar neutropenia, plaquetopenia e elevação de transaminases como efeitos adversos dosedependentes. Pode ainda ocorrer elevação do colesterol total e da lipoproteína de baixa densidade, bem como aumento da ocorrência de infecções.87-89 Deve-se evitar sua utilização em pacientes com maior chance de perfuração intestinal, como indivíduos com doença diverticular do cólon.90
Infecção em pacientes em uso de DMCD biológicas
Recomenda-se a triagem para doenças infecciosas antes do início de DMCD biológicas, incluindo avaliação clínica minuciosa, sorologias para hepatite B e C, e, quando pertinente, HIV e/ou outras doenças endêmicas. A triagem para doenças endêmicas será mais bem detalhada em tópico posterior.
Drogas imunossupressoras
A base do uso de imunossupressores para o tratamento da AR é a evidência de múltiplos mecanismos imunológicos mediando sinovite e outras manifestações extra-articulares da doença.
Diversos mecanismos de ação são descritos, incluindo redução da resposta celular (e menos efetivamente da humoral) e propriedades anti-inflamatórias (interferência sobre a migração e a ação de neutrófilos, linfócitos e monócitos).
O uso dos imunossupressores está restrito para as formas mais severas da AR, já que a maioria dessas drogas apresenta considerável toxicidade (mielossupressão grave, aumento da ocorrência de infecções, esterilidade, toxicidade vesical e aumento da ocorrência de neoplasias).
Azatioprina - AZA
Embora apresente perfil de segurança aceitável, há controvérsias sobre sua ação como DMCD. A AZA é considerada uma opção terapêutica;91 entretanto, seu menor efeito no controle de sinais e sintomas e a ausência de comprovação na redução da progressão radiográfica colocam-na como uma alternativa apenas em casos excepcionais.20
A dose habitual é de 1-3 mg/kg/dia VO. Ela é usada no tratamento de formas moderadas a severas da AR, refratárias a outros tratamentos ou para controle de manifestações extra-articulares graves, como a vasculite.20,91
Ciclofosfamida - CF
Agente alquilante com perfil de toxicidade desfavorável e limitado benefício para controle da sinovite, a CF pode ser usada por VO (1-2 mg/kg/dia) ou preferencialmente por via IV (pulsos de 0,5-1 g/m2de superfície corpórea). Seu uso só se justifica nas formas extra-articulares graves, sobretudo na vasculite.92
Ciclosporina - CS
A CS é uma alternativa eficaz no controle de sinais e sintomas da AR. Pode retardar a progressão do dano articular, mesmo em pacientes com AR grave e refratária a outros tratamentos, embora seu efeito pareça ser inferior ao do MTX, da SSZ e da LEF. Pode ser usada em monoterapia, mas é geralmente prescrita em associação com o MTX.20,93,94
O mecanismo proposto é de uma ação imunomoduladora, relativamente específica para os linfócitos T. É prescrita por VO, com dose de 3-5 mg/kg/dia. Está contraindicada em pacientes com alteração da função renal, hipertensão não controlada e malignidade. Sua toxicidade, entretanto, limita a utilização por pacientes com doença não responsiva a outras DMCD, tornando-a uma droga de exceção para tratamento da doença. É prescrita preferencialmente para pacientes com manifestações extra-articulares, incluindo vasculite, além de ser uma alternativa segura para pacientes com hepatopatia e envolvimento pulmonar. Se houver desenvolvimento de hipertensão ou aumento de creatinina em 30% do valor basal, deve ser realizada redução de 25%-50% da dose. Persistindo a hipertensão ou o aumento de creatinina, o tratamento deve ser descontinuado.20,93,94
ESTRATÉGIAS TERAPÊUTICAS PARA O TRATAMENTO DA AR NO BRASIL
As DMCD devem ser iniciadas imediatamente após o diagnóstico. Sempre que necessário, o tratamento deve ser ajustado em avaliações clínicas frequentes em um período de 30-90 dias.
Estratégias terapêuticas com base em metas específicas produzem melhores desfechos clínicos e capacidade funcional, além de menor dano estrutural radiológico, em comparação com tratamentos convencionais.95A meta a ser alcançada é a remissão, ou pelo menos a baixa atividade, avaliada por índices compostos de atividade da doença (ICAD), considerando-se como resposta terapêutica a redução do valor do ICAD, conforme estabelecido no consenso 2011 da Sociedade Brasileira de Reumatologia para diagnóstico e avaliação inicial da AR.5
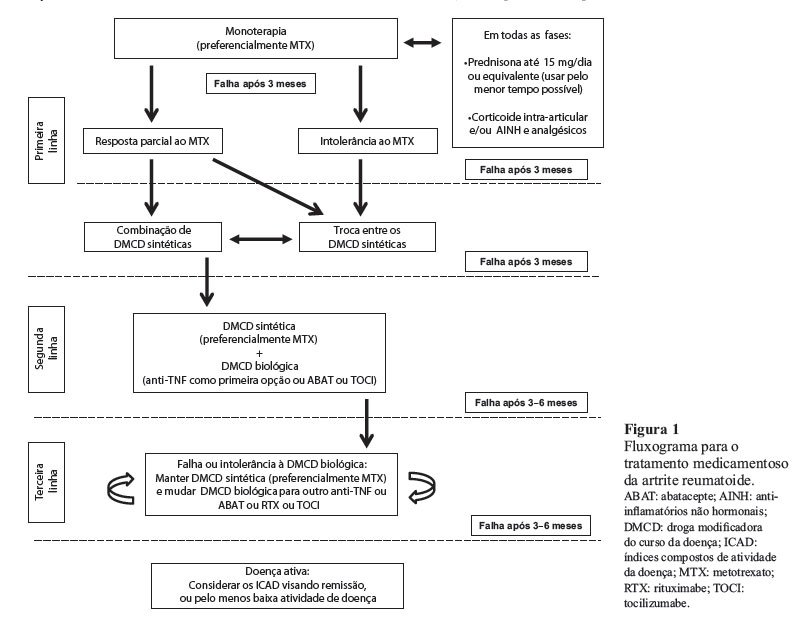
A Figura 1 sintetiza o fluxograma de tratamento medicamentoso para a AR no Brasil, proposto pela Comissão de Artrite Reumatoide da Sociedade Brasileira de Reumatologia.
Primeira linha - DMCD sintéticas
O MTX deve ser a DMCD de primeira escolha.20,96,97 Havendo contraindicação, SSZ98 ou LEF99 podem ser utilizadas como primeira opção.100 Os antimaláricos (DCQ e HCQ)101 devem ser indicados apenas para pacientes com doença leve ou artrite indiferenciada com baixo potencial erosivo. Em casos excepcionais, como pacientes com hipersensibilidade a outras DMCD ou com hepatite viral, sais de ouro podem ser utilizados. O MTX deve ser prescrito preferencialmente em monoterapia, no início do tratamento.102
Não havendo a resposta clínica objetivada (remissão ou baixa atividade da doença) com dose máxima tolerada de MTX, ou na presença de efeitos adversos, recomenda-se a troca por outra DMCD em monoterapia ou o uso de combinações de DMCD. As combinações mais utilizadas são MTX com DCQ/ HCQ, com SSZ ou a associação dessas três drogas,27 bem como MTX associado à LEF.103 A progressão da terapia deve ser rápida, com avaliações mensais do paciente nos primeiros seis meses de tratamento e ajuste de doses e esquemas, conforme necessário. Deve-se aguardar um período máximo de seis meses para definir ausência de resposta à primeira linha de tratamento instituída.20
Doses baixas de corticoides (máximo de 15 mg de prednisona ao dia ou equivalente) podem ser utilizadas no início do tratamento, bem como anti-inflamatórios, recomendando-se, no entanto, cautela e uso pelo menor tempo possível, para minorar a ocorrência de efeitos adversos.20
Segunda linha - DMCD biológicas
A terapia imunobiológica na AR está indicada para os pacientes que persistem com atividade da doença moderada a alta (conforme ICAD), apesar do tratamento com pelo menos dois dos esquemas propostos na primeira linha de tratamento. As drogas anti-TNF são a primeira opção no Brasil, dentre os biológicos, após falha dos esquemas com DMCD sintéticas. Isto é justificável pela experiência mais abrangente pós-comercialização, bem como pelo maior volume de informações de segurança oriundas de estudos clínicos, registros e recomendações nacionais104 e internacionais.20 Entretanto, outras drogas, como o ABAT e o TOCI, podem ser prescritas a critério do médico-assistente após falha da DMCD sintética, tendo em vista a publicação de ensaios clínicos randomizados que embasam essa indicação.78,89A prescrição de RTX deve ser evitada como biológico de primeira escolha,20 a não ser em casos específicos (pacientes com contraindicação a outros biológicos, preferencialmente que sejam positivos para FR e/ou anti-CCP, ou aqueles que apresentam diagnóstico associado de linfoma, por exemplo).
Em situações excepcionais, a DMCD biológica pode ser indicada após falha do primeiro esquema de DMCD sintética naqueles pacientes com vários fatores de mau prognóstico, incluindo doença com atividade muito intensa, elevado número de articulações dolorosas/inflamadas, FR e/ou anti-CCP em altos títulos e ocorrência precoce de erosões radiográficas.20 Os fatores de pior prognóstico foram mais bem detalhados no consenso 2011 da Sociedade Brasileira de Reumatologia para diagnóstico e avaliação inicial da AR.5
O uso de DMCD biológicas como primeira linha para o tratamento da AR não está indicado no Brasil, pois não há evidências de custo-efetividade dessa indicação em nosso país.
Terceira linha - falha/intolerância à DMCD biológica
Em cenários clínicos que cursam com ausência de resposta ao tratamento biológico inicial, evolução para perda da resposta obtida ou presença de eventos adversos importantes, pode ser feita a troca de um agente biológico por outro. Os biológicos que apresentaram benefícios em ensaios clínicos randomizados com pacientes que falharam ao anti-TNF são ABAT, RTX e TOCI.105 Pacientes que apresentaram falha ao primeiro agente anti-TNF também demonstraram benefício com o uso de uma segunda droga da mesma classe, incluindo ADA, CERT, ETN, IFX ou GOL em estudos observacionais prospectivos e também randomizado controlado duplo-cego (GOL), mas persistem incertezas sobre a magnitude de seus efeitos terapêuticos e a custo-efetividade dessa estratégia.106
A escolha da sequência do tratamento a ser empregado fica a critério médico, dependendo de particularidades de cada caso. Recomenda-se um período mínimo de três meses e máximo de seis meses de avaliação clínica para realizar a troca de esquema terapêutico (mudança entre DMCD biológicas).
Retirada de medicações e eventual suspensão de terapia
Não há dados que permitam definir o tempo de uso de terapia para a AR. No momento, a medicação indicada e à qual o paciente apresente resposta adequada deve ser mantida por período indefinido, a critério médico. Em caso de reposta completa (remissão) e sustentada (por mais de 6-12 meses), pode-se tentar a retirada gradual e cuidadosa na seguinte sequência: primeiramente AINH, seguido por corticoides e DMCD biológicas, mantendo-se o uso de DMCD sintéticas.107Excepcionalmente, se a remissão se mantiver, pode-se com muita cautela tentar a retirada da DMCD sintética.20 A remissão sustentada livre de drogas é pouco frequente, especialmente em pacientes com biomarcadores como anti-CCP e/ou FR.
Monitoração do tratamento
Na doença inicial em pacientes que tenham doença ativa com até um ano de sintomas, recomenda-se o acompanhamento intensivo com visitas mensais e progressão medicamentosa rápida, quando necessário.108,109 Os esquemas terapêuticos e seus possíveis efeitos adversos foram abordados em itens anteriores.
Em cada visita deve-se avaliar a eficácia e a segurança da intervenção terapêutica, considerando as comorbidades do paciente e visando preferencialmente remissão ou menor atividade da doença possível, assim como melhora funcional e da qualidade de vida. Em paciente com doença estabelecida, e especialmente naqueles com doença controlada, as visitas podem ser realizadas a cada três meses.108,109
A Tabela 2 resume, de forma esquemática, a frequência de monitoração dos principais parâmetros considerados para avaliação adequada de um paciente com AR em tratamento.
Terapia física e reabilitação
Durante as fases de atividade da doença, o repouso contribui para a redução do processo inflamatório, devendo-se atentar, porém, para a possibilidade de complicações, como rigidez articular e deformidades em flexão.110
A cinesioterapia pode incluir exercícios passivos, nas fases iniciais, e exercícios ativos, isométricos e/ou isotônicos. A finalidade desses programas de exercícios é garantir manutenção, restauração ou ganho da amplitude de movimento articular, fortalecimento e alongamento muscular, capacidade aeróbica e desempenho para habilidades específicas.110
A maioria dos programas de exercícios dinâmicos segue as recomendações do American College of Sports Medicine (ACSM).111 Recomendamos que o exercício tenha duração de 20 minutos ou mais, que seja realizado no mínimo duas vezes por semana e leve a um aumento de 60% da frequência cardíaca prevista para a idade, para apresentar efeitos clínicos positivos e sem detrimento à doença, ou seja, sem piora da atividade da AR e sem causar dor. Quando se compara o exercício dinâmico ao programa de reabilitação articular convencional, observa-se melhora significativa na qualidade de vida de pacientes com AR.112-114
Atividades aeróbicas como bicicleta, caminhada, corrida, hidroginástica e natação possibilitam melhor condicionamento cardiovascular e podem auxiliar na prevenção da limitação relacionada à AR.110 Os meios físicos podem ser utilizados como adjuvantes no controle da dor, da contratura muscular e da rigidez da articulação.115-119
Terapia ocupacional
A terapia ocupacional emprega diversas técnicas para proteção articular e conservação de energia. O alvo do tratamento é a redução da dor por meio do planejamento de atividades de estimulação, repouso regular, alternância nos padrões de movimento articular e uso de órteses e outros dispositivos.120
Adaptações nos ambientes doméstico e de trabalho auxiliam na preservação da independência do indivíduo com limitações pela AR.121
Órtese é qualquer dispositivo médico usado no corpo do paciente para suportar, alinhar, posicionar, imobilizar, prevenir ou corrigir deformidades, auxiliar na força muscular ou melhorar a função articular. A órtese reduz a dor e a inflamação locais pelo alívio da tensão e da carga sobre determinada articulação.121,122 O uso de órteses/talas de repouso (para punhos, por exemplo) previne a ocorrência de contraturas em flexão. As talas funcionais de punho devem ser usadas intermitentemente durante as atividades para restrição de movimento, objetivando proteção articular.123 As órteses para coluna cervical têm indicação para limitação da mobilidade, especialmente a flexão, com consequente redução da dor, da tensão muscular e da parestesia em casos de subluxação atlanto-axial.120
Tratamento cirúrgico
O tratamento cirúrgico bem indicado contribui para melhora da função, da mobilidade, do controle da dor e da qualidade de vida do paciente com AR. Os procedimentos cirúrgicos incluem, entre outros: sinovectomia, liberação de neuropatias compressivas (p. ex., túnel do carpo), reparo e transferência de tendões, artroplastia total e estabilização de vértebras cervicais instáveis.124,125
Sinovectomia radioisotópica
A sinovectomia radioisotópica com ítrio (90Y) ou samário (153SmPHYP) pode ser indicada para pacientes que apresentem sinovite residual em poucas articulações apesar da otimização dos demais tratamentos instituídos, como uma alternativa à sinovectomia cirúrgica.126
Terapias alternativas
Pacientes com doenças crônicas, como é o caso da AR, frequentemente buscam terapias alternativas, algumas vezes em detrimento do tratamento tradicional. Essas terapias incluem dietas, meditação, biofeedback, acupuntura, massagens, quiropraxia, homeopatia, entre outras. Na maioria das vezes, faltam estudos científicos sobre a segurança e a eficácia desses tratamentos.127
O paciente deve ser orientado a sempre consultar seu médico antes do início de uma dessas terapias. Cabe ao médico avaliar se o pretendido tratamento alternativo pode induzir algum dano ao paciente, e então é sua responsabilidade orientá-lo no sentido de que tais métodos não devem substituir a terapia tradicional para a AR.
Manejo de comorbidades
Comorbidades em pacientes com AR são frequentes, e incluem HAS, diabetes mellitus tipo 2, dislipidemia e osteoporose.128-130Além disso, neoplasias, infecções e doenças pulmonares como bronquiectasia e pneumonite intersticial são também mais prevalentes nesses pacientes.131-134A presença dessas comorbidades contribui para a diminuição da qualidade de vida e aumenta a mortalidade dos pacientes com AR - por isso elas devem ser diagnosticadas e tratadas na fase inicial.135
O manejo das comorbidades será revisado em recomendação específica pela SBR.
Tratamento das manifestações extra-articulares da artrite reumatoide
O tratamento da maioria das manifestações extra-articulares graves da AR (vasculite reumatoide, esclerite, alguns subtipos histológicos da doença intersticial pulmonar, serosite recalcitrante) inclui corticoides sistêmicos (orais ou venosos) e imunossupressores, incluindo CF, CS e AZA.136 Resultados anedotais de melhora clínica de casos de vasculite reumatoide e envolvimento pulmonar estão relatados, mas são conflitantes e carecem de estudos para confirmação.
Transplante de células autólogas
Até o momento, faltam dados conclusivos para referendar o papel do transplante de células-tronco hematopoiéticas como indutor de remissão prolongada na AR do adulto.137 Como a toxicidade e a mortalidade associada ao procedimento ainda são significativas, o transplante de células autólogas no Brasil fica reservado para formas graves, com múltiplas manifestações extra-articulares, refratária aos tratamentos instituídos e com risco de óbito.
CONSIDERAÇÕES SOBRE FARMACOECONOMIA DO TRATAMENTO DA ARTRITE REUMATOIDE NO BRASIL
A introdução de potentes DMCD biológicas ampliou as alternativas para um tratamento efetivo da AR.138 No entanto, essas drogas apresentam custos substancialmente altos em comparação às DMCD sintéticas tradicionais, competindo com os limitados recursos da saúde em outras intervenções essenciais.
De maneira geral, o uso de MTX, SSZ e LFN em pacientes com AR ativa sem tratamento prévio com DMCD tem se mostrado custo-efetivo em comparação ao uso de AINH e corticoides em estudos internacionais.139,140 Por outro lado, o uso de terapia biológica em monoterapia ou em combinação com MTX nesse perfil de pacientes não é custo-efetivo em comparação ao MTX em monoterapia.139
Após falha à primeira DMCD sintética, a introdução de LEF pode ser uma estratégia custo-efetiva, à medida que posterga o uso de biológicos.141 Podemos encontrar dados semelhantes na literatura nacional. Em um estudo que utilizou modelo econômico segundo os princípios da análise de Markov, observou-se que o MTX em monoterapia foi o mais custo-efetivo em um período de 48 meses.142
Na falha de tratamento com agentes anti-TNF, o RTX143e o ABAT144 podem ser custo-efetivos. Já com relação ao uso do segundo e terceiro agentes anti-TNF, nesse contexto, não há ensaios clínicos randomizados que permitam a análise de custo-efetividade.
Quanto à realidade da prática reumatológica brasileira, Ferraz et al.145 publicaram os resultados de um questionário aplicado a reumatologistas brasileiros sobre diagnóstico e tratamento da AR. Verificou-se que aproximadamente 50% dos pacientes com AR estão sendo diagnosticados adequadamente, e que apenas metade deles está em tratamento regular. A prática terapêutica realizada nos serviços públicos e privados não variou de maneira marcante. Em ambos os serviços, a associação MTX + DCQ foi a terapia combinada (dois ou mais DMCD) mais comumente utilizada, seguida de MTX + DCQ + SSZ no serviço público e de MTX + LEF no serviço privado. Após a falha dessas terapias, o agente biológico mais utilizado foi o IFX, provavelmente por ser a única opção terapêutica no Sistema Único de Saúde (SUS) durante o período de realização da pesquisa. As principais dificuldades apontadas para o tratamento dos pacientes foram o acesso ao sistema de saúde (serviço público) e o custo da medicação (sistema privado). Outros aspectos que impõem desafios ao manejo adequado dos pacientes reumatoides em nível nacional são diferenças regionais de acesso aos serviços de saúde, distribuição não homogênea de reumatologistas no território nacional e escassez de serviços especializados.146
É necessário desenvolver estudos farmacoeconômicos com base na realidade nacional capazes de gerar informações que orientem racionalmente as tomadas de decisão no tratamento dos pacientes com AR.
SITUAÇÕES ESPECIAIS
Artrite reumatoide e gravidez
A AR não altera por si só a fertilidade, embora alguns medicamentos possam reduzir a taxa de ovulação. Também não há aumento na ocorrência de complicações fetais ou maternas pela doença, excetuando-se as formas graves que cursam com vasculite sistêmica.147
Durante o período gestacional, observa-se geralmente melhora das manifestações clínicas da AR em até 75% das pacientes, embora 90% apresentem recaída nos primeiros seis meses do puerpério.147
A maioria das drogas utilizadas no tratamento da AR é contraindicada durante a gestação e a lactação, com exceção da HCQ e da SSZ, que parecem ser relativamente seguras.148-150 Pacientes em uso de MTX, LEF, agentes imunossupressores e DMCD biológicas devem sempre ser orientadas a utilizar métodos contraceptivos seguros, a fim de evitar a gestação.150,151
Artrite reumatoide e vacinação
Reconhecidamente, o risco global de infecção está aumentado na AR, particularmente para os pacientes em uso de agentes imunobiológicos. Dessa forma, a necessidade de vacinação para tais pacientes deve ser considerada.152-154 Antes de iniciar DMCD sintéticas ou biológicas, deve-se pedir e atualizar o cartão vacinal do paciente. Vacinas que não contenham organismos vivos, como é o caso daquelas contra influenza (IM), pneumocócica (7V e 23V), tétano, difteria, coqueluche, hemófilos tipo B, hepatite viral A e B, poliomielite (inativada - VIP), meningocócica, HPV, febre tifoide (IM) e raiva, podem ser realizadas com segurança e devem ser administradas preferencialmente 14 dias antes do início da medicação. De maneira mais sistematizada, a maioria dos protocolos recomenda ao menos a vacina antiinfluenza (sazonal, anualmente, entre abril e setembro) e a antipneumocócica (inicialmente, e reforço após cinco anos) antes do início da terapia com DMCD biológicas.154
Vacinas com organismos vivos são contraindicadas durante a imunossupressão e pelo menos três meses após o uso de tais drogas. Esse grupo de vacinas inclui tríplice viral (sarampo, caxumba e rubéola), BCG, vacinas contra influenza (nasal), varicela zoster, febre tifoide, poliomielite (oral - VOP), varíola e febre amarela.154 Devemos, no entanto, levar em consideração algumas situações específicas, como é o caso da indicação da vacina contra febre amarela para a população residente em área endêmica para a doença.155,156
É importante observar que as vacinas, quando indicadas, devem ser administradas preferencialmente antes do tratamento com os imunossupressores ou DMCD biológicas, pois a resposta à vacina pode ser diminuída.153
O manejo da vacinação em pacientes com AR será revisado em recomendação específica pela SBR.
Endemias brasileiras
As doenças transmissíveis endêmico-epidêmicas, como tuberculose (TB), hanseníase, malária, doença de Chagas, esquistossomose, febre amarela, dengue, filarioses, helmintíases e hepatite B e C, ainda são relevante problema de saúde pública no Brasil.157
Embora haja poucos estudos sobre a relação entre as endemias infecto-contagiosas e a AR, é importante considerar que essas condições podem afetar tanto o diagnóstico (algumas vezes mimetizando,5 outras vezes superpondo-se aos sintomas articulares e sistêmicos da AR, além da possível ocorrência de marcadores sorológicos como o anti-CCP e o FR em doenças infecciosas158) quanto o manejo da doença. De especial interesse, o uso de terapias imunossupressoras, destacando aqui as DMCD biológicas, deve ser cuidadosamente avaliado nessas situações específicas.159
Em virtude da alta prevalência de TB em nosso meio e dos relatos de reativação da doença em vigência de tratamento imunossupressor,104,160-164 as DMCD biológicas devem ser empregadas com extrema cautela em pacientes com suscetibilidade ou história prévia de TB, recomendando-se a realização de radiografia de tórax e do teste da tuberculina (PPD) antes do início da terapêutica em todos os pacientes.165 O risco é maior para pacientes que farão uso de anti-TNF, em especial anticorpos monoclonais.166No Brasil não há estudos controlados que demonstrem a relação custo-efetividade do teste tuberculínico em duas etapas para pesquisa de fenômeno "booster" na população de pacientes com AR que serão submetidos à terapia biológica. O PPD pode ser negativo em pacientes com AR em função do distúrbio imunológico subjacente ou da terapia em uso.167 Embora os testes de liberação de gamainterferon (IGRA, do inglês, interferon gamma release assays) in vitro, como Quantiferon® ou Elispot®, sejam promissores,168-170 já que são mais específicos, seu papel na investigação da TB latente em nosso meio não está bem definido.168-171
A realização de TC de tórax de alta resolução para investigação de TB latente deve ser avaliada caso a caso. O tratamento com isoniazida na dose de 5-10 mg/kg/dia, até a dose máxima de 300 mg/dia, por período de seis meses, deve ser realizado nos pacientes com PPD > 5 mm (ou IGRA positivo) ou naqueles com alterações radiológicas compatíveis com TB prévia, ou ainda em pacientes que tiveram contato íntimo com indivíduos com TB ativa.165,172-174 O tratamento da forma latente deve ser iniciado pelo menos um mês antes do início da DMCD biológica. Excepcionalmente, porém, o início pode ser concomitante, quando a atividade da doença inflamatória exigir urgência na introdução de terapia biológica. Embora os estudos até o momento não tenham mostrado aumento da ocorrência de casos de TB com o uso de DMCD biológicas não anti-TNF, recomenda-se a realização de triagem para infecção latente.
Sugere-se a pesquisa de hepatite viral B e C, além de HIV, antes do uso de DMCD biológica. Na presença de uma dessas infecções virais, o uso de DMCD biológica deve ser evitado. Em casos excepcionais de infecção pelo vírus C da hepatite, a DMCD biológica pode ser utilizada em associação com o tratamento antiviral.175,176
Pesquisas de infecções específicas, como a doença de Chagas, devem ser realizadas nas regiões endêmicas. Recomenda-se, ainda, a rotina de avaliação e de cuidados odontológicos antes e durante o tratamento, para profilaxia e tratamento de infecções periodontais.177
RECOMENDAÇÕES DA SBR PARA O TRATAMENTO DA ARTRITE REUMATOIDE
Com base nas considerações feitas e em aspectos peculiares da realidade socioeconômica brasileira, os especialistas membros da Comissão de Artrite Reumatoide da Sociedade Brasileira de Reumatologia fazem as recomendações resumidas na Tabela 3 para o tratamento de pacientes com diagnóstico de AR.
CONCLUSÕES
Este consenso tem o objetivo de listar as recomendações para o tratamento da AR no Brasil, considerando as características peculiares de nosso país, como a disponibilidade de drogas, o nível socioeconômico da população, os aspectos farmacoeconômicos e a ocorrência de diversas endemias.
Embora recentes diretrizes norte-americanas e europeias para o tratamento da AR tenham sido publicadas, é importante rever o assunto, considerando aspectos específicos da realidade brasileira. Dessa forma, o propósito final de estabelecer diretrizes consensuais para o tratamento da AR no Brasil é definir o tratamento e embasar os reumatologistas brasileiros, considerando-se as evidências obtidas em estudos científicos e a experiência de uma comissão de especialistas no assunto, a fim de homogeneizar a abordagem terapêutica da AR no contexto socioeconômico brasileiro, mantendo a autonomia do médico na indicação/escolha das alternativas terapêuticas disponíveis.
Como há rápida evolução do conhecimento nesse campo da ciência, sugerimos a atualização destas recomendações a cada dois anos.
Recebido em 19/11/2011
Aprovado, após revisão, em 13/12/2011
Os conflitos de interesse estão declarados ao final deste artigo.
Sociedade Brasileira de Reumatologia.
Conflitos de interesse:
1. Participou de estudos clínicos e/ou experimentais patrocinados pela indústria farmacêutica [IF (laboratórios Roche e Mantecorp)], relacionados ao consenso em questão; recebeu auxílio pessoal ou institucional da IF (Abbott, AstraZeneca, MSD, Roche e Pfizer); ministrou palestra em eventos ou atividades patrocinadas pela IF (Abbott, AstraZeneca, Janssen, MSD, Mantecorp, Roche e Pfizer) relacionados ao consenso em questão. É membro do Conselho Consultivo ou Diretivo da IF ou de comitês normativos de estudos científicos patrocinados pela IF (AstraZeneca e MSD). Elaborou textos científicos em periódicos patrocinados pela IF (Abbot e Pfizer).
2. Participou de estudos clínicos e/ou experimentais patrocinados pela IF (Roche) relacionados ao consenso em questão; recebeu auxílio pessoal ou institucional da IF (Abbott, BMS, Mantecorp, MSD, Novartis, Roche, Wyeth e Pfizer); ministrou palestra em eventos ou atividades patrocinadas pela IF (Abbott, MSD, Novartis, Roche, Wyeth) relacionados ao consenso em questão.
3. Participou de estudos clínicos e/ou experimentais patrocinados pela IF (BMS, Pfizer, Roche e Wyeth) relacionados ao consenso em questão; recebeu auxílio pessoal ou institucional da IF (Abbott, BMS, Mantecorp, MSD, Roche e Wyeth); ministrou palestra em eventos ou atividades patrocinadas pela IF (Abbott e Roche) relacionados ao consenso em questão.
4. Recebeu auxílio pessoal ou institucional da IF (Abbott, MSD, Janssen, Roche, BMS e Pfizer); ministrou palestra em eventos ou atividades patrocinadas pela IF (Abbott, MSD, Janssen, Roche, BMS e Pfizer) relacionados ao consenso em questão. Foi/é membro do Conselho Consultivo ou Diretivo da IF ou de comitês normativos de estudos científicos patrocinados pela IF (Pfizer, Abbott, MSD e BMS).
5. Participou de estudos clínicos e/ou experimentais patrocinados pela IF (BMS, Pfizer e Roche) relacionados ao consenso em questão; recebeu auxílio pessoal ou institucional da IF (Abbott); elaborou textos científicos em periódicos patrocinados pela IF (Wyeth).
6. Ministrou palestra em eventos ou atividades patrocinadas pela IF (Abbott, Sanofi-Aventis e Pfizer) relacionados ao consenso em questão.
7. Recebeu auxílio pessoal ou institucional da IF (Abbott, MSD, Wyeth, Pfizer e Roche); ministrou palestra em eventos ou atividades patrocinadas pela IF (Abbott, MSD, Wyeth, Pfizer e Roche) relacionados ao consenso em questão. Foi/é membro do Conselho Consultivo ou Diretivo da IF ou de comitês normativos de estudos científicos patrocinados pela IF (Wyeth, MSD e AstraZeneca). Elaborou textos científicos em periódicos patrocinados pela IF (Abbott, Wyeth, BMS e AstraZeneca).
8. Participou de estudos clínicos e/ou experimentais patrocinados pela IF (BMS e Roche) relacionados ao consenso em questão; recebeu auxílio pessoal ou institucional da IF (Roche, MSD, Wyeth/Pfizer e Abbott); ministrou palestra em eventos ou atividades patrocinadas pela IF (Roche, MSD, Janssen e Mantecorp) relacionados ao consenso em questão.
9. O autor declara a inexistência de conflito de interesse.
10. Ministrou palestra em eventos ou atividades patrocinadas pela IF (Roche e BMS) relacionados ao consenso em questão. Foi/é membro do Conselho Consultivo ou Diretivo da IF ou de comitês normativos de estudos científicos patrocinados pela IF (AstraZeneca).
11. Participou de estudos clínicos e/ou experimentais patrocinados pela IF (Roche e Mantecorp) relacionados ao consenso em questão; recebeu auxílio pessoal ou institucional da IF (Lilly, Pfizer e Actelion); ministrou palestra em eventos ou atividades patrocinadas pela IF (Lilly, Pfizer e Actelion) relacionados ao consenso em questão. Foi/é membro do Conselho Consultivo ou Diretivo da IF ou de comitês normativos de estudos científicos patrocinados pela IF (MSD).
12. Recebeu auxílio pessoal ou institucional da IF (Roche e Janssen-Cillag).
-
1Alamanos Y, Voulgari PV, Drosos AA. Incidence and prevalence of rheumatoid arthritis, based on the 1987 American College of Rheumatology criteria: a systematic review. Semin Arthritis Rheum 2006;36(3):182-8.
-
2Marques-Neto JF, Gonçalves ET, Langen LFOB, Cunha Mfl, Radominski S, Oliveira SM et al Multicentric study of the prevalence of adult rheumatoid arthritis in Brazilian population samples. Rev Bras Reumatol 1993;33:169-73.
-
3Verstappen SM, van Albada-Kuipers GA, Bijlsma JW, Blaauw AA, Schenk Y, Haanen HC et al A good response to early DMARD treatment of patients with rheumatoid arthritis in the first year predicts remission during follow up. Ann Rheum Dis 2005;64(1):38-43.
-
4Chehata JC, Hassell AB, Clarke SA, Mattey DL, Jones MA, Jones PW et al Mortality in rheumatoid arthritis: relationship to single and composite measures of disease activity. Rheumatology 2001;40(4):447-52.
-
5da Mota LM, Cruz BA, Brenol CV, Pereira IA, Fronza LS, Bertolo MB et al 2011. Consensus of the Brazilian Society of Rheumatology for diagnosis and early assessment of rheumatoid arthritis. Rev Bras Reumatol 2011;51(3):199-219.
-
6de Azevedo AB, Ferraz MB, Ciconelli RM. Indirect costs of rheumatoid arthritis in Brazil. Value Health 2008;11(5):869-77.
-
7McInnes IB, O'Dell JR. State-of-the-art: rheumatoid arthritis. Ann Rheum Dis 2010;69(11):1898-906.
-
8Klarenbeek NB, Kerstens PJ, Huizinga TW, Dijkmans BA, Allaart CF. Recent advances in the management of rheumatoid arthritis. BMJ 2010;341:c6942.
-
9Abourazzak F, El Mansouri L, Huchet D, Lozac'hmeur R, Hajjaj-Hassouni N, Ingels A et al A. Long-term effects of therapeutic education for patients with rheumatoid arthritis. Joint Bone Spine 2009;76(6):648-53.
-
10Lovisi Neto BE, Jennings F, Barros Ohashi C, Silva PG, Natour J. Evaluation of the efficacy of an educational program for rheumatoid arthritis patients. Clin Exp Rheumatol 2009;27(1):28-34.
-
11Masiero S, Boniolo A, Wassermann L, Machiedo H, Volante D, Punzi L. Effects of an educational-behavioral joint protection program on people with moderate to severe rheumatoid arthritis: a randomized controlled trial. Clin Rheumatol 2007;26(12):2043-50.
-
12Niedermann K, de Bie RA, Kubli R, Ciurea A, Steurer-Stey C, Villiger PM et al Effectiveness of individual resource-oriented joint protection education in people with rheumatoid arthritis. A randomized controlled trial. Patient Educ Couns 201;82(1):42-8.
-
13Lineker SC, Bell MJ, Badley EM. Evaluation of an inter-professional educational intervention to improve the use of arthritis best practices in primary care. J Rheumatol 2011;38(5):931-7.
-
14American College of Rheumatology Subcommittee on Rheumatoid Arthritis Guidelines. Guidelines for the management of rheumatoid arthritis: 2002 Update. Arthritis Rheum 2002;46(2):328-46.
-
15Katchamart W, Johnson S, Lin HJ, Phumethum V, Salliot C, Bombardier C. Predictors for remission in rheumatoid arthritis patients: A systematic review. Arthritis Care Res (Hoboken) 2010;62(8):1128-43.
-
16Ferraz-Amaro I, Machín S, Carmona L, González-Alvaro I, Díaz-González F; EMECAR study group. Pattern of use and safety of non-steroidal anti-inflammatory drugs in rheumatoid arthritis patients. A prospective analysis from clinical practice. Reumatol Clin 2009;5(6):252-8.
-
17Solomon DH, Rassen JA, Glynn RJ, Lee J, Levin R, Schneeweiss S. The comparative safety of analgesics in older adults with arthritis. Arch Intern Med 2010; 170(22):1968-76. [Erratum in: Arch Intern Med 2011;171(5):403]
-
18Chen YF, Jobanputra P, Barton P, Bryan S, Fry-Smith A, Harris G et al Cyclooxygenase-2 selective non-steroidal anti-inflammatory drugs (etodolac, meloxicam, celecoxib, rofecoxib, etoricoxib, valdecoxib and lumiracoxib) for osteoarthritis and rheumatoid arthritis: a systematic review and economic evaluation. Health Technol Assess 2008;12(11):1-278, iii.
-
19van Everdingen AA, Jacobs JW, Siewertsz Van Reesema DR, Bijlsma JW. Low-dose prednisone therapy for patients with early rheumatoid arthritis: clinical efficacy, disease-modifying properties, and side effects: a randomized, double-blind, placebo-controlled clinical trial. Ann Intern Med 2002;136(1):1-12.
-
20Smolen JS, Landewé R, Breedveld FC, Dougados M, Emery P, Gaujoux-Viala C et al EULAR recommendations for the management of rheumatoid arthritis with synthetic and biological disease-modifying antirheumatic drugs. Ann Rheum Dis 2010; 69(6):964-75. [Erratum in: Ann Rheum Dis 2011;70(8):1519]
-
21Hoes JN, Jacobs JW, Verstappen SM, Bijlsma JW, Van der Heijden GJ. Adverse events of low- to medium-dose oral glucocorticoids in inflammatory diseases: a meta-analysis. Ann Rheum Dis 2009;68(12):1833-8.
-
22Dernis E, Ruyssen-Witrand A, Mouterde G, Maillefert JF, Tebib J, Cantagrel A et al Use of glucocorticoids in rheumatoid arthritis - pratical modalities of glucocorticoid therapy: recommendations for clinical practice based on data from the literature and expert opinion. Joint Bone Spine 2010;77(5):451-7.
-
23Furst DE, Pangan AL, Harrold LR, Chang H, Reed G, Kremer JM et al Greater likelihood of remission in rheumatoid arthritis patients treated earlier in the disease course: results from the Consortium of Rheumatology Researchers of North America registry. Arthritis Care Res (Hoboken) 2011;63(6):856-64.
-
24Lukas C, Combe B, Ravaud P, Sibilia J, Landew R, van der Heijde D. Favorable effect of very early disease-modifying antirheumatic drug treatment on radiographic progression in early inflammatory arthritis:Data from the Étude et Suivi des polyarthrites indifférenciées récentes (study and followup of early undifferentiated polyarthritis). Arthritis Rheum 2011;63(7):1804-11.
-
25Cronstein B. How does methotrexate suppress inflammation? Clin Exp Rheumatol 2010;28(5 Suppl 61):S21-3.
-
26Pincus T, Cronstein B, Braun J. Methotrexate - the anchor drug - an introduction. Clin Exp Rheumatol 2010;28(5 Suppl 61):S1-2.
-
27O'Dell JR, Haire CE, Erikson N, Drymalski W, Palmer W, Eckhoff PJ et al Treatment of rheumatoid arthritis with methotrexate alone, sulfasalazine and hydroxychloroquine, or a combination of all three medications. N Engl J Med 1996;334(20):1287-91.
-
28Pereira IA, Cruz BA, Xavier RM, Pinheiro GRC, Titton DC, Giorgi RDN et al National recommendations based on scientific evidence and opinions of experts on the use of methotrexate in rheumatic disorders, especially in rheumatoid arthritis: results of the 3E Initiative from Brazil. Rev Bras Reumatol 2009;49(4):346-61.
-
29Williams HJ, Ward JR, Dahl SL, Clegg DO, Willkens RF, Oglesby T et al A controlled trial comparing sulfasalazine, gold sodium thiomalate, and placebo in rheumatoid arthritis. Arthritis Rheum 1988;31(6):702-13.
-
30Boers M, Verhoeven AC, Markusse HM, van de Laar MA, Westhovens R, van Denderen JC et al Randomised comparison of combined step-down prednisolone, methotrexate and sulphasalazine with sulphasalazine alone in early rheumatoid arthritis. Lancet 1997; 350(9074):309-18. [Erratum in: Lancet 1998;351(9097):220]
-
31Rozman B. Clinical pharmacokinetics of leflunomide. Clin Pharmacokinet 2002;41(6):421-30.
-
32Scott DL, Smolen JS, Kalden JR, van de Putte LB, Larsen A, Kvien TK et al, European Leflunomide Study Group. Treatment of active rheumatoid arthritis with leflunomide: two year follow up of a double blind, placebo controlled trial versus sulfasalazine. Ann Rheum Dis 2001; 60(10):913-23.
-
33Kalden JR, Scott DL, Smolen JS, Schattenkirchner M, Rozman B, Williams BD et al, European Leflunomide Study Group. Improved functional ability in patients with rheumatoid arthritis: longterm treatment with leflunomide versus sulfasalazina. European Leflunomide Study Group. J Rheumatol 2001;28(9):1983-91.
-
34Clark P, Casas E, Tugwell P, Medina C, Gheno C, Tenorio G et al Hydroxychloroquine compared with placebo in rheumatoid arthritis. A randomized controlled trial. Ann Intern Med 1993;119(11):1067-71.
-
35A randomized trial of hydroxychloroquine in early rheumatoid arthritis: the HERA study. Am J Med 1995;98(2):156-68.
-
36Marmor MF, Kellner U, Lai TY, Lyons JS, Mieler WF; American Academy of Ophthalmology. Revised recommendations on screening for chloroquine and hydroxychloroquine retinopathy. Ophthalmology 2011;118(2):415-22.
-
37Suarez-Almazor ME, Belseck E, Shea B, Homik J, Wells G, Tugwell P. Antimalarials for treating rheumatoid arthritis. Cochrane Database Syst Rev 2000; (4):CD000959.
-
38Rau R, Herborn G, Menninger H, Sangha O. Radiographic outcome after three years of patients with early erosive rheumatoid arthritis treated with intramuscular methotrexate or parenteral gold. Extension of a one-year double-blind study in 174 patients. Rheumatology (Oxford) 2002;41(2):196-204.
-
39Lehman AJ, Esdaile JM, Klinkhoff AV, Grant E, Fitzgerald A, Canvin J; METGO Study Group. A 48-week, randomized, doubleblind, double-observer, placebo-controlled multicenter trial of combination methotrexate and intramuscular gold therapy in rheumatoid arthritis: results of the METGO study. Arthritis Rheum 2005;52(5):1360-70.
-
40Caporali R, Conti F, Alivernini S, Atzeni F, Seriolo B, Cutolo M et al Recommendations for the use of biologic therapy in rheumatoid arthritis: update from the Italian Society for Rheumatology I. Efficacy. Clin Exp Rheumatol 2011;29(3 Suppl 66):S7-14.
-
41Favalli EG, Caporali R, Sinigaglia L, Pipitone N, Miniati I, Montecucco C et al Recommendations for the use of biologic therapy in rheumatoid arthritis: update from the Italian Society for Rheumatology II. Safety. Clin Exp Rheumatol 2011;29(3 Suppl 66):S15-27.
-
42Agênica Nacioanl de Vigilância Sanitária (ANVISA). Available from: http://portal.anvisa.gov.br/wps/portal/anvisa [Acessed on November 2, 2011]
» link -
43Markatseli TE, Papagoras C, Drosos AA. Prognostic factors for erosive rheumatoid arthritis. Clin Exp Rheumatol 2010;28(1):114-23.
-
44Visser K, Goekoop-Ruiterman YP, de Vries-Bouwstra JK, Ronday HK, Seys PE, Kerstens PJ et al A matrix risk model for the prediction of rapid radiographic progression in patients with rheumatoid arthritis receiving different dynamic treatment strategies: post hoc analyses from the BeSt study. Ann Rheum Dis 2010;69(7):1333-7.
-
45Smolen JS, Aletaha D, Bijlsma JW, Breedveld FC, Boumpas D, Burmester G et al Treating rheumatoid arthritis to target: recommendations of an international task force. Ann Rheum Dis 2010; 69(4):631-7.
-
46Visser K, Katchamart W, Loza E, Martinez-Lopez JA, Salliot C, Trudeau J et al Multinational evidence-based recommendations for the use of methotrexate in rheumatic disorders with a focus on rheumatoid arthritis: integrating systematic literature research and expert opinion of a broad international panel of rheumatologists in the 3E Initiative. Ann Rheum Dis 2009;68(7):1086-93.
-
47Momohara S, Inoue E, Ikari K, Yano K, Tokita A, Honjo Y et al Comparison of characteristics and therapeutic efficacy in rheumatoid arthritis patients treated by rheumatologists and those treated by orthopedic surgeons under a team medicine approach at the same institute. Mod Rheumatol 2011 Jul 15. [Epub ahead of print]
-
48Genovese MC, Cohen S, Moreland L, Lium D, Robbins S, Newmark R et al Combination therapy with etanercept and anakinra in the treatment of patients with rheumatoid arthritis who have been treated unsuccessfully with methotrexate. Arthritis Rheum 2004;50(5):1412-9.
-
49Weinblatt M, Combe B, Covucci A, Aranda R, Becker JC, Keystone E. Safety of the selective costimulation modulator abatacept in rheumatoid arthritis patients receiving background biologic and nonbiologic disease-modifying antirheumatic drugs: A one-year randomized, placebo-controlled study. Arthritis Rheum 2006;54(9):2807-16.
-
50Kiely PD, Brown AK, Edwards CJ, O'Reilly DT, Ostör AJ, Quinn M et al Contemporary treatment principles for early rheumatoid arthritis: a consensus statement. Rheumatology (Oxford) 2009;48(7):765-72.
-
51Hochberg MC, Tracy JK, Hawkins-Holt M, Flores RH. Comparison of the efficacy of the tumour necrosis factor alphablocking agents adalimumab, etanercept, and infliximab when added to methotrexate in patients with active rheumatoid arthritis. Ann Rheum Dis 2003;62(suppl2):ii13-6.
-
52Hetland ML, Christensen IJ, Tarp U, Dreyer L, Hansen A, Hansen IT et al Direct comparison of treatment responses, remission rates, and drug adherence in patients with rheumatoid arthritis treated with adalimumab, etanercept, or infliximab: results from eight years of surveillance of clinical practice in the nationwide Danish DANBIO registry. Arthritis Rheum 2010;62(1):22-32.
-
53Goekoop-Ruiterman YP, de Vries-Bouwstra JK, Allaart CF, van Zeben D, Kerstens PJ, Hazes JM et al Clinical and radiographic outcomes of four different treatment strategies in patients with early rheumatoid arthritis (the BeSt study): a randomized, controlled trial. Arthritis Rheum 2005;52(11):3381-90.
-
54van der Kooij SM, le Cessie S, Goekoop-Ruiterman YP, de Vries-Bouwstra JK, van Zeben D, Kerstens PJ et al Clinical and radiological efficacy of initial vs delayed treatment with infliximab plus methotrexate in patients with early rheumatoid arthritis. Ann Rheum Dis 2009;68(7):1153-8.
-
55Breedveld FC, Weisman MH, Kavanaugh AF, Cohen SB, Pavelka K, van Vollenhoven R et al The PREMIER study: A multicenter, randomized, double-blind clinical trial of combination therapy with adalimumab plus methotrexate versus methotrexate alone or adalimumab alone in patients with early, aggressive rheumatoid arthritis who had not had previous methotrexate treatment. Arthritis Rheum 2006;54(1):26-37.
-
56Emery P, Genovese MC, van Vollenhoven R, Sharp JT, Patra K, Sasso EH. Less radiographic progression with adalimumab plus methotrexate versus methotrexate monotherapy across the spectrum of clinical response in early rheumatoid arthritis. J Rheumatol 2009;36(7):1429-41.
-
57Emery P, Breedveld F, van der Heijde D, Ferraccioli G, Dougados M, Robertson D et al Combination of Methotrexate and Etanercept in Early Rheumatoid Arthritis Trial Group. Two-year clinical and radiographic results with combination etanercept-methotrexate therapy versus monotherapy in early rheumatoid arthritis: a two-year, doubleblind, randomized study. Arthritis Rheum 2010;62(3):674-82.
-
58Kekow J, Moots RJ, Emery P, Durez P, Koenig A, Singh Aet al Patientreported outcomes improve with etanercept plus methotrexate in active early rheumatoid arthritis and the improvement is strongly associated with remission: the COMET trial. Ann Rheum Dis 2010;69(1):222-5.
-
59Smolen JS, Han C, van der Heijde DM, Emery P, Bathon JM, Keystone E et al; Active-Controlled Study of Patients Receiving Infliximab for the Treatment of Rheumatoid Arthritis of Early Onset (ASPIRE) Study Group. Radiographic changes in rheumatoid arthritis patients attaining different disease activity states with methotrexate monotherapy and infliximab plus methotrexate: the impacts of remission and tumour necrosis factor blockade. Ann Rheum Dis 2009;68(6):823-7.
-
60Emery P, Fleischmann RM, Moreland LW, Hsia EC, Strusberg I, Durez P et al Golimumab, a human anti-tumor necrosis factor alpha monoclonal antibody, injected subcutaneously every four weeks in methotrexate-naive patients with active rheumatoid arthritis: twentyfour-week results of a phase III, multicenter, randomized, doubleblind, placebo-controlled study of golimumab before methotrexate as first-line therapy for early-onset rheumatoid arthritis. Arthritis Rheum 2009;60(8):2272-83.
-
61Strand V, Mease P, Burmester GR, Nikaï E, Coteur G, van Vollenhoven R et al Rapid and sustained improvements in health-related quality of life, fatigue, and other patientreported outcomes in rheumatoid arthritis patients treated with certolizumab pegol plus methotrexate over 1 year: results from the RAPID 1 randomized controlled trial. Arthritis Res Ther 2009; 11(6):R170.
-
62Smolen J, Landewé RB, Mease P, Brzezicki J, Mason D, Luijtens K et al Efficacy and safety of certolizumab pegol plus methotrexate in active rheumatoid arthritis: the RAPID 2 study. A randomised controlled trial. Ann Rheum Dis 2009;68(6):797-804.
-
63van Vollenhoven RF, Ernestam S, Geborek P, Petersson IF, Cöster L, Waltbrand E et al Addition of infliximab compared with addition of sulfasalazine and hydroxychloroquine to methotrexate in patients with early rheumatoid arthritis (Swefot trial): 1-year results of a randomised trial. Lancet 2009;374(9688):459-66.
-
64Bejarano V, Quinn M, Conaghan PG, Reece R, Keenan AM, Walker D et al Effect of the early use of the anti-tumor necrosis factor adalimumab on the prevention of job loss in patients with early rheumatoid arthritis. Arthritis Rheum 2008;59(10):1467-74.
-
65Kimel M, Cifaldi M, Chen N, Revicki D. Adalimumab plus methotrexate improved SF-36 scores and reduced the effect of rheumatoid arthritis (RA) on work activity for patients with early RA. J Rheumatol 2008;35(2):206-15.
-
66van Vollenhoven RF, Cifaldi MA, Ray S, Chen N, Weisman MH. Improvement in work place and household productivity for patients with early rheumatoid arthritis treated with adalimumab plus methotrexate: work outcomes and their correlations with clinical and radiographic measures from a randomized controlled trial companion study. Arthritis Care Res (Hoboken) 2010;62(2):226-34.
-
67Furst DE, Schiff MH, Fleischmann RM, Strand V, Birbara CA, Compagnone D et al Adalimumab, a fully human anti tumor necrosis factor-alpha monoclonal antibody, and concomitant standard antirheumatic therapy for the treatment of rheumatoid arthritis: results of STAR (Safety Trial of Adalimumab in Rheumatoid Arthritis). J Rheumatol 2003;30(12):2563-71.
-
68Nam JL, Winthrop KL, van Vollenhoven RF, Pavelka K, Valesini G, Hensor EM et al Current evidence for the management of rheumatoid arthritis with biological disease-modifying antirheumatic drugs: a systematic literature review informing the EULAR recommendations for the management of RA. Ann Rheum Dis 2010;69(6):976-86.
-
69Kavanaugh A, Smolen JS, Emery P, Purcaru O, Keystone E, Richard L et al Effect of certolizumab pegol with methotrexate on home and work place productivity and social activities in patients with active rheumatoid arthritis. Arthritis Rheum 2009;61(11):1592-600.
-
70Genovese MC, Bathon JM, Martin RW, Fleischmann RM, Tesser JR, Schiff MH et al Etanercept versus methotrexate in patients with early rheumatoid arthritis: two-year radiographic and clinical outcomes. Arthritis Rheum 2002; 46(6):1443-50.
-
71Maini R, St Clair EW, Breedveld F, Furst D, Kalden J, Weisman M et al Infliximab (chimeric anti-tumour necrosis factor alpha monoclonal antibody) versus placebo in rheumatoid arthritis patients receiving concomitant methotrexate: a randomised phase III trial. ATTRACT Study Group. Lancet 1999; 354(9194):1932-9.
-
72Keystone E, Genovese MC, Klareskog L, Hsia EC, Hall S, Miranda PC et al Golimumab in patients with active rheumatoid arthritis despite methotrexate therapy: 52-week results of the GO-FORWARD study. Ann Rheum Dis 2010;69(6):1129-35.
-
73Singh JA, Wells GA, Christensen R, Tanjong Ghogomu E, Maxwell L, Macdonald JK et al Adverse effects of biologics: a network meta-analysis and Cochrane overview. Cochrane Database Syst Rev 2011;(2):CD008794.
-
74Curtis JR, Patkar N, Xie A, Martin C, Allison JJ, Saag M et al Risk of serious bacterial infections among rheumatoid arthritis patients exposed to tumor necrosis factor alpha antagonists. Arthritis Rheum 2007;56(4):1125-33.
-
75Dixon WG, Symmons DP, Lunt M, Watson KD, Hyrich KL; British Society for Rheumatology Biologics Register Control Centre Consortium et al Serious infection following anti-tumor necrosis factor alpha therapy in patients with rheumatoid arthritis: lessons from interpreting data from observational studies. Arthritis Rheum 2007;56(9):2896-904.
-
76Radstake TR, Svenson M, Eijsbouts AM, van den Hoogen FH, Enevold C, van Riel PL et al Formation of antibodies against infliximab and adalimumab strongly correlates with functional drug levels and clinical responses in rheumatoid arthritis. Ann Rheum Dis 2009;68(11):1739-45.
-
77Bartelds GM, Wijbrandts CA, Nurmohamed MT, Stapel S, Lems WF, Aarden L et al Anti-infliximab and anti-adalimumab antibodies in relation to response to adalimumab in infliximab switchers and antitumour necrosis factor naive patients: a cohort study. Ann Rheum Dis 2010;69(5):817-21.
-
78Maxwell LJ, Singh JA. Abatacept for rheumatoid arthritis: a Cochrane systematic review. J Rheumatol 2010;37(2):234-45.
-
79Westhovens R, Robles M, Ximenes AC, Nayiager S, Wollenhaupt J, Durez P et al Clinical efficacy and safety of abatacept in methotrexate-naive patients with early rheumatoid arthritis and poor prognostic factors. Ann Rheum Dis 2009;68(12):1870-7.
-
80Bathon J, Robles M, Ximenes AC, Nayiager S, Wollenhaupt J, Durez P et al Sustained disease remission and inhibition of radiographic progression in methotrexate-naïve patients with rheumatoid arthritis and poor prognostic factors treated with abatacept: 2-year outcomes. Ann Rheum Dis 201170(11):1949-56.
-
81Miller KL, Sawitzke AD, Doane J. Abatacept and serious respiratory infections in patients with previous lung disease. Clin Rheumatol 2008;27(12):1569-71.
-
82Cohen SB, Emery P, Greenwald MW, Dougados M, Furie RA, Genovese MC et al Rituximab for rheumatoid arthritis refractory to anti-tumor necrosis factor therapy: Results of a multicenter, randomized, double-blind, placebo-controlled, phase III trial evaluating primary efficacy and safety at twenty-four weeks. Arthritis Rheum 2006;54(9):2793-806.
-
83Emery P, Deodhar A, Rigby WF, Isaacs JD, Combe B, Racewicz AJ et al Efficacy and safety of different doses and retreatment of rituximab: a randomised, placebo-controlled trial in patients who are biological naive with active rheumatoid arthritis and an inadequate response to methotrexate (Study Evaluating Rituximab's Efficacy in MTX iNadequate rEsponders (SERENE)). Ann Rheum Dis 2010;69(9):1629-35.
-
84Keystone E, Emery P, Peterfy CG, Tak PP, Cohen S, Genovese MC et al Rituximab inhibits structural joint damage in patients with rheumatoid arthritis with an inadequate response to tumour necrosis factor inhibitor therapies. Ann Rheum Dis 2009; 68(2):216-21.
-
85Popa C, Leandro MJ, Cambridge G, Edwards JC. Repeated B lymphocyte depletion with rituximab in rheumatoid arthritis over 7 years. Rheumatology (Oxford) 2007;46(4):626-30.
-
86Chatzidionysiou K, Lie E, Nasonov E, Lukina G, Hetland ML, Tarp U et al Highest clinical effectiveness of rituximab in autoantibodypositive patients with rheumatoid arthritis and in those for whom no more than one previous TNF antagonist has failed: pooled data from 10 European registries. Ann Rheum Dis 2011;70(9):1575-80.
-
87Jones G, Sebba A, Gu J, Lowenstein MB, Calvo A, Gomez-Reino JJ et al Comparison of tocilizumab monotherapy versus methotrexate monotherapy in patients with moderate to severe rheumatoid arthritis: the AMBITION study. Ann Rheum Dis 2010;69(1):88-96.
-
88Campbell L, Chen C, Bhagat SS, Parker RA, Östör AJ. Risk of adverse events including serious infections in rheumatoid arthritis patients treated with tocilizumab: a systematic literature review and meta-analysis of randomized controlled trials. Rheumatology (Oxford) 2011; 50(3):552-62.
-
89Singh JA, Beg S, Lopez-Olivo MA. Tocilizumab for rheumatoid arthritis: a Cochrane systematic review. J Rheumatol 2011;38(1):10-20.
-
90Gout T, Östör AJ, Nisar MK. Lower gastrointestinal perforation in rheumatoid arthritis patients treated with conventional DMARDs or tocilizumab: a systematic literature review. Clin Rheumatol 2011;30(11):1471-4.
-
91Suarez-Almazor ME, Spooner C, Belseck E. Azathioprine for treating rheumatoid arthritis. Cochrane Database Syst Rev 2000;(4):CD001461.
-
92Suarez-Almazor ME, Belseck E, Shea B, Wells G, Tugwell P. Cyclophosphamide for treating rheumatoid arthritis. Cochrane Database Syst Rev 2000;(4):CD001157.
-
93Wells G, Haguenauer D, Shea B, Suarez-Almazor ME, Welch VA, Tugwell P. Cyclosporine for rheumatoid arthritis. Cochrane Database Syst Rev 2000;(2):CD001083.
-
94Stein CM, Pincus T, Yocum D, Tugwell P, Wells G, Gluck O et al Combination treatment of severe rheumatoid arthritis with cyclosporine and methotrexate for forty-eight weeks: an open-label extension study. The Methotrexate-Cyclosporine Combination Study Group. Arthritis Rheum1997;40(10):1843-51.
-
95Knevel R, Schoels M, Huizinga TW, Aletaha D, Burmester GR, Combe B et al Current evidence for a strategic approach to the management of rheumatoid arthritis with disease-modifying antirheumatic drugs: a systematic literature review informing the EULAR recommendations for the management of rheumatoid arthritis. Ann Rheum Dis 2010;69(6):987-94.
-
96Katchamart W, Trudeau J, Phumethum V, Bombardier C. Methotrexate monotherapy versus methotrexate combination therapy with non-biologic disease modifying anti-rheumatic drugs for rheumatoid arthritis. Cochrane Database Syst Rev 201014;(4):CD008495.
-
97Scott DL, Wolfe F, Huizinga TW. Rheumatoid arthritis. Lancet 2010;376(9746):1094-108.
-
98Suarez-Almazor ME, Belseck E, Shea B, Wells G, Tugwell P. Sulfasalazine for rheumatoid arthritis. Cochrane Database Syst Rev 2000;(2):CD000958.
-
99Osiri M, Shea B, Robinson V, Suarez-Almazor M, Strand V, Tugwell P et al Leflunomide for treating rheumatoid arthritis. Cochrane Database Syst Rev 2003;(1):CD002047.
-
100Hamilton J, McInnes IB, Thomson EA, Porter D, Hunter JA, Madhok R et al Comparative study of intramuscular gold and methotrexate in a rheumatoid arthritis population from a socially deprived area. Ann Rheum Dis 2001;60(6):566-72.
-
101van der Heijde DM, van Riel PL, Nuver-Zwart IH, van de Putte LB. Sulphasalazine versus hydroxychloroquine in rheumatoid arthritis: 3-year follow-up. Lancet 1990;335(8688):539-53.
-
102Svensson B, Boonen A, Albertsson K, van der Heijde D, Keller C, Hafström I. Low-dose prednisolone in addition to the initial disease-modifying antirheumatic drug in patients with early active rheumatoid arthritis reduces joint destruction and increases the remission rate: a two-year randomized trial. Arthritis Rheum 2005;52(11):3360-70.54.
-
103Kremer JM, Genovese MC, Cannon GW, Caldwell JR, Cush JJ, Furst DE et al Concomitant leflunomide therapy in patients with active rheumatoid arthritis despite stable doses of methotrexate. A randomized, double-blind, placebo-controlled trial. Ann Intern Med 2002;137(9):726-33.
-
104Titton DC, Silveira IG, Louzada-Junior P, Hayata AL, Carvalho HM, Ranza R et al Brazilian biologic registry: BiobadaBrasil implementation process and preliminary results. Rev Bras Reumatol 2011;51(2):152-60.
-
105Salliot C, Finckh A, Katchamart W, Lu Y, Sun Y, Bombardier C et al Indirect comparisons of the efficacy of biological anti-rheumatic agents in rheumatoid arthritis in patients with an inadequate response to conventional disease-modifying anti-rheumatic drugs or to an anti-tumour necrosis factor agent: a meta-analysis. Ann Rheum Dis 2011;70(2):266-71.
-
106Malottki K, Barton P, Tsourapas A, Uthman AO, Liu Z, Routh K et al Adalimumab, etanercept, infliximab, rituximab and abatacept for the treatment of rheumatoid arthritis after the failure of a tumour necrosis factor inhibitor: a systematic review and economic evaluation. Health Technol Assess 2011;15(14):1-278.
-
107O'Mahony R, Richards A, Deighton C, Scott D. Withdrawal of disease-modifying antirheumatic drugs in patients with rheumatoid arthritis: a systematic review and meta-analysis. Ann Rheum Dis 2010;69(10):1823-6.
-
108Grigor C, Capell H, Stirling A, McMahon AD, Lock P, Vallance R et al Effect of a treatment strategy of tight control for rheumatoid arthritis (the TICORA study): a single-blind randomised controlled trial. Lancet 2004;364(9430):263-9.
-
109Deighton C, OMahony R, Tosh J, Turner C, Rudolf M. Guideline Development Group. Management of rheumatoid arthritis: summary of NICE guidance. BMJ 2009;338:b702.
-
110Vliet Vlieland TP. Rehabilitation of people with rheumatoid arthritis. Best Pract Res Clin Rheumatol 2003;17(5):847-61.
-
111Garber CE, Blissmer B, Deschenes MR, Franklin BA, Lamonte MJ, Lee IM et al American College of Sports Medicine. American College of Sports Medicine position stand. Quantity and quality of exercise for developing and maintaining cardiorespiratory, musculoskeletal, and neuromotor fitness in apparently healthy adults: guidance for prescribing exercise. Med Sci Sports Exerc 2011;43(7):1334-59.
-
112Baillet A, Payraud E, Niderprim V-A, Nissen MJ, Allenet B, François P et al A dynamic exercise program to improve patients' disability in rheumatoid arthritis: a prospective randomized controlled trial. Rheumatology 2009; 48(4):10-415.
-
113de Jong Z, Munneke M, Zwinderman AH, Kroon HM, Jansen A, Ronday KH et al Is a long-term high-intensity exercise program effective and safe in patients with rheumatoid arthritis? Results of a randomized controlled trial. Arthritis Rheum 2003;48(9):2415-24.
-
114Munneke M, de Jong Z, Zwinderman AH, Ronday HK, van Schaardenburg D, Dijkmans BA et al Effect of a high-intensity weight-bearing exercise program on radiologic damage progression of the large joints in subgroups of patients with rheumatoid arthritis. Arthritis Rheum 2005;53(3):410-7.
-
115Robinson V, Brosseau L, Casimiro L, Judd M, Shea B, Wells G et al Thermotherapy for treating rheumatoid arthritis. Cochrane Database Syst Rev 2002;(2):CD002826.
-
116Brosseau LU, Pelland LU, Casimiro LY, Robinson VI, Tugwell PE, Wells GE. Electrical stimulation for the treatment of rheumatoid arthritis. Cochrane Database Syst Rev 2002;(2):CD003687.
-
117Brosseau L, Judd MG, Marchand S, Robinson VA, Tugwell P, Wells G et al Transcutaneous electrical nerve stimulation (TENS) for the treatment of rheumatoid arthritis in the hand. Cochrane Database Syst Rev 2003;(3):CD004377.
-
118Brosseau L, Robinson V, Wells G, Debie R, Gam A, Harman K et al Low level laser therapy (Classes I, II and III) for treating rheumatoid arthritis. Cochrane Database Syst Rev 2005; (4):CD002049.
-
119Meireles SM, Jones A, Jennings F, Suda AL, Parizotto NA, Natour J. Assessment of the effectiveness of low-level laser therapy on the hands of patients with rheumatoid arthritis: a randomized doubleblind controlled trial. Clin Rheumatol 2010;29(5):501-9.
-
120Vliet Vlieland TP, van den Ende CH. Nonpharmacological treatment of rheumatoid arthritis. Curr Opin Rheumatol 2011;23(3):259-64.
-
121Hand C, Law M, McColl MA. Occupational therapy interventions for chronic diseases: a scoping review. Am J Occup Ther 2011;65(4):428-36.
-
122Vliet Vlieland TP. Non-drug care for RA - is the era of evidencebased practice approaching? Rheumatology 2007;46(9):1397-404.
-
123Veehof MM, Taal E, Heijnsdijk-Rouwenhorst LM, van de Laar MA. Efficacy of wrist working splints in patients with rheumatoid arthritis: a randomized controlled study. Arthritis Rheum 2008;59(12):1698-704.
-
124Boonen A, Matricali GA, Verduyckt J, Taelman V, Verschueren P, Sileghem A et al Orthopaedic surgery in patients with rheumatoid arthritis: a shift towards more frequent and earlier non-jointsacrificing surgery. Ann Rheum Dis 2006;65(5):694-5.
-
125Kapetanovic MC, Lindqvist E, Saxne T, Eberhardt K. Orthopaedic surgery in patients with rheumatoid arthritis over 20 years: prevalence and predictive factors of large joint replacement. Ann Rheum Dis 2008;67(10):1412-6.
-
126Dos Santos MF, Furtado RN, Konai MS, Castiglioni ML, Marchetti RR, Silva CP et al Effectiveness of radiation synovectomy with Yttrium-90 and Samarium-153 particulate hydroxyapatite in rheumatoid arthritis patients with knee synovitis: a controlled, randomized, double-blinded trial. Clin Rheumatol 2011;30(1):77-85.
-
127Macfarlane GJ, El-Metwally A, De Silva V, Ernst E, Dowds GL, Moots RJ; on behalf of the Arthritis Research UK Working Group on Complementary and Alternative Medicines. Evidence for the efficacy of complementary and alternative medicines in the management of rheumatoid arthritis: a systematic review. Rheumatology (Oxford) 2011;50(9):1672-83.
-
128Mazzantini M, Talarico R, Doveri M, Consensi A, Cazzato M, Bazzichi L et al Incident comorbidity among patients with rheumatoid arthritis treated or not with low-dose glucocorticoids: a retrospective study. J Rheumatol 2010;37(11):2232-6.
-
129Myasoedova E, Davis JM 3rd, Crowson CS, Gabriel SE. Epidemiology of rheumatoid arthritis: rheumatoid arthritis and mortality. Curr Rheumatol Rep 2010;12(5):379-85.
-
130Nurmohamed MT. Atherogenic lipid profiles and its management in patients with rheumatoid arthritis. Vasc Health Risk Manag 2007;3(6):845-52.
-
131Smitten AL, Simon TA, Hochberg MC, Suissa S. A meta-analysis of the incidence of malignancy in adult patients with rheumatoid arthritis. Arthritis Res Ther 2008;10(2):R45.
-
132Geborek P, Jacobsson LT, Lindblad S, Lysholm J, Rantapää-Dahlqvist S, Saxne T et al Risks of solid cancers in patients with rheumatoid arthritis and after treatment with tumour necrosis factor antagonists. Ann Rheum Dis 2005;64(10):1421-6.
-
133Mikuls TR. Co-morbidity in rheumatoid arthritis. Best Pract Res Clin Rheumatol 2003;17:729-52.
-
134Bongartz T, Nannini C, Medina-Velasquez YF, Achenbach SJ, Crowson CS, Ryu JH et al Incidence and mortality of interstitial lung disease in rheumatoid arthritis: a population-based study. Arthritis Rheum 2010; 62(6):1583-91.
-
135Sokka T, Abelson B, Pincus T. Mortality in rheumatoid arthritis: 2008 update. Clin Exp Rheumatol 2008 26(5 Suppl 51):S35-61.
-
136Mielants H, Van den Bosch F. Extra-articular manifestations. Clin Exp Rheumatol 2009;27(4 Suppl 55):S56-61.
-
137Szodoray P, Varoczy L, Szegedi G, Zeher M. Autologous stem cell transplantation in autoimmune and rheumatic diseases: from the molecular background to clinical applications. Scand J Rheumatol 2010;39(1):1-11.
-
138Kobelt G. Health economic issues in rheumatoid arthritis. Scand J Rheumatol 2006;35(6):415-25.
-
139Schoels M, Wong J, Scott DL, Zink A, Richards P, Landewé R et al Economic aspects of treatment options in rheumatoid arthritis: a systematic literature review informing the EULAR recommendations for the management of rheumatoid arthritis. Ann Rheum Dis 2010;69(6):995-1003.
-
140Finckh A, Bansback N, Marra CA, Anis AH, Michaud K, Lubin S et al Treatment of very early rheumatoid arthritis with symptomatic therapy, disease-modifying anti-rheumatic drugs, or biologic agents: a cost-effectiveness analysis. Ann Intern Med 2009;151(9):612-21.
-
141Welsing PM, Severens JL, Hartman M, van Riel PL, Laan RF. Modeling the 5-year cost effectiveness of treatment strategies including tumor necrosis factor-blocking agents and leflunomide for treating rheumatoid arthritis in the Netherlands. Arthritis Rheum 2004;51(6):964-73.
-
142Monteiro RDC, Zanini AC. Cost analysis of drug therapy in rheumatoid arthritis. Revista Brasileira de Ciências Farmacêuticas 2008;44(1):25-33.
-
143Kielhorn A, Porter D, Diamantopoulos A, Lewis G. UK cost-utility analysis of rituximab in patients with rheumatoid arthritis that failed to respond adequately to a biologic disease-modifying anti-rheumatic drug. Curr Med Res Opin 2008;24(9):2639-50.
-
144Vera-Llonch M, Massarotti E, Wolfe F, Shadick N, Westhovens R, Sofrygin O et al Cost-effectiveness of abatacept in patients with moderately to severely active rheumatoid arthritis and inadequate response to tumor necrosis factor-alpha antagonists. J Rheumatol 2008;35(9):1745-53.
-
145Ferraz MB, de Soarez PC, Riera R, Ciconelli RM. Diagnosis and therapeutical management offered to rheumatoid arthritis patients in Brazil - rheumatologists' answers from an assessment questionnaire. Acta Reumatol Port 2009;34(1):44-51.
-
146Cavalcanti FS. Management of rheumatoid diseases: the Brazilian perspective. Rheumatology (Oxford) 2010;49(12):2231-2.
-
147Hazes JM, Coulie PG, Geenen V, Vermeire S, Carbonnel F, Louis E et al Rheumatoid arthritis and pregnancy: evolution of disease activity and pathophysiological considerations for drug use. Rheumatology (Oxford) 2011;50(11):1955-68.
-
148Kuriya B, Hernández-Díaz S, Liu J, Bermas BL, Daniel G, Solomon DH. Patterns of medication use during pregnancy in rheumatoid arthritis. Arthritis Care Res 2011;63(5):721-8.
-
149Abarientos C, Sperber K, Shapiro DL, Aronow WS, Chao CP, Ash JY. Hydroxychloroquine in systemic lupus erythematosus and rheumatoid arthritis and its safety in pregnancy. Expert Opin Drug Saf 2011; 10(5):705-14.
-
150Partlett R, Roussou E. The treatment of rheumatoid arthritis during pregnancy. Rheumatol Int 2011;31(4):445-9.
-
151Thompson AE, Bashook PG. Rheumatologists recommended patient information when prescribing methotrexate for rheumatoid arthritis. Clin Exp Rheumatol 2010;28(4):539-45.
-
152Bengtsson C, Kapetanovic MC, Källberg H, Sverdrup B, Nordmark B, Klareskog L et al; EIRA Study Group. Common vaccinations among adults do not increase the risk of developing rheumatoid arthritis: results from the Swedish EIRA study. Ann Rheum Dis 2010; 69(10):1831-3.
-
153RibeiroAC, Guedes LK, Moraes JC, Saad CG,Aikawa NE, CalichAL et al Reduced seroprotection after pandemic H1N1 influenza adjuvantfree vaccination in patients with rheumatoid arthritis: implications for clinical practice. Ann Rheum Dis 2011;70(12):2144-7.
-
154Heijstek MW, Ott de Bruin LM, Bijl M, Borrow R, van der Klis F, Koné-Paut I et al EULAR recommendations for vaccination in paediatric patients with rheumatic diseases. Ann Rheum Dis 2011;70(10):1704-12.
-
155Scheinberg M, Guedes-Barbosa LS, Mangueira C, Rosseto EA, Mota L, Oliveira AC et al Yellow fever revaccination during infliximab therapy. Arthritis Care Res (Hoboken) 2010;62(6):896-8.
-
156Mota LM, OliveiraAC,Lima RA, Santos-Neto LL, Tauil PL. Vaccination against yellow fever among patients on immunosuppressors with diagnoses of rheumatic diseases. Rev Soc Bras Med Trop 2009;42(1):23-7.
-
157Barreto ML, Teixeira MG, Bastos fi, Ximenes RA, Barata RB, Rodrigues LC. Successes and failures in the control of infectious diseases in Brazil: social and environmental context, policies, interventions, and research needs. Lancet 2011;377(9780):1877-89.
-
158Lima I, Santiago M. Antibodies against cyclic citrullinated peptides in infectious diseases - a systematic review. Clin Rheumatol 2010;29(12):1345-51.
-
159Mody GM, Cardiel MH. Challenges in the management of rheumatoid arthritis in developing countries. Best Pract Res Clin Rheumatol 2008;22(4):621-41.
-
160Wallis RS. Biologics and infections: lessons from tumor necrosis factor blocking agents. Infect Dis Clin North Am 2011;25(4):895-910.
-
161Askling J, Fored CM, Brandt L, Baecklund E, Bertilsson L, Coster L et al Risk and case characteristics of tuberculosis in rheumatoid arthritis associated with tumor necrosis factor antagonists in Sweden. Arthritis Rheum 2005;52(7):1986-92.
-
162Dixon WG, Watson K, Lunt M, Hyrich KL, Silman AJ, Symmons DP. Rates of serious infection, including site-specific and bacterial intracellular infection, in rheumatoid arthritis patients receiving anti-tumor necrosis factor therapy: results from the British Society for Rheumatology Biologics Register. Arthritis Rheum 2006;54(8):2368-76.
-
163Ellerin T, Rubin RH, Weinblatt ME. Infections and anti-tumor necrosis factor alpha therapy.Arthritis Rheum 2003;48(11):3013-22.
-
164Gomez-Reino JJ, Carmona L, Valverde VR, Mola EM, Montero MD. Treatment of rheumatoid arthritis with tumor necrosis factor inhibitors may predispose to significant increase in tuberculosis risk: a multicenter active-surveillance report. Arthritis Rheum 2003;48(8):2122-7.
-
165Sociedade Brasileira de Pneumologia e Tisiologia. III Diretrizes em Tuberculose da SBPT. J Bras Pneumol 2009;35(10):1018-48.
-
166Tubach F, Salmon D, Ravaud P, Allanore Y, Goupille P, Bréban M et al Risk of tuberculosis is higher with anti-tumor necrosis factor monoclonal antibody therapy than with soluble tumor necrosis factor receptor therapy: The three-year prospective French Research Axed on Tolerance of Biotherapies registry. Arthritis Rheum 2009;60(7):1884-94.
-
167Callado MR, Lima JR, Nobre CA, Vieira WP. Low prevalence of reactive PPD prior to infliximab use: comparative study on a population sample of Hospital Geral de Fortaleza. Rev Bras Reumatol 2011;51(1):40-52.
-
168Ponce de Leon D, Acevedo-Vasquez E, Alvizuri S, Gutierrez C, Cucho M, Alfaro J et al Comparison of an interferon-gamma assay with tuberculin skin testing for detection of tuberculosis (TB) infection in patients with rheumatoid arthritis in a TB-endemic population. J Rheumatol 2008;35(5):776-81.
-
169Bocchino M, Matarese A, Bellofiore B, Giacomelli P, Santoro G, Balato N et al Performance of two commercial blood IFN-gamma release assays for the detection of Mycobacterium tuberculosis infection in patient candidates for anti-TNF-alpha treatment. Eur J Clin Microbiol Infect Dis 2008; 27(10):907-13.
-
170Kowada A. Cost effectiveness of interferon-gamma release assay for tuberculosis screening of rheumatoid arthritis patients prior to initiation of tumor necrosis factor-α antagonist therapy. Mol Diagn Ther 2010;14(6):367-73.
-
171Machado A Jr, Emodi K, Takenami I, Finkmoore BC, Barbosa T, Carvalho J et al Analysis of discordance between the tuberculin skin test and the interferon-gamma release assay. Int J Tuberc Lung Dis 2009;13(4):446-53.
-
172Smieja MJ, Marchetti CA, Cook DJ, Smaill FM. Isoniazid for preventing tuberculosis in non-HIV infected persons. Cochrane Database Syst Rev 2000;(2):CD001363.
-
173Pineda NI, Pereira SM, Matos ED, Barreto ML. Quimioprofilaxia na prevenção da tuberculose. J Bras Pneumol 2004;30(4):485-95.
-
174Fonseca JE, Lucas H, Canhão H, Duarte R, Santos MJ, Villar M et al Grupo de Estudos de Artrite Reumatoide da Sociedade Portuguesa de Reumatologia; Comissão de Tuberculose da Sociedade Portuguesa de Pneumologia. Recommendations for the diagnosis and treatment of latent and active tuberculosis in patients with inflammatory joint diseases treated with tumour necrosis factor alpha inhibitors. Acta Reumatol Port 2006;31(3):237-45.
-
175Cabrera Villalba SR, Victoria Hernández Miguel M, Sanmartí Sala R. How does one manage patients with rheumatoid arthritis and positive serology to hepatitis B, hepatitis C, human immunodeficiency virus? Reumatol Clin 2011;7(3):203-7.
-
176Roux CH, Brocq O, Breuil V,Albert C, Euller-Ziegler L. Safety of anti-TNF-alpha therapy in rheumatoid arthritis and spondylarthropathies with concurrent B or C chronic hepatitis. Rheumatology (Oxford) 2006;45(10):1294-7.
-
177Detert J, Pischon N, Burmester GR, Buttgereit F. The association between rheumatoid arthritis and periodontal disease. Arthritis Res Ther 2010;12(5):218.
Correspondência para:
Datas de Publicação
-
Publicação nesta coleção
26 Mar 2012 -
Data do Fascículo
Abr 2012
Histórico
-
Recebido
19 Nov 2011 -
Aceito
13 Dez 2011