Resumos
A Spirulina platensis tem sido estudada devido a seu alto valor protéico, digestibilidade e por apresentar quantidades significativas de ácidos graxos poliinsaturados, vitaminas, fenólicos e ficocianina, podendo ser utilizada na alimentação humana. A utilização de nutrientes de baixo custo é um fator importante na produção da cianobactéria por possibilitar a redução de custos de processo. Objetivou-se com este trabalho estudar o cultivo mixotrófico da S. platensis por meio da adição de uma fonte orgânica de carbono (glicose) em modo bateladaalimentada. Foi utilizado um Planejamento Fatorial Completo 2³ para o cultivo e as variáveis de estudo foram a concentração de glicose (0,5 gL-1 e 1,0 gL-1), a diluição do meio Zarrouk (50% e 75%) e a iluminância (1800 lux e 3000 lux). A concentração celular máxima obtida foi de 5,38 gL-1 com uma velocidade específica máxima de crescimento de 0,0063 h-1, nas condições de 0,5 gL-1 de glicose, diluição do meio de 75% e iluminância de 3000 lux.
Biomassa; glicose; iluminância; mixotrófico; Spirulina platensis
The cyanobacterium Spirulina platensis has been studied due to its high content (~65%) of highly digestible protein as well as significant amounts of polyunsaturated fatty acids, phenolics, vitamins, minerals and phycocyanin which could be useful in the human nutrition. The use of nutrients of low costs in the cyanobacterium growth could reduce the costs of production. We studied the fed-batch mixotrophic growth of the S. platensis in Zarrouk's medium with glucose (0.5 gL-1 and 1.0 gL-1) as carbon source and also investigated the effects of dilution (50% and 75%, with water) and illumination (1,800 lux and 3,000 lux) using a 2³ factorial design. The maximum celular concentration of 5.38 gL-1 and maximum specific growth rate of 0.0063 h-1 were obtained with a glucose concentration of 0.5 gL-1, 50% dilution and 1800 lux of illuminance.
Biomass; glucose; illuminance; mixotrophic; Spirulina platensis
CIÊNCIAS AGRÁRIAS
Cultivo mixotrófico da microalga Spirulina platensis em batelada alimentada
Mixotrophic growth of Spirulina platensis in fed-batch mode
Adriana MuliternoI; Patrícia Correa MoseleI; Jorge Alberto Vieira CostaII; Marcelo HemkemeierIII; Telma Elita BertolinIII; Luciane Maria CollaIII
IAcadêmicas do Curso de Engenharia de Alimentos Faculdade de Engenharia e Arquitetura/FEAR/UPF, Campus I, BR 285, Km 171 Cx. P. 611
99.001-970 Passo Fundo Rio Grande do Sul adridom@via-rs.com.br
IIProfessor do Curso de Engenharia de Alimentos, FURG dqmjorge@furg.br
IIIProfessores do Curso de Engenharia de Alimentos, FEAR/UPF lmcolla@upf.br
RESUMO
A Spirulina platensis tem sido estudada devido a seu alto valor protéico, digestibilidade e por apresentar quantidades significativas de ácidos graxos poliinsaturados, vitaminas, fenólicos e ficocianina, podendo ser utilizada na alimentação humana. A utilização de nutrientes de baixo custo é um fator importante na produção da cianobactéria por possibilitar a redução de custos de processo. Objetivou-se com este trabalho estudar o cultivo mixotrófico da S. platensis por meio da adição de uma fonte orgânica de carbono (glicose) em modo bateladaalimentada. Foi utilizado um Planejamento Fatorial Completo 23 para o cultivo e as variáveis de estudo foram a concentração de glicose (0,5 gL-1 e 1,0 gL-1), a diluição do meio Zarrouk (50% e 75%) e a iluminância (1800 lux e 3000 lux). A concentração celular máxima obtida foi de 5,38 gL-1 com uma velocidade específica máxima de crescimento de 0,0063 h-1, nas condições de 0,5 gL-1 de glicose, diluição do meio de 75% e iluminância de 3000 lux.
Termos para indexação: Biomassa, glicose, iluminância, mixotrófico, Spirulina platensis.
ABSTRACT
The cyanobacterium Spirulina platensis has been studied due to its high content (~65%) of highly digestible protein as well as significant amounts of polyunsaturated fatty acids, phenolics, vitamins, minerals and phycocyanin which could be useful in the human nutrition. The use of nutrients of low costs in the cyanobacterium growth could reduce the costs of production. We studied the fed-batch mixotrophic growth of the S. platensis in Zarrouk's medium with glucose (0.5 gL-1 and 1.0 gL-1) as carbon source and also investigated the effects of dilution (50% and 75%, with water) and illumination (1,800 lux and 3,000 lux) using a 23 factorial design. The maximum celular concentration of 5.38 gL-1 and maximum specific growth rate of 0.0063 h-1 were obtained with a glucose concentration of 0.5 gL-1, 50% dilution and 1800 lux of illuminance.
Index terms: Biomass, glucose, illuminance, mixotrophic, Spirulina platensis.
INTRODUÇÃO
A busca de alternativas alimentares que possam diminuir o déficit nutricional existente em uma parcela significativa da população, a um custo acessível, envolvem a pesquisa de novos processos e matérias-primas. Por outro lado, pesquisas inovadoras envolvendo a biotecnologia, por meio da utilização de microrganismos ou enzimas para a produção de novos produtos, inclusive alimentos, estão revolucionando a sociedade moderna.
A aplicação da biotecnologia moderna na melhoria de qualidade de vida e bem-estar da sociedade, tem ganhado destaque, uma vez que a preocupação com a saúde é um dos pontos fortes da época atual. A busca por produtos mais saudáveis é constante, o que fez com que surgissem os alimentos funcionais e nutracêuticos, que além de possibilitarem uma alimentação adequada, contribuem também para a prevenção e o tratamento de doenças.
A utilização de microalgas na alimentação humana ocorre há séculos, tendo sido usadas como fonte de proteínas por tribos indígenas do Chad e pelos Astecas, que as secavam em lamelas para serem ingeridas (NAVALHO, 1998). Quando cultivadas em meios adequados, certas espécies de microalgas podem duplicar a sua biomassa diariamente, produzindo matéria seca com teor protéico superior a 50% e alcançando produtividades de 30 a 50 g.m-2.dia-1 em peso seco (GOLDMAN, 1980). Esta característica, aliada à simplicidade nas técnicas de cultivo, torna as microalgas um dos objetos de pesquisa prioritários das mais modernas áreas de investigação (BENEMANN et al., 1987).
A microalga Spirulina platensis pode sofrer variações no crescimento de acordo com o meio de cultivo utilizado e as condições do meio externo. A manipulação das condições de cultivo pode estimular a biossíntese de compostos e, além disso, podem-se controlar estas variáveis, a fim de diminuir os custos do processo de produção. A diluição do meio Zarrouk (padrão para o cultivo da microalga Spirulina) torna-se uma alternativa a ser analisada, uma vez que a alta concentração de sais do meio aumenta os custos de produção. Estudos anteriores demonstraram que maiores produtividades podem ser obtidas nos cultivos com o meio Zarrouk diluído (REINEHR, 2003). O estudo de nutrientes para o cultivo da microalga Spirulina platensis justifica-se pelo fato de que os meios utilizados para o cultivo em grande escala ainda são muito onerosos. O estudo de fontes de carbono orgânicas, como a glicose, que possam ser utilizadas no metabolismo da microalga, é de fundamental importância. O processo em batelada alimentada consiste da adição intermitente de um substrato limitante ao longo da fermentação. Este sistema permite um aumento no período produtivo do processo e evita os efeitos tóxicos das elevadas concentrações iniciais de substrato, como ocorre nos processos descontínuos simples.
Objetivou-se estudar o cultivo mixotrófico da microalga Spirulina platensis em modo batelada alimentada, tendo-se como variáveis a concentração de glicose adicionada, a iluminância e a diluição do meio Zarrouk.
MATERIAL E MÉTODOS
Microrganismo e meio de cultivo
Foi utilizada a microalga Spirulina platensis paracas. Para a manutenção do inóculo foi utilizado o meio Zarrouk (ZARROUK, 1966), cuja composição foi (gL-1): NaHCO3 16,8; K2HPO4 0,5; NaNO3 2,5; K2SO4 1,0; NaCl 1,0; MgSO4.7H2O 0,2; CaCl2 0,04; EDTA 0,08 e 1,0 mL.L-1 das soluções A5 e B6. Solução A5 (gL-1): H3BO3 2,86; MnCl2.4H2O 1,81; ZnSO4.7H2O 0,222; CuCO4.5H2O 0,079; MnO3 0,015. Solução B6 (gL-1): NH4VO3 22,86; KCr(SO4)2.12H2O 192; NiSO4.6H2O 44,8; Na2WO4.2H2O 17,94; TiSO4.H2SO4.8H 2O 61,1; CO(NO3)2.6H2O 43,98.
Para o cultivo da microalga foi utilizado o meio Zarrouk diluído com água destilada estéril e adicionado de glicose como fonte de carbono adicional segundo o Planejamento Fatorial Completo 23.
Condições de cultivo e biorreatores
Os cultivos foram realizados em frascos erlenmeyers de 2 L, com um volume inicial de 1,8 L de meio e concentração inicial de inóculo de 0,1 gL-1. A aeração foi realizada por meio de bombas de diafragma com fluxo de ar de 0,02 VVM (volume de ar/volume de meio/minuto). A iluminação foi realizada com a utilização de lâmpadas fluorescentes fornecendo uma iluminância de 1800 lux ou 3000 lux, segundo o Planejamento Fatorial Completo 23. O aparato foi mantido em uma estufa termostatizada não-estéril, com fotoperíodo de 12 h claro/escuro e 30ºC (Costa et al., 2004).
Planejamento experimental
Os experimentos foram realizados segundo um Planejamento Fatorial Completo 23 (PFC), cujas variáveis reais e codificadas estão apresentadas na Tabela 1. A iluminância variou entre 1800 lux e 3000 lux e a diluição do meio Zarrouk, com água destilada estéril, foi de 50% (50% de água destilada estéril e 50% de meio Zarrouk) ou 75% (75% de água e 25% de meio Zarrouk).
A glicose foi adicionada aos cultivos em modo batelada alimentada pela adição de pequenos volumes de uma solução de glicose concentrada (180 gL-1), no tempo inicial em concentrações de 0,5 gL-1 ou 1,0 gL-1 e posteriormente sempre que a concentração de glicose no meio de cultivo fosse próxima a zero gL-1.
Determinações analíticas
A concentração celular da microalga S. platensis e o consumo de glicose pela mesma foram determinados por meio de amostragens nos cultivos a cada 24 h. A concentração celular foi determinada por uma correlação pré-determinada (curva-padrão) entre o peso seco da biomassa e a absorbância a 670 nm. O consumo de glicose pelo microrganismo foi determinado pela quantificação de açúcares pelo método 3,5 DNS.
Análise dos resultados
Curvas de concentração celular versus tempo foram construídas, a partir das quais foram obtidas a concentração celular máxima (Xmax) e a velocidade específica máxima de crescimento (µmax) para cada experimento. A µmax foi calculada a partir da integração da Equação 1, por regressão exponencial dos dados de concentração celular versus tempo na fase logarítmica de crescimento, resultando na Equação 2.
A glicose foi adicionada aos cultivos em modo batelada alimentada pela adição de pequenos volumes de uma solução de glicose concentrada (180 gL-1), no tempo inicial em concentrações de 0,5 gL-1 ou 1,0 gL-1 e posteriormente sempre que a concentração de glicose no meio de cultivo fosse próxima a zero gL-1.
Determinações analíticas
A concentração celular da microalga S. platensis e o consumo de glicose pela mesma foram determinados por meio de amostragens nos cultivos a cada 24 h. A concentração celular foi determinada por uma correlação pré-determinada (curva-padrão) entre o peso seco da biomassa e a absorbância a 670 nm. O consumo de glicose pelo microrganismo foi determinado pela quantificação de açúcares pelo método 3,5 DNS.
Análise dos resultados
Curvas de concentração celular versus tempo foram construídas, a partir das quais foram obtidas a concentração celular máxima (Xmax) e a velocidade específica máxima de crescimento (µmax) para cada experimento. A µmax foi calculada a partir da integração da Equação 1, por regressão exponencial dos dados de concentração celular versus tempo na fase logarítmica de crescimento, resultando na Equação 2.
Em que:
µ: velocidade específica de crescimento (h-1)
µmax: velocidade específica máxima de crescimento (h-1)
Xi = concentração celular (gL-1)
t = tempo(h)
Os resultados de Xmáx e µmáx obtidos foram analisados mediante Análise de Variância.
RESULTADOS E DISCUSSÕES
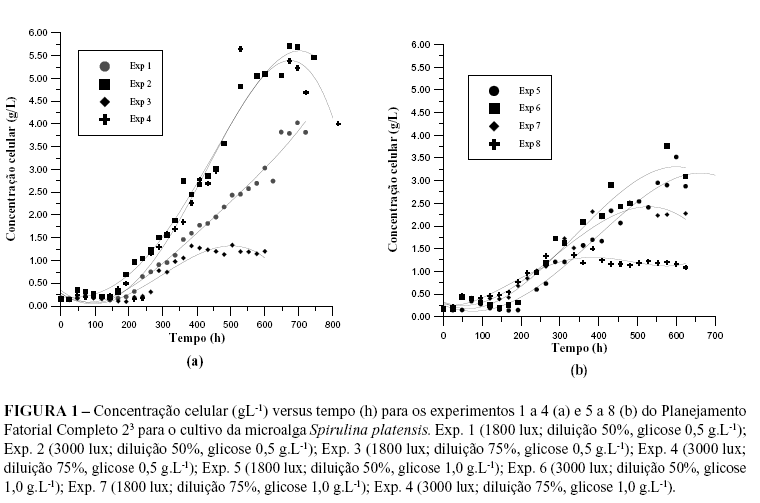
As curvas de concentração celular versus tempo para os experimentos 1 a 8 do PFC 23 do cultivo da microalga S. platensis estão apresentadas na Figura 1.Os experimentos 1, 2 e 4 apresentaram elevadas concentrações celulares, de 4,02 gL-1 a 5,38 gL-1, sendo que o experimento 3 apresentou concentração de biomassa de 1,28 gL-1. Nestes experimentos a adição de glicose em modo batelada alimentada foi realizada no nível inferior do planejamento, ou seja, 0,5 gL1. Os experimentos 5 a 8 (Figura 1b), nos quais adicionou-se 1,0 gL1 de glicose, apresentaram menores concentrações de biomassa (1,50 gL-1 a 3,18 gL1) que os experimentos 1, 2 e 4. Desta forma, maiores concentrações de biomassa foram obtidas com a adição de glicose no nível inferior (0,5 gL1).
Os resultados de µmax e Xmax para cada experimento do PFC 23 estão apresentados na Tabela 2.
As concentrações celulares obtidas nas melhores condições do Planejamento Fatorial 23, da ordem de 5 gL-1, são compatíveis com outros estudos de cultivo com adição de glicose em batelada alimentada, sendo estas concentrações superiores às obtidas nos cultivos descontínuos, em que obtém-se concentrações da ordem de 0,5 gL-1 a 1,5 gL-1. Chen & Zhang (1997) obtiveram concentrações de biomassa de 10,24 gL-1, portanto, 5,1 vezes maiores que nos cultivos fotoautotróficos em batelada simples.
Avaliando-se os resultados de concentração máxima dos experimentos com 0,5 gL1 de glicose em função da iluminância, verifica-se que maiores Xmax, de 5,35 e 5,38 gL1, foram obtidas para os experimentos 2 e 4, em intensidade luminosa de 3000 lux (Tabela 1). Os experimentos nos quais utilizou-se iluminância de 1800 lux (Exp. 1 e 3), apresentaram concentrações celulares de 4,02 gL-1 e 1,28 gL-1, respectivamente. Os experimentos com 1,0 gL-1 de glicose não apresentaram uma tendência quanto à influência da iluminância nas concentrações máximas de biomassa, uma vez que, tanto a maior quanto a menor concentração celular (3,09 gL1, experimento 6; 1,50 gL-1, experimento 8) foram obtidas a 3000 lux. O cultivo a 3000 lux, associado à adição de 1,0 gL1 de glicose, pode resultar em menores produtividades devido estas condições constituírem juntas uma condição de estresse. Isto pode ser explicado devido ao fato de que em altas intensidades luminosas a respiração aeróbia nas células é reduzida, sendo inibida a utilização da glicose pelas células; enquanto que, a baixas intensidades luminosas, a respiração torna-se mais importante requerendo altas concentrações de glicose para manter as demandas do crescimento (ZHANG et al., 1999).
O estudo do cultivo mixotrófico (utilização de fontes orgânicas de carbono associadas a fixação do carbono inorgânico na fotossíntese) da Spirulina platensis tem sido realizado por diferentes pesquisadores, entre eles Zhang et al. (1999), os quais demonstraram, em estudo da influência da concentração inicial de glicose sobre a velocidade específica de crescimento em cultivo descontínuo, que a µmax aumenta até concentrações iniciais de glicose de 2 gL-1. Neste mesmo estudo foi observado que para intensidades luminosas variando entre 500 e 2000 lux, a µmax aumenta conforme aumenta a luminosidade, enquanto que entre 2000 e 4000 lux, a µmax mantém-se constante com o aumento da luminosidade. Foram obtidas concentrações celulares de 2,67 gL-1 com adição de 2 gL-1 de glicose e iluminância de 4000 lux, enquanto que, com concentração 5 gL-1 de glicose e 2000 lux de iluminância, a concentração de biomassa foi de 2,47 gL-1.
As concentrações celulares obtidas mostraram-se independentes da diluição do meio utilizada quando a concentração de glicose adicionada no meio de cultivo foi de 0,5 gL1, uma vez que os maiores valores de Cmax, de 5,35 gL1 e 5,38 gL1, foram obtidos nas duas diluições testadas (50% e 75%), para o experimento 2 (1800 lux, diluição de 50% e 0,5 gL1 de glicose) e para o experimento 4 (3000 lux, diluição de 75% e 0,5 gL1 de glicose). Quando a concentração de glicose adicionada foi de 1,0 gL-1 (experimentos 5 a 8), as maiores concentrações de biomassa de 3,18 gL-1 e 3,09 gL-1, foram obtidas com diluição do meio de 50% (experimentos 5 e 6). Nos experimentos com diluição do meio de 75% (experimentos 7 e 8), os resultados de concentração celular foram inferiores, respectivamente de 2,51 gL-1 e 1,50 gL-1. Reinehr (2001) obteve melhores resultados na produtividade da microalga Spirulina platensis cultivada em biorreator aberto operando em modo semicontínuo com meio Zarrouk a 20%, concluindo que a produtividade obtida com o meio Zarroukpuro foi inferior (37,7 mgL-1.d-1) à produtividade obtida com meio Zarroukdiluído (46,2 mg L-1.d-1). Isto pode significar que o meio sintético usualmente utilizado para o cultivo da microalga Spirulina, proposto por Zarrouk (1966), tem concentrações de sais superestimadas para o modo semicontínuo, em que há alimentação periódica de nutrientes, o que vem ao encontro com os resultados obtidos no presente trabalho, no qual se obteve maiores concentrações de biomassa no meio diluído a 75% e com adição de glicose na concentração de 0,5 gL-1.
Os maiores valores de µmax, de 0,0138 h-1 e 0,0097 h-1, foram obtidos para os experimentos que apresentaram os menores valores de Xmax, de 1,28 gL-1 e 1,50 gL-1, respectivamente. Isto se justifica pelo fato de que, embora esses experimentos tenham apresentado valores elevados de velocidade específica máxima (µmáx), nestes as fases exponenciais foram muito curtas, de 150 h e 200 h, respectivamente. De acordo com Vonshak et al. (1982), quando a iluminância for fator limitante no crescimento, a velocidade específica é inversamente proporcional à concentração de biomassa, o que está de acordo com os resultados obtidos neste trabalho. Excluindo-se estes casos, os quais apresentaram comportamentos diferenciados, verifica-se que as maiores µmax foram obtidas para a alimentação de glicose de 0,5 gL-1.
Quanto à influência da diluição do meio sobre a µmax, observa-se que nos experimentos com 0,5 gL-1 de glicose, os melhores resultados (0,0063 h-1 e 0,0138 h-1) foram obtidos com a maior diluição do meio Zarrouk (75%) e iluminância de 3000 lux.
Analisando-se os experimentos com adição de glicose de 1,0 gL-1, verificou-se que a menor µmax (0,0028 h-1) foi obtida nas condições de 1800 lux de iluminância e diluição do meio de 50%. O melhor resultado de µmax dentre esses experimentos, de 0,0097 h-1 foi obtido nas condições de 3000 lux de iluminância e diluição do meio de 75%. Na condição de diluição do meio de 50% e iluminância de 3000 lux (experimento 6) a µmax foi de 0,0048 h-1. Já para a iluminância de 1800 lux e 75% de diluição do meio (experimento 7) a µmax foi de 0,0041 h-1.
A análise estatística dos resultados de µmáx e Xmáx demonstrou que os fatores iluminância, diluição do meio e concentração de glicose adicionada em modo batelada alimentada foram significantes (p<0,001) para as duas respostas (µmáx e Xmax). Como a interação dos três fatores também foi significativa (p<0,001), esta foi analisada em detrimento da influência isolada de cada fator.
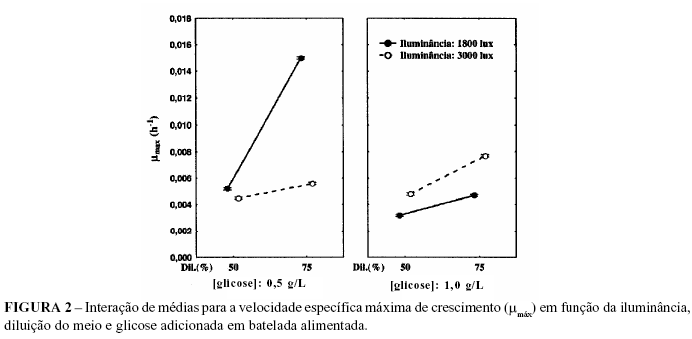
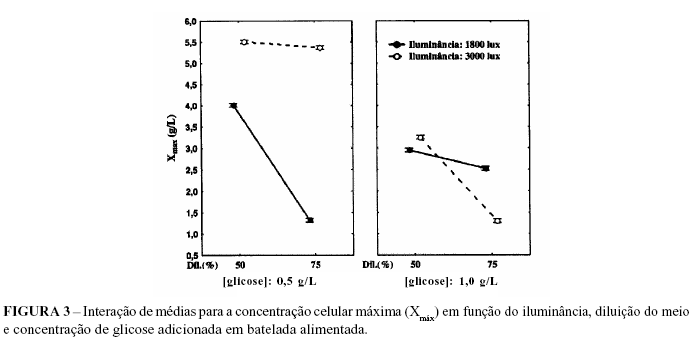
Nas Figuras 2 e 3 apresentam-se as interações de médias dos fatores iluminância, diluição do meio e concentração de glicose adicionada em batelada alimentada sobre as respostas µmax e Xmax, respectivamente.
As maiores µmax foram obtidas a 1800 lux quando a concentração de glicose no meio de cultivo era 0,5 gL-1, enquanto que para adição de 1,0 gL-1 de glicose, as maiores µmax foram obtidas a 3000 lux. Com relação à interação dos fatores sobre a Xmax (Figura 3), para 0,5 gL-1 de glicose, independente da diluição do meio utilizada, maiores concentrações de biomassa foram obtidas a 3000 lux. Para a adição de 1,0 gL-1 de glicose, maiores concentrações de biomassa foram obtidas na diluição de 50% do meio, independente de luminosidade.
CONCLUSÃO
A maior concentração de biomassa (5,38 gL-1) foi obtida com a adição de 0,5 gL-1 glicose ao meio de cultivo, em modo batelada alimentada, iluminância de 3000 lux e diluição de 75% do meio Zarrouk.
As concentrações celulares da microalga Spirulina podem ser aumentadas pelo uso de glicose como fonte de carbono, desde que adicionada em baixas concentrações no meio de cultivo, demonstrando a capacidade metabólica dessa microalga de converter fontes orgânicas de carbono em biomassa. O estudo de outras fontes orgânicas de carbono para a produção de Spirulina, aliado à diluição do meio Zarrouk, possibilita o cultivo da microalga com menores custos e maiores produtividades.
(Recebido para publicação em 3 de junho de 2005 e aprovado em 16 de setembro de 2005)
- BENEMANN, J. R.; TILLETT, D. M.; WEISSMAN, J. C. Microalgae biotechnology. Trends in Biotechnology, Amsterdam, v. 5, p. 47-53, 1987.
- CHEN, F.; ZHANG, Y. High cell density mixotrophic culture of Spirulina platensis on glucose for phycocyanin production using a fed-batch system. Enzime and Microbial Technology, [S.l.], v. 20, p. 221-224, 1997.
- COSTA, J. A. V.; COLLA, L. M.; DUARTE, P. Improving Spirulina platensis biomass yield using a fed-batch process. Bioresource Technology, Essex, v. 92, p. 237-241, 2004.
- GOLDMAN, J. C. Outdoor algal mass cultures: II. photosynthetic yield limitations. Algaes Biomass, [S.l.], v. 11, p. 119-135, 1980.
- NAVALHO, J. Biotecnologia de Dunaliella salina para a produção de beta-caroteno 1998. 112 f. Dissertação (Mestrado em Aquacultura) - Universidade do Algarve, Algarve, 1998.
- REINEHR, C. O. Estudo do cultivo semicontínuo de microalga Spirulina platensis utilizando água da lagoa Mangueira 2001. 132 f. Dissertação (Mestrado em Ciência e Engenharia de Alimentos) Universidade Federal do Rio Grande, Rio Grande, 2001.
- VONSHAK, A.; BOUSSIBA, S.; ABELIOVICH, A. Production of Spirulina biomass: maintenance of monoalgal culture outdoors. Biotechnology and Bioengineering, New York, v. 25, p. 341-349, 1982.
- ZARROUK, C. Contribuition à I'étude d'une Cyanophycée: influence de divers facteurs physiques et chimiques sur la croissance et la photosynthèse de spirulina máxima. 1966. Thesis (Ph.D) - Université Des Paris, Paris, 1966.
- ZHANG, X. W.; ZHANG, Y. M.; CHEN, F. Application of mathematical models to the determination optimal glucose concentration and light intensity for mixotrophic culture of Spirulina platensis Process Biochemistry, [S.l.], v. 34, p. 477-481, 1999.
Datas de Publicação
-
Publicação nesta coleção
18 Ago 2008 -
Data do Fascículo
Dez 2005
Histórico
-
Aceito
16 Set 2005 -
Recebido
03 Jun 2005