Resumos
Os autores tecem considerações sobre a estrutura e funções normais das glândulas paratireóides como introdução à patologia e as repercussões clinico - patológicas tanto do excesso como da redução do paratormônio. Maior ênfase é dedicada ao hiperparatireoidismo primário quanto às causas, a fisiopatologia das alterações, os aspectos anatomopatológicos macro e microscópicos das lesões e sua patogenia, na "Osteite fibrocistica" ou "doença de von Recklinghausen dos ossos" com a correlação aos aspectos radiográficos. Apresentam caso de paciente, cuja história clinica demonstra as dificuldades encontradas para o diagnóstico da doença. Referem-se ainda às alterações e patogenia das formas de hiperparatireoidismo secundário e terciário e ao hipoparatireoidismo.
Hiperparatireoidismo primário; Adenoma; Hiperplasia; Osteite fibrosa cistica; Doença de Von Recklinghausen
The authors present a summary on the normal anatomy and function of the parathyroid glands as well as a brief review of clinical and pathological repercussions of higher and lower parathyroid hormone production. The emphasis is given on the causes, physiopathology, anatomy, macroscopy and microscopy of the lesions and their role in the genesis of fibrocystic osteitis, also known as Von Recklinhausen disease of the bones. Radiological correlation is also given. The authors show the challenges for the diagnosis in the same cases. We also write about secondary and tertiary hyperparathyroidism, as well as hypoparathyroidism.
Hyperparathyroidism primary; Adenoma; Hyperplasia; Cystic fibrous osteitis; Von Recklinghausen Disease
ARTIGO DE REVISÃO
Paratireóides: estrutura, funções e patologia
José Donato de Prospero; Pedro Pericles Ribeiro Baptista; Maria Fernanda Carriel Amary; Priscila Pizzo Crêm dos Santos
Departamento de Ciências Patológicas e Departamento de Ortopedia e Traumatologia da Faculdade de Ciências Médicas da Santa Casa de São Paulo
Endereço para correspondência Endereço para correspondência: Rua Itacolomi, 423, apt11 CEP 01239-020, Higienópolis São Paulo, SP, Brasil E-mail; pripizzo@hotmail.com
RESUMO
Os autores tecem considerações sobre a estrutura e funções normais das glândulas paratireóides como introdução à patologia e as repercussões clinico - patológicas tanto do excesso como da redução do paratormônio. Maior ênfase é dedicada ao hiperparatireoidismo primário quanto às causas, a fisiopatologia das alterações, os aspectos anatomopatológicos macro e microscópicos das lesões e sua patogenia, na "Osteite fibrocistica" ou "doença de von Recklinghausen dos ossos" com a correlação aos aspectos radiográficos. Apresentam caso de paciente, cuja história clinica demonstra as dificuldades encontradas para o diagnóstico da doença. Referem-se ainda às alterações e patogenia das formas de hiperparatireoidismo secundário e terciário e ao hipoparatireoidismo.
Descritores: Hiperparatireoidismo primário. Adenoma. Hiperplasia. Osteite fibrosa cistica. Doença de Von Recklinghausen.
INTRODUÇÃO
A paratireóide se apresenta sob a forma de quatro nódulos originários dos terceiro e quarto arcos branquiais, dois no ápice dos lobos direito e esquerdo da tireóide e os demais nos pólos inferiores. São comuns as variações de topografia, pois às vezes situam-se junto à laringe sem relação com a tireóide, podendo ser encontradas até no mediastino, junto do timo.1 Cada glândula têm crescimento progressivo até a terceira década da vida, atingindo peso médio de 0,45g no sexo masculino e 0.5g no feminino, com maior eixo de 5mm.
Microscopicamente são constituídas por células principais, células claras e células oxífilas. As "principais" são arredondadas com citoplasma homogêneo levemente acidófilo, produtoras de paratormônio. Quando é menor a secreção ou quando estão em estádio de "repouso", acumulam-se grânulos citoplasmáticos de lipídios e de glicogênio, assumindo caracteres das chamadas "células claras".2 As células "oxifilas" são maiores com citoplasma acidófilo por sua afinidade pela eosina e aparecem na puberdade, aumentando progressivamente em número com o avançar da idade, não secretam paratormônio e têm função ainda obscura.1-3 Todas as células dispõem-se em arranjo cordonal, entremeadas por lóbulos de tecido gorduroso.
O paratormônio é uma proteína com 8500 D de peso molecular4, constituída por cadeia simples de polipeptídio com 84 aminoácidos. É antagônico da calcitonina produzida pelas células C, parafoliculares, da tireóide. Age diretamente nas células dos túbulos renais inibindo a reabsorção de fosfatos e regulando a fosfatúria. Nos ossos age nos osteoclastos que, por ação enzimática, reabsorvem a matriz e solubilizam o cálcio. O paratormônio, portanto, tem função primordial no "turnover" ósseo, isto é, no equilíbrio entre aposição e reabsorção, na manutenção do cálcio sérico em tomo de 8,9 a 10 mg/% e na absorção de cálcio no intestino. O cálcio e o fósforo mantêm proporção de 2:1, desde os cristais de hidroxiapatita (fosfato tricálcico), até a fórmula sanguínea que, em valores normais, corresponde a 9mg/% de cálcio e 4mg/% de fósforo, cujo produto em condições normais é de 36 no adulto e 40 na criança. Perante alterações dos níveis séricos de cálcio ou fósforo, sob ação do paratormônio, haverá retirada de variável quantidade de minerais dos ossos, a fim de adequada manutenção do balanço Ca/P.
As alterações decorrentes da falta ou excesso de cada um dos fatores que agem na aposição e na reabsorção óssea determinam as chamadas doenças metabólicas dos ossos que são a osteoporose, o raquitismo na infância e a osteomalacia no adulto e o hiperparatireoidismo.
PATOLOGIA
HIPERPARATIREOIDISMO
É o resultado da hipersecreção persistente do paratormônio podendo ser primário, secundário e terciário.
PRIMÁRIO
A causa principal é o Adenoma da Paratireóide, secundado pela Hiperplasia Primária e pelo Carcinoma. O primeiro relato sobre tumores da paratireóide deve-se a Askanazy5 ao autopsiar um caso de osteíte fibrocistica. Albright e Reifenstein6 descreveram a hiperplasia de células claras da paratireóide e deve-se a Hall e Chaffin7 a primeira descrição do carcinoma da paratireóide. Castleman e Mallory8 descreveram alterações da glândula em 25 casos de hiperparatireoidismo e Pappenheimer e Wilnes9 descreveram a hiperplasia secundária em doenças renais.
ADENOMA
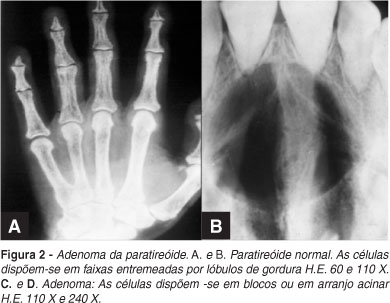
É a principal causa de hiperparatireoidismo primário, presente em cerca de 90% dos casos da forma primária. É mais freqüente em adultos, em geral acima de 50 anos e no sexo feminino, na proporção de 2:1. Caracteriza-se por proliferação predominante das células principais formando nódulo tumoral em geral solitário, raramente em mais de uma glândula.1 (Figura 1) A freqüência de comprometimento de duas glândulas é de 6%5. Tem pequenas proporções, com peso máximo de 10g e 1 a 3cm de diâmetro, bem delimitado por faixa de tecido conjuntivo da cápsula do órgão. Ao corte, é homogêneo, de cor rósea e consistência mole (Figura 1A). Segundo alguns autores, o peso do adenoma é proporcional à intensidade do hiperparatireoidismo e das alterações ósseas, podendo atingir 50g ou mais.10
Histologicamente é constituído por células principais, entremeadas por variável quantidade de células claras que substituem a estrutura da glândula que perde seu clássico arranjo cordonal, pois as células dispõem-se em pequenos blocos ou em arranjo acinar, entremeados por estroma conjuntivo frouxo com rica vascularização capilar.8,11 O tecido gorduroso, normal, é escasso ou inexistente (Figuras 1B,C). O adenoma de células oxífilas é raro e não tem repercussões endócrinas.3
A doença é inicialmente assintomática e pode ser casualmente evidenciada em exames laboratoriais de rotina.12 A evolução clinica é lenta e progressiva, com manifestações variadas, desde náuseas e diarréias, úlceras gastro-intestinais, cálculos urinários ou biliares de repetição, fratura óssea sem causa aparente ou por traumatismo leve, até alterações psíquicas, acompanhadas de fadiga e fraqueza neuro-muscular.13 Estas alterações dependem do tempo de evolução, podendo persistir por meses e anos sem diagnostico e sem tratamento. O diagnóstico deve ser o mais precoce possível, pois em estádios muito avançados, com graves lesões ósseas, pode tomar-se irreversível e mortal por insuficiência renal.
Na suspeita de hiperparatireoidismo, exames de laboratório devem ser realizados. O primeiro sinal bioquímico é hiperfosfatúria, pela ação do paratormônio nos túbulos renais, inibindo a reabsorção de fósforo. Para a manutenção do produto cálcio / fósforo no sangue em torno de 36 no adulto, haverá aumento da reabsorção óssea, que se traduz por hipercalcemia, para 10 ou mais mg/%. Em virtude da hiperfosfatúria haverá hipofofatemia de 3mg/% ou menos. A dosagem elevada de paratormônio no sangue confirmará a doença.
As alterações radiográficas iniciais residem nas falanges das mãos, sob a forma de focos de reabsorção subperiostais e na "lâmina dura" de implantação dos dentes, onde também existem focos de reabsorção.
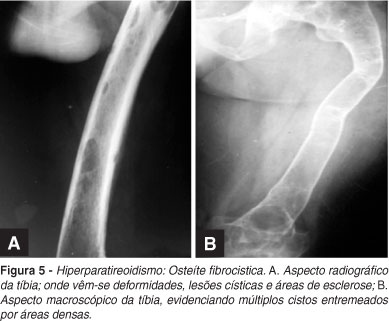
Com a progressão da doença as alterações ósseas serão cada vez mais pronunciadas, até atingir estádios mais graves. Os focos de reabsorção subperiostais passam a comprometer ossos longos (Figuras 2A,B; 3A ) e aparecem lesões císticas de tamanhos variados. (Figuras 4A,B) Os ossos serão cada vez mais frágeis, amolecidos, e apresentarão fraturas de gravidade cada vez maior. (Figuras 5A,B) Os cistos, solitários ou múltiplos, tornam-se bem evidentes nas radiografias (Figura 4A) e ao exame macroscópico dos ossos. (Figura 4B) Em virtude da intensidade da reabsorção, aparecem áreas hemorrágicas que assumem aspecto radiográfico de ''tumores'', epifisários ou metafisários (Figura 6), "tumor marrom".
Microscopicamente os ossos apresentam redução da espessura das traves - osteoporose - e da mineralização - osteomalacia - em meio à proliferação fibrosa. (Figura 7A) Nas bordas das traves ósseas são numerosas as lacunas de reabsorção, com variável número de osteoclastos, às vezes sob a forma de "frentes de reabsorção". (Figura 7B)14 As lesões, que ao exame radiográfico comportam-se como "tumor marrom", são conseqüência de focos hemorrágicos que após a desintegração das hemácias, surgirão acúmulos de hemossiderina permeados por numerosas células gigantes multinucleadas com caracteres de osteoclastos (Figura 6B), que correspondem ao ''tumor marrom do hiperparatireoidismo" e é pseudo-neoplásica. Tanto ao exame radiográfico quanto anátomo patológico assemelha-se ao verdadeiro tumor gigantocelular cujo diagnóstico diferencial em biópsias nem sempre é fácil. A possibilidade de erro deve estar presente e se ocorrer, poderá levar a conduta terapêutica desastrosa para o paciente.12
As alterações radiográficas e anátomo patológicas constituem o quadro da Osteite Fibrocistica generalizada ou doença de von Recklinghausen dos ossos.
Progressivamente as alterações renais, tanto clinica como anátomo patológicas, serão cada vez mais intensas e podem ser mortais, pela nefrocalcinose e consequente insuficiência renal. (Figura 8)
Em virtude da variedade de manifestações clínicas, laboratoriais, radiográficas e anátomo patológicas, afirmamos que o hiperparatireoidismo primário é doença que deve ser conhecida e reconhecida pelos médicos em geral, independentemente de sua especialidade, para que atentem ao fato de que se trata de doença benigna que, se diagnosticada em estádios iniciais, é perfeitamente curável. Deixa de sê-lo quando as lesões ósseas e renais tornam-se irreversíveis, podendo levar o paciente à morte.
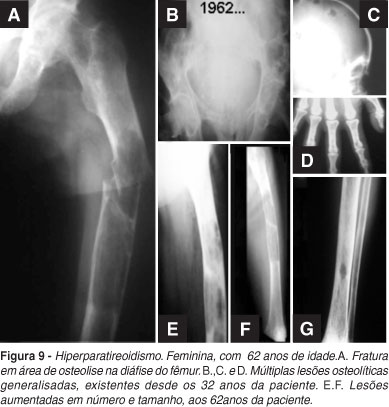
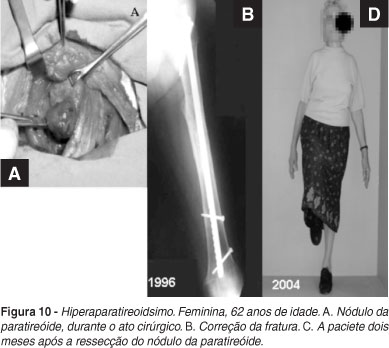
Exemplo significativo de diagnóstico tardio desta entidade é o caso documentado nas figuras 9 e 10. Trata-se de paciente do sexo feminino com 60 anos que sofreu fratura espontânea do fêmur, ao movimentar-se no leito. Os exames radiográficos evidenciaram lesão osteolítica na diáfise femoral. Entretanto, a análise de estudo de imagens anteriores à esta fratura, realizadas desde 1962, já evidenciavam outras lesões, também líticas, nos ossos da bacia, crânio, perna e mãos. No fêmur existiam outras lesões, documentadas por sucessivos exames radiográficos, além da região fraturada. Fizeram naquela época e mantiveram durante todos estes anos, a presunção de diagnóstico clinico e radiográfico de metástases generalizadas de carcinoma. Muitos outros exames clínicos e laboratoriais foram feitos durante todos estes anos, mas as essenciais dosagens de cálcio e fósforo não o foram. A doença evoluiu com progressão das lesões no esqueleto. Em 1992, trinta anos depois, foi por nós examinada e solicitadas as dosagens de cálcio, fósforo e fosfatase alcalina que estavam exageradamente alteradas, assim como o paratormônio. A paciente foi submetida à ressecção do nódulo da paratireóide e a fixação do fêmur, cuja fratura consolidou-se em dois meses com regressão das demais lesões, tamanha era a avidez de cálcio, que o tecido ósseo apresentava. Durante algum tempo foi necessária reposição endovenosa de cálcio, com melhoria geral da paciente. (Figura 10)
Fisiopatologia: o tecido ósseo não tem crescimento intersticial. Cresce à custa de aposição de nova matriz sobre a pré-existente, por atividade osteoblástica que elabora a matriz. Estas células são idênticas aos fibroblastos que elaboram fibras colágenas nos tecidos moles. Nos ossos, o colágeno da matriz tem a capacidade de mineralizar pela deposição de cristais de hidroxiapatita que, em condições normais não ocorre nos demais tecidos. A reabsorção da matriz é realizada pelos osteoclastos, sincícios que se formam na medula óssea e têm caracteres de célula gigante multinucleada. Os osteoclastos agem sob estímulo direto do paratormônio e de agentes locais como o fator alfa (TGF alfa), fator de necrose tumoral e interleucinas.15 A matriz óssea é constituída em cerca de 95% por fibras colágenas. Os demais 5% estão nas linhas de cimento, ou reversas, que marcam as faixas de aposição em relação às pré-existentes, constituídas por glicosaminoglicanos (ácidos hialurônico e condroitinsulfúrico). Diversos fatores contribuem para a formação e manutenção da matriz, principalmente alimentação protéica adequada, vitaminas A e C, estímulos hormonais da hipófise, tireóide, supra-renais, gônadas e atividade muscular que é imprescindível para a atividade osteoblástica. A mineralização da matriz depende de fatores alimentares como aporte de cálcio e vitamina D, raios solares e normalidade do intestino para absorção do cálcio, também sob ação do paratormônio.
O "turnover" ósseo, aposição e reabsorção, persiste durante toda a vida. Intenso na vida intra-uterina e na primeira década, progressivamente menor com o avançar da idade, mas sempre presente até a velhice. O esqueleto é importante fator da homeostase metabólica das proteínas e dos minerais em nosso organismo.12
O excesso de paratormônio provocará desequilíbrio na manutenção óssea, agindo sobre os osteoclastos que, através de enzimas (hialuronidade e colagenase), absorvem a matriz e solubilizam o cálcio.
O tratamento consiste em remoção cirúrgica da paratireóide com o adenoma. Por tratar-se de doença de curso lento que pode perdurar durante anos, a remoção cirúrgica da paratireóide poderá curar definitivamente o paciente com regressão das alterações. Se as repercussões ósseas e as alterações renais pela nefrocalcinose forem muito graves o paciente poderá falecer. (Figura 8)
HIPERPLASIA
Trata-se de aumento numérico das células de uma ou mais paratireóides; raramente das quatro e é a segunda causa de hiperparatireoidismo primário, com freqüência em torno de 7% dos casos13, de etiologia desconhecida. Na maioria dos casos a proliferação é de células principais, com variável quantidade de células claras e oxífilas. Nos estádios iniciais as células dispõem-se em ilhotas, que progressivamente substituem a glândula em cordões ou em arranjo acinar com aumento de tamanho e peso. O diagnóstico diferencial histológico com adenoma, ao exame de apenas de uma glândula, é particularmente difícil, se não indistinguível, principalmente se o exame for por biópsia em congelação durante o ato cirúrgico.
Não raramente, a hiperplasia primária da paratireóide faz parte do quadro de tumores endócrinos mú1tiplos do tipo I, quando associados a tumor de ilhotas de Langerhans do pâncreas e a tumor da hipófise e do tipo II, quando associado a carcinoma medular da tireóide e ao feocromocitoma da medular da glândula supra-renal.13
CARCINOMA
É causa de hiperparatireoidismo primário em cerca de 2,9% de casos.13 Os critérios para diagnóstico microscópico de carcinoma da paratireóide devem ser bem avaliados pelo anatomopatologista. Somente o desarranjo e o polimorfismo celular e nuclear, com mitoses não são elementos absolutos para o diagnóstico. A invasão da cápsula do órgão e o encontro de mitoses atípicas que caracterizam a anaplasia, além da identificação de células neoplásicas na luz de vasos sanguíneos e/ou linfáticos13 contribuem para o diagnóstico. Estes critérios por vezes não são suficientes para diferenciação do adenoma, que em alguns casos apresentam acentuado polimorfismo celular que induz a falso diagnóstico de carcinoma. Certos casos cujo diagnóstico é de adenoma, somente passaram a ser interpretados como carcinoma após a evolução do paciente com metástases para os pulmões.
SECUNDÁRIO
A hipersecreção de hormônio é considerada secundária quando decorre de estímulos extra glandulares, principalmente relacionados a menor concentração sanguínea de íons cálcio, de modo a provocar proliferação das células da paratireóide a fim de, com maior quantidade de hormônio circulante, retirar dos ossos a quantidade de mineral para manutenção do balanço cálcio fósforo no sangue.
Doenças renais crônicas são as principais causas destas alterações metabólicas, pois o defeito na filtração glomerular determina decréscimo na conversão da 25-hidroxicalciferol em 1,25 - diidroxi-colecalciferol, forma ativa da vitamina D. A redução desta vitamina levará a menor absorção intestinal de cálcio, resultando maior estímulo da paratireóide, efeito que se agrava pela elevação do fósforo sanguíneo retido.
As alterações ósseas decorrentes desta disfunção metabólica são designadas "osteodistrofia renal" (raquitismo renal) onde o excesso de paratormônio induziria dupla ação nos ossos, acelerando a reabsorção com maior atividade dos osteoclastos e formação de novo osso por estímulo dos osteoblastos.14,16
Ao exame radiográfico vêem-se áreas de menor ou maior condensação que, ao exame microscópico, se caracterizam por traves ósseas reduzidas em espessura (osteopenia) e desmineralizadas (osteomalácia). Tumores marrons são raro.17
Com menor freqüência, estas alterações são observadas em casos de resistência óssea à ação do paratormônio e nas síndromes intestinais de malabsorção.18
TERCIÁRIO
Embora sujeito a controvérsias é considerada terciária a forma de hiperparatireoidismo causada por proliferação autônoma das células em pacientes portadores de hiperparatireoidismo secundário que passam a apresentar hipercalcemia quando a função renal for restabelecida 12.
CRITÉRIOS
1) doença renal confirmada seguida de hipocalcemia;
2) hipercalcemia apesar da diálise ou do transplante;
3) retorno subseqüente da normalidade da calcemia após paratireoidectomia.
O mecanismo é ainda desconhecido.19 Estudos moleculares sugerem que a progressão para o hipertireoidismo terciário está associada à perda do alelo do cromossomo4, compatível com a proliferação monoclonal que se instala em hiperplasia da paratireóide prévia.
HIPOPARATIREOIDISMO
Caracteriza-se por persistente redução de secreção do paratormônio, seguidos de hipocalcemia e hiperfosfatemia.
O sintoma principal é maior excitabilidade neuro-muscular, bem evidenciado pelo sinal de Chvostek à percussão do nervo facial Quando é mais intensa, chega até a tetania. Podem ocorrer alterações psíquicas e neurológicas, calcificações anômalas intra cranianas e outras alterações, relacionadas à intensidade do hipoparatireoidismo.
As principais causas no adulto são a remoção cirúrgica inadvertida das paratireóides em tireoidectomias ou em casos de linfadenectomia por metástases de carcinoma na região cervical. Outras causas mais raras têm sido assinaladas, como pós-radiação e supressão de produção do paratormônio, em casos de hipercalcemia prolongada. Na criança são citados casos de hipoparatireoidismo idiopático e formas familiares, auto-imunes.13
AGRADECIMENTO
Agradecemos ao Núcleo de Apoio à Publicação da Faculdade de Ciências Médicas da Santa Casa de São Paulo - NAP-SC o suporte técnico-científico à publicação deste manuscrito.
Trabalho recebido em 05/11/07
aprovado em 28/02/08
Todos os autores declaram não haver nenhum potencial conflito de interesses referente a este artigo.
- 1. Castleman B, Roth SI. Tumors of the parathyroid glands. Atlas of tumor pathology. Washington, DC: Armed Force Institute of Pathology; 1978.
- 2. Stevens A, Lowe J. Histologia. São Paulo: Manole; 1995.
- 3. Young B, Heath JW. Histologia funcional. Rio de Janeiro: Guanabara; 2000.
- 4. Junqueira LC, Carneiro J. Histologia básica. Rio de Janeiro: Guanabara Koogan; 1995.
- 5. Askanazy M. Ueber ostitis deformans ohne osteoides Gewebe. Arb Geb Pathol Anat Institut zu Tübingen 1904; 4:398-422.
- 6. Albright F, Reifenstein EC. The parathyroid gland and metabolic bone diseases. Selected studies. Baltimore: William & Wilkins; 1948.
- 7. Hall EM, Chaffin L. Malignant tumors of the parathyroid glands. West J Surg Obstet Gynecol. 1934;42:578-86.
- 8. Castleman B, Mallory TB. The pathology of the parathyroid gland in hyperpaparathyroidism: a study of 25 cases. Am J Pathol. 1935;11:1-69.
- 9. Pappenheimer AM, Wilnes SL. Enlargement of parathyroid glands in renal diseases. Am J Pathol. 1935;11:73-91.
- 10. Lloyd HM. Primary hyperparathyroidism: an analysis of the role of the parathyroid tumor. Medicine (Baltimore). 1968;47:53-71.
- 11. Dedeurwaerdere F, Van Damme B. Histopathology of the parathyroid glands. Acta Otorhinolaryngol Belg. 2001;55:95-101.
- 12. Prospero JD. Tumores ósseos. São Paulo: Roca; 2001.
- 13. Robbins SL, Cotran RS, Kumar V. Patologia estrutural e funcional. Rio de Janeiro: Interamerica; 1986.
- 14. Bartlett NL, Cochran DQ. Reparative process in primary hyperparathyroidism. Radiol Clin North Am. 1964;2:261-79.
- 15. Masi L, Brandi ML. Physiopathological basis of bone turnover. Q J Nucl Med. 2001;45:2-6.
- 16. Douglas CR. Patofisiologia de sistemas renal. São Paulo: Robe Editorial; 2001.
- 17. Dorfman HB, Czerniak B. Bone tumors. St Louis: Mosby; 1997.
- 18. Bullough PG. Orthopaedic pathology. 3rd. ed. London: Mosby-Wolfe; 1988.
- 19. Livolsi VA, Asa SL. Endocrine pathology. Pennsylvania: Churchil & Livingstone; 2002.
Endereço para correspondência:
Datas de Publicação
-
Publicação nesta coleção
02 Jun 2009 -
Data do Fascículo
2009
Histórico
-
Aceito
28 Fev 2008 -
Recebido
05 Nov 2007