Resumos
OBJETIVO: Avaliar as propriedades físico-químicas, microbiológicas e nutricionais de dietas enterais artesanais padronizadas preparadas nos domicílios de pacientes em terapia nutricional domiciliar. MÉTODOS: Foram desenvolvidas duas formulações de dietas enterais (F1=1,2kcal/mL e F2=1,5kcal/mL), elaboradas com maltodextrina (155/155g), concentrado proteico de soro de leite (30/15g) e óleos vegetais (30/60g) dissolvidos em água (q.s.p.1000mL). Os cuidadores receberam os ingredientes e as medidas padrão e foram orientados quanto ao preparo e às boas práticas de manipulação. O estudo teve duração de quatro meses, e amostras das dietas preparadas nos domicílios de 33 pacientes foram coletadas e analisadas no início e no final deste período. As amostras foram avaliadas quanto à sua adequação percentual em relação aos valores prescritos de macronutrientes e energia, bem como aos padrões microbiológicos estabelecidos pela legislação vigente. RESULTADOS: As dietas formuladas (Formulação 1/Formulação 2) apresentaram os seguintes teores de macronutrientes, energia e osmolalidade: água - 73,5/70,0%; proteína - 4,4/6,0%; lipídeo - 4,3/6,6%; carboidrato - 16,9/16,4%; energia - 120/150kcal/100mL; osmolalidade - 440/450mOsm/kg.H2O. As variações nas adequações percentuais das amostras domiciliares foram menores que 20,0% tanto na primeira quanto na última amostragem. As proporções de amostras em desacordo com os padrões legais foram significantemente menores nas amostras finais, 24,0% e 36,0% para bactérias mesófilas e coliformes, respectivamente. CONCLUSÃO: O preparo das dietas nos domicílios apresentou boa reprodutibilidade; no entanto, a qualidade microbiológica ainda permanece uma questão preocupante, exigindo uma atuação cuidadosa do profissional de saúde nos domicílios.
Alimentos formulados; Contaminação; Controle de qualidade; Nutrição enteral; Terapia nutricional
OBJECTIVE: This study assessed the physical, chemical, microbiological and nutritional properties of standardized enteral diets prepared at the homes of patients receiving nutritional therapy. METHODS: Two enteral diet formulations were developed (F1=1.2kcal/mL and F2=1.5kcal/mL) containing maltodextrin (155/155g), whey protein concentrate (30/15g) and vegetable oils (30/60g) dissolved in water (q.s.p.1000mL). The ingredients and measuring devices were given to the caregivers, along with preparation instructions and advice on good handling practices. The study lasted four months and the diets prepared at the homes of 33 patients were collected at baseline and endline for analysis. The samples were analyzed to determine the compliance of their macronutrient and energy contents with the prescription and their microbiological contents with the legislation. RESULTS: The study diets (Formulation 1/Formulation 2) contained the following macronutrient and energy contents and osmolality: water - 73.5/70.0%; protein - 4.4/6.0%; lipids - 4.3/6.6%; carbohydrate - 16.9/16.4%; energy - 120/150kcal/100mL; osmolality - 440/450mOsm/kg.H2O. The percent adequacy of the homemade diets did not vary by more than 20.0% at baseline or end of study. The percentages of samples that did not meet the legal standards were significantly lower at the end of the study: 24.0% and 36.0% for mesophilic bacteria and coliforms, respectively. CONCLUSION: Homemade diets presented good reproducibility but their microbiological quality remains a matter of concern, indicating that health professionals must be careful when working at home.
Food formulated; Contamination; Quality control; Enteral Nutrition; Nutrition therapy
ORIGINAL ORIGINAL
Qualidade nutricional e microbiológica de dietas enterais artesanais padronizadas preparadas nas residências de pacientes em terapia nutricional domiciliar1 1 Artigo elaborado a partir da tese de VFN Santos, intitulada "Dieta enteral não industrializada para pacientes em terapia nutricional domiciliar: parâmetros físicos, químicos e nutricionais, efeito sobre a antropometria e índices bioquímicos, reprodutibilidade na preparação domiciliar e qualidade microbiológica". Universidade Federal de São Paulo; 2012.
Nutritional and microbiological quality of standardized homemade enteral diets for patients in home nutritional therapy
Valdirene Francisca Neves dos Santos; Andrea Bottoni; Tania Beninga Morais* * Correspondência para/ Correspondence to: TB MORAIS. E-mail: < tania.pnut@epm.br>
Universidade Federal de São Paulo, Programa de Pós Graduação em Nutrição, Laboratório de Bromatologia e Microbiologia de Alimentos. R. Napoleão de Barros, 889, 04024-002, São Paulo, SP, Brasil
RESUMO
OBJETIVO: Avaliar as propriedades físico-químicas, microbiológicas e nutricionais de dietas enterais artesanais padronizadas preparadas nos domicílios de pacientes em terapia nutricional domiciliar.
MÉTODOS: Foram desenvolvidas duas formulações de dietas enterais (F1=1,2kcal/mL e F2=1,5kcal/mL), elaboradas com maltodextrina (155/155g), concentrado proteico de soro de leite (30/15g) e óleos vegetais (30/60g) dissolvidos em água (q.s.p.1000mL). Os cuidadores receberam os ingredientes e as medidas padrão e foram orientados quanto ao preparo e às boas práticas de manipulação. O estudo teve duração de quatro meses, e amostras das dietas preparadas nos domicílios de 33 pacientes foram coletadas e analisadas no início e no final deste período. As amostras foram avaliadas quanto à sua adequação percentual em relação aos valores prescritos de macronutrientes e energia, bem como aos padrões microbiológicos estabelecidos pela legislação vigente.
RESULTADOS: As dietas formuladas (Formulação 1/Formulação 2) apresentaram os seguintes teores de macronutrientes, energia e osmolalidade: água - 73,5/70,0%; proteína - 4,4/6,0%; lipídeo - 4,3/6,6%; carboidrato - 16,9/16,4%; energia - 120/150kcal/100mL; osmolalidade - 440/450mOsm/kg.H2O. As variações nas adequações percentuais das amostras domiciliares foram menores que 20,0% tanto na primeira quanto na última amostragem. As proporções de amostras em desacordo com os padrões legais foram significantemente menores nas amostras finais, 24,0% e 36,0% para bactérias mesófilas e coliformes, respectivamente.
CONCLUSÃO: O preparo das dietas nos domicílios apresentou boa reprodutibilidade; no entanto, a qualidade microbiológica ainda permanece uma questão preocupante, exigindo uma atuação cuidadosa do profissional de saúde nos domicílios.
Termos de indexação: Alimentos formulados. Contaminação. Controle de qualidade. Nutrição enteral. Terapia nutricional.
ABSTRACT
OBJECTIVE: This study assessed the physical, chemical, microbiological and nutritional properties of standardized enteral diets prepared at the homes of patients receiving nutritional therapy.
METHODS: Two enteral diet formulations were developed (F1=1.2kcal/mL and F2=1.5kcal/mL) containing maltodextrin (155/155g), whey protein concentrate (30/15g) and vegetable oils (30/60g) dissolved in water (q.s.p.1000mL). The ingredients and measuring devices were given to the caregivers, along with preparation instructions and advice on good handling practices. The study lasted four months and the diets prepared at the homes of 33 patients were collected at baseline and endline for analysis. The samples were analyzed to determine the compliance of their macronutrient and energy contents with the prescription and their microbiological contents with the legislation.
RESULTS: The study diets (Formulation 1/Formulation 2) contained the following macronutrient and energy contents and osmolality: water - 73.5/70.0%; protein - 4.4/6.0%; lipids - 4.3/6.6%; carbohydrate - 16.9/16.4%; energy - 120/150kcal/100mL; osmolality - 440/450mOsm/kg.H2O. The percent adequacy of the homemade diets did not vary by more than 20.0% at baseline or end of study. The percentages of samples that did not meet the legal standards were significantly lower at the end of the study: 24.0% and 36.0% for mesophilic bacteria and coliforms, respectively.
CONCLUSION: Homemade diets presented good reproducibility but their microbiological quality remains a matter of concern, indicating that health professionals must be careful when working at home.
Indexing terms: Food formulated. Contamination. Quality control. Enteral Nutrition. Nutrition therapy.
INTRODUÇÃO
A administração de dieta através da via enteral é um componente de tratamento médico bem aceito e tem contribuído significativamente para a redução da mortalidade e morbidade. O êxito deste tratamento deve-se à evolução dos conhecimentos em nutrição, no intuito de ofertar nutrientes de forma eficaz e segura1,2.
Dentre os vários motivos para que se desenvolvam serviços de terapia nutricional em esquema domiciliar, destaca-se o crescimento da população de idosos e, consequentemente, o aumento de indivíduos portadores de doenças crônicas, necessitando de assistência de saúde por longos períodos3,4. Há uma série de benefícios citados na literatura quanto ao fornecimento de nutrição enteral domiciliar; no entanto, problemas irão surgir se informações e cuidados posteriores com a nutrição enteral não forem orientados adequadamente5-7.
As fórmulas de nutrição enteral são preparadas comercialmente8 ou manualmente9,10; estas últimas são denominadas não industrializadas ou artesanais. Vários estudos científicos demonstraram os benefícios de sua utilização em terapia de nutrição enteral11-15. Dietas artesanais, por sua vez, são constituídas por alimentos in natura, produtos alimentícios e/ou módulos de nutrientes ou mesclas entre eles10.
Nos países desenvolvidos, é comum o uso de dietas enterais industrializadas (tratamento já consagrado) e, no Brasil, o recurso a este tipo de dieta vem aumentando gradativamente. Essas dietas oferecem maior segurança quanto à qualidade microbiológica e à composição nutricional8,11; porém, às vezes, não estão disponíveis, por razão de custo ou logística15. Neste contexto, dietas artesanais ocupam um papel fundamental na recuperação do paciente que depende de sua utilização para manutenção ou recuperação do seu estado nutricional.
A despeito de ser um tratamento estabelecido, muitos questionamentos têm sido descritos na literatura sobre o uso dessas dietas, como a falta de estabilidade e incertezas quanto à composição química e ao efeito osmótico16,17. Além disso, há necessidade de um controle rígido das condições higiênicas no preparo, acondicionamento e administração dos alimentos15,18. Dietas artesanais apresentaram alto grau de contaminação mesmo quando preparadas em ambiente hospitalar19,20.
Durante a elaboração da dieta artesanal, a falta de padronização dos procedimentos, dos ingredientes em medidas caseiras e do tempo de cocção pode contribuir para o caráter variável da composição nutricional. Resíduos retidos no processo de peneiramento também podem alterar sua composição17. Em dietas enterais artesanais preparadas no domicílio, com alimentos in natura, os valores de macronutrientes e energia podem corresponder a menos de 50% dos valores prescritos21, resultando em administração imprecisa dos nutrientes.
Assim, planejou-se o estudo aqui descrito com a finalidade de desenvolver dietas artesanais, sem a utilização de alimentos in natura, de menor custo, adequadas quanto à composição nutricional e à osmolalidade, padronizadas e reprodutíveis em domicílio, e que, ainda, apresentassem maior segurança microbiológica.
MÉTODOS
O estudo foi realizado durante o período de dezembro de 2007 a maio de 2009. Desenvolveram-se duas formulações experimentais (F1 e F2), utilizando ingredientes acessíveis, adequadas quanto à composição nutricional, à concentração osmolar e à qualidade microbiológica, isentas de glúten e sacarose, e de fácil preparo. Com a finalidade de evitar variações indesejáveis nos teores dos nutrientes, objetivou-se também a padronização dos ingredientes em medidas caseiras, a fim de favorecer a reprodução em condições domésticas. Por meio de análises laboratoriais, determinou-se a osmolalidade e os teores de energia, macronutrientes e sódio das formulações.
Após esta etapa, foram selecionados 33 domicílios de pacientes sob terapia nutricional domiciliar utilizando como fonte exclusiva de alimentação dietas artesanais preparadas com alimentos in natura. Estas, então, foram substituídas pelas formulações experimentais, segundo a indicação clínica. A formulação F1 foi indicada para a manutenção do estado nutricional de pacientes eutróficos, enquanto a formulação F2 foi indicada para aqueles pacientes com necessidades energéticas e proteicas aumentadas. O projeto foi aprovado pelo Comitê de Ética em Pesquisa da Universidade Federal de São Paulo (Unifesp) sob o Protocolo nº 1732/08. Termo de Consentimento Livre e Esclarecido foi obtido dos diretores clínicos de quatro empresas de assistência domiciliar, responsáveis médicos dos pacientes, assim como dos familiares responsáveis que concordaram em participar do estudo.
Os cuidadores dos pacientes envolvidos no estudo foram orientados pela pesquisadora quanto ao modo de preparo e às boas práticas de manipulação e armazenamento das formulações. O acompanhamento ocorreu durante quatro meses. No início do acompanhamento, os cuidadores foram orientados verbalmente e por escrito. Além disso, observaram a demonstração passo a passo da execução da formulação feita pela pesquisadora. Posteriormente, com a finalidade de avaliar a adequação à prescrição e às boas práticas de manipulação no preparo domiciliar, amostras das dietas foram coletadas para serem submetidas a análises laboratoriais físico-químicas e microbiológicas, no início e ao final do acompanhamento. Nos domicílios cujos resultados iniciais foram insatisfatórios, a pesquisadora retornou aos locais e acompanhou a execução das dietas pelos cuidadores, corrigindo as falhas observadas.
Para garantir que os pacientes recebessem a dieta experimental como foi prescrita, foram fornecidos às famílias todos os insumos necessários à preparação: matérias-primas, compostos de vitaminas e minerais, copos plásticos descartáveis, colher de café padronizada e jarras de vidro com tampa.
Desenvolvimento das formulações experimentais
As formulações foram desenvolvidas no Laboratório de Bromatologia e Microbiologia de Alimentos da Unifesp em condições semelhantes às domésticas. No seu preparo foram utilizados, como fonte de energia e macronutrientes, maltodextrina, albumina desidratada, concentrado proteico de soro de leite em pó, sal de cozinha, óleo de soja e azeite de oliva. As quantidades destes ingredientes foram padronizadas em copos plásticos descartáveis com capacidades de 300, 200 e 50mL, em medidas cheias e rasas, denominados a seguir como copos 300, 200 e 50.
Para atender às necessidades de vitaminas e minerais, foi utilizado o produto comercial Centrum®. Como este não era suficiente para suprir as necessidades diárias dos micronutrientes necessários para este grupo22, as quantidades de vitaminas e minerais faltantes foram complementadas com compostos de minerais e vitaminas preparados em farmácia de manipulação na forma de sachês. Todas as quantidades foram calculadas para o preparo de 1000mL de formulação. Os ingredientes foram adquiridos em supermercados,
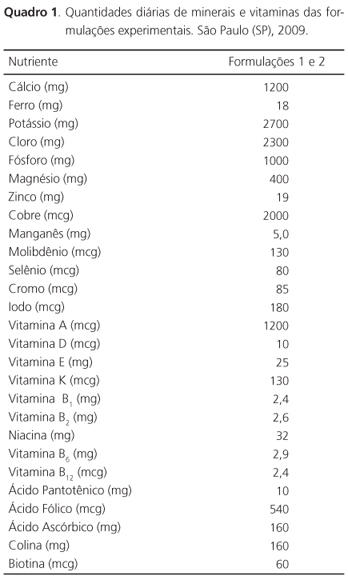
lojas especializadas em suporte nutricional e farmácias, todos facilmente encontrados na cidade de São Paulo (SP). As quantidades de sal adicionadas na composição das formulações F1 e F2 foram suficientes para suprir as necessidades mínimas de iodo e manter os teores adequados de sódio nas formulações22. A composição nutricional das vitaminas e minerais das formulações F1 e F2 está mostrada no Quadro 1 e os demais nutrientes e osmolalidade na Tabela 1.
Preparo da F1
Colocou-se uma medida de copo 300 de maltodextrina em pó (155g) em uma tigela e homogeneizou-se em 100mL de água previamente fervida e resfriada (duas medidas de copo 50mL). A seguir, sempre misturando lentamente, adicionaram-se duas medidas de copo 50 de albumina desidratada (24g), duas medidas de copo 50mL de proteína de soro de leite (30g), uma colher de café (1,5g) de sal de cozinha (NaCl), meia medida de copo 50mL de óleo de soja (15g) e meia medida de copo 50 de azeite de oliva (15g). Dois comprimidos de Centrum®, diluídos em meio medida de copo 50mL de água, e dois sachês de vitaminas e minerais foram adicionados à mistura. Completou-se com 700mL de água previamente fervida e resfriada (q.s.p.1000mL).
Preparo da F2
Nesta formulação, utilizaram-se as mesmas medidas de maltodextrina em pó, de sal de cozinha e de vitaminas e minerais, dobraram-se as quantidades de albumina desidratada (uma medida de copo 200mL), de óleo de soja (uma medida de copo 50mL) e de azeite de oliva (uma medida de copo 50mL), e diminuiu-se pela metade a quantidade de proteína de soro de leite (uma medida de copo 50mL). Completou-se com 700mL de água previamente fervida e resfriada (q.s.p.1000mL).
Análises laboratoriais das formulações experimentais
Para observação da estabilidade e homogeneidade, as formulações foram colocadas em béquer de vidro e armazenadas em geladeira por três horas. Ao final deste intervalo de tempo, foi feita a inspeção visual para verificar se a solução apresentava aspecto homogêneo e se ocorria separação de fases. Na avaliação da fluidez, as soluções foram passadas por equipo para observar-se a ocorrência de entupimentos.
As formulações foram analisadas para a determinação dos seguintes parâmetros: umidade, proteína, lipídeos totais, carboidratos, cinzas, sódio e energia Association of Official Analytical Chemists (AOAC)23. Teor de umidade foi obtido pelo método gravimétrico com aquecimento da amostra em estufa a 102ºC, até peso constante. Os lipídeos foram determinados após hidrólise ácida e extração com éter pelo extrator de Soxhlet; proteínas, por determinação da fração nitrogenada - método Kjeldahl -, e multiplicando por 6,25 como fator de conversão; cinzas, por incineração da matéria orgânica da amostra em mufla a 500-550ºC. Sódio foi obtido a partir das cinzas e determinado por espectrofotômetro de absorção atômica. Os teores de carboidratos foram determinados pela diferença e o valor energético calculado pela conversão de Atwater correspondentes à soma da multiplicação dos teores de proteínas e carboidratos por 4kcal e lipídeos por 9kcal, respectivamente.
A osmolalidade das formulações experimentais foi determinada em osmômetro (Advanced Wide-Range Osmometer 3W2) pelo método crioscópico, que se baseia na diminuição do ponto de congelamento à medida que se eleva a carga de soluto, obtendo-se o valor diretamente em mOsm/kg16. Considerou-se adequada a concentração osmolar inferior a 500 miliosmóis por quilo de água, de acordo com os parâmetros definidos pela Agência Nacional de Vigilância Sanitária (Anvisa)24.
Orientações aos cuidadores quanto às boas práticas de manipulação e armazenamento das formulações
Os cuidadores foram encorajados a utilizar as dietas no menor tempo possível após o seu preparo. Na impossibilidade, orientou-se que as dietas fossem acondicionadas em jarra de vidro com tampa e mantidas no compartimento superior do refrigerador, à temperatura entre 4ºC e 6ºC, por um período não superior a 12 horas.
Quanto à superfície de apoio ao preparo da dieta, orientações foram ministradas quanto à importância da limpeza de sujidades antes do preparo e aplicação de álcool a 70% após a limpeza. Para os utensílios utilizados no preparo, orientou-se a utilização de escaldamento com água fervente antes da utilização.
Devido à maior chance de contaminação cruzada, a utilização de panos de pratos foi desencorajada e vetada em todos os domicílios, recomendando-se o uso de toalhas de papel descartáveis. Quanto aos procedimentos de desinfecção das superfícies de apoio e de limpeza, orientouse a desinfecção das embalagens das matériasprimas. Especial atenção foi ministrada na limpeza e desinfecção das mãos e antebraço dos cuidadores antes do preparo das formulações.
Coleta e análises laboratoriais das formulações preparadas nos domicílios
A primeira coleta de amostras das formulações preparadas nos domicílios foi agendada para a semana subsequente ao início do acompanhamento pela pesquisadora. Devido à necessidade de iniciarem-se as análises microbiológicas em até duas horas após a coleta, e considerando-se as grandes distâncias entre os domicílios e o laboratório, foi necessário contratar serviço de mensageiro em motocicleta para o transporte das amostras. Assim, após o agendamento da coleta, um mensageiro era direcionado ao local com o material necessário, que consistia em caixa térmica de isopor, frasco de vidro com tampa esterilizado e bolsa térmica em gel. As coletas das dietas nas residências foram realizadas em horários aleatórios ao preparo. No domicílio, os cuidadores, já devidamente orientados quanto aos cuidados de coleta, transferiam aproximadamente 250mL da dieta a ser consumida pelo paciente naquele dia para o frasco esterilizado, que era acondicionado na caixa térmica, e com a bolsa térmica, para manutenção da temperatura de refrigeração da amostra, e imediatamente levado para o laboratório. Os horários do mensageiro, de saída e de chegada, foram anotados para controlar o intervalo máximo de duas horas.
As amostras das dietas coletadas nos domicílios foram submetidas a análises químicas23 e microbiológicas25. A partir dos teores encontrados de água, proteínas, lipídeos, carboidratos e energia, foram calculadas as adequações percentuais em relação aos teores prescritos. Na avaliação da qualidade microbiológica, foram realizadas as contagens de bactérias aeróbias facultativas mesófilas e a determinação do Número Mais Provável (NMP) de coliformes totais e de Escherichia coli. Os resultados foram comparados aos padrões microbiológicos definidos para estes microrganismos pela Resolução nº 63 da Anvisa. As análises estatísticas foram realizadas utilizando-se o software Sigma Stat for Windows 2.026. Em todos os testes, fixou-se nível de significância de 5% (p<0,05) para a rejeição da hipótese de nulidade.
RESULTADOS
As formulações F1 e F2 apresentaram-se homogêneas, com aspecto uniforme, não ocorrendo separação de fases após três horas do preparo, isentas de sacarose e glúten. Na análise da fluidez, as formulações passaram pelo pela equipo sem entupimentos, demonstrando que a concentração de sólidos existente na formulação permitiu um escoamento adequado das soluções.
Na Tabela 1 estão mostradas as composições centesimais das duas formulações desenvolvidas em laboratório. A F2 apresenta quantidade de energia 25% maior que na formulação F1, devido à maior quantidade de lipídeos e proteínas existentes nessa formulação. A formulação F2 apresentou maior densidade energética e maior proporção de nitrogênio por calorias não proteicas. A concentração osmolar foi adequada aos parâmetros exigidos pela legislação nas duas formulações.
Os valores expressos em mediana e percentis P25 e P75 da adequação percentual de água, macronutrientes e energia das duas dietas preparadas nos domicílios, nas amostras iniciais e finais, estão mostrados na Tabela 2. Observa-se que houve maior adequação à prescrição para água, tanto nas amostras iniciais e quanto nas finais. Quanto aos lipídeos e carboidratos, verificou-se que aumentou a adequação à prescrição nas amostras finais, sendo estas diferenças estatisticamente significativas. Energia também mostrou maior adequação ao final. O inverso foi observado em relação às proteínas, ocorrendo um aumento de sua quantidade e, consequentemente, uma diminuição da adequação à prescrição nas amostras finais, sendo esta diferença estatisticamente significativa.
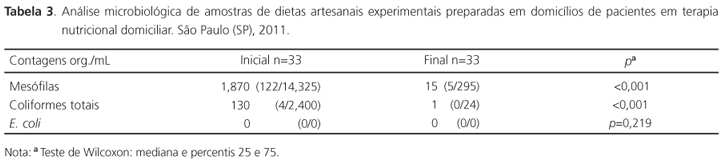
Na Tabela 3, observa-se a mediana e percentis P25 e P75 das contagens de bactérias mesófilas, coliformes totais e E. coli de amostras das dietas (F1 ou F2) preparadas nos domicílios, coletadas no início e ao final. Os valores das contagens das bactérias mesófilas e coliformes totais foram significativamente menores nas amostras finais, quando comparados àqueles valores de início; o mesmo não ocorreu com os valores das contagens de E. coli.
Quanto à adequação das dietas preparadas no domicílio aos padrões microbiológicos, 36% e 24% das amostras estavam adequadas quanto a bactérias mesófilas e coliformes, respectivamente, no início do acompanhamento; ao final, estas proporções aumentaram para 76 e 64%, respectivamente.
Na Tabela 4 estão os resultados das amostras das dietas F1 e F2, preparadas nos domicílios, no início e no final do acompanhamento. O teste de McNemar mostrou que o número de amostras em desacordo para bactérias mesófilas e coliformes totais foi significativamente menor ao final do acompanhamento. Quanto aos resultados de E. coli, o teste estatístico mostrou que, naqueles domicílios cujas amostras iniciais estavam positivas, estas permaneceram positivas também nas amostras finais.
O consumo médio das dietas F1 e F2 pelos pacientes foi de 1500mL/dia. A partir destes dados, apurou-se o custo médio de R$12,70 para F1(1,2kcal/mL) e de R$12,30 para F2 (1,5kcal/mL) no primeiro trimestre de 2012, a partir de pesquisa de preços junto aos fornecedores de matéria-prima. Neste mesmo período, os preços médios das dietas industrializadas líquidas de 1,2kcal/mL e 1,5kcal/mL foram de R$19,88 e R$36,75, respectivamente.
DISCUSSÃO
Escolher e adequar as fontes de nutrientes nas dietas artesanais é uma tarefa difícil e complexa para os nutricionistas. Além de adequadas quanto à composição nutricional e quanto à qualidade microbiológica, estas formulações devem ser estáveis e apresentar viscosidade e concentração osmolar apropriadas. A estas dificuldades somam-se, nos domicílios, os desafios de orientar e treinar os cuidadores para que estas formulações possam cumprir seu papel na recuperação e manutenção da saúde de pacientes em assistência domiciliar.
No estudo aqui descrito, muitos destes obstáculos foram vencidos - as formulações mostraram-se adequadas quanto às suas propriedades nutricionais e físico-químicas. Obteve-se sucesso, também, na observância, pelos cuidadores, das quantidades de ingredientes na preparação das formulações. As variações da adequação percentual de macronutrientes e energia, nas amostras coletadas nas residências, foram menores que 20%. A título de comparação, esta é a variação permitida pela Anvisa para rotulagem nutricional de alimentos industrializados27. Este resultado demonstrou que a padronização de medidas foi eficaz para manter as formulações dentro de variações aceitáveis, permitindo uma administração mais precisa de nutrientes.
Quanto à escolha da matéria-prima a ser utilizada na preparação, optou-se pela utilização da albumina desidratada e da proteína do soro do leite como fontes de proteína nas formulações (F1 e F2). No seu processamento, a albumina desidratada sofre um processo de pasteurização que aumenta a sua segurança microbiológica, quando comparada à utilização da clara do ovo in natura, assim como também elimina fatores antinutricionais presentes na clara do ovo crua (avidina)28.
Como fonte de carboidratos, a utilização da maltodextrina teve como vantagens a facilidade de diluição em água; o fato de ser insípida; de ter baixa osmolalidade; de não apresentar sobrecarga de solutos15; não elevar rapidamente os índices glicêmicos devido o esvaziamento gástrico ser mais lento quando comparado aos açúcares simples como a sacarose. Neste estudo, dez pacientes diabéticos utilizaram as formulações experimentais sem apresentar alterações nos níveis glicêmicos. Estas vantagens compensaram a sua utilização apesar do maior custo em relação à sacarose. A hipótese de acrescentar o amido de milho nas formulações foi descartada por apresentar propriedade constipante.
A utilização de fibras na dieta implica elevação no custo e aumento da viscosidade da dieta artesanal, sendo que dietas industrializadas sem fibras são comumente utilizadas na prática clínica sem prejuízos a muitos pacientes. No estudo realizado, para aqueles pacientes que apresentaram alteração do ritmo intestinal foram prescritos sachês de fibra em pó utilizados na água de hidratação, nos intervalos entre as dietas, até a normalização dos distúrbios.
A qualidade microbiológica de dietas artesanais ainda permanece como motivo de preocupação. Neste estudo, proporção expressiva de amostras - aproximadamente 40% -, das dietas preparadas nos domicílios apresentaram-se em desacordo com os padrões microbiológicos, ainda que tenha ocorrido diminuição estatisticamente significativa de desacordo ao final do acompanhamento, fato relacionado à facilidade no preparo da dieta, pela utilização de medidores padronizados e rápida execução, e também devido ao reforço das orientações da pesquisadora aos cuidadores quanto às boas práticas de manipulação durante a elaboração, armazenamento e distribuição da dieta.
A análise estatística também mostrou que, naqueles domicílios cujas amostras iniciais estavam positivas para E. coli, estas permaneceram positivas também nas amostras finais. Estes resultados indicam que, possivelmente, maior atenção deve ser dada, pelos profissionais de saúde, à qualidade microbiológica de dietas não industrializadas, no sentido de corrigir as falhas de manipulação. É possível, também, que nem todos os domicílios tenham condições de preparar dietas não industrializadas. Neste caso, será necessária uma avaliação cuidadosa do profissional de saúde in loco para definir aqueles que estão ou não aptos.
CONCLUSÃO
Os resultados desta pesquisa permitem concluir que foi possível tanto o desenvolvimento de dietas artesanais nutricionalmente adequadas como a sua reprodução em ambiente domiciliar, devido ao uso de medidas padronizadas e de orientação aos cuidadores sobre o modo de preparo. Portanto, estas formulações experimentais apresentam-se como opção para uma individualização de dieta enteral por sonda enteral ou gastrostomia na terapia nutricional domiciliar.
As contagens de micro-organismos, indicadoras de condições higiênicas inadequadas nos domicílios, apontam para a necessidade de melhor controle quanto às Boas Práticas de Manipulação (BPM) durante o preparo, armazenamento e administração das dietas. Assim, os autores sugerem a criação de um instrumento específico de BPM nos domicílios, para uma investigação mais acurada quanto às causas da contaminação das dietas nas residências.
AGRADECIMENTOS
Ao Conselho Nacional de Desenvolvimento Cientifico e Tecnológico, pelo apoio à pesquisa por intermédio do Programa de Pós-Graduação em Nutrição da Universidade Federal de São Paulo, concedendo bolsa de estudos a um dos pesquisadores.
COLABORADORES
VFN SANTOS participou da concepção e do desenho do estudo, da coleta, análise e interpretação dos dados e da redação do artigo. A BOTTONI participou da concepção e do desenho do estudo, da análise e da interpretação dos dados, e da revisão da redação do artigo. TB MORAES participou da concepção e do desenho do estudo, da análise e interpretação dos dados, da revisão da redação do artigo e da aprovação final da versão a ser publicada.
Recebido em: 4/5/2012
Versão final em: 30/7/2012
Aprovado em: 13/11/2012
- 1. Kreymann KG, Berger MM, Deutz NEP, Hiesmayr M, Jolliet P, Kazandjiev G, et al Espen Guidelines on enteral nutrition. Clin Nutr. 2006; 25(2):210-23. doi: 10.1016/j.clnu.2006.01.021.
- 2. Hernández JÁ, Torres NP, Jiménez M. Clinical use of enteral nutrition. Nutr Hospitalaria. 2006; 21(2): 85-97.
- 3. Scheneider SM. Virtual Clinical Nutrition University: Nutrition in the elderly-artificial nutrition. Eur J Clin Nutr Metab. 2009; 4(2):81-5. doi:10.1016/j.eclnm. 2008.11.004.
- 4. Russel CA, Rollins H. The needs of patients requiring home enteral tube feeding. Nutr Clin Care. 2002; 17(8):500-2.
- 5. Bodoky G, Smith LK. Basics in clinical nutrition: Complications of enteral nutrition. Eur J Clin Nutr Metabol. 2009; 4(5):209-11. doi: 10.1016/j.eclnm. 2009.05.003.
- 6. Carpentier YA. Basics in clinical nutrition: Substrates used in parenteral and enteral nutrition energy. Eur J Clin Nutr Metab. 2009; 4(2):55-6. doi: 10.10 16/j. eclnm.2008.07.014.
- 7. Howard P. Basics in clinical nutrition: Enteral nutrition. Eur J Clin Nutr Metab. 2009, 4(5):223-5. doi: 10.1016/j.eclnm.2009.05.008.
- 8. Zadák Z, Smith LK. Basics in clinical nutrition: Commercially prepared formulas. Eur J Clin Nutr Metab. 2009; 4(5):212-5. doi: 10.1016/j.eclnm. 2009.05.005.
- 9. Atzingen MCV, Silva MEMP. Desenvolvimento e análise de custo de dietas enterais artesanais à base de hidrolisado protéico de carne. Rev Bras Nutr Clin. 2007; 22(3):210-13.
- 10. Mitne C. Preparações não industrializadas para nutrição enteral. In: Waitzberg DL. Nutrição oral, enteral e parenteral na prática clínica. 3Ş ed. São Paulo: Atheneu; 2001.
- 11. Moreno JM, Shaffer J, Staun M, Hebuterne X, Bozzetti F, Pertkiewicz M, et al Survey on legislation and funding of home artificial nutrition in different european countries. Clin Nutr. 2001; 20(2):117-23. doi: 10.1054/clnu.2000.0363.
- 12. Desneves KJ, Todorovic BE, Cassar A, Crowe TC. Treatment with supplementary arginine, vitamin C and Zinc in patients with pressure ulcers: A randomized controlled trial. Clin Nutr. 2005; 24(6): 979-87. doi: 10.1016/j.clnu.2005.06.011.
- 13. Vaisman N, Haenen GRMM, Zaruk Y, Verduyn C, Bindels JG,Verlaan S, et al Enteral feeding enriched with carotenoids normalizes the carotenoid status and reduces oxidative stress in long-term enterally fed patients. Clin Nutr. 2006; 25(6):897-905. doi: 10.1016/j.clnu.2006.06.002.
- 14. Silk DBA, Walters ER, Duncan HD, Green CJ. The effect of a polymeric enteral formula supplemented with a mixture of six fibres on normal human bowel function and colonic motility. Clin Nutr. 2001; 20(1): 49-58. doi: 10.1054/clnu.2000.0359.
- 15. Schuitema CFJ. Basics in clinical nutrition: Diets for enteral nutrition. Eur J Clin Nutr Metab. 2009; 4(4):168-9. doi: 10.1016/j.eclnm.2009.05.002.
- 16. Henriques GS, Rosado GP. Formulação de dietas enterais artesanais e determinação da osmolalidade pelo método crioscópico. Rev Nutr. 1999; 12(3): 225-32. doi: 10.1590/S1415-527319990003000 03.
- 17. Menegassi B, Santana LS, Coelho JC, Martins AO, Pinto JPAN, Costa TMB, et al Características físico-químicas e qualidade nutricional de dietas enterais não-industrializadas. Alim Nutr. 2007; 18(2):127-32.
- 18. Brasil. Agência Nacional de Vigilância Sanitária. Resolução nş 63, de 6 de julho de 2000. Regulamento técnico para terapia de nutrição enteral. Diário Oficial da União. 2000 6 jul.
- 19. Carvalho MLR, Morais TB, Amaral DF, Sigulem DM. Hazard analysis and critical control point system approach in the evaluation of environmental and procedural sources of contamination of enteral feedings in three hospitals. J Parenter Enteral Nutr. 2000; 24(5):296-303.
- 20. Sullivan M M, Sorreda EP, Santos EE, Platon BG, Castro CG, Idrisalman ER, et al Bacterial contamination of blenderized whole food and commercial enteral tube feedings in the Philippines. J Hosp Infect. 2001; 49(4):268-73. doi: 10.1053/jhin.2001.1093.
- 21. Santos VFN, Morais TB. Nutritional quality and osmolality of home-made enteral diets, and follow-up of growth of severely disabled children receiving home enteral nutrition therapy. J Trop Pediatr. 2010; 56(2):127-8. doi: 10.1093/tropej/fmp033.
- 22. Shenkin A. Basics in clinical nutrition: Trace elements and vitamins in parenteral and enteral nutrition. Eur J Clin Nutr Metab. 2008; 3(6): e293-e7. doi: 10.1016/j.eclnm.2008.07.011.
- 23. Association of Official Analytical Chemists. Official methods of analysis. 17th ed. Virginia: AOAC; 2003.
- 24. Brasil. Agência Nacional de Vigilância Sanitária. Resolução da Diretoria Colegiada nş 449, de 9 de setembro de 1999. Regulamento técnico sobre padrões de identidade e qualidade de produtos de nutrição enteral. Diário Oficial da União. 1999 set 13.
-
25American Public Health Association. Compendium of methods for the microbiological examination of foods. 3th ed. Washington: APHA; 1992.
- 26. Sigma Stat [Software]. Version 2.0. Chicago (IL): Jandel Scientific Software; 1996.
- 27. Brasil. Agência Nacional de Vigilância Sanitária. Resolução nş 40, de 21 de março de 2001. Regulamento técnico para rotulagem nutricional obrigatória de alimentos e bebidas embalados. Diário Oficial da União. 2001 mar 22.
- 28. Domene SMA. A técnica dietética estudada segundo os grupos de alimentos. In: Domene SMA. Técnica dietética, teoria e aplicações. Rio de Janeiro: Guanabara; 2011.
Datas de Publicação
-
Publicação nesta coleção
27 Maio 2013 -
Data do Fascículo
Abr 2013
Histórico
-
Recebido
04 Maio 2012 -
Aceito
13 Nov 2012