Resumos
As plantas medicinais vêm sendo cada vez mais utilizadas devido às suas propriedades preventivas, paleativas e curativas, além de ser uma terapia alternativa que traz inúmeros benefícios aos usuários. As espécies Mikania glomerata e M. laevigata pertencem à família Asteraceae e são popularmente conhecidas como guaco sendo utilizadas no tratamento de enfermidades do trato respiratório. Além disso, as duas espécies são frequentemente confundidas ou citadas na literatura de forma errada. O presente trabalho teve por objetivo realizar uma revisão bibliográfica sobre a farmacologia, farmacobotânica e fitoquímica dos metabólitos secundários de Guaco, tendo destaque a cumarina, a biossíntese e as ações biológicas. As ações broncodilatadora, expectorante, anti-inflamatória e antialérgica, além de interações com alguns antibióticos e anticoagulantes, também foram descritas neste estudo.
fitoterapia; guaco; metabólitos secundários; biossíntese
Medicinal plants have been increasingly used due to their preventive, palliative and curative properties, besides being an alternative therapy that brings a large number of benefits to their users. The species Mikania glomerata belongs to the Asteraceae family and is popularly known as guaco, being employed to treat diseases of the respiratory tract. This study aimed to carry out a literature review about the pharmacology, pharmacobotany and phytochemistry of the secondary metabolites of M. glomerata, particularly coumarin, its biosynthesis and biological actions. The bronchodilator, expectorant, anti-inflammatory and antiallergic actions, as well as the interactions with some antibiotics and anticoagulants, were also described in this study.
phytotherapy; guaco; secondary metabolites; biosynthesis
REVISÃO
Farmacobotânica, fitoquímica e farmacologia do Guaco: revisão considerando Mikania glomerata Sprengel e Mikania laevigata Schulyz Bip. ex Baker
Morpho-anatomy, phytochemistry and pharmacology of Mikania glomerata Sprengel: a brief literature review
Czelusniak, K.E.; Brocco, A.; Pereira, D.F.; Freitas, G.B.L.* * guilhermebarroso@pop.com.br
Universidade Estadual do Centro-Oeste, Campus Cedeteg, Departamento de Farmácia, CEP: 85045-000, Guarapuava-Brasil
RESUMO
As plantas medicinais vêm sendo cada vez mais utilizadas devido às suas propriedades preventivas, paleativas e curativas, além de ser uma terapia alternativa que traz inúmeros benefícios aos usuários. As espécies Mikania glomerata e M. laevigata pertencem à família Asteraceae e são popularmente conhecidas como guaco sendo utilizadas no tratamento de enfermidades do trato respiratório. Além disso, as duas espécies são frequentemente confundidas ou citadas na literatura de forma errada. O presente trabalho teve por objetivo realizar uma revisão bibliográfica sobre a farmacologia, farmacobotânica e fitoquímica dos metabólitos secundários de Guaco, tendo destaque a cumarina, a biossíntese e as ações biológicas. As ações broncodilatadora, expectorante, anti-inflamatória e antialérgica, além de interações com alguns antibióticos e anticoagulantes, também foram descritas neste estudo.
Palavras-chave: fitoterapia, guaco, metabólitos secundários, biossíntese
ABSTRACT
Medicinal plants have been increasingly used due to their preventive, palliative and curative properties, besides being an alternative therapy that brings a large number of benefits to their users. The species Mikania glomerata belongs to the Asteraceae family and is popularly known as guaco, being employed to treat diseases of the respiratory tract. This study aimed to carry out a literature review about the pharmacology, pharmacobotany and phytochemistry of the secondary metabolites of M. glomerata, particularly coumarin, its biosynthesis and biological actions. The bronchodilator, expectorant, anti-inflammatory and antiallergic actions, as well as the interactions with some antibiotics and anticoagulants, were also described in this study.
Key words: phytotherapy, guaco, secondary metabolites, biosynthesis
INTRODUÇÃO
Há muito tempo as plantas medicinais vêm sendo estudadas na tentativa de descoberta de novos princípios ativos. Plantas medicinais são assim chamadas por apresentarem propriedades curativas e/ou preventivas para determinadas doenças.
As referências históricas afirmam que o uso de plantas medicinais faz parte da evolução humana e que essa prática é relatada na maioria das antigas civilizações, sendo a primeira referência escrita encontrada na obra Pen Ts'ao "A Grande Fitoterapia", do chinês Shen Nung, a qual remonta a 2800 a.C (Dorta, 1998). A fitoterapia foi um dos primeiros recursos terapêuticos utilizados pelos povos, além de ser por muito tempo a única terapia disponível ao homem. Em algumas ocasiões as plantas curavam, em outras matavam ou produziam graves efeitos colaterais (De Melo et al., 2009), sendo, portanto, essencial o uso responsável, racional, seguro e não abusivo das mesmas.
Fitoterapia significa tratamento de uma dada doença mediante o uso de plantas. Pode-se dizer então que a fitoterapia é uma terapêutica caracterizada pelo uso de plantas medicinais nas diferentes formas farmacêuticas. Emitida pela Agência Nacional de Vigilância Sanitária (ANVISA), a RDC nº 48, de 16 de março de 2004, classifica o medicamento fitoterápico como aquele obtido empregando-se exclusivamente matérias-primas ativas vegetais. Essa RDC não considera medicamento fitoterápico aquele que inclua substâncias ativas isoladas na composição, nem as associações destas com extratos vegetais. A eficácia e segurança são validadas em levantamentos etno-farmacológicos de utilização, documentações tecnocientíficas em publicações ou ensaios clínicos fase 3 (ANVISA, 2004).
Segundo dados da Organização Mundial de Saúde (OMS), o uso de plantas medicinais pela população mundial vem obtendo cada vez mais espaço, incentivado pela própria Organização, a qual acredita ser esta prática a principal opção terapêutica de aproximadamente 80% da população mundial (Pinto et al., 2002).
A partir da segunda metade dos anos 70 e década de 80, verificou-se o crescimento das medicinas alternativas, entre elas a fitoterapia. No Brasil, assim como em outros países em desenvolvimento e, até mesmo, em países desenvolvidos, tendo grande destaque a Alemanha, a fitoterapia tornou-se realidade (Alves & Silva, 2002). O aumento do consumo de fitoterápicos pode ser associado ao fato de que as pessoas têm questionado os perigos do uso abusivo e irracional de produtos farmacêuticos que não sejam de origem natural, procurando substituí-los por práticas alternativas, como o uso de plantas medicinais. A comprovação da ação terapêutica também favorece essa dinâmica. Além disso, registra-se a insatisfação da população perante o sistema de saúde e também a necessidade de poder controlar o próprio corpo, assumindo essas práticas alternativas de promoção, prevenção e recuperação da saúde (Leite, 2000).
O mercado mundial de fitoterápicos movimenta cerca de US$ 22 bilhões por ano. No Brasil estima-se que o comércio de fitoterápicos seja de 5% em relação ao mercado total de medicamentos, avaliando-o em mais de US$ 400 milhões (Pinto et al., 2002). Este comércio emprega várias espécies nativas brasileiras como, por exemplo, Mikania glomerata Sprengel (Alvarenga et al., 2009).
Entre diversas plantas na Lista de Medicamentos Fitoterápicos de Registro Simplificado, publicada pela ANVISA em 2008, e entre as incluídas nas edições da Farmacopea, está Mikania glomerata, popularmente conhecida como guaco (ANVISA, 2008). Tal é a importância desta espécie, que a inclusão foi feita já na primeira edição da Farmacopéia Brasileira, em 1929 (Silva, 1929). Além disso, na RDC nº 10, de 10 de março de 2010, a ANVISA publicou medidas, entre elas a união de ciência e tradição, esclarecendo quando e como as plantas medicinais devem ser utilizadas, garantindo os efeitos benéficos e evitando que o uso incorreto possa causar efeitos indesejáveis e toxicidade (ANVISA, 2010).
O Programa de Pesquisas de Plantas Medicinais, desenvolvido pela extinta Central de Medicamentos (CEME), reconheceu a eficácia de certas espécies, dentre elas o guaco. Seguindo as pesquisas anteriores, a Empresa Brasileira de Pesquisa Agropecuária (EMBRAPA) possui projetos de coleta e distribuição de plantas medicinais, além de apresentar um convênio com a Universidade do Mississipi (EUA), com o objetivo de produzir fitoterápicos de qualidade. Segundo o pesquisador da Embrapa Agroindústria Tropical, Flávio Pimentel, a partir deste convênio e estabelecendo normas de cultivo e processamento das plantas, os fitoterápicos terão mais qualidade, podendo ser utilizados em várias terapias pelo Sistema Único de Saúde (SUS), como uma estratégia para redução de custos (EMBRAPA, 2010).
Assim, a fitoterapia pode atender várias demandas da saúde da população, desde que abranja às exigências de controle de qualidade na produção e processamento das plantas, garantindo a eficácia e segurança aos usuários (Tomazzoni et al., 2006). Se este controle não for realizado efetivamente, alterações na composição química, eficácia, pureza e autenticidade da matéria-prima vegetal podem desenvolver fitoterápico de má qualidade. Esta é a preocupação atual quando se refere ao controle e produção de fitoterápicos de qualidade, visto que o uso de fitoterápicos pela população mundial vem aumentando nos últimos anos (Carvalho et al., 2008; Silveira et al., 2008).
No Brasil, esses problemas são encontrados com frequência em várias regiões do país e, um paradigma pode ser observado. A região norte é a maior produtora de fitoterápicos e, em contrapartida, é uma das que menos fiscaliza tais produtos (Borella & Fontoura, 2002; Amaral et al., 2003; Melo et al., 2004; Marliére et al., 2008; Veiga Junior, 2008).
O uso de plantas medicinais não pode mais ser considerado apenas como cultura de povos ou tradição, mas como ciência que vem sendo estudada, aperfeiçoada e utilizada por grande parte da população mundial, como terapia alternativa, a qual pode trazer inúmeros benefícios aos usuários (Tomazzoni et al., 2006). Isto é comprovado em relação ao Guaco, através de estudos sobre sua farmacobotânica, composição química e ações biológicas. Para a fitoterapia é fundamental também o conhecimento sobre os metabólitos secundários da planta, os efeitos e a biossíntese, além dos fatores que podem influenciar no acúmulo ou redução destes componentes na planta (Gobbo-Neto & Lopes, 2007).
Apesar da ampla quantidade de estudos sobre Mikania glomerata (guaco), é possível notar a ausência de um trabalho que englobe os principais pontos referentes ao uso de uma espécie de planta medicinal, i.e. rota biossintética dos metabólitos secundários, propriedades biológicas (farmacológicas e tóxicas) dos mesmos, morfoanatomia da espécie vegetal, assim como fatores intrínsecos e do meio (por exemplo, luz, vento, calor, chuva) que alteram o potencial de biossíntese. Por conseguinte, o presente estudo tem por objetivo realizar uma revisão bibliográfica sobre o guaco a fim de reunir os principais pontos sobre a espécie em único artigo atualizado e sucinto.
1. Família Asteraceae
O grupo mais numeroso dentro das Angiospermas é a família Asteraceae, que compreende cerca de 1.100 gêneros e 25.000 espécies. É constituída por plantas com características variadas, incluindo geralmente pequenas ervas ou arbustos e raramente árvores (Verdi et al., 2005). Aproximadamente 98% dos gêneros são compostos por plantas de pequeno porte que são encontradas em todos os tipos de habitats, principalmente nas regiões tropicais montanhosas da América do Sul (Joly, 1967).
Na constituição desta família, a composição química torna-se mais importante do que a morfologia devido à presença de várias classes de metabólitos secundários (Emerenciano et al.,1986).
1.1. Gênero Mikania
Eupatorieae é uma grande tribo que constitui a maior parte da família Asteraceae na região Neotropical. Essa tribo é composta por 16 subtribos e 170 gêneros, com aproximadamente 2.400 espécies, disseminadas pela América Central e pela América do Sul (Bautista, 2000).
Mikania é um dos gêneros mais estáveis dessa tribo, embora as espécies sejam de difícil delimitação, devido à grande variabilidade morfológica que estas plantas apresentam. O gênero Mikania conta com aproximadamente 430 espécies distribuídas nas regiões tropicais e subtropicais da América, sendo que 171 espécies são encontradas no Brasil (King & Robinson, 1987).
Entre a diversidade de plantas medicinais, que em virtude das propriedades terapêuticas são utilizadas pela população, se destacam as plantas do gênero Mikania, em especial o guaco, pela eficácia demonstrada no tratamento de diversas enfermidades (Rodrigues et al., 1996).
2. Guaco
2.1. Farmacobotânica do Guaco
A planta é subarbusto silvestre, escandente, de folhagem densa e perene, com caule cilíndrico, ramificado e glabro. Quando seco, o caule apresenta fratura fibrosa e aspecto estriado no sentido longitudinal, enquanto que, estando jovem, apresenta coloração verde-claro passando a arroxeada e a cinzento-escura nas partes suberificadas. As folhas são pecioladas, cordiforme-deltoides, oval-lanceoladas, tri ou pentanervadas e agudas no ápice (Figura 1) (Simões et al., 1988).
As flores são esbranquiçadas e carnosas, dispostas em inflorescência panícula tirsoide, com até 30 cm de comprimento, onde os capítulos se encontram reunidos em glomérulos (Figura 1). As bractéolas são lineares e apresentam medidas próximas a 2 mm de comprimento. O aquênio é pentangular, com aproximadamente 3 mm (Freitas, 2006).
O Guaco tem seu hábitat nas margens dos rios, crescendo espontaneamente em matas primárias, capoeiras, capoeirões, orla de matas, terrenos de aluvião, várzeas sujeitas a inundações e possui boa adaptação ao cultivo doméstico. A planta é bastante procurada por abelhas melíferas durante a época da floração. Reproduz-se por sementes ou plantio de estacas do caule, preferencialmente em terrenos arenosos e úmidos (Cabrera & Klein, 1989; Ritter & Miotto, 1992).
3. Fitoquímica do Guaco
3.1. Composição química
Na composição química de Mikania glomerata estão presentes a cumarina (Figura 2, 1), lupeol (Figura 2, 2), ácido α-isobutiriloxi-caur-16-en-19-oico (Figura 2, 3). São encontrados ainda óleos essenciais, entre eles sesquiterpenos e diterpenos do tipo caurano (Figura 2, 4), e.g. ácidos caurenoico (Figura 2, 5), grandiflórico (Figura 2, 6), cinamoilgrandiflórico (Figura 2, 7) e caurenol (Figura 2, 8). Outros metabólitos secundários como β-sitosterol (Figura 2, 9), friedelina (Figura 2, 10), estigmasterol (Figura 2, 11), taninos hidrolisáveis, flavonoides e saponina, também estão presentes na composição de Mikania (Oliveira et al., 1998; Santos, 2005; Vaz, 2010).
A cumarina é um dos principais responsáveis pelas atividades farmacológicas. Já foram identificadas cerca de 1.300 cumarinas em fontes naturais, como vegetais, fungos e bactérias, sendo encontradas principalmente nas famílias Asteraceae, Fabaceae, Oleaceae, Moraceae, Thymeleaceae, Apiaceae e Rutaceae. No guaco, a cumarina é utilizada no controle de qualidade na produção dos extratos, devido ao aroma característico que concede às folhas (Santos, 2005).
O ácido caurenoico é diterpeno encontrado em muitas espécies do gênero Mikania e, assim como a cumarina, apresenta importantes ações biológicas (Santos, 2005).
3.2. Biossíntese da cumarina
As cumarinas são derivadas da via do ácido chiquímico, o qual é formado pela condensação de dois metabólitos da glicose, o fosfoenolpiruvato e a eritrose-4-fosfato. A junção do ácido chiquímico com uma molécula de fosfoenolpiruvato dá origem ao ácido corísmico, ou corismato, dando continuidade à via. A partir deste, há a formação de aminoácidos aromáticos, precursores de alcaloides, tais como os essenciais triptofano, fenilalanina e o não-essencial tirosina. A fenilalanina sofre ação da fenilalanina-amônio-liase (PAL), a qual retira uma amônia da fenilalanina, dando origem ao ácido cinâmico, que por sua vez origina o ácido o-cumárico. Nos ácidos cinâmicos a isomerização cis/trans ocorre facilmente, catalisada pela luz com incidência de 360 nanômetros e, a radiação UV é suficiente para produzir uma mistura equilibrada de isômeros que podem ser isolados (Dewick, 2002; Scio, 2004; Peres, 2004).
O ácido o-cumárico sofre, em seguida, glicosilação e isomerização cis/trans, o que é fundamental para o processo de lactonização e formação final da cumarina. A cumarina é liberada apenas após hidrólise enzimática e lactonização, processos que ocorrem na danificação dos tecidos vegetais durante extração e processamento (Santos, 2005).
A Figura 3 mostra com detalhes as etapas da biossíntese da cumarina. A hidroxilação orto da cadeia lateral do ácido cinâmico é um passo fundamental na formação, catalisada pela enzima trans-cinamato-4-hidroxilase (Figura 3, a). Na etapa (b) ocorre uma o-glicosilação do ácido o-cumárico. Em seguida, etapa c, ocorre uma isomerização cis/trans da dupla ligação da cadeia lateral. A última etapa (d) é o processo de lactonização do ácido o-cumárico, por ação enzimática e na presença de calor (Scio, 2004).
Outras substâncias são formadas após a ação enzimática da PAL, como as ligninas, os flavonoides e o ácido benzoico precursor do ácido salicílico, importante na defesa das plantas contra patógenos. A fenilalanina-amônio-liase sofre alterações mediante fatores ambientais, tais como luz, disponibilidade nutricional e infecção por fungos (Peres, 2004).
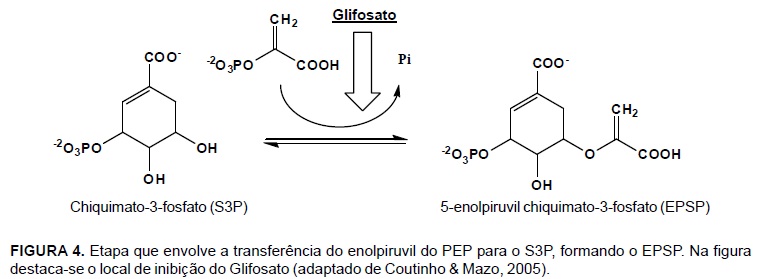
Outra importante enzima nessa via é a 5-enolpiruvil-3-fosfochiquimato sintase (EPSP sintase), a qual é inibida pelo herbicida glifosato, suspendendo a síntese de aminoácidos aromáticos. Em condições normais, a enzima EPSP catalisa, na planta, a reação que envolve a transferência do enolpiruvil do fosfoenolpiruvato (PEP) para o chiquimato-3-fosfato (S3P), formando 5-enolpiruvil-chiquimato-3-fosfato (EPSP) e fosfato inorgânico, Pi (Figura 4) (Coutinho & Mazo, 2005).
3.3. Fatores que influenciam no acúmulo ou redução de metabólitos secundários
É fundamental o conhecimento sobre os fatores que podem influenciar na composição química do fitoterápico e saber identificar em que partes da planta são encontrados maiores teores de metabólitos, a fim de otimizar a produtividade e tornar o produto final economicamente mais viável, além de melhorar a qualidade dos medicamentos sem aumentar os custos na sua produção.
As proporções dos metabólitos podem variar com alterações (Figura 5) sazonais, circadianas, intra e interplanta, idade e desenvolvimento da planta, incluindo desenvolvimento foliar, surgimento de novos órgãos, processos bioquímicos, fisiológicos, ecológicos e evolutivos. Temperatura, altitude, índice pluviométrico, radiação UV, composição a poluição atmosférica, disponibilidade de nutrientes e água no solo, herbivoria e ataque de patógenos são outros fatores que influenciam no metabolismo secundário.
A época de coleta é um dos fatores fundamentais, sendo relatada em praticamente todos os metabólitos secundários.
Outros fatores de grande importância são as condições de produção, coleta e estocagem da planta (Gobbo-Neto & Lopes, 2007).
Há uma relação entre intensidade de luz e produção de metabólitos secundários, pois todas as substâncias produzidas pelas plantas estão envolvidas com a fotossíntese, o que causa consequentemente, alterações anatômicas, fisiológicas e químicas. O teor de cumarina, especialmente, apresenta alterações significativas com relação às variações na intensidade de luz, tendo maior produção em pleno sol. Importantes variações de cumarina são encontradas dependendo do órgão, sendo que no Guaco os maiores teores deste metabólito são observados em folhas jovens (5,20 mg g-1 de matéria seca), seguidos por flores (1,04 mg g-1 de matéria seca), caules (1,05 mg g-1 de matéria seca) e raízes (0,11 mg g-1 de matéria seca). Além disso, as maiores concentrações de cumarina foram observadas perto da gema apical nas folhas, apontando os tecidos meristemáticos como locais de síntese. Os maiores valores são encontrados em partes superiores da planta, o que indica a relação com o crescimento e processo de desenvolvimento do guaco, quando ocorre maior acúmulo (Castro et al., 2006).
4. Propriedades farmacológicas do Guaco
4.1. Ações biológicas
O guaco é usado na cultura popular há séculos devido às propriedades das folhas, que incluem ação tônica, depurativa, antipirética e broncodilatora, além de estimulante do apetite e antigripal (Lorenzi & Matos, 2008). É ainda empregada no tratamento da asma, bronquite e adjuvante no combate à tosse (Teske & Trentini, 1997).
Estudos relataram que o guaco age diretamente causando broncodilatação e relaxamento da musculatura lisa respiratória, o que pode estar relacionado ao bloqueio dos canais de cálcio, acompanhado de ações anti-inflamatória e antialérgica (Moura et al., 2002; Castro et al., 2006), que são extremamente benéficas ao tratamento da asma, a qual caracteriza-se por obstrução e inflamação das vias aéreas e, resposta broncodilatadora exagerada (Santos, 2005).
Apesar de possuir várias indicações terapêuticas populares, somente a ação broncodilatadora, antitussígena, expectorante e edematogênica sobre as vias respiratórias foram comprovadas (Oliveira et al., 1998). Outros estudos mostram potencial atividade antialergênica (Fierro et al., 1999), antimicrobiana (Pessini et al., 2003), além de atividade analgésica (Ruppelt et al., 1991), anti-inflamatória (Falcão et al., 2005), antioxidante (Vicentino & Menezes, 2007) e antidiarreica (Salgado et al., 2005). Segundo a ANVISA, o guaco pode ser usado sob as formas de tintura e extrato (ANVISA, 2008).
Dentre os metabólitos encontrados no Guaco se destacam a cumarina e o ácido caurenoico pelas ações farmacológicas, tais como anti-inflamatória e expectorante. Acredita-se que o ácido caurenoico tenha a propriedade de inibir o crescimento de Staphylococcus aureus e Candida albicans, podendo ser este, juntamente com o ácido cinamolgrandiflórico os responsáveis pela atividade antibiótica (Soares et al., 2006). Apresenta também atividade antimicrobiana contra Staphylococcus epidermidis, Bacillus cereus, Bacillus subtilis e Streptococcus pneumoniae, além de ser ativo in vitro contra formas tripomastigotas de Trypanosoma cruzi. Potente ação relaxante da contração uterina, através de mecanismos independentes de receptores â2-adrenérgicos e como antagonista de canais de cálcio, também foi observada (Santos, 2005).
Estudos recentes avaliaram a composição química de extratos do guaco e sua atividade antimicrobiana sobre Streptococcus mutans. Observou-se efeito inibitório efetivo sobre as cepas bacterianas e inibição da aderência dos micro-organismos à superfície do vidro. A ação antimicrobiana de Mikania glomerata classifica-o como fonte promissora de novos agentes terapêuticos (Yatsuda et al., 2005), o que pode ser observado pela ação dos óleos essenciais de Mikania glomerata na atividade contra candidíase (Duarte et al., 2005).
As cumarinas apresentam atividade citotóxica, anti-HIV1 pela inibição da transcriptase reversa, antifúngica, inseticida, vasodilatadora coronariana através da inibição da cAMP-fosfodiesterase e anticoagulante, inibindo a formação de tromboxana nas plaquetas (Scio, 2004).
O extrato de guaco administrado por via subcutânea reduz a permeabilidade vascular, a migração de leucócitos e a adesão aos tecidos inflamados. A cumarina é capaz de inibir a migração de neutrófilos para o local afetado. Este efeito anti-inflamatório do fitoterápico pode ser devido à inibição da produção de citocinas pró-inflamatórias no local de inflamação (Alves et al., 2009).
O tratamento com Mikania glomerata também está indicado em casos de pneumoconiose, que é caracterizada por inflamação pulmonar causada pela exposição ao pó de carvão. A utilização reduz a infiltração pulmonar inflamatória induzida pelo pó de carvão, o que aponta o fitoterápico como preventivo de lesão pulmonar oxidativa (Freitas et al., 2008).
4.1.1. Interações medicamentosas e toxicidade
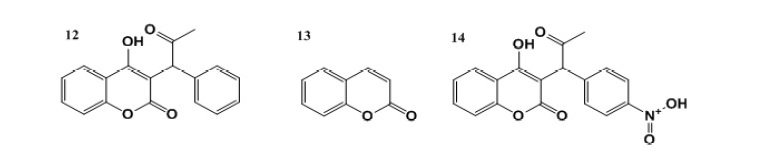
A varfarina (Figura 6, 12) cuja estrutura química resulta de uma modificação da cumarina (Figura 6, 13), é um anticoagulante oral que atua como inibidor da vitamina K, um cofator essencial para a síntese de fatores da coagulação II, VII, IX e X (Chaves et al., 2010). Outras moléculas com o esqueleto químico das cumarinas, como acenocumarol (Figura 6, 14), femprocumona (Figura 6, 15) e dicumarol (Figura 6, 16), também apresentam atividade anticoagulante (Chaves et al., 2010).
Como o guaco é rico em cumarinas, é desaconselhável o uso para crianças com idade inferior a um ano e mulheres no período gestacional. Além disso, o uso prolongado pode provocar acidentes hemorrágicos, pelo antagonismo à vitamina K (Freitas, 2006).
Além da interação com anticoagulantes, um estudo demonstrou que extratos secos de guaco poderão interagir, sinergicamente in vitro, com alguns antibióticos como tetraciclinas, cloranfenicol, gentamicina, vancomicina e penicilina, no entanto, o mecanismo de ação ainda é desconhecido (Betoni et al., 2006).
CONCLUSÃO
Os estudos citados neste trabalho demonstraram a presença de metabólitos secundários na composição química do Guaco, tais como óleos essenciais, estigmasterol, taninos hidrolisáveis, flavonoides e saponina, além da cumarina e do ácido caurenoico com propriedades farmacológicas descritas na literatura.
A cumarina, presente principalmente nas folhas do Guaco , é o principal metabólito e apresenta ações biológicas no combate a enfermidades do trato respiratório, devido as ações broncodilatadora, expectorante, antiinflamatória e antialérgica, comprovadas pelos diversos estudos realizados, o que faz do guaco um potente fitoterápico contra asma e bronquite.
Os registros apresentados demonstram a necessidade de novas pesquisas sobre plantas medicinais, incluindo o Guaco, esclarecendo sobre sua composição química e ações biológicas de seus componentes, além de possíveis interações medicamentosas, toxicidade e descoberta de novas atividades farmacológicas. Assim, a fitoterapia, aplicada de forma segura e racional, pode trazer os benefícios esperados aos usuários e ser cada dia mais utilizada como terapia alternativa.
A compreensão das enzimas envolvidas na rota biossintética dos metabólitos secundários com ação biológica pode auxiliar na modulação de efeitos farmacológicos e toxicológicos do extrato de Guaco. Isto se torna possível por meio da inibição de determinada via biossintética, o que consequentemente acarretaria inibição de determinado metabólito.
AGRADECIMENTO
À Universidade Estadual do Centro-Oeste (UNICENTRO), ao Programa de Pós-graduação em Química do IQ/UFRJ e ao órgão de fomento Capes-Proex.
Recebido para publicação em 13/11/2010
Aceito para publicação em 06/06/2011
- ALVARENGA, F.C.R. et al. Avaliação da qualidade de amostras comerciais de folhas e tinturas de guaco. Revista Brasileira de Farmacognosia, v.19, n.2a, p.442-8, 2009.
- ALVES, C.F. et al. Anti-inflammatory activity and possible mechanism of extract from Mikania laevigata in carrageenan-induced peritonitis. Journal of Pharmacy and Pharmacology, v.61, n.8, p.1097-104, 2009.
- ALVES, D.L.; SILVA, C.R. Fitohormônios: abordagem natural da terapia hormonal. São Paulo: Editora Atheneu, 2002. 105p.
- AMARAL, F.M.M. et al. Avaliação da qualidade de drogas vegetais comercializadas em São Luís/Maranhão. Revista Brasileira de Farmacognosia, v.13, n.1, p.27-30, 2003.
- BAUTISTA, H.P. Acritopappus diamantinicus (Asteraceae, Eupatorieae), a new species from Chapada Diamantina, Bahia, Brazil. Nordic Journal of Botany, v.20, n.2, p.173-7, 2000.
- BETONI, J.E.C. et al. Synergism between plant extract and antimicrobial drugs used on Staphylococcus aureus diseases. Memórias do Instituto Oswaldo Cruz, v.101, n.4, p.387-90, 2006.
- BORELLA, J.C.; FONTOURA, A. Avaliação do perfil cromatográfico e do teor de flavonóides em amostras de Baccharis trimera (Less.) DC. Asteraceae (carqueja) comercializadas em Ribeirão Preto, SP, Brasil. Revista Brasileira de Farmacognosia, v.12, n.2, p.63-7, 2002.
- BRASIL. Ministério da Saúde. Agência Nacional de Vigilância Sanitária. Resolução de Diretoria Colegiada (RDC) nº 48, de 16 de março de 2004. Dispõe sobre o registro de medicamentos fitoterápicos. Diário Oficial da União, Brasília, DF, 17 março. 2004.
- BRASIL. Ministério da Saúde. Agência Nacional de Vigilância Sanitária. Instrução Normativa (IN) nº 5, de 11 de dezembro de 2008. Lista de medicamentos fitoterápicos de registro simplificado. Diário Oficial da União, Brasília, DF, 12 dezembro. 2008.
- BRASIL. Ministério da Saúde. Agência Nacional de Vigilância Sanitária. Resolução de Diretoria Colegiada (RDC) nº 10, de 10 de março de 2010. Dispõe sobre a notificação de drogas vegetais. Diário Oficial da União, Brasília, DF, março, 2010.
- CABRERA¸ A.L.; KLEIN, M. Compostas (Eupatoriae). In: REITZ, R. Flora Ilustrada Catarinense Itajaí: Herbário Barbosa Rodrigues, 1989. p.649-750.
- CARVALHO, A.C.B. et al. Situação do registro de medicamentos fitoterápicos no Brasil. Revista Brasileira de Farmacognosia, v.18, n.2, p.314-9, 2008.
- CASTRO, E.M. et al. Coumarin contents in young Mikania glomerata plants (Guaco) under different radiation levels and photoperiod. Acta Farmacêutica Bonaerense, v.25, n.3, p.387-92, 2006.
- CHAVES, D.S.A. et al. Metabólitos secundários de origem vegetal: uma fonte potencial de fármacos antitrombóticos. Química Nova, v.33, n.1, p.172-80, 2010.
- COUTINHO, C.F.; MAZO, L.H. Complexos metálicos com o herbicida glifosato: revisão. Química Nova, v.28, n.6, p.1038-45, 2005.
- DEWICK, P.M. Medicinal natural products: a biosynthetic approach. 2.ed. London: West Sussex John Wiley & Sons, 2002. 507p.
- DORTA, E.J. Introdução: especial de plantas medicinais. Escala Rural, v.1, n.4, p.1-62, 1998.
- DUARTE, M.C. et al. Anti-Candida activity of Brazilian medicinal plants. Journal of Ethnopharmacology, v.97, n.2, p.305-11, 2005.
- EMBRAPA - Empresa Brasileira de Pesquisa Agropecuária. Convênio entre Brasil e Estados Unidos busca avanços em pesquisas com fitoterápicos. Disponível em: <http://www.embrapa.br/imprensa/noticias/2010/fevereiro/3a-semana/convenio-entre-brasil-e-estados-unidos-busca-avancos-em-pesquisas-com-fitoterapicos/?searchterm=guaco>. Acesso em: 25 ago. 2010.
- EMERENCIANO, V.P. et al. Evolution of sesquiterpene lactones in Asteracea. Biochemical Systematics and Ecology, v.14, n.6, p.585-9, 1986.
- FALCÃO, H.S. et al. Review of the plants with anti-inflammatory activity studied in Brazil. Revista Brasileira de Farmacognosia, v.15, n.4, p.381-91, 2005.
- FIERRO, I.O. et al. Studies on the anti-allergic activity of Mikania glomerata Journal of Ethnopharmacology, v.66, n.1, p.19-24, 1999.
- FREITAS, T.P. Avaliação dos efeitos de Mikania glomerata Sprengel e Mikania laevigata Schultz Bip. ex Baker (Asteraceae) no processo inflamatório induzido pela exposição aguda ao carvão mineral. 2006. 48p. Dissertação (Pós-Graduação em Ciências Ambientais) - Universidade do Extremo Sul Catarinense, Criciúma.
- FREITAS, T.P. et al. Effects of Mikania glomerata Sprengel. and Mikania laevigata Schultz Bip. ex Baker (Asteraceae) extracts on pulmonary inflammation and oxidative stress caused by acute coal dust exposure. Journal of Medicinal Food, v.11, n.4, p.761-6, 2008.
- GOBBO-NETO, L.; LOPES, N.P. Plantas medicinais: fatores de influência no conteúdo de metabólitos secundários. Química Nova, v.30, n.2, p.374-81, 2007.
- JOLY, A.B. Botânica: introdução a taxonomia vegetal. 7.ed. São Paulo: Cia Editora Nacional, 1967.159p.
- LEITE, S.N. Além da medicação: a contribuição da fitoterapia para a saúde pública. 2000. 114p. Dissertação (Mestrado em Saúde Pública) - Departamento de Saúde Materno-Infantil, Universidade de São Paulo, São Paulo.
- LORENZI, H.; MATOS, F.J.A. Plantas medicinais no Brasil: nativas e exóticas. 2.ed. Nova Odessa: Instituto Plantarum, 2008. 544p.
- MARLIÉRE, L.D.P. et al. Utilização de fitoterápicos por idosos: resultados de um inquérito domiciliar em Belo Horizonte (MG), Brasil. Revista Brasileira de Farmacognosia, v.18, p.754-60, 2008.
- MELO, J.G. et al. Avaliação da qualidade de amostras comerciais de boldo (Peumus boldus Molina), pata-de-vaca (Bauhinia spp.) e ginco (Ginkgo biloba L.). Revista Brasileira de Farmacognosia, v.14, n.2, p.111-20, 2004.
- MELO, R.R. et al. Características farmacobotânicas, químicas e biológicas de Syzygium malaccense (L.) Merr. & l. M. Perry. Revista Brasileira de Farmácia, v.90, n.4, p.298-302, 2009.
- MOURA, R.S. et al. Antiophidian properties of the aqueous extract of Mikania glomerata Journal of Pharmacy and Pharmacology, v.54, n.2, p.249-56, 2002.
- OLIVEIRA, F.; AKISUE, G.; AKISUE, M.K. Farmacognosia São Paulo: Atheneu,1998. 412p.
- PERES, L.E.P. Metabolismo secundário. Escola Superior de Agricultura Luiz de Queiroz, p.1-26. 2004. Disponível em: http://docentes.esalq.usp.br/lazaropp/FisioVegGrad Bio/MetSec.pdf Acesso em: 26 out. 2010.
- PESSINI, G.L. et. al. Avaliação da atividade antibacteriana e antifúngica de extratos de plantas utilizados na medicina popular. Revista Brasileira de Farmacognosia, v.13, p.21-4, 2003.
- PINTO, C.A. et al. Produtos naturais: atualidade, desafios e perspectivas. Química Nova, v.25, p.45-61, 2002.
- RITTER, M.R.; MIOTTO, S.T.S. Taxonomia de Mikania Willd. (Asteraceae) no Rio Grande do Sul, Brasil. HOEHNEA - Periódico Científico do Instituto de Botânica, v.32, n.3, p.309-59, 2005.
- RODRIGUES, R.O.; ALVARENGA, M.A.; KATO, E.T.M. Constituintes químicos de Mikania malacolepsis Robinson. Lecta - Universidade São Francisco, v.14, n.1, p.29-47, 1996.
- RUPPELT, B.M. et al. Pharmacological screening of plants recommended by folk medicine as anti-snake venon. I. Analgesic and anti-inflammatory activity. Memórias do Instituto Oswaldo Cruz, v.86, n.2, p.203-5, 1991.
- SALGADO, H.R.N.; RONCARI, A.F.F.; MOREIRA, R.R.D. Antidiarrhoeal effects of Mikania glomerata Sprengel (Asteraceae) leaf extract in mice. Revista Brasileira de Farmacognosia, v.15, n.3, p.205-8. 2005.
- SANTOS, S.C. Caracterização cromatográfica de extratos medicinais de guaco: Mikania laevigata Schulyz Bip. ex Baker e M. glomerata Sprengel e ação de M. laevigata na inflamação alérgica pulmonar. 2005. 93p. Dissertação (Mestrado em Ciências Farmacêuticas) - Universidade do Vale do Itajaí, Itajaí
- SCIO, E. Cumarinas encontradas no gênero Kielmeyera - Família Clusiaceae. Revista Brasileira de Farmácia, v.85, n.1, p.27-31, 2004.
- SILVA, R.A.D. Pharmacopeia dos Estados Unidos do Brasil São Paulo: Companhia Editora Nacional, 1926. 1147p.
- SILVA JUNIOR, S.A.A. Essentia herba: plantas bioativas. Florianópolis: Epagri, 2006. 634p.
- SILVEIRA, P.F.; BANDEIRA, M.A.M.; ARRAIS, P.S.D. Farmacovigilância e reações adversas às plantas medicinais e fitoterápicos: uma realidade. Revista Brasileira de Farmacognosia, v.18, n.4, p.618-26, 2008.
- SIMÕES, C.M.O. et al. Pharmacological investigations on Achyrocline satureioides Journal of Ethnopharmacology, v.22, n.3, p.281-93, 1988.
- SOARES, A.K.A. et al. Avaliação da segurança clínica de um fitoterápico contendo Mikania glomerata, Grindelia robusta, Copaifera officinalis, Myroxylon toluifera, Nasturtium officinale, própolis e mel em voluntários saudáveis. Revista Brasileira de Farmacognosia, v.16, n.4, p.447-54, 2006.
- TESKE, M.; TRENTINI, A.M.M. Herbarium compêndio de fitoterapia 3.ed. Curitiba: Herbarium, 1997. 317p.
- TOMAZZONI, M.I.; NEGRELLE, R.R.B.; CENTA, M.L. Fitoterapia popular: a busca instrumental enquanto prática terapeuta. Texto & Contexto Enfermagem, v.15, n.1, p.115-21, 2006.
- VAZ, A.P.A. Série plantas medicinais, condimentares e aromáticas - guaco. Disponível em: <http://www.campinas.snt.embrapa.br/plantasMedicinais/guaco.pdf>. Acesso em: 16 jun. 2010.
- VEIGA JUNIOR, V.F. Estudo do consumo de plantas medicinais na Região Centro-Norte do Estado do Rio de Janeiro: aceitação pelos profissionais de saúde e modo de uso pela população. Revista Brasileira de Farmacognosia, v.18, n.2, p.308-13, 2008.
- KING, R.M.; ROBINSON, H. The genera of the Eupatorieae (Asteraceae). v.22. St. Louis: Missouri Botanical Garden, 1987. 581p.
- VERDI, L.G.; BRIGHENTE, I.M.C.; PIZZOLATTI, M.G. The Baccharis genus (Asteraceae): chemical, economic and biological aspects. Química Nova, v.28, n.1, p.85-94, 2005.
- VICENTINO, A.R.R.; MENEZES, F.S. Atividade antioxidante de tinturas vegetais, vendidas em farmácias com manipulação e indicadas para diversos tipos de doenças pela metodologia do DPPH. Revista Brasileira de Farmacognosia, v.17, n.3, p.384-7, 2007.
- YATSUDA, R. et al. Effects of Mikania genus plants on growth and cell adherence of mutans streptococci. Journal of Ethnopharmacology, v.97, n.2, p.183-9, 2005.
Datas de Publicação
-
Publicação nesta coleção
02 Out 2012 -
Data do Fascículo
2012
Histórico
-
Recebido
13 Nov 2010 -
Aceito
06 Jun 2011