Resumos
Echinodorus grandiflorus e Echinodorus macrophyllus, conhecidas como chapéu-de-couro, são empregadas de forma indistinta como anti-inflamatório. O objetivo deste trabalho foi realizar análises físico-químicas de três amostras (A, B e C) de folhas de chapéu-de-couro (E. grandiflorus) provenientes de fornecedores de São Paulo buscando avaliar a qualidade e autenticidade destas amostras considerando a Farmacopéia Brasileira, 5ª edição, como referência. Verificou-se que as amostras estavam de acordo com as especificações farmacopeicas em relação às características organolépticas, material estranho, umidade, cinzas totais, cinzas sulfatadas (exceto amostras A e B) e teores de derivados de ácido o-hidroxicinâmico (exceto amostra A). Na descrição macro e microscópica foram identificadas estruturas características de E. grandiflorus. Após análise dos perfis cromatográficos por cromatografia em camada delgada de sílica (CCDS) constatou-se a presença de ácido caféico, isoorientina e swertiajaponina, conforme a monografia da espécie. A amostra C foi a única droga vegetal aprovada segundo os critérios da Farmacopeia Brasileira, evidenciando-se a necessidade da realização do controle de qualidade de matérias-primas vegetais para garantir a obtenção de fitoterápicos seguros e eficazes.
Echinodorus grandiflorus; autenticidade; perfil cromatográfico; marcadores morfológicos
Echinodorus grandiflorus and Echinodorus macrophyllus, known as "chapéu-de-couro", have been differently used as anti-inflammatory agents. The aim of the present study was to carry out physicochemical analyses of three leaf samples (A, B and C) from "chapéu-de-couro" (E. grandiflorus) obtained from suppliers in São Paulo to assess the quality and the authenticity of these samples according to the Brazilian Pharmacopoeia (BP) 5th edition. All samples were in agreement with the specifications of the Pharmacopoeia considering their organoleptic characteristics, foreign material, humidity, total ash and sulfated ash (except for samples A and B), as well as the levels of o-hydroxycinnamic acid derivatives (except for sample A). Macroscopic and microscopic analysis of the samples revealed structures typical of E. grandiflorus. Analysis of chromatographic profiles by thin-layer chromatography (TLC) on silica gel indicated the presence caffeic acid, isoorientin and swertiajaponin, which are in accordance with the monography for this species. Sample C was the only plant drug approved according to the criteria of the Brazilian Pharmacopoeia, evidencing the need of quality control of raw plant material to ensure the production of safe and effective phytomedicines.
Echinodorus grandiflorus; authenticity; chromatographic profile; morphological markers
Qualidade e autenticidade de folhas de chapéu-de-couro (Echinodorus grandiflorus) oriundas de fornecedores de São Paulo
Quality and authenticity of leaves of "chapéu-de-couro" (Echinodorus grandiflorus) from suppliers in São Paulo
Dias, E.G.E.I, II; Valenzuela, V.C.T.I; Alves, M.R.I; Duarte, M.G.R.I; Garcia, E.F.II,* * elianafgh@yahoo.com.br
IDivisão de Vigilância Sanitária, Fundação Ezequiel Dias (FUNED), Rua Conde Pereira Carneiro, 80, Gameleira, 30510-010, Belo Horizonte, MG, Brasil
IICentro Universitário Newton Paiva, Av. Silva Lobo, 1720, 30460-000, Nova Granada, Belo Horizonte, MG, Brasil
RESUMO
Echinodorus grandiflorus e Echinodorus macrophyllus, conhecidas como chapéu-de-couro, são empregadas de forma indistinta como anti-inflamatório. O objetivo deste trabalho foi realizar análises físico-químicas de três amostras (A, B e C) de folhas de chapéu-de-couro (E. grandiflorus) provenientes de fornecedores de São Paulo buscando avaliar a qualidade e autenticidade destas amostras considerando a Farmacopéia Brasileira, 5ª edição, como referência. Verificou-se que as amostras estavam de acordo com as especificações farmacopeicas em relação às características organolépticas, material estranho, umidade, cinzas totais, cinzas sulfatadas (exceto amostras A e B) e teores de derivados de ácido o-hidroxicinâmico (exceto amostra A). Na descrição macro e microscópica foram identificadas estruturas características de E. grandiflorus. Após análise dos perfis cromatográficos por cromatografia em camada delgada de sílica (CCDS) constatou-se a presença de ácido caféico, isoorientina e swertiajaponina, conforme a monografia da espécie. A amostra C foi a única droga vegetal aprovada segundo os critérios da Farmacopeia Brasileira, evidenciando-se a necessidade da realização do controle de qualidade de matérias-primas vegetais para garantir a obtenção de fitoterápicos seguros e eficazes.
Palavras-chave:Echinodorus grandiflorus, autenticidade, perfil cromatográfico, marcadores morfológicos.
ABSTRACT
Echinodorus grandiflorus and Echinodorus macrophyllus, known as "chapéu-de-couro", have been differently used as anti-inflammatory agents. The aim of the present study was to carry out physicochemical analyses of three leaf samples (A, B and C) from "chapéu-de-couro" (E. grandiflorus) obtained from suppliers in São Paulo to assess the quality and the authenticity of these samples according to the Brazilian Pharmacopoeia (BP) 5th edition. All samples were in agreement with the specifications of the Pharmacopoeia considering their organoleptic characteristics, foreign material, humidity, total ash and sulfated ash (except for samples A and B), as well as the levels of o-hydroxycinnamic acid derivatives (except for sample A). Macroscopic and microscopic analysis of the samples revealed structures typical of E. grandiflorus. Analysis of chromatographic profiles by thin-layer chromatography (TLC) on silica gel indicated the presence caffeic acid, isoorientin and swertiajaponin, which are in accordance with the monography for this species. Sample C was the only plant drug approved according to the criteria of the Brazilian Pharmacopoeia, evidencing the need of quality control of raw plant material to ensure the production of safe and effective phytomedicines.
Key words:Echinodorus grandiflorus, authenticity, chromatographic profile, morphological markers
INTRODUÇÃO
Os fitoterápicos sempre representaram uma parcela significativa no mercado de medicamentos. Dados mais recentes estimam o mercado mundial de fitoterápicos em cerca de US$ 44 bilhões anuais, segundo a consultoria Analize and Realize, que atende algumas das maiores indústrias farmacêuticas do mundo, estando este ainda em expansão (Mioto, 2010). Segundo a Associação Brasileira de Empresas do Setor Fitoterápico (ABIFISA), não existem dados oficiais sobre o tamanho desse mercado no Brasil, apesar das estimativas variarem entre US$ 350 milhões e US$ 550 milhões. O ritmo de crescimento das vendas de fitoterápicos no mercado brasileiro atinge taxa de 15% ao ano, enquanto para medicamentos sintéticos a taxa anual de crescimento é de 4% (Febrafarma, 2007; Monte, 2007; Carvalho et al., 2008).
O aumento no uso de fitoterápicos pela população mundial também tem se traduzido em preocupação com a qualidade de tais produtos, devido aos problemas comumente encontrados referentes à autenticidade, pureza e composição química das matérias-primas vegetais que contribuem para um fitoterápico de má qualidade. Pesquisas realizadas no Brasil têm mostrado que a situação dos produtos à base de plantas medicinais é precária em vários centros urbanos (Amaral et al., 2003; Carvalho et al., 2004; Melo et al., 2004; Zaroni et al., 2004; Zuin et al., 2004; Tobias et al., 2007).
Nesse contexto, o Ministério da Saúde do Brasil edita normas federais para disciplinar o registro e a comercialização de produtos fitoterápicos no país. Atualmente, está em vigor a Resolução RDC nº14 que estabelece regras para o registro de medicamentos fitoterápicos, baseadas em rígidos parâmetros de qualidade, segurança e eficácia terapêutica. Esta resolução contempla a matéria-prima vegetal, os derivados de droga vegetal e o medicamento fitoterápico (Carvalho et al., 2008; Brasil, 2010). Espera-se assim que, o mercado de produtos registrados corrija gradativamente suas falhas e passe a ofertar fitoterápicos de maior qualidade à população (Ribeiro et al., 2005).
Brito & Brito (1993) apontaram diversos estudos químicos e/ou farmacológicos realizados com espécies da flora nativa, ressaltando as potencialidades de utilização de várias delas, bem como a necessidade de maiores estudos da riquíssima flora tropical brasileira. No Brasil, várias espécies nativas são largamente empregadas pela população com fins medicinais; entre estas podem ser citadas a goiabeira (Psidium guajava L.), a capeba (Pothomorphe umbellata (L.) Miq.) e o chapéu de couro (Echinodorus grandiflorus (Cham. & Schltdl.) Micheli) (Di Stasi et al., 2002), sendo a última selecionada para estudo no presente trabalho.
Echinodorus grandiflorus (Cham. & Schltdl.) Micheli e Echinodorus macrophyllus (Kunth) Micheli (Alismataceae) são denominadas popularmente de chapéu-de-couro (Panizza, 1997). As monografias de "chapéu-de-couro" presentes na Farmacopeia Brasileira 1ª e 2ª edições (Pharmacopeia..., 1926, Farmacopeia..., 1959) se referem apenas à espécie E. macrophyllus. No entanto, a monografia de Echinodorus grandiflorus foi recentemente publicada na quinta edição da Farmacopeia Brasileira (Farmacopeia..., 2010).
Tradicionalmente as folhas destas espécies são empregadas para o tratamento de processos inflamatórios (reumatismo, artrite) entre outros usos (Panizza, 1997; Lorenzi & Matos, 2002), tanto na forma de chás caseiros como em preparações fitoterápicas (Stehmann & Brandão, 1995; Marodin & Baptista, 2001; Di Stasi et al., 2002; Nunes et al., 2003). Apesar do amplo emprego pela população, não há atualmente nenhum medicamento fitoterápico contendo chapéu de couro registrado no Brasil, devido à falta de estudos que comprovem sua eficácia e segurança, conforme preconizado pela legislação vigente. Todavia, as drogas vegetais bem como alguns de seus derivados encontram-se atualmente no mercado nacional, comercializados por diferentes laboratórios.
As folhas de E. grandiflorus apresentam em sua composição diterpenos (do tipo clerodano e cembrano), flavonoides (C-heterosídeos de flavonas como a isoorientina e a swertiajaponina), derivados do ácido o-hidroxicinâmico (ácidos chicórico e caftárico), esteróides, ácidos graxos, arilpropanoides simples (ácido cafeico, ferúlico e isoferúlico) e ácido trans-aconítico (Tanaka, 2000; Pimenta; 2002; Schnitzler et al., 2007). Para a espécie E. macrophyllus foram isolados até o momento diterpenos clerodânicos, cembrânicos e labdânicos (Kobayashi et al., 2000a, 2000b, 2000c; Shigemori et al., 2002). Ressalta-se que diterpenos ocorrem em ambas espécies, no entanto, os constituintes com esqueletos clerodano e cembrano isolados das duas espécies são distintos e diterpenos labdânicos foram encontrados apenas em E. macrophyllus.
As duas espécies são utilizadas popularmente de forma indistinta para as mesmas finalidades medicinais em diversas regiões do Brasil (Panizza, 1997; Lorenzi & Matos, 2002); no entanto, os dados da literatura indicam composição química diferenciada para as espécies, evidenciando-se a necessidade de novos estudos químicos e farmacológicos buscando identificar as substâncias ativas.
Este trabalho foi desenvolvido com o objetivo de avaliar a qualidade e autenticidade de folhas de chapéu-de-couro (E. grandiflorus), provenientes de fornecedores do Estado de São Paulo, confrontando com os parâmetros preconizados pela monografia farmacopeica publicada em 2010.
MATERIAIS E MÉTODOS
Amostras avaliadas
Três amostras (A, B, C) de folhas rasuradas de chapéu-de-couro (aprox. 500 g) foram adquiridas de três fornecedores distintos de matéria prima vegetal, situados em São Paulo - SP, no período de março a abril de 2011. As amostras de drogas vegetais foram adquiridas pela indústria mineira "Belém Jardim Fitoterápicos" para fabricação de produtos a base de chapéu-de-couro.
Amostragem
A amostragem das drogas vegetais A, B e C foi efetuada por quarteamento como descrito na Farmacopeia Brasileira para lotes menores de 10 Kg de folhas, obtendo - se, como amostra final, 250 g de folhas que foram empregadas nas análises (Farmacopéia Brasileira, 2010).
Caracterização organoléptica
As amostras de drogas vegetais foram analisadas quanto à cor, odor e aspecto, a partir dos parâmetros descritos pela Farmacopeia Brasileira (Farmacopéia Brasileira, 2010). Para melhor visualização das características, as drogas vegetais foram transferidas para folhas de papel branco, e observadas sob luz natural.
Descrições macro e microscópica
A determinação macroscópica foi realizada a olho nu e com auxílio de um microscópio estereoscópio Olympus SZX9, avaliando-se os aspectos morfológicos externos comparando-os com bibliografia de referência (Haynes & Holm-Nielsen, 1994; Oliveira, 1998; Farmacopéia Brasileira, 2010). A caracterização microscópica foi realizada por meio de técnicas usuais de anatomia vegetal: diafanização, dissociação e coloração (Kraus & Arduin, 1997; Oliveira, 1998; Who, 1998; Farmacopéia Brasileira, 2010), utilizando microscópico Olympus CX31. As fotomicrografias foram obtidas a partir da câmara fotográfica Olympus QColor 5, acoplada ao microscópio.
Determinação de material estranho
As amostras (250 g) foram submetidas a uma tamisação sequencial (MESH 10, 20, 32, 80 e fundo). As frações retidas em cada tamis foram pesadas e armazenadas separadamente. Os materiais estranhos foram retirados manualmente, a olho nu, sendo posteriormente transferidos para placas de Petri e observados ao microscópio esterioscópio. Os diferentes tipos de materiais estranhos foram separados, pesados e os percentuais calculados (Farmacopéia Brasileira, 2010).
Determinação de água
Para a determinação do teor de água utilizou-se o método gravimétrico descrito na Farmacopeia Brasileira (Farmacopéia Brasileira, 2010). As análises foram realizadas em triplicata para todas as amostras e os resultados expressos em porcentagem de água em relação à droga vegetal.
Determinação de cinzas totais e sulfatadas
Na determinação do teor de cinzas totais e sulfatadas utilizou-se o método descrito na Farmacopeia Brasileira (Farmacopéia Brasileira, 2010). As análises foram realizadas em triplicata e as porcentagens de cinzas foram calculadas em relação à droga vegetal.
Obtenção dos perfis cromatográficos por CCD
Para as amostras de drogas vegetais, fez-se extração prévia por turbolização seguida de partição conforme monografia do chapéu-de-couro (Farmacopéia Brasileira, 2010). Para a obtenção dos perfis cromatográficos das drogas vegetais utilizaram-se cromatoplacas de alumínio recobertas por sílica gel 60G F254 Merck, sendo empregado como eluente acetato de etila, tolueno, ácido fórmico e água (100:10:10:1) e solução metanólica de difenilborato de aminoetanol a 1%, sob luz UV365nm, como revelador. A isoorientina e o ácido cafeico (ambos da Extrasynthése, França) foram utilizados como padrão. Os fatores de retenção (Rf) foram calculados para as manchas fluorescentes observadas.
Doseamento de derivados do ácido o-hidroxicinâmico por UV
As amostras de drogas vegetais foram extraídas, sob refluxo, com etanol a 50% (v/v) de acordo com metodologia descrita pela Farmacopéia Brasileira (2010), em triplicata. As análises foram realizadas em espectrofotômetro Fento (modelo 482), empregando-se o reagente de Arnow (nitrito de sódio e molibdato de sódio), em meio ácido. Mediu-se a absorvância da solução em 525 nm frente ao branco. Os teores de derivados do ácido o-hidroxicinâmico, expressos em porcentagem de verbascosídeo, foram calculados como descrito na monografia do chapéu de couro (Farmacopeia..., 2010).
Análise estatística
Os resultados obtidos nos ensaios de pureza e no doseamento foram submetidos à análise de variância (ANOVA), e posteriormente, ao teste de Tukey para comparação dos teores médios. As análises estatísticas foram realizadas pelo programa GraphPad Prism, versão 5 (2007) da GraphPad Software.
RESULTADOS E DISCUSSÃO
Os resultados dos testes físico-químicos e do doseamento estão apresentados na Tabela 1. Em relação às características organolépticas todas as amostras de drogas vegetais apresentaram sabor amargo e odor característico, conforme descrito na monografia da espécie. Nas análises macro e microscópica as características descritas na farmacopéia foram observadas nas folhas e pecíolos da droga vegetal. Porém, detalhes das folhas como formato da base e ápice, comprimento e largura, e detalhes das nervuras não puderam ser avaliados, visto que as amostras adquiridas encontravam-se rasuradas. Foram observados pontos translúcidos abundantes correspondentes aos ductos secretores nas lâminas foliares das três amostras. Estas estruturas são características apenas da espécie E. grandiflorus e são importantes na sua diferenciação em relação à E. macrophyllus, visto que as folhas destas espécies apresentam características anatômicas semelhantes (Haynes & Holm-Nielsen, 1994). Constatou-se que a epiderme em vista frontal, em ambas as faces da lâmina, é formada de células de paredes sinuosas, com estômatos paralelocíticos, com células-guarda alongadas e com dois pares de células subsidiárias adjacentes (Figura 1-I). Sobre as nervuras não ocorrem estômatos, mas são observados tricomas pluricelulares estrelados.
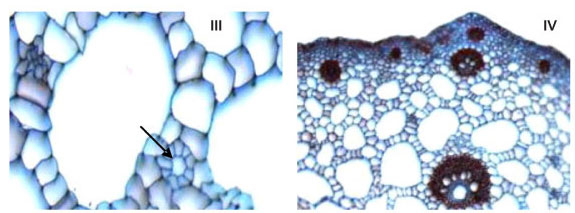
FIGURA 1. Aspectos microscópicos das três amostras de folhas de Echinodorus grandiflorus. (I) Epiderme abaxial, em vista frontal, com estômatos paralelocíticos (200X); (II) Feixe vascular de maior calibre circundado por aerênquima formando amplas lacunas (400X); (III) Espaço intercelular e ducto secretor (seta) nas trabéculas do aerênquima (200X); (IV) Pecíolo em secção transversal (100X).
Resultados dos ensaios de pureza e doseamento realizados para as amostras de folhas de chapéu-de-couro (A, B e C) adquiridas de fornecedores situados em São Paulo - SP.
Cortes transversais da lâmina foliar revelaram a epiderme uniestratificada. O mesófilo é composto por uma camada de parênquima paliçádico e pelo parênquima esponjoso, cujas células apresentam pequenas expansões braciformes (Figura 1-II). As nervuras principais são biconvexas circundadas por aerênquima formando amplas lacunas. Nestas lacunas, ocorrem ductos secretores (Figura 1-III) e trabéculas compostas por células braciformes com reentrâncias espessadas. O pecíolo, em secção transversal, é formado por aerênquima com as mesmas características da nervura principal (Figura 1-IV).
Nas amostras A e C observou-se grande quantidade de fragmentos de capítulos florais, o que indica que a colheita foi realizada na época de floração da espécie. No entanto, vale ressaltar que os capítulos florais não são preconizados pela farmacopéia, caracterizando adulteração destas amostras (Rocha, 2009; Farmacopeia..., 2010). Os pecíolos presentes nas três amostras, com menor predominância em B, são contemplados e descritos macro e microscopicamente na monografia farmacopeica da espécie. Dentre os materiais estranhos encontrados nas amostras avaliadas destacam-se capítulos florais da própria espécie, materiais plásticos, insetos vivos e fragmentos de insetos mortos (Figura 2). Considerando-se os limites preconizados na monografia do chapéu-de-couro (Farmacopeia..., 2010) para os ensaios de material estranho (máx. 2%), umidade (máx. 9%), cinzas totais (máx. 11%) e cinzas sulfatadas (máx. 13%) (Tabela 1), constatou-se que as amostras avaliadas apresentaram valores dentro dos limites estabelecidos pela farmacopéia, excetuando-se os teores de cinzas sulfatadas das amostras A e B (13,10 ± 0,02% e 14,44 ± 0,02%, respectivamente). Ressalta-se que um teor elevado de cinzas sulfatadas corresponde a um conteúdo elevado de impurezas inorgânicas nestas amostras (Rocha, 2009).
Materiais estranhos encontrados nas três amostras de chapéu-de-couro. (I) Capítulos florais da própria espécie; (II) Materiais plásticos; (III) Insetos e fragmentos de insetos
Nos perfis cromatográficos por CCD, as três amostras apresentaram manchas referentes aos marcadores da espécie: ácido cafeico (Rf = 0,72), isoorientina (Rf = 0,17) e swertiajaponina (Rf = 0,12) (Figura 3), conforme monografia do chapéu-de-couro (Farmacopeia..., 2010).
Perfis cromatográficos das amostras A, B e C, obtidos por CCDS. Padrões: ácido cafeico (1) e isoorientina (2). Eluente: acetato de etila-tolueno-ácido fórmico-água (100:10:10:1). Revelador: difenilborato de aminoetanol a 1%, em MeOH / UV365m (Farmacopeia..., 2010)
No doseamento de derivados do ácido o-hidroxicinâmico (DAH) (mín. 2,8%), constatou-se que as amostras B (3,89 ± 0,13%) e C (2,82 ± 0,03%) apresentaram teores de acordo com a monografia da espécie, enquanto a amostra A (2,10 ± 0,03%) exibiu teor inferior ao mínimo preconizado (Tabela 1). Teores de metabólitos secundários abaixo do preconizado podem estar associados a vários procedimentos inadequados, tais como condições de cultivo, colheita, pós-colheita, secagem e armazenamento (Farias, 2004). De acordo com a literatura, os derivados do ácido o-hidroxicinâmico como os ácidos caftárico e chicórico, já descritos em E. grandiflorus, exibem atividade anti-inflamatória (Facino et al., 1993; Barrett, 2003; Pellatti et al., 2005), assim, o baixo teor observado para a amostra A poderia comprometer o efeito terapêutico esperado para a espécie.
CONCLUSÃO
Foi confirmada a autenticidade das três amostras avaliadas pela identificação, na análise microscópica, dos pontos translúcidos correspondentes aos ductos secretores, os quais constituem característica diagnóstica da espécie E. grandiflorus.
A amostra C foi a única droga vegetal aprovada segundo os critérios da Farmacopeia Brasileira, podendo ser empregada como matéria-prima na indústria de fitoterápicos. As amostras A e B apresentaram um ou mais dos parâmetros avaliados fora dos valores preconizados pela monografia farmacopeica. Os resultados obtidos evidenciam a necessidade de realização do controle de qualidade de matérias-primas vegetais, visando à obtenção de medicamentos fitoterápicos padronizados, eficientes e seguros, segundo as normas estabelecidas pela legislação brasileira.
AGRADECIMENTO
À farmacêutica Luciana Regina Duarte da Indústria Belém Jardim Fitoterápicos pela orientação durante o estágio concedido a E.G.E.D.
REFERÊNCIA
AMARAL, F.M.M.; COUTINHO, D.F.; RIBEIRO, M.N.S.; OLIVEIRA, M.A. Avaliação da qualidade de drogas vegetais comercializadas em São Luís/ Maranhão. Revista Brasileira de Farmacognosia, v. 13, n. 1, p.27-30, 2003.
BARRET, B. Medicinal properties of Echinacea: A critical review. Phytomedicine, v.10, n.1, p. 66-86, 2003.
BRASIL. Ministério da Saúde. Agência Nacional de Vigilância Sanitária. Resolução RDC nº 14 de 31.03.10. Aprova o Regulamento Técnico visando normatizar o registro de medicamentos fitoterápicos junto ao Sistema de Vigilância Sanitária. Diário Oficial da União, 05.03.10.
BRITO, A.R.M.S.; BRITO, A.A.S. Forty years of brazilian medicinal plant research. Journal of Ethnopharmacology, v.39, n.1, p.53-67, 1993.
CARVALHO, A.C.B.; FERNÁNDEZ, M.G.; SANTOS, E.J.V.; MELO, A.F.M.; MEDEIROS, I.A.; DINIZ, M.F.F.M. Avaliação legal da propaganda e publicidade de medicamentos fitoterápicos anunciados na Paraíba (Brasil). Acta Farmacêutica Bonaerense, v.23, n.3, p. 413-417, 2004.
CARVALHO A.C.B.; BALBINO, E.E.; MACIEL. A.; PERFEITO, J.P.S. Situação do registro de medicamentos fitoterápicos no Brasil. Revista Brasileira de Farmacognosia, v. 18, n. 2, p. 314-319, Abr./Jun. 2008.
DI STASI, L.C.; OLIVEIRA, G.P.; CARVALHAES, M.A.; QUEIROZ-JUNIOR, M.; TIEN, O.S.; KAKINAMI, S.H.; REIS, M.S. Medicinal plants popularly used in the Brazilian Tropical Atlantic Forest. Fitoterapia, v.73, n.1, p.69-91, 2002.
FACINO, R.M.; CARINI, M.; ALDINI, G.; MARINELLO, C.; ARLANDINI, E.; FRANZOI, L.; COLOMBO, M.; PIETTA, P.; MAURI, P. Direct characterization of caffeoyl esters with antihyaluronidade activity in crude extracts from Echinacea angustifolia roots by fast atom bombardment tandem mass spectrometry. Il Farmaco, v.48, n.10, p.1447-1461, 1993.
FARIAS, M.R. Avaliação da qualidade de matérias-primas vegetais. In: SIMÕES, C. M. O.; SCHENKEL, E.P.; GOSMANN, G.; MELLO, J.C.P.; MENTZ, L.A.; PETROVICK, P.R. (orgs). Farmacognosia da Planta ao Medicamento. 5.ed. Rio Grande do Sul/ Florianópolis: Editora da UFSC e Editora da UFRGS, 2004. p.263-288.
Farmacopeia Brasileira. 5 ed. Vol. 1 e 2. Brasília: Agência Nacional de Vigilância Sanitária, 2010. 808p. Disponível em: http://www.anvisa.gov.br/hotsite/cd_farmacopeia/index.htm. Acesso em: 22 ago. 2011.
FEBRAFARMA, 2007. Fitoterápico atrai investimentos. Disponível em: http://www.febrafarma.org.br/areas.php?area=pu&secao=38&modulo=materias. Acesso em: 28 mar. 2011.
HAYNES, R.R.; HOLM-NIELSEN, L.B. Flora neotropica. Monograph 64. The Alismataceae. New York: Organization for Flora Neotropica by the New York Botanical Garden, 1994. 112p.
KRAUS, J.E., ARDUIN, M. Manual básico de métodos em morfologia vegetal. Rio de Janeiro: EDUR, 1997. 198p.
LORENZI, H.; MATOS, F.J.A. Plantas Medicinais no Brasil: nativas e exóticas cultivadas. Nova Odessa, SP: Instituto Plantarum, 2002. p.39-40.
MARODIN, S.M.; BAPTISTA, L.R.M. O uso de plantas com fins medicinais no município de Dom Pedro de Alcântara, Rio Grande do Sul, Brasil. Revista Brasileira de Plantas Medicinais, v.4, n.1, p.57-68, 2001.
MELO, J.G., NASCIMENTO, V.T., AMORIM, E.L.C.; ANDRADE LIMA, C.S.; ALBUQUERQUE, U.P. Avaliação da qualidade de amostras comerciais de boldo (Peumus boldus Molina), pata-de-vaca (Bauhinia spp.) e ginco (Ginkgo biloba L.). Revista Brasileira de Farmacognosia, v.14, n.2, p. 111-120, 2004.
MIOTO, R. País deixa de gerar US$ 5 bi por ano com fitoterápicos. Folha.com [online], São Paulo, 7 jun. 2010. Disponível em http://www1.folha.uol.com.br/ciencia/746386-pais-deixa-de-gerar-us-5-bi-por-ano-com-fitoterapicos.shtml Acesso em: 11 jan. 2011.
MONTE, C. Fitos e interfaces. T & C Amazônia, ano V. n. 11, p.2-8, 2007. Disponível em: https://portal.fucapi.br/tec/imagens/revistas/completa_revista_tc11_final.pdf. Acesso em: 12 jan, 2011.
NUNES, G.P.; SILVA, M.F.; RESENDE, U.M.; SIQUEIRA, J.M. Plantas medicinais comercializadas por raízeiros no centro de Campo Grande, Mato Grosso do Sul. Revista Brasileira de Farmacognosia, v.13, n.2, p.83-92, 2003.
OLIVEIRA, F., AKISUE, G., AKISUE, M.K. Farmacognosia. Rio de Janeiro, São Paulo: Atheneu, 1998. 412 p.
PANIZZA, S. Plantas que curam: cheiro de mato. 28. ed. São Paulo: IBRASA, 1997. p.79-80.
PELLATI, F.; BENVENUTI, S.; MELEGARI, M., LASSEIGNE, T. Variability in the composition of anti-oxidant compounds in Echinacea species by HPLC. Phytochemical Analysis, v.16, n.2, p.77-85, 2005.
RIBEIRO, A.Q.; LEITE, J.P.V.; DANTAS-BARROS, A.M. Perfil de utilização de fitoterápicos em farmácias comunitárias de Belo Horizonte sob a influência da legislação nacional. Revista Brasileira de Farmacognosia, v. 15, n.1, p.65-70, 2005.
ROCHA, L.M. Controle de qualidade de drogas vegetais e fitoterápicos. In: LEITE, J.P.V. Fitoterapia: bases científicas e tecnológicas. São Paulo: Editora Atheneu, 2009. p.253-276.
SCHNITZLER, M.; PETEREIT, F.; NAHRSTEDT, A. Trans-aconitic acid, glucosylflavones and hydroxycinnamoyltartaric acids from the leaves of Echinodorus grandiflorus ssp. aureus, a Brazilian medicinal plant. Revista Brasileira de Farmacognosia, v. 17, n.2, p.149-154, 2007.
SHARAPIN, N. Fundamentos de Tecnologia de Produtos Fitoterápicos. Santafé de Bogotá: CAB e CYTED, 2000. 248p.
SHIGEMORI, H; SHIMAMOTO, S.; SEKIGUCHI, M.; OHSAKI, A.; KOBAYASHI, J. Echinodolides A and B, new cembrane diterpenoids with an eight membered lactone ring from the leaves of Echinodorus macrophyllus. Journal of Natural Products, v.65, n.1, p.82-84, 2002.
STEHMANN, J.R.; BRANDÃO, M.G.L. Medicinal plants of Lavras Novas (Minas Gerais, Brazil). Fitoterapia, v. LXVI, n.6, 1995.
TANAKA, C.M.A. Constituintes químicos de cinco espécies de Echinodorus e avaliação do beta-pineno como substrato para obtenção de quirons mais elaborados. 2000. 202p. Tese (Doutorado em Química), Instituto de Química, Universidade Estadual de Campinas, Campinas.
TOBIAS, M.L.; OLIVEIRA, F.; OLIVEIRA, K.P.; MARQUES, L.C. Controle de qualidade de drogas vegetais de Farmácias de manipulação de Maringá (Paraná - Brasil). Revista Eletrônica de Farmácia, v. IV, n. 1, p. 95-103, 2007. Disponível em: revistas.ufg.br/index.php/REF/article/download/2126/2073. Acesso em: 03 abri. 2011.
ZARONI, M.; PONTAROLO, R.; ABRAHÃO, W.S.M.; FÁVERO, M.L.D; CORREA JÚNIOR, C.; STREMEL, D.P. Qualidade microbiológica das plantas medicinais produzidas no estado do Paraná. Revista Brasileira de Farmacognosia, v.14, n.1, p. 29-39, 2004.
ZUIN, V.G.; YARIWAKE, J.H.; BICCHI, C. Avaliação da qualidade de drogas vegetais a base de Passiflora spp. Comercializadas no Brasil: presença de resíduos de pesticidas. Revista Brasileira de Plantas Medicinais, v.6, n.2, p. 60-66, 2004.
WORLD HEALTH ORGANIZATION (WHO). Quality Control Methods for Medicinal Plant Materials. Geneva: WHO, 1998. 115p.
Recebido para publicação em 25/08/2011
Aceito para publicação em 28/11/2012
- AMARAL, F.M.M.; COUTINHO, D.F.; RIBEIRO, M.N.S.; OLIVEIRA, M.A. Avaliação da qualidade de drogas vegetais comercializadas em São Luís/ Maranhão. Revista Brasileira de Farmacognosia, v. 13, n. 1, p.27-30, 2003.
- BARRET, B. Medicinal properties of Echinacea: A critical review. Phytomedicine, v.10, n.1, p. 66-86, 2003.
- BRASIL. Ministério da Saúde. Agência Nacional de Vigilância Sanitária. Resolução RDC nş 14 de 31.03.10. Aprova o Regulamento Técnico visando normatizar o registro de medicamentos fitoterápicos junto ao Sistema de Vigilância Sanitária. Diário Oficial da União, 05.03.10.
- BRITO, A.R.M.S.; BRITO, A.A.S. Forty years of brazilian medicinal plant research. Journal of Ethnopharmacology, v.39, n.1, p.53-67, 1993.
- CARVALHO, A.C.B.; FERNÁNDEZ, M.G.; SANTOS, E.J.V.; MELO, A.F.M.; MEDEIROS, I.A.; DINIZ, M.F.F.M. Avaliação legal da propaganda e publicidade de medicamentos fitoterápicos anunciados na Paraíba (Brasil). Acta Farmacêutica Bonaerense, v.23, n.3, p. 413-417, 2004.
- CARVALHO A.C.B.; BALBINO, E.E.; MACIEL. A.; PERFEITO, J.P.S. Situação do registro de medicamentos fitoterápicos no Brasil. Revista Brasileira de Farmacognosia, v. 18, n. 2, p. 314-319, Abr./Jun. 2008.
- DI STASI, L.C.; OLIVEIRA, G.P.; CARVALHAES, M.A.; QUEIROZ-JUNIOR, M.; TIEN, O.S.; KAKINAMI, S.H.; REIS, M.S. Medicinal plants popularly used in the Brazilian Tropical Atlantic Forest. Fitoterapia, v.73, n.1, p.69-91, 2002.
- FACINO, R.M.; CARINI, M.; ALDINI, G.; MARINELLO, C.; ARLANDINI, E.; FRANZOI, L.; COLOMBO, M.; PIETTA, P.; MAURI, P. Direct characterization of caffeoyl esters with antihyaluronidade activity in crude extracts from Echinacea angustifolia roots by fast atom bombardment tandem mass spectrometry. Il Farmaco, v.48, n.10, p.1447-1461, 1993.
- FARIAS, M.R. Avaliação da qualidade de matérias-primas vegetais In: SIMÕES, C. M. O.; SCHENKEL, E.P.; GOSMANN, G.; MELLO, J.C.P.; MENTZ, L.A.; PETROVICK, P.R. (orgs). Farmacognosia da Planta ao Medicamento. 5.ed. Rio Grande do Sul/ Florianópolis: Editora da UFSC e Editora da UFRGS, 2004. p.263-288.
- Farmacopeia Brasileira. 5 ed. Vol. 1 e 2. Brasília: Agência Nacional de Vigilância Sanitária, 2010. 808p. Disponível em: http://www.anvisa.gov.br/hotsite/cd_farmacopeia/index.htm Acesso em: 22 ago. 2011.
» link - FEBRAFARMA, 2007. Fitoterápico atrai investimentos Disponível em: http://www.febrafarma.org.br/areas.php?area=pu&secao=38&modulo=materias. Acesso em: 28 mar. 2011.
- HAYNES, R.R.; HOLM-NIELSEN, L.B. Flora neotropica Monograph 64. The Alismataceae. New York: Organization for Flora Neotropica by the New York Botanical Garden, 1994. 112p.
- KRAUS, J.E., ARDUIN, M. Manual básico de métodos em morfologia vegetal Rio de Janeiro: EDUR, 1997. 198p.
- LORENZI, H.; MATOS, F.J.A. Plantas Medicinais no Brasil: nativas e exóticas cultivadas. Nova Odessa, SP: Instituto Plantarum, 2002. p.39-40.
- MARODIN, S.M.; BAPTISTA, L.R.M. O uso de plantas com fins medicinais no município de Dom Pedro de Alcântara, Rio Grande do Sul, Brasil. Revista Brasileira de Plantas Medicinais, v.4, n.1, p.57-68, 2001.
- MELO, J.G., NASCIMENTO, V.T., AMORIM, E.L.C.; ANDRADE LIMA, C.S.; ALBUQUERQUE, U.P. Avaliação da qualidade de amostras comerciais de boldo (Peumus boldus Molina), pata-de-vaca (Bauhinia spp.) e ginco (Ginkgo biloba L.). Revista Brasileira de Farmacognosia, v.14, n.2, p. 111-120, 2004.
- MIOTO, R. País deixa de gerar US$ 5 bi por ano com fitoterápicos. Folha.com [online], São Paulo, 7 jun. 2010. Disponível em http://www1.folha.uol.com.br/ciencia/746386-pais-deixa-de-gerar-us-5-bi-por-ano-com-fitoterapicos.shtml Acesso em: 11 jan. 2011.
- MONTE, C. Fitos e interfaces. T & C Amazônia, ano V. n. 11, p.2-8, 2007. Disponível em: https://portal.fucapi.br/tec/imagens/revistas/completa_revista_tc11_final.pdf. Acesso em: 12 jan, 2011.
- NUNES, G.P.; SILVA, M.F.; RESENDE, U.M.; SIQUEIRA, J.M. Plantas medicinais comercializadas por raízeiros no centro de Campo Grande, Mato Grosso do Sul. Revista Brasileira de Farmacognosia, v.13, n.2, p.83-92, 2003.
- OLIVEIRA, F., AKISUE, G., AKISUE, M.K. Farmacognosia Rio de Janeiro, São Paulo: Atheneu, 1998. 412 p.
- PANIZZA, S. Plantas que curam: cheiro de mato. 28. ed. São Paulo: IBRASA, 1997. p.79-80.
- PELLATI, F.; BENVENUTI, S.; MELEGARI, M., LASSEIGNE, T. Variability in the composition of anti-oxidant compounds in Echinacea species by HPLC. Phytochemical Analysis, v.16, n.2, p.77-85, 2005.
- RIBEIRO, A.Q.; LEITE, J.P.V.; DANTAS-BARROS, A.M. Perfil de utilização de fitoterápicos em farmácias comunitárias de Belo Horizonte sob a influência da legislação nacional. Revista Brasileira de Farmacognosia, v. 15, n.1, p.65-70, 2005.
- ROCHA, L.M. Controle de qualidade de drogas vegetais e fitoterápicos In: LEITE, J.P.V. Fitoterapia: bases científicas e tecnológicas. São Paulo: Editora Atheneu, 2009. p.253-276.
- SCHNITZLER, M.; PETEREIT, F.; NAHRSTEDT, A. Trans-aconitic acid, glucosylflavones and hydroxycinnamoyltartaric acids from the leaves of Echinodorus grandiflorus ssp. aureus, a Brazilian medicinal plant. Revista Brasileira de Farmacognosia, v. 17, n.2, p.149-154, 2007.
- SHARAPIN, N. Fundamentos de Tecnologia de Produtos Fitoterápicos Santafé de Bogotá: CAB e CYTED, 2000. 248p.
- SHIGEMORI, H; SHIMAMOTO, S.; SEKIGUCHI, M.; OHSAKI, A.; KOBAYASHI, J. Echinodolides A and B, new cembrane diterpenoids with an eight membered lactone ring from the leaves of Echinodorus macrophyllus Journal of Natural Products, v.65, n.1, p.82-84, 2002.
- STEHMANN, J.R.; BRANDÃO, M.G.L. Medicinal plants of Lavras Novas (Minas Gerais, Brazil). Fitoterapia, v. LXVI, n.6, 1995.
- TANAKA, C.M.A. Constituintes químicos de cinco espécies de Echinodorus e avaliação do beta-pineno como substrato para obtenção de quirons mais elaborados 2000. 202p. Tese (Doutorado em Química), Instituto de Química, Universidade Estadual de Campinas, Campinas.
- TOBIAS, M.L.; OLIVEIRA, F.; OLIVEIRA, K.P.; MARQUES, L.C. Controle de qualidade de drogas vegetais de Farmácias de manipulação de Maringá (Paraná - Brasil). Revista Eletrônica de Farmácia, v. IV, n. 1, p. 95-103, 2007. Disponível em: revistas.ufg.br/index.php/REF/article/download/2126/2073. Acesso em: 03 abri. 2011.
- ZARONI, M.; PONTAROLO, R.; ABRAHÃO, W.S.M.; FÁVERO, M.L.D; CORREA JÚNIOR, C.; STREMEL, D.P. Qualidade microbiológica das plantas medicinais produzidas no estado do Paraná. Revista Brasileira de Farmacognosia, v.14, n.1, p. 29-39, 2004.
- ZUIN, V.G.; YARIWAKE, J.H.; BICCHI, C. Avaliação da qualidade de drogas vegetais a base de Passiflora spp. Comercializadas no Brasil: presença de resíduos de pesticidas. Revista Brasileira de Plantas Medicinais, v.6, n.2, p. 60-66, 2004.
- WORLD HEALTH ORGANIZATION (WHO). Quality Control Methods for Medicinal Plant Materials Geneva: WHO, 1998. 115p.
Datas de Publicação
-
Publicação nesta coleção
18 Jun 2013 -
Data do Fascículo
2013
Histórico
-
Recebido
25 Ago 2011 -
Aceito
28 Nov 2012