Resumos
No presente trabalho fez-se a análise da organização estrutural das folhas de Cunila microcephala em microscopia fotônica e microscopia eletrônica de varredura. Seguiram-se as técnicas convencionais no preparo do material para obtenção das lâminas semipermanentes. Para a preparação de lâminas permanentes utilizou-se a técnica de inclusão em glicol metacrilato (GMA). A organização estrutural das folhas desta espécie revela: estômatos em ambas as faces com predominância na face abaxial (folha anfi-hipoestomática). Os estômatos da face adaxial são do tipo diacítico. As paredes anticlinais das células epidérmicas da face adaxial são sinuosas e apresentam espessamentos irregulares. As epidermes de ambas as faces são uniestratificadas. Tricomas tectores unisseriados e tricomas glandulares do tipo capitado unicelular e pluricelular se fazem presentes em ambas as faces. O mesofilo é heterogêneo dorsiventral. Idioblastos contendo cristais de inulina se fazem presentes em toda a extensão do limbo. A nervura principal em secção transversal, na porção mediana da lâmina foliar revela uma organização bastante simples, pouco saliente, na qual o parênquina clorofiliano paliçádico apresenta solução de continuidade. Os feixes vasculares são colaterais.
Cunila microcephala; Anatomia foliar; Tricomas glandulares; Inulina; Lamiaceae
This work has focused on the structural organization analysis of Cunila microcephala leaves in photonic microscopic and electronic scanning. Conventional techniques have been used to prepare the material for obtaining semi-permanent plates. For the preparation of permanent plates, the immersion into glycol methacrylate (GMA) has been performed. The structural organization of leaves belonging to this species reveals stomata in both faces with predominance in the abaxial face (amphihypostomatic leaf). The adaxial face stomata belongs to the diacytic type. The anticlinal walls of the epidermis cells of the adaxial face are sinuous and present irregular thickening. The epidermis of both faces is single layered. Uniserial tectorial trichomes and single celled and multicelled capitate glandular trichomes are present in both faces. The mesophyll is heterogeneous dorsi-ventral. Idioblasts containing inulin crystals are present throughout the foliar plate. The central veins in cross-section, in the medium portion of the foliar plate, have shown a very simple organization, not an outstanding one, where the chlorophyllian palisade parenchyma presents a solution of continuity. The vascular fagots are collateral.
Cunila microcephala; Foliar anatomy; Glandular trichome; Inulin; Lamiaceae
TRABALHOS ORIGINAIS
Caracterização anatômica das folhas de Cunila microcephala Benth. (Lamiaceae)
Anatomic characterization of Cunila microcephala Benth. (Lamiaceae) leaves
Maria da Graça Teixeira de ToledoI; Yedo AlquiniII; Tomoe NakashimaI
IDepartamento de Farmácia, Universidade Federal do Paraná
IIDepartamento de Botânica, Universidade Federal do Paraná
Correspondência Correspondência M. G. T. Toledo Universidade Federal do Paraná Departamento de Farmácia Av. Pref. Lothário Meissner, 3.400 - Jd. Botânico 80210-170 - Curitiba - PR E-mail: toledo@ufpr.br
RESUMO
No presente trabalho fez-se a análise da organização estrutural das folhas de Cunila microcephala em microscopia fotônica e microscopia eletrônica de varredura. Seguiram-se as técnicas convencionais no preparo do material para obtenção das lâminas semipermanentes. Para a preparação de lâminas permanentes utilizou-se a técnica de inclusão em glicol metacrilato (GMA). A organização estrutural das folhas desta espécie revela: estômatos em ambas as faces com predominância na face abaxial (folha anfi-hipoestomática). Os estômatos da face adaxial são do tipo diacítico. As paredes anticlinais das células epidérmicas da face adaxial são sinuosas e apresentam espessamentos irregulares. As epidermes de ambas as faces são uniestratificadas. Tricomas tectores unisseriados e tricomas glandulares do tipo capitado unicelular e pluricelular se fazem presentes em ambas as faces. O mesofilo é heterogêneo dorsiventral. Idioblastos contendo cristais de inulina se fazem presentes em toda a extensão do limbo. A nervura principal em secção transversal, na porção mediana da lâmina foliar revela uma organização bastante simples, pouco saliente, na qual o parênquina clorofiliano paliçádico apresenta solução de continuidade. Os feixes vasculares são colaterais.
Unitermos: Cunila microcephala. Anatomia foliar. Tricomas glandulares. Inulina. Lamiaceae.
ABSTRACT
This work has focused on the structural organization analysis of Cunila microcephala leaves in photonic microscopic and electronic scanning. Conventional techniques have been used to prepare the material for obtaining semi-permanent plates. For the preparation of permanent plates, the immersion into glycol methacrylate (GMA) has been performed. The structural organization of leaves belonging to this species reveals stomata in both faces with predominance in the abaxial face (amphihypostomatic leaf). The adaxial face stomata belongs to the diacytic type. The anticlinal walls of the epidermis cells of the adaxial face are sinuous and present irregular thickening. The epidermis of both faces is single layered. Uniserial tectorial trichomes and single celled and multicelled capitate glandular trichomes are present in both faces. The mesophyll is heterogeneous dorsi-ventral. Idioblasts containing inulin crystals are present throughout the foliar plate. The central veins in cross-section, in the medium portion of the foliar plate, have shown a very simple organization, not an outstanding one, where the chlorophyllian palisade parenchyma presents a solution of continuity. The vascular fagots are collateral.
Uniterms:Cunila microcephala. Foliar anatomy. Glandular trichome. Inulin. Lamiaceae.
INTRODUÇÃO
Cunila microcephala Benth., pertencente à família Lamiaceae, é uma erva rasteira, conhecida popularmente como poejinho, nativa da região sul do Brasil, Argentina e Uruguai.
As folhas são brevemente pecioladas, oblongas, obtusas, serrado-crenadas ou inteiras, de ambos os lados glabras e planas. As flores são alvas com pontos roxos, dispostas em capítulos pequenos, globosos, subterminais agregados. Caule herbáceo, procumbente (Martius; Eichler, 1857 - 1864; Pharmacopeia dos Estados Unidos do Brasil, 1926).
O poejinho possui cheiro aromático, sabor quente e fracamente amargo (Pharmacopeia dos Estados Unidos do Brasil, 1926). O óleo essencial de Cunila microcephala apresenta composição química bastante diversificada. Bordignon et al. (1997) constataram a presença de 82,3-85,1% de mentofurano, 2,1-3,8% de limoneno, 3,3-3,9% de b-cariofileno, a-pineno, canfeno, b-pineno, sabineno, b-mirceno, 1-8-cineol, b-ocimeno, g-terpineno, linalol, pulegona, a-terpineol e germacreno D.
As folhas e flores são usadas na forma de chá como estimulante, antiespasmódico e no tratamento de tosses crônicas e infecção respiratória.
O presente trabalho tem por objetivo contribuir com o estudo de Cunila microcephala através da análise da organização estrutural das folhas em microscopia fotônica e microscopia eletrônica de varredura, fornecendo, deste modo, subsídios que venham a contribuir para a identificação farmacognóstica desta espécie.
MATERIAL E MÉTODOS
Obtenção do material botânico
O presente trabalho foi executado a partir de amostras de Cunila microcephala Benth. coletadas na Fazenda Experimental do Canguiri, Setor de Ciências Agrárias da Universidade Federal do Paraná no município de Quatro Barras-PR e identificadas pelo Prof. Dr. Olavo Araújo Guimarães do Departamento de Botânica da Universidade Federal do Paraná.
Ensaios botânicos
Folhas de Cunila microcephala Benth. (Lamiaceae) foram objeto de uma análise da organização estrutural em microscopia fotônica (MF) e microscopia eletrônica de varredura (MEV).
Microscopia óptica
As folhas foram fixadas em FAA 70% (Johansen, 1940) e armazenadas em álcool 70%. Para a montagem de lâminas semipermanentes seguiram-se as técnicas convencionais (Berlyn, Mikshe, 1976). As secções foram realizadas à mão livre. A clarificação foi realizada com hipoclorito de sódio a 20% (Foster, 1949). As secções foram coradas com azul de toluidina 0,05% e montadas em glicerina a 40% (Berlyn e Mikshe, 1976). Para a lutagem das lâminas utilizou-se esmalte de unha incolor. Para a preparação de lâminas permanentes utilizaram-se as técnicas de inclusão em glicol metacrilato (Feder, O'Brien, 1968; Bennet et al., 1976). A microtomização foi realizada em micrótomo rotatório. Na técnica de inclusão em glicol metacrilato, obtiveram-se secções de 7 mm. As secções foram distendidas na lâmina e secadas em mesa térmica. Para coloração utilizou-se azul de toluidina e azul de astra 1% + fucsina básica 0,0125% em solução aquosa (Brito, Alquini, 1996). Para os testes microquímicos, foram obtidas secções à mão livre da região mediana da folha. Utilizou-se cloreto férrico (Johansen, 1940) para comprovação de compostos fenólicos. Os registros fotográficos foram realizados em Fotomicróscopio ZEISS MC80 e Fotomicroscópio ZEISS Standard 20. Escalas micrométricas foram fotografadas e ampliadas nas condições das fotografias. Para a detecção dos cristais de inulina utilizou-se microscópio óptico provido de filtros de luz polarizada (entre nicóis cruzados), mediante a exibição de Cruz de Malta (Oliveira, Akissue, 1989).
Microscopia eletrônica
Para microscopia eletrônica de varredura, folhas inteiras, previamente desidratadas em álcool etílico 90% (duas horas) e álcool absoluto (duas vezes por duas horas) foram submetidas ao ponto crítico com auxílio de CO2 líquido (Balzers CPD 010) para total desidratação. As amostras (faces abaxial e adaxial) foram, então, coladas em suporte metálico com cola a base de prata e submetidas a metalização com ouro, em aparelho Balzers SCD 030, sendo, então, examinadas e fotomicrografadas em Microscópio Eletrônico de Varredura SEM 505 Philips.
RESULTADOS
Caracterização microscópica das folhas
Em vista frontal, a epiderme da lâmina foliar apresenta tricomas de três tipos em ambas as faces, ou seja, tectores unisseriados ao longo das nervuras, glandulares unicelulares e glandulares pluricelulares com oito células (Figuras 1 a 4). As células epidérmicas de ambas as faces apresentam a superfície cuticular ornamentada de estrias (Figuras 1 a 4). A folha é anfi-hipoestomática, com estômatos do tipo diacítico, que predominam na face abaxial (Figuras 5 e 6). As células epidérmicas apresentam paredes anticlinais sinuosas e espessamentos irregulares (Figuras 1 a 6), com grande número de campos de pontoação primária (Figuras 5 e 6).
Em secção transversal a epiderme é uniestratificada (Figura 7) e o mesofilo é heterogêneo, dorsiventral, composto de parênquima paliçádico provido de um estrato de células, células coletoras e parênquima esponjoso com 3 a 4 camadas (Figura 7). Idioblastos contendo cristais de inulina se fazem presentes em toda a extensão do limbo (Figuras 8 e 9).
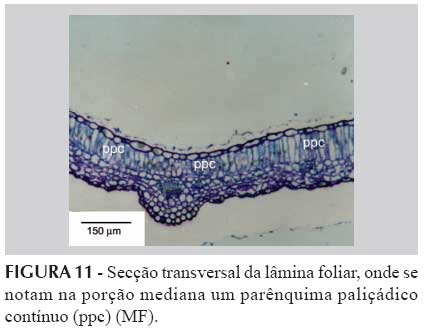
A nervura principal, em secção transversal, apresenta na face abaxial uma cutícula estriada seguida da epiderme e de dois estratos de colênquima de padrão predominantemente lamelar, acompanhando o feixe vascular maior, do tipo colateral (Figura 10). A porção mediana da lâmina foliar voltada para a face adaxial apresenta uma organização bastante simples, com o parênquima paliçádico contínuo (Figura 11). Os testes microquímicos revelaram a presença de compostos fenólicos (Figura 12).
DISCUSSÃO
Os óleos essenciais podem ocorrer em estruturas secretoras especializadas, tais como tricomas glandulares (Lamiaceae), idioblastos (Lauraceae, Piperaceae e Poaceae), canais oleíferos (Apiaceae) ou em bolsas lisígenas ou esquizolisígenas (Pinaceae e Rutaceae) (Simões, Spitzer, 1999). As estruturas anatômicas nas quais os óleos essenciais são depositados evoluíram de células oleíferas, cavidades e canais secretores a tricomas glandulares. Estas estruturas caracterizam linhagens evolutivas de Angiospermas (Gottlieb, Salatino, 1987).
A análise morfo-anatômica da folha de Cunila microcephala Benth. mostrou a presença de estruturas como os tricomas glandulares capitados unicelulares e pluricelulares (com oito células), que secretam óleo essencial. Estas estruturas anatômicas foram descritas por vários autores, como Metcalfe e Chalk (1988), Buvat (1989), Fahn (1990), Pharmacopoea Helvetica (1993), como típicas da família Lamiaceae . Estes autores descrevem tricomas glandulares com uma cabeça composta por quatro a oito células dispostas radialmente a um eixo.
Esta espécie apresentou estômatos do tipo diacítico, como descrito por Metcalfe e Chalk (1988) para a família Lamiaceae.
Testes microquímicos revelaram a presença de compostos fenólicos, que fornecem um indicativo da presença de alguns metabólitos secundários, como, por exemplo, os taninos. Na família Lamiaceae encontra-se um tipo de tanino que possui a capacidade de precipitar proteínas, mas não é apropriado para curtir a pele, conhecido por "tanino das Labiadas".
Idioblastos contendo cristais de inulina encontram-se presentes em toda a extensão do limbo foliar. A inulina ocorre em várias espécies da família Asteraceae e também da família Liliaceae (Oliveira, Akisue, 1989). A inulina pode ser obtida de tubérculos de alcachofra de Jerusalém (Helianthus tuberosus L.), dente-de-leão (Taraxacum officinale Weber), chicória (Cichorium intybus L.) e dália (Dahlia pinnata Cav.) (Hauly, 1991). A British Pharmacopoeia (1993) descreve a inulina como um polissacarídeo obtido de tubérculos de Dahlia variabilis Desf., Helianthus tuberosus L. e de outros gêneros da família Asteraceae. A inulina é um polímero de b-D-frutofuranose. Este polissacarídeo tem sido alvo de muitas pesquisas devido à sua labilidade às hidrólises química e enzimática, que fornecem, principalmente, a frutose e/ou di-D-frutofuranose dianidridos. Estes compostos podem ser usados como agentes edulcorantes em alimentos ou, então, na indústria química para obtenção de outros compostos, como manitol, glicerol, etanol e hidroximetilfurfural (Hauly, 1991). A inulina é usada para avaliação da função renal, predominantemente eliminada na urina pela filtração glomerular, não sendo metabolizada (Martindale, 1989).
A literatura mostra que, embora a Cunila microcephala Benth. esteja descrita na Pharmacopeia dos Estados Unidos do Brasil (1926), poucos são os estudos realizados até o presente. Os mais recentes, sobre a composição química do óleo essencial, foram feitos por Mendes (1994) e Bordignon et al. (1997).
O estudo botânico mostrou a presença de estruturas características da família Lamiaceae e de cristais de inulina, os quais não são mencionados na literatura para esta família.
Esta pesquisa poderá contribuir para a identificação farmacognóstica de Cunila microcephala conhecida popularmente como "poejinho".
Recebido para publicação em 22 de julho de 2003
Aceito para publicação em 08 de dezembro de 2004
- BENNET, H. S. et al. Science and art in preparing tissues embedded in plastic for light microscopy, with special reference to glycol methacrylate, glass knives and simple stains. Staintech, v.55, n.1, p.71-97, 1976.
- BERLYN, G. P.; MIKSCHE, J. P. P. Botanical microtechnique and citochemistry Iowa: State University Press, 1976. 326 p.
- BORDIGNON, S. A. L. et al. The essential oil composition of Cunila microcephala and Cunila fasciculata Phytochemistry, Oxford, v.44, n.7, p.1283-1286, 1997.
- BRITISH Pharmacopoeia. London: HMSO, 1993. v.1, p.357-358.
- BRITO, J. F. A. ; ALQUINI, Y. A new method for staining botanical material embedded in glicol metacrilato (GMA). Arq. Biol. Tecnol, Curitiba, v.39, n.4, p.949-951, 1996.
- BUVAT, R. Ontogeny, cell differention and structure of vascular plants New York: Springer Verlag, 1989. 581 p.
- FAHN, A. Plant anatomy. Madrid: Pergamon Press, 1990. 599 p.
- FEDER, N.; BRIEN, T. P. Plant. microthecnique: some principles and new methods. Amer. J. Bot., v.55, n.1, p.123-142, 1968.
- FOSTER, A. S. Practical plant anatomy New York: Van Nostrand, 1949. 228 p.
- GOTTLIEB, O. R.; SALATINO, A. Função e evolução de óleos essenciais e de suas estruturas secretoras. Cienc. Cult., v.39, n.8, p.707-715, 1987.
- HAULY, M. C. O. Inulina de dália; extração e avaliação da hidrólise e dos efeitos biológicos dos subprodutos. Curitiba, 1991. 185 p. [ Tese de Doutorado Departamento de Bioquímica, Universidade Federal do Paraná.] .
- JOHANSEN, D. A. Plant microtechnique New York: McGraw Hill Book, 1940. 523 p.
- MARTINDALE. The Extra Pharmacopoeia. 29. ed. London: The Pharmaceutical Press, 1989. 1896 p.
- MARTIUS, C. F. P. de; EICHLER, A. G. Flora brasiliensis: enumeratio plantarum in brasilia hactenus detectarum quas suis aliorumque botanicorum studiis descriptas et methodo naturali digestas partim icone illustratas. Monachii: Frid. Fleischer, 1857 - 1864. v.8, pt.1, p.166.
- MENDES, H. B. Estudo fitoquímico da espécie Cunila microcephala Benth. Labiatae. Curitiba, 1994. 96 p. [ Tese de Mestrado Departamento de Botânica, Universidade Federal do Paraná] .
- METCALFE, C.R.: CHALK, L. Anatomy of the dicotyledons Oxford at the Clarendon Press, l988. 276 p.
- OLIVEIRA, F.; AKISUE, G. Fundamentos de farmacobotânica São Paulo: Livraria Atheneu Editora, 1989. 221 p.
- PHARMACOPOEA Helvetica. 7. ed. Berne: Département Fédéral de l'Intérieur, 1993. v. 4. 103. pag. irreg.
- PHARMACOPEIA dos Estados Unidos do Brasil. São Paulo: Ed. Nacional, 1926. p. 742-743.
- SIMÕES, C. M. O.; SPITZER, V. Óleos voláteis. In: SIMÕES, C. M. O. et al Farmacognosia da planta ao medicamento Porto Alegre: UFRGS, 1999. p.387-415.
Datas de Publicação
-
Publicação nesta coleção
29 Nov 2005 -
Data do Fascículo
Dez 2004
Histórico
-
Aceito
08 Dez 2004 -
Recebido
22 Jul 2003