Resumos
Os materiais cerâmicos têm sido amplamente estudados durante várias décadas para utilização em Células a Combustível, principalmente em Células a Combustível de Óxido Sólido de Temperatura Alta. Entretanto, não tendo sido superados completamente todos os problemas decorrentes da alta temperatura de operação desses dispositivos, continuam os trabalhos de pesquisa e de desenvolvimento na busca de materiais compatíveis para operacionalizar esses dispositivos em altas temperaturas, assim como em temperaturas intermediárias. Por esses motivos, muitos esforços têm sido concentrados para minimizar os problemas que ocorrem com esses materiais e a atenção vem sendo direcionada para a seleção e obtenção de materiais cerâmicos utilizados na Célula a Combustível de Óxido Sólido de Temperatura Intermediária. Seguindo este contexto, o presente trabalho tem como objetivo apresentar as principais características dos pós de Nd1-XSrXMnO3 e La1-XSrXCo1-YFeYO3, que constituem o eletrodo catódico. Os pós foram obtidos pelo método cerâmico de mistura de pós e pela técnica dos citratos, respectivamente. Os pós desses materiais foram caracterizados e analisados por técnicas químicas, físicas e microestruturais. Como principal resultado, verificou-se que a homogeneidade das partículas destes pós é adequada para a preparação de suspensões que podem ser aplicadas no eletrólito sólido.
Célula a combustível de óxido sólido; catodo; mistura de pós; técnica dos citratos
The ceramic materials have been studied during some decades for use in Fuel Cells, mainly in High Temperature Solid Oxide Fuel Cells. However, not having been surpassed completely all the decurrently problems of the high operating temperature of the devices developed currently, continue the works of research and development in the search of compatible materials to operate these devices in high temperatures, as well as in intermediate temperatures has been considered. For these reasons, many efforts was concentrated to minimize the problems that occur with these materials and the attention comes being directed for the election and attainment of ceramic materials used in the Intermediate Temperature Solid Oxide Fuel Cell. Following this context, the present work has as objective to present the main characteristics of Nd1-X SrX MnO3 and La1-X SrX Co1-Y FeY O3, powders that they constitute the cathodic electrode. The mentioned methods by powders mixture and citrates technique were used for obtaining these powders, respectively. The powders obtained were characterized and analyzed for chemical, physical and microstructural techniques. As main result, it was verified that the homogeneity of particles is adequate for the preparation of suspensions that can be applied in the solid electrolyte.
Solid oxide fuel cell; cathode; powders mixture; citrates technique
Síntese e caracterização dos pós de Nd1-xSrxMnO3 e La1-xSrxCo1-yFeyO3
Synthesis and characterization of Nd1-xSrxMnO3 and La1-xSrxCo1-yFeyO3 powders
R.A. Vargas; R. Chiba; M. Andreoli; E.S.M. Seo
Laboratório de SOFC - Insumos e Componentes Centro de Ciência e Tecnologia de Materiais (CCTM) Instituto de Pesquisas Energéticas e Nucleares (IPEN) Av. Prof. Lineu Prestes, 2.242, Cidade Universitária (USP), São Paulo, SP, Brasil. CEP: 05508-900 e-mails: ravargas@ipen.br, rchiba@ipen.br, mandreol@ipen.br, esmiyseo@ipen.br
RESUMO
Os materiais cerâmicos têm sido amplamente estudados durante várias décadas para utilização em Células a Combustível, principalmente em Células a Combustível de Óxido Sólido de Temperatura Alta. Entretanto, não tendo sido superados completamente todos os problemas decorrentes da alta temperatura de operação desses dispositivos, continuam os trabalhos de pesquisa e de desenvolvimento na busca de materiais compatíveis para operacionalizar esses dispositivos em altas temperaturas, assim como em temperaturas intermediárias. Por esses motivos, muitos esforços têm sido concentrados para minimizar os problemas que ocorrem com esses materiais e a atenção vem sendo direcionada para a seleção e obtenção de materiais cerâmicos utilizados na Célula a Combustível de Óxido Sólido de Temperatura Intermediária. Seguindo este contexto, o presente trabalho tem como objetivo apresentar as principais características dos pós de Nd1-XSrXMnO3 e La1-XSrXCo1-YFeYO3, que constituem o eletrodo catódico. Os pós foram obtidos pelo método cerâmico de mistura de pós e pela técnica dos citratos, respectivamente. Os pós desses materiais foram caracterizados e analisados por técnicas químicas, físicas e microestruturais. Como principal resultado, verificou-se que a homogeneidade das partículas destes pós é adequada para a preparação de suspensões que podem ser aplicadas no eletrólito sólido.
Palavras chaves: Célula a combustível de óxido sólido, catodo, mistura de pós, técnica dos citratos.
ABSTRACT
The ceramic materials have been studied during some decades for use in Fuel Cells, mainly in High Temperature Solid Oxide Fuel Cells. However, not having been surpassed completely all the decurrently problems of the high operating temperature of the devices developed currently, continue the works of research and development in the search of compatible materials to operate these devices in high temperatures, as well as in intermediate temperatures has been considered. For these reasons, many efforts was concentrated to minimize the problems that occur with these materials and the attention comes being directed for the election and attainment of ceramic materials used in the Intermediate Temperature Solid Oxide Fuel Cell. Following this context, the present work has as objective to present the main characteristics of Nd1-XSrXMnO3 and La1-XSrXCo1-YFeYO3, powders that they constitute the cathodic electrode. The mentioned methods by powders mixture and citrates technique were used for obtaining these powders, respectively. The powders obtained were characterized and analyzed for chemical, physical and microstructural techniques. As main result, it was verified that the homogeneity of particles is adequate for the preparation of suspensions that can be applied in the solid electrolyte.
Keywords: Solid oxide fuel cell, cathode, powders mixture, citrates technique.
1 INTRODUÇÃO
A Célula a Combustível (Fuel Cell: FC), é um dispositivo eletroquímico que converte diretamente a energia química fornecida por um combustível (hidrogênio) e por um oxidante (oxigênio) em energia elétrica e vapor de água. Este vapor de água, pode nos fornecer energia térmica (calor) para diversas finalidades, inclusive para gerar mais energia elétrica (co-geração). As Células a Combustível (CaC) possuem a eficiência termodinâmica não limitada pelo "Ciclo de Carnot" e são sistemas extremamente silenciosos e sem aparente agressão ao meio ambiente, se comparados com os processos convencionais de geração de energia elétrica. Essa vantagem depende, entretanto, de como os combustíveis que serão utilizados podem ser reformados para produzir hidrogênio (H2) e dióxido de carbono (CO2) [1, 2].
Cada unidade de uma CaC, como apresentada na Figura 1, é constituída de três componentes básicos: o eletrólito, o eletrodo catódico (catodo) e o eletrodo anódico (anodo) [1, 2].
Os componentes presentes nas diferentes tecnologias de CaC são fabricados com diversos materiais (cerâmicos, metálicos, poliméricos e compósitos). Os materiais cerâmicos têm sido amplamente estudados durante várias décadas para utilização em CaC principalmente na Célula a Combustível de Óxido Sólido de Temperatura Alta: CaCOS-TA (High Temperature Solid Oxide Fuel Cell: HTSOFC), que opera entre 800 e 1000 °C. Entretanto, não tendo sido superados completamente todos os problemas de materiais que suportem a alta temperatura de operação, continuam o desenvolvimento e a busca de novos materiais que sejam compatíveis para operacionalizar esses dispositivos em altas temperaturas, bem como na busca de materiais que permitam a operação em temperaturas mais baixas [2, 3].
Por esses motivos, muitos esforços têm sido concentrados para minimizar os problemas de degradação, principalmente quanto à estabilidade do eletrólito e dos eletrodos, e neste sentido, a atenção vem sendo direcionada para a seleção e obtenção de materiais cerâmicos utilizados na Célula a Combustível de Óxido Sólido de Temperatura Intermediária: CaCOS-TI (Intermediate Temperature Solid Oxide Fuel Cell: ITSOFC), que opera entre 500 e 800 °C. A Figura 2 mostra o esquema de funcionamento que serve tanto para uma CaCOS-TA como para uma CaCOS-TI [3-5].
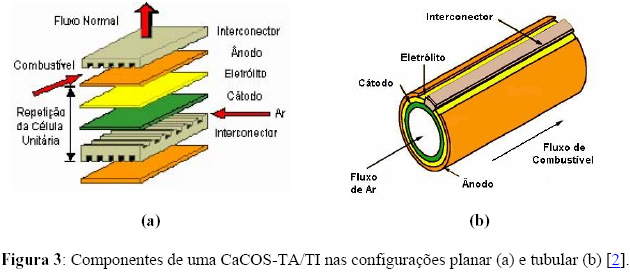
As CaCOS-TA/TI possuem quatro componentes básicos e de grande importância para o seu correto funcionamento: o eletrólito, o eletrodo catódico, o eletrodo anódico e o interconector. Além destes componentes, não podemos esquecer de mencionar o "selante" que está sendo estudado atualmente por diversos pesquisadores, com a finalidade de diminuir alguns dos problemas relacionados com a alta temperatura de operação dos dispositivos atuais. Existem algumas configurações geométricas em estudo para os componentes deste tipo de célula, sendo as configurações planar e tubular as mais consolidadas até o presente momento. A Figura 3a mostra o esquema de uma configuração planar e a Figura 3b mostra o esquema de uma configuração tubular para uma CaCOS-TA ou CaCOS-TI [2].
Os materiais cerâmicos utilizados nas CaCOS-TA/TI, possuem estruturas similares às estruturas conhecidas como perovskitas (ABO3), como apresentado na Figura 4; ademais, devem ser chamadas de pseudo-perovskitas (Figura 5b), pois é a denominação mais adequada para representar a estrutura perovskita em sua forma distorcida [5].
As estruturas dessa família podem ser dopadas, em ambos os sítios A e B, com alguns tipos de cátions. Os cátions com grande raio iônico (por exemplo: Sr e Ca) substituem preferencialmente os sítios A e os cátions com pequeno raio iônico (por exemplo: Co, Fe, Ni, Mn e Cr) preferem ocupar os sítios B [5, 6].
É interessante notar através da Figura 4, que existe a formação de um octaedro, formado por átomos de "O" (coloração vermelha) que estão localizados no centro de cada uma das seis faces da célula unitária. Estes octaedros, quando estão na forma regular, representam à estrutura típica da perovskita (Figuras 4 e 5a) e quando estão em uma forma distorcida, representam à estrutura pseudo-peroviskita (Figura 5b) [6].
Tradicionalmente, as estruturas pseudo-perovskitas, baseadas no sistema La1-xSrxMnO3 (Manganita de Lantânio Dopada com Estrôncio: LSM) são reconhecidas como um dos primeiros materiais catódicos promissores para utilização em CaCOS-TA e também o mais consolidado, devido ao seu excelente desempenho eletroquímico, as suas estabilidades química e térmica e as suas compatibilidades química e mecânica com o eletrólito sólido de Zircônia Estabilizada com Ítria (YSZ) [3, 7].
Entretanto, o material catódico tradicional, LSM, apresenta alta resistência de condução iônica em temperaturas mais baixas devido à sua pobre condução dos íons oxigênio e, além disso, o seu desempenho como eletrodo das células é melhorado somente se existirem duas fases no catodo; uma formada pela interface do compósito YSZ e a outra, de LSM [7].
Devido principalmente a esses problemas mencionados, a problemas relacionados ao custo de manufatura, da escolha limitada de materiais e da degradação dos componentes das células que operam em alta temperatura, vários esforços têm-se concentrado no uso de materiais que operam em temperaturas intermediárias tais como sistemas que contém neodímio (Nd), praseodímio (Pr), cério (Ce), gadolínio (Gd), samário (Sm), entre outros [5, 8].
A operação da célula em temperaturas intermediárias reduziria extremamente os problemas associados com a fabricação e com os materiais envolvidos, melhorando a confiabilidade da própria célula durante uma operação por um período mais prolongado. Algumas CaCOS-TI que utilizam metanol direto como combustível e operam em torno de 500 °C estão contribuindo significativamente para as pesquisas nesta área. A operação em temperaturas intermediárias necessita da seleção de materiais apropriados para todos os seus componentes, principalmente para a interconexão [8, 9].
Os eletrodos para CaCOS-TI, como já mencionado anteriormente, devem atender os requisitos necessários para serem compatíveis com o eletrólito sólido [10]. Neste contexto, este trabalho é uma contribuição ao processo de obtenção de dois materiais cerâmicos, que são utilizados como eletrodos catódicos em CaCOS-TI. O objetivo principal deste trabalho é, portanto, a preparação e a caracterização de pós de Nd1-xSrxMnO3 (Manganita de Neodímio Dopada com Estrôncio: NSm) obtida pelo método cerâmico de mistura de pós e de La1-XSrXCo1-YFeYO3 (Cobaltita Férrica de Lantânio Dopada com Estrôncio: LSCF) obtida pela técnica dos citratos.
O composto NSM é um material de estrutura do tipo pseudo-perovskita, onde A e B são terras raras (Nd) e metal de transição (Mn), respectivamente. A literatura mostra que o NSM é um condutor com alta condutividade dos íons negativos de oxigênio (O2-) e com boa propriedade eletrônica, operando a temperaturas intermediárias em combinação com eletrólitos à base de cério, gadolínio, entre outros [11].
O composto LSCF também é um material de estrutura do tipo pseudo-perovskita. Dentre as várias aplicações, destacam-se como: material catódico em CaC [12-15], como membrana de separação dos íons e das moléculas de oxigênio [13], como catalisador para reações de combustão de hidrocarbonetos e de redução de peróxido de hidrogênio em soluções alcalinas [16] e como membranas cerâmicas para redução parcial do metano para síntese de gás [17].
Se comparado com outro material alternativo para a mesma função, o La1-xSrxCoO3 (Cobaltita de Lantânio Dopada com Estrôncio: LSCO), o potencial uso do LSCF, como eletrodo catódico da CaCOS-TI, se deve ao valor elevado do coeficiente de expansão térmica do LSCO e sua reatividade com a YSZ abaixo de 900 ºC. Neste sentido, o LSCF é mais atrativo, pois a dopagem com o Fe3+ nos sítios de Cobalto (Co) pode reduzir o coeficiente de expansão térmica [12, 14].
Dentre as diferentes rotas de obtenção encontradas na literatura para o composto de NSM, o método cerâmico de mistura de pós (carbonatos ou óxidos) [12, 18] se mostrou um dos mais adequados para se obter pós com características físicas, químicas e microestruturais adequadas. Para o composto de LSCF, dentre as diferentes rotas de obtenção citadas na literatura, destacam-se as técnicas sol gel [19] e citratos [10, 18-20].
O método sol gel é adequado para obtenção de pós com características adequadas [19], entretanto, os precursores alcoóxidos sol gel são bastante sensíveis à umidade e a manutenção da sua característica de estado é curta, de forma que, normalmente, segundo a literatura, provoca trincas nos filmes poliméricos durante a etapa de secagem. Nos últimos anos, a técnica dos citratos, derivada do método PECHINI [21], vem sendo amplamente adotada para obtenção de precursores poliméricos para deposição em substratos [19].
Portanto, utilizou-se o método cerâmico de mistura de pós para a obtenção do NSM e a técnica dos citratos para obtenção de LSCF, caracterizando os produtos obtidos na forma de pós e com o objetivo de conseguir pós com características adequadas para a preparação de suspensões.
A principal contribuição deste artigo é apresentar algumas características dos pós de Nd1-XSrXMnO3 para x = 0,50, ou seja, Nd0,50Sr0,50MnO3 e de La1-XSrXCo1-YFeYO3, para x = 0,40 e y = 0,80, ou seja, La0,60Sr0,40Co0,20Fe0,80O3; valores estes, que foram definidos seguindo a literatura técnica referente a estes dois materiais. Para o caso do LSCF, verificou-se que as melhores características para uso em CaCOS-TI, citadas na literatura técnica, é para concentrações molares baixas ou altas de lantânio e de estrôncio, baixas de cobalto e altas de ferro [10, 12, 14].
Dentro de todo o contexto apresentado, pretende-se que as informações apresentadas contribuam na literatura técnica relativa, pois são poucos os trabalhos publicados e divulgados para estes compostos no Brasil, especificamente sobre as características físicas, químicas e microestruturais dos pós desses materiais.
2 MATERIAIS E MÉTODOS
2.1 Mistura de Pós
O composto NSM foi obtido pelo método cerâmico de mistura de pós, demonstrado simplificadamente no fluxograma da Figura 6. Como matérias-primas, utilizaram-se os carbonatos de neodímio - Nd2(CO3)3 com aproximadamente 98,5 % de pureza, de estrôncio - SrCO3 com 99,9 % de pureza e de manganês - MnCO3 também com 99,9 % de pureza. Os três materiais foram secados em estufa. Após o período de secagem do material, misturaram-se os carbonatos com a presença de álcool isopropílico para a realização de um processo de moagem.
A amostra obtida de NSM foi calcinada a 1100 °C. Após a etapa de calcinação e antes da realização das análises de caracterização do material na forma de pós, a amostra foi submetida a uma nova moagem e posteriormente peneirada para a desaglomeração de suas partículas. Nessas condições, foi determinada a "massa específica" através da técnica de Picnometria por Gás Hélio (PGH), que é uma medida representativa da densidade real do material.
O material foi então submetido a Análise Térmica Gravimétrica (ATG) e a Análise Térmica Diferencial (ATD) para a identificação dos compostos voláteis da reação. Tanto para a ATG quanto para a ATD foram utilizadas a temperatura de 1300 °C, com a amostra exposta em atmosfera de ar sintético.
Em seguida, realizaram-se as análises de Fluorescência de Raios X (FRX) para a identificação dos elementos constituintes em sua composição, Difração de Raios X (DRX) para a identificação de suas estruturas cristalinas, Distribuição Granulométrica (CILAS) para a identificação do tamanho médio de partícula e Microscopia Eletrônica de Varredura (MEV) para a identificação, através das micrografias, a morfologia das partículas.
2.2 Técnica dos Citratos
O composto LSCF foi obtido a partir de uma solução que foi preparada de acordo com a técnica dos citratos, demonstrada simplificadamente nos fluxogramas (a) e (b) da Figura 7. Esta técnica, consiste na formação de um quelato citrato, que nada mais é do que um íon metálico formado pela reação entre ácido cítrico e a solução dos cátions metálicos, na forma de nitratos, cloretos, oxalatos, acetatos ou hidróxidos. A adição de álcool polihidroxílico, por exemplo, etileno glicol, e a eliminação do excesso de solvente por elevação da temperatura, promovem a formação de uma resina polimérica de alta viscosidade que impede a segregação dos cátions durante a decomposição térmica. A oxidação ocorre simultaneamente à saída da matéria orgânica, gerando uma fase cristalina com homogeneidade química.
Para o caso do LSCF foram realizadas duas experiências distintas. Na primeira experiência de síntese, denominada de LSCF01, os nitratos de cobalto, de ferro e de lantânio nas proporções requeridas e o carbonato de estrôncio, foram dissolvidos em ácido nítrico. O ácido cítrico e o etileno glicol foram misturados em proporções adequadas (60:40) respectivamente e adicionados na solução de nitratos. Após a neutralização com hidróxido de amônio, a solução foi aquecida a 100 ºC, ocorrendo uma reação de condensação formando um éster e liberando água. O gel polimérico amorfo é aquecido a 400 ºC para decomposição dos nitratos e das substâncias orgânicas (poliesterificação). Na seqüência, foi levado à calcinação à uma temperatura de 800 ºC e posteriormente a 1000 ºC, para eliminação do carbono residual.
O segundo experimento, denominado de LSCF02 consistiu no uso de todos os precursores à base de nitratos dissolvidos em água destilada à 100 ºC, sob agitação. Depois da completa dissolução dos sais, as quantidades acima citadas de ácido cítrico e etileno glicol foram utilizadas como complexantes. O pH da solução foi ajustado em "2" com a adição de ácido nítrico. A solução foi aquecida à temperatura aproximadamente 200 ºC tornando-a viscosa devido à liberação de água e outros materiais voláteis. Seguiu-se as etapas de poliesterificação e de calcinação. Para estas duas etapas finais, foram adotadas as mesmas condições da síntese do LSCF01.
Para o LSCF01, os pós foram caracterizados empregando-se as técnicas de Picnometria por Gás Hélio (PGH), Análise de Fluorescência de Raios X (FRX), Análise Térmica Gravimétrica (ATG), Calorimetria Diferencial de Varredura (CDV), Distribuição Granulométrica (CILAS), Difração de Raios X (DRX) e Microscopia Eletrônica de Varredura (MEV). No caso do LSCF02, foram realizadas as análises de DRX e MEV.
3 RESULTADOS E DISCUSSÃO
3.1 Densidades
Para os pós de NSM, foi determinada a massa específica via picnometria de gás hélio, que é uma medida representativa da densidade real do material. O valor de 5,48 g/cm3 foi determinado com um desvio padrão de ± 0,01 g/cm3 e corresponde a 86,43 % da densidade teórica que é de aproximadamente 6,34 g/cm3.
Para os pós de LSCF, foi determinado o valor de 5,12 g/cm3 para a densidade real, também com um desvio padrão de ± 0,01 g/cm3 e corresponde a 80,50 % da densidade teórica que é de 6,36 g/cm3.
Uma observação importante é notar que o valor da densidade real referente ao material composto de LSCF é inferior ao material composto de NSM. O valor da densidade teórica é muito próximo em relação aos dois materiais. Os valores obtidos são apresentados na Tabela 1.
3.2 Fluorescência de Raios X
A composição química foi determinada por Fluorescência de Raios X (FRX) para os pós sintetizados, com a finalidade de identificar a estequiometria real dos elementos constituintes em sua composição. Para os pós de NSM foi encontrada a estequiometria Nd0,42Sr0,58MnO3; muito próxima à estequiometria calculada teoricamente (Nd0,50Sr0,50MnO3). Para os pós de LSCF foi encontrada a estequiometria La0,55Sr0,45Co0,30Fe0,70O3; também muito próxima à estequiometria calculada teoricamente (La0,60Sr0,40Co0,20Fe0,80O3). Os resultados das análises químicas, apresentados na Tabela 2, mostram a formação do NSM com composição igual a Nd0,42Sr0,58MnO3 e a formação LSCF com composição igual a La0,55Sr0,45Co0,30Fe0,70O3.
3.3 Análises Térmicas
Para a caracterização térmica dos pós de NSM foram realizadas Análise Térmica Gravimétrica (ATG) e Análise Térmica Diferencial (ATD). A curva ATG, obtida com as variáveis "perda de massa (%) x temperatura (ºC)" é apresentada na Figura 8(a), permite diferenciar três etapas distintas de decomposição dos elementos químicos. Essas mudanças distintas referem-se a:
·Entre 100 ºC e 380 °C, existe uma relativa perda de massa, que corresponde à perda da água de hidratação presente no material. Esta perda é de aproximadamente 5 % em massa;
·Entre 380 ºC e 550 °C, existe decomposição dos carbonatos formando CO, CO2 e alguns carbonatos intermediários. A liberação dos produtos gasosos formados é em torno de 9 % em massa;
·Entre 550 ºC e 880 °C, existe uma relativa decomposição dos carbonatos intermediários a um produto final estável de Nd0,42Sr0,58MnO3 e a liberação dos gases CO e CO2 com uma perda de aproximadamente 9 % em massa.
A partir da curva ATD, localizada na Figura 8(b), verificou-se a presença de dois picos exotérmicos e de um pico endotérmico. O primeiro pico exotérmico, ocorre aproximadamente a 280 °C, e refere-se principalmente à eliminação da água de hidratação. O segundo pico exotérmico, ocorre à cerca de 860 °C e se relaciona à decomposição dos carbonatos intermediários presentes e a transformação a óxidos de seus elementos. O pico endotérmico que ocorre a 490 °C refere-se à decomposição dos carbonatos em CO e CO2 e dos carbonatos intermediários.
Para a caracterização térmica dos pós de LSCF foram realizadas ATG e Calorimetria Diferencial de Varredura (CDV). Nestas análises foram avaliados os comportamentos térmicos do gel preparado à temperatura entre 80 ºC e 100 ºC. A curva ATG, apresentada na Figura 9(a) e a curva CDV apresentada na Figura 9(b), da amostra de LSCF permitem diferenciar quatro etapas distintas de decomposição. Partindo-se de uma massa inicial de 11,280 mg do material, a curva ATG revela as seguintes etapas de decomposição:
·Entre 25 ºC e 150 ºC, existe uma relativa perda de massa equivalente a 1,5 mg, devido à liberação de moléculas de água e traços de íons nitrato;
·Entre 150 ºC e 380 ºC, ocorre a liberação de excesso de água e de íons nitrato com uma perda de 3,5 mg. Nesta fase, ocorre a formação da resina polimérica de coloração "marrom avermelhada" composta de La, Co, Fe e C;
·Entre 380 ºC e 480 ºC, ocorre uma pequena perda de massa de aproximadamente 1,3 mg, resultante da decomposição do composto SrCO3. Segundo JIN. et.al. (13), a perda de massa existente nesta faixa de temperatura é devido à decomposição do SrCO3;
· Entre 480 ºC e 850 ºC, ocorre uma perda de massa da decomposição total do polímero com a liberação do carbono residual em aproximadamente 1,0 mg.
A análise de CDV, Figura 9(b), foi conduzida em atmosfera de argônio. Os dois picos endotérmicos entre 100 ºC e 125 ºC, estão associados com a liberação de moléculas de água e de traços de íons nitrato. Um pico endotérmico menos acentuado, a cerca de 150 ºC está relacionado com a liberação do excesso de água e de íons nitrato. A 275 ºC, a endotermia é observada devido à decomposição da resina polimérica e a 360 ºC, conforme os resultados da ATG, a reação é endotérmica devido à decomposição do SrCO3.
3.4 Distribuição Granulométrica
Na análise granulométrica por espalhamento de feixe de laser (CILAS), foi determinado o diâmetro médio equivalente por massa acumulada dos pós sintetizados de NSM e LSCF, como demonstrado na Figura 10. Os resultados obtidos mostram que para os pós de NSM, o diâmetro médio é de aproximadamente 1,60 mm; e para os pós de LSCF é de aproximadamente 0,95 mm. Tais granulometrias, são adequadas, de acordo com a literatura, ao processamento cerâmico desses materiais para a preparação de suspensões.
3.5 Difração de raios X
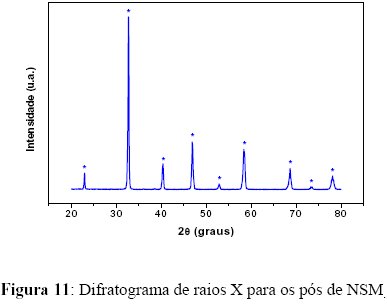
As Figuras 11 e 12 apresentam os difratogramas dos pós de NSM e de LSCF (LSCF1a, LSCF1b e LSCF02) respectivamente. A caracterização por DRX para os pós de NSM foi baseada no trabalho de GHARBAGE et al. [22]. Para as concentrações de neodímio (Nd) e de estrôncio (Sr) utilizadas neste trabalho; é esperado obter uma estrutura ortorrômbica com parâmetros de rede de aproximadamente: a = 5,454 Å, b = 5,446 Å e c = 7,730 Å. Os resultados obtidos utilizando o difratograma foram de a = (5,43±0,02) Å, b = (5,46±0,02) Å e c = (7,71±0,06) Å, comprovando a formação da estequiometria Nd0,42Sr0,58MnO3. A partir do resultado obtido por DRX, como mostra a Figura 11, e comparando com os trabalhos de KOSTOGLOUDIS et al. [11] e ARUNA et al. [23], pode-se comprovar a formação de uma estrutura pseudo-perovskita ortorrômbica para o material composto de Nd0,42Sr0,58MnO3.
O difratograma da amostra LSCF01, apresenta a presença de duas fases, sendo uma de LSCF e outra de Sr2FeO4 (LSCF01a). Esta mesma amostra foi submetida à dissolução nítrica e posterior secagem e calcinação a 800 ºC, observando que não houve a formação da fase Sr2FeO4 (LSCF01b). O difratograma da amostra LSCF02 apresenta apenas a presença da fase LSCF. Portanto, conforme os resultados de DRX para as amostras LSCF (Figura 12) e baseando-se nos trabalhos de QIU. et al. [12], de TAI. et al. [10] e de
JIN. et al. [20], verificou-se a formação somente de uma fase pseudo-perovskita ortorrômbica.
3.6 Microscopia Eletrônica de Varredura
Na análise de Microscopia Eletrônica de Varredura (MEV) é observada a morfologia das partículas dos pós obtidos de NSM e LSCF após a etapa de calcinação. A morfologia apresentada na Figura 13 para os pós de NSM mostra nitidamente a homogeneidade das partículas. Por sua vez, na Figura 14(a), observa-se uma boa homogeneidade das partículas dos pós de LSCF01 e na Figura 14(b) das partículas dos pós de LSCF02.
4 CONCLUSÕES
As principais conclusões estabelecidas para os pós de NSM são:
· Os resultados das análises térmicas permitiram observar que a formação do composto estequiométrico Nd0,42Sr0,55MnO3 estável se inicia à temperaturas acima de 880 °C;
· Os dados de caracterização dos pós de NSM obtido pela rota de mistura de pós mostraram que é possível a obtenção de compostos de NSM à temperatura de até 1100 °C;
· Durante a calcinação a 1100 ºC dos precursores à base de carbonatos, forma-se a estrutura pseudo-perovskita ortorrômbica;
· Verificou-se a homogeneidade das partículas dos pós de NSM obtido via método cerâmico de mistura de pós, possibilitando uma melhor performance na etapa de processamento para a preparação de suspensões cerâmicas;
As principais conclusões estabelecidas para os pós de LSCF são:
· Partindo-se do precursor SrCO3, as análises por DRX demonstraram a formação de duas fases. Portanto, a metodologia adotada a partir de soluções de nitratos de todos os elementos é mais adequada, formando apenas a fase LSCF;
· Durante a calcinação a 1000 ºC dos precursores à base de nitratos, forma-se a estrutura pseudo-perovskita ortorrômbica;
· O diâmetro médio de partícula, bem como a morfologia destes pós, são adequados para preparação de suspensões cerâmicas.
No geral, verificou-se que a homogeneidade das partículas dos pós de NSM e LSCF é adequada para a preparação de suspensões cerâmicas que podem ser aplicadas na forma de filmes finos na superfície do eletrólito sólido em CaCOS-TI.
5 AGRADECIMENTOS
Os autores agradecem a todos os profissionais e amigos do CCTM, do CQMA e do PROCEL, pertencentes ao IPEN pelas análises realizadas em seus laboratórios. Os autores agradecem ao CNPq (Conselho Nacional de Desenvolvimento Científico e Tecnológico), ao CTENERG (Fundo Setorial de Energia), a Rede PaCOS (Rede de Pilhas a Combustível de Óxido Sólido) pelo apoio financeiro.
6 BIBLIOGRAFIA
Data de envio: 31/01/06 Data de aceite: 08/07/06
- [1] KORDESCH, K., SIMADER, G., Fuel Cells and Their Applications, 1 ed., New York-Cambridge, 1996.
- [2] BLOMEN, J.M.J., MUGERWA, M.N., Fuel Cell Systems, 1 ed. New York-Plenum Press, 1993.
- [3] MINH, N.Q., "Solid Oxide Fuel Cell Technology - Features and Applications", Solid State Ionics, v. 174, n. 1-4, pp. 271-277, Oct. 2004.
- [4] CHOY, K., BAI, W., CHAROJROCHKUL, S., STEELE, B.C.H., "The Development of Intermediate-temperature Solid Oxide Fuel Cells for the next Millennium", Journal of Power Sources, v. 71, n. 1-2, pp. 361-369, Mar. 1998.
- [5] CHIBA, R., "Obtençăo e Caracterizaçăo de Manganito de Lantânio Dopado com Estrôncio para Aplicaçăo em Células a Combustível de Óxido Sólido", Dissertaçăo M.Sc. em Tecnologia Nuclear Materiais, Instituto de Pesquisas Energéticas e Nucleares, IPEN/CNEN-SP, pp. 67, Săo Paulo, Maio 2005.
- [6] CHEMBYTES E-ZINE, http://www.chemsoc.org/chembytes/ezine/2001/dann_dec01.htm, acessado em fevereiro de 2006.
- [7] STEVENSON, J.W., ARMSTRONG, T.R., CARNEIM, R.D., PEDERSON, W.J., WEBER, J., " Electrochemical Properties of Mixed Conducting Perovskites La1xMxCo1yFeyO3(M = Sr, Ba, Ca)", Jornal of The Electrochemical Society, v. 143, n. 9, pp. 2722-2729, Sep. 1996.
- [8] SINGHAL, S.C., "Advances in Solid Oxide Fuel Cell Technology", Solid State Ionics, v. 135, n. 1-4, pp. 305-313, Nov. 2000.
- [9] HUIJSMANS, J.P.P., VAN BERKEL, F.P.F., CHRISTIE, G.M., "Intermediate Temperature SOFC - A Promise for the 21st Century", Journal of Power Sources, v. 71, n. 1-2, pp. 107-110, Mar. 1998.
- [10] TAI, L.W., NASRALLAH, M.M., ANDERSON, H.U., SPARLING, D.M., SEHLIN, S.R., "Structure and Electrical Properties of La1−xSrxCo1−yFeyO3 Part 1. The system La0.8Sr0.2Co1−yFeyO3", Solid State Ionics, v. 76, n. 3-4, pp. 259-271, Mar. 1995.
- [11] KOSTOGLOUDIS, G.CH., VASILAKOS, N., FTIKOS, J., "Preparation and Characterization of Pr1-xSrxMnO3ąδ (x=0, 0.15, 0.3, 0.4, 0.5) as a Potential SOFC Cathode Material Operating at Intermediate temperatures (500-700°C)", Journal of European Ceramic Society, v. 17, n. 12, pp. 1513-1521, Feb. 1997.
- [12] QIU, L., ICHIKAWA, T., HIRANO, A., IMANISHI, N., TAKEDA, Y.,"Ln1−xSrxCo1−yFeyO3−δ (Ln=Pr, Nd, Gd; x=0.2, 0.3) for the Electrodes of Solid Oxide Fuel Cells", Solid State Ionics, v. 158, n. 1-2, pp. 55-65, Feb. 2003.
- [13] STEELE, B.C.H., "Oxygen ion Conductors and their Technological Applications", Material Science Engineering B, v. 13, n. 2, pp. 79-87, Mar. 1992.
- [14] WANG, S., KATSUKI, M., DOKIYA, M., TASHIMOTO, T., "High Temperature Properties of La0.6Sr0.4Co0.8Fe0.2O3−δ Phase Structure and Electrical Conductivity", Solid State Ionics, v. 159, n. 1-2, pp. 71-78, Mar. 2003.
- [15] WANG, S., KATO, T., NAGATA, S., HONDA, T., TANEKO, T., IWASHITA, N., DOKIYA, M., "Performance of a La0.6Sr0.4Co0.8Fe0.2O3Ce0.8Gd0.2O1.9Ag Cathode for Ceria Electrolyte SOFCs", Solid State Ionics, v. 146, n. 3-4, pp. 203-210, Feb. 2002.
- [16] ZHANG, H.M., SHIMIZU, Y., TERAOKA, Y., MIURA, N., YAMAZOE, N., IWASHITA, N., "Oxygen sorption and catalytic properties of La1−xSrxCo1−yFeyO3 Perovskite-type Oxides", Journal of Catalysis, v. 121, n. 2, pp. 432-440, Feb. 1990.
- [17] TSAI, C.Y., DIXON, A.G., MOSER, W.R., MA, Y.H., "Dense Perovskite Membrane Reactors for Partial Oxidation of Methane to Syngas", AIChE Journal, v. 43, n. S11, pp. 2741-2750, Jun. 2004.
- [18] XU, S.J., THOMSON, W.J., "Stability of La0.6Sr0.4Co0.2Fe0.8O3- Perovskite Membranes in Reducing and Nonreducing Environments", Industrial & Engineering Chemistry Research, v. 37, n. 4, pp. 1290-1299, Mar. 1998.
- [19] LI, S., JIN, W., XU, N., SHI, J., "Synthesis and Oxygen Permeation Properties of La0.2Sr0.8Co0.2Fe0.8O3−δ Membranes", Solid State Ionics, v. 124, n. 1-2, pp. 161-170, Sep. 1999.
- [20] JIN, W., LI, S., HUANG, P., XU, N., SHI, J., "Fabrication of La0.2Sr0.8Co0.8Fe0.2O3−δ Mesoporous Membranes on Porous Supports from Polymeric Precursors", Journal of Membrane Science, v. 170, n. 1, pp. 9-17, May. 2000.
- [21] PECHINI, M.P., "Method of Preparing Lead and Alkaline-earth Titanates and Niobates and Coating Method Using the Same to form Capacitors", US Patent nş 3330697, 1967.
- [22] GHARBAGE, B., HENAULT, M., PAGNIER, T., HAMMOU, A., "Preparation of La1−xSrxMnO3 Thin Films by a Pyrosol Derived Method", Materilas Research Bulletin, v. 26, n. 10, pp. 1001-1007, Oct. 1991.
- [23] ARUNA, S.T., MUTHURAMAN, M., KASHINARH, P.C., "Combustion Synthesis and Properties of Strontium Substituted Lanthanum Manganites La1-xSrxMnO3 (0 ≤ x ≤ 0,3)", Journal of Materials Chemistry, v. 7, n. 12, pp. 2499-2503. Feb. 1997.
Datas de Publicação
-
Publicação nesta coleção
26 Jun 2007 -
Data do Fascículo
2007
Histórico
-
Aceito
08 Jul 2006 -
Recebido
31 Jan 2006