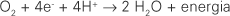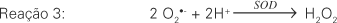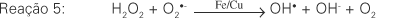Resumos
O interesse acerca dos mecanismos de geração e adaptação de radicais livres de oxigênio (RLO) ao exercício aumentou significativamente a partir da demonstração de sua relação com o consumo de oxigênio. Os RLO são formados pela redução incompleta do oxigênio, gerando espécies que apresentam alta reatividade para outras biomoléculas, principalmente lipídios e proteínas das membranas celulares e, até mesmo, o DNA. As injúrias provocadas por estresse oxidativo apresentam efeitos cumulativos e estão relacionadas a uma série de doenças, como o câncer, a aterosclerose e o diabetes. O exercício físico agudo, em função do incremento do consumo de oxigênio, promove o aumento da formação de RLO. No entanto, o treinamento físico é capaz de gerar adaptações capazes de mitigar os efeitos deletérios provocados pelos RLO. Estas adaptações estão relacionadas a uma série de sistemas, dos quais os mais importantes são os sistemas enzimáticos, compostos pela superóxido dismutase, catalase e glutationa peroxidase, e o não enzimático, composto por ceruloplasmina, hormônios sexuais, coenzima Q, ácido úrico, proteínas de choque térmico e outros. Tais adaptações, apesar das controvérsias sobre os mecanismos envolvidos, promovem maior resistência tecidual a desafios oxidativos, como aqueles proporcionados pelo exercício de alta intensidade e longa duração. As técnicas de avaliação de estresse oxidativo, na maioria das vezes, não são capazes de detectar injúria em exercícios de curta duração. Dessa forma, esforços estão sendo feitos para o estudo de esforços físicos realizados por longos períodos de tempo ou efetuados até a exaustão. Novos marcadores de lesão por ação dos RLO estão sendo descobertos e novas técnicas para sua determinação estão sendo criadas. O objetivo deste trabalho é discutir os mecanismos da formação dos RLO e das adaptações ao estresse oxidativo crônico provocado pelo treinamento físico.
Exercício; Radicais livre de oxigênio; Estresse oxidativo; Antioxidantes; Treinamento
El interés a cerca de los mecanismos de generación y adaptación de radicales libres de oxígeno (RLO) al ejercicio aumentó significativamente a partir de la demostración de su relación con el consumo de oxígeno. Los RLO son formados por la reducción incompleta de del oxígeno, generando especies que presentan una alta reactividad para otras biomoléculas, principalmente lípidos y proteínas de las membranas celulares y, así mismo, el DNA. Las injurias provocadas por el estrés oxidativo presentan efectos acumulativos y están relacionados a una serie de enfermedades, como el cáncer, la arteriosclerosis o la diabetes. El ejercicio físico agudo, en función del incremento del consumo de oxígeno promueve un aumento en la formación de los RLO. No en tanto, el entrenamiento físico es capaz de generar adaptaciones capaces de mitigar los efectos deletéreos provocados por los RLO. Estas adaptaciones están relacionadas a una serie de sistemas de los cuales los mas importantes son los sistemas enzimáticos, compuestos por la peróxido dismutasa, catalasa y glutation peroxidasa y los sistemas no enzimáticos compuestos por ceruloplasmina, hormonas sexuales, la coenzima Q, ácido úrico, proteínas de choque térmico, y otros. Tales adaptaciones, a pesar de las controversias sobre los mecanismos comprendidos, promueven una mayor resistencia tisular a los desafíos oxidativos, como son aquellos proporcionados por el ejercicio físico de alta intensidad y de larga duración. Las técnicas de evaluación del estrés oxidativo, la mayoría de las veces, no son capaces de detectar injurias en ejercicios de corta duración. De esta forma, los esfuerzos están siendo realizados por largos periodos de tiempo o realizados hasta la extenuación. Nuevos marcadores de lesión por acción de los RLO están siendo descubiertos y nuevas técnicas para su determinación están siendo creadas. El objetivo de este trabajo es discutir los mecanismos de formación de los RLO y de adaptación al estrés oxidativo crónico provocado por el entrenamiento físico.
Ejercicio; Radicales libres de oxígeno; Estrés oxidativo; Antioxidantes; Entrenamiento
The interest about the mechanisms of generation and adaptation of oxygen free radicals (OFR) to exercise has increased significantly from the demonstration of its relation with the oxygen intake. The OFR are formed through the incomplete reduction of oxygen, generating species presenting high reactivity to other biomolecules, especially lipids and proteins of the cell membranes and even DNA. The injuries caused by the oxidative stress present accumulative effects, being related to several diseases such as cancer, arteriosclerosis and diabetes. The acute physical exercise furthers the increase on the formation of OFR in function of the increment on the oxygen intake. However, the physical training generates adaptations able to soften the harmful effects caused by OFR. These adaptations are related to several systems, among which the most important are the enzymatic system, composed by the superoxide dysmutase, catalase and glutathione peroxidase; and the non-enzymatic system, composed by the ceruloplasmine, the sexual hormones, co-enzyme Q, uric acid, thermal shock proteins, among others. Such adaptations, despite the controversies about the mechanisms involved, further a higher tissue resistance and oxidative challenges such as those provided by long-duration high intensity exercises. The evaluations techniques of the oxidative stress, most times are not able to detect injuries in short-duration exercises. Thus, studies of physical efforts performed for long periods or until exhaustion have been conducted. New lesion markers by OFR action have been discovered and new techniques for its determination have been created. The objective of this work is discuss the formation mechanisms of OFR and the adaptations to the chronic oxidative stress caused by physical training.
Exercise; Oxygen free radicals oxidative stress; Antioxidants; Training
ARTIGO DE REVISÃO
Radicais livres de oxigênio e exercício: mecanismos de formação e adaptação ao treinamento físico
Radicales libres de oxigeno y ejercicio: mecanismos de formación y adaptación al entrenamiento
Cláudia Dornelles Schneider; Alvaro Reischak de Oliveira
Programa de Pós-Graduação em Ciências do Movimento Humano, Grupo de Estudos em Bioquímica e Fisiologia do Exercício, Laboratório de Pesquisa do Exercício - Escola de Educação Física, UFRGS, Porto Alegre, Brasil
Endereço para correspondência Endereço para correspondência Rua Felizardo, 750 90690-200 - Porto Alegre, RS E-mail: claudiadschneider@ig.com.br/ aroliveira@esef.ufrgs.br
RESUMO
O interesse acerca dos mecanismos de geração e adaptação de radicais livres de oxigênio (RLO) ao exercício aumentou significativamente a partir da demonstração de sua relação com o consumo de oxigênio. Os RLO são formados pela redução incompleta do oxigênio, gerando espécies que apresentam alta reatividade para outras biomoléculas, principalmente lipídios e proteínas das membranas celulares e, até mesmo, o DNA. As injúrias provocadas por estresse oxidativo apresentam efeitos cumulativos e estão relacionadas a uma série de doenças, como o câncer, a aterosclerose e o diabetes. O exercício físico agudo, em função do incremento do consumo de oxigênio, promove o aumento da formação de RLO. No entanto, o treinamento físico é capaz de gerar adaptações capazes de mitigar os efeitos deletérios provocados pelos RLO. Estas adaptações estão relacionadas a uma série de sistemas, dos quais os mais importantes são os sistemas enzimáticos, compostos pela superóxido dismutase, catalase e glutationa peroxidase, e o não enzimático, composto por ceruloplasmina, hormônios sexuais, coenzima Q, ácido úrico, proteínas de choque térmico e outros. Tais adaptações, apesar das controvérsias sobre os mecanismos envolvidos, promovem maior resistência tecidual a desafios oxidativos, como aqueles proporcionados pelo exercício de alta intensidade e longa duração. As técnicas de avaliação de estresse oxidativo, na maioria das vezes, não são capazes de detectar injúria em exercícios de curta duração. Dessa forma, esforços estão sendo feitos para o estudo de esforços físicos realizados por longos períodos de tempo ou efetuados até a exaustão. Novos marcadores de lesão por ação dos RLO estão sendo descobertos e novas técnicas para sua determinação estão sendo criadas. O objetivo deste trabalho é discutir os mecanismos da formação dos RLO e das adaptações ao estresse oxidativo crônico provocado pelo treinamento físico.
Palavras-chave: Exercício. Radicais livre de oxigênio. Estresse oxidativo. Antioxidantes. Treinamento.
RESUMEN
El interés a cerca de los mecanismos de generación y adaptación de radicales libres de oxígeno (RLO) al ejercicio aumentó significativamente a partir de la demostración de su relación con el consumo de oxígeno. Los RLO son formados por la reducción incompleta de del oxígeno, generando especies que presentan una alta reactividad para otras biomoléculas, principalmente lípidos y proteínas de las membranas celulares y, así mismo, el DNA. Las injurias provocadas por el estrés oxidativo presentan efectos acumulativos y están relacionados a una serie de enfermedades, como el cáncer, la arteriosclerosis o la diabetes. El ejercicio físico agudo, en función del incremento del consumo de oxígeno promueve un aumento en la formación de los RLO. No en tanto, el entrenamiento físico es capaz de generar adaptaciones capaces de mitigar los efectos deletéreos provocados por los RLO. Estas adaptaciones están relacionadas a una serie de sistemas de los cuales los mas importantes son los sistemas enzimáticos, compuestos por la peróxido dismutasa, catalasa y glutation peroxidasa y los sistemas no enzimáticos compuestos por ceruloplasmina, hormonas sexuales, la coenzima Q, ácido úrico, proteínas de choque térmico, y otros. Tales adaptaciones, a pesar de las controversias sobre los mecanismos comprendidos, promueven una mayor resistencia tisular a los desafíos oxidativos, como son aquellos proporcionados por el ejercicio físico de alta intensidad y de larga duración. Las técnicas de evaluación del estrés oxidativo, la mayoría de las veces, no son capaces de detectar injurias en ejercicios de corta duración. De esta forma, los esfuerzos están siendo realizados por largos periodos de tiempo o realizados hasta la extenuación. Nuevos marcadores de lesión por acción de los RLO están siendo descubiertos y nuevas técnicas para su determinación están siendo creadas. El objetivo de este trabajo es discutir los mecanismos de formación de los RLO y de adaptación al estrés oxidativo crónico provocado por el entrenamiento físico.
Palabras-clave: Ejercicio. Radicales libres de oxígeno. Estrés oxidativo. Antioxidantes. Entrenamiento.
INTRODUÇÃO
O aumento do consumo de oxigênio, assim como a ativação de vias metabólicas específicas durante ou após o exercício, resulta na formação de radicais livres de oxigênio, substâncias conhecidas simplesmente como radicais livres(1-3). Estas moléculas estão aumentadas nos exercícios de alta intensidade(4,5) e extenuantes(6) e foram relacionadas a um grande número de doenças como enfisema pulmonar, doenças inflamatórias, aterosclerose, câncer e envelhecimento, a partir da década de 80(7,8). Por outro lado, sabe-se que a atividade física é uma conhecida forma de estresse e a exposição crônica a ela, chamada treinamento físico, é capaz de disparar adaptações em resposta a uma maior produção destes radicais livres. Neste sentido os estudos mais recentes estabelecem o papel da atividade física na prevenção e controle de diversas doenças, como câncer de cólon, e possivelmente câncer de mama e de próstata(9), diabetes e hipertensão(10), dislipidemias e aterosclerose(11), entre outras. Este artigo proporciona uma revisão acerca dos mecanismos de geração dos radicais livres através do exercício, bem como os processos adaptativos e respectivas conseqüências induzidas pelo treinamento físico.
RADICAIS LIVRES
Os radicais livres de oxigênio (RLO) são produzidos naturalmente em nosso organismo através de processos metabólicos oxidativos e, muitas vezes, são de extrema utilidade, como nas situações em que há necessidade de ativação do sistema imunológico (como exemplo, os macrófagos utilizam o peróxido de hidrogênio para destruir bactérias e outros elementos estranhos); na desintoxicação de drogas; e na produção do fator relaxante derivado do endotélio, o óxido nítrico, extremamente importante nos processos que desencadeiam o relaxamento dos vasos sanguíneos(12).
Conforme Halliwell(1), o oxigênio (O2) que respiramos é metabolizado em nosso organismo da seguinte maneira: aproximadamente 85 a 90% são utilizados pela mitocôndria, através da cadeia de transporte de elétrons, e os 10 a 15% restantes são utilizados por diversas enzimas oxidases e oxigenases e também por reações químicas de oxidação diretas. Na parte terminal da cadeia de transporte de elétrons, a enzima citocromo oxidase (reação 1) remove um elétron de cada uma das quatro moléculas reduzidas de citocromo c, oxidando-as, e adiciona os quatro elétrons ao O2 para formar água (em torno de 95 a 98% dos 85 a 90% citados acima). Os 2 a 5% restantes são reduzidos univalentemente em metabólitos denominados espécies reativas de oxigênio.
Reação 1 - redução tetravalente do oxigênio
FORMAÇÃO DAS ESPÉCIES REATIVAS DE OXIGÊNIO
Em razão da sua configuração eletrônica, o oxigênio tem forte tendência a receber um elétron de cada vez. A conversão univalente do oxigênio à água processa-se da seguinte maneira:
(a) A adição de um elétron a uma molécula de oxigênio no estado fundamental gera a formação do radical superóxido (O2-) (reação 2).
(b) O superóxido ao receber mais um elétron e dois íons hidrogênio forma peróxido de hidrogênio (H2O2), através do processo chamado dismutação(13). Essa reação é catalisada pela enzima superóxido dismutase (SOD) que é encontrada em quantidades elevadas nas células de mamíferos e que acelera a reação a 104 vezes a freqüência para dismutação espontânea num pH fisiológico (reação 3).
(c) Quando o H2O2 recebe mais um elétron e um íon hidrogênio, é formado o radical hidroxil (OH), que é o mais reativo dos intermediários, pois pode reagir e alterar qualquer estrutura celular que esteja próxima e assim influenciar enzimas, membranas ou ácidos nucléicos(6).
O radical hidroxil pode ser formado quando o H2O2 reage com íons ferro ou cobre (reação 4). A reação é conhecida como Reação de Fenton.
Os íons de metais de transição podem também catalisar a reação entre H2O2 e superóxido, conduzindo à produção de radical hidroxil (reação 5), a chamada Reação de Haber-Weiss.
Os radicais superóxido e hidroxil têm elétrons desemparelhados em sua órbita mais externa e são, portanto, chamados radicais livres. O peróxido de hidrogênio não é um radical livre; no entanto, representa um metabólito de oxigênio parcialmente reduzido. Outras espécies reativas de interesse são os oxigênio singletes, que são formas de oxigênio spin-alteradas. Esses metabólitos derivados do oxigênio, considerados em conjunto, são denominados espécies reativas de oxigênio (ERO), em função da sua aumentada reatividade para as biomoléculas(14), e em geral alteram o tamanho e a forma dos compostos com os quais eles interagem.
Além disso, o radical superóxido pode reagir diretamente com o óxido nítrico (NO), um radical livre centrado no nitrogênio, gerando peroxinitrito. Este pode levar à formação de um oxidante com características do radical hidroxil (reação 6).
Cada ERO tem suas próprias características, mostrando diferentes reatividades e tempos de meia-vida(13,15).
ESTRESSE OXIDATIVO
O termo estresse oxidativo é utilizado em circunstâncias nas quais o "desafio" por radicais livres resulta em dano tecidual ou na produção de compostos tóxicos ou danosos aos tecidos. Pode-se dizer que um organismo encontra-se sob estresse oxidativo (EO) quando ocorre um desequilíbrio entre os sistemas prooxidantes e antioxidantes, de maneira que os primeiros sejam predominantes(16). Um dos principais mecanismos de lesão é a lipoperoxidação (LPO), ou seja, a oxidação da camada lipídica da membrana celular. Além disso, o EO pode gerar danos a proteínas e ao DNA, provocando diversas alterações na função celular e, portanto, tecidual.
DEFESA ANTIOXIDANTE
Como as ERO são continuamente formadas em pequenas quantidades pelos processos normais do metabolismo, todas as células possuem mecanismos para mitigar seus efeitos agressores. Cabe salientar que a composição das defesas antioxidantes difere de tecido a tecido, de tipo de célula a tipo de célula e possivelmente de célula a célula do mesmo tipo, em um dado tecido(1).
O sistema de defesa antioxidante está dividido em enzimático e não enzimático. O primeiro inclui as enzimas superóxido dismutase (SOD), catalase (CAT) e glutationa peroxidase (GPx).
A catalase desempenha importante papel na eliminação do H2O2, promovendo a sua catálise até água.
A GPx também funciona como mecanismo de proteção contra o estresse oxidativo, convertendo a glutationa reduzida (GSH) à glutationa oxidada (GSSG), removendo H2O2 e formando água (reação 8)(17).
Dessa forma, tanto a CAT quanto a GPx evitam o acúmulo de radical superóxido e de peróxido de hidrogênio para que não haja produção de radical hidroxil, contra o qual não existe sistema enzimático de defesa(13).
O perfeito equilíbrio entre as enzimas antioxidantes (CuZnSOD, MnSOD, CAT, GPx) é importante para a manutenção da integridade celular.
Já o sistema não enzimático inclui compostos sintetizados pelo organismo humano como bilirrubina, ceruloplasmina, hormônios sexuais, melatonina, coenzima Q, ácido úrico, e outros, ingeridos através da dieta regular ou via suplementação como ácido ascórbico (vitamina C), a-tocoferol (vitamina E), b-caroteno (precursor de vitamina A) e grupos fenóis de plantas (flavonóides).
Em estudos desenvolvidos em nosso laboratório(18,19), utilizando corações isolados de ratos, em um modelo de perfusão coronariana (Langendorff), demonstramos que tanto a vitamina A quanto o Trolox (análogo hidrossolúvel da vitamina E) agiram reduzindo os níveis de lipoperoxidação e os efeitos inotrópico, cronotrópico e lusitrópico negativos induzidos por H2O2. Isto se deve à capacidade quencher de oxigênio singlete de ambas as vitaminas. Um quencher é uma molécula que capta a energia de excitação do oxigênio singlete para si, levando-o ao estado fundamental e tornando-se excitada(1).
MECANISMOS DE FORMAÇÃO DAS ESPÉCIES REATIVAS DE OXIGÊNIO
Durante a atividade muscular, a demanda energética pode superar em 35 vezes a demanda de repouso(20). Dessa forma, durante a sua realização ocorre um grande aumento no consumo de oxigênio, na sua maior parte em decorrência do aumento de trabalho muscular. Pelo fato de as ERO serem produzidas através do metabolismo intermediário, o exercício provoca aumento da sua produção. Como exemplo, imaginemos um homem adulto de 70kg, que em repouso utiliza 3,5mL O2.kg-1.min-1 ou 352,8L.d-1 ou 14,7mol.d-1. Se 1% gera O2-, isto significa 0,147mol.d-1 ou 53,66mol.ano-1 ou @ 1,7 kg.ano-1 (de O2-). Já durante o esforço físico, com o aumento do consumo de O2, isto pode aumentar de 10 a 15 vezes(1).
Segundo Viña et al.(21), o grau de estresse oxidativo e de dano muscular não depende da intensidade absoluta do exercício, mas do grau de exaustão da pessoa que realiza o exercício. Além disso, conhecer os mecanismos de formação de RL com o exercício é importante para prevenir o estresse oxidativo e o dano associados com a atividade física exaustiva. Os mecanismos de formação são os seguintes:
(1) Interrupções temporárias das bombas de ATP dependentes de cálcio (Ca++) levam ao aumento das concentrações intracelulares de cálcio, o que durante o exercício pode ativar a via da xantina oxidase. Concentrações aumentadas de cálcio intramuscular durante períodos de exercício de alta intensidade podem ativar as proteases dependentes de cálcio, as quais convertem a xantina desidrogenase em xantina oxidase. A xantina oxidase usa o oxigênio molecular ao invés do NAD+ como aceitante de elétrons e assim gera o radical superóxido;
(2) Períodos de exercício intenso podem aumentar o estresse oxidativo devido à hipóxia e reoxigenação temporárias, que ocorrem no músculo exercitado em função das contrações e relaxamentos estabelecidos ciclicamente. Durante a contração, a compressão vascular estabelece um quadro de isquemia e, portanto, de hipóxia. No relaxamento, ocorre a reperfusão e, conseqüentemente, a reoxigenação. Sob condições de hipóxia, os equivalentes reduzidos podem se acumular dentro da cadeia de transporte de elétrons mitocondrial, resultando em um fenômeno conhecido como estresse redutivo (reductive stress). Na reoxigenação, uma explosão (burst) de reduções monoeletrônicas pode converter o oxigênio molecular em radicais superóxido;
(3) A ativação de leucócitos pode estimular a produção de radicais livres para melhorar os mecanismos de defesa do hospedeiro em resposta ao dano muscular induzido pelo exercício. Em particular, os neutrófilos podem reduzir o oxigênio molecular a radical superóxido via NADPH oxidase, a qual está inativa nas células em repouso. Processos similares têm sido observados em monócitos e eosinófilos;
(4) O aumento das concentrações de Ca++ pode ativar a enzima fosfolipase A2, a qual libera o ácido araquidônico a partir dos fosfolipídeos. A ciclooxigenase reage com o ácido araquidônico para gerar o radical hidroxil;
(5) Condições hipóxicas também têm sido mostradas no aumento da atividade da óxido nítrico sintase (NOS), levando à formação de radicais do óxido nítrico. Estes radicais podem exercer um efeito pró-oxidante fraco por eles próprios ou se combinar com o superóxido para formar um oxidante mais potente, o peroxinitrito(22), como já demonstrado (reação 6).
Sendo assim, durante o metabolismo aeróbio, a possibilidade de ocorrer lesão oxidativa nos tecidos vai depender de um preciso equilíbrio entre a geração de radicais de oxigênio e a eficácia dos mecanismos antioxidantes.
EXERCÍCIO FÍSICO E ESPÉCIES REATIVAS DE OXIGÊNIO
Diversos estudos da década de 80 apresentaram resultados nos quais repetidas cargas de exercício levavam a dano ou envelhecimento acelerado do músculo em indivíduos ou cobaias que se exercitavam regularmente. Entretanto Heath et al.(23), depois de acompanhar atletas durante muitos anos, verificaram que seu potencial metabólico e sua capacidade funcional muscular não eram prejudicados. Além disso, Gutteridge et al.(24) apontaram como possibilidade de mecanismo protetor o fato de terem encontrado incremento nos níveis de ferro e cobre no suor de atletas após o exercício, especulando que a excreção de tais metais no suor diminuiria a extensão do dano oxidativo mediado por tais metais. A partir destes estudos levantou-se a possibilidade de que o exercício regular pudesse promover um aumento adaptativo dos mecanismos de defesa do músculo esquelético capaz de proteger contra as lesões produzidas pelas ERO.
Em 1982, Davies et al.(25) propuseram que a formação de radicais livres induzida por exercício pudesse ser o estímulo inicial para a biogênese mitocondrial em uma situação de treinamento crônico. Nesta linha de trabalho, Ji(26) demonstrou que em músculo esquelético uma carga isolada de trabalho exaustivo produzia um aumento de LPO e que a atividade das enzimas antioxidantes glutationa redutase, GPx, SOD e CAT estava significativamente aumentada. Da mesma forma, Alessio(27) mostrou aumento de LPO em fibras musculares lentas e rápidas, de ratos submetidos a cargas de exercício, indicando aumento de estresse oxidativo induzido pela atividade física. Esse estresse era melhor tolerado por ratos treinados, sugerindo uma adaptação dos sistemas antioxidantes.
Ao estudar humanos, Nies et al.(28) demonstraram a ocorrência de dano ao DNA nos leucócitos circulantes após exercício exaustivo em esteira. Pela primeira vez isto foi mostrado em indivíduos treinados, mas, como a extensão do dano foi pequena, os autores sugerem que a adaptação ao treinamento de resistência aeróbia pode reduzir os efeitos do EO, como o dano ao DNA. No mesmo ano, os resultados do trabalho de Mills et al.(29), com cavalos de corrida, mostraram que o exercício pode induzir mudanças nos parâmetros bioquímicos que são indicativos de estresse oxidativo, e que estes são exacerbados na presença de altas temperaturas e umidade. Em interessante trabalho, envolvendo um modelo de sobrecarga de treinamento, Palazzetti et al.(30) estudaram triatletas submetidos a um incremento de carga de trabalho da ordem de 21% na natação, 51% no ciclismo e 44% na corrida, por quatro semanas. O simples fato de o atleta ser submetido à sobrecarga de treinamento já provocava elevação significativa de adrenalina urinária e atividade da CK plasmática em repouso. No entanto, as maiores diferenças apareciam ao avaliar os efeitos de um duatlo (corrida e ciclismo) simulado. Os atletas em condições de sobrecarga de treinamento apresentavam maiores índices de lipoperoxidação, avaliada pelo nível de substâncias reativas ao ácido tiobarbitúrico (TBA-RS), CK-MB e mioglobina plasmáticos, marcadores de lesão muscular, além de queda da relação GSH:GSSG, indicando claramente que esta sobrecarga compromete os mecanismos de defesa antioxidantes relacionados à resposta induzida por exercício.
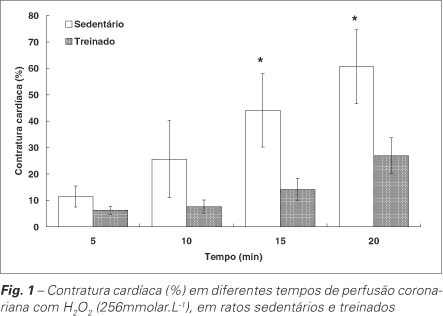
Foi proposto por Margaritis et al.(31) que a magnitude da melhora do sistema de defesa antioxidante depende das cargas de treinamento. Os mesmos autores demonstraram ainda que quanto mais alto o  , em triatletas, mais alta a atividade da enzima antioxidante GPX nos eritrócitos, protegendo o organismo do dano à membrana celular. Leeuwenburgh et al.(32) acrescentam que o estresse oxidativo induzido pelo exercício pode disparar adaptações em resposta ao treinamento e que tais adaptações seriam tecido-específicas, sugerindo um mecanismo regulatório complexo. Além disso, Leaf et al.(33) sugerem que em indivíduos saudáveis o exercício físico induz a peroxidação lipídica transitoriamente e que existe remoção dos produtos da LPO durante a fase de recuperação. O trabalho de Venditti e Di Meo(34) com ratos adultos submetidos a um programa de treinamento regular com duração de um ano comprovou a hipótese de que tal treinamento prolonga a capacidade de resistência aeróbia e aumenta as defesas antioxidantes, limitando assim o dano tecidual causado por RL. Da mesma forma, em nosso laboratório, demonstramos que o treinamento aeróbio, realizado através de corrida em esteira, em ratos, aumenta a capacidade miocárdica de manejar um desafio por perfusão com H2O2, provocando menor contratura e menor formação de TBA-RS(35) (figuras 1 e 2). Na mesma linha de investigação, 11 semanas de treinamento aeróbio em ratos idosos, além de provocar bradicardia e aumento do índice glicose/insulina (um marcador da resistência à insulina), estavam associadas a uma resposta reduzida ao estresse oxidativo induzido por peróxido de hidrogênio. Neste estudo, demonstramos uma correlação positiva entre a FC basal e os níveis de TBA-RS (figura 3), ou seja, quanto maior a FC basal, maiores eram os níveis de lesão radicalar(36). Estes efeitos podem ser parcialmente explicados pela maior atividade da SOD encontrada em outro estudo de nosso grupo(37), em que ratos de apenas 21 dias foram submetidos a treinamento a 50% do
, em triatletas, mais alta a atividade da enzima antioxidante GPX nos eritrócitos, protegendo o organismo do dano à membrana celular. Leeuwenburgh et al.(32) acrescentam que o estresse oxidativo induzido pelo exercício pode disparar adaptações em resposta ao treinamento e que tais adaptações seriam tecido-específicas, sugerindo um mecanismo regulatório complexo. Além disso, Leaf et al.(33) sugerem que em indivíduos saudáveis o exercício físico induz a peroxidação lipídica transitoriamente e que existe remoção dos produtos da LPO durante a fase de recuperação. O trabalho de Venditti e Di Meo(34) com ratos adultos submetidos a um programa de treinamento regular com duração de um ano comprovou a hipótese de que tal treinamento prolonga a capacidade de resistência aeróbia e aumenta as defesas antioxidantes, limitando assim o dano tecidual causado por RL. Da mesma forma, em nosso laboratório, demonstramos que o treinamento aeróbio, realizado através de corrida em esteira, em ratos, aumenta a capacidade miocárdica de manejar um desafio por perfusão com H2O2, provocando menor contratura e menor formação de TBA-RS(35) (figuras 1 e 2). Na mesma linha de investigação, 11 semanas de treinamento aeróbio em ratos idosos, além de provocar bradicardia e aumento do índice glicose/insulina (um marcador da resistência à insulina), estavam associadas a uma resposta reduzida ao estresse oxidativo induzido por peróxido de hidrogênio. Neste estudo, demonstramos uma correlação positiva entre a FC basal e os níveis de TBA-RS (figura 3), ou seja, quanto maior a FC basal, maiores eram os níveis de lesão radicalar(36). Estes efeitos podem ser parcialmente explicados pela maior atividade da SOD encontrada em outro estudo de nosso grupo(37), em que ratos de apenas 21 dias foram submetidos a treinamento a 50% do  , por quatro semanas. Não foi encontrado qualquer aumento de TBA-RS ou QL nos corações destes animais, o que sugere que adaptações compensatórias no sistema antioxidante tecidual tenham ocorrido. Neste sentido, Ramires e Ji(38) demonstraram que o treinamento físico associado à suplementação de glutationa protege o coração de ratos contra a lesão oxidativa e depressão da função cardíaca provocados por isquemia e reperfusão in vivo. O mecanismo para esta adaptação foi a elevação do conteúdo miocárdico de glutationa e da capacidade antioxidante, através do incremento das atividades de SOD, GPx, GSH redutase, e g-glutamil transpeptidase miocárdicas.
, por quatro semanas. Não foi encontrado qualquer aumento de TBA-RS ou QL nos corações destes animais, o que sugere que adaptações compensatórias no sistema antioxidante tecidual tenham ocorrido. Neste sentido, Ramires e Ji(38) demonstraram que o treinamento físico associado à suplementação de glutationa protege o coração de ratos contra a lesão oxidativa e depressão da função cardíaca provocados por isquemia e reperfusão in vivo. O mecanismo para esta adaptação foi a elevação do conteúdo miocárdico de glutationa e da capacidade antioxidante, através do incremento das atividades de SOD, GPx, GSH redutase, e g-glutamil transpeptidase miocárdicas.
Ainda utilizando o modelo animal, Smolka et al.(39) analisaram o efeito de dois protocolos diferentes de treinamento sobre a expressão de HSP72 (Heat shock protein - 72 KDa), uma proteína de estresse com a função de manter e reparar a conformação protéica. Esta proteína está implicada na proteção das células contra diferentes tipos de insultos. Alguns destes insultos, como o estresse oxidativo, estresse térmico e baixo pH resultante do acúmulo de lactato são gerados durante o exercício. Além das adaptações já bastante bem descritas, de incremento da atividade de citrato sintase, catalase e GSH redutase musculares após o treinamento, um achado original deste estudo foi a demonstração de que a indução de HSP72 provocada por uma carga isolada de exercício ocorre somente no grupo mantido sedentário, sugerindo que esta age como um mecanismo protetor complementar ao estresse oxidativo induzido por exercício. Além disso, o grupo de animais submetidos a um protocolo de alta intensidade e curta duração apresentou maior suscetibilidade ao desafio proporcionado pelo exercício agudo que o grupo treinado através de protocolo contínuo. No estudo de Child et al.(40), indivíduos treinados foram submetidos a uma prova de meia maratona simulada; observou-se, através da medida da capacidade antioxidante total e do ácido úrico, uma maior habilidade scavenger (capacidade de neutralizar os radicais livres formando compostos menos reativos) sobre os RL do soro. Mas mesmo assim o exercício induziu aumento das concentrações de malondialdeído, sugerindo que tais respostas foram insuficientes para prevenir a LPO induzida pelo exercício.
Powers et al.(41) afirmam que o treinamento habitual de alta intensidade que é necessário para o nível de competição de elite é capaz de aumentar as defesas antioxidantes. Nesta linha de pesquisa, Halliwell(1) refere que atletas têm altas concentrações de ceruloplasmina no plasma. A ceruloplasmina é uma a-globulina que está envolvida no transporte e na regulação do cobre, podendo reduzir diretamente o oxigênio sem intermediários conhecidos, e portanto participante no sistema de defesa antioxidante extracelular.
Em 2000, o estudo de Selamoglu et al.(42) apresentou diferenças adaptativas entre os exercícios aeróbios e anaeróbios. A atividade da enzima GPx em eritrócitos estava aumentada nos corredores de longa distância comparados com levantadores de peso. Na mesma linha de trabalho, Inal et al.(43), analisando o metabolismo anaeróbio em exercício agudo de natação, observaram que a produção de RL foi maior do que a capacidade antioxidante. Por outro lado, Subudhi et al.(22), avaliando esquiadores alpinos de elite após treinamento intenso, não observaram mudança nos marcadores de estresse oxidativo, supondo então que estes atletas tiveram uma adaptação positiva em seus mecanismos antioxidantes com o treinamento.
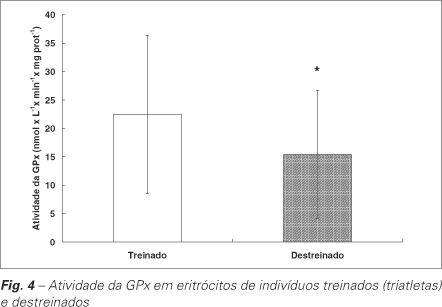
Recentemente, em nosso laboratório, Schneider(44), Schneider et al.(45) e Oliveira et al.(46) encontraram uma maior atividade eritrocitária da enzima GPx em triatletas treinados comparados a indivíduos não treinados (figura 4) e uma capacidade antioxidante total plasmática (TRAP) aumentada após o exercício em esteira rolante em ambos os grupos (figura 5). A maior atividade da GPx está de acordo com diversos estudos que mostram adaptação do sistema de defesa enzimático(32,41,47-49). O aumento no TRAP também foi observado no estudo de Child et al.(38) e deve ter ocorrido graças a uma maior liberação de substâncias antioxidantes, entre elas o ácido úrico, como ocorreu no trabalho de Mastaloudis et al.(49).
CONSIDERAÇÕES FINAIS
Conforme o exposto acima, observamos que os fatores mais importantes na formação do estresse oxidativo são a intensidade e conseqüentemente o nível de exaustão do indivíduo submetido ao exercício e, portanto, a exposição a um maior fluxo de oxigênio. Talvez alguns trabalhos não sejam capazes de demonstrar um desequilíbrio nos sistemas pró e antioxidantes em razão do curto tempo de exposição ao exercício. Além disso, podemos observar protocolos de exercício diversos, em geral baseados em um percentual do consumo máximo de oxigênio, ou seja, não relativizando a carga de trabalho aos sujeitos do estudo, bem como diferentes técnicas de detecção do estresse oxidativo.
O processo adaptativo do treinamento físico é capaz de proteger os indivíduos treinados na maioria das situações de exposição ao exercício. Uma falha em detectar qualquer mudança na lipoperoxidação ou outro alvo de dano pode sugerir que algumas mudanças compensatórias no sistema antioxidante podem ter ocorrido. Os resultados apontam uma up-regulation em relação às enzimas GPx e SOD em músculo esquelético e eritrócitos, mas em relação à enzima catalase os resultados são conflitantes. É interessante notar que diversos trabalhos que avaliam o sistema de defesa antioxidante humano analisam o sistema da glutationa, a GPx e SOD, a capacidade antioxidante total, mas não incluem a atividade da enzima catalase em seus estudos.
Além disso, a ativação de HSPs em exercício agudo e crônico participa do processo de proteção antioxidante. Este mecanismo tem merecido atenção maior nos últimos anos.
Finalmente, como alternativas de estudo podemos apontar no sentido da utilização de protocolos que contemplem exercícios de longa duração e/ou extenuantes aliados a uma dieta rica em nutrientes antioxidantes ou à suplementação de vitaminas e co-fatores de enzimas sobre o estresse oxidativo induzido pelo exercício, bem como o estudo da expressão gênica das enzimas antioxidantes, oxidação de proteínas e DNA, a partir de técnicas mais sensíveis.
Recebido em 21/3/04. 2a versão recebida em 22/5/04. Aceito em 25/5/04
Todos os autores declararam não haver qualquer potencial conflito de interesses referente a este artigo.
- 1. Halliwell B, Gutteridge JMC. Free radicals in biology and medicine. 3rd ed. New York: Oxford, 1999.
- 2. Heunks LMA, Viña J, Van Herwaarden CLA, Folgering HTM, Gimeno A, Dekhuijzen PNR. Xanthine oxidase is involved in exercise-induced oxidative stress in chronic obstructive pulmonary disease. Am J Physiol 1999;277:R1697-704.
- 3. Rowlands DS, Downey B. Physiology of triathlon. In: Garrett WE Jr, Kirkendall DT, editors. Exercise and sport science. Philadelphia: Lippincott Williams & Wilkins, 2000;921-2.
- 4. Lovlim R, Cottle W, Pyke I, Kavanagh M, Belcastro AN. Are indices of free radical damage related to exercise intensity? Eur J Appl Physiol 1987;56:312-6.
- 5. Ebelling CB, Clarkson PM. Exercise-induced muscle damage and adaptation. Sports Med 1989;7:207-34.
- 6. Jenkins RR. Free radical chemistry relationship to exercise. Sports Med 1988;5: 156-70.
- 7. Meneguini R. A toxicidade do oxigênio. Ciência Hoje 1987;5:28.
- 8. Southorn PA, Powis G. Free radicals in medicine II. Involvement in human disease. Mayo Clin Proc 1988b;63:390-408.
- 9. Marret LD, Theis B, Ashbury FD. Workshop report: physical activity and cancer prevention. Chronic Dis Can 2000;21:143-9.
- 10. Albright A, Franz M, Hornsby G, Kriska A, Marrero D, Ullrich I, et al. American college of sports medicine position stand. Exercise and type 2 diabetes. Med Sci Sports Exerc 2000;32:1345-60.
- 11. Diretrizes Brasileiras Sobre Dislipidemias e Diretriz de Prevenção da Aterosclerose do Departamento de Aterosclerose da Sociedade Brasileira de Cardiologia, III. Arq Bras Cardiol 2001;77(Supl 3):1-48.
- 12. Moncada S, Higgs A. Nitric oxide: role in human disease. Encyclopedia of Life Sciences, 2001. Disponível em www.els.net em 20 dez 2001.
- 13. Pal Yu B. Cellular defenses against damage from reactive oxygen species. Physiol Rev 1994;74:139-62.
- 14. Fischer AB. Intracellular production of oxygen-derived free radicals. Proceedings of a Brook Lodge Symposium, Augusta, Apr. 1987;27-29:99-104.
- 15. Del Maestro RF. An approach to free radicals in medicine and biology. Acta Physiol Scand 1980;492:153-68.
- 16. Sies H. Biochemistry of oxidative stress. Angew Chem Int Ed Ingl 1986;25:1058-71.
- 17. Ferrari R, Ceconi C, Curello S, Guarnieri C, Caldarera M, Albertini A, Visioli O. Oxygen-mediated myocardial damage during ischaemia and reperfusion: role of the cellular defenses against oxygen toxicity. J Mol Cell Cardiol 1985;17:937-45.
- 18. Belló-Klein A, Oliveira AR, Brunetto AF, Irigoyen MC, Llesuy S, Belló AA. Effect of vitamin A on cardiac contracture induced by hydrogen peroxide. Med Sci Res 1994;22:411-13.
- 19. Belló-Klein A, Oliveira AR, Miranda MFS, Irigoyen MC, Homem-de-Bittencourt Jr PI, Llesuy S, et al. Effect of trolox C on cardiac contracture induced by hydrogen peroxide. Braz J Med Biol Res 1997;30:1337-42.
- 20. Åstrand PO, Rodhal K, Dahl HA, StrØmme SB. Textbook of work physiology. Physiological basis of exercise. 4th ed. Champaign: Human Kinetics, 2003.
- 21. Viña J, Gomez-Cabrera MC, Lloret A, Marquez R, Miñana JB, Pallardó FV, et al. Free radical in exhaustive physical exercise: mechanism of production, and protection by antioxidants. IUBMB Life 2000;50:271-7.
- 22. Subudhi AW, Davis SL, Kipp RW, Askew EW. Antioxidant status and oxidative stress in elite alpine ski racers. Int J Sport Nutr Exerc Metab 2001;11:32-41.
- 23. Heath GW, Hagberg JM, Ehsani AA, Holloszy JO. A physiological comparison of young and older endurance athletes. J Appl Physiol 1981;51:634-40.
- 24. Gutteridge JMC, Rowley DA, Halliwell B, Cooper DF, Heeley DM. Cooper and iron complexes catalytic for oxygen radical reactions in sweat from human athletes. Clin Chim Acta 1985;145:267-73.
- 25. Davies KJA, Quintanilha AT, Brooks GA, Packer L. Free radicals and tissue damage produced by exercise. Biochem Biophys Res Commun 1982;107:1198-205.
- 26. Ji LL, Fu R. Responses of glutathione system and antioxidant enzymes to exhaustive exercise and hydroperoxide. J Appl Physiol 1992;72:549-54.
- 27. Alessio HM. Exercise-induced oxidative stress. Med Sci Sports Exerc 1993;25: 218-24.
- 28. Nies AM, Hartmann A, Grunert-Fuchs M, Poch B, Speit G. DNA damage after exhaustive treadmill running in trained and untrained men. Int J Sports Med 1996;17:397-403.
- 29. Mills PC, Smith NC, Casas I, Harris P, Harris RC, Marlin DJ. Effects of exercise intensity and environmental stress on indices of oxidative stress and iron homeostasis during exercise in the horse. Eur J Appl Physiol 1996;74:60-6.
- 30. Palazzetti S, Richard M-J, Favier A, Margaritis I. Overloaded training increases exercise-induced oxidative stress and damage. Can J Appl Physiol 2003;28:588-604.
- 31. Margaritis I, Tessier F, M-J Richard, Marconnet P. No evidence of oxidative stress after a triathlon race in highly trained competitors. Int J Sports Med 1997;18: 186-90.
- 32. Leeuwenburgh C, Hollander J, Leichtweis S, Griffiths M, Gore M, Ji LL. Adaptations of glutathione antioxidant system to endurance training are tissue and muscle fiber specific. Am J Physiol 1997;272:R363-9.
- 33. Leaf DA, Kleinman MT, Hamilton M, Barstow TJ. The effect of exercise intensity on lipid peroxidation. Med Sci Sports Exerc 1997;29:1036-9.
- 34. Venditti P, Di Meo S. Effect of training on antioxidant capacity, tissue damage, and endurance of adult male rats. Int J Sports Med 1997;18:497-502.
- 35. Belló AA, Belló-Klein A, Oliveira AR, Brunetto AF, Irigoyen MC, Bauermann LF, et al. Hydrogen peroxide as a tool for studying oxidative stress in the heart. J Braz Assoc Adv Sci 1996;48:28-36.
- 36. De Angelis KLD, Oliveira AR, Werner A, Bock P, Bello-Klein A, Fernandes TG, et al. Exercise training in aging: hemodynamic, metabolic, and oxidative stress evaluations. Hypertension 1997;30:767-71.
- 37. Belló-Klein A, Lagranha CJ, Bock P, Barp J, Araújo ASR, Llesuy S, et al. Submaximal exercise training in postnatal rats: hemodynamic and oxidative stress changes. Exp Clin Cardiol 2000;5:149-53.
- 38. Ramires PR, Ji LL. Glutathione supplementation and training increases myocardial resistance to ischemia-reperfusion in vivo. Am J Physiol 2001;281:H679-88.
- 39. Smolka MB, Zoppi CC, Alves AA, Silveira LR, Marangoni S, Pereira-Da-Silva L, et al. HSP72 as a complementary protection against oxidative stress induced by exercise in the soleus muscle of rats. Am J Physiol 2000;279:R1539-45.
- 40. Child RB, Wilkinson DM, Fallowfield JL, Donnelly AE. Elevated serum antioxidant capacity and plasma malondialdehyde concentration in response to a simulated half-marathon run. Med Sci Sports Exerc 1998;30:1603-7.
- 41. Powers SK, Ji LL, Leeuwenburgh C. Exercise training-induced alterations in skeletal muscle antioxidant capacity: a brief review. Med Sci Sports Exerc 1999;31: 987-97.
- 42. Selamoglu S, Turgay F, Kayatekin BM, Günenc S, Yslegen C. Aerobic and anaerobic training effects on the antioxidant enzymes of the blood. Acta Physiol Hung 2000;87:267-73.
- 43. Inal M, Akyüz F, Turgut A, Getsfrid WM. Effect of aerobic and anaerobic metabolism on free radical generation swimmers. Med Sci Sports Exerc 2001;33:564-7.
- 44. Schneider CD. Avaliação do estresse oxidativo em indivíduos submetidos a diferentes intensidades de exercício em esteira rolante [Dissertação apresentada para obtenção do título de mestre em ciências do movimento humano]. Porto Alegre: Escola de Educação Física da Universidade Federal do Rio Grande do Sul, 2002.
- 45. Schneider CD, Barp J, Ribeiro JL, Belló-Klein A, Oliveira AR. Oxidative stress after three different intensities of running. Can J Appl Physiol 2004 (submetido).
- 46. Oliveira AR, Schneider CD, Ribeiro JL, Deresz LF, Barp J, Belló-Klein A. Oxidative stress after three different intensities of running. Med Sci Sports Exerc 2003;35:S367.
- 47. Tessier F, Margaritis I, Richard M-J, Moynot C, Marconnet P. Selenium and training effects on the glutathione system and aerobic performance. Med Sci Sports Exerc 1995;27:390-6.
- 48. Hellstein Y, Apple F, Sjodin B. Effect of sprint cycle training on activities of antioxidant enzymes in human skeletal muscle. J Appl Physiol 1996;81:1484-7.
- 49. Mastaloudis A, Leonard SW, Traber MG. Oxidative stress in athletes during extreme endurance exercise. Free Radic Biol Med 2001;31:911-22.
Datas de Publicação
-
Publicação nesta coleção
10 Nov 2004 -
Data do Fascículo
Ago 2004