Resumos
INTRODUÇÃO: O alongamento passivo ou estático (EAL) é frequentemente utilizado em programas de reabilitação e na área desportiva; porém, as alterações morfofuncionais ocorridas ainda não estão bem claras, principalmente após imobilização prolongada. OBJETIVOS: Examinar as alterações morfofuncionais musculares produzidas em resposta a três semanas de exercícios de EAL em um modelo animal de imobilização prolongada de membro posterior (MP) em posição encurtada. MÉTODOS: Foram utilizados 32 ratos Wistar divididos em quatro grupos (n = 8, em cada): A - grupo controle (CONT), B - grupo imobilizado por 21 dias (IMOB), C - grupo remobilizado por 21 dias (LIVRE), D - grupo alongados por 21 dias (ALONG). Foram comparadas as variações morfofuncionais entre grupos experimentais. As variáveis foram: peso corporal e muscular, comprimento muscular e ósseo, número de miofibrilas e quantidade de colágeno, determinadas através de histomorfometria muscular por contraste de cor. RESULTADOS: A IMOB do bíceps femoral em posição encurtada produziu uma importante hipotrofia com hiperplasia muscular compensatória, além do aumento (p < 0,05) na deposição de colágeno no perimísio e intramuscular de ratos. A remobilização livre ou o alongamento passivo reduziram significativamente (p < 0,05) estas alterações morfofuncionais observados no grupo IMOB. CONCLUSÃO: Através desses resultados, pode-se concluir que tanto o EAL quanto a remobilização livre promovem a restauração das alterações morfofuncionais no bíceps femoral esquerdo induzida pela imobilização prolongada, embora somente o EAL foi capaz de reduzir a relação entre colágeno/músculo.
fisioterapia manual; alongamento passivo; imobilização prolongada; atrofia muscular; histomorfometria
BACKGROUND: Passive or static stretching (ALMP) is often used in rehabilitation programs and in sports; however, the morphological changes occurred are not very clear, especially after prolonged immobilization. AIMS:This study aimed to examine the muscle morphological and functional changes produced in response to three weeks of ALMP in an animal model of prolonged immobilization of hind limb (HL) in the short range. METHODS: For this purpose, 32 rats (Wistar) were used and divided in 4 groups (n = 8 each): A- control group (CONT), B - immobilized group for 21 days (IMMOB), C - remobilized group for 21 days (FREE), D - elongated group for 21 days (ELONG). The variables evaluated were body weight and muscle mass, muscle and bone length, number of myofibrils and quantity of collagen, determined by histomorphometry muscle by color contrast. The morphological variations between all the experimental groups were compared. RESULTS: The IMMOB of the femoral biceps in shortened position produced important muscular atrophy with compensatory hyperplasia, and increase (p <0.05) in collagen deposition in the perimysium and intramuscular of rats. The free remobilization and the passive stretching reduced significantly (p <0.05) these morphological changes observed in group IMMOB. CONCLUSIONS: Based on these results, it was concluded that both passive stretch and free remobilization promote restoration of the morphological changes induced by prolonged immobilization in the left femoral biceps of rats; however only passive stretching was able to reduce the correlation between collagen/muscle.
manual physiotherapy; passive stretching; prolong immobilization; muscle atrophy; histomorphometry
ARTIGO ORIGINAL
CIÊNCIAS DO EXERCÍCIO E DO ESPORTE
Alterações morfofuncionais musculares em resposta ao alongamento passivo em modelo animal de imobilização prolongada de membro posterior
Muscle morphological changes in response to passive stretching in an animal model of prolonged immobilization of hind limb
Wanize Almeida RochaI,II;Gustavo Abrahão GobbiIII; Vitor de Freitas AraujoIII; Cíntia Helena SantuzziI,IV; Gilma Correa CoutinhoI;Breno Valentim NogueiraI; Washington Luiz Silva GonçalvesI
ILaboratório de Investigações Experimentais e Clínicas em Fisioterapia e Terapia Ocupacional, Centro de Ciência da Saúde, Universidade Federal do Espírito Santo (UFES) Vitória, ES
IINúcleo de Pesquisas em Fisioterapia da Faculdade Novo Milênio (FNM) Vila Velha, ES
IIIEscola Superior de Ciências da Saúde da Santa Casa de Misericórdia de Vitória (Emescam) Vitoria, ES
IVDepartamento de Fisioterapia da Faculdade Salesiana de Vitória (FSV) Vitória, ES
Endereço para correspondência Endereço para correspondência: Washington Luiz Silva Gonçalves Programa de Pós-Graduação em Ciências Fisiológicas, CCS-UFES Avenida Marechal Campos, 1.468, Maruípe 29040-755 Vitoria, ES, Brasil E-mail: wash.goncalves@gmail.com
RESUMO
INTRODUÇÃO: O alongamento passivo ou estático (EAL) é frequentemente utilizado em programas de reabilitação e na área desportiva; porém, as alterações morfofuncionais ocorridas ainda não estão bem claras, principalmente após imobilização prolongada.
OBJETIVOS: Examinar as alterações morfofuncionais musculares produzidas em resposta a três semanas de exercícios de EAL em um modelo animal de imobilização prolongada de membro posterior (MP) em posição encurtada.
MÉTODOS: Foram utilizados 32 ratos Wistar divididos em quatro grupos (n = 8, em cada): A grupo controle (CONT), B grupo imobilizado por 21 dias (IMOB), C grupo remobilizado por 21 dias (LIVRE), D grupo alongados por 21 dias (ALONG). Foram comparadas as variações morfofuncionais entre grupos experimentais. As variáveis foram: peso corporal e muscular, comprimento muscular e ósseo, número de miofibrilas e quantidade de colágeno, determinadas através de histomorfometria muscular por contraste de cor.
RESULTADOS: A IMOB do bíceps femoral em posição encurtada produziu uma importante hipotrofia com hiperplasia muscular compensatória, além do aumento (p < 0,05) na deposição de colágeno no perimísio e intramuscular de ratos. A remobilização livre ou o alongamento passivo reduziram significativamente (p < 0,05) estas alterações morfofuncionais observados no grupo IMOB.
CONCLUSÃO: Através desses resultados, pode-se concluir que tanto o EAL quanto a remobilização livre promovem a restauração das alterações morfofuncionais no bíceps femoral esquerdo induzida pela imobilização prolongada, embora somente o EAL foi capaz de reduzir a relação entre colágeno/músculo.
Palavras-chave: fisioterapia manual, alongamento passivo, imobilização prolongada, atrofia muscular, histomorfometria.
ABSTRACT
BACKGROUND: Passive or static stretching (ALMP) is often used in rehabilitation programs and in sports; however, the morphological changes occurred are not very clear, especially after prolonged immobilization.
AIMS:This study aimed to examine the muscle morphological and functional changes produced in response to three weeks of ALMP in an animal model of prolonged immobilization of hind limb (HL) in the short range.
METHODS: For this purpose, 32 rats (Wistar) were used and divided in 4 groups (n = 8 each): A- control group (CONT), B immobilized group for 21 days (IMMOB), C - remobilized group for 21 days (FREE), D - elongated group for 21 days (ELONG). The variables evaluated were body weight and muscle mass, muscle and bone length, number of myofibrils and quantity of collagen, determined by histomorphometry muscle by color contrast. The morphological variations between all the experimental groups were compared.
RESULTS: The IMMOB of the femoral biceps in shortened position produced important muscular atrophy with compensatory hyperplasia, and increase (p <0.05) in collagen deposition in the perimysium and intramuscular of rats. The free remobilization and the passive stretching reduced significantly (p <0.05) these morphological changes observed in group IMMOB.
CONCLUSIONS: Based on these results, it was concluded that both passive stretch and free remobilization promote restoration of the morphological changes induced by prolonged immobilization in the left femoral biceps of rats; however only passive stretching was able to reduce the correlation between collagen/muscle.
Keywords: manual physiotherapy, passive stretching, prolong immobilization, muscle atrophy, histomorphometry
INTRODUÇÃO
O alongamento muscular é frequentemente efetuado em várias práticas terapêuticas e desportivas com o objetivo de aumentar a flexibilidade muscular e a amplitude articular, assim como diminuir o risco de lesões e possivelmente melhorar o desempenho dinâmico(1,2). O alongamento de forma passiva ou estático é realizado por uma força externa, aplicada manualmente e/ou mecanicamente em um músculo esquelético, enquanto o indivíduo está relaxado(3). Estudos prévios demonstraram que o músculo esquelético diminui o comprimento e a extensibilidade quando mantido em posição encurtada (imobilização), facilitando o aparecimento de contraturas musculares e atrofia muscular. É definido como contratura muscular, o encurtamento de um músculo ou de outros tecidos moles que cruzam uma articulação, resultando em limitação da mobilidade articular e atrofia muscular ou hipotrofia como a perda de trofismo(1-3).
Inúmeras investigações têm demonstrado que as fibras musculares esqueléticas apresentam uma grande plasticidade, ou seja, têm a tendência de assumir um comprimento novo após as forças externas implicadas pelo alongamento passivo ter sido removida, bem como após remoção das forças biomecânicas por uma imobilização prolongada. O efeito plástico é garantido devido às propriedades que os tecidos contráteis e não contráteis possuem de adquirir novos comprimentos na presença ou ausência de novas forças mecânicas(3-7). Mostram ainda que a principal fonte de resistência ao alongamento passivo do músculo é a malha de tecido conjuntivo que há dentro dele, e não os seus componentes contráteis ativos(3,5,6). Os músculos, principalmente os esqueléticos, aumentam seu comprimento por meio da adição de novos sarcômeros ao longo das fibras musculares(4-6). Alguns trabalhos clássicos mostram que a imobilização dos músculos em posição alongada também acarreta o aumento no comprimento muscular, pela adição no número de sarcômeros em série, particularmente nas duas regiões terminais das fibras musculares(3-7). Porém, nos estudos in vitro, Deyne(6) verificou que a aplicação de alongamento passivo uniaxial não inibiu, nem facilitou, o aparecimento de linhas Z ou bandas A, assim como sugeriu que é a contração ativa e não o alongamento passivo (estático) o responsável pela miofibrilogenesis (síntese de actina e miosina).
Alguns autores mostram também que a imobilização prolongada, seja em posição encurtada ou alongada, é comumente utilizada nas rotinas traumato-ortopédicas de membros inferiores e parecem reduzir significantemente o número de sarcômeros em série, além de aumentar a deposição de tecido conectivo (colágeno) intramuscular e no perimísio. Este aumento do colágeno muscular poderia reduzir a força relativa e a dinâmica muscular para o movimento ativo, acarretando déficits funcionais no segmento corporal.
Estudos clássicos de Tabary et al.(5) demonstraram que a imobilização em longo prazo do músculo solear na posição encurtada produz uma diminuição de 40% no número de sarcômeros em série. Foi também observada por Williams e Goldspink(4), Williams et al.(7) e Yang et al.(8) um remodelamento do perimísio no músculo sóleo de camundongos, duas semanas após imobilização em posição de encurtamento. Além disso, é bem descrito na literatura que os músculos imobilizados em posição encurtada apresentam abundância de tecido conjuntivo com significante remodelamento nos períodos subsequentes à imobilização. E que esta redução do comprimento da fibra muscular ocorre não somente quando é imobilizado em posição encurtada, mas também quando o músculo está trabalhando (remobilização) em amplitude articular diminuída(4-8). Diante do exposto, o objetivo deste estudo foi examinar as alterações morfofuncionais musculares (bíceps femoral) produzidas em resposta a três semanas exercícios de alongamento passivo (estático), após imobilização prolongada em posição encurtada de membro posterior (MP) de ratos sadios.
MÉTODOS
Animais e grupos experimentais
Foram utilizados 32 ratos machos Wistar (Rattus norvergicus albinus) adultos, provenientes do Biotério do CCS-UFES. Os animais foram pesados e aleatoriamente distribuídos em quatro grupos experimentais (n = 8, em cada): A grupo (CONT) sem intervenção; B grupo imobilizado (IMOB) em posição encurtada por 21 dias; C grupo remobilizado (LIVRE) por 21 dias; D grupo alongado (ALONG) por 21 dias. Durante todo o estudo, os animais foram alojados em caixas individuais com fundo sólido, forradas com maravalha, em sala com luminosidade (12h claro e 12h escuro) e temperatura (20 a 25ºC) controlada, e receberam dieta sólida (ração Nuvilab®) e água ad libitum. Não houve perda amostral e a investigação ocorreu de acordo com as normas estabelecidas pelo Guide Care and Use of Laboratory Animals e os critérios adotados pelo Colégio Brasileiro de Experimentação Animal COBEA(9), aprovada pelo Comitê de Ética em Pesquisa Animal (CEUA/UFES parecer nº 014/2008).
Modelo animal de imobilização prolongada de membro posterior por órtese estática
Os animais experimentais foram sedados com halotano a 3%, vaporizado em câmara de contenção. Sob anestesia, o encurtamento do músculo bíceps femoral esquerdo foi realizado pela técnica de imobilização na posição encurtada por órtese contentora estática(10-12). Este tipo de imobilização está baseado na moldagem de uma órtese em material termoplástico flexível de 2,4mm de espessura, OMEGA® MAX 3/32" (North Coast Medical, Morgan Hill, CA, EUA). Os grupos IMOB e ALONG tiveram a órtese contentora moldada diretamente no membro inferior esquerdo (MIE) de cada animal, sendo colocada de forma que a pata traseira dos ratos permanecesse em flexão completa (joelho e tornozelo), isto é, posição de encurtamento do músculo bíceps femoral, a qual foi mantida por 21 dias consecutivos, conforme ilustrado na figura 1. O modelo de imobilização utilizado neste estudo foi baseado no proposto por Booth e Kelso(10), readequado para um membro por Matheus e Shimano(11), com adaptação do material utilizado para construção da órtese.
Alongamento passivo (estático) e procedimentos cirúrgicos
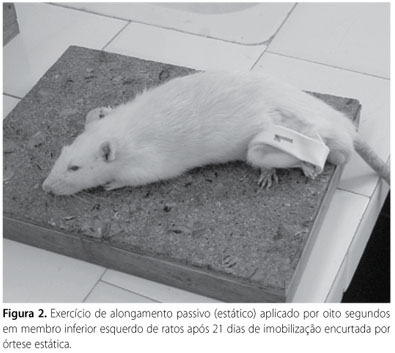
Logo após o período de imobilização do membro inferior esquerdo, a órtese estática foi retirada e os animais do grupo ALONG foram tratados com um exercício de alongamento estático (passivo) no limite da amplitude articular impedida pela resistência dos tecidos moles (cápsulas, ligamentos e tendões do joelho e tornozelo). O exercício de alongamento estático foi aplicado no membro inferior E, uma vez ao dia, no período matutino, durante oito minutos(2) por três semanas consecutivas, resultando em um total de 21 dias de alongamento passivo (figura 2). No grupo LIVRE, após o período de imobilização de 21 dias, foram retiradas as órteses, permitindo movimentos livres em suas gaiolas por mais 21 dias. Após este período, os animais foram sacrificados com uma dose letal de anestésico (Pentobarbital sódico) e então realizados os procedimentos cirúrgicos e coleta do músculo bíceps femoral e do osso fêmur. Em todos os animais, foi realizada uma incisão cirúrgica de 5,0cm na região posterior da coxa da pata traseira direita, na qual o músculo bíceps femoral direito foi isolado e retirado de suas enteses proximal e distal para pesagem úmida e, na sequência, o processamento da rotina histológica. O fêmur esquerdo (homolateral) foi desarticulado e removido para medidas de comprimento (mm), realizadas a partir do ponto mais proximal da cabeça femoral até o sulco intercondilar da articulação do joelho E, utilizando-se um paquímetro digital (Mitutoyo Sul Americana Ltda, Suzano, SP, Brasil).
Determinação do índice de trofismo muscular e da forca muscular relativa
O índice de trofismo muscular foi calculado pela razão entre o peso úmido do músculo bíceps femoral (mg) e o peso corporal final (g) dos animais experimentais. Para determinar a força muscular relativa, ou seja, a força da massa muscular do bíceps femoral exercida sobre o osso fêmur, realizou-se uma correção do peso da massa muscular em relação ao comprimento do fêmur homolateral descrito pela equação: mf = Pm/f, onde mf representa a massa muscular, Pm representa o peso do músculo (mg) e f representa o comprimento do osso fêmur (mm).
Análises histomorfométricas
As amostras de tecido muscular (bíceps femoral E) foram obtidas e fixadas em paraformaldeído-10% (pH 7,0) por período mínimo de 24 horas. Após a fixação, as amostras de músculo foram desidratadas gradativamente em concentrações crescentes de álcool etílico (70% a 100%), diafanizadas em xilol, embebidas e incluídas em parafina, conforme métodos histológicos de rotina. Os fragmentos incluídos em parafina foram cortados em pares de seções de 5µm de espessura utilizando micrótomo Spence modelo 820. As lâminas histológicas foram mantidas em estufa para secagem, e os cortes de tecido posteriormente submetidos à coloração por sirius red (SR), para posterior análise morfométrica das fibras musculares e do colágeno. Foi realizada captura de imagens de cinco campos (mm2) microscópicos de cada lâmina histológica com câmera digital (com objetiva de 40x) do microscópio de luz polarizada modelo AX70 Plus (Olympus®, Tóquio, Japão). As análises histomorfométricas foram realizadas e avaliadas através das imagens de cada grupo capturadas por sistema computadorizado de imagens Sigma-pro® (Sigma, St Louis, MO, EUA) e armazenadas. No final do estudo, as imagens dos cortes histológicos arquivadas foram submetidas à contagem da fração volumétrica de fibras musculares e de colágeno (mm2) com auxílio de marcação digital por contraste de cor(13,14).
Análise Estatística
Os dados obtidos neste estudo foram inseridos em planilhas específicas e analisadas por software estatístico Prism-5® (GraphPad Software, Inc., San Diego, CA, EUA). A distribuição dos dados foi verificada pelo teste de Shapiro Wilk. Foi utilizada a análise de variância (ANOVA) de uma via, seguido do teste de Tukey como post hoc, e o teste não paramétrico de Mann-Witney U, quando apropriado. Os valores estão expressos como média ± erro padrão da média (EPM). O nível de significância para diferenças estatísticas foi estabelecido em p < 0,05.
RESULTADOS
Na tabela 1 estão apresentados os efeitos morfofuncionais da imobilização prolongada em posição de encurtamento e do exercício de alongamento passivo (estático). Em relação ao peso corporal, não foram observadas alterações significantes entre os valores nos diferentes grupos experimentais. Conforme esperado, no grupo IMOB foi verificada uma redução significativa nos valores de massa muscular e no comprimento do osso fêmur, assim como uma atrofia muscular (diminuição do trofismo) com redução da força muscular relativa quando comparado com os grupos CONT, LIVRE e ALONG. O alongamento passivo no grupo ALONG promoveu um significante aumento da massa do músculo bíceps femoral quando comparado com os grupos IMOB e CONT.
Na avaliação histomorfométrica do músculo bíceps femoral (tabela 2, figura 3) verificou-se que a imobilização prolongada na posição encurtada (IMOB) promoveu uma hiperplasia muscular (aumento de miofibrilas), além de um aumento do colágeno no perimísio muscular em relação aos grupos CONT, LIVRE e ALONG. Já o tratamento de três semanas com alongamento passivo promoveu uma melhora do índice de trofismo muscular com significante redução da deposição de colágeno no perimísio muscular quando comparado aos grupos CONT, IMOB e LIVRE. No entanto, apesar de o grupo LIVRE ter reduzido a deposição de colágeno em relação ao grupo IMOB, apresentou um aumento em relação ao grupo ALONG.
A hiperplasia miofibrilar, ou seja, a quantidade de miofibrilas no músculo bíceps femoral, os animais do grupo ALONG apresentaram uma significante redução quando comparados com os do grupo IMOB, assim como uma melhora do grau de trofismo miofibrilar. No entanto, no grupo LIVRE não houve diferenças em relação ao CONT e ALONG. Na relação colágeno/músculo intramuscular, foi constatado que a imobilização prolongada (IMOB) em posição encurtada por órtese estática promoveu aumento da razão colágeno/músculo quando comparado com os grupos CONT, LIVRE e ALONG. Mostrou também que três semanas de tratamento com alongamento passivo diminuiu a relação colágeno/músculo quando comparados os grupos CONT e LIVRE (tabela 2, figura 3).
DISCUSSÃO
Neste estudo, foram demonstradas as alterações das propriedades musculares plásticas produzidas pela imobilização prolongada (posição encurtada), remobilização livre e pelo alongamento passivo, que foram avaliadas através de parâmetros histomorfométricos e biomecânicos do músculo bíceps femoral em membro posterior de ratos sadios. Os dados deste estudo mostraram que a imobilização prolongada do músculo bíceps femoral na posição encurtada modificou todos os parâmetros morfofuncionais musculares avaliados, ou seja, ocasionou uma significante hipotrofia muscular com hiperplasia miofibrilar compensatória, encurtamento muscular e ósseo, além de aumento da deposição de colágeno no perimísio, o que pode ter facilitado a elevação do grau de atrofia miofibrilar aguda e redução da força relativa observadas no músculo bíceps femoral dos ratos, dados estes que corroboram outros achados na literatura em modelos animais de imobilização encurtada(12,15,16). Este estudo também demonstra que três semanas consecutivas de exercício de alongamento passivo com duração de oito segundos foram suficientes para restabelecer o grau de trofismo muscular e reduzir significantemente a hiperplasia miofibrilar, além de diminuir a deposição de colágeno no perimísio do bíceps femoral de ratos sadios após imobilização. Mostrou ainda que a remobilização livre foi capaz de retornar os níveis de hiperplasia e a atrofia miofibrilar observadas; contudo, não melhorou a relação entre a deposição de tecido conectivo e a massa contrátil do músculo bíceps.
Estudos clássicos, assim como investigações recentes, demonstram que, tanto a imobilização prolongada como o desuso, são caracterizados principalmente pela disfunção muscular contrátil associada com atrofia muscular aguda, que vem sendo considerado um processo passivo sofrido pelo tecido muscular(4,5,7,8,16,17). Mostram também que a imobilização gera uma atrofia aguda das fibras musculares tipos I e II, as quais estão associadas com um aumento na proteólise, e não no decréscimo da síntese proteica muscular(12,15-18). Neste estudo, verificou-se que a imobilização prolongada promoveu uma significante hiperplasia miofibrilar compensatória, ocorrida provavelmente em resposta à atrofia miofibrilar (hipotrofia) produzida pelo desuso e observadas no bíceps femoral dos animais do grupo imobilizados. Por outro lado, observou-se que o alongamento passivo aplicado por oito segundos nos membro posterior esquerdo de ratos durante 21 dias, reduz significantemente a deposição de colágeno e a hiperplasia muscular após imobilização encurtada de bíceps femoral. Chang et al.(19) e outros autores(16,17,20) descrevem que níveis teciduais de óxido nítrico (NO) estão envolvidos na sinalização para regulação do número de sarcômeros musculares e com a miofibrilogênese (síntese de actina e miosina). Alguns autores sugerem também que o desuso induzido pela imobilização prolongada em posição encurtada aumente o número de microlesões nas miofibrilas acarretando elevação da produção de espécies reativas de oxigênio e radicais livres no tecido muscular. O que poderia favorecer a redução da biodisponibilidade do NO com consequente diminuição na miofibrilogênese.
Adicionalmente, ao contrário do tecido muscular, quando o tecido conectivo é submetido à imobilização, provavelmente não ocorre diminuição no número de fibras colágenas(21,22). Alguns experimentos demonstraram aumento da degradação e síntese do colágeno sem alteração na sua concentração(23). Ao mesmo tempo, está descrito que ocorre uma redução na quantidade de água e glicosaminoglicanas, tornando o tecido menos elástico e mais quebradiço(23,24). Outros estudos mostram que a diminuição do espaço entre as fibras colágenas, aliada à produção e deposição aleatória de colágeno imaturo, favorece a formação de ligações intermoleculares em locais indesejáveis e limita a amplitude de movimento articular(22). Como consequência à limitação articular, maior quantidade de força será requerida para mover o segmento imobilizado através da amplitude de movimento normal(22-24). Woo et al.(23) demonstraram que após imobilizar o joelho de coelhos em flexão durante nove semanas, o torque necessário para estender a articulação aumentou 10 vezes quando comparado com o grupo controle não imobilizado. Seus resultados também mostraram que esse torque diminuía à medida que o joelho era sucessivamente estendido, sugerindo que, nas primeiras tentativas de imobilização, o movimento forçado era capaz de romper ligações estabelecidas entre as moléculas de colágeno. A quebra de ligações intermoleculares aumenta a mobilidade da articulação e facilita os movimentos subsequentes, o que justificaria uma menor deposição de colágeno no grupos ALONG e LIVRE quando comparados com o grupo IMOB.
Todavia, a aplicação do alongamento passivo pode ter efeitos a curto e longo prazos, promovendo alterações tanto no tecido muscular quanto nos tecidos conectivos(25). Os efeitos a curto prazo ou agudos (segundos ou minutos) podem incluir eventos como alteração no comprimento do tendão; nos elementos dos componentes elásticos em série ou em paralelo ou na distribuição do comprimento dos sarcômeros dentro das fibras musculares. Portanto, os efeitos imediatos do alongamento (primeiros 60 segundos) contemplam as alterações viscoelásticas passivas, o que leva à redução da resistência ao alongamento. Os efeitos em longo prazo do alongamento (várias semanas) são, principalmente, a hipertrofia induzida, a qual parece aumentar a força tecidual(26-28). Sendo assim, é evidente na literatura que de alguma forma, o alongamento passivo altera as propriedades mecânicas do músculo e aumenta o comprimento muscular(29-33). Segundo Goldspink et al.(4,5,7,8,31), as modificações na estrutura e propriedades musculares são possíveis devido à alta capacidade de remodelação do tecido muscular, ou seja, a reconhecida plasticidade muscular. Esses e outros estudos(12,15-17) corroboram nossos achados que apresentam aumento na massa muscular (hipertrofia), redução da hiperplasia miofibrilar e diminuição da deposição de colágeno no perimísio do bíceps femoral, além de demonstrar uma redução na relação colágeno/músculo de ratos sadios após alongamento passivo crônico.
Apesar de resultados semelhantes encontrados na literatura quanto às análises abordadas no desuso muscular, alguns pontos se diferenciam devido à diversidade de fatores que o influenciam, destacando-se a tipagem de fibra, a posição articular, o tempo de aplicação da técnica e a técnica de alongamento escolhida (alongamento passivo). Nesse sentido, há uma necessidade de maiores estudos, com análises e técnicas de biologia celular e molecular que contemplem as diferentes variáveis que interferem nesse processo.
AGRADECIMIENTOS
Os autores agradecem aos professores CA. Redins e JC. Novaes por disponibilizarem os laboratórios de histologia e imunohistoquímica e pelo auxílio na confecção e análises dos cortes histológicos do presente estudo. Esta pesquisa foi parcialmente financiada pela bolsa de recém-doutor nº 028/2008 (CDV-Facitec).
Todos os autores declararam não haver qualquer potencial conflito de interesses referente a este artigo.
- 1. Safran MR, Seaber AV, Garret WE. Warm-up and muscular injury prevention: an update. Clin J Sport Med. 1989;8:239-49.
- 2. Endlich PW, Farina GR, Dambroz C, Gonçalves WLS, Moyses MR, Mill JG, Abreu GR. Efeitos agudos do alongamento estático no desempenho da força dinâmica em homens jovens. Rev Bras Med Esp. 2009;15:200-3.
- 3. Kisner C, Colby LA. In: Exercícios terapêuticos: fundamentos e técnicas. 3Ş edição, ed. Manole Ltda: São Paulo, 1998, p.141-57.
- 4. Williams PE, Goldspink G. Connective tissue changes in immobilised muscle. J Anat. 1984;138:343-50.
- 5. Tabary JC, Tabary C, Tardieu C, Tardieu G, Goldspink G. Physiological and structural changes in the cat's soleus muscle due to immobilization at different lengths by plaster casts. J Physiol. 1972;224:231-44.
- 6. Deyne PG. Formation of sarcomeres in developing myotubes: role of mechanical stretch and contractile activation. J Physiol Cell. 2000;279:1801-11.
- 7. Williams PE, Catanese T, Lucey EG, Goldspink G. The importance of stretch and contractile activity in the prevention of connective tissue accumulation in muscle. J Anat. 1988;158:109-14.
- 8. Yang H, Alnaqeeb M, Simpson H, Goldspink G. Changes in muscle fibre type, muscle mass and IGF-I gene expression in rabbit skeletal muscle subjected to stretch. J Anat. 1997;190:613-22.
- 9. Andersen ML, D'Almeida V, Ko GM, Kawakami R, Martins PJF, Magalhães LE, Tufik D. Princípios éticos e práticos do uso de animais de experimentação. São Paulo: UNIFESP, 2004.
- 10. Booth FW, Kelso JR. Production of rat muscle atrophy by cast fixation. J Appl Physiol. 1973;34:404-6.
- 11. Matheus JPC, Shimano AC. Efeitos da estimulação elétrica neuromuscular durante a imobilização nas propriedades mecânicas do músculo esquelético. Rev Bras Med Esp. 2007;13:55-9.
- 12. Coutinho EL, Gomes ARS, Franca CN, Salvini TF. A new model for the immobilization of the rat hind limb. Braz J Med Biol Res. 2002;35:1329-32.
- 13. Gonçalves WLS, Souza FM, Conti CL, Cirqueira JP, Rocha WA, Pires JGP, et al. Influence of He-Ne laser therapy on the dynamics of wound healing in mice treated with anti-inflammatory drugs. Braz J Med Biol Res. 2007;40:877-84.
- 14. Santuzzi CH, Buss HF, Pedrosa DF, Freire MOVM, Nogueira BV, Gonçalves WLS. Uso combinado da laserterapia de baixa potência e da inibição da ciclooxigenase-2 na reepitelização de ferida incisional em pele de camundongos: Um estudo pré-clínico. An Bras Dermatol. 2010;85 [in press]
- 15. Gomes ARS, Coutinho EL, Franca CN, Polônio J, Salvini TF. Effects of one stretch a week applied to the immobilized soleus muscle on rat muscle fiber morphology. Braz J Med Biol Res. 2004;37:1473-80.
- 16. Coutinho EL, Gomes ARS, Franca CN, Oishi J, Salvini TF. Effect of passive stretching on the immobilized soleus muscle fiber morphology. Braz J Med Biol Res. 2004;37:1853-61.
- 17. Gomes ARS, Cornachione A, Salvini TF, Mattielo-Sverzut AC. Morphological effects of two protocols of passive stretch over the immobilized rat soleus muscle. J Anat. 2007;210:328-35.
- 18. Durigan JLQ, Cancelliero KM, Polacow MLO, Silva CA, Guirro RRJ. Modelos de desuso muscular e estimulação elétrica neuromuscular: aspectos pertinentes à reabilitação fisioterapêutica. Fisioter Moviment. 2005;18:53-62.
- 19. Chang WJ, Iannaccone ST, Lau KS, Masters BS, McCabe TJ, McMillan K, et al. Neuronal nitric oxide synthase and dystrophin-deficient muscular dystrophy. Proc Nat Acad Sci. 1996;93:9142-7.
- 20. Koh TJ, Tidball W. Nitric oxide synthase inhibitors reduce sarcomere addition in rat skeletal muscle. J Physiol. 1999;519:189-96.
- 21. Aquino CF, Viana SO, Fonseca ST. Comportamento biomecânico e resposta dos tecidos biológicos ao estresse e à imobilização. Fisioter Moviment. 2005;18:35-43.
- 22. Akeson WH, Amiel D, Abel MF, Garfin SR, Woo SL. Effects of immobilization on joints. Clin Orthop Relat Res. 1987;219:28-37.
- 23. Woo SL-Y, Matthews JV, Akeson WH, Amiel D, Convery FR. Connective tissue response to immobility: Correlative study of biomechanical measurements of normal and immobilized rabbit knees. Arthritis Rheum. 1975;18:257-64.
- 24. Engles M, Donatelli RA, Wooden MJ. Tissue response. In: Orthopaedic Physical Therapy. 3Ş edição, ed. Philadelphia: Churchill Livingstone, 2001, p.1-24.
- 25. Black JDJ, Freeman M, Stevens ED. A 2 week routine stretching programme did not prevent contraction-induced injury in mouse muscle. J Physiol. 2006;544:137-47.
- 26. Kubo K, Kanehisa H, Fukunaga T. Effects of resistance and stretching training programmes on the viscoelastic properties of human tendon structures in vivo. J Physiol. 2002;538:219-26.
- 27. Magnusson SP, Simonensen EB, Aagaard P, Kjaer M. Biomechanical responses to repeated stretches in human hamstring muscle in vivo. Am J Sports Med. 1996;24:622-8.
- 28. Malliaropoulos N, Papalexandris S, Papalada A, Papacostas E. The role of stretching in rehabilitation of hamstring injuries: 80 athletes follow-up. Med Sci Sports Exerc. 2004;36:756-9.
- 29. Taylor DC, Dalton JD, Seaber AV, Garrett WE. Viscoelastic properties of muscle-tendon units. Am J Sports Med. 1990;18:300-9.
- 30. Weir DE, Tingley J, Elder GCB. Acute passive stretching alters the mechanical properties of human plantar flexors and the optimal angle for maximal voluntary contraction. Eur J Appl Physiol. 2005;93:614-23.
- 31. Goldspink G. Changes in muscle mass and phenotype and the expression of autocrine and systemic growth factors by muscle in response to stretch and overload. J Anat. 1995;194:323-34.
- 32. Fowles JR, Sale DG, Macdougall JD. Reduced strength after passive stretch of the human plantar flexors. J Appl Physiol. 2000;89:1179-88.
- 33. Avela J, Finni T, Liikavainio T, Niemelã E, Komi PV. Neural and mechanical responses of the triceps surae muscle group after 1h of repeated fast passive stretches. J Appl Physiol. 2004;96:2325-32.
Datas de Publicação
-
Publicação nesta coleção
13 Dez 2011 -
Data do Fascículo
Dez 2010