Resumos
Acaricidas inibidores da respiração celular são importantes para o controle de Brevipalpus phoenicis (Geijskes) na cultura dos citros no Brasil. Foram conduzidos estudos para avaliar: (a) a variabilidade na suscetibilidade de populações de B. phoenicis coletadas em pomares de citros para cihexatim, azociclotim, propargite e enxofre; (b) relações de resistência cruzada entre propargite e os acaricidas azociclotim, cihexatim, dinocape, piridabem e enxofre; e (c) o custo adaptativo associado à resistência de B. phoenicis a propargite em condições de laboratório. O método de bioensaio adotado foi o contato residual. A suscetibilidade foi estimada com concentrações diagnósticas baseadas na CL95 de cada acaricida. A resistência cruzada foi avaliada pela caracterização da curva de concentração-mortalidade das linhagens suscetível (S) e resistente a propargite (Propargite-R). O custo adaptativo foi avaliado mediante comparação de parâmetros biológicos das linhagens S e Propargite-R em frutos de laranja a 25 ± 1ºC e fotofase de 14h. Diferenças significativas na sobrevivência de B. phoenicis foram verificadas aos acaricidas cihexatim (de 16,3% a 80,5%), azociclotim (de 3,0% a 15,0%), propargite (de 1,0% a 71,6%) e enxofre (de 9,0% a 82,6%). Baixa intensidade de resistência cruzada foi verificada entre propargite e os acaricidas azociclotim (1,8 vezes), cihexatim (4,6 vezes), dinocape (3,5 vezes) e piridabem (3,5 vezes). Por outro lado, a intensidade de resistência cruzada a enxofre (> 111 vezes) foi bastante alta. Não foi verificada presença de custo adaptativo associado à resistência de B. phoenicis a propargite. Portanto, o uso desses acaricidas também deve ser feito de maneira criteriosa no manejo da resistência de B. phoenicis a acaricidas.
Ácaro-da-leprose; propargite; cihexatim; manejo da resistência
Acaricides that inhibit cellular respiration play an important role in the control of Brevipalpus phoenicis (Geijskes) in citrus groves in Brazil. Studies were conducted to evaluate: (a) the variability in the susceptibility among B. phoenicis populations collected from citrus groves to cyhexatin, azocyclotin, propargite and sulphur; (b) cross-resistance relationships between propargite and azocyclotin, cyhexatin, dinocap, pyridaben and sulphur; and (c) the fitness cost associated with propargite resistance in B. phoenicis under laboratory conditions. A residual-type contact bioassay was used to characterize the susceptibility. The susceptibility was estimated with diagnostic concentrations based LC95 of each acaricide. The cross-resistance was evaluated by characterizing the concentration-mortality responses of susceptible (S) and propargite-resistant (Propargite-R) strains. The fitness cost was evaluated by measuring the biological parameters of S and Propargite-R strains on citrus fruits at 25 ± 1ºC and fotophase of 14h. Significant differences in the susceptibility of B. phoenicis were detected at diagnostic concentration of cyhexatin (survivorship from 16.3% to 80.5%), azocyclotin (from 3.0% to 15.0%), propargite (from 1.0% a 71.6%) and sulphur (from 9.0% to 82.6%). A low intensity of cross-resistance was detected between propargite and the acaricides azocyclotin (1.8-fold), cyhexatin (4.6-fold), dinocap (3.5-fold) and pyridaben (3.5-fold). On the other hand, the intensity of cross-resistance to sulphur (> 111-fold) was very high. There was no fitness cost associated with B. phoenicis resistance to propargite, based on biological parameters evaluated. Therefore, the use of these acaricides should also be done very carefully in resistance management of B. phoenicis to acaricides.
Flat mite; propargite; cyhexatin; resistance management
CROP PROTECTION
Resistência de Brevipalpus phoenicis (Geijskes) (Acari: Tenuipalpidae) a acaricidas inibidores da respiração celular em citros: resistência cruzada e custo adaptativo
Resistance of Brevipalpus phoenicis (Geijskes) (Acari: Tenuipalpidae) to acaricides that inhibit cellular respiration in citrus: cross-resistance and fitness cost
Cláudio R. FrancoI; Nádia F.B. CasarinI; Felipe A. DominguesII; Celso OmotoI, III
IDepto. Entomologia, Fitopatologia e Zoologia Agrícola, Escola Superior de Agricultura "Luiz de Queiroz", USP 13.418-900, Piracicaba, SP
IIUniv. Metodista de Piracicaba, Rod. do Açúcar, km 156, 13.400-911, Piracicaba, SP
RESUMO
Acaricidas inibidores da respiração celular são importantes para o controle de Brevipalpus phoenicis (Geijskes) na cultura dos citros no Brasil. Foram conduzidos estudos para avaliar: (a) a variabilidade na suscetibilidade de populações de B. phoenicis coletadas em pomares de citros para cihexatim, azociclotim, propargite e enxofre; (b) relações de resistência cruzada entre propargite e os acaricidas azociclotim, cihexatim, dinocape, piridabem e enxofre; e (c) o custo adaptativo associado à resistência de B. phoenicis a propargite em condições de laboratório. O método de bioensaio adotado foi o contato residual. A suscetibilidade foi estimada com concentrações diagnósticas baseadas na CL95 de cada acaricida. A resistência cruzada foi avaliada pela caracterização da curva de concentração-mortalidade das linhagens suscetível (S) e resistente a propargite (Propargite-R). O custo adaptativo foi avaliado mediante comparação de parâmetros biológicos das linhagens S e Propargite-R em frutos de laranja a 25 ± 1ºC e fotofase de 14h. Diferenças significativas na sobrevivência de B. phoenicis foram verificadas aos acaricidas cihexatim (de 16,3% a 80,5%), azociclotim (de 3,0% a 15,0%), propargite (de 1,0% a 71,6%) e enxofre (de 9,0% a 82,6%). Baixa intensidade de resistência cruzada foi verificada entre propargite e os acaricidas azociclotim (1,8 vezes), cihexatim (4,6 vezes), dinocape (3,5 vezes) e piridabem (3,5 vezes). Por outro lado, a intensidade de resistência cruzada a enxofre (> 111 vezes) foi bastante alta. Não foi verificada presença de custo adaptativo associado à resistência de B. phoenicis a propargite. Portanto, o uso desses acaricidas também deve ser feito de maneira criteriosa no manejo da resistência de B. phoenicis a acaricidas.
Palavras-chave: Ácaro-da-leprose, propargite, cihexatim, manejo da resistência
ABSTRACT
Acaricides that inhibit cellular respiration play an important role in the control of Brevipalpus phoenicis (Geijskes) in citrus groves in Brazil. Studies were conducted to evaluate: (a) the variability in the susceptibility among B. phoenicis populations collected from citrus groves to cyhexatin, azocyclotin, propargite and sulphur; (b) cross-resistance relationships between propargite and azocyclotin, cyhexatin, dinocap, pyridaben and sulphur; and (c) the fitness cost associated with propargite resistance in B. phoenicis under laboratory conditions. A residual-type contact bioassay was used to characterize the susceptibility. The susceptibility was estimated with diagnostic concentrations based LC95 of each acaricide. The cross-resistance was evaluated by characterizing the concentration-mortality responses of susceptible (S) and propargite-resistant (Propargite-R) strains. The fitness cost was evaluated by measuring the biological parameters of S and Propargite-R strains on citrus fruits at 25 ± 1ºC and fotophase of 14h. Significant differences in the susceptibility of B. phoenicis were detected at diagnostic concentration of cyhexatin (survivorship from 16.3% to 80.5%), azocyclotin (from 3.0% to 15.0%), propargite (from 1.0% a 71.6%) and sulphur (from 9.0% to 82.6%). A low intensity of cross-resistance was detected between propargite and the acaricides azocyclotin (1.8-fold), cyhexatin (4.6-fold), dinocap (3.5-fold) and pyridaben (3.5-fold). On the other hand, the intensity of cross-resistance to sulphur (> 111-fold) was very high. There was no fitness cost associated with B. phoenicis resistance to propargite, based on biological parameters evaluated. Therefore, the use of these acaricides should also be done very carefully in resistance management of B. phoenicis to acaricides.
Key words: Flat mite, propargite, cyhexatin, resistance management
Os acaricidas inibidores da respiração celular têm sido bastante utilizados no manejo de ácaros em diversas culturas, devido à sua eficiência no controle e ao seu mecanismo de ação diferenciado. Esses acaricidas atuam em diversas etapas da respiração celular comprometendo, principalmente, a geração de energia (adenosina tri-fosfato - ATP) e são divididos de acordo com o seu provável modo de ação: (a) inibidores da fosforilação oxidativa via disrupção da síntese de ATP (organoestânicos, diafentiurom, propargite e tetradifom), (b) desacopladores da fosforilação oxidativa via disrupção do gradiente de próton H+ (clorfenapir e dinocape), (c) inibidores do transporte de elétrons no complexo I (piridabem, fenpiroximate, fenazaquim e tebufenpirade) e (d) no complexo III (acequinocil). Embora não esteja muito bem elucidado, o grupo dos inibidores da fosforilação oxidativa via disrupção da síntese de ATP são subdivididos em: (i) organoestânicos (cihexatim, óxido de fenbutatim e azociclotim), (ii) propargite e tetradifom e (iii) diafentiurom (Corbett et al. 1984, Dekeyser 2005, IRAC 2007). Além desses acaricidas orgânicos, o enxofre, um acaricida-fungicida inorgânico, apresenta um possível efeito na respiração celular (Hassall 1982).
Na citricultura brasileira são utilizados, principalmente para o controle do ácaro-da-leprose, Brevipalpus phoenicis (Geijskes), importante praga da cultura por ser o transmissor do vírus causador da leprose dos citros (Kitajima et al. 1972). Atualmente, entre os ingredientes ativos registrados para o seu controle quase a metade interfere na respiração celular (organoestânicos, propargite, clorfenapir, dinocape, piridabem, fenpiroximate e enxofre) (MAPA 2007). Dentro desse grupo de acaricidas, destacam-se os organoestânicos, propargite e enxofre (Nakano 1995, Cooperativa dos Cafeicultores e Citricultores de São Paulo 2001 - informação pessoal).
Como conseqüência da utilização intensa desses acaricidas um dos grandes entraves para a continuidade do sucesso no seu uso tem sido a rápida evolução da resistência detectada em várias espécies de ácaros de importância econômica (Edge & James 1986, Stumpf & Nauen 2001). Casos de resistência cruzada envolvendo acaricidas inibidores da respiração celular têm sido registrados, por exemplo, entre acaricidas organoestânicos (Edge & James 1986), entre inibidores do transporte de elétrons no complexo I (Stumpf & Nauen 2001) e com acaricidas de modos de ação distintos, por exemplo, entre propargite e dicofol (Grafton-Cardwell et al. 1987) e entre fenpiroximate e os acaricidas piridabem e dimetoato (Sato et al. 2004).
A estabilidade da resistência de ácaros a acaricidas inibidores da respiração celular tem comprometido as estratégias de manejo da resistência, ou seja, a freqüência de resistência se mantém relativamente estável mesmo na ausência da pressão de seleção. Os principais fatores que afetam a dinâmica da resistência são: (a) o custo adaptativo dos indivíduos resistentes na ausência de pressão de seleção e (b) a imigração de indivíduos suscetíveis. Casos de estabilidade da resistência a acaricidas inibidores da respiração celular em condições de laboratório e campo já foram detectados para cihexatim, propargite e óxido de fenbutatim (Hoy & Conley 1989, Hoy et al. 1988, Tian et al. 1992). Casos de instabilidade da resistência também têm sido relatados para cihexatim e fenpiroximate, no entanto, a reversão para a suscetibilidade foi bastante lenta (Edge & James 1986, Sato et al. 2004).
A evolução da resistência de B. phoenicis a acaricidas tem comprometido a eficácia de diversos acaricidas que são utilizados em rotação. Casos de resistência foram detectados para dicofol (modo de ação desconhecido), para hexitiazox (regulador de crescimento de ácaros) e para propargite (inibidor da fosforilação oxidativa via disrupção da síntese de ATP) (Omoto et al. 2000, Campos & Omoto 2002, Franco 2002). Apesar do intenso uso de acaricidas organoestânicos, até o ano de 1999, não foram detectados casos de resistência a níveis acima da freqüência crítica (> 10% de indivíduos resistentes) em populações de B. phoenicis para óxido de fenbutatim e cihexatim em pomares de citros do estado de São Paulo (Konno et al. 2001). Entretanto, nos últimos anos, aumentaram as reclamações de falhas no controle de B. phoenicis pelo uso de organoestânicos e outros acaricidas inibidores da respiração celular, sendo aludida a evolução da resistência como um dos fatores associados a essas falhas.
O objetivo do presente trabalho foi avaliar se os relatos de falhas no controle de B. phoenicis a acaricidas inibidores da respiração celular em pomares de citros se devem à resistência, bem como fornecer subsídios para o manejo da resistência. Inicialmente foram realizados estudos para avaliar a variabilidade na suscetibilidade de populações de B. phoenicis aos acaricidas cihexatim, azociclotim, propargite e enxofre. Posteriormente, foram realizados estudos para avaliar as relações de resistência cruzada entre propargite (inibidor da ATPase mediada pelo íon Mg2+) e os acaricidas cihexatim e azociclotim (ambos organoestânicos), dinocape (desacoplador da fosforilação oxidativa via disrupção do gradiente de próton H+), piridabem (inibidor do transporte de elétrons no complexo I) e enxofre (acaricida-fungicida inorgânico). Por fim, avaliou-se o custo adaptativo associado à resistência de B. phoenicis a propargite em condições de laboratório.
Material e Métodos
Populações de B. phoenicis. Foram coletadas 17 populações de B. phoenicis em diferentes pomares de citros do estado de São Paulo, de 2004 a 2006 (Tabela 1). Em cada pomar foram coletados cerca de 40 frutos infestados com o ácaro-da-leprose. Esses frutos foram acondicionados em caixas de papelão ou isopor. No laboratório, os ácaros foram retirados dos frutos utilizando um pincel com apenas um pêlo, sob microscópio estereoscópico, e transferidos para frutos de citros. As populações em laboratório foram iniciadas com cerca de 200 a 300 ácaros.
Além dessas populações, foram utilizadas as linhagens de B. phoenicis suscetível (S) e resistente a propargite (Propargite-R). A linhagem S foi coletada em um pomar de citros no município de Piracicaba, SP, em 2000. A linhagem Propargite-R, com razão de resistência estimada em 10 vezes, foi obtida a partir de uma população coletada em Barretos, SP, e selecionada em condições de laboratório (Franco 2002).
Criação de B. phoenicis. As populações de B. phoenicis foram mantidas em frutos de laranja das variedades Valência ou Pera Rio. Os frutos foram lavados em água corrente e parafinados, deixando uma área de 10 cm2 a 16 cm2 para permitir a colonização dos ácaros. Essa área foi delimitada com cola entomológica para evitar a fuga dos ácaros e circundada com uma fita plástica de poliestireno de aproximadamente 1,5 cm de largura. Uma mistura de areia, gesso, farinha de trigo e água na proporção de 4:1:1:3 foi pincelada nos frutos para simular sintomas de verrugose que favorecem o desenvolvimento do ácaro. Os frutos foram renovados em intervalos de 20 a 30 dias, deixando a área do fruto novo e do fruto infestado em contato, por uma semana, para a transferência dos ácaros para o fruto novo. A sala de criação foi mantida a 25 ± 2°C, umidade relativa de 70 ± 10% e fotofase de 14h.
Bioensaios toxicológicos. O método de bioensaio adotado para a caracterização toxicológica das populações de B. phoenicis foi o de contato residual. Foram utilizadas as formulações comerciais dos seguintes ingredientes ativos (I.A.) para realização dos bioensaios: azociclotim (Caligur, 500 g de I.A./L, suspensão concentrada, Bayer CropScience Ltda.), cihexatim (Hokko Cyhexatin 500, 500 g de I.A./kg, pó molhável, Hokko do Brasil Indústria Química e Agropecuária Ltda.), dinocape (Karathane EC, 369 g de I.A./L, concentrado emulsionável, Dow AgroSciences Industrial Ltda.), piridabem (Sanmite, 200 g de I.A./L, concentrado emulsionável, Basf S.A.), enxofre (Kumulus DF, 800 g de I.A./kg, granulado dispersível, Basf S.A.) e propargite (Omite 720 CE, 720 g de I.A./L, concentrado emulsionável, Crompton Ltda.). As diferentes concentrações de acaricidas foram preparadas a partir da diluição do produto comercial em água destilada.
O bioensaio foi realizado em discos de folha de laranja da variedade Valência de 2,6 cm de diâmetro. A superfície adaxial dos discos foi pulverizada com um volume de 2 ml de cada concentração do acaricida testado, utilizando a torre de pulverização de Potter (Burkard Manufacturing, Rickmansworth, Inglaterra) calibrada à pressão de 68,95 kPa. Nessas condições de pulverização foi obtido um depósito médio de 1,5 mg de solução/cm2. Em seguida, os discos de folha foram acondicionados em placas acrílicas de 3,5 cm de diâmetro (Falcon 1008, Becton Dickinson Labware, Lincoln Park, NJ, Estados Unidos) contendo aproximadamente 2 ml de uma mistura não-geleificada de ágar-água na concentração de 2,5%. Uma barreira dessa mistura foi construída ao redor dos discos de folha para evitar a fuga dos ácaros (Kabir et al. 1993). Foram transferidos 10 ácaros adultos de B. phoenicis para cada placa, com auxílio de um pincel com um pêlo sob dois microscópios estereoscópico. As placas foram mantidas em câmara climatizada regulada a 25 ± 1ºC e fotofase de 14h.
A avaliação da mortalidade foi realizada após 24h de exposição para o azociclotim, cihexatim, dinocape, piridabem e propargite; e após 48h de exposição para o enxofre. O critério de mortalidade adotado foi os ácaros que não responderam ao toque com um pincel de um pêlo com movimentos vigorosos e coordenados de seus apêndices foram colocados com a face ventral voltada para cima e os que não conseguiram voltar à posição normal foram considerados mortos. Os bioensaios que apresentaram mortalidade na testemunha superior a 15% foram descartados.
Monitoramento da suscetibilidade de populações de B. phoenicis a acaricidas inibidores da respiração celular. A suscetibilidade das populações de B. phoenicis coletadas em pomares de citros do estado de São Paulo foi avaliada para os acaricidas cihexatim, azociclotim, propargite e enxofre. As concentrações diagnósticas utilizadas foram 180 mg de cihexatim/L de água (Konno et al. 2001) e 720 mg de propargite/L de água (Franco 2002). Para os acaricidas azociclotim e enxofre, as concentrações diagnósticas foram definidas após caracterização da curva de concentração-mortalidade da linhagem S de B. phoenicis para esses dois acaricidas. Foram utilizadas cinco concentrações de cada acaricida, espaçadas em escala logarítmica, que proporcionaram mortalidade entre 5% e 99%. O delineamento experimental adotado foi inteiramente casualizado. O método de bioensaio adotado foi o contato residual. Cada concentração foi repetida cinco vezes, sendo que cada repetição foi constituída por quatro placas de bioensaio por concentração e duas placas na testemunha (pulverização com água destilada). Os dados de mortalidade foram submetidos à análise de Probit para estimar a concentração letal 50 (CL50) utilizando o programa POLO-PC (LeOra Software 1987). A concentração diagnóstica foi baseada na CL95 da linhagem S. O nível de significância do teste foi de a = 0,05.
Para o monitoramento da suscetibilidade de populações aos acaricidas cihexatim, propargite, enxofre e azociclotim o delineamento experimental adotado foi inteiramente casualizado. Para cada concentração diagnóstica testada, os bioensaios foram repetidos cinco vezes, sendo que cada repetição foi constituída por quatro placas de bioensaio por concentração e duas placas na testemunha (pulverização com água destilada). Os dados de porcentagem de sobrevivência (x) nas concentrações diagnósticas de cada acaricida foram transformados por arc sen  . Para avaliar a variabilidade quanto à suscetibilidade aos acaricidas testados os dados foram submetidos à análise de variância e as médias comparadas com a linhagem S pelo teste bilateral de Dunnett (proc glm). Para avaliar a possível relação de resistência cruzada entre os acaricidas testados os dados de sobrevivência nas concentrações diagnósticas foram submetidos à análise de correlação para verificar a relação entre a sobrevivência ao acaricida cihexatim e aos acaricidas azociclotim, propargite e enxofre; entre o acaricida propargite e os acaricidas azociclotim e enxofre; e entre o acaricida enxofre e azociclotim (proc corr). As análises foram realizadas com o programa estatístico SAS System for Windows versão 8.2. Os níveis de significância dos testes foram de a = 0,05.
. Para avaliar a variabilidade quanto à suscetibilidade aos acaricidas testados os dados foram submetidos à análise de variância e as médias comparadas com a linhagem S pelo teste bilateral de Dunnett (proc glm). Para avaliar a possível relação de resistência cruzada entre os acaricidas testados os dados de sobrevivência nas concentrações diagnósticas foram submetidos à análise de correlação para verificar a relação entre a sobrevivência ao acaricida cihexatim e aos acaricidas azociclotim, propargite e enxofre; entre o acaricida propargite e os acaricidas azociclotim e enxofre; e entre o acaricida enxofre e azociclotim (proc corr). As análises foram realizadas com o programa estatístico SAS System for Windows versão 8.2. Os níveis de significância dos testes foram de a = 0,05.
Relação de resistência cruzada entre acaricidas inibidores da respiração celular em B. phoenicis. A avaliação da resistência cruzada entre propargite e outros acaricidas que interferem no processo da respiração celular em B. phoenicis foi realizada mediante a caracterização das curvas de concentração-mortalidade das linhagens S e Propargite-R aos acaricidas azociclotim, cihexatim, dinocape, piridabem e enxofre. Foram utilizadas quatro ou cinco concentrações de cada acaricida, espaçadas em escala logarítmica, que proporcionaram mortalidade entre 5% e 99%. O delineamento experimental adotado foi inteiramente casualizado. O método de bioensaio adotado foi o contato residual. Cada concentração dos acaricidas testados foi repetida cinco vezes, sendo que cada repetição foi constituída por quatro placas de bioensaio por concentração e duas placas na testemunha (pulverização com água destilada). Os dados de mortalidade das linhagens S e Propargite-R de cada acaricida foram submetidos à análise de Probit para estimar a CL50 e aos testes de paralelismo e de igualdade das curvas de concentração-mortalidade. A intensidade da resistência cruzada foi obtida pela divisão da CL50 da linhagem Propargite-R pela CL50 da linhagem S e o intervalo de confiança foi estimado conforme método descrito por Robertson & Preisler (1992). O programa estatístico utilizado foi o POLO-PC. O nível de significância dos testes foi a = 0,05.
Avaliação do custo adaptativo associado à resistência de B. phoenicis a propargite. Os parâmetros biológicos das linhagens S e Propargite-R foram avaliados em frutos de laranja da variedade Valência em laboratório a 25 ± 1ºC e fotofase de 14h. Os frutos foram lavados em água corrente e parafinados, deixando uma área de cerca de 12 cm2. Para confinar os ácaros nos frutos foram utilizados tubos de acrílico transparente de 2,5 cm de diâmetro por 2 cm de altura. Esse tubo possuía duas aberturas de 1 cm de diâmetro fechadas com tela de poliéster (100 fios) para permitir ventilação. Cada tubo foi fixado na área sem parafina de um fruto, utilizando cera natural de abelha. Posteriormente, foram transferidos cinco ácaros adultos para cada fruto e o tubo foi fechado na parte superior com um filme de PVC. Após 12h, os ácaros foram retirados da arena, deixando-se apenas um ovo por fruto. A biologia foi iniciada com 41 e 32 ovos das linhagens S e Propargite-R respectivamente. As observações foram realizadas em intervalos de 12h para estimar os parâmetros de duração e mortalidade dos estágios de desenvolvimento (ovo, larva, protocrisálida, protoninfa, deutocrisálida, deutoninfa e teliocrisálida), período de pré-oviposição, oviposição e pós-oviposição e fecundidade (número de ovos/fêmea).
O delineamento experimental foi inteiramente casualizado. Os dados dos parâmetros biológicos avaliados para as linhagens S e Propargite-R foram comparados pelo teste t (proc ttest). O programa estatístico utilizado foi SAS System for Windows versão 8.2. O nível de significância do teste foi a = 0,05. A partir dos dados da biologia foi confeccionada a Tabela de Vida e Fertilidade para as linhagens S e Propargite-R utilizando o método descrito por Silveira Neto et al. (1976).
Resultados e Discussão
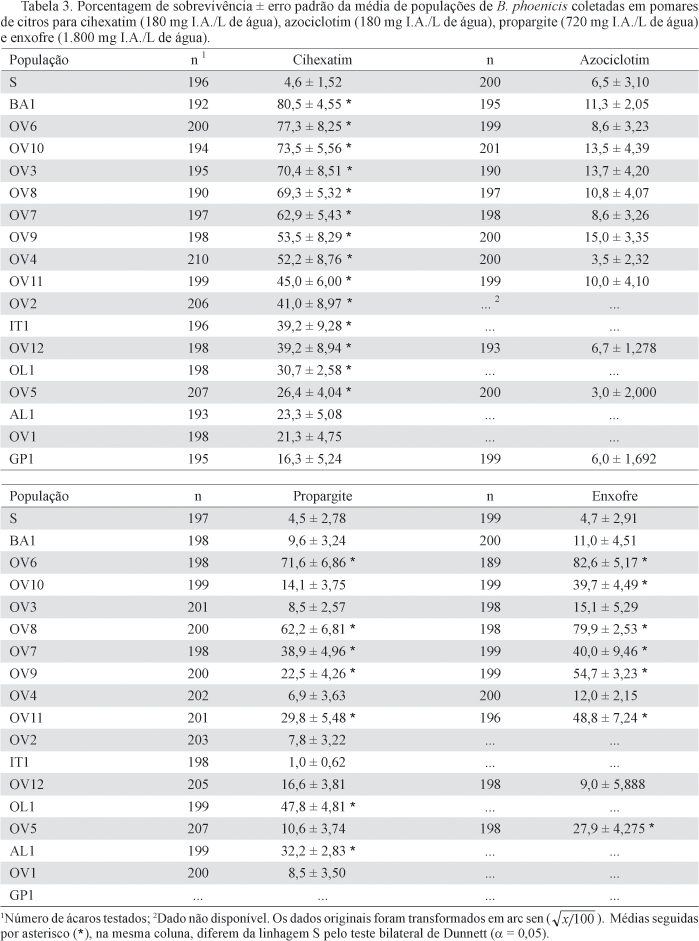
Monitoramento da suscetibilidade de populações de B. phoenicis a acaricidas inibidores da respiração celular. As concentrações diagnósticas definidas para o monitoramento da suscetibilidade de populações de B. phoenicis aos acaricidas azociclotim e enxofre foram 180 e 1.800 mg de I.A./L de água respectivamente (Tabela 2). Essas concentrações de azociclotim e enxofre proporcionaram mortalidades (± erro padrão da média) da linhagem S de 95,97% (± 1,007) e 97,92% (± 0,981) respectivamente.
Diferenças significativas na suscetibilidade de populações de B. phoenicis coletadas em pomares comerciais de citros foram verificadas aos acaricidas cihexatim, azociclotim, propargite e enxofre (Tabela 3). Para cihexatim, a sobrevivência estimada pela concentração diagnóstica variou entre 16,3% e 80,5% (F = 12,41; g.l. = 17, 72; P < 0,0001). Para azociclotim, a sobrevivência variou entre 3,0% e 15,0% (F = 2,16; g.l. = 11, 48; P = 0,0334), para propargite entre 1,0% e 71,6% (F = 17,08; g.l. = 17, 72; P < 0,0001) e para enxofre entre 9,0% e 82,6% (F = 22,30; g.l. = 11, 48; P < 0,0001). Para azociclotim, embora tenha sido observada diferença significativa entre as populações na concentração diagnóstica, as sobrevivências obtidas nas populações testadas não diferiram da linhagem S pelo teste bilateral de Dunnett (Tabela 3).
O monitoramento da suscetibilidade de populações de B. phoenicis a cihexatim, realizado em 1999, mostrou diferenças pouco expressivas na suscetibilidade, sendo que a sobrevivência na concentração diagnóstica foi inferior a 11% (Konno et al. 2001). Nos últimos anos, houve um aumento expressivo nos relatos de falhas no controle de B. phoenicis pelo uso dos acaricidas organoestânicos, sendo questionada a evolução da resistência como um dos fatores associados a essas falhas. Pelos resultados observados no presente trabalho, a existência de variabilidade quanto à suscetibilidade de populações de B. phoenicis a cihexatim, a sobrevivência na concentração diagnóstica próxima a 80% em algumas populações. A resistência foi identificada como um dos fatores para explicar essas falhas no controle.
Nas populações OV4, OV6, OV7, OV8 e OV11 não foram realizadas pulverizações de cihexatim nos últimos anos, mas a sobrevivência foi entre 45,0% e 77,3%, enquanto que na população IT1 a sobrevivência foi de 39,2% e foram realizadas quatro pulverizações de cihexatim (Tabelas 1 e 3). Uma hipótese que pode explicar esse resultado é a possibilidade de resistência cruzada entre cihexatim e outros acaricidas que favoreceram a seleção de ácaros resistentes para cihexatim.
A análise de correlação entre a sobrevivência das populações testadas na concentração diagnóstica de cihexatim e a sobrevivência na concentração diagnóstica de azociclotim foi significativa (r = 0,62; P = 0,0403). Portanto, a sobrevivência observada nas populações de B. phoenicis a cihexatim pode ser explicada pelo uso do azociclotim. A seleção de ácaros resistentes a cihexatim pelo uso do azociclotim pode ter ocorrido porque ambos acaricidas são organoestânicos e, portanto, atuam no mesmo sítio de ação, ou seja, inibem uma das etapas da fosforilação oxidativa (Corbett et al. 1984, IRAC 2007). Uma segunda explicação refere-se ao processo de degradação do azociclotim no ambiente que é degradado em cihexatim (Kordel & Stein 1997). A resistência cruzada entre os acaricidas cihexatim, óxido de fenbutatim e azociclotim já foi documentada em Tetranychus urticae Koch na Austrália (Edge & James 1986) e entre cihexatim e óxido de fenbutatim em T. urticae e Tetranychus pacificus McGregor nos Estados Unidos (Hoy et al. 1988, Tian et al. 1992).
Por outro lado, a análise de correlação entre a sobrevivência de B. phoenicis aos acaricidas cihexatim e propargite não foi significativa (r = 0,32; P = 0,2099), assim como, entre os acaricidas cihexatim e enxofre (r = 0,27; P = 0,4309). Entretanto, as populações de B. phoenicis OL1, OV6, OV7, OV8, OV9 e OV11 apresentaram alta sobrevivência nas concentrações diagósticas de cihexatim e de propargite (Tabela 3). As populações OV5, OV6, OV7, OV8, OV9, OV10 e OV11 também tiveram alta sobrevivência nas concentrações dignósticas de cihexatim e de enxofre (Tabela 3). Sendo assim, é possível que ocorra resistência cruzada ou múltipla entre cihexatim e propargite e entre cihexatim e enxofre em B. phoenicis.
A variabilidade na sobrevivência de populações de B. phoenicis para propargite também pode ser influenciada por outros acaricidas. A análise de correlação entre a sobrevivência nas concentrações diagnósticas de propargite e de azociclotim foi rejeitada (r = 0,16; P = 0,6358), enquanto que entre propargite e enxofre a correlação foi significativa (r = 0,89; P = 0,0002), indicando a possibilidade de relação de resistência cruzada entre propargite e enxofre. Por fim, a correlação entre a sobrevivência nas concentrações diagnósticas de enxofre e de azociclotim foi rejeitada (r = 0,29; P = 0,3949). Entre os acaricidas empregados no controle de ácaros nos pomares de citros avaliados o enxofre foi o principal ingrediente ativo, representou 31,7% a 67,7% (Tabela 1).
Relação de resistência cruzada entre acaricidas inibidores da respiração celular em B. phoenicis. Verificou-se resistência cruzada positiva entre propargite e os acaricidas azociclotim, cihexatim, dinocape, piridabem e enxofre em B. phoenicis (Tabela 4). Para azociclotim, a hipótese de igualdade entre as curvas de concentração-mortalidade das linhagens S e Propargite-R foi rejeitada (c2 = 166,36; g.l. = 2; P < 0,05), ou seja, as curvas foram diferentes, mas foi aceita a hipótese de igualdade dos coeficientes angulares (c2 = 0,50; g.l. = 1; P > 0,05), ou seja, as curvas foram paralelas (Fig. 1a). Para cihexatim, a hipótese de igualdade foi rejeitada (c2 = 552,11; g.l. = 2; P < 0,05) e aceita a hipótese de paralelismo (c2 = 1,46; g.l. = 1; P > 0,05) (Fig. 1b). Para dinocape, foram rejeitadas as hipóteses de igualdade (c2 = 564,51; g.l. = 2; P < 0,05) e de paralelismo (c2 = 6,58; g.l. = 1; P < 0,05) (Fig. 1c). Para piridabem, a hipótese de igualdade foi rejeitada (c2 = 492,84; g.l. = 2; P < 0,05) e a hipótese de paralelismo aceita (c2 = 0,082; g.l. = 1; P > 0,05) (Fig. 1d). Para enxofre, não foi possível estimar a CL50 da linhagem Propargite-R, sendo que a concentração de 56.000 mg I.A./L de água proporcionou mortalidade (± erro padrão da média) de 38,59% (± 3,733) (Fig. 2).
Os acaricidas inibidores da respiração celular atuam em diversas etapas causando a inibição ou disrupção da síntese de energia (ATP). Então, a presença de resistência cruzada entre alguns desses acaricidas observada em B. phoenicis pode ser devida à similaridade do modo de ação. Embora os acaricidas propargite e os organoestânicos azociclotim e cihexatim, inibidores da fosforilação oxidativa via disrupção da síntese de ATP, sejam classificados em subgrupos distintos (IRAC 2007), houve resistência cruzada entre propargite e os acaricidas azociclotim (intensidade da resistência cruzada de 1,8 vezes) e cihexatim (4,6 vezes).
O acaricida propargite interfere na síntese de ATP pela inibição da ATPase e os organoestânicos na inibição da fosforilação oxidativa (Corbett et al. 1984). Segundo Kadir & Knowles (1991) propargite proporcionou inibição de 90% da atividade da ATPase-Mg2+ e 32% da ATPase-Na+K+, enquanto que cihexatim foi responsável por 88% e 95% da inibição, respectivamente, sugerindo que a ATPase é um sítio de ação comum entre esses acaricidas. O acaricida dinocape atua como desacoplador da fosforilação oxidativa, entretanto, no processo de hidrólise um dos compostos metabolizados tem alta atividade como inibidor da fosforilação oxidativa (Corbett et al. 1984) que poderia explicar a resistência cruzada entre propargite e dinocape (3,5 vezes).
Casos de resistência cruzada envolvendo propargite foram observados com cihexatim em Tetranychus cinnabarinus (Boisduval) (Mansour & Plaut 1979) e com dicofol em T. urticae e T. pacificus (Grafton-Cardwell et al. 1987). Segundo Alves et al. (2000) não foi observada resistência cruzada entre o acaricida dicofol e os acaricidas propargite, óxido de fenbutatim e fenpiroximate em B. phoenicis.
No estudo do monitoramento da suscetibilidade de populações de B. phoenicis coletadas em pomares de citros não se encontrou correlação entre a sobrevivência na concentração diagnóstica de cihexatim e a sobrevivência na concentração diagnóstica de propargite, visto que algumas populações de B. phoenicis apresentaram alta sobrevivência a cihexatim e baixa sobrevivência a propargite (Tabela 3). Esses resultados podem ter sido causados por resistência múltipla, na qual dois ou mais mecanismos de resistência estariam envolvidos. Segundo Grafton-Cardwell et al. (1987) a resistência entre propargite e dicofol pode ser um caso de resistência múltipla porque apenas 9% das populações de T. urticae e 16% das populações de T. pacificus avaliadas quanto à suscetibilidade a propargite e dicofol mostraram resistência a ambos acaricidas.
A resistência cruzada observada em B. phoenicis entre propargite e piridabem (3,5 vezes) e entre propargite e enxofre (> 111 vezes) poderia ser um caso de resistência múltipla, pois são compostos que atuam em sítios de ação distintos. No entanto, a maior atividade das monooxigenases dependentes do citocromo P-450 e as esterases em linhagens resistentes a acaricidas inibidores da respiração celular tem sido apontada como responsável pela destoxificação metabólica (Stumpf & Nauen 2001, Leeuwen et al. 2005). Sendo assim, trabalhos futuros também deverão focar os mecanismos de resistência envolvidos na evolução da resistência de B. phoenicis a acaricidas para certificar se trata de um caso de resistência cruzada ou resistência múltipla.
No manejo da resistência, a rotação de acaricidas tem sido uma das principais estratégias utilizadas para prevenir e/ou retardar a evolução da resistência de artrópodes a pesticidas, inclusive para B. phoenicis (Alves et al. 2000). A recomendação dos acaricidas em rotação ou mistura é baseada no seu modo de ação e na ausência de resistência cruzada.
Os acaricidas organoestânicos e propargite pertencem ao grupo dos inibidores da fosforilação oxidativa via disrupção da síntese de ATP, mas são recomendados em rotação por causa de diferenças nos sítios de ação (IRAC 2007). No entanto, no presente trabalho a resistência cruzada foi registrada entre esses acaricidas, assim como entre propargite e os acaricidas dinocape (desacoplador da fosforilação oxidativa) e piridabem (inibidor do transporte de elétrons - complexo I). Entretanto, é necessário estudar a persistência da atividade biológica desses acaricidas na discriminação de ácaros resistentes em condições de campo porque é possível que a baixa intensidade de resistência não seja suficiente para causar fracasso no controle quando utilizados em rotação com propargite. Por outro lado, deve-se evitar pulverizar propargite antes ou logo após a pulverização de enxofre ou em mistura nos pomares de citros, devida à alta intensidade de resistência cruzada (> 111 vezes).
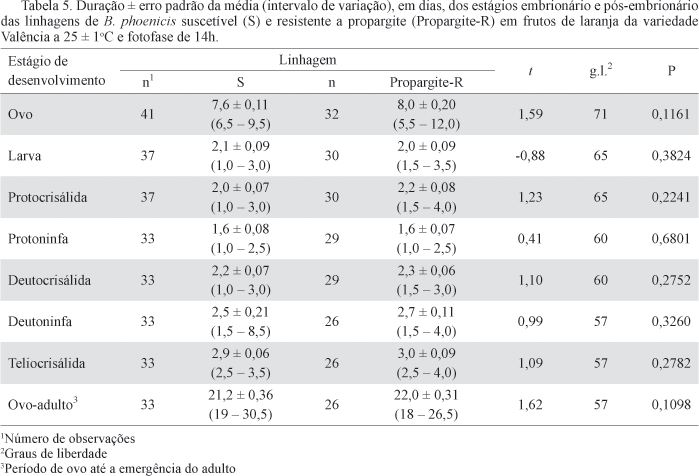
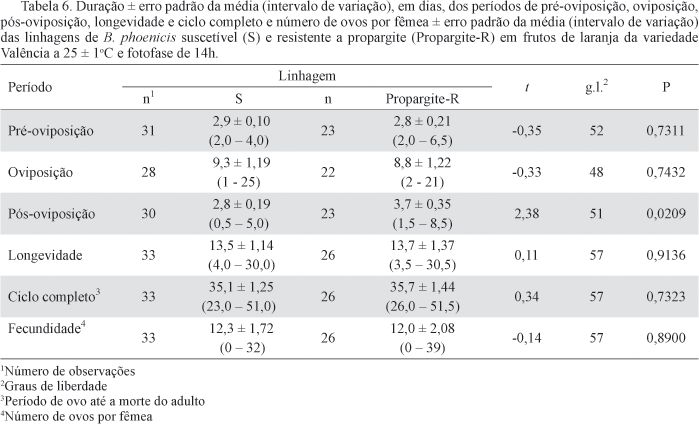
Avaliação do custo adaptativo associado à resistência de B. phoenicis a propargite. Não foram observadas diferenças significativas entre as linhagens S e Propargite-R quanto à duração dos estágios de desenvolvimento de ovo a adulto (Tabela 5), assim como, na fase adulta quanto à duração do período de pré-oviposição, oviposição, longevidade e fecundidade (número médio de ovos/fêmea), exceto para o período de pós-oviposição que foi maior para a linhagem Propargite-R do que para a linhagem S (Tabela 6).
Os parâmetros biológicos estimados a partir do cálculo da tabela de vida e fertilidade foram bastante próximos entre as linhagens S e Propargite-R. A taxa líquida de reprodução (Ro) da linhagem S e Propargite-R foi 20,49 e 19,50, a capacidade intrínseca de aumento (rm) foi 0,100 e 0,097, a razão finita de aumento (l) foi 1,105 e 1,102 e a duração média de uma geração foi 30,35 e 30,70 dias respectivamente.
Segundo Flexner et al. (1989), a reversão para a suscetibilidade em T. urticae a cihexatim ocorreu após três ou seis gerações, em condições de laboratório e a presença de custo adaptativo foi um dos fatores responsáveis pela instabilidade da resistência, uma vez que o tempo de desenvolvimento foi maior na linhagem resistente que na linhagem suscetível. Outros casos de instabilidade da resistência também ocorreram em T. urticae a cihexatim e fenpiroximate, entretanto, a reversão para a suscetibilidade foi lenta (Edge & James 1986, Sato et al. 2004). Casos de estabilidade da resistência de ácaros aos acaricidas inibidores da respiração celular já foram observados em condições de laboratório em T. pacificus a cihexatim e propargite (Hoy et al. 1988, Hoy & Conley 1989) e em condições de campo em T. urticae a cihexatim e óxido de fenbutatim (Tian et al. 1992).
A resistência de B. phoenicis a hexitiazox (razão de resistência > 10.000 vezes) foi estável em condições de laboratório e associada à ausência de custo adaptativo. No entanto, em condições de campo, a resistência apresentou instabilidade em rotação de acaricidas (Campos & Omoto 2002, 2006). A presença de custo adaptativo em B. phoenicis é importante para o restabelecimento da suscetibilidade, uma vez que a imigração de ácaros suscetíveis provenientes de plantas hospedeiras para plantas cítricas foi considerada baixa (Alves et al. 2005). O custo adaptativo pode se expressar não apenas em parâmetros biológicos, como tempo de desenvolvimento e fecundidade, mas em outras características importantes para sobrevivência e reprodução, como aspectos comportamentais, competição intra e interespecífica (predação). Essas diferenças também podem ser influenciadas pelas condições ambientais como temperatura, umidade e hospedeiro.
Pelos resultados deste trabalho conclui-se que não há custo adaptativo de B. phoenicis associado à resistência a propargite para os parâmetros biológicos avaliados no laboratório. Entretanto, são necessários estudos de dinâmica da resistência em condições de campo para que estratégias efetivas de manejo da resistência de B. phoenicis a propargite possam ser implementadas.
Implicações para o manejo da resistência de B. phoenicis aos acaricidas inibidores da respiração celular. Estudos de monitoramento da suscetibilidade são de grande importância prática para verificar a magnitude da resistência. Também é fundamental a conscientização dos citricultores e técnicos da necessidade da adoção de estratégias de manejo da resistência. Para o controle satisfatório de B. phoenicis em citros, além dos estudos de monitoramento da suscetibilidade, resistência cruzada e dinâmica da resistência, são importantes trabalhos que visem aprimorar a tecnologia de aplicação de agroquímicos, maximizando a eficiência no controle, estudos de seletividade a inimigos naturais, refinamento das técnicas de amostragem da densidade populacional de ácaros e outros métodos de controle que contribuam na redução da pressão de seleção pelo uso constante de acaricidas. Dessa forma será possível implementar programas efetivos de manejo da resistência de B. phoenicis em citros, assim manter a citricultura competitiva, principalmente, com o aumento das exigências do mercado e a redução no número de ingredientes ativos disponíveis para o controle dessa praga.
Agradecimentos
À Fischer S.A. pelo auxílio e fornecimento de material para execução deste trabalho. Ao Fundo de Defesa da Citricultura (FUNDECITRUS) e à Fundação de Amparo à Pesquisa do Estado de São Paulo (FAPESP) pelo apoio financeiro para o desenvolvimento desse projeto e pela concessão de bolsas de estudo.
Received 29/I/07. Accepted 19/III/07.
- Alves, E.B., C. Omoto & C.R. Franco. 2000. Resistência cruzada entre o dicofol e outros acaricidas em Brevipalpus phoenicis (Geijskes) (Acari: Tenuipalpidae). An. Soc. Entomol. Brasil 29: 765-771.
- Alves, E.B., N.F.B. Casarin & C. Omoto. 2005. Mecanismos de dispersão de Brevipalpus phoenicis (Geijskes) (Acari: Tenuipalpidae) em pomares de citros. Neotrop. Entomol. 34: 89-96.
- Campos, F.J. & C. Omoto. 2002. Resistance to hexythiazox in Brevipalpus phoenicis (Acari: Tenuipalpidae) from Brazilian citrus. Exp. Appl. Acarol. 26: 243-251.
- Campos, F.J. & C. Omoto. 2006. Estabilidade da Resistência de Brevipalpus phoenicis (Geijskes) (Acari: Tenuipalpidae) a hexythiazox em pomares de citros. Neotrop. Entomol. 35: 840-848.
- Corbett, J.R., K.Wright & A.C. Baillie. 1984. The biochemical mode of action of pesticides. London, Academic Press, 382p.
- Dekeyser, M.A. 2005. Acaricide mode of action. Pest Manag. Sci. 61: 103-110.
- Edge, V.E. & D.G. James. 1986. Organo-tin resistance in Tetranychus urticae (Acari: Tetranychidae) in Australia. J. Econ. Entomol. 79: 1477-1483.
- Flexner, J.L., K.M. Theiling, B.A. Croft & P.H. Westigard. 1989. Fitness and immigration: Factors affecting reversion of organotin resistance in the Twospotted spider mite (Acari: Tetranychidae). J. Econ. Entomol. 82: 996-1002.
- Franco, C.R. 2002. Detecção e caracterização da resistência de Brevipalpus phoenicis (Geijskes, 1939) (Acari: Tenuipalpidae) ao acaricida propargite. Dissertação de Mestrado, Escola Superior de Agricultura "Luiz de Queiroz", USP, Piracicaba, 64p.
- Grafton-Cardwell, E.E., J. Granett & T.F. Leigh. 1987. Spider mites species (Acari: Tetranychidae) response to propargite: Basis for an acaricide resistance management program. J. Econ. Entomol. 80: 579-587.
- Hassall, K.A. 1982. The chemistry of pesticides: Their metabolism, mode of action and uses in crop protection. London, The Macmillan Press, 372p.
- Hoy, M.A. & J. Conley. 1989. Propargite resistance in Pacific spider mite (Acari: Tetranychidae): Stability and mode of inheritance. J. Econ. Entomol. 82: 11-16.
- Hoy, M.A., J. Conley & W. Robinson. 1988. Cyhexatin and fenbutatin-oxide resistance in pacific spider mite (Acari: Tetranychidae): stability and mode of inheritance. J. Econ. Entomol. 81: 57-64.
- IRAC. Insecticide Resistance Action Committee. 2007. The Irac eClassification: An interactive mode of action (MoA) tool. Disponível em www.irac-online.org/eclassification/ Acesso em 22/01/2007.
- Kabir, K.H., R.B. Chapman & D.R. Penman. 1993. Miticide bioassays with spider mites (Acari: Tetranychidae): Effect of test method, exposure period and mortality criterion on the precision of response estimates. Exp. Appl. Acarol. 17: 695-708.
- Kadir, H.A. & C.O. Knowles. 1991. Inhibition of ATP dephosphorylation by acaricides with emphasis on the anti-ATPase activity of the carbodiimide metabolite of diafenthiuron. J. Econ. Entomol. 84: 801-805.
- Kitajima, E.W., G.W. Müller, A.S. Costa & V.A. Yuki. 1972. Short, rod-like particles associated with citrus leprosies. Virology 50: 254-258.
- Konno, R.H., C.R. Franco & C. Omoto. 2001. Suscetibilidade de populações de Brevipalpus phoenicis (Geijskes, 1939) (Acari: Tenuipalpidae) a acaricidas organoestânicos em citros. Sci. Agric. 58: 703-709.
- Kordel, W. & B. Stein. 1997. Fate of the organotin pesticide azocyclotin in aquatic microcosms. Chemosphere 35: 191-207.
- Leeuwen, T. Van, S. Van Pottelberge & L. Tirry. 2005. Comparative acaricide susceptibility and detoxifying enzyme activities in field-collected resistant and susceptible strains of Tetranychus urticae Koch. Pest Manag. Sci. 61: 499-507.
- LeOra Software. 1987. Polo-PC: A user's guide to probit or logit analysis. Berkeley, 20p.
- Mansour, F.A. & H.N. Plaut. 1979. The effectiveness of various acaricides against resistant and susceptible carmine spider mites. Phytoparasitica 7: 185-193.
- MAPA. Ministério da Agricultura, Pecuária e Abastecimento. 2007. AGROFIT: Sistema de Agrotóxicos Fitossanitários. Disponível em www.agricultura.gov.br/ Acesso em 25/01/2007.
- Nakano, O. 1995. Rotatividade de ingredientes ativos em citros, p.189-194. In C.A.L. Oliveira & L.C. Donadio (eds.), Leprose dos citros. Jaboticabal, Funep, 219p.
- Omoto, C., E.B. Alves & P.C. Ribeiro. 2000. Detecção e monitoramento da resistência de Brevipalpus phoenicis (Geijskes) (Acari: Tenuipalpidae) ao dicofol. An. Soc. Entomol. Brasil 29: 757-764.
- Robertson, J.L. & H.K. Preisler. 1992. Pesticide bioassay with arthropods. Boca Ranton, CRC Press, 127p.
- Sato, M.E., T. Miyata, M. da Silva, A. Raga & M.F. de Souza Filho. 2004. Selections for fenpyroximate resistance and susceptibility, and inheritance, cross-resistance and stability of fenpyroximate resistance in Tetranychus urticae Koch (Acari: Tetranychidae). Appl. Entomol. Zool. 39: 293-302.
- Silveira Neto, S., O. Nakano, D. Barbin & N.A. Villa Nova. 1976. Manual de ecologia dos insetos. Piracicaba, Agronômica Ceres, 419p.
- Stumpf, N. & R. Nauen. 2001. Cross resistance, inheritance, and biochemistry of mitochondrial electron transport inhibitor-acaricide resistance in Tetranychus urticae (Acari: Tetranychidae). J. Econ. Entomol. 94: 1577-1583.
- Tian, T., E.E. Grafton-Cardwell & J. Granett. 1992. Resistance of Tetranychus urticae Koch (Acari: Tetranychidae) to cyhexatin and fenbutatin-oxide in California pears. J. Econ. Entomol. 85: 2088-2095.
Datas de Publicação
-
Publicação nesta coleção
02 Out 2007 -
Data do Fascículo
Ago 2007
Histórico
-
Aceito
19 Mar 2007 -
Recebido
29 Jan 2007