Resumos
Este trabalho resume os dados de florística e fitossociologia de 11, das 14 parcelas de 1 ha, alocadas ao longo do gradiente altitudinal da Serra do Mar, São Paulo, Brasil. As parcelas começam na cota 10 m (Floresta de Restinga da Praia da Fazenda, município de Ubatuba) e estão distribuídas até a cota 1100 m (Floresta Ombrófila Densa Montana da Trilha do rio Itamambuca, município de São Luis do Paraitinga) abrangendo os Núcleos Picinguaba e Santa Virgínia do Parque Estadual da Serra do Mar. Na Restinga o solo é Neossolo Quartzarênico francamente arenoso, enquanto que na encosta o solo é um Cambisolo Háplico Distrófico argilo-arenoso, sendo que todas as parcelas apresentaram solo ácido (pH 3 - 4) com alta diluição de nutrientes e alta saturação de alumínio. Na Restinga e no sopé da encosta o clima é Tropical/Subtropical Úmido (Af/Cfa), sem estação seca, com precipitação média anual superior a 2.200 mm e temperatura média anual de 22 ºC. Subindo a encosta mantêm-se a média de precipitação, mas há um gradativo resfriamento, de forma que a 1.100 m o clima é Subtropical Úmido (Cfa/Cfb), sem estação seca, com temperatura média anual de 17 ºC. Destaca-se ainda que, quase diariamente, a parte superior da encosta, geralmente acima de 400 m, é coberta por uma densa neblina. Nas 14 parcelas foram marcados, medidos e amostrados 21.733 indivíduos com DAP > 4,8 cm, incluindo árvores, palmeiras e fetos arborescentes. O número médio de indivíduos amostrados nas 14 parcelas foi de 1.264 ind.ha-1 (± 218 EP de 95%). Dentro dos parâmetros considerados predominaram as árvores (71% FOD Montana a 90% na Restinga), seguidas de palmeiras (10% na Restinga a 25% na FOD Montana) e fetos arborescentes (0% na Restinga a 4% na FOD Montana). Neste aspecto destaca-se a FOD Terras Baixas Exploradas com apenas 1,8% de palmeiras e surpreendentes 10% de fetos arborescentes. O dossel é irregular, com altura variando de 7 a 9 m, raramente as árvores emergentes chegam a 18 m, e a irregularidade do dossel permite a entrada de luz suficiente para o desenvolvimento de centenas de espécies epífitas. Com exceção da FOD Montana, onde o número de mortos foi superior a 5% dos indivíduos amostrados, nas demais fitofisionomias este valor ficou abaixo de 2,5%. Nas 11 parcelas onde foi realizado o estudo florístico foram encontradas 562 espécies distribuídas em 195 gêneros e 68 famílias. Apenas sete espécies - Euterpe edulis Mart. (Arecaceae), Calyptranthes lucida Mart. ex DC. e Marlierea tomentosa Cambess (ambas Myrtaceae), Guapira opposita (Vell.) Reitz (Nyctaginaceae), Cupania oblongifolia Mart. (Sapindaceae) e as Urticaceae Cecropia glaziovii Snethl. e Coussapoa microcarpa (Schott) Rizzini - ocorreram da Floresta de Restinga à FOD Montana, enquanto outras 12 espécies só não ocorreram na Floresta de Restinga. As famílias com o maior número de espécies são Myrtaceae (133 spp), Fabaceae (47 spp), Rubiaceae (49) e Lauraceae (49) ao longo de todo gradiente da FOD e Monimiaceae (21) especificamente nas parcelas da FOD Montana. Em termos de número de indivíduos as famílias mais importantes foram Arecaceae, Rubiaceae, Myrtaceae, Sapotaceae, Lauraceae e na FOD Montana, Monimiaceae. Somente na parcela F, onde ocorreu exploração de madeira entre 1960 e 1985, a abundância de palmeiras foi substituída pelas Cyatheaceae. O gradiente estudado apresenta um pico da diversidade e riqueza nas altitudes intermediárias (300 a 400 m) ao longo da encosta (índice de Shannon-Weiner - H' - variando de 3,96 a 4,48 nats.indivíduo -1). Diversas explicações para este resultado são apresentadas neste trabalho, incluindo o fato dessas altitudes estarem nos limites das expansões e retrações das diferentes fitofisionomias da FOD Atlântica durante as flutuações climáticas do Pleistoceno. Os dados aqui apresentados demonstram a extraordinária riqueza de espécies arbóreas da Floresta Ombrófila Densa Atlântica dos Núcleos Picinguaba e Santa Virgínia do Parque Estadual da Serra do Mar, reforçando a importância de sua conservação ao longo de todo o gradiente altitudinal. A diversidade desta floresta justifica também o investimento de longo prazo, através de parcelas permanentes, para compreender sua dinâmica e funcionamento, bem como monitorar o impacto das mudanças climáticas nessa vegetação.
Parque Estadual da Serra do Mar; Núcleo Picinguaba; Núcleo Santa Virgínia; riqueza de espécies; fitofisionomias; Sistema de Classificação da Vegetação; Projeto BIOTA Gradiente Funcional
This paper summarizes floristic and phytossociology data of 11, out of 14 plots of 1 ha, allocated along an altitudinal gradient in the Serra do Mar, São Paulo, Brazil. The study was conducted at Serra do Mar State Park and the plots start at the sea level (10 m - plot of Restinga Forest that occurs at Praia da Fazenda, Picinguaba, municipality of Ubatuba) up to 1100 m above sea level (the Montane Ombrophilous Dense occurs alongside the Itamambuca Trail, municipality of São Luis do Paraitinga). The Restinga Forest occurs in Pleistocenic Coastal Plain where the soil is classified as a sandy Quartzipsamment (Quartzenic Neosol), while along the slopes of the Serra do Mar, the Ombrophylus Dense Forest grows on the top of a pre-Cambrian crystalline basement with granitic rocks, where the soil is a sandy-loam Dystrophic Inceptisol (Cambisol/Latosol). In all 14 plots soils are acidic (pH 3 - 4), chemically poor, with high dilution of nutrients and high saturation of aluminum. In the Restinga and at the foot of the slope the climate is Tropical/Subtropical Humid (Af/Cfa), with no dry season, an average annual rainfall over 2,200 mm and an average annual temperature of 22 ºC. Towards the top of the Serra do Mar there is a gradual cooling along the slope, but there is no reduction in rainfall, so at 1,100 m above sea level the climate is classified as Humid Subtropical (Cfa/Cfb), with no dry season and an average annual temperature of 17 ºC. It is important to remark that, almost daily, from 400 m above sea level up to the top of slopes the mountains are covered by a dense fog. In the 14 plots 21,733 individuals with DBH > 4.8 cm, including trees, palms and ferns, were marked, measured and sampled. The average number of individuals sampled in each plot was 1264 ind.ha-1(± 218 SE 95%). Within the parameters considered trees prevailed (71% in the Montane ODF to 90% in the Restinga Forest), followed by palms (10% in the RF and 25% in the Montane Ombrophilous Dense Forest/ODF) and ferns (0% % in the RF and 4% in the Montane ODF). Regarding these proportions the Exploited Lowlands ODF differs from the others with only 1.8% of palm trees and striking 10% of ferns. The forest canopy is irregular with heights ranging from 7 to 9 m, rarely emergent trees reach 18 m, and due to this irregularity of the canopy the amount of light that gets through sets conditions for the development of hundreds of epiphytic species. Aside from Montana ODF, where the number of dead trees was more than 5% of individuals sampled, in the other phytophysiognomies this value was below 2.5%. In the 11 plots where the floristic study was conducted we found 562 species in 195 genera and 68 families. Only seven species - Euterpe edulis Mart. (Arecaceae), Calyptranthes lucida Mart. ex DC. and Marlierea tomentosa Cambess (both Myrtaceae), Guapira opposita (Vell.) Reitz (Nyctaginaceae), Cupania oblongifolia Mart. (Sapindaceae), Cecropia glaziovii Snethl. and Coussapoa microcarpa (Schott) Rizzini (both Urticaceae) - occurred from Restinga to Montane ODF, while 12 other species did not occur only in the Restinga Forest. Families with the greatest number of species are Myrtaceae (133 spp), Fabaceae (47 spp), Rubiaceae (49) and Lauraceae (49) throughout the gradient and Monimiaceae (21) specifically in portions Montane ODF. Only in the F plot, where logging has occurred between 1950 and 1985, the abundance of palm trees has been replaced by Cyatheaceae. The study shows a peak of diversity and richness, Shannon-Weiner index (H') ranging from 3.96 to 4.48 nats.ind-1, in the intermediate altitudes (300 to 400 m) along the slope. Several explanations for this result are raised here, including the fact that these elevations are within the limits expansions and retractions of the different phytophysiognomies of the Atlantic ODF due to climate fluctuations during the Pleistocene. The results presented in this paper demonstrate the extraordinary richness of tree species of the Atlantic Rainforest from the northeastern coast of the State of Sao Paulo, reinforcing the importance of its conservation throughout the altitudinal gradient. The richness of this forest justifies a long term commitment to study its dynamics and functioning through permanent plots, and monitor the impacts of climate change in this vegetation.
Serra do Mar State Park; Nucleo Picinguaba; Nucleo Santa Virginia; species richness; phytophysiognomies; Vegetation Classification System; BIOTA Functional Gradient Project
ARTIGOS
Florística e fitossociologia em parcelas permanentes da Mata Atlântica do sudeste do Brasil ao longo de um gradiente altitudinal
Floristic and phytosociology in permanent plots of the Atlantic Rainforest along an altitudinal gradient in southeastern Brazil
Carlos Alfredo JolyI,* * Autor para correspondência, Carlos Alfredo Joly, e-mail: cjoly@unicamp.br ; Marco Antonio AssisII; Luis Carlos BernacciIII; Jorge Yoshio TamashiroI; Mariana Cruz Rodrigues de CamposI; José Ataliba Mantelli Aboin GomesIII; Maryland Sanchez LacerdaIV; Flávio Antonio Mães dos SantosI; Fernando PedroniIV; Larissa de Souza PereiraI; Maíra de Campos Gorgulho PadgurschiI; Eduardo Magalhães Borges PrataII; Eliana RamosIII; Roseli Buzanelli TorresIII; André RochelleI; Fernando Roberto MartinsI; Luciana Ferreira AlvesV; Simone Aparecida VieiraVI; Luiz Antonio MartinelliVII; Plínio Barbosa de CamargoVII; Marcos Pereira Marinho AidarV; Pedro Vasconcellos EisenlohrI; Eliane SimõesVIII; João Paulo VillaniIX; Renato BelinelloI
IDepartamento Biologia Vegetal, Instituto de Biologia - IB, Universidade Estadual de Campinas - UNICAMP, CP 6109, Barão Geraldo, CEP 13081-970, Campinas, SP, Brasil
IIDepartamento de Botânica, Instituto de Biociências, Universidade Estadual Paulista - UNESP, Av. 24A,1515, Bela Vista, CP 199, CEP 13506900, Rio Claro, SP, Brasil
IIINúcleo de Pesquisa e Desenvolvimento Jardim Botânico - CEC, Instituto Agronômico de Campinas - IAC, Av. Barão de Itapura, 1481, CP 28, Jardim Guanabara, CP 28, CEP 13001-970, Campinas, SP, Brasil
IVInstituto de Ciências Biológicas e da Saúde, Universidade Federal de Mato Grosso do Sul - UFMS, Rod. MT 100, Km 3,5, Setor Universitário, CEP 78698-000, Pontal do Araguaia, MT, Brasil
VInstituto de Botânica - IBt, Secretaria do Meio Ambiente do Estado - SMA, Av. Miguel Estéfano, 3687, Água Funda, CEP 04301-902, São Paulo, SP, Brasil
VINúcleo de Estudos e Pesquisas Ambientais - NEPAM, Universidade Estadual de Campinas - UNICAMP, Rua dos Flamboyants, 155, Cidade Universitária, CEP 13083-867, Campinas, SP, Brasil
VIILaboratório de Ecologia Isotópica, Centro de Energia Nuclear na Agricultura - CENA, Universidade de São Paulo - USP, Av. Centenário, 303, São Dimas, CEP 13416-903, Piracicaba, SP, Brasil
VIIINúcleo Picinguaba, Parque Estadual da Serra do Mar - PESM, Secretaria do Meio Ambiente do Estado - SMA, BR 101, Km 08, CP 157, CEP 11680-000, Ubatuba, SP, Brasil
IXNúcleo Santa Virgínia, Parque Estadual da Serra do Mar - PESM, Secretaria do Meio Ambiente do Estado - SMA, Rod. Owaldo Cruz, Km 78, Alto da Serra, CEP 12140-000, São Luiz do Paraitinga, SP, Brasil
RESUMO
Este trabalho resume os dados de florística e fitossociologia de 11, das 14 parcelas de 1 ha, alocadas ao longo do gradiente altitudinal da Serra do Mar, São Paulo, Brasil. As parcelas começam na cota 10 m (Floresta de Restinga da Praia da Fazenda, município de Ubatuba) e estão distribuídas até a cota 1100 m (Floresta Ombrófila Densa Montana da Trilha do rio Itamambuca, município de São Luis do Paraitinga) abrangendo os Núcleos Picinguaba e Santa Virgínia do Parque Estadual da Serra do Mar. Na Restinga o solo é Neossolo Quartzarênico francamente arenoso, enquanto que na encosta o solo é um Cambisolo Háplico Distrófico argilo-arenoso, sendo que todas as parcelas apresentaram solo ácido (pH 3 - 4) com alta diluição de nutrientes e alta saturação de alumínio. Na Restinga e no sopé da encosta o clima é Tropical/Subtropical Úmido (Af/Cfa), sem estação seca, com precipitação média anual superior a 2.200 mm e temperatura média anual de 22 ºC. Subindo a encosta mantêm-se a média de precipitação, mas há um gradativo resfriamento, de forma que a 1.100 m o clima é Subtropical Úmido (Cfa/Cfb), sem estação seca, com temperatura média anual de 17 ºC. Destaca-se ainda que, quase diariamente, a parte superior da encosta, geralmente acima de 400 m, é coberta por uma densa neblina. Nas 14 parcelas foram marcados, medidos e amostrados 21.733 indivíduos com DAP > 4,8 cm, incluindo árvores, palmeiras e fetos arborescentes. O número médio de indivíduos amostrados nas 14 parcelas foi de 1.264 ind.ha-1 (± 218 EP de 95%). Dentro dos parâmetros considerados predominaram as árvores (71% FOD Montana a 90% na Restinga), seguidas de palmeiras (10% na Restinga a 25% na FOD Montana) e fetos arborescentes (0% na Restinga a 4% na FOD Montana). Neste aspecto destaca-se a FOD Terras Baixas Exploradas com apenas 1,8% de palmeiras e surpreendentes 10% de fetos arborescentes. O dossel é irregular, com altura variando de 7 a 9 m, raramente as árvores emergentes chegam a 18 m, e a irregularidade do dossel permite a entrada de luz suficiente para o desenvolvimento de centenas de espécies epífitas. Com exceção da FOD Montana, onde o número de mortos foi superior a 5% dos indivíduos amostrados, nas demais fitofisionomias este valor ficou abaixo de 2,5%. Nas 11 parcelas onde foi realizado o estudo florístico foram encontradas 562 espécies distribuídas em 195 gêneros e 68 famílias. Apenas sete espécies - Euterpe edulis Mart. (Arecaceae), Calyptranthes lucida Mart. ex DC. e Marlierea tomentosa Cambess (ambas Myrtaceae), Guapira opposita (Vell.) Reitz (Nyctaginaceae), Cupania oblongifolia Mart. (Sapindaceae) e as Urticaceae Cecropia glaziovii Snethl. e Coussapoa microcarpa (Schott) Rizzini - ocorreram da Floresta de Restinga à FOD Montana, enquanto outras 12 espécies só não ocorreram na Floresta de Restinga. As famílias com o maior número de espécies são Myrtaceae (133 spp), Fabaceae (47 spp), Rubiaceae (49) e Lauraceae (49) ao longo de todo gradiente da FOD e Monimiaceae (21) especificamente nas parcelas da FOD Montana. Em termos de número de indivíduos as famílias mais importantes foram Arecaceae, Rubiaceae, Myrtaceae, Sapotaceae, Lauraceae e na FOD Montana, Monimiaceae. Somente na parcela F, onde ocorreu exploração de madeira entre 1960 e 1985, a abundância de palmeiras foi substituída pelas Cyatheaceae. O gradiente estudado apresenta um pico da diversidade e riqueza nas altitudes intermediárias (300 a 400 m) ao longo da encosta (índice de Shannon-Weiner - H' - variando de 3,96 a 4,48 nats.indivíduo -1). Diversas explicações para este resultado são apresentadas neste trabalho, incluindo o fato dessas altitudes estarem nos limites das expansões e retrações das diferentes fitofisionomias da FOD Atlântica durante as flutuações climáticas do Pleistoceno. Os dados aqui apresentados demonstram a extraordinária riqueza de espécies arbóreas da Floresta Ombrófila Densa Atlântica dos Núcleos Picinguaba e Santa Virgínia do Parque Estadual da Serra do Mar, reforçando a importância de sua conservação ao longo de todo o gradiente altitudinal. A diversidade desta floresta justifica também o investimento de longo prazo, através de parcelas permanentes, para compreender sua dinâmica e funcionamento, bem como monitorar o impacto das mudanças climáticas nessa vegetação.
Palavras-chave: Parque Estadual da Serra do Mar, Núcleo Picinguaba, Núcleo Santa Virgínia, riqueza de espécies, fitofisionomias, Sistema de Classificação da Vegetação, Projeto BIOTA Gradiente Funcional
ABSTRACT
This paper summarizes floristic and phytossociology data of 11, out of 14 plots of 1 ha, allocated along an altitudinal gradient in the Serra do Mar, São Paulo, Brazil. The study was conducted at Serra do Mar State Park and the plots start at the sea level (10 m - plot of Restinga Forest that occurs at Praia da Fazenda, Picinguaba, municipality of Ubatuba) up to 1100 m above sea level (the Montane Ombrophilous Dense occurs alongside the Itamambuca Trail, municipality of São Luis do Paraitinga). The Restinga Forest occurs in Pleistocenic Coastal Plain where the soil is classified as a sandy Quartzipsamment (Quartzenic Neosol), while along the slopes of the Serra do Mar, the Ombrophylus Dense Forest grows on the top of a pre-Cambrian crystalline basement with granitic rocks, where the soil is a sandy-loam Dystrophic Inceptisol (Cambisol/Latosol). In all 14 plots soils are acidic (pH 3 - 4), chemically poor, with high dilution of nutrients and high saturation of aluminum. In the Restinga and at the foot of the slope the climate is Tropical/Subtropical Humid (Af/Cfa), with no dry season, an average annual rainfall over 2,200 mm and an average annual temperature of 22 ºC. Towards the top of the Serra do Mar there is a gradual cooling along the slope, but there is no reduction in rainfall, so at 1,100 m above sea level the climate is classified as Humid Subtropical (Cfa/Cfb), with no dry season and an average annual temperature of 17 ºC. It is important to remark that, almost daily, from 400 m above sea level up to the top of slopes the mountains are covered by a dense fog. In the 14 plots 21,733 individuals with DBH > 4.8 cm, including trees, palms and ferns, were marked, measured and sampled. The average number of individuals sampled in each plot was 1264 ind.ha-1(± 218 SE 95%). Within the parameters considered trees prevailed (71% in the Montane ODF to 90% in the Restinga Forest), followed by palms (10% in the RF and 25% in the Montane Ombrophilous Dense Forest/ODF) and ferns (0% % in the RF and 4% in the Montane ODF). Regarding these proportions the Exploited Lowlands ODF differs from the others with only 1.8% of palm trees and striking 10% of ferns. The forest canopy is irregular with heights ranging from 7 to 9 m, rarely emergent trees reach 18 m, and due to this irregularity of the canopy the amount of light that gets through sets conditions for the development of hundreds of epiphytic species. Aside from Montana ODF, where the number of dead trees was more than 5% of individuals sampled, in the other phytophysiognomies this value was below 2.5%. In the 11 plots where the floristic study was conducted we found 562 species in 195 genera and 68 families. Only seven species - Euterpe edulis Mart. (Arecaceae), Calyptranthes lucida Mart. ex DC. and Marlierea tomentosa Cambess (both Myrtaceae), Guapira opposita (Vell.) Reitz (Nyctaginaceae), Cupania oblongifolia Mart. (Sapindaceae), Cecropia glaziovii Snethl. and Coussapoa microcarpa (Schott) Rizzini (both Urticaceae) - occurred from Restinga to Montane ODF, while 12 other species did not occur only in the Restinga Forest. Families with the greatest number of species are Myrtaceae (133 spp), Fabaceae (47 spp), Rubiaceae (49) and Lauraceae (49) throughout the gradient and Monimiaceae (21) specifically in portions Montane ODF. Only in the F plot, where logging has occurred between 1950 and 1985, the abundance of palm trees has been replaced by Cyatheaceae. The study shows a peak of diversity and richness, Shannon-Weiner index (H') ranging from 3.96 to 4.48 nats.ind-1, in the intermediate altitudes (300 to 400 m) along the slope. Several explanations for this result are raised here, including the fact that these elevations are within the limits expansions and retractions of the different phytophysiognomies of the Atlantic ODF due to climate fluctuations during the Pleistocene. The results presented in this paper demonstrate the extraordinary richness of tree species of the Atlantic Rainforest from the northeastern coast of the State of Sao Paulo, reinforcing the importance of its conservation throughout the altitudinal gradient. The richness of this forest justifies a long term commitment to study its dynamics and functioning through permanent plots, and monitor the impacts of climate change in this vegetation.
Keywords: Serra do Mar State Park, Nucleo Picinguaba, Nucleo Santa Virginia, species richness, phytophysiognomies, Vegetation Classification System, BIOTA Functional Gradient Project.
Introdução
A Mata Atlântica sensu lato (Joly et al. 1999) é a segunda maior floresta tropical do continente americano (Tabarelli et al. 2005). A maior parte dos Sistemas de Classificação da vegetação brasileira reconhece que no Domínio Atlântico (sensu Ab'Saber 1977) esse bioma pode ser dividido em dois grandes grupos: a Floresta Ombrófila Densa, típica da região costeira e das escarpas serranas com alta pluviosidade (Mata Atlântica - MA - sensu stricto), e a Floresta Estacional Semidecidual, que ocorre no interior, onde a pluviosidade, além de menor, é sazonal. Na região costeira podem ocorrer também Manguezais (Schaeffer-Novelli 2000), ao longo da foz de rios de médio e grande porte, e as Restingas (Scarano 2009), crescendo sobre a planície costeira do quaternário. No topo das montanhas, geralmente acima de 1500 m, estão os Campos de Altitude (Ribeiro & Freitas 2010).
Em 2002, a Fundação SOS Mata Atlântica em parceria com o INPE (Instituto..., 2002) realizaram um levantamento que indica que há apenas 7,6% da cobertura original da Mata Atlântica (s.l.). Mais recentemente Ribeiro et al. (2009) refinaram a estimativa incluindo fragmentos menores, que não haviam sido contabilizados, e concluíram que resta algo entre 11,4 e 16% da área original. Mesmo com esta fragmentação, o mosaico da Floresta Atlântica brasileira possui um dos maiores níveis de endemismos do mundo (Myers et al. 2000) e cerca da metade desses remanescentes de grande extensão estão protegidos na forma de Unidades de Conservação (Galindo & Câmara 2005). Entre os dois centros de endemismo reconhecidos para a MA (Fiaschi & Pirani 2009), o bloco das regiões sudeste/sul é o que conserva elementos da porção sul de Gondwana (Sanmartin & Ronquist 2004), tido como a formação florestal mais antiga do Brasil (Colombo & Joly 2010).
Segundo Hirota (2003), parte dos remanescentes de MA está no estado de São Paulo, onde cerca de 80% de sua área era coberta por florestas (Victor 1977) genericamente enquadradas como Mata Atlântica "sensu lato" (Joly et al. 1999). Dados de Kronka et al. (2005) mostram que no estado restam apenas 12% de área de mata e menos do que 5% são efetivamente florestas nativas pouco antropizadas. Nos 500 anos de fragmentação e degradação das formações naturais, foram poupadas apenas as regiões serranas, principalmente a fachada da Serra do Mar, por serem impróprias para práticas agrícolas.
Usando o sistema fisionômico-ecológico de classificação da vegetação brasileira adotado pelo IBGE (Veloso et al. 1991), a Floresta Ombrófila Densa, na área de domínio da Mata Atlântica, foi subdividida em quatro faciações ordenadas segundo a hierarquia topográfica, que refletem fisionomias de acordo com as variações das faixas altimétricas e latitudinais. No estado de São Paulo, na latitude entre 16 e 24 ºS temos: 1) Floresta Ombrófila Densa das Terras Baixas - 5 a 50 m de altitude; 2) Floresta Ombrófila Densa Submontana - no sopé da Serra do Mar, com cotas de altitude variando entre 50 e 500 m; 3) Floresta Ombrófila Densa Montana - recobrindo a encosta da Serra do Mar propriamente dita, em altitudes que variam de 500 a 1.200 m; 4) Floresta Ombrófila Densa Altimontana - ocorrendo no topo da Serra do Mar, acima dos limites estabelecidos para a formação montana, onde a vegetação praticamente deixa de ser arbórea, pois predominam os campos de altitude.
Nas últimas três décadas muita informação vem sendo acumulada sobre a composição florística e a estrutura do estrato arbóreo dos remanescentes florestais do estado, conforme mostram as revisões de Oliveira-Filho & Fontes (2000) e Scudeller et al. (2001). Em florestas tropicais este tipo de informação, assim como dados sobre a riqueza de espécies, reflete não só fatores evolutivos e biogeográficos, como também o histórico de perturbação, natural ou antrópica, das respectivas áreas (Gentry 1992, Hubbell & Foster 1986). A síntese dessas informações tem permitido a definição de unidades fitogeográficas com diferentes padrões de riqueza de espécies e apontam para uma diferenciação, entre as florestas paulistas, no sentido leste/oeste (Salis et al. 1995, Torres et al. 1997, Santos et al. 1998).
Segundo Bakker et al. (1996) um método adequado para acompanhar e avaliar as mudanças na composição das espécies e dinâmica da floresta ao longo do tempo é por meio de parcelas permanentes (em inglês Permanent Sample Plots -PSPs). Essa metodologia tem sido amplamente utilizada em estudos de longa duração em florestas tropicais, pois permite avaliar a composição e a estrutura florestal e monitorar sua mudança no tempo (Dallmeier 1992, Condit 1995, Sheil 1995, Malhi et al. 2002, Lewis et al. 2004). Permite avaliar também as consequências para a floresta de problemas como o aquecimento global e a poluição atmosférica (Bakker et al. 1996).
No Brasil os projetos/programas que utilizam a metodologia de Parcelas Permanentes tiveram origem, praticamente, com o Projeto Dinâmica Biológica de Fragmentos Florestais/PDBFF (http://pdbff.inpa.gov.br/instituto1p.html), iniciado no final da década de 70, com uma parceria entre o INPA e o Smithsonian Institution. Mais recentemente programas de pesquisa que utilizam esta metodologia têm se organizado em Redes, como por exemplo, a Rede de Monitoramento da Dinâmica de Florestas da Amazônia Brasileira, a Rede de Parcelas Permanentes no Cerrado e Pantanal e a Rede de Parcelas Permanentes na Mata Atlântica e Pampa (http://www.cnpf.embrapa.br/pesquisa/sispp/SisPP_historico.htm). Entretanto, poucos protocolos de monitoramento estão descritos detalhadamente na literatura.
No âmbito do Programa BIOTA/FAPESP, vários projetos vêm sendo desenvolvidos com o objetivo de compreender melhor a Floresta Ombrófila Densa Atlântica. Esses trabalhos, entretanto, têm se concentrado nos Parques da região do Vale do Ribeira (Parque Estadual Intervales, Parque Estadual Carlos Botelho, Parque Estadual da Ilha do Cardoso) ou em regiões próximas à Grande São Paulo (Reserva Estadual do Morro Grande). Poucos são os trabalhos desse tipo na porção nordeste da Serra do Mar, inexistindo trabalhos focados nas variações da composição florística e da estrutura da floresta ao longo do gradiente altitudinal das escarpas da Serra do Mar. Ainda que de amplitude restrita, se comparado aos trabalhos realizados em outras regiões do mundo (Kessler 2001, Wang et al. 2002, Borges et al. 2011), a variação altitudinal de 0 a 1100 m acima do nível do mar delimita, praticamente, a região de ocorrência florestal na região sudeste do Brasil.
Os objetivos deste trabalho são: i) descrever o protocolo utilizado para estudos da vegetação em parcelas permanentes na Floresta Ombrófila Densa Atlântica, e ii) sintetizar dados da variação na composição e da estrutura do componente arbóreo dessa formação florestal ao longo do gradiente de altitude dos Núcleos Picinguaba (NPIC) e Santa Virgínia (NSV), entre 23º 19' 31" - 23º 22' 52" S e 44º 49' 55" - 45º 05' 02" O, do Parque Estadual da Serra do Mar.
Material e Métodos
1. Estabelecimento e manutenção de parcelas permanentes - padronização do protocolo para inventários florestais
A metodologia de parcelas permanentes permite avaliar a composição e a estrutura florestal e monitorar sua mudança no tempo (Dallmeier 1992, Condit 1995, Sheil 1995, Malhi et al. 2002, Lewis et al. 2004). Além disso, a partir dessa metodologia é possível compreender em que extensão fatores como clima e solo em nível regional determinam a estrutura florestal e afetam os estoques de carbono (Phillips et al. 1998, Clark & Clark 2000, Malhi et al. 2002, Vieira et al. 2008).
Nos últimos anos têm sido propostas e discutidas metodologias e protocolos a fim de padronizar as técnicas de implantação e monitoramento de estudos de longo prazo e, assim, tornar possível a comparação desses estudos em uma escala regional (Sheil 1995, Clark 2002, Phillips & Baker 2002, Phillips et al. 2002, Rodrigues 2003). Devido ao elevado custo financeiro e à exigência de comprometimento a longo-prazo de especialistas e técnicos para o estabelecimento e a manutenção das parcelas, uma série de procedimentos devem ser cuidadosamente avaliados e considerados durante a instalação e coleta de dados para se evitar inacurácias, erros e tendências nos dados (Sheil 1995, Phillips & Baker 2002, Phillips et al. 2002). Deficiências metodológicas nos estágios de estabelecimento da parcela, plaqueamento dos indivíduos e no inventário propriamente dito têm implicações em todo o processo e podem gerar tendências nos dados, resultando em sub ou super estimativas de determinado parâmetro (Sheil 1995, Clark 2002). Assim, a recomendação geral é que a marcação da área de amostragem (parcela e subparcelas) deve ser feita de forma permanente, utilizando material de longa duração e de fácil manipulação. A numeração dos indivíduos amostrados deve ser preferencialmente sequencial, também feita com material resistente e de boa qualidade. Um sistema de coordenadas deve ser estabelecido para identificar os limites das subparcelas, além do mapeamento dos indivíduos para facilitar a localização em censos posteriores.
Dentro desta perspectiva, o projeto BIOTA Gradiente Funcional padronizou um protocolo de campo para o estabelecimento, mapeamento e levantamento das variáveis de cada indivíduo das parcelas permanentes localizadas na Floresta Ombrófila Densa dos Núcleos Picinguaba e Santa Virgínia do Parque Estadual da Serra do Mar. O protocolo foi uma adaptação do proposto por Phillips & Baker (2002).
2 Seleção das áreas de estudo
A primeira etapa consistiu na interpretação de imagens de satélite e ortofotos para a escolha preliminar das áreas amostrais. Posteriormente, essa etapa orientou a equipe multidisciplinar que foi ao campo visitar as áreas pré-selecionadas. Com a aferição, a equipe verificou que algumas das áreas previamente selecionadas não poderiam ser utilizadas para instalação das parcelas, pois apresentavam vegetação nitidamente secundária ou estavam a mais de 3 horas de caminhada, o que inviabilizaria a realização do trabalho de campo.
Realizou-se então um sobrevôo para identificação de novas áreas que atendessem os quesitos de conservação e logística. O plano de vôo foi traçado sobre as cartas IBGE 1:50.000 da região com base na interpretação das ortofotos e das visitas ao campo. As imagens e mapas existentes e os registros constatados em campo nos forneceu uma abrangência dos diferentes trechos e fitofisionomias de floresta. Nesta etapa confirmou-se a inexistência de outros remanescentes de Floresta de Restinga adequados para amostragem, além daquele selecionado no Núcleo Picinguaba. Constatou-se também que a fitofisionomia Floresta Ombrófila Densa das Terras Baixas praticamente desapareceu no município de Ubatuba, com exceção das áreas do Sertão da Casa da Farinha (ao longo das margens do rio da Fazenda e da Trilha do Corisco). Mesmo acima dos 100 m de altitude poucos são os remanescentes aparentemente bem conservados e de grandes dimensões, e os que restam localizam-se, geralmente, em pontos de grande declividade e inacessíveis, sendo, portanto, impróprios para o estudo. Para a fitofisionomia Floresta Ombrófila Densa Submontana (FODS) foi identificada uma área nas cabeceiras do rio Indaiá, na Fazenda Capricórnio (Sertão da Taquara, Praia do Perequê-Açu). Parte da equipe esteve na área e constatou que ela efetivamente atendia às necessidades do projeto.
Ao longo dessas visitas de campo foi possível confirmar dados de literatura (Assis 1999) que mostram que, no litoral norte do Estado de São Paulo, a floresta que ocorre sobre os solos arenosos da restinga aparenta ter composição florística e estrutura distinta das três principais fisionomias da Floresta Ombrófila Densa (Terras Baixas, Submontana e Montana) que recobrem a encosta da Serra do Mar. Desta forma, optamos por designar neste estudo a floresta sobre os solos arenosos da Planície Costeira como Floresta de Restinga. No sentido de confirmar se a floresta sobre os cordões arenosos é de fato uma formação ímpar, instalamos uma parcela (1 ha) nesta formação.
3. Desenho amostral
Instalação de apenas uma parcela de 1 ha na Floresta de Restinga (Parcela A - Figura 1);
Em cada uma das três fitofisionomias: FOD das Terras Baixas ao longo da Trilha do Corisco, Casa da Farinha (Parcelas B, C, D e E - Figura 1); FOD Submontana na Fazenda Capricórnio (Parcelas G, H, I e J - Figura 1); FOD Montana ao longo da Trilha do rio Itamambuca no Núcleo Santa Virgínia (Parcelas K, L, M e N - Figura 1) foram instaladas 4 parcelas de 1 ha cada, isoladas entre si e, portanto, consideradas como réplicas (Joly et al. 2008).
Como por razões logísticas não foi possível instalar as parcelas de FOD Submontana e Montana ao longo da Trilha do Corisco, então, adicionalmente, instalamos uma 5ª parcela de FOD das Terras Baixas (Parcela F - Figura 1) na Fazenda Capricórnio, a cerca de 40 km de distância das Parcelas B a E.
Ao todo foram instaladas 14 parcelas quadradas de 1 ha subdivididas em 100 subparcelas de 10 × 10 m (Tabela 1). As parcelas foram delimitadas por equipe especializada de topografia, utilizando-se instrumentos de alta precisão, como teodolito e nível digitais, altímetro e GPS. O limite externo das parcelas foi delimitado colocando-se estacas de 1,2 m de tubo de PVC ¾ a cada 10 m. A cada 50 m foi colocada uma estaca de tubo de PVC de 5 polegadas, georeferenciada de forma a permitir a plotagem da parcela em imagens de satélite e ortofotos. A partir desta delimitação externa as parcelas foram subdivididas em subparcelas de 10 × 10 m, tendo uma estaca em cada um dos vértices. Em cada ponto correspondente à posição das estacas foi registrado o nível altimétrico, que permitiu a elaboração precisa do mapeamento topográfico das áreas.
4. Plaqueamento, mapeamento e medição dos indivíduos arbóreos.
Com a finalidade de facilitar a orientação dentro das parcelas, os eixos X e Y de cada área receberam números e letras, respectivamente, de forma que cada estaca possui uma coordenada, constituída de uma letra seguida de um número. As coordenadas x = 0 e y = 0 correspondem à subparcela 1, por onde foi iniciado o plaqueamento.
4.1. Plaqueamento
Os indivíduos arbóreos foram plaqueados de forma sequencial, partindo da subparcela 1, em ordem, até a 100 seguindo a forma de um "U" ou de um "caracol" dentro de cada subparcela. Via de regra, as placas foram colocadas sempre voltadas para o eixo X da parcela, facilitando sua a visualização.
Cada indivíduo recebeu uma placa de alumínio onde constava a letra referente à parcela e um número, referente ao indivíduo. Foram utilizados pregos niquelados de dois tamanhos (18 × 27 e 17 × 21 mm). A fixação do prego foi feita deixando espaço suficiente para que a árvore pudesse crescer livremente, sem "engolir" a placa.
Todas as árvores vivas, incluindo palmeiras e pteridófitas (fetos arborescentes), com perímetro à altura do peito (PAP) >15 cm (4,8 cm de diâmetro ao nível do peito - DAP) foram plaqueadas. Indivíduos mortos em pé e ligeiramente tombados (<30º) também foram plaqueados. Nos indivíduos que apresentaram bifurcações ou rebrotas ("perfilhos") abaixo de 1,30 m (altura de medição do perímetro) foram plaqueados apenas os caules com PAP >15 cm. Neste caso, o caule principal (maior PAP) recebeu a placa de metal e os demais receberam uma placa de plástico branca, numerada com caneta de marcação permanente no momento do plaqueamento ( p.ex ., indivíduo D0747 com três caules, recebeu além da placa de alumínio colocada no fuste principal, duas placas brancas numeradas como D0747 A e D0747 B). Caules da mesma espécie localizados muito próximos foram avaliados para verificar a existência de possíveis conexões por raízes imediatamente abaixo do solo antes de seu plaqueamento. Foram considerados pertencentes a cada subparcela os indivíduos que apresentavam mais de 50% de sua área basal dentro dessa.
A altura do plaquemento (1,60 m) e da medição do PAP (1,30 m) foi definida para cada indivíduo com o auxilio de uma haste graduada, firmemente colocada no solo a partir do começo do tronco (excluindo raízes). Para árvores inclinadas, a haste foi posicionada no sentido do maior comprimento (1,30 m) e em terrenos inclinados a partir do ponto superior do terreno. Para indivíduos que apresentaram deformidades a 1,30 m, o ponto de medição foi realocado no ponto mais próximo a esse onde não houvesse deformidades. A altura do ponto de medição foi então registrada e a placa metálica colocada 30 cm acima deste novo ponto. Árvores com raízes tabulares, raízes-escora ou com grandes irregularidades a 1,30 m tiveram seu ponto de medição definido a 50 cm acima do topo da raiz e a placa foi colocada a 1,60 m. Nestes casos foi anotada a altura de medição e foi colocada uma placa plástica branca 30 cm acima do ponto de medição. Uma escada de alumínio foi utilizada para acessar o ponto de medição sempre que necessário.
4.2. Mapeamento
O mapeamento dos indivíduos plaqueados foi realizado com o auxílio de uma trena. Tomando-se os vértices de cada subparcela como referência, foi medida e anotada a distância do indivíduo em relação aos eixos X e Y. Tais dados foram convertidos posteriormente em coordenadas X e Y da parcela.
4.3. Medições
Foram medidos todos os indivíduos plaqueados sendo que para a medida do PAP utilizou-se uma fita métrica graduada com precisão de 1 mm. Árvores sem folhas foram incluídas como vivas se o câmbio abaixo do lenho (casca) estivesse vivo.
A altura total e a altura do fuste foram estimadas visualmente para cada indivíduo registrado. Posteriormente, foi realizada a medida de altura de uma subamostra de indivíduos distribuídos em diferentes classes de diâmetro ao longo do gradiente altitudinal. Essa medida foi realizada com auxílio de trenas telescópicas (alcance de 15 m) e hipsômetro eletrônico (Laser Ranger Finder, Impulse-200LR, Laser Technology Inc., Englewood, Colorado) para indivíduos maiores do que 15 m (Scaranello et al. 2012). As alturas medidas em campo a partir de instrumentos de precisão foram comparadas com as alturas estimadas visualmente. A altura mediana do dossel foi comparada entre as cotas altitudinais por ANOVA de Kruskal-Wallis.
Para cada fitofisionomia foi construída uma regressão entre o diâmetro (DAP) e a altura, sendo a altura estimada por esta equação utilizada posteriormente para os cálculos de biomassa (para detalhes das equações ver Alves et al. 2010). O efeito da variação altitudinal na estrutura e distribuição da biomassa viva acima do solo das parcelas estudadas foi avaliado e discutido por Alves et al. (2010).
5. Índice de iluminação
A disponibilidade potencial de luz para cada indivíduo foi estimada por meio do Índice de Iluminação da Copa (em inglês Crown illumination index - CII), que indica a direção e a exposição relativa da copa de uma árvore à luz (Clark & Clark, 1992). Segundo Alves et al. (2010), quando bem calibrado por seus observadores esse índice fornece um método simples e rápido de estimar o ambiente luminoso disponível para cada árvore (ver Clark & Clark 1992, Keeling & Phillips 2007 para mais detalhes). As análises estatísticas foram feitas utilizando o Teste G e o coeficiente de Spearman (Zar 1999).
6. Entrada e auditoria dos dados
As planilhas de campo foram digitalizadas separadamente para cada parcela. Todos os dados foram conferidos, pelo menos duas vezes, por diferentes pesquisadores do Projeto. Na ausência e/ ou discrepância em algum dado, este foi anotado e verificado em posterior visita ao campo.
Os dados de PAP foram convertidos posteriormente para diâmetro (DAP = PAP/π) e Área basal (AB = PAP2/4π). Para indivíduos com caules múltiplos, o DAP foi calculado a partir da área basal total [DAP = √ (4 ABT/π)].
7. Identificação botânica
Os indivíduos vivos amostrados tiveram ramos coletados (segundo orientações de Fidalgo & Bononi 1984) e herborizados (ver Mori et al. 1989) para, posteriormente, serem determinados taxonomicamente e/ou servirem de material testemunho, exceção feita àqueles que foram prontamente identificados no campo. As identificações foram realizadas com o auxílio da literatura pertinente e de consultas aos especialistas, além de comparações com as coleções dos Herbários UEC, IAC e HRCB, nos quais os materiais foram depositados. As espécies e morfo-espécies foram identificadas em famílias botânicas de acordo com o Angiosperm Phylogeny Group/APG II (Angiosperm... 2003) e revisão de Souza & Lorenzi (2008) para a flora brasileira.
8. Localização e caracterização das áreas de estudo
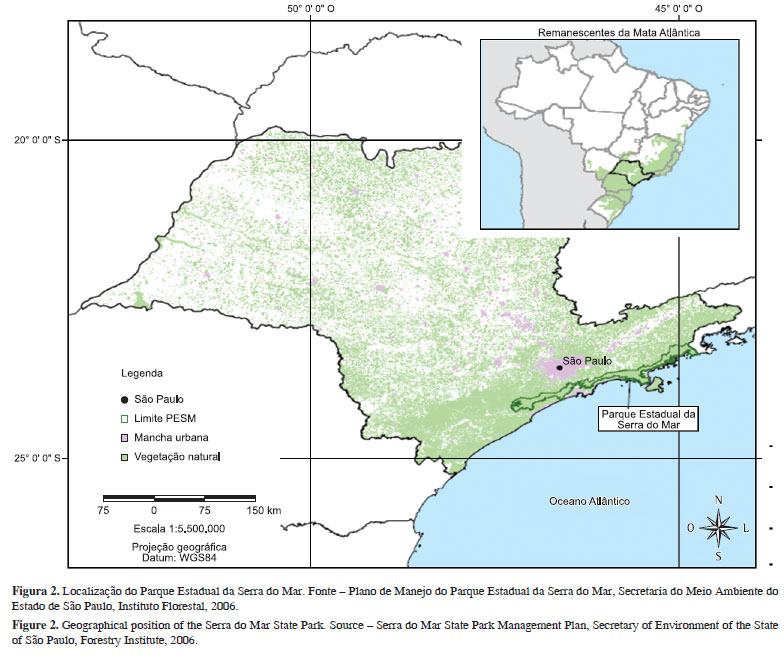
As áreas de estudo ficaram limitadas aos Núcleos Picinguaba e Santa Virgínia do Parque Estadual da Serra do Mar (Figuras 2 e 3).
8.1. Núcleo Picinguaba
O Núcleo Picinguaba (23º 31' - 23º 34' S e 45º 02' - 45º 05' O) está situado no município de Ubatuba, sendo a única porção do Parque Estadual da Serra do Mar que atinge a orla marinha (São Paulo 1996). Consequentemente, o NPIC apresenta um mosaico vegetacional que inclui Formações Pioneiras com Influência Marinha (Dunas); Formações Pioneiras com Influência Fluvial (Caxetal); Formações Pioneiras com Influência Flúvio-Marinha (Mangue), Floresta Ombrófila Densa de Terras Baixas (Mata de Restinga), Floresta Ombrófila Densa Submontana e Floresta Ombrófila Densa Montana (Assis 1999).
O relevo da região é dominado pela Planície Costeira, passa pelos morros isolados e serras alongadas da Morraria Costeira, atingindo no seu limite interior as escarpas, festonadas ou com espigões digitados (Ponçano et al. 1981). As altitudes no Núcleo Picinguaba variam do nível do mar a 1.340 m. O clima regional é Tropical Úmido (segundo a classificação de Köppen - 1948 - Af ou Cfa, dependendo da intensidade do verão), sem estação seca, com uma temperatura média anual de 22 ºC (Setzer 1966, EMBRAPA 2009) e precipitação média anual superior a 2.200 mm (Figura 4). Mesmo nos meses mais secos, junho a agosto, a precipitação média mensal nunca é inferior a 80 mm. A Tabela 2 resume os dados físico-químicos dos solos das parcelas estudadas no Núcleo Picinguaba.
8.2. Núcleo Santa Virgínia
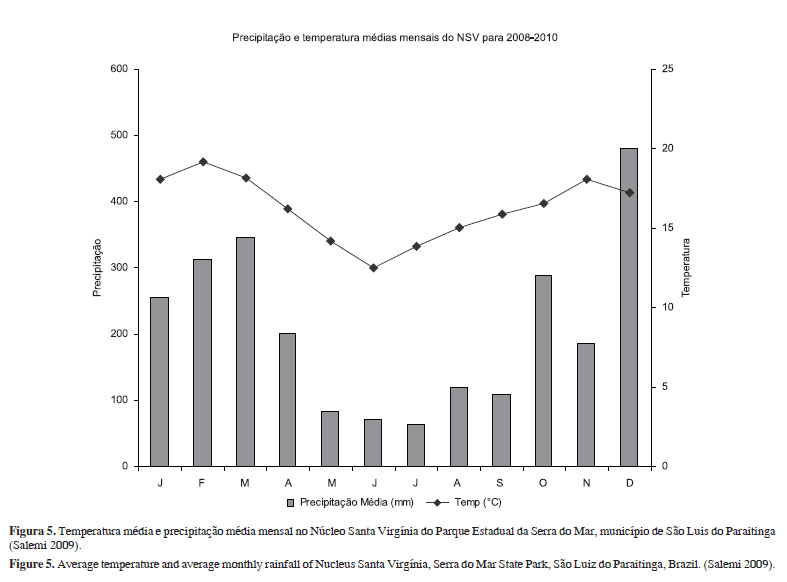
Com cerca de 17.000 ha recobertos, predominantemente, pela Floresta Ombrófila Densa Montana (Veloso et al. 1991), o Núcleo Santa Virgínia (23º 17' - 23º 24' S e 45º 03' - 45º 11' O) situa-se a uma altitude que varia de 740 a 1600 m entre os municípios de São Luís do Paraitinga (70%), Cunha (20%) e Ubatuba (10%). Na área da Base Itamambuca, próximo às nascentes dos rios Indaiá e Itamambuca, o clima é Subtropical Úmido [Cfa ou Cfb de acordo com a classificação de Köppen (1948)], com temperatura média anual de 17 ºC (Setzer 1966, Salemi 2009) e precipitação média anual de 2.300 mm (Figura 5, Salemi 2009). Nos meses mais secos, julho e agosto, a precipitação média mensal nunca é inferior a 60 mm. Essa região é quase diariamente coberta por uma densa neblina, especialmente no inverno. A Tabela 2 resume os dados físico-químicos dos solos das parcelas estudadas no Núcleo Santa Virgínia.
9. Diversidade e similaridade florística
Em cada área, a diversidade foi estimada pelo índice de Shannon-Wiener (Magurran 2004). Para se ter uma visão geral da similaridade florística entre as 11 áreas onde foi feita a amostragem, foi gerado um dendrograma pelo método UPGMA, aplicando-se o índice de similaridade de Sørensen a dados de presença e ausência das espécies, e uma ordenação por Análise de Correspondência, a partir de dados de densidade relativa. Esses dois métodos são explicados por Wildi (2010). O programa utilizado foi o PC-ORD 6.0 (McCune & Mefford 2011). Análises florísticas comparativas pormenorizadas constam em Eisenlohr et al. (em preparo).
Resultados e Discussão
1. Estrutura florestal
Ao longo das 14 parcelas foram amostrados 21.733 indivíduos arbóreos incluindo árvores, palmeiras e fetos arborescentes. O número médio de indivíduos amostrados com DAP > 4,8 cm, por parcela, foi de 1.264 ± 218 ind.ha -1 (± Erro Padrão de 95%) (Tabela 3). O número médio de indivíduos com DAP >10 cm também apresentou padrão semelhante de variação (627 ± 57 ind.ha -1).
Os resultados sobre a composição florística e estrutura florestais abaixo apresentados incluem também dados sobre um hectare de FOD das Terras Baixas submetido à exploração seletiva entre 1950 e 1985 (Parcela F).
A distribuição dos principais componentes estruturais incluídos diferiu entre as fitofisionomias, contribuindo para a variação na estrutura florestal (Tabelas 3 e 4). A proporção de árvores e palmeiras apresentou uma relação inversa, com diminuição na proporção de árvores e aumento na de palmeiras com a altitude (Tabela 4). A densidade total de indivíduos foi menor na FOD de Terras Baixas em relação às demais fitofisionomias (Alves et al. 2010). As árvores foram mais abundantes na FOD Submontana e na Restinga (>1400 ind.ha -1; Tabela 3). A densidade de palmeiras aumentou ao longo do gradiente altitudinal, alcançando mais de 400 ind.ha -1 na FOD Montana. Entretanto, as palmeiras apresentaram baixa densidade na parcela de FOD de Terras Baixas Explorada (Parcela F). As pteridófitas não estiveram presentes na Restinga, e só alcançaram alta densidade nas parcelas da FOD Montana e na de Terras Baixas Explorada. Ao longo de todas as parcelas amostradas, a área basal média de indivíduos foi de 34 m2.ha -1 (± 4,1) e os indivíduos com DAP > 10 cm representaram cerca de 90% da área basal total.
Apenas uma pequena proporção dos indivíduos amostrados (<10%) nas diferentes fitofisionomias atingiram mais do que 15 m de altura. Essa proporção foi menor nas FOD de Terras Baixas e Terras Baixas Explorada (4-6,5%). A altura mediana do dossel foi maior nas áreas de FOD Montana e Submontana (mediana = 7,5 e 8,0 m, respectivamente) do que nas áreas de menor altitude (mediana = 7,0 m) (ANOVA de Kruskal-Wallis; K = 93,08; p < 0,001). Os dados indicam uma pequena variação na estrutura vertical entre áreas de maior e menor altitude, em grande parte devido à contribuição das árvores mais altas (>15 m).
Em todas as áreas de FOD estudadas, a maior proporção dos indivíduos teve sua copa pouco exposta à luz vertical (IC = 3; Tabela 5). A proporção de indivíduos com copas emergentes, completamente expostas à luz, variou de 6 a 13,6% entre as áreas e foi mais alta na Restinga (Tabela 5). Em todas as fitofisionomias, a copa da maior parte dos indivíduos ocorreram com maior freqüência sob baixa luz vertical que o esperado em relação ao acaso (Teste G; Gtotal = 73,01 g.l. = 5, p < 0,001; Tabela 5), mas essa proporção não diferiu entre as fitofisionomias (Teste G; Gheterogeneidade = 14,78, g.l. = 4, p > 0,05).
Apesar da estrutura vertical estar restrita a três estratos, ao longo de todo o gradiente encontramos associação positiva e significativa entre altura e demanda por luz. (rSpearman = 0,51-0,59, <0,01 para todas as correlações; Alves et al. 2010) e a maior proporção da biomassa viva está estocada nos indivíduos com copas muito iluminadas ou emergentes (Alves et al. 2010). Esses dados sugerem que a existência de um forte gradiente vertical de luz pode estar limitando, em parte, a altura média do dossel por intensa competição entre os indivíduos no subosque da floresta. A maioria dos indivíduos segue o perfil vertical de luz da floresta, distribuindo-se em ambientes de baixa intensidade luminosa. Provavelmente, poucos indivíduos (e espécies) são capazes de atingir uma alta estatura com um baixo custo de construção (grande alocação de biomassa para o tronco) e suporte (baixa densidade da madeira) (Alves & Santos 2002, Poorter et al. 2003, 2005).
2. Características físicas e florística
Parcela A - nas coordenadas 23º 21' 22" S e 44º 51' 03" O (Figuras 1 e 6 ), está localizada na Praia da Fazenda. A topografia é quase plana, altitude variando entre 9,5 e 10,5 m. O solo é classificado como Neossolo Quartzarênico, francamente arenoso, sazonalmente inundado, ácido, com alta diluição de nutrientes e alta saturação de alumínio (Tabela 2, Martins 2010).
Na Floresta de Restinga (Parcela A) os 1626 indivíduos amostrados pertenciam a 84 espécies distribuídas em 32 famílias. As famílias Myrtaceae com 21 espécies e Fabaceae com oito espécies, são as que apresentaram maior diversidade (Assis et al. 2011), enquanto que em termos de abundância Myrtaceae, Arecaceae e Euphorbiaceae reúnem 57% dos indivíduos amostrados. Destaca-se nesta floresta a tolerância de algumas espécies á inundação sazonal (Oliveira 2011), especialmente o guanandi, Calophyllum brasiliense Camb. (Clusiaceae) (Oliveira & Joly 2010). A diversidade de espécies com DAP > 4,8 cm foi de 3,38 nats.indivíduo -1 (H' de Shannon-Wiener) (Assis et al. 2011).
Parcela B - nas coordenadas 23º 20' 13" S e 44º 50' 08" O (Figura 1), está localizada ao longo da Trilha do Corisco, no Sertão da Casa da Farinha. A topografia é fortemente ondulada, com altitudes variando de 33 a 57 m. O solo é classificado como Cambisolo háplico distrófico típico, argiloso, ácido (pH 3,3 a 3,9), com alta diluição de nutrientes e alta saturação de alumínio (Martins 2010). Na parcela ocorrem áreas muito pedregosas bem como afloramentos rochosos de granito/gnaisse.
Na Parcela B, FOD de Terras Baixas, foram amostrados 1.183 indivíduos, pertencentes a 137 espécies distribuídas em 38 famílias). Myrtaceae (21 espécies) e Rubiaceae (14 espécies) foram as famílias mais ricas. A diversidade de espécies com DAP > 4,8 cm foi de 4,00 nats.indivíduo -1 (Assis et al. 2011). Dentre as famílias identificadas, são evidentes as diferenças existentes em relação ao número de seus representantes, sendo algumas famílias muito abundantes, contrastando com outras com apenas um ou poucos indivíduos amostrados. Rubiaceae foi a família mais abundante, com 230 indivíduos, o que equivale a 21% das plantas determinadas até família. Em seguida, a família Myrtaceae, com 224 indivíduos, representa cerca de 20% do total identificado e Arecaceae, com 135 indivíduos, detém cerca de 12%. Outras famílias também numerosas foram: Monimiaceae (81), Sapotaceae (79), Nyctaginaceae (43), e Lauraceae (38) (Prata 2009).
Contrastando com essa expressiva representatividade acima descrita, algumas famílias foram muito pouco representadas, tais como: Apocynaceae, Lechytidaceae, Magnoliaceae, Melastomataceae, e Protecaceae (todas com 1 indivíduo cada), Araliaceae e Polygonaceae (2), e Caricaceae e Chrysobalanaceae (3) (Prata 2009, Assis et al. 2011).
Parcela D - nas coordenadas 23º 20' 09" S e 44º 50' 00" O (Figura 1), também está localizada ao longo da Trilha do Corisco, no Sertão da Casa da Farinha. A topografia é fortemente ondulada, com altitudes variando de 43 a 69 m. O solo apresenta as mesmas características da parcela B (Martins 2010).
Na parcela D foram amostrados 1.284 indivíduos vivos, pertencentes a 156 espécies distribuídas em 41 famílias botânicas. As famílias com maior riqueza de espécies foram Myrtaceae (32 espécies em 204 indivíduos), Rubiaceae (15 em 227), Fabaceae (13 em 45), Sapotaceae (10 em 93) e Moraceae (oito em 20). Os maiores valores de importância foram obtidos por Myrtaceae, Rubiaceae, Arecaceae (Prata et al. 2011).
Do total de indivíduos amostrados, 234 eram palmeiras (Astrocaryum aculeatissimum (Schott) Burret, Euterpe edulis Mart. e Syagrus pseudococos (Raddi) Glassman, Arecaceae) e 18 eram samambaias arborescentes (Alsophila sternbergii (Sternb.) D.S.Conant , Cyatheaceae). As oito (5%) espécies mais abundantes concentraram 45% dos indivíduos, enquanto 46 espécies (29.4%) foram representadas por apenas uma árvore. As espécies de maior densidade foram: Euterpe edulis Mart. (com 191 indivíduos, 14,8%), Mollinedia schottiana (Spreng.) Perkins (66, 5,1%), Rustia formosa (Cham. & Schltdl. ex DC.) Klotzsch (32, 4,8%), Chrysoplhyllum flexuosum Mart. (60, 4,7%), Coussarea meridionalis (Vell.) Müll.Arg . var. porophylla (Vell.) M.Gomes (60, 4,7%). Assim como na Parcela B a diversidade de espécies com DAP > 4,8 cm foi de 4,00 nats.indivíduo -1 (Prata 2009, Prata et al. 2011).
Em um levantamento realizado no estrato regenerante de espécies arbóreas (H >1,5 m e DAP < 4,8 cm) em 0,4 ha, nesta mesma parcela, as diversidades estimadas foram iguais a H' = 4,25 e 1-D = 0,97, num total de 176 espécies. A riqueza alcançou 192 espécies arbóreas somando os estratos arbóreo (1 ha) e regenerante (0,4 ha) na parcela D (Prata et al. 2011).
Estes resultados mostram que a riqueza local de espécies arbóreas é surpreendentemente ainda mais alta quando considerados também os estratos regenerantes na amostragem da comunidade (Prata et al. 2011).
Parcela E - encontra-se nas coordenadas 23º 20' 05" S e 44º 49' 55" O (Figura 1). Assim como as parcelas B e D também está localizada ao longo da Trilha do Corisco, no Sertão da Casa da Farinha. A topografia é fortemente ondulada, com altitudes variando de 64 a 89 m. O solo apresenta as mesmas características da parcela B (Tabela 2, Martins 2010), mas além de raso foram observados afloramentos de leitos de rio, que tornam o solo mais arenoso em alguns trechos (Campos 2008). Os afloramentos rochosos são conspícuos e rochas com mais do que 50 cm de diâmetro ocupam áreas significativas das sub-parcelas.
Na parcela E foram marcados 1.240 indivíduos vivos pertencentes a 142 espécies e/ou morfotipos distribuídas em 41 famílias botânicas (Campos et al. 2011). As cinco espécies mais importantes em número de indivíduos são: Euterpe edulis, Mollinedia schottiana, Bathysa mendoncaei, Coussarea accedens e Rustia formosa. Em relação às famílias destacam-se Myrtaceae (27 espécies) e Rubiaceae (14), seguidas por Fabaceae (11), Euphorbiaceae (8) Lauraceae (8). Além do palmito destacam-se outras duas espécies de Arecaceae - Syagrus pseudococos (Raddi) Glassman, o pati, com 37 individuos e Astrocaryum aculeatissimum (Schott) Burret, a brejaúva, com sete indivíduos. Os quatro fetos arborescentes encontrados (Familia Cyatheaceae), conhecidos popularmente como samambaia-uçu, pertencem a duas espécies: Alsophila sternbergii e Cyathea phalerata (Campos 2008, Campos et al. 2011).
Os dados de campo, quando analisados separadamente, mostram que a florística dos indivíduos crescendo sobre os grandes matacões (cerca de 30 espécies) diferente daquela da parcela como um todo. Dentre as 29 espécies com 10 ou mais indivíduos na parcela como um todo, somente 13 ocorrem sobre rochas, e dentre elas, predominantemente Euterpe edulis (com 29% de seus indivíduos sobre rochas), Guapira opposita (25%) e Cecropia glaziovi (20%). O índice de diversidade de Shannon-Wiener foi de 4,05 nats.indivíduo -1 (Campos 2008, Campos et al. 2011).
2.1. Comparação entre as Parcelas da Floresta Ombrófila Densa das Terras Baixas
Nas três parcelas de 1 ha foram registrados 3.707 indivíduos arbóreos, sendo identificadas 250 espécies, pertencentes a 48 famílias. Dentre as famílias com maior número de espécies (mais ricas) destacam-se Myrtaceae (35 espécies), Rubiaceae (20) e Fabaceae (20). Em relação à abundância de indivíduos por família, prevalecem Rubiaceae (694 indivíduos), Myrtaceae (637), Arecaceae (556), Monimiaceae (253), Sapotaceae (227), Nyctaginaceae (132) e Fabaceae (101). Para espécies, verifica-se que Euterpe edulis (445 indivíduos), Mollinedia schottiana (223), Rustia formosa (165), Coussarea meridionalis var. porophylla (158), Chrysophyllum flexuosum (156), Coussarea accedens (154) e Bathysa mendoncaei (135) são as mais abundantes.
Por outro lado, encontramos numerosas espécies representadas por um único ou poucos indivíduos, tais como: Pera glabrata (Schott) Poepp. ex Baill., Cryptocaria aschersoniana Mez, Ocotea glaziovii Mez, Dalbergia frutescens (Vell.) Britton, Lonchocarpus cultratus (Vell.) A.M.G. Azevedo & H.C. Lima, Inga nutans Mart., Myrocarpus frondosus Allemão, Platymiscium floribundum Vogel, Pseudopiptadenia warmingii (Benth.) G.P. Lewis & M.P. Lima, Pterocarpus rohrii Vahl. Exceto por P. glabrata, as demais pertencem à Lauraceae e Fabaceae. Também com um número reduzido de indivíduos encontramos ainda Inga cauliflora Willd. e I. striata com apenas dois indivíduos (Campos 2008, Prata 2009, Assis et al. 2011, Campos et al. 2011, Prata et al. 2011).
A diversidade de espécies com DAP > 4,8 cm das três parcelas é alto (H' >4,00 nats/ind), mas comparável ao encontrado por Silva & Leitão Filho (1982) em outra área de FOD das Terras Baixas do município de Ubatuba (H' = 4,07) e por Guilherme et al. (2004) na FOD das Terras Baixas de Sete Barras (H' = 3,85).
Parcela F - entre as coordenadas 23º 22' 53" S e 45º 04' 44" O (Figura 1), esta localizada na Fazenda Capricórnio, sertão do Pereque-Açu. A topografia é ondulada, com altitudes variando de 80 a 120 m. O solo apresenta características semelhantes as da parcela B (Martins 2010), mas além de raso foram observados afloramentos de leitos de rio, que tornam o solo mais pedregoso em alguns trechos (Ramos 2009). Inicialmente esta parcela foi escolhida para evidenciar a similaridade florística da vertente que acompanha o Rio Indaiá, com as parcelas B a E no Sertão da Casa da Farinha. Posteriormente, funcionários antigos da Fazenda Capricórnio relataram que, naquela área, as árvores de maior diâmetro com potencial madeireiro foram retiradas para uso e comercialização, sendo a madeira processada em serraria da própria fazenda. Restos de troncos de grandes árvores cortados são evidências dessa atividade, que ocorria com mais intensidade nas áreas de menor altitude, por serem mais acessíveis. Nas partes mais altas, a extração também ocorreu, porém de forma mais discreta. A exploração de árvores na fazenda cessou em 1985 (Sr. Salvador dos Santos, informação pessoal). Por esta razão, passamos a denominar a Parcela F como Parcela de FOD de Terras Baixas Explorada, com composição distinta tanto das demais parcelas de FOD das Terras Baixas como da FOD Submontana.
Na parcela F foram marcados 1240 indivíduos vivos pertencentes a 104 espécies, 72 gêneros e 38 famílias (Ramos et al. 2011). As famílias mais ricas são Myrtaceae (oito gêneros, 17 espécies), Fabaceae (sete, oito) e Lauraceae (seis, sete), Rubiaceae (cinco, sete) e Melastomataceae (três, seis), totalizando 29 gêneros e 45 espécies (43,2% do total de espécies do trecho). As famílias mais importantes são Rubiaceae, Fabaceae, Myrtaceae, Cyatheaceae e Phyllantaceae.
Além de apresentar composição e estrutura distintas das demais parcelas desta altitude a Parcela F se caracterizou por uma elevada abundância (103 indivíduos amostrados) de Alsophila sternbergii (Sternb.) D.S.Conant (Cyatheaceae) e, proporcionalmente, um número reduzido (20 indivíduos amostrados) de Euterpe edulis Mart. (Arecaceae) (Ramos et al. 2011). Possivelmente, durante o período de exploração de madeira os palmitos também tenham sido explorados intensivamente, reduzindo o número de matrizes reprodutivas na área, cujo reflexo é a baixa densidade populacional da espécie se comparada com as outras 10 parcelas.
O índice de Shannon-Wiener do componente arbóreo (DBH >4,8 cm), H' = 3.56 nats.indivíduo -1, que pode ser considerado baixo se comparado ao obtido nas parcelas demais parcelas (B, D e E) de FOD das Terras Baixas, estudadas pelo projeto.
Parcela G - nas coordenadas 23º 22' 26" S e 45º 04' 51" O (Figura 1), também localizada na Fazenda Capricórnio, topograficamente apresenta um declive moderado de 22 m de altitude ao longo dos 100 m de extensão da parcela, com altitudes variando de 176-198 m. O solo apresenta características semelhantes às das parcelas de Terras Baixas (Martins 2010).
Na parcela G foram marcados 1.496 indivíduos vivos distribuídos em 152 espécies, 101 gêneros e 41 famílias. A família mais rica foi Myrtaceae, com 30 espécies (20% da riqueza total); destas, oito espécies foram amostradas somente nesta cota altitudinal, e talvez possam ser utilizadas como indicadoras de distribuição restrita em estudos de modelagem de nicho (Giovanelli et al. 2010). A segunda família com maior riqueza foi Fabaceae, com 18 espécies (12% da riqueza), seguida por Rubiaceae, com 15 espécies (10%), Lauraceae e Sapotaceae, com oito espécies cada (5% da riqueza total, cada). Quinze famílias apresentaram uma única espécie, sendo que três delas (Lacistemaceae, Ochnaceae e Rosaceae) foram amostradas somente nessa cota altitudinal (Gomes et al. 2011).
Rudgea jasminoides (Cham.) Müll. Arg. (Rubiaceae) (234 indivíduos - 16% do total) foi a espécie mais abundante, seguida por Euterpe edulis (116 indivíduos - 8%), sendo que muitos deles foram cortados por palmiteiros no decorrer do estudo, Mollinedia schottiana (Sprengel) Perkins (64 indivíduos), Coussarea accendens Müll. Arg. (60) e Eugenia prasina O.Berg (57), cada uma correspondendo a cerca de 5% dos indivíduos. O índice de Shannon-Wiener do componente arbóreo (DBH > 4,8 cm) foi de H' = 3.96 nats.indivíduo -1 (Gomes et al. 2011).
Parcela H - nas coordenadas 23º 22' 52" S e 45º 04' 43" O (Figura 1), também se situa na Fazenda Capricórnio. A topografia ondulada, com altitudes variando de 200 a 216 m. O solo apresenta características semelhantes as da parcela B (Martins 2010).
Na parcela H foram registrados 1.459 indivíduos vivos distribuídos em 152 espécies, 98 gêneros e 44 famílias, sendo as famílias mais importantes Myrtaceae, Rubiaceae, Arecaceae e Sapotaceae. As espécies mais importantes são Rudgea jasminoides, Euterpe edulis e Eriotheca pentaphylla (Vell.) A.Robyns que, apesar de ter um número menor (42) de indivíduos do que Mollinedia schottiana (74), Coussarea meridionalis var. porophylla (Vell.) Müll. Arg. (65) e Coussarea accedens (52), aparece em terceiro lugar em importância em função do elevado valor de cobertura (Ramos et al. 2011).
Myrtaceae é também a família com o maior número de espécies, 32 espécies de oito gêneros. Quatro famílias - Aquifoliaceae, Burseraceae, Magnoliaceae e Salicaceae - e 78 gêneros são representadas por uma única espécie e 41 espécies são representadas por apenas um indivíduo. Na parcela H o índice de Shannon-Wiener foi de H' = 4,05 nats.indivíduo -1 (Ramos et al. 2011).
Parcela I - nas coordenadas 23º 22' 01" S e 45º 05' 01" O (Figura 1) também localizada na Fazenda Capricórnio, em uma área com um forte declive, com uma amplitude de 49 m entre a altitude mais baixa (325 m) e a altitude mais alta (374 m). Assim como as demais parcelas no sopé e nas encostas da Serra do Mar estudadas, o solo é um Cambisolo háplico distrófico, ácido e com alta saturação de alumínio (Martins 2010).
Na parcela I foram registrados 1.993 indivíduos vivos, distribuídos em 203 espécies, 111 gêneros e 50 famílias. A família mais rica foi Myrtaceae, com 50 espécies (25% da riqueza), seguida por Rubiaceae, com 19 espécies, Fabaceae, com 15 espécies, Lauraceae, com dez espécies e Sapotaceae, com nove espécies. Vinte e quatro famílias apresentaram uma única espécie.
A família Rubiaceae, foi a mais abundante, com 518 indivíduos (26% dos indivíduos), seguida por Arecaceae, com 301 indivíduos (15%), Myrtaceae, com 278 (14%), Sapotaceae, com 88 (4%) e Monnimiaceae, com 68 indivíduos (3% dos indivíduos). No outro extremo, sete famílias (Asteraceae, Combretaceae, Lamiaceae, Malpighiaceae, Opiliaceae, Phytolaccaceae e Picramniaceae) foram representadas por um único indivíduo cada (Gomes et al. 2011).
A espécie mais freqüente foi Euterpe edulis que ocorreu em 63 das 100 subparcelas, totalizando 139 idivíduos. A espécie mais abundante foi Bathysa mendoncaei K.Schum ., com 218 indivíduos. Na parcela I o índice de Shannon-Wiener foi de H' = 4,34 nats.indivíduo -1 (Gomes et al. 2011).
Parcela J - nas coordenadas 23º 21' 59" S e 45º 05' 02" O (Figura 1) também se situa na Fazenda Capricórnio, em uma área com declive acentuado, amplitude de 47 m entre a altitude mais baixa (348 m) e a mais elevada (395 m). O solo é semelhante ao encontrado nas demais parcelas da encosta (Tabela 2, Martins 2010).
Nesta parcela foram registrados 1.823 indivíduos vivos, distribuídos em 206 espécies, 102 gêneros e 48 famílias. As famílias de maior abundância na comunidade foram Rubiaceae (346 indivíduos), Myrtaceae (256), Arecaceae (237) e Sapotaceae (107), que juntas somaram 50,29% do total de indivíduos. As famílias de maior riqueza na comunidade foram Myrtaceae (43 espécies), Rubiaceae (19), Lauraceae (16), Fabaceae (13), Sapotaceae (oito) e Melastomataceae (oito) que juntas somaram 51,45% das espécies (Rochelle et al. 2011).
As espécies mais abundantes na área foram Euterpe edulis Mart., com 179 indivíduos e presença em 78 das 100 subparcelas, e Bathysa mendoncaei K. Schum., com 147 indivíduos e presente em 65 subparcelas. Por outro lado 44 espécies (21,36% do total) foram amostradas com apenas um indivíduo (Rochelle et al. 2011).
Nessa parcela foram registradas duas espécies novas e duas espécies tiveram seu primeiro registro para o estado de São Paulo. A diversidade, estimada pelo índice de Shannon-Wiener (H') foi de 4,48 nats.indivíduo -1, e a riqueza da área (206 espécies em 1 ha) estão entre as maiores registradas em levantamentos de florestas brasileiras (Rochelle 2008, Rochelle et al. 2011).
2.2. Comparação entre as Parcelas da Floresta Ombrófila Densa Submontana
Essas quatro parcelas apresentaram índices de diversidade semelhantes (variando de H' = 3,96 na parcela G a H' = 4,48 nats. indivíduo -1 na parcela J) aos das parcelas deste estudo amostradas nas FOD das Terras Baixas. Os índices são elevados quando comparados aos valores encontrados em Juréia/Itatins (Melo et al. 1998), Cachoeira do Macau (Kurtz & Araujo 2000), Morro do Baú (Lisboa 2001), Macaé (Guedes-Bruni et al. 1997, Pessoa et al. 1997), se considerarmos apenas estudos realizados em áreas contínuas e utilizando mesmo critério de inclusão (DAP > 4,8 cm). Entretanto, apesar de elevados, os índices de diversidade desse trecho da encosta da Serra do Mar ainda são inferiores aos encontrados por Thomaz & Monteiro (1997) em Santa Teresa, no Espírito Santo.
Nas quatro parcelas as famílias com o maior número de espécies foram Myrtaceae, Fabaceae, Lauraceae e Sapotaceae. Já em termos de número de indivíduos as famílias que mais se destacam são Rubiaceae, especialmente os gêneros Rudgea, Bathysa e Coussarea, Arecaceae, Euterpe, Syagrus e Astrocaryum, Myrtaceae, diversos gêneros com destaque para Eugenia e Marlierea, Sapotaceae, Chrysophyllum, Ecclinusa e Pouteria, e Lauraceae, Cryptocarya e Ocotea. Em relação às Fabaceae, cada gênero ocorre um número relativamente reduzido de indivíduos, mas em função do porte dos indivíduos se destaca em termos de valor de importância (VI).
Como destacando anteriormente, no caso da Parcela F, onde ocorreu uma exploração seletiva de espécies madeireiras, as samambaiaçus da família Cyatheaceae, gêneros Alsophila e Cyathea, aparece entre as com maior número de indivíduos.
Parcela K - nas coordenadas 23º 19' 31" S e 45º 04' 07" O (Figura 1), está localizada ao longo da Trilha do rio Itamambuca, Núcleo Santa Virgínia. Segundo Padgurschi et al. (2011) a topografia é fortemente inclinada (40º), com altitudes variando de 1.050 a 1.100 m, aproximadamente. O solo é classificado como Cambissolo háplico distrófico típico, argiloso, ácido (pH 3,5), com alta diluição de nutrientes e alta saturação de alumínio (Tabela 2, Martins 2010).
Nesta parcela foram amostrados 1.965 indivíduos, sendo 114 (5,8%) mortos e o restante pertencente a 189 espécies distribuídas em 43 famílias botânicas (Padgurschi et al. 2011). Dentre essas Myrtaceae foi a que apresentou o maior número de espécies (49), seguida por Lauraceae (26), Monimiaceae (11) e Rubiaceae (nove). A família mais abundante foi Arecaceae com 562 indivíduos (28,6%) e somada a esta outras cinco famílias (Myrtaceae, Lauraceae, Sapotaceae e Monimiaceae) totalizaram 1203 indivíduos (61,22%) (Padgurschi 2010). No outro extremo estão oito famílias com apenas um indivíduo cada (Caricaceae, Malpighiaceae, Rosaceae, Phytolacaceae, Cardiopteridaceae, Solanaceae, Celastraceae, Phyllantaceae).
Nesta parcela Padgurschi (2010) mapeou 579 moitas da taquara Merostachys neesii Ruprecht (Poaceae). Entretanto, a autora concluiu que a presença das taquaras no hectare estudado não apresentou relações negativas com o componente arbóreo. Porem, como Merostachys neesii se dissemina rapidamente em áreas perturbadas, talvez ela responda mais rapidamente a alterações do ambiente, seja pelo surgimento de clareira natural ou por ações antrópicas, ocupando essas áreas sem proporcionar oportunidade para o recrutamento de indivíduos de outras espécies.
Considerando os indivíduos com DBH > 4,8 cm a diversidade, estimada pelo índice de Shannon-Wiener (H'), foi de 3,72 nats.indivíduo -1 (Padgurschi et al. 2011).
Parcela N - nas coordenadas 23º 20' 36" S e 45º 04' 22" O (Figura 5), está localizada ao longo da Trilha do Itamambuca, Núcleo Santa Virgínia. A topografia é fortemente inclinada, com altitudes variando de 1010 a 1040 m. Como nas demais parcelas da encosta o solo é classificado como Cambisolo háplico distrófico típico, argiloso, ácido (pH ~4), com alta diluição de nutrientes e alta saturação de alumínio (Martins 2010).
Na Parcela N, da FOD Montana, foram amostrados 1.560 indivíduos, sendo 121 (8,4%) mortos, pertencentes a 149 espécies, distribuídas em 40 famílias (Padgurschi et al. 2011). Myrtaceae apresentou a maior riqueza para as famílias; dentre 30 espécies identificadas, o gênero Eugenia apresentou 11 espécies. Segue-se Lauraceae com 16 espécies, destacando-se as seis espécies de Ocotea. Fabaceae é a terceira família em riqueza de espécies e, dentre essas Inga é o gênero com maior número de espécies (quatro). As famílias Solanaceae, Rubiaceae, Monimiaceae e Cyatheaceae apresentaram oito espécies cada.
As famílias com o maior número de indivíduos foram Arecaceae (298 ind), Myrtaceae (266), Monimiaceae (114), Lauraceae (113), Cyatheaceae (70). As famílias Quiinaceae, Chloranthaceae, Sabiaceae, Opiliaceae e Proteaceae estão representadas por apenas um indivíduo.
A diversidade dos indivíduos com DAP > 4,8 cm, determinada pelo índice de Shannon-Wiener (H') foi de 4,09 nats.indivíduo -1 (Pereira 2011).
As cinco espécies mais abundantes foram Euterpe edulis (298 indivíduos), Licania hoehnei (42), Calyptranthes lucida (40), Ocotea catharinensis (37) e Mollinedia argyrogyna (35). As espécies com 10 ou mais indivíduos inventariados da parcela N e compõem, aproximadamente, um quarto (40 espécies) do total (161) das espécies identificadas e 75% (1.074 inds) do total de indivíduos coletados (1.439 inds.).
2.3. Comparação entre Parcelas da Floresta Ombrófila Densa Montana
Nas duas parcelas de FOD Montana foram registrados 3.288 indivíduos vivos, distribuídos em 265 espécies pertencentes a 51 famílias (Padgurschi 2010, Pereira 2011, Padgurschi et al. 2011).
Em termos de número de indivíduos as duas parcelas estudadas (K e N) são dominadas por Euterpe edulis Mart. (palmito-Jussara), para a qual foram registrados 860 indivíduos, e apresentam uma elevada ocorrência de moitas da taquara Merostachys neesii Ruprecht. Além de Arecaceae, destacam-se pelo grande número de indivíduos Myrtaceae (561 indivíduos), especialmente Myrcia, Lauraceae (255), especialmente Ocotea, Monimiaceae (215), especialmente Mollinedia, e Cyatheaceae (159), especialmente Cyathea. Por outro lado, 71 espécies na parcela K e 37 espécies na Parcela N estão representadas por apenas um indivíduo, das quais se destacam Prunus myrti folia (L.) Urb. (Rosaceae), Cedrela odorata L. (Meliaceae), Agonandra excelsa Griseb. (Opiliaceae), Weinmannia paulliniifolia Pohl (Cunoniaceae) e Drimys brasiliensis Miers (Winteraceae) (Padgurschi 2010, Pereira 2011, Padgurschi et al. 2011).
As famílias com a maior riqueza de espécies são Myrtaceae (57 espécies), Lauraceae (33), Fabaceae (15), Monimiaceae (15) e Rubiaceae (13). Destaca-se a diversidade de espécies de Monimiaceae, família Pantropical com cinco gêneros ocorrendo no Brasil, considerada como típica da Floresta Montana (Peixoto et al. 2002).
3. Comparações florísticas ao longo do gradiente
Nas 11 parcelas onde foi realizado o estudo florístico foram encontradas 562 espécies, distribuídas em 195 gêneros e 68 famílias (Anexo 1). Apenas oito espécies - Euterpe edulis, Calyptranthes lucida, Marlierea tomentosa, Guapira opposita, Hieronyma alchorneoides, Cupania furfuracea, Cecropia glaziovii Snethl. e Coussapoa microcarpa - ocorreram da Restinga até FOD Montana podendo ser consideradas de grande amplitude nesta formação. Ao longo do gradiente as famílias com o maior número de espécies foram Myrtaceae (133) e Fabaceae (47), acrescidas de Rubiaceae (49), Lauraceae (49), sendo que Monimiaceae (15) aparece especificamente nas parcelas FOD Montana. Em termos de número de indivíduos as famílias mais importantes são Arecaceae, Rubiaceae, Myrtaceae, Sapotaceae, Lauraceae e na FOD Montana, Monimiaceae. Somente na parcela F, onde ocorreu exploração madeireira, a abundância de palmeiras foi substituída pelas Cyatheaceae. O gênero Eugenia (Myrtaceae) foi o que teve a maior densidade de espécies em todas as áreas, exceto para a parcela K, onde a densidade maior se deu para o gênero Ocotea (Lauraceae). Ao longo da encosta, a composição florística variou substancialmente, mas em um padrão não diretamente relacionado com a altitude (Figura 7). A ausência deste padrão "áreas baixas - áreas intermediárias - áreas altas" nas ordenações sugere que outros fatores além da altitude, estariam influenciando a distribuição das espécies ao longo da encosta.
A ocorrência frequente de neblina, que na região estudada usualmente cobre a encosta da Serra do Mar desde as regiões mais altas até a zona de transição entre a FOD Submontana e a FOD Montana, pode ser um destes fatores que influenciam na distribuição das espécies. Na região da Serra do Mar, ao longo de um gradiente de altitude, massas de ar resfriam-se adiabaticamente ≈0.6 ºC a cada 100 m, o que leva a uma diferença média de temperatura de 6 ºC do nível do mar, parcela de Floresta de Restinga, até a cota de 1.000 m, parcelas de FOD Montana.
Pouco se sabe sobre o papel desse evento climático na manutenção de processos fisiológicos, hidrológicos e biogeoquímicos de florestas situadas nas cotas mais elevadas da Serra do Mar. Recentemente, por exemplo, Rosado et al. (2012) demonstraram que espécies arbóreas da FOD transpiram à noite. Por outro lado, diversos estudos têm sugerido que a precipitação por neblina representa uma proporção significante no balanço hídrico e de nutrientes em florestas tropicais e subtropicais situadas em cotas mais elevadas (Bruijnzeel 1990). Por exemplo, eventos de neblina contribuíram com um valor entre 30 a 60% do total da água precipitada em florestas de altitude nos Andes (Cavalier & Golstein 1989), florestas de sequóias na Califórnia (Dawson 1998) e florestas subtropicais na Austrália (Hutley et al. 1997).
Em estudo realizado com Drimys brasiliensis Miers (Winteraceae), Eremanthus erythropappus (DC.) MacLeish (Asteraceae) e Myrsine umbellata Mart. (Primulaceae), Lima (2010), usando experimentos com água deuterada e sais traçadores apoplásticos, demonstrou que estas espécies podem absorver água diretamente pelas folhas. "A absorção foliar pode contribuir em até 42% do conteúdo de água das folhas em D. brasiliensis, que inclusive apresentou fluxo reverso de seiva e menores taxas de transpiração noturna quando expostas à neblina" (Lima 2010). Essa última espécie citada ocorre na parcela K (FOD Montana).
A Floresta de Restinga e a FOD Atlântica ocorrem sobre solos distróficos com baixa disponibilidade de nitrogênio (Martins 2010), assim como a maioria das florestas tropicais do planeta. Entretanto, considera-se que essas florestas sejam mais limitadas por fósforo do que propriamente nitrogênio (Martinelli et al. 1999). Em relação à FOD Atlântica, o conteúdo de nitrogênio no solo aumentou com a altitude, provavelmente em função da queda de temperatura como indicam Vieira et al. (2011).
A família Fabaceae está bem representada ao longo do gradiente altitudinal, tendo sido encontradas 140 espécies (18 Caesalpinioideae, 42 Mimosoideae e 80 Papilionoideae; 61 são arbóreas, 56 são subarbustos e arbustos e 23 são lianas) no levantamento florístico realizado por Silva & Tozzi (2011). Apesar dessa freqüência em termos florísticos, a importância das espécies arbóreas da referida família na estrutura da vegetação foi surpreendentemente pouco significativa. Os levantamentos fitossociológicos indicam um mínimo de oito espécies para a Floresta de Restinga e o máximo de 18 espécies para a fisionomia FOD Submontana, sendo que de modo geral, os valores de importância alcançados pela família Fabaceae não ultrapassam 5%. Cabe notar que o gênero Inga ocorreu em todas as altitudes estudadas apresentando 13 espécies com diferentes distribuições.
Fabaceae, especialmente as subfamílias Mimosoideae e Faboideae, com a fixação de nitrogênio contribuem significativamente para disponibilidade desse nutriente essencial através da decomposição de folhas, ramos, galhos, troncos e estruturas reprodutivas. Manarin (2012) constatou a ocorrência de nodulação ativa na FOD Atlântica, sendo que o número de raízes noduladas e as atividades da enzima nitrogenase foram muito maiores na FOD Terras Baixas quando comparadas com a FOD Montana.
Na análise de gradientes (Figura 7) o 1º eixo separou a Parcela A, em função da Floresta de Restinga ocorrer sobre um tipo de solo (Neossolo Quartzarênico) distinto daquele da encosta (Cambisolo Háplico Distrófico). Certamente o fato do solo da Floresta de Restinga ser sazonalmente inundado, característica esta que exerce forte pressão seletiva, pois poucas espécies arbóreas toleram esse estresse (Oliveira & Joly 2010, Oliveira 2011), atua de forma sinergística reforçando esta separação da Parcela A observada na Figura 7b
As diferenças na estrutura e composição do componente com DAP > 4,8 cm entre a Floresta de restinga e a adjacente Floresta Ombrófila Densa das Terras Baixas é discutida em profundidade no trabalho de Assis et al. (2011). Diferenças florísticas significativas entre estas duas formações ocorrem também em termos de pteridófitas (Nóbrega et al. 2011) e briófitas (Santos et al. 2011). Essas diferenças reforçam a necessidade apontada por Marques et al. (2011) quanto à conservação de ambas as formações, Floresta de restinga e FOD Terras Baixas.
A separação da parcela F, evidenciada principalmente no segundo eixo (Figura 7b), poderia ser explicada como uma alteração na composição florística em decorrência do corte seletivo de Hyeronima alchorneoides para extração de madeira entre 1950 e 1985. Apesar de seletiva, essa extração certamente influenciou a dinâmica e a sucessão na área, favorecendo algumas espécies e eliminando outras. A separação das Parcelas A e F em relação às demais também ficou evidente na análise de agrupamento (Figura 7a).
Outros trabalhos feitos no Brasil mostraram que a altitude foi, ao menos aparentemente, importante na detecção de afinidades florísticas. Scudeller et al. (2001) encontraram elevado compartilhamento de espécies entre amostras feitas em elevadas altitudes no estado de São Paulo. Moreno et al. (2003) encontraram diferenças significativas na análise de similaridade em duas áreas de Mata Atlântica, uma a 50 m e outra a 200 m de altitude. Em uma Floresta Alto-Montana com características climáticas peculiares ao longo da amplitude altitudinal investigada, Meireles et al. (2008) obtiveram boa separação entre parcelas nas menores altitudes e as demais e, como tendência secundária, uma separação das parcelas mais altas daquelas situadas em altitudes intermediárias.
3.1. Riqueza de espécies
Em cada nível da encosta, a vegetação é resultado de uma interação entre as espécies constituintes, solos (essencialmente o mesmo em toda amplitude da encosta), topografia, exposição da vertente e clima. Cabe destacar que na FOD Montana o clima é mais frio (em média 5 ºC abaixo da temperatura ao nível do mar), o que reduz a taxa de decomposição da matéria orgânica e, consequentemente, aumenta o acúmulo de carbono e nitrogênio no solo (Vieira et al. 2011). Essa interação, que vem ocorrendo há milhares de anos, pode apresentar como resultado uma zonação altitudinal, com reflexos nas diferenças dos níveis de diversidade em diferentes regiões da encosta (Zhao et al. 2005). O gradiente estudado apresenta um pico de diversidade e riqueza nas altitudes intermediárias (em torno de 400 m), com índice de diversidade (H') variando de 3,96 a 4,48 nats.individuo -1 (Figura 8). Trata-se de uma cota altitudinal de riqueza ímpar, uma vez que é pouco comum encontrarmos, nas amostragens realizadas na Floresta Ombrófila Densa Atlântica, riqueza superior a 200 espécies (Siqueira 1994, Tabarelli & Mantovani 1999, Scudeller et al. 2001). Esse pico de diversidade e riqueza nas altitudes intermediárias ao longo da encosta é similar aos resultados encontrados em outras florestas no mundo, como na Arábia Saudita (Hegazy et al. 1998), no Nepal (Grytnes & Vetaas 2002) e na Costa Rica (Sesnie et al. 2009) em um gradiente altitudinal muito parecido com o deste estudo, (40-1.200 m), mas com amostragem muito maior (127 "plots" de 0,25 ha). Esse padrão se repete em famílias específicas, como é o caso de Arecaceae no gradiente aqui estudado (Fisch 2009) e em outras áreas na região Neotropical (Svenning et al 2008, Eiserhardt et al. 2011).
Além disso, o resultado aproxima-se, ou mesmo supera, a riqueza encontrada em várias outras florestas neotropicais (ver Tabarelli & Mantovani 1999). O resultado contrasta com o argumento de Tabarelli & Mantovani (1999) de que as florestas atlânticas de encosta apresentam menor riqueza de espécies arbóreas em relação às outras florestas neotropicais. De maneira geral, não houve uma relação linear significativa entre riqueza e diversidade de espécies e a altitude. Em áreas mais altas (>500 m, na Floresta Ombrófila Densa Montana) a riqueza decai em relação às áreas de altitude intermediária (400 m) (Figura 8). Há atualmente um intenso debate na literatura sobre os fatores causais deste padrão, com hipóteses relacionadas com a produtividade (Evans et al. 2005), temperatura (Sanders et al. 2007), a Teoria Metabólica da Ecologia (MET) (Brown et al. 2004), o efeito geométrico ("mid-domain effect" Colwell & Lees 2000) e o efeito "Massenerhebung" (Grubb 1971, Bruijnzeel et al. 1993).
Dando continuidade ao Projeto BIOTA Gradiente Funcional, algumas destas hipóteses poderão ser testadas, tão logo o levantamento das parcelas O (600-650 m) e P (Figura 800-850 m), em altitudes intermediárias entre a parcela J (348-395 m) e a parcela K (1050-1100 m), seja concluído.
Outra explicação, que não exclui as anteriores, é a variação do limite altitudinal de ocorrência das fitofisionomias, durante as flutuações climáticas do Pleistoceno. Meireles et al. (2010) projetando os limites das fitofisionomias da FOD Atlântica durante o Último Máximo Glacial, aproximadamente entre 20 e 13 mil anos atrás, mostraram que o limite altitudinal inferior da FOD Alto Montana (que ocorre hoje acima de 1.200 m) estaria entre 400 e 500 m.
3.2. Estrutura da Floresta Ombrófila Densa
A Tabela 6 resume os dados de 11 das 14 parcelas do Projeto BIOTA Gradiente Funcional.
De maneira geral, a FOD no Parque Estadual da Serra do Mar apresentou uma estrutura vertical com poucos estratos bem definidos: o subosque, com plantas de até 3 m; um estrato intermediário, com plantas de até 10 m; o dossel, com árvores de até 18 m; e poucas árvores emergentes, com alturas inferiores a 30 m. A comparação da estrutura vertical entre as diferentes fitofisionomias mostrou que todas apresentaram um estrato intermediário muito denso, com uma grande proporção de indivíduos entre 5 e 10 m de altura. Apenas uma pequena proporção dos indivíduos amostrados (<10%) nas diferentes fitofisionomias atingiram mais do que 18 m de altura. Essa proporção atingiu valores mais baixos nas FOD de Terras Baixas e Terras Baixas Explorada (4-6,5%) (Alves et al. 2010, Scaranello et al. 2012).
Todas as fitofisionomias de Floresta Ombrófila Densa apresentarem uma distribuição assimétrica do número total de indvíduos.ha -1 por classe de diâmetro, com maior proporção (47- 53%) de indivíduos de menor tamanho (<10 cm), os quais foram responsáveis por apenas 7-12% da área basal total.
Diferenças significativas entre as fitofisionomias puderam ser observadas em relação à distribuição da área basal total. Na Restinga e na FOD Explorada, menos de 50% da área basal total (34-47%) esteve concentrada nas maiores classes de diâmetro (>30 cm), enquanto nas demais fitofisionomias - FOD de Terras Baixas, Submontana e Montana - a contribuição dos indivíduos com mais de 30 cm de DAP ultrapassou 50% (51-56%). Nas parcelas de FOD Submontana e Montana, as maiores classes de diâmetro (30-50 e >50 cm) apresentaram maior área basal do que as demais fitofisionomias. As maiores diferenças foram observadas na contribuição de Indivíduos muito grandes (>50 cm). As estimativas de área basal variaram 4,5 vezes entre as fitofisionomias (Alves et al. 2010).
Considerações Finais
Os dados aqui apresentados mostram a extraordinária riqueza de espécies arbóreas da Floresta Ombrófila Densa Atlântica dos Núcleos Picinguaba e Santa Virgínia do Parque Estadual da Serra do Mar. Uma vez mais, temos uma floresta tropical luxuriante sobre um solo com baixa disponibilidade de nutrientes, demonstrando a importância e a eficiência da ciclagem de nutrientes em uma região de alta pluviosidade e com um diferencial significativo de temperatura entre o nível do mar e o topo da serra, diferencial esse que reduz a velocidade do processo de decomposição e resulta em um crescente acúmulo de matéria orgânica no solo.
O conjunto de dados gerados pelo Projeto BIOTA Gradiente Funcional sugerem fortemente que a estrutura e a composição florística do componente com DAP > 4,8 cm também são afetadas por fatores abióticos ao longo do gradiente. Esses fatores são sensíveis às mudanças climáticas globais (Laurance et al. 2011, Stegen et al. 2011), justificando, portanto a utilização de Parcelas Permanentes onde os reflexos destas alterações na composição, estrutura e funcionamento da floresta podem ser monitorados a longo prazo, visando compreender os processos que geram e/ou mantêm a riqueza e a diversidade de espécies.
É de fundamental importância também utilizar essa base de dados para elucidar a relação entre a diversidade e os serviços ecossistêmicos, gerando subsídios para o envolvimento da comunidade local no esforço de preservação desta magnífica floresta.
Agradecimentos
Agradecemos aos funcionários do Parque Estadual da Serra do Mar, Núcleos Picinguaba e Santa Virginia pelo apoio constante ao longo do projeto. Ao grande auxílio prestado durante a implantação das parcelas permanentes dos alunos: Carolina Virillo, Christiane E. Corrêa, Juliano van Melis, Bruno Aranha, Marcos Scaranello, Yvonne Bakker, Valéria Martins, Viviane Camila de Oliveira, Larissa Veiga, Amanda Calil, Maria Hunter, Eduardo Miranda, Cristina Felsemburgh, Bruno Ascenção, Patrícia Jungbluth, Rafael Tannus, Tatiana Andrade; técnicos: Jesuíno Ferrari, Edmar Mazzi, Fernando Perencin, Luiz Ramalho, Claudio Paladini, e aos pesquisadores: Rafael Oliveira, Daniela Mariano, Frederico Guilherme, Roque Filho, Michael Keller; aos funcionários da Fazenda Capricórnio, Sr. Salvador e Sr. Osvaldo, ao Sr. Roberto e seu filho (comunidade Casa da Farinha).
Este trabalho foi financiado pela Fundação de Amparo à Pesquisa do Estado de São Paulo (FAPESP) no âmbito do Projeto Temático Biota Gradiente Funcional (Processo 03/12595-7), que faz parte do Programa BIOTA/FAPESP - O Instituto Virtual da Biodiversidade (www.biota.org.br). Autorização COTEC/IF 41.065/2005 e autorização IBAMA/CGEN 093/2005.
Recebido em 20/12/2010
Versão reformulada recebida em 10/01/2012
Publicado em 15/03/2012
- AB'SABER, A.N. 1977. Os domínios morfoclimáticos na América do Sul. Primeira aproximação. Geomorfologia. 52:1-21.
- ALVES, L.F. & SANTOS, F.A.M. 2002. Tree allometry and crown shape of four tree species in Atlantic rain forest, SE Brazil. J. Trop. Ecol. 18:245-260.
- ALVES, L.F., VIEIRA, S., SCARANELLO, M., CAMARGO, P.B., SANTOS, F.A.M., JOLY, C.A. & MARTINELLI, L.A. 2010. Forest structure and live aboveground biomass variation along an elevational gradient of tropical Atlantic moist forest (Brazil). Forest Ecol. Manag. 260:679-691. http://dx.doi.org/10.1016/j.foreco.2010.05.023
- ANGIOSPERM PHYLOGENY GROUP - APG II. 2003. An update of the Angiosperm Phylogeny Group classification for the orders and families of flowering plants. Bot. J. Linn. Soc. 141:399-436. http://dx.doi.org/10.1046/j.1095-8339.2003.t01-1-00158.x
- ASSIS, M.A. 1999. Florística e caracterização das comunidades vegetais da Planície Costeira de Picinguaba, Ubatuba/SP. Tese de Doutorado, Universidade Estadual de Campinas, Campinas.
- ASSIS, M.A., PRATA, E.M.B., PEDRONI, F., SANCHEZ, M., EISENLOHR, P.V., MARTINS, F.R., SANTOS, F.A.M., TAMASHIRO, J.Y., ALVES, L.F., VIEIRA, S.A., PICCOLO, M.C., MARTINS, S.C., CAMARGO, P.B., CARMO, J.B., SIMÕES, E., MARTINELLI, L.A. & JOLY, C.A. 2011. Florestas de Restinga e de Terras Baixas do Núcleo Picinguaba, PESM, Ubatuba, Sudeste do Brasil: vegetação e heterogeneidade ambiental. Biota Neotrop. 11(2): http://www.biotaneotropica.org.br/v11n2/pt/abstract?article+bn02111022011
- BAKKER, J. P., OLFF, H., WILLEMS, J. H., ZOBEL, M. 1996. Why Do We Need Permanent Plots in the Study of Long-Term Vegetation Dynamics? J. Veg. Sci. 7(2):147-155. http://dx.doi.org/10.2307/3236314
- BORGES, R.F.; CARNEIRO, M.A. & VIANA, P. 2011 Altitudinal distribution and species richness of herbaceous plants in campos rupestres of the Southern Espinhaço Range, Minas Gerais, Brazil. Rodriguésia. 62(1):139-152.
- BROWN, J.H., GILLOOLY, J.F., ALLEN, A.P., SAVAGE, V.M. & WEST, G.B. 2004 Toward a metabolic theory of ecology. Ecology. 85:1771-1789. http://dx.doi.org/10.1890/03-9000
- BRUIJNZEEL, L.A. 1990 Hydrology of Moist Tropical Forests and Effects of Conversion: a State of Knowledge Review. IHP-UNESCO Humid Tropical Programme, Paris.
- BRUIJNZEEL, L.A., WATERLOO, M.J., PROCTOR, J., KUITERS A.T. & KOTTERINK, B. 1993. Hydrological observations in montane rain forests on Gunung Silam, Sabah, Malaysia, with special reference to the "Massenerhebung" effect. J. Ecol. 81:145-1. http://dx.doi.org/10.2307/2261231
- CAMPOS, M.C.R. 2008. Relação da composição e estrutura do componente arbóreo com variáveis microtopográficas e edáficas da Floresta Ombrófila Densa do Núcleo Picinguaba/PESM, Ubatuba/SP. Dissertação de Mestrado, Universidade Estadual de Campinas, Campinas.
- CAMPOS, M.C.R., TAMASHIRO, J.Y., ASSIS, M.A. & JOLY, C.A. 2011. Florística e fitossociologia do componente arbóreo da transição Floresta Ombrófila Densa das Terras Baixas - Floresta Ombrófila Densa Submontana do Núcleo Picinguaba/PESM, Ubatuba, sudeste do Brasil. Biota Neotrop. 11(2) http://www.biotaneotropica.org.br/v11n2/pt/abstract?inventory+bn02311022011
- CAVALIER, J. & GOLDSTEIN, G. 1989. Mist and fog interception in elfin cloud forests in Columbia and Venezuela. J. Trop. Ecol. 5:309-322. http://dx.doi.org/10.1017/S0266467400003709
- CLARK, D.A. 2002. Are tropical forests an important carbon sink? Reanalysis of the long-term plot data. Ecol. Appl. 12:3-7. http://dx.doi.org/10.1890/1051-0761(2002)012[0003:ATFAIC]2.0.CO;2
- CLARK, D.B. & CLARK, D.A. 1992 Life-History diversity of canopy and emergent trees in a neotropical rain-forest. Ecol. Monogr. 62(3):315-344. http://dx.doi.org/10.2307/2937114
- CLARK, D.B. & CLARK, D.A. 2000. Landscape-scale variation in forest structure and biomass in a tropical rain forest. Forest Ecol. Manag. 137:185-198. http://dx.doi.org/10.1016/S0378-1127(99)00327-8
- COLOMBO, A.F. & JOLY, C.A. 2010. Brazilian Atlantic Forest lato sensu: the most ancient Brazilian forest, and a biodiversity hotspot, is highly threatened by climate change. Braz. J. Biol. 70(3):697-708. http://dx.doi.org/10.1590/S1519-69842010000400002
- COLWELL, R.K. & LEES, D.C. 2000. The mid-domain effect: geometric constraints on the geography of species richness. Trends Ecol. Evol. 15:70-76. http://dx.doi.org/10.1016/S0169-5347(99)01767-X
- CONDIT, R. 1995. Research in large, long-term tropical forest plots. Trends Ecol. Evol. 10:18-22. http://dx.doi.org/10.1016/S0169-5347(00)88955-7
- DALLMEIER, F. 1992. Long-term monitoring of biological diversity in tropical forest areas: methods for establishment and inventory of permanent plots. MAB Digest 11, Unesco, Paris.
- DAWSON, T.E. 1998. Fog in the California redwood forest: ecosystem inputs and use by plants. Oecologia 117:476-485. http://dx.doi.org/10.1007/s004420050683
- EMBRAPA. 2009. Banco de dados climáticos do Brasil. http://www.bdclima.cnpm.embrapa.br/ (último acesso em 31/01/2012).
- EISERHARDT, W.L.; BJORHOLM, S.; SVENNING, J-C.; RANGEL, T.F. & BALSLEV, H. 2011. Testing the Water-Energy Theory on American Palms (Arecaceae) Using Geographically Weighted Regression. PLoS ONE 6(11): e27027. PMid:22073244. PMCid:3207816. http://dx.doi.org/10.1371/journal.pone.0027027
- EVANS, K.L., WARREN, P.H. & GASTON, K.J. 2005. Species-energy relationships at the macroecological scale: a review of the mechanisms. Biol. Rev. 80:1-25. PMid:15727036. http://dx.doi.org/10.1017/S1464793104006517
- FIASCHI, P. & PIRANI, J.R. 2009. Review of plant biogeographic studies in Brazil. J. Syst. Evol. 47:477-496. http://dx.doi.org/10.1111/j.1759-6831.2009.00046.x
- FIDALGO, O. & BONONI, V.L.R. 1984. Técnicas de coleta, preservação e herborização de material botânico. Instituto de Botânica, São Paulo.
- FISCH, S. T. V. 2009. Is the palm community a good indicator for altitudinal zonation in the Atlantic Rain Forest? In Annual Meeting ATBC - Impacts of global change on tropical ecosystems: cross-cuting the abiotic, biotic and human spheres. Marburg, Germany.
- FUNDAÇÃO SOS MATA ATLÂNTICA & INSTITUTO NACIONAL DE PESQUISAS ESPACIAIS - INPE. 2002. Atlas dos remanescentes da Mata Atlântica 1995-2000. Fundação SOS Mata Atlântica, São Paulo.
- GALINDO, L. & CÂMARA, I.G. 2005. Mata Atlântica: Biodiversidade, Ameaças e Perspectivas. Fundação SOS Mata Atlântica; Conservation International, São Paulo.
- GENTRY, A.H. 1992. Tropical forest biodiversity: distributional patterns and their conservational significance. Oikos 63:19-82. http://dx.doi.org/10.2307/3545512
- GIOVANELLI, J.G.R., SIQUEIRA, M. F., HADDAD, C.F.B. & ALEXANDRINO, J. 2010. Modeling a spatially restricted distribution in the Neotropics: How the size of calibration area affects the performance of five presence-only methods. Ecol. Model. 221:215-224. http://dx.doi.org/10.1016/j.ecolmodel.2009.10.009
- GOMES, J.A.M.A., BERNACCI, L.C. & JOLY, C.A. 2011. Diferenças florísticas e estruturais entre duas cotas altitudinais da Floresta Ombrófila Densa Submontana Atlântica, do Parque Estadual da Serra do Mar, município de Ubatuba/SP, Brasil. Biota Neotrop. 11(2): http://www.biotaneotropica.org.br/v11n2/pt/abstract?article+bn02611022011
- GRYTNES, J.A. & VETAAS, O.R. 2002 Species richness and altitude: a comparison between simulation models and interpolated plant species richness along the Himalayan altitudinal gradient, Nepal. Am. Natur.159: 294-304.
- GUEDES-BRUNI, R.R., PESSOA, S.V.A. & KURTZ, B.C. 1997. Florística e estrutura do componente arbustivo-arbóreo de um trecho preservado da floresta montana na Reserva Ecológica de Macaé de Cima. In Serra de Macaé de Cima: Diversidade Florística e Conservação em Mata Atlântica (H.C. Lima & R.R. Guedes-Bruni, eds.). Jardim Botânico do Rio de Janeiro, Rio de Janeiro, p.127-146.
- GUILHERME, F.A.G., MORELLATO, L.P.C. & ASSIS, M.A. 2004. Horizontal and vertical tree community structure in a lowland Atlantic Rain Forest, Southeastern Brazil. Rev. Bras. Bot. 27(4):725-737.
- GRUBB, P.J. 1971. Interpretation of the 'Massenerhebung' Effect on Tropical Mountains Nature 229: 44 - 45.
- HEGAZY, A.K., EL-DEMERDASH, M.A & and HOSNI, H.A. 1998. Vegetation, species diversity and floristic relations along an altitudinal gradient in south-west Saudi J. Arid Environ. 38:3-13. http://dx.doi.org/10.1006/jare.1997.0311
- HIROTA, M.M. 2003. Monitoring the Brazilian Atlantic Forest cover. In: The Atlantic Forest of South America: biodiversity status, trends, and outlook (C. Galindo-Leal & I.G. Câmara, eds.). Center for Applied Biodiversity Science e Island Press, Washington, p.60-65.
- HUBBELL, S.P. & FOSTER, R.B. 1986. Commonness and rarity in a neotropical forest: implications for tropical tree conservation. In Conservation Biology: the science of scarcity and diversity (M. Soulé, ed.). Sunderland, Massachusetts, p.205-231.
- HUTLEY, L. B., DOLEY, D., YATES, D. J. & BOONSANER, A. 1997. Water Balance of an Australian Subtropical Rainforest at Altitude: the Ecological and Physiological Significance of Intercepted Cloud and Fog. Aust. J. Bot. 45(2):311-329. http://dx.doi.org/10.1071/BT96014
- JOLY, C.A., AIDAR, M.P.M., KLINK, C.A., MCGRATH, D.G., MOREIRA, A.G., MOUTINHO, P., NEPSTAD, D.C., OLIVEIRA, A.A., POTT, A., RODAL, M.J.N. & SAMPAIO, E.V.S.B. 1999. Evolution of the Brazilian phytogeography classification systems: implications for biodiversity conservation. Cien. Cult. 51(5-6):331-348.
- JOLY, C.A., MARTINELLI, L.A., ALVES, L.F., VIEIRA, S.A., TAMASHIRO, J.Y., AIDAR, M.P.M., CAMARGO, P.B., ASSIS, M.A., BERNACCI, L.C. & DURIGAN, G. 2008. As parcelas permanentes do Projeto Temático BIOTA Gradiente Funcional: Composição florística, estrutura e funcionamento da Floresta Ombrófila Densa dos Núcleos Picinguaba e Santa Virgínia do Parque Estadual da Serra do Mar, São Paulo, Brasil. In Experiências de monitoramento no bioma Mata Atlântica com uso de parcelas permanentes. (C.R. Sanquetta, org.). Rede de Parcelas Permanentes dos Biomas Mata Atlântica e Pampa - RedeMAP; Fundação Universidade do Paraná - Funpar, Curitiba, p.109-148.
- KEELING, H.C. & PHILLIPS, O.L. 2007. The global relationship between forest productivity and biomass. Global Ecol. Biogeogr. 16(5):618-631. http://dx.doi.org/10.1111/j.1466-8238.2007.00314.x
- KESSLER, M. 2001 Patterns of diversity and range size of selected plant groups along an elevational transect in the Bolivian Andes. Biodivers. Conserv. 10:1897-1921. http://dx.doi.org/10.1023/A:1013130902993
- KÖPPEN, W. 1948. Climatologia. Fondo de Cultura Econômica, México.
- KRONKA, F.J.N., NALON, M.A., MATSUKUMA, C.K., PAVÃO, M., YWANE, M.S.S., KANASHIRO, M.M., LIMA, L.M.P.R., PIRES, A.S., SHIDA, C.N., FUKUDA, J.C., GUILLAUMON, J.R., BARBOSA, O., BARRADAS, A.M.F., BORGO, S.C., MONTEIRO, C.H.B., PONTINHAS, A.A.S., ANDRADE, G.G., JOLY, C.A., COUTO, H.T.Z. & BAITELLO, J.B. 2005. Inventário florestal da vegetação nativa do Estado de São Paulo. Secretaria do Meio Ambiente, Instituto Florestal, São Paulo.
- KURTZ, B.C. & ARAUJO, D.S.D. 2000. Composição florística e estrutura do componente arbóreo de um trecho de Mata Atlântica na Estação Ecológica Estadual do Paraíso, Cachoeiras de Macacu, Rio de Janeiro, Brasil. Rodriguésia. 51(78-79):69-111.
- LAURANCE, W.F., USECHE, D.C., SHOO, L.P., HERZOG, S.K., KESSLER, M., ESCOBAR, F., BREHM, G., . AXMACHER, J.C., CHEN, I-C., HIETZ, P., FIEDLER, K., PYRCZ, T.I., WOLFM, J., MERKORD, C.L., CARDELUS, C., MARSHALL, A.R., AH-PENG, C., APLET, G.H., ARIZMENDI, M.C., BAKER, W.J., BARONE, J., BRÜHL, C.A., BUSSMANN, R.W., CICUZZA, D., EILU, G., FAVILA, M.E., HEMPZ, A., HEMPZ, C., HOMEIER, J., HURTADO, J., JANKOWSKI, J., KATTÁN, G., KLUGE, J., KRÖMER, T., LEES, D.C., LEHNERT, M., LONGINO, J.T., LOVETT, J., MARTIN, P.H., PATTERSON, B.D., PEARSON, R.G., PEH, K. S-H., RICHARDSON, B., RICHARDSON, M., SAMWAYS, M.J., SENBETA, F., SMITH, T.B., UTTERIDGE, T.M.A., WATKINS, J.E., WILSON, R., WILLIAMS, S.E. & THOMAS, C.D. 2011. Global warming, elevational ranges and the vulnerability of tropical biota. Biol Conserv. 144:548-557. http://dx.doi.org/10.1016/j.biocon.2010.10.010
- LEWIS, S.L., PHILLIPS, O.L., BAKER, T.R., LLOYD, J., MALHI, Y., ALMEIDA, S., HIGUCHI, N., LAURANCE, W.F., NEILL, D.A., SILVA, J.N.M., TERBORGH, J., LEZAMA, A.T., MARTINEZ, R.V., BROWN, S., CHAVE, J., KUEBLER, C., VARGAS, P.N. & VINCETI, B. 2004. Concerted changes in tropical forest structure and dynamics: evidence from 50 South American long-term plots. Philos. T. Roy. Soc. Lon. B. 359:421-436. PMid:15212094. http://dx.doi.org/10.1098/rstb.2003.1431
- LIMA, A.L. 2010 O papel ecológico da neblina e a absorção foliar de água em três espécies lenhosas de Matas Nebulares, SP - Brasil. Dissertação de Mestrado, Universidade Estadual de Campinas, Campinas.
- LISBOA, R.B.Z. 2001. Análise fitossociológica de uma comunidade arbórea, na Floresta Ombrófila Densa, no Parque Botânico Morro do Bau - Ilhota/SC. Dissertação de Mestrado, Universidade Federal de Santa Catarina, Florianópolis.
- MAGURRAN, A.E. 2004. Measuring biological diversity. Blackwell Publishing, Oxford.
- MALHI, Y., PHILLIPS, O.L., LLOYD, J., BAKER, T., WRIGHT, J., ALMEIDA, S., ARROYO, L., FREDERIKSEN, T., GRACE, J., HIGUCHI, N., KILLEEN, T., LAURANCE, W.F., LEANO, C., LEWIS, S., MEIR, P., MONTEAGUDO, A., NEILL, D., VARGAS, P.N., PANFIL, S.N., PATINO, S., PITMAN, N., QUESADA, C.A., RUDAS-LL, A., SALOMÃO, R., SALESKA, S., SILVA, N., SILVEIRA, M., SOMBROEK, W.G., VALENCIA, R., MARTINEZ, R. V., VIEIRA, I. C. G. & VINCETI, B. 2002. An international network to monitor the structure, composition and dynamics of Amazonian forests (RAINFOR). J. Veg. Sci. 13:439-450. http://dx.doi.org/10.1111/j.1654-1103.2002.tb02068.x
- MANARIN, E.C. 2012. Capacidade de fixação de nitrogênio por Leguminosas e Cianobactérias em trecho de Floresta Atlântica do Estado de São Paulo. Dissertação de Mestrado, Universidade Estadual de Campinas, Campinas.
- MARQUES, M.C.M., SWAINE, M.D. & LIEBSCH, D. 2011 Diversity distribution and floristic differentiation of the coastal lowland vegetation: implications for the conservation of the Brazilian Atlantic Forest. Biodivers. Conserv. 20:153-168. http://dx.doi.org/10.1007/s10531-010-9952-4
- MARTINELLI, L.A., PICCOLO, M.C., TOWNSEND, A.R., VITOUSEK, P.M., CUEVAS, E., MCDOWELL, W., ROBERTSON, G.P., SANTOS, O.C. & TRESEDER, K. 1999. Nitrogen stable isotopic composition of leaves and soil: Tropical versus temperate forests. Biogeochemistry. 46:45-65. http://dx.doi.org/10.1007/BF01007573
- MARTINS, S.C. 2010. Perdas de nitrogênio pela emissão de óxido nitroso (N2O) e sua relação com a decomposição da serapilheira e biomassa de raízes na floresta de Mata Atlântica. Tese de Doutorado, Universidade de São Paulo, Piracicaba.
- McCUNE, B. & MEFFORD M. J. 2011. PC-ORD: Multivariate Analysis of Ecological Data. version 6. MjM Software, Gleneden Beach, Oregon.
- MEIRELES, L. D.; SHEPHERD, G.J. & KINOSHITA, L.S. 2008 Variações na composição florística e na estrutura fitossociológica de uma floresta ombrófila densa alto-montana na Serra da Mantiqueira, Monte Verde, MG. Rev. Bras. Bot. 31(4):559-574.
- MEIRELES, L. D., KOCH, I. & SHEPHERD, G. J. 2010. Impacto de los cambios climáticos del Cuaternario Tardio en la distribición geográfica de espécies de arboles de los Bosques Montanos Atlanticos. In Anais do Congresso Latinoamericano de Botánica. La Serena.
- MELO, M.M.R.F., OLIVEIRA, R.J., ROSSI, L., MAMEDE, M.C.H. & CORDEIRO, I. 1998. Fitossociologia de trecho de Mata Atlântica na Planície do Rio Verde, Estação Ecológica de Juréia, Itatins, SP, Brasil. In Anais do IV Simpósio de Ecossistemas Brasileiros (S. Watanabe, coord.). ACIESP, São Paulo, v.2, p.49-56.
- MORENO, M.R., NASCIMENTO, M.T. & KURTZ, B.C. 2003. Estrutura e composição florística do estrato arbóreo em duas zonas altitudinais na mata atlântica de encosta da região do Imbé, RJ. Acta Bot. Bras. 17(3):371-386.
- MORI, S.A., MATTOS-SILVA, L.A., LISBOA, G. & CORADIN, L. 1989. Manual de manejo do herbário fanerogâmico. 2nd ed. CEPLAC, Ilhéus.
- MYERS, N., MITTERMEIER, R.A., MITTERMEIER, C.G., FONSECA, G.A.B. & KENT, J. 2000. Biodiversity hotspots for conservation priorities. Nature. 403:853-858. PMid:10706275. http://dx.doi.org/10.1038/35002501
- NÓBREGA, G.A., EISENLOHR, P.V., PACIÊNCIA, M.L.B., PRADO, J. & AIDAR, M.P.M. 2011. A composição florística e a diversidade de pteridófitas diferem entre a Floresta de Restinga e a Floresta Ombrófila Densa das Terras Baixas do Núcleo Picinguaba/PESM, Ubatuba/SP? Biota Neotrop. 11(2): http://www.biotaneotropica.org.br/v11n2/pt/fullpaper?bn02911022011+pt
- OLIVEIRA, V.C. 2011. Sobrevivência, morfo-anatomia, crescimento e assimilação de carbono de seis espécies arbóreas neotropicais submetidas à saturação hídrica do solo. Tese de Doutorado, Universidade Estadual de Campinas, Campinas.
- OLIVEIRA, V.C. & JOLY, C.A. 2010. Flooding tolerance of Calophyllum brasiliense Camb. (Clusiaceae): morphological, physiological and growth responses. Trees-Struct. Funct. 24:185-193. http://dx.doi.org/10.1007/s00468-009-0392-2
- OLIVEIRA FILHO, A.T. & FONTES, M.A. L. 2000 Patterns of floristic differentiation among Atlantic forests in Southeastern Brazil, and the influence of climate. Biotropica. 32(4b):793-810. http://dx.doi.org/10.1111/j.1744-7429.2000.tb00619.x
- PADGURSCHI, M.C.G. 2010. Composição e estrutura arbórea de um trecho de Floresta Ombrófila Densa Montana com taquaras na Mata Atlântica. Dissertação de Mestrado, Universidade Estadual de Campinas, Campinas.
- PADGURSCHI, M.C.G., PEREIRA, L.P., TAMASHIRO, J.Y. & JOLY, C.A. 2011. Composição e similaridade florística entre duas áreas de Floresta Atlântica Montana, São Paulo, Brasil. Biota Neotrop. 11(2): http://www.biotaneotropica.org.br/v11n2/pt/abstract?article+bn02811022011
- PEDRONI, F. 2001. Aspectos da estrutura e dinâmica da comunidade arbórea na Mata Atlântica de planície e encosta em Picinguaba, Ubatuba, SP. Tese de Doutorado, Universidade Estadual de Campinas, Campinas.
- PEIXOTO, A.L., PEREIRA-MOURA, M.V.L., SANTOS, I. 2002 . Monimiaceae de São Paulo. In Flora Fanerogânica do Estado de São Paulo (M.G.L. Wanderley, G. Shepherd & A.M. Giulietti, org.). Hucitec; FAPESP, São Paulo, v.2, p.189-207.
- PEREIRA, L.S. 2011. Composição e estrutura do componente arbóreo da Floresta Ombrófila Densa Montana do Núcleo Santa Virgínia/PESM, São Luiz do Paraitinga/SP. Dissertação de Mestrado, Universidade Estadual de Campinas, Campinas.
- PESSOA, S.V.A., GUEDES-BRUNI, R.R. & KURTZ, B.C. 1997. Composição florística e estrutura do componente arbustivo-arbóreo de um trecho secundário de floresta montana na Reserva Ecológica de Macaé de Cima. In Serra de Macaé de Cima: Diversidade Florística e Conservação em Mata Atlântica (H.C. Lima & R.R. Guedes-Bruni, eds.). Jardim Botânico do Rio de Janeiro, Rio de Janeiro. p.147-167.
- PHILLIPS, O.L. & BAKER, T. 2002. RAINFOR - Field manual for plot establishment and remeasurement. http://www.geog.leeds.ac.uk/projects/rainfor/ (último acesso em 05/2006).
- PHILLIPS, O.L., MALHI, Y., HIGUCHI, N., LAURANCE, W.F., NUNEZ, P.V., VASQUEZ, R.M., LAURANCE, S.G., FERREIRA, L.V., STERN, M., BROWN, S. & GRACE, J. 1998. Changes in the carbon balance of tropical forests: evidence from long-term plots. Science. 282:439-442. PMid:9774263. http://dx.doi.org/10.1126/science.282.5388.439
- PHILLIPS, O.L., MALHI, Y., VINCETI, B., BAKER, T., LEWIS, S.L., HIGUCHI, N., LAURANCE, W.F., VARGAS, P.N., MARTINEZ, R.V., LAURANCE, S., FERREIRA, L.V., STERN, M., BROWN, S. & GRACE, J. 2002. Changes in growth of tropical forests: evaluating potential biases. Ecol. Appl. 12:576-587. http://dx.doi.org/10.1890/1051-0761(2002)012[0576:CIGOTF]2.0.CO;2
- PONÇANO, W.L., CARNEIRO, C.D.R., BRITICHI, C.A., ALMEIDA, F.F.M. & PRANDINI, F.L. 1981. Mapa geomorfológico do Estado de São Paulo. Instituto de Pesquisas Tecnológicas, São Paulo, v.1.
- POORTER, L., BONGERS, F., STERCK, F.J. & WOLL, H. 2003. Architecture of 53 rain forest tree species differing in adult stature and shade tolerance. Ecology. 84:602-608. http://dx.doi.org/10.1890/0012-9658(2003)084[0602:AORFTS]2.0.CO;2
- POORTER, L., BONGERS, F., STERCK, F.J. & WOLL, H. 2005. Beyond the regeneration phase: differentiation of height-light trajectories among tropical tree species. J. Ecol. 93:256-267. http://dx.doi.org/10.1111/j.1365-2745.2004.00956.x
- PRATA, E.M.B. 2009. Composição florística, estrutura e distribuição espacial de espécies arbóreas numa área de Floresta Atlântica Ombrófila Densa, Ubatuba/SP. Dissertação de Mestrado, Universidade Estadual de São Paulo, Rio Claro.
- PRATA, E.M.B, ASSIS, M.A. & JOLY, C.A. 2011. Composição florística e estrutura da comunidade arbórea na transição da Floresta Ombrófila Densa das Terras Baixas-Floresta Ombrófila Densa Submontana do Núcleo Picinguaba/PESM, Ubatuba, sudeste do Brasil. Biota Neotrop. 11(2): http://www.biotaneotropica.org.br/v11n2/pt/abstract?inventory+bn02211022011
- RAMOS, E., TORRES, R.B., VEIGA, R.F.A. & JOLY, C.A. 2011. Estudo do componente arbóreo de trechos da Floresta Ombrófila Densa Submontana em Ubatuba (SP). Biota Neotrop. 11(2): http://www.biotaneotropica.org.br/v11n2/pt/abstract?inventory+bn02411022011
- RAMOS, E. 2009. Estudos Florísticos e Fitossociológicos em trecho da Mata Atlântica (Ubatuba, SP) como subsídio para a conservação de recursos fitogenéticos. Dissertação de Mestrado, Instituto Agronômico de Campinas, Campinas.
- RIBEIRO, K.T. & FREITAS, L. 2010. Impactos potenciais das alterações no Código Florestal sobre a vegetação de campos rupestres e campos de altitude. Biota Neotrop. 10(4): http://www.biotaneotropica.org.br/v10n4/en/abstract?article+bn04310042010
- RIBEIRO, M.C., METZGER, J.P., MARTENSEN, A.C., PONZONI, F.J. & HIROTA, M.M. 2009. The Brazilian Atlantic Forest: how much is left, and how is the remaining forest distributed? Implications for conservation. Biol. Conserv. 142:1141-1153. http://dx.doi.org/10.1016/j.biocon.2009.02.021
- ROCHELLE, A.L.C. 2008. Heterogeneidade ambiental, diversidade e estrutura da comunidade arbórea de um trecho de Floresta Ombrófila Densa Atlântica. Dissertação de Mestrado, Universidade Estadual de Campinas, Campinas.
- ROCHELLE, A.L.C., CIELO-FILHO, R. & MARTINS, F.R. 2011. Florística e estrutura da comunidade arbórea de um trecho de Floresta Ombrófila Densa Atlântica Submontana no Parque Estadual da Serra do Mar, em Ubatuba/SP, Brasil. Biota Neotrop. 11(2): http://www.biotaneotropica.org.br/v11n2/pt/abstract?inventory+bn02711022011
- RODRIGUES, R.R. 2003. Diversidade, dinâmica e conservação em florestas do Estado de São Paulo: 40 ha de parcelas permanentes. Relatório Científico II. Projeto Temático - Programa BIOTA/FAPESP. http://www.lerf.esaq.usp.br (último acesso em 05/2011).
- ROSADO, B.H.P., OLIVEIRA, R.S., JOLY, C.A., AIDAR, M.P.M. & BURGESS, S.S.O. 2012. Diversity in nighttime transpiration behavior of woody species of the Atlantic Rain Forest, Brazil. Agr. Forest. Meteorol. 158:13-20. http://dx.doi.org/10.1016/j.agrformet.2012.02.002
- SALEMI, L.F. 2009. Balanço de água e de nitrogênio em uma microbacia coberta por pastagem no litoral norte do Estado de São Paulo. 2009. Dissertação de Mestrado, Universidade de São Paulo, Piracicaba.
- SALIS, S.M., SHEPHERD, G.J. & JOLY, C.A. 1995. Floristic comparison between mesophytic forests of the interior of the state of São Paulo, S.E. Brazil. Vegetatio. 119:155-164. http://dx.doi.org/10.1007/BF00045595
- SANDERS, N.J., LESSARD, J.P., FITZPATRICK, M.C. and DUNN, R.R. 2007. Temperature, but not productivity or geometry, predicts elevational diversity gradients in ants across spatial grains. Global Ecol. Biogeogr. 16: 640-649. http://dx.doi.org/10.1111/j.1466-8238.2007.00316.x
- SANMARTIN, I. & RONQUIST, F. 2004. Southern hemisphere biogeography inferred by event-based models: plant versus animal patterns. Syst. Biol. 53:216-243. PMid:15205050. http://dx.doi.org/10.1080/10635150490423430
- SANTOS, F.A.M., PEDRONI, F., ALVES, L.F. & SANCHEZ, M. 1998. Structure and dynamics of tree species of the Atlantic forest. An. Acad. Bras. Cienc. 70:874-880.
- SANTOS, N.D., COSTA, D.P., KINOSHITA, L.S. & SHEPHERD. G.J. 2011. Aspectos brioflorísticos e fitogeográficos de duas formações costeiras de Floresta Atlântica da Serra do Mar, Ubatuba/SP, Brasil. Biota Neotrop. 11(2): http://www.biotaneotropica.org.br/v11n2/pt/fullpaper?bn03011022011+pt
- SCARANELLO, M.A.S., ALVES, L.F., VIEIRA, S.A., CAMARGO, P.B., JOLY, C.A. & MARTINELLI, L.A. 2012. Height-diameter relationships of tropical Atlantic moist forest trees in southeastern. Sci. Agric. 69(1):26-37. http://dx.doi.org/10.1590/S0103-90162012000100005
- SCARANO F.R. 2009. Plant communities at the periphery of the Atlantic rain forest: rare-species bias and its risks for conservation. Biol. Conserv. 142:1201-1208. http://dx.doi.org/10.1016/j.biocon.2009.02.027
- SCHAEFFER-NOVELLI, Y. 2000. Manguezal, os dispositivos legais como instrumento da conservação. In Simpósio de Ecossistemas Brasileiros: Conservação e Duna. ACIESP, São Paulo, p.10-17.
- SCUDELLER, V.V., MARTINS, F.R. & SHEPHERD, G.J. 2001. Distribution and abundance of arboreal species in the Atlantic ombrophilous dense forest in Southeastern Brazil. Plant Ecol. 152:185-199. http://dx.doi.org/10.1023/A:1011494228661
- SESNIE, S.E., FINEGAN, B., GESSLER, P.E. and RAMOS, Z. 2009 Landscape-Scale Environmental and Floristic Variation in Costa Rican Old-Growth Rain Forest Remnants. Biotropica. 41(1):16-26. http://dx.doi.org/10.1111/j.1744-7429.2008.00451.x
- SETZER, J. 1966. Atlas climatológico do estado de São Paulo. Comissão Interestadual da Bacia do Paraná-Paraguai; CESP, São Paulo.
- SHEIL, D. 1995. A critique of permanent plot methods and analysis with examples from Budongo Forest, Uganda. Forest Ecol. Manag. 77:11-34. http://dx.doi.org/10.1016/0378-1127(95)03583-V
- SILVA, A.F. & LEITÃO FILHO, H.F. 1982. Composição forística e estrutura de um trecho de Mata Atlântica de encosta no município de Ubatuba (São Paulo - Brasil). Rev. Bras. Bot. 5:43-52.
- SILVA, E.D. & TOZZI, A.M.G.A. 2011. Leguminosae na Floresta Ombrófila Densa do Núcleo Picinguaba, Parque Estadual da Serra do Mar, São Paulo, Brasil. Biota Neotrop. 11(4): http://www.biotaneotropica.org.br/v11n4/pt/abstract?inventory+bn03111042011
- SIQUEIRA, M.F. 1994. Classificação da vegetação e ordenação de espécies arbóreas da Mata Atlântica. Dissertação de Mestrado, Universidade Estadual de Campinas, Campinas.
- SOUZA, V.C. & LORENZI, H. 2008. Botânica sistemática: guia ilustrado para identificação das famílias de Angiospermas da flora brasileira, baseado em APG II. 2nd ed. Instituto Plantarum, Nova Odessa.
- STEGEN, J.C., SWENSON, N.G., ENQUIST, B.J., WHITE, E.P., PHILLIPS, O.L., JØRGENSEN, P.M., WEISER, M.D., MENDOZA, A.M. & VARGAS, P.N. 2011 Variation in above-ground forest biomass across broad climatic gradients. Global Ecol. Biogeogr. 20(5):744-754. http://dx.doi.org/10.1111/j.1466-8238.2010.00645.x
- SVENNING, J-C., BORCHSENIUS, F., BJORHOLM, S. & BALSLEV, H. 2008 High tropical net diversification drives the New World latitudinal gradient in palm (Arecaceae) species richness. J. Biogeogr. 35:394-406. http://dx.doi.org/10.1111/j.1365-2699.2007.01841.x
- TABARELLI, M. & MANTOVANI, W. 1999. A riqueza de espécies arbóreas na floresta de encosta no estado de São Paulo, Brasil. Rev. Bras. Bot. 22(2):217-233.
- TABARELLI, M., PINTO, L.P., SILVA, J.M.C., HIROTA, M.M., BEDÊ, L.C. 2005. Desafios e oportunidades para a conservação da biodiversidade na Mata Atlântica brasileira. Megadiversidade. 1(1):132-138.
- TANNER, E.V.J., VITOUSEK, P.M. & CUEVAS, E. 1998. Experimental investigation of nutrient limitation of forest growth on wet tropical mountains. Ecology 79:10-22. http://dx.doi.org/10.1890/0012-9658(1998)079[0010:EIONLO]2.0.CO;2
- THOMAZ, L.D. & MONTEIRO, R. 1997. Composição florística da Mata Atlântica de encosta da Estação Biológica de Santa Lúcia, município de Santa Teresa-ES. Bol. Mus. Biol. Mello Leitao, Nov. Ser. 7:3-48.
- TORRES, R.B., MARTINS, F.R. & KINOSHITA, L.S. 1997. Climate, soil and tree flora relationships in forests in the state of São Paulo, southestern Brazil. Rev. Bras. Bot. 20(1):41-49.
- VELOSO, H.P., RANGEL-FILHO, A.L.R. & LIMA, J.C.A. 1991. Classificação da Vegetação Brasileira, Adaptada a um Sistema Universal. IBGE, Rio de Janeiro.
- VICTOR, M.A.M. 1977. A Devastação Florestal. UNIPRESS, Sociedade Brasileira de Silvicultura, São Paulo.
- VIEIRA, S.A., ALVES, L.F., AIDAR, M.P.M., ARAÚJO, L.S., BAKER, T., BATISTA, J.L.F., CAMPOS, M.C.R., CAMARGO, P.B., CHAVE, J., DELITTI, W.B., HIGUCHI, N., HONÓRIO, E., JOLY, C.A., KELLER, M., MARTINELLI, L.A., DE MATTOS, E.A., METZKER, T., PHILLIPS, O., SANTOS, F.A.M., SHIMABUKURO, M.T., SILVEIRA, M. & TRUMBORE, S.E. 2008. Estimativas de biomassa e estoque de carbono: o caso da Mata Atlântica. Biota Neotrop. 8(2): http://www.biotaneotropica.org.br/v8n2/pt/abstract?point-of-view+bn00108022008
- VIEIRA, S.A., ALVES, L.F., DUARTE-NETO, P.J., MARTINS, S.C., VEIGA, L.G., SCARANELLO, M.A., PICOLLO, M.C., CAMARGO, P.B., CARMO, J.B., SOUSA NETO, E., SANTOS, F.A.M., JOLY, C.A. & MARTINELLI, L.A. 2011. Stocks of carbon and nitrogen and partitioning between above- and belowground pools in the Brazilian coastal Atlantic Forest elevation range. Ecol. Evol. 1(3):421-434. PMid:2239351. PMCid:3287305. http://dx.doi.org/10.1002/ece3.41
- WANG, G., ZHOU, G., YANG, L. & LI, Z. 2002 Distribution, species diversity and life-form spectra of plant communities along an altitudinal gradient in the northern slopes of Qilianshan Mountains, Gansu, China. Plant Ecology; 165:169-181. http://dx.doi.org/10.1023/A:1022236115186
- WILDI, O. 2010. Data analysis in vegetation ecology. Wiley-Blackwell, Chichester. http://dx.doi.org/10.1002/9780470664971
- ZAR, J.H. 1999. Biostatistical analysis. 4nd ed. Prentice Hall, Upper Saddle River.
- ZHAO, C.M., CHEN, W.L., TIAN, Z.Q. & XIE, Z.Q. 2005. Altitudinal pattern of plant species diversity in Shennongjia Mountains, Central China. J. Integr. Plant Biol. 47:1431-1449. http://dx.doi.org/10.1111/j.1744-7909.2005.00164.x
Datas de Publicação
-
Publicação nesta coleção
24 Jul 2012 -
Data do Fascículo
Mar 2012
Histórico
-
Recebido
20 Dez 2010 -
Aceito
15 Mar 2012 -
Revisado
10 Jan 2012