Resumos
OBJETIVO: Este estudo teve como objetivo averiguar a atividade enzimática da N-acetil-β-D-glicosaminidase (NAG) como possível biomarcador precoce de disfunção renal para a exposição ocupacional ao chumbo inorgânico. MATERIAIS E MÉTODOS: Foi selecionado um grupo de 30 pessoas do sexo masculino expostas ao chumbo inorgânico em uma fábrica de baterias localizada no estado do Paraná. Fizeram parte do grupo os funcionários que mostraram valores de chumbo sanguíneo inferiores a 40 mg/dl. O grupo controle foi representado por 15 adultos saudáveis com similaridade em relação à idade e ao gênero do grupo exposto. Foram determinados os níveis de plumbemia, do ácido d-aminolevulínico urinário e a atividade da NAG urinária. RESULTADOS E DISCUSSÃO: Foi evidenciado que a atividade urinária da NAG foi significativamente maior (p < 0,05; teste U de Mann-Whitney) no grupo exposto ao chumbo inorgânico quando comparado ao grupo controle, e houve uma correlação negativa com significância (p < 0,05; correlação de Spearman Rank Order) entre o indicador biológico de exposição plúmbica e a atividade urinária da NAG. CONCLUSÃO: Os resultados demonstraram que o aumento da atividade urinária da NAG pode ser utilizado como um biomarcador precoce da exposição ao chumbo inorgânico.
Chumbo; N-acetil-β-D-glicosaminidase; Biomarcador; Saúde ocupacional; Urina
OBJECTIVE: This study aimed to verify the enzymatic activity of N-acetyl-β-D-glucosaminidase (NAG) as a possible early biomarker of renal dysfunction due to occupational exposure to inorganic lead. MATERIALS AND METHODS: We selected a group of 30 males that had been exposed to inorganic lead in a battery factory in the state of Paraná. This group comprised those employees whose blood lead levels were below 40 mg/dl. The control group consisted of 15 healthy adults of similar age and gender compared with the exposed group. Blood lead concentrations, d-aminolevulinic acid levels and urinary NAG activity were measured. RESULTS AND DISCUSSION: It was shown that urinary NAG activity was significantly higher (p < 0.05, U test of Mann-Whitney) in the exposed group in comparison to the control group, and there was a significant negative correlation (p < 0.05, Spearman Rank Order correlation) between the biological indicator of lead exposure and urinary NAG activity. CONCLUSION: The results showed that the increase of urinary NAG activity may be used as an early biomarker of the exposure to inorganic lead.
Lead; N-acetyl-β-D-glucosaminidase; Biomarker; Occupational health; Urine
ARTIGO ORIGINAL ORIGINAL ARTICLE
N-acetil-β-D-glicosaminidase como biomarcador precoce de disfunção renal para a exposição ocupacional ao chumbo inorgânico
N-acetyl- β -D-glucosaminidase as an early biomarker of renal dysfunction due to occupational exposure to inorganic lead
Leandro Nishikawa GonçalesI; Mônica Maria Bastos PaolielloII; Vanderly JaneiroIII; Miguel Machinski JuniorIV
IMestrando do Curso de Pós-Graduação em Análises Clínicas da Universidade Estadual de Maringá (UEM)
IIProfessora associada da disciplina de Toxicologia da Universidade Estadual de Londrina (UEL)
IIIProfessor assistente do Departamento de Estatística da UEM
IVProfessor associado da disciplina de Toxicologia do Departamento de Análises Clínicas da UEM
Endereço para correspondência Endereço para correspondência: Miguel Machinski Junior Departamento de Análises Clínicas da UEM Av. Colombo, 5.790 CEP 87020-900 Maringá-PR Tel.: (44) 3261-4489 e-mail: mmjunior@uem.br
RESUMO
OBJETIVO: Este estudo teve como objetivo averiguar a atividade enzimática da N-acetil-β-D-glicosaminidase (NAG) como possível biomarcador precoce de disfunção renal para a exposição ocupacional ao chumbo inorgânico.
MATERIAIS E MÉTODOS: Foi selecionado um grupo de 30 pessoas do sexo masculino expostas ao chumbo inorgânico em uma fábrica de baterias localizada no estado do Paraná. Fizeram parte do grupo os funcionários que mostraram valores de chumbo sanguíneo inferiores a 40 mg/dl. O grupo controle foi representado por 15 adultos saudáveis com similaridade em relação à idade e ao gênero do grupo exposto. Foram determinados os níveis de plumbemia, do ácido d-aminolevulínico urinário e a atividade da NAG urinária.
RESULTADOS E DISCUSSÃO: Foi evidenciado que a atividade urinária da NAG foi significativamente maior (p < 0,05; teste U de Mann-Whitney) no grupo exposto ao chumbo inorgânico quando comparado ao grupo controle, e houve uma correlação negativa com significância (p < 0,05; correlação de Spearman Rank Order) entre o indicador biológico de exposição plúmbica e a atividade urinária da NAG.
CONCLUSÃO: Os resultados demonstraram que o aumento da atividade urinária da NAG pode ser utilizado como um biomarcador precoce da exposição ao chumbo inorgânico.
Unitermos: Chumbo, N-acetil-β-D-glicosaminidase, Biomarcador, Saúde ocupacional, Urina
ABSTRACT
OBJECTIVE: This study aimed to verify the enzymatic activity of N-acetyl-β-D-glucosaminidase (NAG) as a possible early biomarker of renal dysfunction due to occupational exposure to inorganic lead.
MATERIALS AND METHODS: We selected a group of 30 males that had been exposed to inorganic lead in a battery factory in the state of Paraná. This group comprised those employees whose blood lead levels were below 40 mg/dl. The control group consisted of 15 healthy adults of similar age and gender compared with the exposed group. Blood lead concentrations, d-aminolevulinic acid levels and urinary NAG activity were measured.
RESULTS AND DISCUSSION: It was shown that urinary NAG activity was significantly higher (p < 0.05, U test of Mann-Whitney) in the exposed group in comparison to the control group, and there was a significant negative correlation (p < 0.05, Spearman Rank Order correlation) between the biological indicator of lead exposure and urinary NAG activity.
CONCLUSION: The results showed that the increase of urinary NAG activity may be used as an early biomarker of the exposure to inorganic lead.
Key words: Lead, N-acetyl-β-D-glucosaminidase, Biomarker, Occupational health, Urine
Introdução
Os perigos da exposição ocupacional ao chumbo são bastante documentados graças ao controle dos efeitos tóxicos agudos do chumbo inorgânico em trabalhadores expostos. Devido a esse controle, grande atenção tem sido direcionada às desordens crônicas ou subclínicas atribuídas a tais exposições. Entre esses efeitos crônicos têm-se visto historicamente a hipertensão e as disfunções renais como as patogêneses mais importantes. No entanto, as conseqüências fisiológicas são inúmeras, com efeitos neurológicos, hematológicos, gastrointestinais, cardiovasculares, endócrinos e carcinogênicos(3, 4, 16, 21).
Várias evidências denotam que altos níveis de exposição ao chumbo podem ocasionar falência renal crônica. Com a exposição excessiva e prolongada ao chumbo a doença renal é progressiva e irreversível. A nefropatia por chumbo é caracterizada por redução gradual da função renal e freqüentemente acompanhada por hipertensão. Os efeitos tóxicos do chumbo sobre os rins se dividem principalmente em disfunção tubular renal reversível e nefropatia tubular irreversível. A disfunção reversível ocorre, na maior parte das vezes, em crianças sob exposição aguda e algumas vezes em trabalhadores expostos. As características da nefropatia aguda incluem corpos de inclusão nuclear, alterações fisiológicas na mitocôndria e citomegalia das células epiteliais dos túbulos proximais. A nefropatia irreversível, um efeito direto da exposição crônica ao chumbo sobre os rins, é caracterizada por esclerose vascular, atrofia ou hiperplasia da célula tubular, fibrose intersticial progressiva, nenhum ou poucos corpos de inclusão e esclerose glomerular. A forma crônica é descrita principalmente em trabalhadores expostos, cuja exposição primária se dá por inalação(15-17).
O rim, por ser um órgão compensatório, não mostra mudanças na proteinúria, uréia ou creatinina sérica, mesmo com 50% de perda da capacidade funcional. As alterações dos valores de uréia sangüínea e creatinina sérica ocorrem com a perda de dois terços da função renal. Devido à relativa insensibilidade dos testes clínicos tradicionais de avaliação da função renal para a detecção de injúria precoce ou função renal alterada, há um considerável interesse sobre potenciais biomarcadores de efeito precoce de injúria renal por exposição ao chumbo(3, 12, 16, 19).
A N-acetil-β-D-glicosaminidase (NAG) ι uma enzima hidrolítica localizada nos lisossomos das células dos túbulos proximais do sistema renal que possui a função auxiliar na degradação de glicoproteínas(18). Essas proteínas são degradadas, nessas organelas, em aminoácidos, que são levados, via membrana basolateral, para a circulação sangüínea. Baixos níveis da NAG são normalmente encontrados na urina como resultado das atividades de exocitose e pinocitose das células epiteliais tubulares(19). Danos nos túbulos renais aumentam os níveis da NAG na urina no estágio precoce das lesões e durante a evolução da quebra estrutural das células tubulares, o que resulta em necrose celular. Por conseguinte, uma alta atividade urinária da NAG pode causar suspeita da presença de doença renal ou dano tóxico. Por isso tem-se sugerido que a quantificação da atividade da NAG urinária serve como parâmetro no diagnóstico de danos renais(9).
Na exposição de trabalhadores ao chumbo inorgânico, a NAG parece ser um marcador precoce de nefrotoxicidade, no entanto as relações dose-efeito ainda não estão bem estabelecidas, e tampouco o significado e os mecanismos do aumento da atividade da NAG urinária neste tipo de exposição(2). Portanto a avaliação nas mudanças da atividade urinária da NAG pode refletir alterações bioquímicas e estruturais nas células tubulares renais. Assim, o objetivo deste estudo foi averiguar a atividade enzimática da NAG como possível biomarcador precoce de disfunção renal para a exposição ocupacional ao chumbo inorgânico, sendo esta atividade enzimática relacionada com a plumbemia e o ácido δ-aminolevulínico (ALA-U) na urina, biomarcadores de exposição e efeito ao chumbo, respectivamente.
Material e métodos
População
Foi selecionado um grupo de 30 pessoas do sexo masculino expostas ao chumbo numa fábrica de baterias localizada no estado do Paraná. O critério de seleção foi baseado no resultado da análise de chumbo sangüíneo (PbS) previamente obtido desses trabalhadores. Fizeram parte do grupo aqueles que mostraram níveis de chumbo sangüíneo < 40 µg/dl, faixa considerada de normalidade de acordo com o valor de referência adotado pela Norma Regulamentadora nº 7 do Programa de Controle Médico de Saúde Ocupacional do Ministério do Trabalho(1). A decisão pelo nível de exposição apresentado foi fundamentada na necessidade de avaliar a atividade da NAG como biomarcador precoce de dano renal.
O grupo controle foi representado por 15 adultos saudáveis com similaridade em relação à idade e ao gênero do grupo exposto. A composição do grupo se firmou com a apresentação voluntária dos participantes e a aplicação de um questionário individual. Foram considerados aptos os indivíduos masculinos entre 20 e 55 anos de idade, sem histórico de nefropatias, hipertensão e diabetes ou qualquer atividade associada à exposição ao chumbo. Todos os participantes assinaram um termo de consentimento livre e esclarecido. Este estudo foi aprovado pelo Comitê Permanente de Ética em Pesquisa Envolvendo Seres Humanos (COPEP) da Universidade Estadual de Maringá (UEM). O protocolo foi apreciado de acordo com a Resolução nº 196/96, sob o registro nº 0039.0.093.000-05.
Amostras
As amostras de urina colhidas matutinamente nos laboratórios de toxicologia da Universidade Estadual de Londrina (UEL) e da UEM foram fracionadas para os ensaios de atividade da NAG, a análise de creatinina e a determinação do ALA-U. Para a determinação da atividade da NAG, 3 ml da amostra foram centrifugados, sendo o sobrenadante fracionado e estocado em frasco de polietileno por no máximo 30 dias a -20ºC. Outra porção de 3 ml foi separada para a análise de creatinina, realizada logo após a coleta. O restante da amostra foi acidificado com ácido clorídrico 6 N até atingir o pH 2-3 e refrigerado por no máximo dois dias para a determinação do ALA-U.
Para a determinação da plumbemia (PbS) foram colhidos 10 ml de sangue total heparinizado em seringa BD de 10 ml. A amostra foi estocada na própria seringa a -20ºC até o momento da análise, realizada num intervalo máximo de 15 dias após a coleta.
Determinação da atividade da N-acetil- β -D-glicosaminidase na urina
A determinação da NAG urinária foi baseada no método descrito por Maruhn(13). A amostra contendo a NAG foi adicionada a uma solução contendo p-nitrofenil-N-acetil-β-D-glicosaminida (Acros® 10 mmol/l) dissolvido em solução tampão citrato de sódio 0,2 mol/l (pH 4,4). A mistura resultante foi incubada a 37ºC por 15 minutos para que ocorresse a hidrólise enzimática do substrato com liberação do íon p-nitrofenilato. A ação enzimática foi interrompida com a adição de solução tampão de Kolthoff 0,5 mol/l (pH 10,25). O produto da reação foi medido em espectrofotômetro Shimadzu® (UV-1601PC), em 405 nm, sendo a absorbância proporcional à atividade urinária da NAG após correção com a urina sem substrato.
O cálculo da atividade urinária de NAG foi obtido conforme descrito por Horak et al.(10):
A atividade da NAG também é apresentada como U/g de creatinina. Para isso a atividade urinária da NAG expressa em U/l foi dividida pelo teor de creatinina urinária (g/l) obtida de cada indivíduo.
A precisão intradia da atividade urinária da NAG foi obtida por meio de um pool de urinas normais. Esta determinação ocorreu em todos os ensaios de análise da NAG dos grupos exposto e controle. A atividade obtida foi de 2,56 ± 0,1 U/l com um coeficiente de variação de 3,9%.
Determinação de chumbo no sangue
A determinação de PbS foi realizada segundo Hessel(8). Após hemólise da amostra de sangue com Triton X-100 (Merck®), o chumbo foi complexado com pirrolidinaditiocarbamato de amônio (Sigma®) e o complexo foi extraído em metil-isobutilcetona (Merck®). O conteúdo de chumbo na fase orgânica foi determinado por espectrofotometria de absorção atômica em 283,3 nm, usando-se a chama de ar acetileno. Validação intralaboratorial: a) linearidade 6 a 160 µg/dl; b) limite de detecção 1 µg/dl; c) limite de quantificação 6 µg/dl; d) precisão 5 %; e) recuperação 94% a 120%.
Determinação de ácido δ -aminolevulínico na urina
O ALA-U foi determinado de acordo com Tomokumi e Ogata(23). A determinação quantitativa foi baseada na condensação do ácido δ-aminolevulínico com acetoacetato de etila, produzindo o composto 2-metil-3-carbetoxi-4-(ácido-3-propiônico) pirrol. Este composto ALA-pirrol, após extração com acetato de etila, complexou-se com reativo de Ehrlich modificado, resultando num composto colorido determinado por espectrofotometria em 553 nm (Shimadzu®-UV-1601PC). Validação intralaboratorial: a) linearidade 1 a 30 mg/l; b) limite de detecção 0,1 mg/l; c) limite de quantificação 1 mg/l; d) precisão 9,8 %; e) recuperação 93% a 117%.
Determinação de creatinina na urina
A quantificação de creatinina urinária foi realizada usando-se o teste da Labtest®. A creatinina forma um complexo com a solução de picrato em meio alcalino, segundo a reação de Jaffé, que foi medido fotometricamente em 540 nm (colorímetro Siel® 300).
Métodos estatísticos
Para os cálculos estatísticos foi utilizado o programa Statistic Analysis System (SAS Institute, Cary, NC, USA), versão 6.0. As diferenças estatísticas entre os grupos foram avaliadas com aplicação do teste U de Mann-Whitney. Para a obtenção da relação entre as variáveis foi utilizada a correlação de Spearman Rank Order. Os testes que obtiveram p < 0,05 foram considerados significativos.
Resultados
A exposição ocupacional ao chumbo inorgânico pode ser avaliada por indicadores biológicos. O indicador de dose interna mais utilizado é a determinação de chumbo no sangue (PbS). O indicador de efeito do chumbo no organismo, por sua vez, é a determinação de ALA-U, que representa a ação inibitória do chumbo sobre a enzima ALA-desidratase.
A análise comparativa dos indicadores biológicos de dose interna e de efeito da exposição ao chumbo na população estudada está representada na Tabela 1. Nesta foi constatado que o indicador biológico de dose interna (PbS) difere significativamente entre o grupo exposto e o grupo-controle, e não houve diferença quando se comparou o biomarcador de efeito (ALA-U) relacionado com a biossíntese da heme.
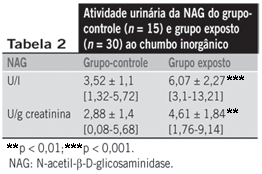
Ao se avaliar a atividade urinária da NAG (Tabela 2). é possível observar que o grupo exposto ao chumbo inorgânico apresentou, significativamente, uma atividade de excreção urinária maior desta enzima quando em comparação com o grupo-controle. Esta significância foi obtida tanto na atividade da NAG em unidades de atividade enzimática por litro de urina (U/l), quanto após a correção pela creatinina (U/g creatinina).
A faixa referencial da atividade urinária da NAG foi obtida após análise da população-controle. Com cobertura de 95%, estimou-se que o intervalo referencial da NAG em U/l foi de 1,32-5,72 e que a atividade da NAG em U/g de creatinina foi de 0,08-5,68, conforme demonstra a Tabela 2. Este intervalo está em conformidade com os propostos por Horak et al.(10), 0,4-5,6 U/g de creatinina, e Whiting et al.(24), 0,2-5,8 U/g de creatinina, com a utilização da mesma metodologia analítica.
Pelo coeficiente de correlação entre a atividade urinária da NAG e o biomarcador de dose interna no referente estudo, observou-se correlação negativa com significância, conforme mostra a Tabela 3.
A Figura 1 demonstra que, no grupo exposto ao Pb, 33% apresentaram aumento da atividade da NAG (U/g creatinina) quando em comparação com o valor de referência estudado por Horak et al.(10). Entre o grupo controle, uma atividade da NAG maior que o índice referencial foi observada em apenas dois (13%) participantes.
Discussão
Nos túbulos proximais renais, a degradação protéica lisossomal é realizada por hidrolases como as cisteína-protein ases e a N-acetil-β-D-glicosaminidase, que auxiliam na degradaη ão de glicoproteínas(18). A NAG é uma enzima que, por ser encontrada em altas concentrações nos túbulos renais, ser estável na urina e não comumente influenciável por variações pré-renais, pode ser utilizada como marcador diagnóstico e prognóstico de disfunção tubular renal(7, 11, 19, 20).
Neste estudo, os níveis de atividade urinária da NAG num grupo de indivíduos expostos ao chumbo inorgânico (menos de 40 µg/dl de plumbemia) foram avaliados e comparados com os níveis de um grupo-controle não-exposto ao metal. As dosagens da NAG foram comparadas entre os grupos e correlacionadas com os indicadores biológicos de efeito (ALA-U) e de dose interna (PbS). Os resultados mostraram que no grupo exposto os níveis de PbS foram significativamente maiores quando em comparação com o controle, demonstrando o caráter expositivo deste grupo. No entanto não houve diferença no indicador ALA-U entre os grupos controle e exposto (Tabela 1). Esta não-constatação de efeito sobre a biossíntese do grupo heme pela determinação de ALA-U pode ser justificada pelos baixos teores de plumbemia da população exposta (24,05 ± 10,45 µg/dl).
A avaliação da atividade urinária da NAG foi significativamente maior no grupo exposto ao chumbo quando em comparação com o controle. Portanto, no grupo exposto ao chumbo, em níveis de PbS considerados normais, pode haver lesões dos túbulos renais e, conseqüentemente, um efeito tóxico sobre o sistema renal, com evidência de nefrotoxicidade subclínica (Tabela 2). Mortada et al.(15), ao avaliarem policiais de trânsito expostos ao chumbo, demonstraram um aumento urinário de NAG e albumina, ratificando os danos nos túbulos e glomérulos, respectivamente. Meyer et al.(14) e Sonmez et al.(22) relataram um aumento na atividade urinária da NAG na exposição ocupacional ao chumbo. Gerhardsson et al.(6), contrariamente, ao avaliarem os efeitos renais do chumbo em trabalhadores com longa exposição, não encontraram significância na excreção urinária da NAG ou outros marcadores de função renal entre os grupos exposto e não-exposto. Em Gennart et al.(5), a avaliação de um grupo exposto com PbS acima de 40 µg/dl também não evidenciou diferença significativa da NAG quando em comparação com um grupo controle nem correlação com os indicadores biológicos PbS e ALA-U. De acordo com Chia et al.(2), a falta de correlação entre a atividade urinária da NAG e os vários indicadores de exposição ao chumbo decorre do fato de que estes não refletem uma sobrecarga renal por chumbo. Além disso, o aumento na atividade urinária da NAG pode não ser devido ao acúmulo crônico deste metal nos túbulos. Estes mesmos autores sugeriram ainda que a atividade urinária aumentada da NAG seja uma resposta aguda ao aumento repentino de chumbo sobre o sistema renal. Isto pode explicar a incoerência de resultados e justificar o aumento da atividade urinária da NAG quando trabalhadores são novamente expostos ao metal.
No presente estudo foi encontrada baixa correlação negativa entre o biomarcador PbS e a atividade urinária da NAG (Tabela 3), expressa em (U/l). Este aumento da NAG poderia ser justificado pela exposição contínua dos participantes ao chumbo. Não houve correlação entre o PbS e a atividade da NAG quando corrigida pela creatinina (Tabela 3). A correlação também não foi obtida entre o biomarcador de efeito (ALA-U) e a atividade da NAG (Tabela 3). Portanto o aumento da atividade urinária da NAG parece ocorrer somente quando há sobrecarga de chumbo sobre o sistema renal, o que parece acarretar uma lesão tubular, não apresentando progressão de aumento com os biomarcadores de efeito e de dose interna.
Ao se avaliar a porcentagem de participantes com aumento da atividade da NAG entre os grupos exposto e controle, constatou-se que, no grupo exposto, 33% de seus integrantes demonstraram aumento da atividade da NAG. No grupo-controle, apenas dois indivíduos (13%) apresentaram este aumento da atividade da NAG quando em comparação com os limites referenciais obtidos neste estudo (Figura 1) e nos de Horak et al.(10). Este dado demonstrou maior porcentagem de indivíduos com aumento da NAG e possível lesão tubular entre os participantes do grupo exposto ao chumbo inorgânico.
Conclusão
Com os resultados obtidos conclui-se que o aumento da atividade urinária da NAG e o possível efeito subclínico da exposição a baixos níveis de chumbo (< 40 µg/dl) podem ser evidenciados antes da alteração dos níveis de ALA-U, o biomarcador de efeito de escolha na exposição a este metal. Isto sugere que o aumento da atividade urinária da NAG poderia ser utilizado como um biomarcador precoce de disfunção renal na exposição plúmbica.
Agradecimentos
À Fundação Araucária, chamada nº 07/2004, protocolo 7576, pelo auxílio financeiro.
Primeira submissão em 10/05/07
Última submissão em 10/05/07
Aceito para publicação em 04/09/08
Publicado em 20/08/08
-
1BRASIL. Ministério do Trabalho. Programa de Controle Médico de Saúde Ocupacional, 1996. Disponível em: <http://www.mte.gov.br>. Acesso em: 19 nov. 2004.
- 2. CHIA, K. S. et al Urinary N-acetyl-beta-D-glucosaminidase activity in workers exposed to inorganic lead. Occup Environ Med, v. 51, p. 125-9, 1994.
- 3. EHRLICH, R. et al Lead absorption and renal dysfunction in a South African battery factory. Occup Environ Med, v. 55, p. 453-60, 1998.
- 4. EL-SAFTY, A. M. et al Effects of smoking and lead exposure on proximal tubular integrity among Egyptian industrial workers. Arch Med Res, v. 35, n. 1, p. 59-65, 2004.
- 5. GENNART, J. P. et al Assessment of thyoid, tests, kidney and autonomic nervous system function in lead-exposed workers. Int Arch Occup Environ Health, v. 64, n. 1, p. 49-57, 1992.
- 6. GERHARDSSON, L. et al Kidney effects in long term exposed lead esmelter workers. Br J Ind Med, v. 49, p. 186-92, 1992.
- 7. GUDER, W. G.; HOFMANN, W. Markers for the diagnosis and monitoring of renal tubular lesions. Clin Nephrol, v. 38, p. 3-7, 1992.
- 8. HESSEL, D. W. A simple and rapid quantitative determination of lead in blood. At Absorpt Newsl, v. 7, p. 55-6, 1968.
- 9. HOFMANN, W. Diagnostic strategies for the exclusion and differentiation of proteinuria, leukocyturia and hematuria. Wien Klin Wochenschr, v. 103, p. 16-20, 1991.
- 10. HORAK, E.; HOPFER, S. M.; SUNDERMAN Jr, F. W. Spectrophotometric assay for urinary N-acetyl-β-D-glucosaminidase activity. Clin Chem, v. 27, p. 1180-5, 1981.
- 11. ITOH, Y. et al Varied value of urinary N-acetyl-β-D-glucosaminidase isoenzyme B in males of reproductive age. Kidney Int, v. 46, p. 38-42, 1994.
- 12. LANDRIGAN, P. J. Lead in the modern workplace. Am J Publ Health, v. 80, n. 8, p. 907-8, 1990.
- 13. MARUHN, D. Rapid colorimetric assay of β-galactosidase and N-acetyl-β-glucosaminidase in human urine. Clin Chim Acta, v. 73, n. 3, p. 453-61, 1976.
- 14. MEYER, R. B. et al Increased urinary enzime excretion in workers exposed to nephrotoxic chemicals. Am J Ind Med, v. 76, p. 989-98, 1984.
- 15. MORATADA, W. I. et al Study of lead exposure from automobile exhaust as a risk for nephrotoxicity among traffic policemen. Am J Nephrol, v. 21, p. 274-9, 2001.
- 16. MOREIRA, F. R.; MOREIRA, J. C. A cinética do chumbo no organismo humano e sua importância para a saúde. Ciênc Saúde Colet, v. 9, n. 1, p. 167-81, 2004.
- 17. NOLAN, C. V.; SHAIKH, Z. A. Lead nephrotoxicity and associated disorders: biochemical mechanisms. Toxicology, v. 73, n. 2, p. 127-46, 1992.
- 18. OLBRICHT, C. J. Distribution of cathepsins B and L in the kidney and their role in tubular protein absorption. Eur J Clin Chem Clin Biochem, v. 30, p. 675-81, 1992.
- 19. PRINCE, R. G . The role of NAG (N-acetyl-β-D-glucosaminidase) in the diagnosis of kidney disease including the monitoring of nephrotoxicity. Clin Nephrol, v. 38, p. 14-9, 1992.
- 20. SCHAEFER, L. et al Urinary excretion of cathepsin B and cystatins as parameters of tubular damage. Kidney Int, v. 46, p. 64-7, 1994.
- 21. SILBERGELD, E. K. Facilitative mechanisms of lead as a carcinogen. Mut Res, v. 533, p. 121-33, 2003.
- 22. SONMEZ, F. et al Lead exposure and urinary N-acetyl-β-D-glucosaminidase activity in adolescent workers in auto repair workshops. J Adolesc Health, v. 30, n. 3, p. 213-6, 2002.
- 23. TOMOKUNI, K.; OGATA, M. Simple method for determination of urinary δ-aminolevulinic acid as index of lead exposure. Clin Chem, v. 18, p. 1534-6, 1972.
- 24. WHITING, P. H. et al Patterns of N-acetyl-β-glucosaminidase excretion after renal transpl antation. Clin Chim Acta, v. 108, n. 1, p. 1-7, 1980.
Datas de Publicação
-
Publicação nesta coleção
30 Jan 2009 -
Data do Fascículo
Ago 2008
Histórico
-
Aceito
04 Set 2008 -
Revisado
10 Maio 2007 -
Recebido
10 Maio 2007