Resumo
A história natural do hematoma intramural (HI) e da úlcera penetrante (UP) é muito variável, já que podem progredir para a formação de aneurisma, ruptura, dissecção, e podem até mesmo regredir, no caso específico do HI. Exames de imagem têm crescente papel no manejo clínico e operatório da UP e do HI. Ao contrário das projeções semelhantes a úlcera, achados de lagos sanguíneos não são relatados nos estudos tomográficos de pacientes com HI. O entendimento das características da imagem e do curso natural de cada uma dessas entidades ajudará clínicos e cirurgiões a identificar os pacientes com maior risco para um mau prognóstico e pode melhorar os desfechos. A fisiopatologia dessas entidades, as controvérsias no que se refere a suas histórias naturais e os fatores prognósticos das imagens tomográficas são discutidos neste artigo.
Palavras-chave:
síndrome aórtica aguda; hematoma intramural da aorta; hematoma aórtico; úlcera penetrante da aorta
Abstract
The natural histories of intramural hematoma (IMH) and penetrating atherosclerotic ulcer (PAU) are highly variable as they may progress to aneurysm formation, rupture, or dissection, or even resolve, in the specific case of IMH. Imaging plays an increasingly important role in clinical and surgical management of IMH and PAU. In contrast to ulcer-like projections, images of intramural blood pools have not been widely reported in CT studies of patients with IMH. Understanding the imaging characteristics and the natural course of each of these entities would help clinicians and surgeons to identify patients at greatest risk for bad prognosis and may improve outcomes. This paper discusses the pathophysiology of these entities, the controversies regarding their natural history, and the prognostic factors that should be identified in CT scans.
Keywords:
acute aortic syndrome; intramural aortic hematoma; aortic hematoma; penetrating ulcers of aorta
INTRODUÇÃO
O hematoma intramural (HI) e a úlcera penetrante (UP) da aorta são considerados, pela maioria das publicações, como variantes da dissecção clássica dentro da denominação genérica de síndrome aórtica aguda. Nessas três condições clínicas, a classificação de Stanford é utilizada para orientar o tratamento11 Daily PO, Trueblood HW, Stinson EB, Wuerflein RD, Shumway NE. Management of acute aortic dissections. Ann Thorac Surg. 1970;10(3):237-47. http://dx.doi.org/10.1016/S0003-4975(10)65594-4. PMid:5458238.
http://dx.doi.org/10.1016/S0003-4975(10)...
. Entretanto, a fisiopatologia e a história natural do HI e da UP são motivo de muitas dúvidas e não guardam relação com a dissecção clássica em muitos aspectos.
O HI é definido como hematoma da parede aórtica sem evidência de ruptura médio-intimal de entrada. Por outro lado, em muitos casos, pequenas rupturas da íntima podem ser evidenciadas durante procedimentos abertos ou pelos modernos métodos de imagem de alta resolução. A ruptura dos vasa vasorum (VV) como causa do HI é motivo de debate, e várias evidências sugerem que essa ruptura constitui fenômeno secundário e não a causa primordial do HI22 Sundt TM. Intramural hematoma and penetrating atherosclerotic ulcer of the aorta. Ann Thorac Surg. 2007;83(2):835-4. http://dx.doi.org/10.1016/j.athoracsur.2006.11.019. PMid:17257937.
http://dx.doi.org/10.1016/j.athoracsur.2...
.
A UP é definida como a erosão da íntima e da membrana elástica interna, com subsequente penetração do sangue na túnica média a partir de placas ateroscleróticas. As séries clínicas da literatura incluem um número restrito de pacientes com UP e HI, e a história natural dessas patologias é motivo de muito debate22 Sundt TM. Intramural hematoma and penetrating atherosclerotic ulcer of the aorta. Ann Thorac Surg. 2007;83(2):835-4. http://dx.doi.org/10.1016/j.athoracsur.2006.11.019. PMid:17257937.
http://dx.doi.org/10.1016/j.athoracsur.2...
.
Ambas as entidades ocorrem em pacientes mais idosos do que aqueles com dissecção clássica, o que tem implicações na apresentação clínica e radiológica inicial e na história natural dessas lesões da parede aórtica.
ALTERAÇÕES DA PAREDE AÓRTICA EM IDOSOS
Para um melhor entendimento da apresentação clínica e radiológica da UP, do HI e da dissecção clássica, precisamos levar em consideração as alterações estruturais que ocorrem na aorta com o envelhecimento. Em comparação à dissecção clássica, a UP e o HI ocorrem em pacientes mais idosos e, portanto, com alterações parietais distintas. Com o envelhecimento, aparecem espaços entre as lamelas elásticas, devido à perda das finas fibras elásticas que as unem, e se identifica fibrose da túnica média. Essas alterações resultam em espessamento e aumento da rigidez da parede, que se agravam com a hipertensão arterial e o aparecimento de calcificações.
A elastina é sintetizada pelas células musculares lisas (CML), que por sua vez são escassas nas grandes artérias elásticas e diminuem em número com a idade. Além da apoptose de um número considerável das CML, estas se afastam uma das outras e modificam seu fenótipo para um estado de senescência. A perda da elasticidade da aorta resulta em rigidez, dilatação, alongamento e tortuosidade33 Davidson JM, Hill KE, Alford JL. Developmental changes in collagen and elastin biosynthesis in the porcine aorta. Dev Biol. 1986;118(1):103-11. http://dx.doi.org/10.1016/0012-1606(86)90077-1. PMid:3770292.
http://dx.doi.org/10.1016/0012-1606(86)9...
4 Selmin O, Volpin D, Bressan GM. Changes of cellular expression of mRNA for tropoelastin in the intraembryonic arterial vessels of developing chick revealed by in situ hybridization. Matrix. 1991;11(5):347-58. http://dx.doi.org/10.1016/S0934-8832(11)80206-4. PMid:1811165.
http://dx.doi.org/10.1016/S0934-8832(11)...
-55 Wang M, Zhang J, Jiang LQ, et al. Proinflammatory profile within the grossly normal aged human aortic wall. Hypertension. 2007;50(1):219-27. http://dx.doi.org/10.1161/HYPERTENSIONAHA.107.089409. PMid:17452499.
http://dx.doi.org/10.1161/HYPERTENSIONAH...
.
A correlação entre a síntese da tropoelastina pelas CML e os níveis de mRNA também é modificada. A expressão da tropoelastina na parede diminui a cada década de vida após os 60 anos, o que representa uma redução de 94% do potencial elastogênico regenerativo, quando extrapolada para os 40 anos66 Bruce MC, Honaker CE. Transcriptional regulation of tropoelastin expression in rat lung fibroblasts: Changes with age and hyperoxia. Am J Physiol. 1998;274(6):L940-50. PMid:9609733.
7 Heinz A, Jung MC, Duca L, et al. Degradation of tropoelastin by matrix metalloproteinases – cleavage site specificities and release of matrikines. FEBS J. 2010;277(8):1939-56. http://dx.doi.org/10.1111/j.1742-4658.2010.07616.x. PMid:20345904.
http://dx.doi.org/10.1111/j.1742-4658.20...
-88 Fritze O, Romero B, Schleicher M, et al. Age-Related changes in the elastic tissue of the human aorta. J Vasc Res. 2012;49(1):77-86. http://dx.doi.org/10.1159/000331278. PMid:22105095.
http://dx.doi.org/10.1159/000331278...
.
Essas alterações histológicas ligadas ao envelhecimento são observadas com maior intensidade no terço externo da túnica e são consideradas como fundamentais no mecanismo fisiopatológico da dissecção aórtica e do HI99 Schlatmann TJM, Becker AE. Histologic changes in the normal aging aorta: implications for dissecting aortic aneurysm. Am J Cardiol. 1977;39(1):13-20. http://dx.doi.org/10.1016/S0002-9149(77)80004-0. PMid:831420.
http://dx.doi.org/10.1016/S0002-9149(77)...
,1010 Schlatmann TJM, Becker AE. Pathogenesis of dissecting aneurysm of aorta: comparative histopathologic study of significance of medial changes. Am J Cardiol. 1977;39(1):21-6. http://dx.doi.org/10.1016/S0002-9149(77)80005-2. PMid:831424.
http://dx.doi.org/10.1016/S0002-9149(77)...
.
HEMATOMA INTRAMURAL E O PAPEL DOS VASA VASORUM
Os VV adventiciais estão presentes nos grandes vasos elásticos com mais de 29 lamelas, e por essa razão estão em maior número na aorta ascendente, no arco aórtico e na aorta descendente, e em pequeno número na aorta abdominal.
A relação entre ruptura de VV e HI foi estabelecida pela primeira vez em 1920 por Krukenberg1111 Krukenberg E. Beitrage zur frage des aneurysma dissecans. Beitr Pathol Anat Allg Pathol. 1920;67:329-51. e, desde então, é aceita como possível causa do HI. O HI sem UP tende a ser mais extenso, às vezes comprometendo aorta ascendente, arco aórtico e aorta descendente. A maioria das publicações aceita essa relação de causa e efeito entre ruptura dos VV e HI, mas as evidências nesse sentido são escassas. Parece difícil explicar que esses pequenos vasos, com baixa pressão intraluminal, possam dissecar grandes porções da aorta e, muitas vezes, levar à ruptura da parede arterial. Esse mecanismo também não explica por que, no HI secundário à UP, o hematoma tende a ser mais restrito apesar de haver comunicação direta entre a luz e a túnica média. Por outro lado, a frequência detectada de ruptura da íntima em pacientes com HI do tipo A (aorta ascendente) submetidos a cirurgia e nos quais a tomografia não demonstrava qualquer defeito no pré-operatório foi de 73% no estudo de Park et al.1212 Park KH, Lim C, Choi JH, et al. Prevalence of aortic intimal defect in surgically treated acute type A intramural hematoma. Ann Thorac Surg. 2008;86(5):1494-500. http://dx.doi.org/10.1016/j.athoracsur.2008.06.061. PMid:19049737.
http://dx.doi.org/10.1016/j.athoracsur.2...
.
Em outras palavras, grande parte dos HI classificados como do tipo A pela tomografia eram na verdade casos de dissecção com pequeno orifício de entrada que havia selado espontaneamente. Talvez essas pequenas rupturas íntimo-mediais sejam ainda mais frequentes, porque, nos casos de ruptura distal com extensão retrógrada do hematoma para o arco aórtico e a aorta ascendente, essas lesões são também classificadas erroneamente como do tipo A de Stanford. Não é surpresa, portanto, que durante a cirurgia não sejam identificadas rupturas intimais (Figura 1).
Angiotomografia mostrando hematoma intramural (HI) comprometendo a aorta ascendente (A) em paciente de 78 anos com dor torácica aguda. Em (B) se identifica local de dissecção distal próxima à origem do tronco celíaco. Em (C) se observa a reabsorção completa do HI na aorta ascendente após 30 dias do implante de endoprótese na aorta descendente e sem compressão da luz verdadeira distalmente (D). Esse caso demonstra por que alguns HI classificados como tipo A de Stanford são na verdade HI originados na aorta descendente com progressão retrógrada do hematoma.
Os exames de tomografia de alta resolução mais recentes têm demonstrado com crescente frequência pequenas lesões intimais e lesões secundárias semelhantes a úlcera (ulcer like projections) ou lagos sanguíneos intramurais (intramural blood pools) nos exames seriados de acompanhamento dos HI, que muitas vezes são interpretados de maneira equivocada.
A hipertensão crônica é condição presente na maioria dos pacientes e se associa à oclusão dos VV com neovascularização, maior rigidez arterial e aterosclerose acelerada. Na crise hipertensiva, a isquemia da média pode se agravar devido à vasoconstrição dos VV. As porções mais internas da média permanecem nutridas por difusão a partir da luz arterial. Esse conjunto de fatores resulta em duas regiões com características distintas na túnica média: uma porção interna mais elástica e outra externa mais rígida. Devido às diferenças no módulo elástico das duas regiões, uma diferença na força de cisalhamento ocorre nessa interface1313 Heistad DD, Marcus ML, Law EG, Armstrong ML, Ehrhardt JC, Abboud FM. Regulation of blood flow to the aortic media in dogs. J Clin Invest. 1978;62(1):133-40. http://dx.doi.org/10.1172/JCI109097. PMid:659626.
http://dx.doi.org/10.1172/JCI109097...
14 Marcus ML, Heistad DD, Armstrong ML, Abboud FM. Effects of chronic hypertension on vasa vasorum in the thoracic aorta. Cardiovasc Res. 1985;19(12):777-81. http://dx.doi.org/10.1093/cvr/19.12.777. PMid:4084935.
http://dx.doi.org/10.1093/cvr/19.12.777...
15 Ohhira A, Ohhashi T. Effects of aortic pressure and vasoactive agents on the vascular resistance of the vasa vasorum in canine isolated thoracic aorta. J Physiol. 1992;453(1):233-45. http://dx.doi.org/10.1113/jphysiol.1992.sp019226. PMid:1464829.
http://dx.doi.org/10.1113/jphysiol.1992....
16 Larson EW, Edwards WD. Risk factors for aortic dissection: a necropsy study of 161 cases. Am J Cardiol. 1984;53(6):849-55. http://dx.doi.org/10.1016/0002-9149(84)90418-1. PMid:6702637.
http://dx.doi.org/10.1016/0002-9149(84)9...
17 Roberts WC. Aortic dissection: anatomy, consequences and causes. Am Heart J. 1981;101(2):195-214. http://dx.doi.org/10.1016/0002-8703(81)90666-9. PMid:7008565.
http://dx.doi.org/10.1016/0002-8703(81)9...
18 Olivetti G, Melissari M, Marchetti G, Anversa P. Quantitative structural changes of the rat thoracic aorta in early spontaneous hypertension. Tissue composition, and hypertrophy and hyperplasia of smooth muscle cells. Circ Res. 1982;51(1):19-26. http://dx.doi.org/10.1161/01.RES.51.1.19. PMid:6211295.
http://dx.doi.org/10.1161/01.RES.51.1.19...
-1919 Pereira AH. Rupture of vasa vasorum and intramural hematoma of the aorta: A changing paradigma. J Vasc Bras. 2010;9(2):57-60. http://dx.doi.org/10.1590/S1677-54492010000200008.
http://dx.doi.org/10.1590/S1677-54492010...
. No caso da dissecção clássica, a tendência é a compressão da luz verdadeira, pois a porção externa é mais rígida. Essa alteração no módulo elástico também poderia explicar por que a falsa luz (menos elástica e mais delgada) se expande ao longo do tempo.
Essas alterações das características elástico-mecânicas foram demonstradas experimentalmente em modelo animal pela ressecção da adventícia para exclusão dos VV e ligadura de intercostais (de onde os VV se originam na aorta descendente), provocando isquemia das porções mais externas da túnica média2020 Stefanadis C, Vlachopoulos C, Karayannacos P, et al. Effect of vasa vasorum flow on structure and function of the aorta in experimental animals. Circulation. 1995;91(10):2669-78. http://dx.doi.org/10.1161/01.CIR.91.10.2669. PMid:7743631.
http://dx.doi.org/10.1161/01.CIR.91.10.2...
,2121 Angouras D, Sokolis DP, Dosios T, et al. Effect of impaired vasa vasorum flow on the structure and mechanics of the thoracic aorta: implications for the pathogenesis of aortic dissection. Eur J Cardiothorac Surg. 2000;17(4):468-73. http://dx.doi.org/10.1016/S1010-7940(00)00382-1. PMid:10773572.
http://dx.doi.org/10.1016/S1010-7940(00)...
. Após 2 semanas, se observou degradação das fibras elásticas das porções mais externas da túnica média e, em alguns animais, observou-se uma dissecção espontânea. Esse experimento foi replicado em nosso meio com dados adicionais após 4 e 8 semanas2222 Fagundes A, Pereira AH, Corrêa RK, Oliveira MT, Rodriguez R. Effects of removal of the adventitia of the descending aorta and structural alterations in the tunica media in pigs. Rev Col Bras Cir. 2012;39(2):133-8. http://dx.doi.org/10.1590/S0100-69912012000200009. PMid:22664520.
http://dx.doi.org/10.1590/S0100-69912012...
. Nesse estudo, ficou demonstrado que, ao longo das semanas, a isquemia da parede arterial levou ao aumento da extensão da degeneração da túnica média, envolvendo agora as porções mais internas. Portanto, quando há isquemia avançada da parede arterial, a maior parte da túnica média evolui para fibrose. Uma interpretação desses achados é de que a oclusão progressiva dos VV com a idade, agravada pela hipertensão e pela aterosclerose associadas, pode levar à degeneração difusa da túnica média. Nesses casos, quando ocorre a ruptura da íntima, o plano de clivagem passa a ser mais externo (junto à adventícia) e o hematoma da parede tende a não comprimir a luz verdadeira. Isso poderia explicar em parte por que, em muitos HI, apesar de se identificar ruptura da íntima e grande hematoma ao longo da aorta, não se observa, na maioria dos casos, compressão significativa da luz verdadeira ou oclusão de ramos viscerais. Esses achados também poderiam explicar por que, em se tratando da UP, o hematoma mural, que aparece em muitos casos, é limitado: a túnica média degenerada e com fibrose extensa não permite que o hematoma se propague.
Recentemente, Osada et al. estudaram as alterações histopatológicas em pacientes com dissecção aórtica e confirmaram a presença de degeneração e oclusão dos VV, associada com degradação das fibras elásticas e acúmulo de matriz extracelular no terço externo da túnica média onde se desenvolveu a dissecção2323 Osada H, Kyogoku M, Matsuo T, Kanemitsu N. Histopathological evaluation of aortic dissection: A comparison of congenital versus acquired aortic wall weakness. Interact Cardiovasc Thorac Surg. 2018;27(2):277-83. http://dx.doi.org/10.1093/icvts/ivy046. PMid:29514205.
http://dx.doi.org/10.1093/icvts/ivy046...
.
Ao contrário do que muitos pensam, a compressão da luz verdadeira não pode ser explicada apenas por diferenças pressóricas, pois estudos experimentais demonstram que não se observa maior pressão sistólica ou pressão de pulso na falsa luz. É claro que outros fatores, como o tamanho da ruptura da íntima e a presença ou não de amplos orifícios de reentrada com grande fluxo retrógrado, têm papel importante na compressão da luz verdadeira2424 Tsai TT, Schlicht MS, Khanafer K, et al. Tear size and location impacts false lumen pressure in an ex vivo model of chronic type B aortic dissection. J Vasc Surg. 2008;47(4):844-51. http://dx.doi.org/10.1016/j.jvs.2007.11.059. PMid:18381145.
http://dx.doi.org/10.1016/j.jvs.2007.11....
25 Khanafer K, Berguer R. Fluid-structure interaction analysis of Turbulent pulsatile flow within a layered aortic wall as related to aortic dissection. J Biomech. 2009;42(16):2642-8. http://dx.doi.org/10.1016/j.jbiomech.2009.08.010. PMid:19765711.
http://dx.doi.org/10.1016/j.jbiomech.200...
-2626 Rudenick PA, Segers P, Pineda V, et al. Lumen Flow Patterns and their Relation with Morphological and Biomechanical Characteristics of Chronic Aortic Dissections. Computational Model Compared with Magnetic Resonance Imaging Measurements. PLoS One. 2017;12(1):e0170888. http://dx.doi.org/10.1371/journal.pone.0170888. PMid:28125720.
http://dx.doi.org/10.1371/journal.pone.0...
.
No caso específico do HI, já se demonstrou experimentalmente que o pico de estresse na túnica média (peak wall stress) é muito maior do que o observado na artéria sem hematoma, o que pode explicar a evolução para ruptura em direção à luz ou dissecção franca2727 Bukač M, Alber M. Multi-component model of intramural hematoma. J Biomech. 2017;50:42-9. http://dx.doi.org/10.1016/j.jbiomech.2016.11.040. PMid:27876369.
http://dx.doi.org/10.1016/j.jbiomech.201...
.
SIGNIFICADO FISIOPATOLÓGICO DAS PROJEÇÕES SEMELHANTES A ÚLCERA E LAGOS SANGUÍNEOS NO HI
No caso de uma dissecção com pequena ruptura íntimo-medial e sem reentrada distal para a luz verdadeira, o HI assim formado pode ser seguido do selamento do orifício de entrada. O aspecto radiológico seria então de HI sem entrada detectável. Nesse caso, a túnica média fica submetida a um estresse muito elevado, conforme já foi demonstrado experimentalmente2727 Bukač M, Alber M. Multi-component model of intramural hematoma. J Biomech. 2017;50:42-9. http://dx.doi.org/10.1016/j.jbiomech.2016.11.040. PMid:27876369.
http://dx.doi.org/10.1016/j.jbiomech.201...
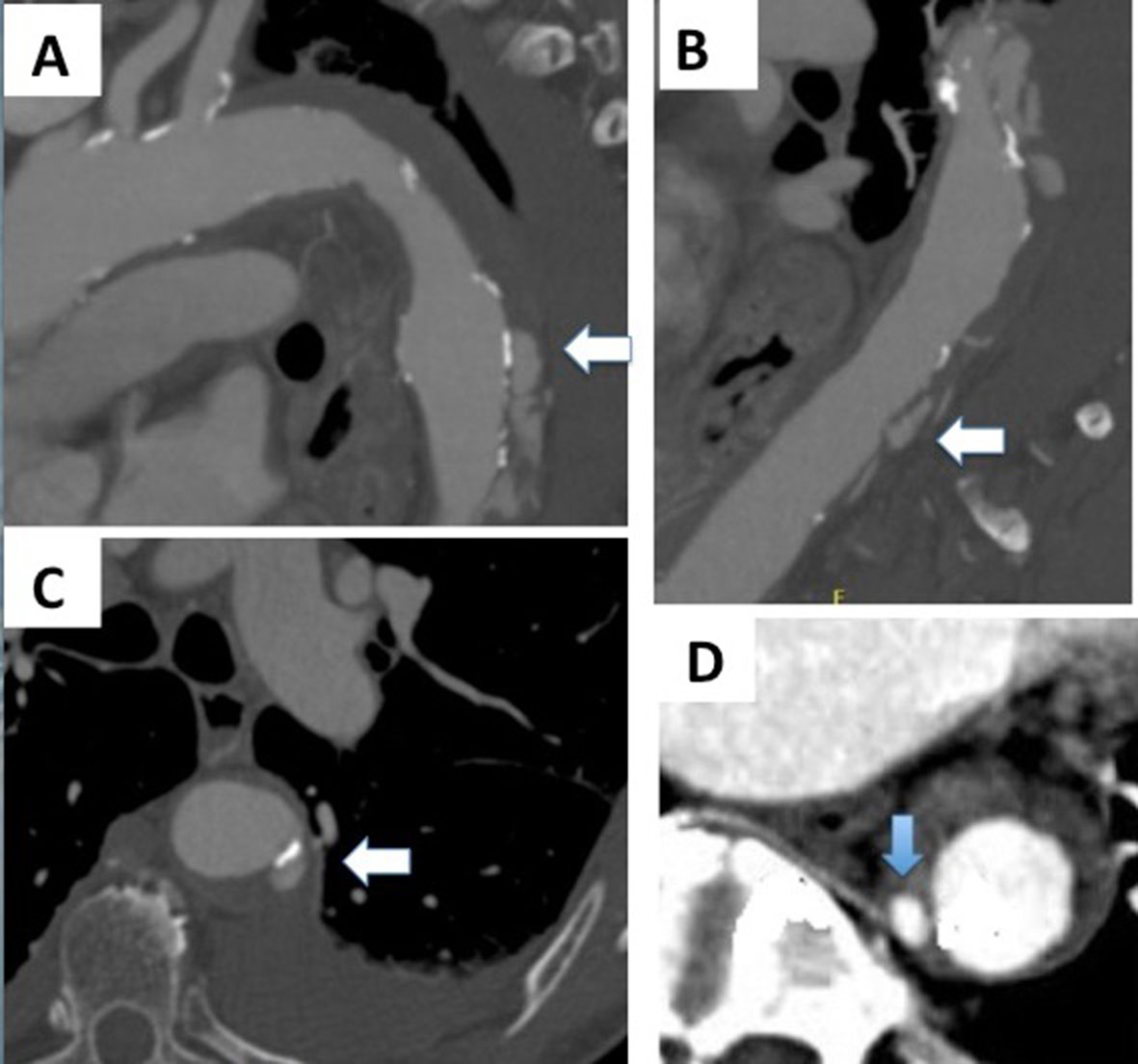
. Como o HI se estabelece nas porções mais externas da média, pode evoluir para desinserção da origem das intercostais e fluxo retrógrado para a parede, gerando os lagos sanguíneos detectados na face externa do hematoma. Os lagos sanguíneos podem ainda ser originados por pequenas rupturas intimais que aparecem agora na face interna do hematoma. As outras possibilidades são: reabsorção completa do hematoma, ruptura em direção à luz (gerando as projeções semelhantes a úlcera) ou dissecção continuada, formação de pseudoaneurisma ou ruptura franca para a cavidade torácica (Figura 2).
Em (A) se observa uma projeção semelhante a úlcera. Em (B) se identificam lagos sanguíneos. Em (C) se observa nova projeção semelhante a úlcera com derrame pleural adjacente. Em (D) se observa a relação de um lago sanguíneo com uma artéria intercostal.
A análise seriada de pacientes com HI com imagens típicas de lagos sanguíneos e projeções semelhantes a úlcera demonstra que essas lesões têm histórias naturais completamente diferentes2828 Wu MT, Wang YC, Huang YL, et al. Intramural blood pools accompanying aortic intramural hematoma: CT appearance and natural course. Radiology. 2011;258(3):705-13. http://dx.doi.org/10.1148/radiol.10101270. PMid:21212368.
http://dx.doi.org/10.1148/radiol.1010127...
. A análise das tomografias seriadas desses pacientes com HI demonstra que os lagos sanguíneos presentes no início ou que apareciam ao longo do tempo não se associam a complicações na maioria dos casos. A regressão logística no estudo de Wu et al. apontou que os seguintes fatores estiveram relacionados a complicações: diâmetro aórtico maior do que 45 mm, localização na aorta ascendente e aparecimento de projeções semelhantes a úlcera2828 Wu MT, Wang YC, Huang YL, et al. Intramural blood pools accompanying aortic intramural hematoma: CT appearance and natural course. Radiology. 2011;258(3):705-13. http://dx.doi.org/10.1148/radiol.10101270. PMid:21212368.
http://dx.doi.org/10.1148/radiol.1010127...
.
No caso específico das projeções semelhantes a úlcera (ruptura para a íntima) que estavam presentes no início do quadro ou que apareciam no seguimento, o prognóstico é pior2929 Jang YM, Seo JB, Lee YK, et al. Newly developed ulcer-like projection (ULP) in aortic intramural haematoma on follow-up CT: is it different from the ULP seen on the initial CT? Clin Radiol. 2008;63(2):201-6. http://dx.doi.org/10.1016/j.crad.2007.07.020. PMid:18194697.
http://dx.doi.org/10.1016/j.crad.2007.07...
30 Lee CW, Kang JW, Lee HJ, Lim TH. MDCT evaluation of intimal defects in intramural hematoma of the aorta: initial findings and follow-up. Int J Cardiovasc Imaging. 2010;26(S2, Suppl 2):295-302. http://dx.doi.org/10.1007/s10554-010-9709-x. PMid:20878253.
http://dx.doi.org/10.1007/s10554-010-970...
-3131 Bosma MS, Quint LE, Williams DM, Patel HJ, Jiang Q, Myles JD. Ulcerlike projections developing in noncommunicating aortic dissections: CT findings and natural history. AJR. 2009;193(3):895-905. http://dx.doi.org/10.2214/AJR.08.2073. PMid:19696307.
http://dx.doi.org/10.2214/AJR.08.2073...
. A formação de pseudoaneurisma e a evolução para dissecção ou ruptura ocorrem em 31% a 70% dos casos e se manifestam com maior frequência na aorta ascendente.
Existe muita discussão em relação à descrição da história natural dessas lesões e à interpretação das imagens na tomografia, já que algumas publicações, como uma recente diretriz europeia e uma publicação do UpToDate de 2018, referem que o HI pode evoluir para UP ou não fazem diferenciação entre UP e projeções semelhantes a úlcera3232 Riambau V, Böckler D, Brunkwall J, Cao P, Chiesa R. Management of descending thoracic aorta diseases clinical practice guidelines of the European Society for Vascular Surgery (ESVS). Eur J Vasc Endovasc Surg. 2017;53(1):4-52.,3333 Manning W, Je Black JH. Overview of acute aortic dissection and other acute aortic syndromes. UpToDate. 2018.. Por definição, a UP, como já vimos, caracteriza-se pela erosão da íntima e da média a partir de uma placa de ateroma. Por outro lado, as projeções semelhantes a úlcera e os lagos sanguíneos aparecem no início ou na evolução do HI e são decorrentes da ruptura para a íntima, ocorrendo, portanto, no sentido oposto ao da UP. Além disso, cada uma dessas lesões tem significado clínico e evolução particulares.
ÚLCERA PENETRANTE
A UP de aorta foi inicialmente descrita por Shennan em 19343434 Shennan T. Dissecting aneurysms. London: Medical Research Council; 1934. (Special Report Series; no. 193).. Assim como o HI, a UP da aorta é considerada uma variante da dissecção clássica, mas também com apresentação e evolução clínica distintas.
As ulcerações na aorta torácica são relativamente frequentes na população idosa, particularmente após a sétima década de vida, mas a real prevalência ainda está para ser determinada (Figura 3). Assim como ocorre com os pacientes com HI da aorta, a maioria dos pacientes são hipertensos. Ulcerações profundas na parede aórtica podem desencadear sintomas semelhantes aos da dissecção clássica e podem se associar a um HI secundário (Figura 3). As ulcerações associadas ocorrem quase exclusivamente na aorta torácica descendente, são frequentemente múltiplas, e podem variar em tamanho e profundidade; o envolvimento da aorta abdominal é menos comum. A evolução para ruptura ou dissecção franca está associada a morbimortalidade elevada.
Paciente de 82 anos com múltiplas úlceras penetrantes em arco aórtico e aorta descendente, associadas a aneurisma da aorta abdominal. As medidas da profundidade ou do tamanho do colo das úlceras não são sinais seguros para a indicação de tratamento endovascular.
História natural
A história natural da UP de aorta não é bem conhecida, apesar de a UP representar um dos espectros da síndrome aórtica aguda3535 von Kodolitsch Y, Csosz SK, Koschyk DH, et al. Intramural hematoma of the aorta: predictors of progression to dissection and rupture. Circulation. 2003;107(8):1158-63. http://dx.doi.org/10.1161/01.CIR.0000052628.77047.EA. PMid:12615795.
http://dx.doi.org/10.1161/01.CIR.0000052...
,3636 Vilacosta I, Aragoncillo P, Cañadas V, San Román JA, Ferreirós J, Rodríguez E. Acute aortic syndrome: a new sight to an old conundrum. Heart. 2009;95(14):1130-9. PMid:19131440..
Como bem esclarece Ganaha et al.3737 Ganaha F, Miller DC, Sugimoto K, et al. The prognosis of Aortic Intramural Hematoma: The Prognosis of aortic Intramural hematoma with and without Penetrating Atherosclerotic ulcer: a clinical and radiologic analysis. Circulation. 2002;106(3):342-8. http://dx.doi.org/10.1161/01.CIR.0000022164.26075.5A. PMid:12119251.
http://dx.doi.org/10.1161/01.CIR.0000022...
, existe certa confusão na literatura quanto ao comportamento da UP. Observa-se um comportamento mais agressivo nos pacientes sintomáticos3838 Stanson AW, Kazmier FJ, Hollier LH, et al. Penetrating atherosclerotic ulcers of the thoracic aorta: natural history and clinicopathologic correlations. Ann Vasc Surg. 1986;1(1):15-23. http://dx.doi.org/10.1016/S0890-5096(06)60697-3. PMid:3504683.
http://dx.doi.org/10.1016/S0890-5096(06)...
,3939 Coady MA, Rizzo JA, Hammond GL, Pierce JG, Kopf GS, Elefteriades JA. Penetrating ulcer of the thoracic aorta: what is it? How do we recognize it? How do we manage it? J Vasc Surg. 1998;27(6):1006-16. http://dx.doi.org/10.1016/S0741-5214(98)70003-5. PMid:9652462.
http://dx.doi.org/10.1016/S0741-5214(98)...
, em contraste com um curso mais benigno nos pacientes oligossintomáticos e, principalmente, nos assintomáticos4040 Harris JA, Bis KG, Glover JL, Bendick PJ, Shetty A, Brown OW. Penetrating atherosclerotic ulcers of the aorta. J Vasc Surg. 1994;19(1):90-9. http://dx.doi.org/10.1016/S0741-5214(94)70124-5. PMid:8301743.
http://dx.doi.org/10.1016/S0741-5214(94)...
,4141 Quint LE, Williams DM, Francis IR, et al. Ulcer like lesions of the aorta: imaging features and natural history. Radiology. 2001;218(3):719-23. http://dx.doi.org/10.1148/radiology.218.3.r01mr24719. PMid:11230645.
http://dx.doi.org/10.1148/radiology.218....
. A dor torácica persistente ou recorrente, apesar do agressivo tratamento anti-hipertensivo, o aumento do derrame pleural e a presença de sintomas agudos são fatores prognósticos negativos, com maior risco de progressão para dissecção ou ruptura aórtica. Assim como ocorre no HI, as úlceras que ocorrem na aorta ascendente e na porção proximal da aorta descendente apresentam um maior número de complicações. As possíveis explicações para esse comportamento incluem uma maior agressão hemodinâmica na parede arterial nesses pontos e a preponderância da elastina sobre o colágeno na camada média da aorta proximal4242 Borst HG, Heinemann MK, Stone CD. Pathogenesis. In: Surgical treatment of aortic dissection. New York: Churchill Livingstone Inc; 1996. p. 47-54.. A UP é responsável por cerca de 2-7% dos casos de síndrome aórtica aguda, com progressão da doença tanto em pacientes sintomáticos quanto em assintomáticos, justificando a necessidade do controle seriado com exames de imagem4343 Nathan DP, Boonn W, Lai E, et al. Presentation, complications, and natural history of penetrating atherosclerotic ulcer disease. J Vasc Surg. 2012;55(1):10-5. http://dx.doi.org/10.1016/j.jvs.2011.08.005. PMid:22047830.
http://dx.doi.org/10.1016/j.jvs.2011.08....
,4444 Pauls S, Orend KH, Sunder-Plassmann L, et al. Endovascular repair of symptomatic penetrating atherosclerotic ulcer of the thoracic aorta. Eur J Vasc Endovasc Surg. 2007;34(1):66-73..
Nos pacientes sintomáticos, o tratamento aberto ou endovascular está justificado. Entretanto, em pacientes com UP assintomática, aparentemente o tratamento conservador parece ser mais apropriado, pois ainda não existem critérios bem definidos que justifiquem o tratamento intervencionista tanto no segmento torácico quanto no abdominal4343 Nathan DP, Boonn W, Lai E, et al. Presentation, complications, and natural history of penetrating atherosclerotic ulcer disease. J Vasc Surg. 2012;55(1):10-5. http://dx.doi.org/10.1016/j.jvs.2011.08.005. PMid:22047830.
http://dx.doi.org/10.1016/j.jvs.2011.08....
,4545 Georgiadis GS, Antoniou GA, Georgakarakos EI, et al. Surgical or endovascular therapy of abdominal penetrating aortic ulcers and their natural history: A systematic review. J Vasc Interv Radiol. 2013;24(10):1437-49. http://dx.doi.org/10.1016/j.jvir.2013.05.067. PMid:23932417.
http://dx.doi.org/10.1016/j.jvir.2013.05...
. Nesses pacientes, a extensão da penetração na túnica média e o tamanho do colo da lesão são critérios discutíveis para a indicação cirúrgica, como ficou demonstrado na maior série clínica da literatura4343 Nathan DP, Boonn W, Lai E, et al. Presentation, complications, and natural history of penetrating atherosclerotic ulcer disease. J Vasc Surg. 2012;55(1):10-5. http://dx.doi.org/10.1016/j.jvs.2011.08.005. PMid:22047830.
http://dx.doi.org/10.1016/j.jvs.2011.08....
. A indicação de cirurgia aberta ou endovascular em pacientes assintomáticos fica restrita aos casos com formação de evidente pseudoaneurisma.
Quadro clínico
A maioria das úlceras que ocorrem nos pacientes idosos e hipertensos não penetra profundamente a túnica média e não causa sintomas. Nesses pacientes, episódios de microembolização podem ocorrer e conduzir ao diagnóstico. Todavia, a indicação para o implante de endoprótese nessas situações é discutível, pois as ulcerações podem ocorrer em vários segmentos da aorta descendente e abdominal, o que implicaria na cobertura de grandes extensões da aorta toracoabdominal, com riscos evidentes.
Fisiopatologia
Na UP, a placa ateromatosa se estende profundamente na parede arterial, rompendo a membrana elástica interna e penetrando a camada média. Quando ocorre essa penetração, a camada média fica exposta ao fluxo arterial pulsátil, o que pode causar hemorragia e HI. Na série da Clínica Mayo, 80% dos casos de UP se acompanhavam de HI4646 Cho KR, Stanson AW, Potter DD, Cherry KJ, Schaff HV, Sundt TM 3rd. Penetrating atherosclerotic ulcer of the descending thoracic aorta and arch. J Thorac Cardiovasc Surg. 2004;127(5):1393-9. http://dx.doi.org/10.1016/j.jtcvs.2003.11.050. PMid:15115998.
http://dx.doi.org/10.1016/j.jtcvs.2003.1...
, mas séries mais recentes relatam uma frequência muito menor de HI associado. A pergunta que se impõe é se muitas dessas ulcerações não seriam na verdade projeções semelhantes a úlcera que apareceram na evolução de um HI e foram erroneamente referidas como UP.
Métodos de imagem
O diagnóstico da UP de aorta é estabelecido por critérios anatômicos no estudo tomográfico, evidenciado por uma área localizada de placa ateromatosa com ulceração focal e espessamento da parede aórtica. A descrição clássica na tomografia computadorizada é de uma imagem sacular preenchida por contraste que penetra a parede da aorta, circundada por um HI.
CONCLUSÕES
As publicações que tratam da fisiopatologia do HI e da UP são escassas na literatura, o que gera confusão na interpretação clínico-radiológica dessas lesões, de muitos aspectos da sua história natural e da sua real prevalência na população. Vários estudos experimentais nos têm ajudado a interpretar melhor os achados clínicos e radiológicos. A possibilidade de que se realizem estudos prospectivos em futuro próximo é remota e, portanto, o caminho a seguir é a criação de registros bem conduzidos, como o International Registry of Aortic Dissection (IRAD), que há duas décadas vem acumulando informações sobre a síndrome aórtica aguda4747 Hagan PG, Nienaber CA, Isselbacher EM, et al. The International Registry of Dissection (IRAD): New Insights into an old disease. JAMA. 2000;283(7):897-903. http://dx.doi.org/10.1001/jama.283.7.897. PMid:10685714.
http://dx.doi.org/10.1001/jama.283.7.897...
. É preciso reconhecer que não há padrões bem estabelecidos na descrição radiológica (reporting standards) e no acompanhamento a médio e longo prazo no que se refere ao HI e à UP. Essas deficiências precisam ser corrigidas por nossas sociedades de especialidade com registros específicos, para um melhor entendimento das alterações parietais da aorta responsáveis tanto pela gênese como pelo comportamento evolutivo da UP e do HI. Como dizia Jean Martin Charcot (1825-1893) em De l'éxpectation en médecine4848 Charcot JM. De l’éxpectation en médecine. Paris: Librairie de Germer; 1847.: “A doença é muito antiga e nada nela mudou. Somos nós que mudamos quando aprendemos a reconhecer o que antes não era percebido (Disease is very old and nothing about it has changed. It is we who change, as we learn to recognize what was formerly imperceptible).
-
Como citar: Pereira AH. Hematoma intramural e úlcera penetrante da aorta: incertezas e controvérsias. J Vasc Bras. 2019;18: e20180119. https://doi.org/10.1590/1677-5449.180119
-
Fonte de financiamento: Nenhuma.
-
O estudo foi realizado no Hospital de Clínicas de Porto Alegre (HCPA), Universidade Federal do Rio Grande do Sul (UFRGS), Porto Alegre, RS, Brasil.
REFERÊNCIAS
-
1Daily PO, Trueblood HW, Stinson EB, Wuerflein RD, Shumway NE. Management of acute aortic dissections. Ann Thorac Surg. 1970;10(3):237-47. http://dx.doi.org/10.1016/S0003-4975(10)65594-4 PMid:5458238.
» http://dx.doi.org/10.1016/S0003-4975(10)65594-4 -
2Sundt TM. Intramural hematoma and penetrating atherosclerotic ulcer of the aorta. Ann Thorac Surg. 2007;83(2):835-4. http://dx.doi.org/10.1016/j.athoracsur.2006.11.019 PMid:17257937.
» http://dx.doi.org/10.1016/j.athoracsur.2006.11.019 -
3Davidson JM, Hill KE, Alford JL. Developmental changes in collagen and elastin biosynthesis in the porcine aorta. Dev Biol. 1986;118(1):103-11. http://dx.doi.org/10.1016/0012-1606(86)90077-1 PMid:3770292.
» http://dx.doi.org/10.1016/0012-1606(86)90077-1 -
4Selmin O, Volpin D, Bressan GM. Changes of cellular expression of mRNA for tropoelastin in the intraembryonic arterial vessels of developing chick revealed by in situ hybridization. Matrix. 1991;11(5):347-58. http://dx.doi.org/10.1016/S0934-8832(11)80206-4 PMid:1811165.
» http://dx.doi.org/10.1016/S0934-8832(11)80206-4 -
5Wang M, Zhang J, Jiang LQ, et al. Proinflammatory profile within the grossly normal aged human aortic wall. Hypertension. 2007;50(1):219-27. http://dx.doi.org/10.1161/HYPERTENSIONAHA.107.089409 PMid:17452499.
» http://dx.doi.org/10.1161/HYPERTENSIONAHA.107.089409 -
6Bruce MC, Honaker CE. Transcriptional regulation of tropoelastin expression in rat lung fibroblasts: Changes with age and hyperoxia. Am J Physiol. 1998;274(6):L940-50. PMid:9609733.
-
7Heinz A, Jung MC, Duca L, et al. Degradation of tropoelastin by matrix metalloproteinases – cleavage site specificities and release of matrikines. FEBS J. 2010;277(8):1939-56. http://dx.doi.org/10.1111/j.1742-4658.2010.07616.x PMid:20345904.
» http://dx.doi.org/10.1111/j.1742-4658.2010.07616.x -
8Fritze O, Romero B, Schleicher M, et al. Age-Related changes in the elastic tissue of the human aorta. J Vasc Res. 2012;49(1):77-86. http://dx.doi.org/10.1159/000331278 PMid:22105095.
» http://dx.doi.org/10.1159/000331278 -
9Schlatmann TJM, Becker AE. Histologic changes in the normal aging aorta: implications for dissecting aortic aneurysm. Am J Cardiol. 1977;39(1):13-20. http://dx.doi.org/10.1016/S0002-9149(77)80004-0 PMid:831420.
» http://dx.doi.org/10.1016/S0002-9149(77)80004-0 -
10Schlatmann TJM, Becker AE. Pathogenesis of dissecting aneurysm of aorta: comparative histopathologic study of significance of medial changes. Am J Cardiol. 1977;39(1):21-6. http://dx.doi.org/10.1016/S0002-9149(77)80005-2 PMid:831424.
» http://dx.doi.org/10.1016/S0002-9149(77)80005-2 -
11Krukenberg E. Beitrage zur frage des aneurysma dissecans. Beitr Pathol Anat Allg Pathol. 1920;67:329-51.
-
12Park KH, Lim C, Choi JH, et al. Prevalence of aortic intimal defect in surgically treated acute type A intramural hematoma. Ann Thorac Surg. 2008;86(5):1494-500. http://dx.doi.org/10.1016/j.athoracsur.2008.06.061 PMid:19049737.
» http://dx.doi.org/10.1016/j.athoracsur.2008.06.061 -
13Heistad DD, Marcus ML, Law EG, Armstrong ML, Ehrhardt JC, Abboud FM. Regulation of blood flow to the aortic media in dogs. J Clin Invest. 1978;62(1):133-40. http://dx.doi.org/10.1172/JCI109097 PMid:659626.
» http://dx.doi.org/10.1172/JCI109097 -
14Marcus ML, Heistad DD, Armstrong ML, Abboud FM. Effects of chronic hypertension on vasa vasorum in the thoracic aorta. Cardiovasc Res. 1985;19(12):777-81. http://dx.doi.org/10.1093/cvr/19.12.777 PMid:4084935.
» http://dx.doi.org/10.1093/cvr/19.12.777 -
15Ohhira A, Ohhashi T. Effects of aortic pressure and vasoactive agents on the vascular resistance of the vasa vasorum in canine isolated thoracic aorta. J Physiol. 1992;453(1):233-45. http://dx.doi.org/10.1113/jphysiol.1992.sp019226 PMid:1464829.
» http://dx.doi.org/10.1113/jphysiol.1992.sp019226 -
16Larson EW, Edwards WD. Risk factors for aortic dissection: a necropsy study of 161 cases. Am J Cardiol. 1984;53(6):849-55. http://dx.doi.org/10.1016/0002-9149(84)90418-1 PMid:6702637.
» http://dx.doi.org/10.1016/0002-9149(84)90418-1 -
17Roberts WC. Aortic dissection: anatomy, consequences and causes. Am Heart J. 1981;101(2):195-214. http://dx.doi.org/10.1016/0002-8703(81)90666-9 PMid:7008565.
» http://dx.doi.org/10.1016/0002-8703(81)90666-9 -
18Olivetti G, Melissari M, Marchetti G, Anversa P. Quantitative structural changes of the rat thoracic aorta in early spontaneous hypertension. Tissue composition, and hypertrophy and hyperplasia of smooth muscle cells. Circ Res. 1982;51(1):19-26. http://dx.doi.org/10.1161/01.RES.51.1.19 PMid:6211295.
» http://dx.doi.org/10.1161/01.RES.51.1.19 -
19Pereira AH. Rupture of vasa vasorum and intramural hematoma of the aorta: A changing paradigma. J Vasc Bras. 2010;9(2):57-60. http://dx.doi.org/10.1590/S1677-54492010000200008
» http://dx.doi.org/10.1590/S1677-54492010000200008 -
20Stefanadis C, Vlachopoulos C, Karayannacos P, et al. Effect of vasa vasorum flow on structure and function of the aorta in experimental animals. Circulation. 1995;91(10):2669-78. http://dx.doi.org/10.1161/01.CIR.91.10.2669 PMid:7743631.
» http://dx.doi.org/10.1161/01.CIR.91.10.2669 -
21Angouras D, Sokolis DP, Dosios T, et al. Effect of impaired vasa vasorum flow on the structure and mechanics of the thoracic aorta: implications for the pathogenesis of aortic dissection. Eur J Cardiothorac Surg. 2000;17(4):468-73. http://dx.doi.org/10.1016/S1010-7940(00)00382-1 PMid:10773572.
» http://dx.doi.org/10.1016/S1010-7940(00)00382-1 -
22Fagundes A, Pereira AH, Corrêa RK, Oliveira MT, Rodriguez R. Effects of removal of the adventitia of the descending aorta and structural alterations in the tunica media in pigs. Rev Col Bras Cir. 2012;39(2):133-8. http://dx.doi.org/10.1590/S0100-69912012000200009 PMid:22664520.
» http://dx.doi.org/10.1590/S0100-69912012000200009 -
23Osada H, Kyogoku M, Matsuo T, Kanemitsu N. Histopathological evaluation of aortic dissection: A comparison of congenital versus acquired aortic wall weakness. Interact Cardiovasc Thorac Surg. 2018;27(2):277-83. http://dx.doi.org/10.1093/icvts/ivy046 PMid:29514205.
» http://dx.doi.org/10.1093/icvts/ivy046 -
24Tsai TT, Schlicht MS, Khanafer K, et al. Tear size and location impacts false lumen pressure in an ex vivo model of chronic type B aortic dissection. J Vasc Surg. 2008;47(4):844-51. http://dx.doi.org/10.1016/j.jvs.2007.11.059 PMid:18381145.
» http://dx.doi.org/10.1016/j.jvs.2007.11.059 -
25Khanafer K, Berguer R. Fluid-structure interaction analysis of Turbulent pulsatile flow within a layered aortic wall as related to aortic dissection. J Biomech. 2009;42(16):2642-8. http://dx.doi.org/10.1016/j.jbiomech.2009.08.010 PMid:19765711.
» http://dx.doi.org/10.1016/j.jbiomech.2009.08.010 -
26Rudenick PA, Segers P, Pineda V, et al. Lumen Flow Patterns and their Relation with Morphological and Biomechanical Characteristics of Chronic Aortic Dissections. Computational Model Compared with Magnetic Resonance Imaging Measurements. PLoS One. 2017;12(1):e0170888. http://dx.doi.org/10.1371/journal.pone.0170888 PMid:28125720.
» http://dx.doi.org/10.1371/journal.pone.0170888 -
27Bukač M, Alber M. Multi-component model of intramural hematoma. J Biomech. 2017;50:42-9. http://dx.doi.org/10.1016/j.jbiomech.2016.11.040 PMid:27876369.
» http://dx.doi.org/10.1016/j.jbiomech.2016.11.040 -
28Wu MT, Wang YC, Huang YL, et al. Intramural blood pools accompanying aortic intramural hematoma: CT appearance and natural course. Radiology. 2011;258(3):705-13. http://dx.doi.org/10.1148/radiol.10101270 PMid:21212368.
» http://dx.doi.org/10.1148/radiol.10101270 -
29Jang YM, Seo JB, Lee YK, et al. Newly developed ulcer-like projection (ULP) in aortic intramural haematoma on follow-up CT: is it different from the ULP seen on the initial CT? Clin Radiol. 2008;63(2):201-6. http://dx.doi.org/10.1016/j.crad.2007.07.020 PMid:18194697.
» http://dx.doi.org/10.1016/j.crad.2007.07.020 -
30Lee CW, Kang JW, Lee HJ, Lim TH. MDCT evaluation of intimal defects in intramural hematoma of the aorta: initial findings and follow-up. Int J Cardiovasc Imaging. 2010;26(S2, Suppl 2):295-302. http://dx.doi.org/10.1007/s10554-010-9709-x PMid:20878253.
» http://dx.doi.org/10.1007/s10554-010-9709-x -
31Bosma MS, Quint LE, Williams DM, Patel HJ, Jiang Q, Myles JD. Ulcerlike projections developing in noncommunicating aortic dissections: CT findings and natural history. AJR. 2009;193(3):895-905. http://dx.doi.org/10.2214/AJR.08.2073 PMid:19696307.
» http://dx.doi.org/10.2214/AJR.08.2073 -
32Riambau V, Böckler D, Brunkwall J, Cao P, Chiesa R. Management of descending thoracic aorta diseases clinical practice guidelines of the European Society for Vascular Surgery (ESVS). Eur J Vasc Endovasc Surg. 2017;53(1):4-52.
-
33Manning W, Je Black JH. Overview of acute aortic dissection and other acute aortic syndromes. UpToDate. 2018.
-
34Shennan T. Dissecting aneurysms. London: Medical Research Council; 1934. (Special Report Series; no. 193).
-
35von Kodolitsch Y, Csosz SK, Koschyk DH, et al. Intramural hematoma of the aorta: predictors of progression to dissection and rupture. Circulation. 2003;107(8):1158-63. http://dx.doi.org/10.1161/01.CIR.0000052628.77047.EA PMid:12615795.
» http://dx.doi.org/10.1161/01.CIR.0000052628.77047.EA -
36Vilacosta I, Aragoncillo P, Cañadas V, San Román JA, Ferreirós J, Rodríguez E. Acute aortic syndrome: a new sight to an old conundrum. Heart. 2009;95(14):1130-9. PMid:19131440.
-
37Ganaha F, Miller DC, Sugimoto K, et al. The prognosis of Aortic Intramural Hematoma: The Prognosis of aortic Intramural hematoma with and without Penetrating Atherosclerotic ulcer: a clinical and radiologic analysis. Circulation. 2002;106(3):342-8. http://dx.doi.org/10.1161/01.CIR.0000022164.26075.5A PMid:12119251.
» http://dx.doi.org/10.1161/01.CIR.0000022164.26075.5A -
38Stanson AW, Kazmier FJ, Hollier LH, et al. Penetrating atherosclerotic ulcers of the thoracic aorta: natural history and clinicopathologic correlations. Ann Vasc Surg. 1986;1(1):15-23. http://dx.doi.org/10.1016/S0890-5096(06)60697-3 PMid:3504683.
» http://dx.doi.org/10.1016/S0890-5096(06)60697-3 -
39Coady MA, Rizzo JA, Hammond GL, Pierce JG, Kopf GS, Elefteriades JA. Penetrating ulcer of the thoracic aorta: what is it? How do we recognize it? How do we manage it? J Vasc Surg. 1998;27(6):1006-16. http://dx.doi.org/10.1016/S0741-5214(98)70003-5 PMid:9652462.
» http://dx.doi.org/10.1016/S0741-5214(98)70003-5 -
40Harris JA, Bis KG, Glover JL, Bendick PJ, Shetty A, Brown OW. Penetrating atherosclerotic ulcers of the aorta. J Vasc Surg. 1994;19(1):90-9. http://dx.doi.org/10.1016/S0741-5214(94)70124-5 PMid:8301743.
» http://dx.doi.org/10.1016/S0741-5214(94)70124-5 -
41Quint LE, Williams DM, Francis IR, et al. Ulcer like lesions of the aorta: imaging features and natural history. Radiology. 2001;218(3):719-23. http://dx.doi.org/10.1148/radiology.218.3.r01mr24719 PMid:11230645.
» http://dx.doi.org/10.1148/radiology.218.3.r01mr24719 -
42Borst HG, Heinemann MK, Stone CD. Pathogenesis. In: Surgical treatment of aortic dissection. New York: Churchill Livingstone Inc; 1996. p. 47-54.
-
43Nathan DP, Boonn W, Lai E, et al. Presentation, complications, and natural history of penetrating atherosclerotic ulcer disease. J Vasc Surg. 2012;55(1):10-5. http://dx.doi.org/10.1016/j.jvs.2011.08.005 PMid:22047830.
» http://dx.doi.org/10.1016/j.jvs.2011.08.005 -
44Pauls S, Orend KH, Sunder-Plassmann L, et al. Endovascular repair of symptomatic penetrating atherosclerotic ulcer of the thoracic aorta. Eur J Vasc Endovasc Surg. 2007;34(1):66-73.
-
45Georgiadis GS, Antoniou GA, Georgakarakos EI, et al. Surgical or endovascular therapy of abdominal penetrating aortic ulcers and their natural history: A systematic review. J Vasc Interv Radiol. 2013;24(10):1437-49. http://dx.doi.org/10.1016/j.jvir.2013.05.067 PMid:23932417.
» http://dx.doi.org/10.1016/j.jvir.2013.05.067 -
46Cho KR, Stanson AW, Potter DD, Cherry KJ, Schaff HV, Sundt TM 3rd. Penetrating atherosclerotic ulcer of the descending thoracic aorta and arch. J Thorac Cardiovasc Surg. 2004;127(5):1393-9. http://dx.doi.org/10.1016/j.jtcvs.2003.11.050 PMid:15115998.
» http://dx.doi.org/10.1016/j.jtcvs.2003.11.050 -
47Hagan PG, Nienaber CA, Isselbacher EM, et al. The International Registry of Dissection (IRAD): New Insights into an old disease. JAMA. 2000;283(7):897-903. http://dx.doi.org/10.1001/jama.283.7.897 PMid:10685714.
» http://dx.doi.org/10.1001/jama.283.7.897 -
48Charcot JM. De l’éxpectation en médecine. Paris: Librairie de Germer; 1847.
Datas de Publicação
-
Publicação nesta coleção
18 Jul 2019 -
Data do Fascículo
2019
Histórico
-
Recebido
20 Nov 2018 -
Aceito
26 Mar 2019