Resumo
A isquemia crítica de membro inferior sem leito distal tem opções restritas para tratamento. Desviar o fluxo sanguíneo de maneira retrógrada através da circulação venosa é uma alternativa amparada em evidências de inúmeros trabalhos publicados. Comparou-se através de mapeamento dúplex a distribuição do fluxo sanguíneo arterial em membros posteriores de suínos mantidos em circulação fisiológica com o contralateral submetido à isquemia e reperfusão por circulação retrógrada. O fluxo nos membros em circulação fisiológica e retrógrada foi avaliado por mapeamento dúplex através da determinação da velocidade de pico sistólico (VPS), da velocidade diastólica final (VDF) e do índice de resistividade (IR) em artérias selecionadas. A análise comparativa das extremidades mantidas em circulação fisiológica em relação às mantidas em isquemia e reperfusão, por circulação retrógrada, mostrou nestas, ao mapeamento dúplex, que as alterações nos padrões de onda espectral e nas variáveis hemodinâmicas são indicadores satisfatórios e sugerem boa distribuição do fluxo sanguíneo vascular distal.
Palavras-chave:
arterialização venosa; isquemia; reperfusão
Abstract
Treatment options for critical lower limb ischemia in the absence of the distal bed are limited. Diverting blood flow in a retrograde direction through the venous circulation is one alternative option that is supported by evidence from several published articles. Duplex scanning was used to compare the distribution of arterial flow in hind limbs of pigs maintained in physiological circulation to contralateral limbs subjected to ischemia and reperfusion by retrograde circulation. Flow in limbs with physiological and retrograde circulation was evaluated by duplex scanning with analysis of Peak Systolic Velocity (PSV), End Diastolic Velocity (EDV), and the Resistivity Index (RI) for selected arteries. This comparative analysis of extremities maintained in physiological circulation in relation to those subjected to ischemia and reperfusion by retrograde circulation showed, via duplex scanning, that changes in spectral wave patterns and hemodynamic variables are satisfactory indicators and suggest good distribution of distal blood flow.
Keywords:
venous arterialization; ischemia; reperfusion
INTRODUÇÃO
Em isquemia crítica sem leito arterial distal, não é possível derivar o sangue para uma extremidade arterial pérvia distal à obstrução. Desviar o fluxo sanguíneo de maneira retrógrada através da circulação venosa é uma alternativa viável amparada em evidências de inúmeros trabalhos publicados11 Alexandrescu V, Ngongang C, Vincent G, Ledent G, Hubermont G. Deep calf veins arterialization for inferior limb preservation in diabetic patients with extended ischaemic wounds, unfit for direct arterial reconstruction: preliminary results according to an angiosome model of perfusion. Cardiovasc Revasc Med. 2011;12(1):10-9. http://dx.doi.org/10.1016/j.carrev.2009.12.002. PMid:21241966.
http://dx.doi.org/10.1016/j.carrev.2009....
2 Djoric P. Early individual experience with distal venous arterialization as a lower limb salvage procedure. Am Surg. 2011;77(6):726-30. http://dx.doi.org/10.1177/000313481107700628. PMid:21679641.
http://dx.doi.org/10.1177/00031348110770...
3 Busato CR, Utrabo CA, Gomes RZ, et al. Utilização da safena magna in situ para arterialização do arco venoso do pé. J Vasc Bras. 2010;9(3):119-23. http://dx.doi.org/10.1590/S1677-54492010000300004.
http://dx.doi.org/10.1590/S1677-54492010...
4 Taylor RS, Belli AM, Jacob S. Distal venous arterialization for salvage of critically ischaemic inoperable limbs. Lancet. 1999;354(9194):1962-5. http://dx.doi.org/10.1016/S0140-6736(99)03164-5. PMid:10622299.
http://dx.doi.org/10.1016/S0140-6736(99)...
5 Mutirangura P, Ruangsetakit C, Wongwanit C, Sermsathanasawadi N, Chinsakchai K. Pedal bypass with deep venous arterialization: the therapeutic option in critical limb ischemia and unreconstructable distal arteries. Vascular. 2011;19(6):313-9. http://dx.doi.org/10.1258/vasc.2010.oa0278. PMid:22008976.
http://dx.doi.org/10.1258/vasc.2010.oa02...
6 Lengua F, La Madrid A, Acosta C, Vargas J. Arterializacion venosa temporal del pie diabético. J Vasc Bras. 2010;9(1):14-20. http://dx.doi.org/10.1590/S1677-54492010005000007.
http://dx.doi.org/10.1590/S1677-54492010...
7 Lu XW, Idu MM, Ubbink DT, Legemate DA. Meta-analysis of the clinical effectiveness of venous arterialization for salvage of critically ischaemic limbs. Eur J Vasc Endovasc Surg. 2006;31(5):493-9. http://dx.doi.org/10.1016/j.ejvs.2005.12.017. PMid:16488164.
http://dx.doi.org/10.1016/j.ejvs.2005.12...
8 Özbek C, Kestelli M, Emrecan B, et al. A novel approach: ascending venous arterialization for atherosclerosis obliterans. Eur J Vasc Endovasc Surg. 2005;29(1):47-51. http://dx.doi.org/10.1016/j.ejvs.2004.09.027. PMid:15570271.
http://dx.doi.org/10.1016/j.ejvs.2004.09...
-99 Schreve MA, Minnee RC, Bosma J, Leijdekkers VJ, Idu MM, Vahl AC. Comparative study of venous arterialization and pedal bypass in a patient cohort with critical limb ischemia. Ann Vasc Surg. 2014;28(5):1123-7. http://dx.doi.org/10.1016/j.avsg.2013.08.010. PMid:24189192.
http://dx.doi.org/10.1016/j.avsg.2013.08...
. Esse conceito baseia-se na teoria de que, na ausência ou diminuição de pressão arterial primária nas arteríolas, o sangue fornecido utilizando o sistema venoso distal por meio da arterialização é capaz de suprir os tecidos periféricos e fornecer oxigenação adequada33 Busato CR, Utrabo CA, Gomes RZ, et al. Utilização da safena magna in situ para arterialização do arco venoso do pé. J Vasc Bras. 2010;9(3):119-23. http://dx.doi.org/10.1590/S1677-54492010000300004.
http://dx.doi.org/10.1590/S1677-54492010...
4 Taylor RS, Belli AM, Jacob S. Distal venous arterialization for salvage of critically ischaemic inoperable limbs. Lancet. 1999;354(9194):1962-5. http://dx.doi.org/10.1016/S0140-6736(99)03164-5. PMid:10622299.
http://dx.doi.org/10.1016/S0140-6736(99)...
-55 Mutirangura P, Ruangsetakit C, Wongwanit C, Sermsathanasawadi N, Chinsakchai K. Pedal bypass with deep venous arterialization: the therapeutic option in critical limb ischemia and unreconstructable distal arteries. Vascular. 2011;19(6):313-9. http://dx.doi.org/10.1258/vasc.2010.oa0278. PMid:22008976.
http://dx.doi.org/10.1258/vasc.2010.oa02...
,1010 Busato CR, Utrabo CA, Lipinski LC, et al. Experimental model for the study of retrograde flow. J Vasc Bras. 2016;15(2):93-8. http://dx.doi.org/10.1590/1677-5449.008915. PMid:29930572.
http://dx.doi.org/10.1590/1677-5449.0089...
.
Trabalhos procuraram comparar, através de variáveis físicas e laboratoriais, o grau de isquemia e a reperfusão produzida por arterialização venosa em modelos animais1111 Busato CR, Utrabo CAL, Lipinski LC, et al. Isquemia e reperfusão por circulação retrógrada: estudo comparativo experimental. J Vasc Bras. 2017;16(3):187-94. http://dx.doi.org/10.1590/1677-5449.009016. PMid:29930645.
http://dx.doi.org/10.1590/1677-5449.0090...
. Este trabalho comparou a distribuição do fluxo vascular arterial em membros mantidos em circulação fisiológica com contralaterais submetidos à arterialização venosa, através da medida de variáveis hemodinâmicas e índices Doppler nos leitos vasculares.
Este projeto foi aprovado pelo Comitê de Ética em Pesquisa Animal (CEUA – 024/2017) da Universidade Estadual de Ponta Grossa (UEPG), Ponta Grossa, PR, Brasil. Foi realizado um estudo observacional, em que foram utilizados quatro suínos cruzados Large White e Landrace, livres de qualquer procedimento cirúrgico prévio, destinados às aulas práticas de Técnica Operatória antes dos procedimentos cirúrgicos. Os animais receberam medicação pré-anestésica com ketamina (14 mg/kg), xilazina (0,2 mg/kg) e acepromazina (0,4 mg/kg). Foram induzidos à anestesia com propofol (5 mg/kg) e mantidos em anestesia inalatória com isofluorano em concentração alveolar mínima de 1,2 a 1,7%.
Membros posteriores direitos dos animais estudados foram mantidos em circulação fisiológica enquanto membros posteriores esquerdos foram submetidos à isquemia e reperfusão por arterialização venosa. Realizaram-se, à esquerda, dissecções de veias safenas laterais. Após anticoagulação sistêmica com 5.000 UI de heparina, procederam-se ligaduras proximais, venotomias longitudinais e rotura das válvulas a jusante com auxílio de valvulótomo de Lengua. Foi feita a dilatação das extremidades distais com soro heparinizado através de sonda nº 4 e cateterização, fixação e fechamento das sondas após aplicação local com 10 mL de soro heparinizado (5.000 UI/500 mL de soro fisiológico). As dissecções das artérias femorais comuns esquerdas com ligadura das extremidades distais foram realizadas. As extremidades proximais foram cateterizadas com sondas nº 6, as quais, após fixação e aplicação local com 10 mL de soro heparinizado, foram imediatamente conectadas às veias safenas laterais utilizando-se cateteres de silicone (extensor para Cateter Reversível Luer Lock 20 cm, 2 conectores macho – 10F; Hartmann®, Rio de Janeiro, Brasil), estabelecendo-se a arterialização venosa da extremidade. O tempo médio de isquemia entre a ligadura da artéria femoral distal e o estabelecimento da circulação retrógrada foi de 20 minutos (Figura 1).
A avaliação do fluxo vascular nas extremidades fisiológica e arterializada dos membros foi realizada através do exame de mapeamento dúplex. O exame foi realizado de forma aberta, sempre pelo mesmo radiologista, sem contraconferência, em um aparelho de ultrassom Samsung/Medison SonoAce R7® (Coreia do Sul) com transdutor linear modelo LN5-12 de frequência 8MHz, lubrificado com gel eletrocondutor para ultrassom Sonic-Plus® e posicionado na região dos leitos vasculares eleitos, as artérias femoral comum, safena e plantar medial. No modo de medição Doppler espectral e colorido, utilizou-se o preset do fabricante para estudo vascular periférico, do qual se obteve resultados arteriais de velocidade de pico sistólico (VPS), velocidade diastólica final (VDF) e padrão de onda espectral (PO). Sobre esses, foi calculado o índice Doppler de resistividade (IR). O tempo médio entre o estabelecimento da circulação retrógrada e o final da leitura nas artérias dos membros posteriores direito e esquerdo foi de 60 minutos. Ao final dos procedimentos do experimento e das aulas de Técnica Operatória, os animais foram submetidos à eutanásia conforme resolução 1000/2012 do Conselho Federal de Medicina Veterinária (CFMV).
Cada animal teve as variáveis hemodinâmicas e índices Doppler determinados, e aqueles dos membros com circulação fisiológica foram comparados aos dos membros contralaterais arterializados (Tabela 1). Para efeitos de comparação, foram consideradas as razões entre os membros arterializado e fisiológico das variáveis supracitadas. Assim, tem-se um índice apontando a proporção de uma determinada variável no membro arterializado correspondente à do lado fisiológico do mesmo animal (Tabela 1).
Proporções obtidas através da relação membro arterializado/fisiológico dos animais e leitos vasculares selecionados e suas respectivas médias.
A pesquisa de fluxo sanguíneo arterial ao Doppler em membros arterializados demonstrou equivalência entre os padrões de onda trifásicos e bifásicos na artéria femoral, predominância de padrão bifásico na artéria safena e monofásico na artéria plantar medial (Tabela 2). O número amostral reduzido resultou em grande heterogeneidade nos dados coletados, o que impossibilitou a análise estatística. Tal diversidade foi verificada principalmente através do coeficiente de variação da VDF nos leitos vasculares estudados.
Padrões de onda encontrados nos leitos arteriais selecionados e suas proporções (%) nos membros fisiológicos e arterializados dos animais.
Embora o melhor parâmetro para avaliar a circulação em um membro seja o seu contralateral, as determinações são realizadas de maneira sequencial de tal forma que as condições hemodinâmicas não são idênticas. A utilização de cateteres inelásticos de calibres menores aos dos vasos pode aumentar a resistividade enquanto o desvio para o sistema venoso e arterial de menor pressão, pela ligadura da femoral, pode diminui-la. Assim, o resultado dessa equação em números pode apresentar algumas diversidades.
As variáveis hemodinâmicas utilizadas neste estudo têm a finalidade de avaliar quantitativamente o espectro Doppler. Na visualização de uma onda espectral arterial (Figura 2), o ponto máximo corresponde à VPS, ou seja, à máxima velocidade alcançada no leito vascular durante um ciclo cardíaco; o ponto mínimo na morfologia da onda é o valor da VDF1212 Carvalho CF, Chammas MC, Cerri GG. Princípios . Princípios físicos do Doppler em ultrassonografia: revisão bibliográfica. Cienc Rural. 2008;38(3):872-9. http://dx.doi.org/10.1590/S0103-84782008000300047.
http://dx.doi.org/10.1590/S0103-84782008...
,1313 Castelló CM, Bragato N, Martins I, Santos TV, Borges NC. Ultrassonografia Doppler colorido e Doppler espectral para o estudo de pequenos fluxos. Enciclopédia Biosfera. Centro Científico Conhecer. 2015;11(22):2691-713..
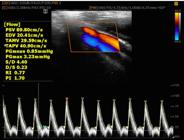
Padrão de onda espectral trifásico em artéria femoral de membro mantido em circulação fisiológica. PSV = peak systolic velocity; EDV = end-diastolic velocity; TAMV = time-averaged mean velocity; TAPV = time-averaged peak velocity; PGmean = mean pressure gradient; PGmax = maximum pressure gradient; S/D = PSV/EDV; D/S = EDV/PSV; RI = resistivity index; PI = pulsatility index.
Já os índices Doppler fornecem dados acerca da resistência vascular periférica por meio dos valores obtidos nas variáveis supracitadas (VPS, VDF). O IR, descrito por Pourcelot em 1974, é determinado através da subtração entre a VPS e a VDF, dividida pela VPS (IR = VPS – VDF/VPS)1212 Carvalho CF, Chammas MC, Cerri GG. Princípios . Princípios físicos do Doppler em ultrassonografia: revisão bibliográfica. Cienc Rural. 2008;38(3):872-9. http://dx.doi.org/10.1590/S0103-84782008000300047.
http://dx.doi.org/10.1590/S0103-84782008...
,1313 Castelló CM, Bragato N, Martins I, Santos TV, Borges NC. Ultrassonografia Doppler colorido e Doppler espectral para o estudo de pequenos fluxos. Enciclopédia Biosfera. Centro Científico Conhecer. 2015;11(22):2691-713..
As alterações nos índices hemodinâmicos auxiliam na identificação de desordens que afetem a perfusão tecidual ou a complacência dos leitos vasculares. Diversos fatores além da resistência ao fluxo sanguíneo nos vasos periféricos, como a frequência cardíaca, a pressão sanguínea e o comprimento e a elasticidade dos vasos, influenciam nos valores dos índices Doppler1212 Carvalho CF, Chammas MC, Cerri GG. Princípios . Princípios físicos do Doppler em ultrassonografia: revisão bibliográfica. Cienc Rural. 2008;38(3):872-9. http://dx.doi.org/10.1590/S0103-84782008000300047.
http://dx.doi.org/10.1590/S0103-84782008...
, ressaltando-se a importância da comparação entre os lados fisiológico e arterializado do mesmo animal, como encontrado na literatura1414 Thaveau F, Zoll J, Bouitbir J, et al. Contralateral leg as a control during skeletal muscle ischemia-reperfusion. J Surg Res. 2009;155(1):65-9. http://dx.doi.org/10.1016/j.jss.2008.08.001. PMid:19159910.
http://dx.doi.org/10.1016/j.jss.2008.08....
,1515 Mansour Z, Bouitbir J, Charles AL, et al. Remote and local ischemic preconditioning equivalently protects rat skeletal muscle mitochondrial function during experimental aortic cross-clamping. J Vasc Surg. 2012;55(2):497-505.e1. http://dx.doi.org/10.1016/j.jvs.2011.07.084. PMid:22056287.
http://dx.doi.org/10.1016/j.jvs.2011.07....
. Embora as dissecções e os cateterismos para circulação retrógrada tenham sido realizados à esquerda, é provável que o membro direito tenha sofrido alterações no fluxo sanguíneo, provocadas por modificações da resistência periférica à esquerda.
Embora a leitura pelo ultrassom à esquerda tenha sido feita a montante do ponto de ligadura da artéria femoral comum, os membros em circulação retrógrada poderiam apresentar alterações, em relação ao fisiológico, na dependência da variação da resistência periférica encontrada (Tabela 1 e Tabela 2). Já em uma artéria safena, verificou-se um PO monofásico e redução da VPS e da VDF com manutenção do IR, sugerindo cenário da circulação retrógrada (Tabela 2).
Nos leitos arteriais distais (artéria plantar medial), o esperado era a diminuição dos IRs para poder caracterizar a existência de fluxo pós-arterialização. Os resultados mostraram que esse fluxo monofásico está presente através dos dados do IR (Tabela 1 e Tabela 2).
O PO trifásico (Figura 2) é típico de leitos vasculares com IR elevado e é graficamente representado por picos sistólicos afilados e fluxo sanguíneo reverso no início da diástole. O fluxo sanguíneo diastólico reverso ocorre nesses vasos porque a VPS elevada é refletida com alta impedância pelo leito vascular periférico, mas, à medida que o diâmetro vascular retorna ao normal, o fluxo sanguíneo diastólico torna-se contínuo1212 Carvalho CF, Chammas MC, Cerri GG. Princípios . Princípios físicos do Doppler em ultrassonografia: revisão bibliográfica. Cienc Rural. 2008;38(3):872-9. http://dx.doi.org/10.1590/S0103-84782008000300047.
http://dx.doi.org/10.1590/S0103-84782008...
.
O PO bifásico (Figura 3) é típico de regiões onde há perda da alta resistividade, como em um tecido com circulação pós-estenótica. Caracteriza-se pela presença de picos sistólicos também afilados, porém mais amplos que os PO trifásicos, e fluxo sanguíneo diastólico contínuo, sem fluxo reverso1212 Carvalho CF, Chammas MC, Cerri GG. Princípios . Princípios físicos do Doppler em ultrassonografia: revisão bibliográfica. Cienc Rural. 2008;38(3):872-9. http://dx.doi.org/10.1590/S0103-84782008000300047.
http://dx.doi.org/10.1590/S0103-84782008...
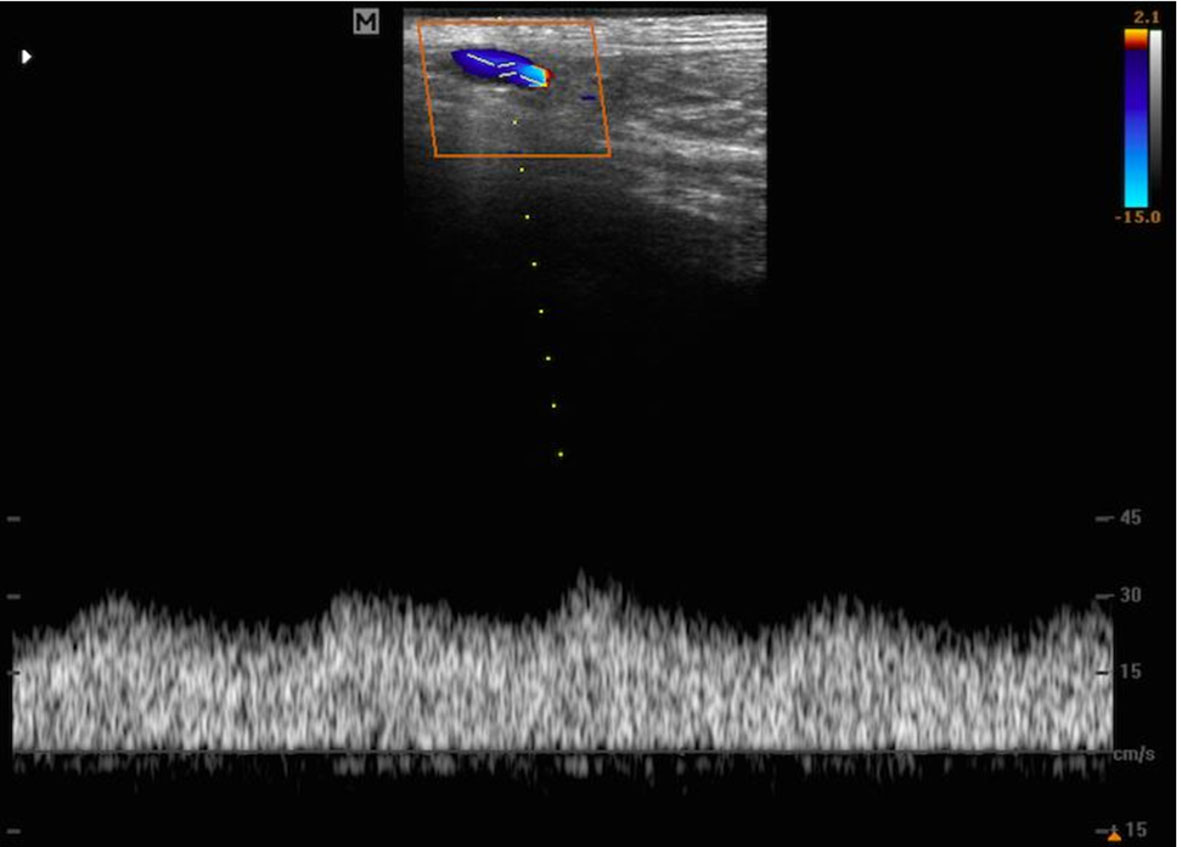
. Já o PO monofásico (Figura 4) é tipicamente venoso ou de leitos com baixa resistividade, como em fístula arteriovenosa (baixo IR), sendo geralmente laminar1212 Carvalho CF, Chammas MC, Cerri GG. Princípios . Princípios físicos do Doppler em ultrassonografia: revisão bibliográfica. Cienc Rural. 2008;38(3):872-9. http://dx.doi.org/10.1590/S0103-84782008000300047.
http://dx.doi.org/10.1590/S0103-84782008...
.
Padrão de onda espectral bifásico em artéria femoral de membro arterializado. PSV = peak systolic velocity; EDV = end-diastolic velocity; TAPV = time-averaged peak velocity; PGmean = mean pressure gradient; PGmax = maximum pressure gradient; S/D = PSV/EDV; D/S = EDV/PSV; RI = resistivity index; PI = pulsatility index.
Padrão de onda espectral monofásico em leito vascular distal de artéria plantar medial em membro arterializado.
Quanto aos leitos arteriais fisiológicos, o PO na artéria femoral comum foi equivalente na distribuição entre os padrões tri e bifásicos, enquanto o bifásico predominou nas demais artérias. Já nos vasos arterializados, se verificou alterações no PO de uma artéria safena e de três artérias plantares mediais com predominância de ondas monofásicas, caracterizando mudança para um padrão de baixa resistividade compatível com fluxo sanguíneo arterializado. A importância da avaliação dos POs no contexto da arterialização venosa é a identificação da mudança para que se possa sugerir que o fluxo sanguíneo nos leitos vasculares seja proveniente de uma via diferente da fisiológica.
Possíveis vieses anatômicos poderiam ser reduzidos com sorteio do lado a arterializar. Medidas pré-operatórias, que não foram realizadas, poderiam demonstrar possíveis alterações hemodinâmicas, no lado fisiológico, após a arterialização venosa contralateral. A medida de índice tornozelo braquial, pré e pós-arterialização venosa, poderia ter dado suporte para as possíveis alterações que pudessem ser encontradas ao mapeamento dúplex.
A análise comparativa das extremidades mantidas em circulação fisiológica em relação às mantidas em isquemia e reperfusão por circulação retrógrada mostrou nestas, ao mapeamento dúplex, que os padrões de onda espectral e as variáveis hemodinâmicas são indicadores satisfatórios e sugerem boa distribuição do fluxo sanguíneo nos leitos vasculares. No entanto, novos estudos são necessários para se avaliar com maior precisão os parâmetros do eco-Doppler nos vasos envolvidos.
-
Como citar: Busato CR, Utrabo CAL, Lipinski LC, Dreweck MO, Fernandes ACV, Sviercoski G. Estudo comparativo experimental da distribuição do fluxo arterial, em isquemia e reperfusão por circulação retrógrada, através de mapeamento dúplex. J Vasc Bras. 2020;19:e20190052. https://doi.org/10.1590/1677-5449.190052
-
Fonte de financiamento: Nenhuma.
-
O estudo foi realizado no Laboratório de Técnica Operatória e Cirurgia Experimental, Universidade Estadual de Ponta Grossa (UEPG), Ponta Grossa, PR, Brasil.
REFERÊNCIAS
-
1Alexandrescu V, Ngongang C, Vincent G, Ledent G, Hubermont G. Deep calf veins arterialization for inferior limb preservation in diabetic patients with extended ischaemic wounds, unfit for direct arterial reconstruction: preliminary results according to an angiosome model of perfusion. Cardiovasc Revasc Med. 2011;12(1):10-9. http://dx.doi.org/10.1016/j.carrev.2009.12.002 PMid:21241966.
» http://dx.doi.org/10.1016/j.carrev.2009.12.002 -
2Djoric P. Early individual experience with distal venous arterialization as a lower limb salvage procedure. Am Surg. 2011;77(6):726-30. http://dx.doi.org/10.1177/000313481107700628 PMid:21679641.
» http://dx.doi.org/10.1177/000313481107700628 -
3Busato CR, Utrabo CA, Gomes RZ, et al. Utilização da safena magna in situ para arterialização do arco venoso do pé. J Vasc Bras. 2010;9(3):119-23. http://dx.doi.org/10.1590/S1677-54492010000300004
» http://dx.doi.org/10.1590/S1677-54492010000300004 -
4Taylor RS, Belli AM, Jacob S. Distal venous arterialization for salvage of critically ischaemic inoperable limbs. Lancet. 1999;354(9194):1962-5. http://dx.doi.org/10.1016/S0140-6736(99)03164-5 PMid:10622299.
» http://dx.doi.org/10.1016/S0140-6736(99)03164-5 -
5Mutirangura P, Ruangsetakit C, Wongwanit C, Sermsathanasawadi N, Chinsakchai K. Pedal bypass with deep venous arterialization: the therapeutic option in critical limb ischemia and unreconstructable distal arteries. Vascular. 2011;19(6):313-9. http://dx.doi.org/10.1258/vasc.2010.oa0278 PMid:22008976.
» http://dx.doi.org/10.1258/vasc.2010.oa0278 -
6Lengua F, La Madrid A, Acosta C, Vargas J. Arterializacion venosa temporal del pie diabético. J Vasc Bras. 2010;9(1):14-20. http://dx.doi.org/10.1590/S1677-54492010005000007
» http://dx.doi.org/10.1590/S1677-54492010005000007 -
7Lu XW, Idu MM, Ubbink DT, Legemate DA. Meta-analysis of the clinical effectiveness of venous arterialization for salvage of critically ischaemic limbs. Eur J Vasc Endovasc Surg. 2006;31(5):493-9. http://dx.doi.org/10.1016/j.ejvs.2005.12.017 PMid:16488164.
» http://dx.doi.org/10.1016/j.ejvs.2005.12.017 -
8Özbek C, Kestelli M, Emrecan B, et al. A novel approach: ascending venous arterialization for atherosclerosis obliterans. Eur J Vasc Endovasc Surg. 2005;29(1):47-51. http://dx.doi.org/10.1016/j.ejvs.2004.09.027 PMid:15570271.
» http://dx.doi.org/10.1016/j.ejvs.2004.09.027 -
9Schreve MA, Minnee RC, Bosma J, Leijdekkers VJ, Idu MM, Vahl AC. Comparative study of venous arterialization and pedal bypass in a patient cohort with critical limb ischemia. Ann Vasc Surg. 2014;28(5):1123-7. http://dx.doi.org/10.1016/j.avsg.2013.08.010 PMid:24189192.
» http://dx.doi.org/10.1016/j.avsg.2013.08.010 -
10Busato CR, Utrabo CA, Lipinski LC, et al. Experimental model for the study of retrograde flow. J Vasc Bras. 2016;15(2):93-8. http://dx.doi.org/10.1590/1677-5449.008915 PMid:29930572.
» http://dx.doi.org/10.1590/1677-5449.008915 -
11Busato CR, Utrabo CAL, Lipinski LC, et al. Isquemia e reperfusão por circulação retrógrada: estudo comparativo experimental. J Vasc Bras. 2017;16(3):187-94. http://dx.doi.org/10.1590/1677-5449.009016 PMid:29930645.
» http://dx.doi.org/10.1590/1677-5449.009016 -
12Carvalho CF, Chammas MC, Cerri GG. Princípios . Princípios físicos do Doppler em ultrassonografia: revisão bibliográfica. Cienc Rural. 2008;38(3):872-9. http://dx.doi.org/10.1590/S0103-84782008000300047
» http://dx.doi.org/10.1590/S0103-84782008000300047 -
13Castelló CM, Bragato N, Martins I, Santos TV, Borges NC. Ultrassonografia Doppler colorido e Doppler espectral para o estudo de pequenos fluxos. Enciclopédia Biosfera. Centro Científico Conhecer. 2015;11(22):2691-713.
-
14Thaveau F, Zoll J, Bouitbir J, et al. Contralateral leg as a control during skeletal muscle ischemia-reperfusion. J Surg Res. 2009;155(1):65-9. http://dx.doi.org/10.1016/j.jss.2008.08.001 PMid:19159910.
» http://dx.doi.org/10.1016/j.jss.2008.08.001 -
15Mansour Z, Bouitbir J, Charles AL, et al. Remote and local ischemic preconditioning equivalently protects rat skeletal muscle mitochondrial function during experimental aortic cross-clamping. J Vasc Surg. 2012;55(2):497-505.e1. http://dx.doi.org/10.1016/j.jvs.2011.07.084 PMid:22056287.
» http://dx.doi.org/10.1016/j.jvs.2011.07.084
Datas de Publicação
-
Publicação nesta coleção
31 Jul 2020 -
Data do Fascículo
2020
Histórico
-
Recebido
13 Abr 2019 -
Aceito
29 Set 2019