Resumo
Introdução
Modelos laboratoriais de biofilmes vêm sendo desenvolvidos com a finalidade de simular o ambiente bucal e o processo de formação da cárie dental.
Objetivo
Estabelecer e padronizar um modelo de biofilme in vitro para o desenvolvimento de lesões de cárie em dentina.
Material e método
Doze discos padronizados de dentina bovina foram divididos em três tempos experimentais: 4, 7 e 10 dias. As amostras de cada tempo experimental foram inoculadas com Streptococcus mutans UA 159 em meio de cultura BHI com 1% de sacarose e cultivadas em anaerobiose. As variáveis de resposta foram a perda de dureza integrada (ΔS) dos discos de dentina e dureza do substrato em diferentes profundidades. Os dados de ΔS foram analisados através de ANOVA seguido do teste Tukey, ambos com significância de 5%, e os dados de dureza de profundidade de lesão analisados descritivamente.
Resultado
Houve maior perda mineral aos 10 dias de crescimento microbiológico quando comparados aos 4 dias (p = 0,034), no entanto não houve diferença entre 7 e 10 dias (p = 0,853). O grupo de 4 dias mostrou perda de dureza em regiões mais superficiais (10-40µm); e o grupo de 10 dias mostrou desmineralização em áreas mais profundas, até 150 µm.
Conclusão
O modelo proposto mostrou-se capaz de desenvolver lesões de cárie artificiais em dentina. Em 7 dias, as lesões subsuperficiais de dentina foram adequadas para estudos de des-remineralização.
Descritores:
Placa dentária; cárie dentária; desmineralização; dentina
Abstract
Introduction
Oral laboratory biofilm models have been developed to reproduce the oral environment and the process of caries lesion formation in vitro.
Objective
To establish and standardize an in vitro biofilm model for the development of caries lesions in dentin.
Material and method
Twelve standardized bovine dentin discs were assigned into three experimental times: 4, 7, and 10 days. Samples of each experimental period were inoculated with Streptococcus mutans UA 159 in a BHI culture medium with 1% sucrose, and cultured under anaerobic conditions. The integrated hardness loss (ΔS) of dentin discs and the hardness of the substrate at different depths were considered as response variables. The ΔS data were analysed by ANOVA followed by Tukey's test, both with significance level of 5%, and the data of hardness at different depths were analysed descriptively.
Result
There was a higher hardness loss after 10 days of microbial growth when compared to 4 days (p = 0.034), however, there was no difference between 7 and 10 days (p = 0.853). The 4-day group showed loss of hardness of the surface layers (10-40μm) and the 10-day group showed demineralization in the deeper area around 150µm.
Conclusion
The proposed model was able to develop artificial caries lesions in dentin. In 7 days, the dentin sub superficial lesions were suitable to des-remineralisation studies.
Descriptors:
Dental plaque; dental caries; demineralization; dentin
INTRODUÇÃO
A cárie dentária ocorre quando há um desequilíbrio na relação físico-química entre o substrato dentário e o biofilme cariogênico formado sobre essa estrutura, resultando na sua destruição11 Maske TT, van de Sande FH, Arthur RA, Huysmans MCDNJM, Cenci MS. In vitro biofilm models to study dental caries: a systematic review. Biofouling. 2017 Sep;33(8):661-75. PMid:28792234. http://dx.doi.org/10.1080/08927014.2017.1354248.
http://dx.doi.org/10.1080/08927014.2017....
. A etiologia da doença está relacionada principalmente à interação de fatores determinantes como dieta rica em sacarose, microbiota bucal e higiene bucal inadequada22 Zero DT, Fontana M, Martinez-Mier EA, Ferreira-Zandona A, Ando M, Gonzalez-Cabezas C, et al. The biology, prevention, diagnosis and treatment of dental caries: scientific advances in the United States. J Am Dent Assoc. 2009 Sep;140(Suppl 1):25S-34S. PMid:19723928. http://dx.doi.org/10.14219/jada.archive.2009.0355.
http://dx.doi.org/10.14219/jada.archive....
. Nos últimos anos, especial ênfase tem sido dada aos aspectos comportamentais da doença e em especial ao hábito de consumo de carboidratos fermentáveis33 Sheiham A, James WP. Diet and dental caries: the pivotal role of free sugars reemphasized. J Dent Res. 2015 Oct;94(10):1341-7. PMid:26261186. http://dx.doi.org/10.1177/0022034515590377.
http://dx.doi.org/10.1177/00220345155903...
e principalmente sacarose, o principal causador da doença cárie. Estudos mostram que a redução na ingesta de sacarose conduz ao menor aparecimento da doença cárie44 Moynihan P. Sugars and dental caries: evidence for setting a recommended threshold for intake. Adv Nutr. 2016 Jan;7(1):149-56. PMid:26773022. http://dx.doi.org/10.3945/an.115.009365.
http://dx.doi.org/10.3945/an.115.009365...
,55 Moynihan PJ, Kelly SA. Effect on caries of restricting sugars intake: systematic review to inform WHO guidelines. J Dent Res. 2014 Jan;93(1):8-18. PMid:24323509. http://dx.doi.org/10.1177/0022034513508954.
http://dx.doi.org/10.1177/00220345135089...
.
Modelos laboratoriais de biofilmes vêm sendo desenvolvidos com a finalidade de simular in vitro o ambiente bucal66 Campos PH, Sanabe ME, Rodrigues JA, Duarte DA, Santos MT, Guare RO, et al. Different bacterial models for in vitro induction of non-cavitated enamel caries-like lesions: Microhardness and polarized light miscroscopy analyses. Microsc Res Tech. 2015 Jun;78(6):444-51. PMid:25783414. http://dx.doi.org/10.1002/jemt.22493.
http://dx.doi.org/10.1002/jemt.22493...
7 Rudney JD, Chen R, Lenton P, Li J, Li Y, Jones RS, et al. A reproducible oral microcosm biofilm model for testing dental materials. J Appl Microbiol. 2012 Dec;113(6):1540-53. PMid:22925110. http://dx.doi.org/10.1111/j.1365-2672.2012.05439.x.
http://dx.doi.org/10.1111/j.1365-2672.20...
8 Tang G, Yip H-K, Cutress TW, Samaranayake LP. Artificial mouth model systems and their contribution to caries research: a review. J Dent. 2003 Mar;31(3):161-71. PMid:12726700. http://dx.doi.org/10.1016/S0300-5712(03)00009-5.
http://dx.doi.org/10.1016/S0300-5712(03)...
9 van de Sande FH, Azevedo MS, Lund RG, Huysmans MC, Cenci MS. An in vitro biofilm model for enamel demineralization and antimicrobial dose-response studies. Biofouling. 2011 Oct;27(9):1057-63. PMid:22044385. http://dx.doi.org/10.1080/08927014.2011.625473.
http://dx.doi.org/10.1080/08927014.2011....
-1010 Wong L, Sissions CH. A comparison of human dental plaque microcosm biofilms grown in an undefined medium and a chemically defined artificial saliva. Arch Oral Biol. 2001 Jun;46(6):477-86. PMid:11311195. http://dx.doi.org/10.1016/S0003-9969(01)00016-4.
http://dx.doi.org/10.1016/S0003-9969(01)...
, devido à dificuldade de investigação do biofilme in vivo, limitação de quantidade amostral, complexidade do ambiente bucal e a questões éticas relacionadas com estudos envolvendo cárie dentária em seres humanos88 Tang G, Yip H-K, Cutress TW, Samaranayake LP. Artificial mouth model systems and their contribution to caries research: a review. J Dent. 2003 Mar;31(3):161-71. PMid:12726700. http://dx.doi.org/10.1016/S0300-5712(03)00009-5.
http://dx.doi.org/10.1016/S0300-5712(03)...
,1010 Wong L, Sissions CH. A comparison of human dental plaque microcosm biofilms grown in an undefined medium and a chemically defined artificial saliva. Arch Oral Biol. 2001 Jun;46(6):477-86. PMid:11311195. http://dx.doi.org/10.1016/S0003-9969(01)00016-4.
http://dx.doi.org/10.1016/S0003-9969(01)...
. E embora estudos in situ possam ser utilizados como uma ponte entre estudos in vitro e in vivo, através do uso de dispositivos intraorais que viabilizam a remoção das amostras em períodos de tempo predeterminados, o acesso às características do biofilme e perfil de desmineralização também possuem limitações como custos, tempo e dependência da colaboração do paciente. Estudos in vitro permitem a realização de investigações em ambientes controlados, com menor variabilidade1111 Botelho JN, Villegas-Salinas M, Troncoso-Gajardo P, Giacaman RA, Cury JA. Enamel and dentine demineralization by a combination of starch and sucrose in a biofilm: caries model. Braz Oral Res. 2016 May;30(1):1-8. PMid:27223133. http://dx.doi.org/10.1590/1807-3107BOR-2016.vol30.0052.
http://dx.doi.org/10.1590/1807-3107BOR-2...
. Além disso, estudos in vitro são precursores de estudos in vivo, além de permitirem a confirmação de achados clínicos1212 Fernández CE, Tenuta LM, Cury JA. Validation of a cariogenic biofilm model to evaluate the effect of fluoride on enamel and root dentine demineralization. PLoS One. 2016 Jan;11(1):e0146478. PMid:26731743. http://dx.doi.org/10.1371/journal.pone.0146478.
http://dx.doi.org/10.1371/journal.pone.0...
. Ainda, dentro desse contexto, os modelos microbiológicos parecem se aproximar mais do processo de formação da cárie dental e da mimetização da morfologia das lesões1313 Marquezan M, Corrêa FN, Sanabe ME, Rodrigues Filho LE, Hebling J, Guedes-Pinto AC, et al. Artificial methods of dentine caries induction: a hardness and morphological comparative study. Arch Oral Biol. 2009 Dec;54(12):1111-7. PMid:19878926. http://dx.doi.org/10.1016/j.archoralbio.2009.09.007.
http://dx.doi.org/10.1016/j.archoralbio....
.
A utilização de modelos de biofilme em monocultura como, por exemplo, de Streptococcus mutans tem sido útil no estudo de variáveis específicas dentro da complexidade da doença cárie dentária1414 Giacaman RA, Campos P, Munoz-Sandoval C, Castro RJ. Cariogenic potential of commercial sweeteners in an experimental biofilm caries model on enamel. Arch Oral Biol. 2013 Sep;58(9):1116-22. PMid:23631998. http://dx.doi.org/10.1016/j.archoralbio.2013.03.005.
http://dx.doi.org/10.1016/j.archoralbio....
,1515 Muñoz-Sandoval C, Munoz-Cifuentes MJ, Giacaman RA, Ccahuana-Vasquez RA, Cury JA. Effect of bovine milk on Streptococcus mutans biofilm cariogenic properties and enamel and dentin demineralization. Pediatr Dent. 2012 Nov-Dec;34(7):e197-201. PMid:23265155.. Além disso, modelos desse tipo permitem respostas rápidas para avaliação do efeito antimicrobiano ou anticariogênico de substâncias ainda em testes iniciais1616 Cavalcanti YW, Bertolini MM, da Silva WJ, Del-Bel-Cury AA, Tenuta LM, Cury JA. A three-species biofilm model for the evaluation of enamel and dentin demineralization. Biofouling. 2014;30(5):579-88. PMid:24730462. http://dx.doi.org/10.1080/08927014.2014.905547.
http://dx.doi.org/10.1080/08927014.2014....
. Diversos métodos microbiológicos de monocultura foram descritos1414 Giacaman RA, Campos P, Munoz-Sandoval C, Castro RJ. Cariogenic potential of commercial sweeteners in an experimental biofilm caries model on enamel. Arch Oral Biol. 2013 Sep;58(9):1116-22. PMid:23631998. http://dx.doi.org/10.1016/j.archoralbio.2013.03.005.
http://dx.doi.org/10.1016/j.archoralbio....
,1515 Muñoz-Sandoval C, Munoz-Cifuentes MJ, Giacaman RA, Ccahuana-Vasquez RA, Cury JA. Effect of bovine milk on Streptococcus mutans biofilm cariogenic properties and enamel and dentin demineralization. Pediatr Dent. 2012 Nov-Dec;34(7):e197-201. PMid:23265155., porém poucos padronizam os seus resultados para uma condição cariogênica específica. Tratamentos preventivos para a cárie dentária com a utilização de diferentes tipos de materiais vêm sendo amplamente estudados11 Maske TT, van de Sande FH, Arthur RA, Huysmans MCDNJM, Cenci MS. In vitro biofilm models to study dental caries: a systematic review. Biofouling. 2017 Sep;33(8):661-75. PMid:28792234. http://dx.doi.org/10.1080/08927014.2017.1354248.
http://dx.doi.org/10.1080/08927014.2017....
e nesse contexto a padronização de modelos simplificados ou complexos que desenvolvam lesões de cárie em laboratório parece ser útil para investigações acerca do efeito desses materiais.
Ainda, a maior parte dos estudos publicados na literatura sobre a indução de lesões em dentina reportam o uso de diferentes protocolos, sendo baseados normalmente na imersão em ácido ou ciclagem de pH1313 Marquezan M, Corrêa FN, Sanabe ME, Rodrigues Filho LE, Hebling J, Guedes-Pinto AC, et al. Artificial methods of dentine caries induction: a hardness and morphological comparative study. Arch Oral Biol. 2009 Dec;54(12):1111-7. PMid:19878926. http://dx.doi.org/10.1016/j.archoralbio.2009.09.007.
http://dx.doi.org/10.1016/j.archoralbio....
. O presente estudo baseia-se no uso de microrganismos para a indução das lesões, que simulam de forma mais próxima da real os eventos que ocorrem na cavidade oral, em comparação aos modelos anteriormente citados, e permite a interação entre substrato e bactéria. A partir disso, o presente estudo objetivou padronizar o desenvolvimento de lesões de cárie em dentina em um modelo de biofilme de monocultura simplificado (Streptococcus mutans), para auxiliar em estudos de desmineralização e remineralização. A hipótese testada foi de que o modelo de biofilme proposto permitiria o desenvolvimento de lesões artificiais de dentina.
MATERIAL E MÉTODO
Delineamento Experimental
Biofilmes de monocultura (Streptococcus mutans UA 159) foram crescidos sobre 12 discos de dentina bovina, os quais foram alocados em três grupos (n = 4) de acordo com o tempo de incubação: 4, 7 e 10 dias. Todos os grupos experimentais foram expostos ao desafio cariogênico constante através da imersão em caldo BHI (Brain Heart Infusion) inoculados com Streptococcus mutans UA 159, enriquecidos com sacarose a 1% e incubados em atmosfera de anaerobiose a 37 °C. Após cada tempo experimental, analisaram-se as amostras através do teste de dureza transversal para obtenção dos dados de ΔS e dados de dureza em relação às profundidades de indentação (Figura 1).
Delineamento experimental do estudo; (A) Confecção da amostra: 1 e 2 - Obtenção do disco padronizado a partir do dente bovino; 3 e 4 - Corte na junção amelodentinária e obtenção de discos de dentina; 5 - Cobertura com esmalte de unha cosmético, exceto janela superior de 2 mm2; (B) Modelo microbiológico: Crescimentos de biofilme de S. mutans em BHI com 1% de sacarose pelos tempos experimentais de 4, 7 e 10 dias; (C) Corte transversal das amostras e posicionamento das indentações para leituras de dureza.
Preparo dos Espécimes
Doze dentes incisivos bovinos irrompidos e livres de falhas foram selecionados para o estudo e seccionados com auxílio de uma furadeira de bancada ao nível do terço médio para obtenção de discos padronizados (4 mm de diâmetro). Através de uma cortadeira de precisão, os mesmos foram seccionados transversalmente ao nível da junção amelodentinária, separando-se assim os discos de dentina. Os discos obtidos foram polidos e padronizados com a espessura de 1,5 mm. A dureza superficial dos discos selecionados foi de 65,07 ± 3,6 (kgf/mm2). Cada disco teve a superfície totalmente recoberta por esmalte de unha cosmético, exceto a porção superior, na qual uma janela de 2 mm2 de dentina permaneceu exposta. Os espécimes foram autoclavados e mantidos em atmosfera úmida (4 °C) até o uso99 van de Sande FH, Azevedo MS, Lund RG, Huysmans MC, Cenci MS. An in vitro biofilm model for enamel demineralization and antimicrobial dose-response studies. Biofouling. 2011 Oct;27(9):1057-63. PMid:22044385. http://dx.doi.org/10.1080/08927014.2011.625473.
http://dx.doi.org/10.1080/08927014.2011....
.
Processo de Indução de Cárie
As amostras foram dispostas em tubos Falcon codificados contendo 1 mL de BHI inoculado com Streptococcus mutans 159 UA e enriquecido com sacarose 1% (1,5 × 108 CFU/mL). Os espécimes foram incubados em jarras de anaerobiose sob temperatura de 37 °C por até 4, 7 ou 10 dias. A renovação do meio foi realizada a cada 24 h, e o pH de cada meio de cultura descartado foi verificado para cada grupo (4,13 ± 0,25).
Análise da Perda de Dureza
Após o período experimental de cada grupo, os discos de dentina foram coletados do tubo Falcon e delicadamente limpos com escova dental de cerdas macias. As amostras foram seccionadas de forma perpendicular ao centro da superfície de dentina exposta, usando uma cortadeira de precisão. Todo o processo ocorreu sob refrigeração. As metades de cada amostra foram embutidas em tubos de policloreto de vinila (PVC) com auxílio de resina epóxi e polidas com lixas d’água de 600, 1.200, 1.500 e 2.000, através da utilização de uma politriz. O ensaio de microdureza transversal foi realizado através de um microdurômetro (Future-Tech FM) com indentação do tipo Knoop, com 5 gramas de carga por 5 segundos. Foram realizadas 14 indentações, divididas em 2 colunas com distância de 100 µm entre elas, iniciadas a partir da superfície externa da lesão (Figura 1), segundo as profundidades de 10, 20, 30, 40, 50, 100, 150 µm. A perda mineral integrada foi calculada através da subtração do perfil de dureza desmineralizado (Knoop Hardness Number, kgf/mm2) a partir do perfil hígido de cada amostra, como previamente descrito1717 Sousa RP, Zanin IC, Lima JP, Vasconcelos SM, Melo MA, Beltrao HC, et al. In situ effects of restorative materials on dental biofilm and enamel demineralisation. J Dent. 2009 Jan;37(1):44-51. PMid:19026481. http://dx.doi.org/10.1016/j.jdent.2008.08.009.
http://dx.doi.org/10.1016/j.jdent.2008.0...
.
Análise Estatística
Os dados de perda de dureza integrada foram analisados de acordo com os pressupostos de homogeneidade e normalidade1818 Box GE, Hunter WG, Hunter JS. Statistics for experimenters:: an introduction to design, data analysis and model building. New York: Wiley; 1978. e comparados por meio de Análise de Variância de uma via (ANOVA), seguido do teste Tukey, utilizando-se o programa estatístico SPSS V.20 (IBM, USA), ambos com significância de 5%.
RESULTADO
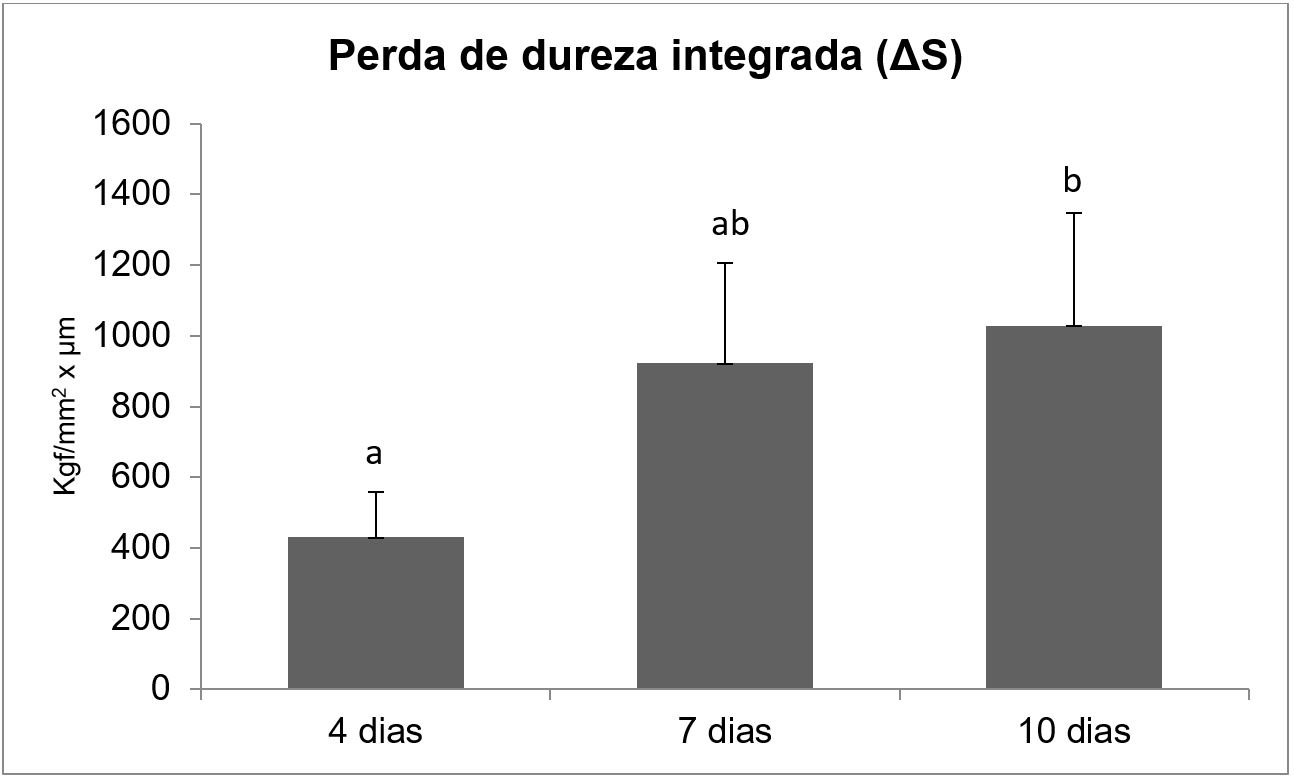
Os dados de perda de dureza integrada estão na Figura 2. Observou-se maior perda de dureza integrada para os tempos experimentais de 7 e 10 dias e não houve diferença entre esses dois períodos (p = 0,853). Foram encontradas diferenças entre os tempos de 4 e 10 dias (p = 0,034).
Perda de dureza integrada (ΔS = média + desvio-padrão) para cada tempo experimental in vitro. Letras diferentes indicam diferença estatística (p < 0,05).
Analisando-se os dados brutos de perda de dureza em relação à profundidade de indentação pôde-se observar, considerando todas as profundidades avaliadas, que a perda de dureza em dentina parece aumentar conforme o número de dias, ou seja, parece ser crescente do grupo 4 dias para os grupos 7 e 10 dias. A perda de dureza encontrada nos grupos 7 e 10 dias estendeu-se desde a superfície da lesão até a profundidade de 40-100 μm, conforme pode-se analisar na Figura 3. No entanto, o grupo experimental de 10 dias demostrou perda de dureza além dessa profundidade, alcançando a totalidade da profundidade mensurada no espécime.
Relação do teste de microdureza Knoop em relação à profundidade de indentação na lesão cariosa induzida in vitro.
DISCUSSÃO
O presente estudo estabeleceu um modelo de monocultura que permite o desenvolvimento de cárie em dentina in vitro de forma padronizada, sendo útil em estudos voltados a desmineralização e remineralizarão. Inúmeros são os modelos para o desenvolvimento de cárie in vitro, entre os quais destacam-se os modelos de géis acidificados, ciclagem de pH1313 Marquezan M, Corrêa FN, Sanabe ME, Rodrigues Filho LE, Hebling J, Guedes-Pinto AC, et al. Artificial methods of dentine caries induction: a hardness and morphological comparative study. Arch Oral Biol. 2009 Dec;54(12):1111-7. PMid:19878926. http://dx.doi.org/10.1016/j.archoralbio.2009.09.007.
http://dx.doi.org/10.1016/j.archoralbio....
e modelos microbiológicos de microcosmos, consórcios e de monocultura, como o modelo usado no presente estudo1919 McBain AJ. Chapter 4: in vitro biofilm models: an overview. Adv Appl Microbiol. 2009;69:99-132. PMid:19729092. http://dx.doi.org/10.1016/S0065-2164(09)69004-3.
http://dx.doi.org/10.1016/S0065-2164(09)...
20 Sissons CH. Artificial dental plaque biofilm model systems. Adv Dent Res. 1997 Apr;11(1):110-26. PMid:9524448. http://dx.doi.org/10.1177/08959374970110010201.
http://dx.doi.org/10.1177/08959374970110...
-2121 Steiner-Oliveira C, Rodrigues LKA, Zanin ICJ, Carvalho CL, Kamiya RU, Hara AT, et al. An in vitro microbial model associated with sucrose to produce dentin caries lesions. Cent Eur J Biol. 2011 Jun;6(3):414-21. http://dx.doi.org/10.2478/s11535-011-0011-2.
http://dx.doi.org/10.2478/s11535-011-001...
. Dentre os modelos vigentes, modelos microbiológicos são aqueles que melhor mimetizam o processo de cárie natural1313 Marquezan M, Corrêa FN, Sanabe ME, Rodrigues Filho LE, Hebling J, Guedes-Pinto AC, et al. Artificial methods of dentine caries induction: a hardness and morphological comparative study. Arch Oral Biol. 2009 Dec;54(12):1111-7. PMid:19878926. http://dx.doi.org/10.1016/j.archoralbio.2009.09.007.
http://dx.doi.org/10.1016/j.archoralbio....
. Modelos de biofilme simplificados que utilizam uma só espécie bacteriana parecem ser úteis em casos em que seja necessária uma análise rápida dos resultados, e com baixo custo de implementação, quando comparados aos modelos mais complexos, tais como de microcosmos ou de consórcios de bactérias1919 McBain AJ. Chapter 4: in vitro biofilm models: an overview. Adv Appl Microbiol. 2009;69:99-132. PMid:19729092. http://dx.doi.org/10.1016/S0065-2164(09)69004-3.
http://dx.doi.org/10.1016/S0065-2164(09)...
.
O modelo de biofilme escolhido mostrou-se adequado para desenvolver lesões artificiais de dentina e, portanto, a hipótese deste estudo foi aceita. A condição cariogênica estabelecida proporcionou perda de dureza integrada para todos os tempos experimentais. Ao fim do primeiro tempo experimental observou-se uma menor desmineralização, principalmente localizada nas áreas mais superficiais (até 40 µm), o que vai ao encontro de estudos com modelos microbiológicos previamente descritos na literatura1313 Marquezan M, Corrêa FN, Sanabe ME, Rodrigues Filho LE, Hebling J, Guedes-Pinto AC, et al. Artificial methods of dentine caries induction: a hardness and morphological comparative study. Arch Oral Biol. 2009 Dec;54(12):1111-7. PMid:19878926. http://dx.doi.org/10.1016/j.archoralbio.2009.09.007.
http://dx.doi.org/10.1016/j.archoralbio....
,2222 Maske TT, Nascimento CN, van de Sande FH, Azevedo MS, Oliveira EF, Cenci MS. The effect of non-restorative treatments on the progression of artificial dentine caries lesions underneath enamel. Rev Odonto Ciênc. 2015 Jun;29(2):40-5. http://dx.doi.org/10.15448/1980-6523.2014.2.12753.
http://dx.doi.org/10.15448/1980-6523.201...
. Aos 7 dias observou-se perda de dureza em profundidade até aproximadamente 100 μm, caracterizando o desenvolvimento de lesão artificial de cárie, uma vez que a partir dessa profundidade foram observados valores de dureza correspondentes a superfícies hígidas (~60 kgf/mm2). Após 10 dias de experimento foi possível observar lesões mais profundas, alcançando 150 μm. Como foram observadas áreas pontuais de erosão superficial nessas amostras, a leitura até profundidades maiores foi descontinuada.
Conforme discutido acima, sugere-se que o tempo mais adequado para estudos de des- e remineralização corresponde a 7 dias, uma vez que ao fim desse tempo experimental obteve-se perda de dureza integrada semelhante a dos 10 dias, porém com menor profundidade de lesão. Além disso, esse tempo experimental não demonstrou a presença de lesões de erosão superficial. A partir dessa condição cariogênica torna-se possível induzir lesões subsuperficias de dentina padronizadas in vitro e, a partir disso, realizar estudos de ganho e perda mineral, assim como outros já executados para avaliar o efeito preventivo de agentes contendo flúor2323 Preston KP, Smith PW, Higham SM. The influence of varying fluoride concentrations on in vitro remineralisation of artificial dentinal lesions with differing lesion morphologies. Arch Oral Biol. 2008 Jan;53(1):20-6. PMid:17920030. http://dx.doi.org/10.1016/j.archoralbio.2007.08.001.
http://dx.doi.org/10.1016/j.archoralbio....
,2424 Okuyama K, Nakata T, Pereira PN, Kawamoto C, Komatsu H, Sano H. Prevention of artificial caries: effect of bonding agent, resin composite and topical fluoride application. Oper Dent. 2006 Jan-Feb;31(1):135-42. PMid:16536205. http://dx.doi.org/10.2341/0361-7734(2006)31[135:POACEO]2.0.CO;2.
http://dx.doi.org/10.2341/0361-7734(2006...
e outros tratamentos2525 Tantbirojn D, Feigal RJ, Ko CC, Versluis A. Remineralized dentin lesions induced by glass ionomer demonstrate increased resistance to subsequent acid challenge. Quintessence Int. 2006 Apr;37(4):273-81. PMid:16594358., porém em um ambiente mais semelhante ao que ocorre na cavidade oral.
Embora os resultados obtidos neste estudo tenham ido ao encontro da hipótese inicial proposta, os autores reconhecem a presença de limitações, como o número de amostras por grupo, como também as inerentes ao modelo simplificado usado, por esse não possuir a capacidade de mimetizar todos os aspectos da cavidade oral e do processo cárie, como ocorre em modelos complexos com utilização de inóculos de microcosmos. Outra limitação do estudo é a descontinuação da análise em profundidades maiores que 150 µm no grupo experimental de 10 dias. Esse fato levou a uma subestimação dos valores de perda mineral para o respectivo tempo experimental. No entanto, o modelo simplificado apresentado ainda parece ser mais representativo que modelos de desenvolvimento de cárie artificiais que utilizam somente géis ácidos ou ciclagem de pH88 Tang G, Yip H-K, Cutress TW, Samaranayake LP. Artificial mouth model systems and their contribution to caries research: a review. J Dent. 2003 Mar;31(3):161-71. PMid:12726700. http://dx.doi.org/10.1016/S0300-5712(03)00009-5.
http://dx.doi.org/10.1016/S0300-5712(03)...
,2020 Sissons CH. Artificial dental plaque biofilm model systems. Adv Dent Res. 1997 Apr;11(1):110-26. PMid:9524448. http://dx.doi.org/10.1177/08959374970110010201.
http://dx.doi.org/10.1177/08959374970110...
.
Como prospectos futuros a pesquisas relacionadas à utilização desse modelo destacam-se as possibilidades de investigação de materiais dentários com propriedades antimicrobianas ou anticariogênicas (efeito remineralizador), com relação à possibilidade de adesão microbiana e seu envelhecimento, e, principalmente, de estudos de remineralização e desmineralização envolvendo o substrato dentinário previamente desmineralizado.
CONCLUSÃO
O modelo microbiano investigado mostrou-se adequado para o desenvolvimento de lesões artificiais de dentina, sendo uma ferramenta útil para estudos no campo da cariologia. Dentre os tempos experimentais analisados, o período de 7 dias mostrou-se apropriado para desenvolvimento de lesões subsuperficiais simuladas in vitro.
AGRADECIMENTOS
Os autores gostariam de agradecer à Carmem Lúcia Machado Lopes, técnica do Laboratório de Microbiologia da Universidade Federal de Pelotas, pelo suporte aos experimentos descritos nesse manuscrito.
REFERÊNCIAS
-
1Maske TT, van de Sande FH, Arthur RA, Huysmans MCDNJM, Cenci MS. In vitro biofilm models to study dental caries: a systematic review. Biofouling. 2017 Sep;33(8):661-75. PMid:28792234. http://dx.doi.org/10.1080/08927014.2017.1354248
» http://dx.doi.org/10.1080/08927014.2017.1354248 -
2Zero DT, Fontana M, Martinez-Mier EA, Ferreira-Zandona A, Ando M, Gonzalez-Cabezas C, et al. The biology, prevention, diagnosis and treatment of dental caries: scientific advances in the United States. J Am Dent Assoc. 2009 Sep;140(Suppl 1):25S-34S. PMid:19723928. http://dx.doi.org/10.14219/jada.archive.2009.0355
» http://dx.doi.org/10.14219/jada.archive.2009.0355 -
3Sheiham A, James WP. Diet and dental caries: the pivotal role of free sugars reemphasized. J Dent Res. 2015 Oct;94(10):1341-7. PMid:26261186. http://dx.doi.org/10.1177/0022034515590377
» http://dx.doi.org/10.1177/0022034515590377 -
4Moynihan P. Sugars and dental caries: evidence for setting a recommended threshold for intake. Adv Nutr. 2016 Jan;7(1):149-56. PMid:26773022. http://dx.doi.org/10.3945/an.115.009365
» http://dx.doi.org/10.3945/an.115.009365 -
5Moynihan PJ, Kelly SA. Effect on caries of restricting sugars intake: systematic review to inform WHO guidelines. J Dent Res. 2014 Jan;93(1):8-18. PMid:24323509. http://dx.doi.org/10.1177/0022034513508954
» http://dx.doi.org/10.1177/0022034513508954 -
6Campos PH, Sanabe ME, Rodrigues JA, Duarte DA, Santos MT, Guare RO, et al. Different bacterial models for in vitro induction of non-cavitated enamel caries-like lesions: Microhardness and polarized light miscroscopy analyses. Microsc Res Tech. 2015 Jun;78(6):444-51. PMid:25783414. http://dx.doi.org/10.1002/jemt.22493
» http://dx.doi.org/10.1002/jemt.22493 -
7Rudney JD, Chen R, Lenton P, Li J, Li Y, Jones RS, et al. A reproducible oral microcosm biofilm model for testing dental materials. J Appl Microbiol. 2012 Dec;113(6):1540-53. PMid:22925110. http://dx.doi.org/10.1111/j.1365-2672.2012.05439.x
» http://dx.doi.org/10.1111/j.1365-2672.2012.05439.x -
8Tang G, Yip H-K, Cutress TW, Samaranayake LP. Artificial mouth model systems and their contribution to caries research: a review. J Dent. 2003 Mar;31(3):161-71. PMid:12726700. http://dx.doi.org/10.1016/S0300-5712(03)00009-5
» http://dx.doi.org/10.1016/S0300-5712(03)00009-5 -
9van de Sande FH, Azevedo MS, Lund RG, Huysmans MC, Cenci MS. An in vitro biofilm model for enamel demineralization and antimicrobial dose-response studies. Biofouling. 2011 Oct;27(9):1057-63. PMid:22044385. http://dx.doi.org/10.1080/08927014.2011.625473
» http://dx.doi.org/10.1080/08927014.2011.625473 -
10Wong L, Sissions CH. A comparison of human dental plaque microcosm biofilms grown in an undefined medium and a chemically defined artificial saliva. Arch Oral Biol. 2001 Jun;46(6):477-86. PMid:11311195. http://dx.doi.org/10.1016/S0003-9969(01)00016-4
» http://dx.doi.org/10.1016/S0003-9969(01)00016-4 -
11Botelho JN, Villegas-Salinas M, Troncoso-Gajardo P, Giacaman RA, Cury JA. Enamel and dentine demineralization by a combination of starch and sucrose in a biofilm: caries model. Braz Oral Res. 2016 May;30(1):1-8. PMid:27223133. http://dx.doi.org/10.1590/1807-3107BOR-2016.vol30.0052
» http://dx.doi.org/10.1590/1807-3107BOR-2016.vol30.0052 -
12Fernández CE, Tenuta LM, Cury JA. Validation of a cariogenic biofilm model to evaluate the effect of fluoride on enamel and root dentine demineralization. PLoS One. 2016 Jan;11(1):e0146478. PMid:26731743. http://dx.doi.org/10.1371/journal.pone.0146478
» http://dx.doi.org/10.1371/journal.pone.0146478 -
13Marquezan M, Corrêa FN, Sanabe ME, Rodrigues Filho LE, Hebling J, Guedes-Pinto AC, et al. Artificial methods of dentine caries induction: a hardness and morphological comparative study. Arch Oral Biol. 2009 Dec;54(12):1111-7. PMid:19878926. http://dx.doi.org/10.1016/j.archoralbio.2009.09.007
» http://dx.doi.org/10.1016/j.archoralbio.2009.09.007 -
14Giacaman RA, Campos P, Munoz-Sandoval C, Castro RJ. Cariogenic potential of commercial sweeteners in an experimental biofilm caries model on enamel. Arch Oral Biol. 2013 Sep;58(9):1116-22. PMid:23631998. http://dx.doi.org/10.1016/j.archoralbio.2013.03.005
» http://dx.doi.org/10.1016/j.archoralbio.2013.03.005 -
15Muñoz-Sandoval C, Munoz-Cifuentes MJ, Giacaman RA, Ccahuana-Vasquez RA, Cury JA. Effect of bovine milk on Streptococcus mutans biofilm cariogenic properties and enamel and dentin demineralization. Pediatr Dent. 2012 Nov-Dec;34(7):e197-201. PMid:23265155.
-
16Cavalcanti YW, Bertolini MM, da Silva WJ, Del-Bel-Cury AA, Tenuta LM, Cury JA. A three-species biofilm model for the evaluation of enamel and dentin demineralization. Biofouling. 2014;30(5):579-88. PMid:24730462. http://dx.doi.org/10.1080/08927014.2014.905547
» http://dx.doi.org/10.1080/08927014.2014.905547 -
17Sousa RP, Zanin IC, Lima JP, Vasconcelos SM, Melo MA, Beltrao HC, et al. In situ effects of restorative materials on dental biofilm and enamel demineralisation. J Dent. 2009 Jan;37(1):44-51. PMid:19026481. http://dx.doi.org/10.1016/j.jdent.2008.08.009
» http://dx.doi.org/10.1016/j.jdent.2008.08.009 -
18Box GE, Hunter WG, Hunter JS. Statistics for experimenters:: an introduction to design, data analysis and model building. New York: Wiley; 1978.
-
19McBain AJ. Chapter 4: in vitro biofilm models: an overview. Adv Appl Microbiol. 2009;69:99-132. PMid:19729092. http://dx.doi.org/10.1016/S0065-2164(09)69004-3
» http://dx.doi.org/10.1016/S0065-2164(09)69004-3 -
20Sissons CH. Artificial dental plaque biofilm model systems. Adv Dent Res. 1997 Apr;11(1):110-26. PMid:9524448. http://dx.doi.org/10.1177/08959374970110010201
» http://dx.doi.org/10.1177/08959374970110010201 -
21Steiner-Oliveira C, Rodrigues LKA, Zanin ICJ, Carvalho CL, Kamiya RU, Hara AT, et al. An in vitro microbial model associated with sucrose to produce dentin caries lesions. Cent Eur J Biol. 2011 Jun;6(3):414-21. http://dx.doi.org/10.2478/s11535-011-0011-2
» http://dx.doi.org/10.2478/s11535-011-0011-2 -
22Maske TT, Nascimento CN, van de Sande FH, Azevedo MS, Oliveira EF, Cenci MS. The effect of non-restorative treatments on the progression of artificial dentine caries lesions underneath enamel. Rev Odonto Ciênc. 2015 Jun;29(2):40-5. http://dx.doi.org/10.15448/1980-6523.2014.2.12753
» http://dx.doi.org/10.15448/1980-6523.2014.2.12753 -
23Preston KP, Smith PW, Higham SM. The influence of varying fluoride concentrations on in vitro remineralisation of artificial dentinal lesions with differing lesion morphologies. Arch Oral Biol. 2008 Jan;53(1):20-6. PMid:17920030. http://dx.doi.org/10.1016/j.archoralbio.2007.08.001
» http://dx.doi.org/10.1016/j.archoralbio.2007.08.001 -
24Okuyama K, Nakata T, Pereira PN, Kawamoto C, Komatsu H, Sano H. Prevention of artificial caries: effect of bonding agent, resin composite and topical fluoride application. Oper Dent. 2006 Jan-Feb;31(1):135-42. PMid:16536205. http://dx.doi.org/10.2341/0361-7734(2006)31[135:POACEO]2.0.CO;2
» http://dx.doi.org/10.2341/0361-7734(2006)31[135:POACEO]2.0.CO;2 -
25Tantbirojn D, Feigal RJ, Ko CC, Versluis A. Remineralized dentin lesions induced by glass ionomer demonstrate increased resistance to subsequent acid challenge. Quintessence Int. 2006 Apr;37(4):273-81. PMid:16594358.
Datas de Publicação
-
Publicação nesta coleção
22 Fev 2018 -
Data do Fascículo
Jan-Feb 2018
Histórico
-
Recebido
17 Jul 2017 -
Aceito
24 Jan 2018