Resumos
O feijão (Phaseolus vulgaris L.) é de grande expressão alimentícia. A emergência da cultura é dependente de água e considerada a fase mais crítica. Os objetivos deste trabalho foram simular a deficiência de água no início da germinação em laboratório, em sementes de feijão 'Pérola', utilizando-se: manitol, CaCl2, MgCl2 e NaCl em potenciais de 0; -0,3; -0,6; -0,9 e - 1,2 MPa, estabelecidos pela equação de Van't Hoff e avaliar o perfil eletroforético de proteínas totais solúveis por meio de SDS-PAGE. Foram avaliados: germinação, classificação de vigor, massa seca de raiz e de parte aérea e resposta diferencial de expressão de proteínas. O delineamento experimental foi inteiramente casualizado. Os dados foram analisados pela aplicação do teste F, para análise de variância, regressão polinomial para os níveis de potencial osmóticos para cada uma das variáveis fisiológicas estudadas. O bandeamento eletroforético foi avaliado visualmente por imagem dos géis. A simulação do estresse permitiu avaliar a drasticidade do NaCl em todos os parâmetros avaliados e a ausência de proteínas de baixo peso molecular neste osmótico. As proteínas de 110 e 30 kDa foram indicativas de estresse hídrico, mas não do salino.
Phaseolus vulgaris L.; deficiência de água; HSPs
Snap-beans (Phaseolus vulgaris L.) have a high nutritionally value. Successful seedling emergence is dependent on the availability of water and is considered the most critical phase in plant development. The objectives of this work were to simulate water deficiency at the beginning of the germination period. Snap-bean seeds of the variety 'Pérola' were submitted to osmotic stress under laboratory conditions. Mannitol, CaCl2, MgCl2 and NaCl were used to develop five degrees of osmotic potential: 0, -0.3, -0.6, -0.9 and -1.2 MPa. Van't Hoff's equation was used to calculate the osmotic potential. The protein pattern of the total soluble proteins after electrophoresis was evaluated with SDS-PAGE. The response parameters were evaluated including the germination, the vigour classification, the root dry weight, the shoot dry weight and the resultant differential protein expression. The experimental design was completely randomised. Data were analysed using the F test (ANOVA), and polynomial regression was used for the osmotic potential levels for each parameter. The protein banding pattern was evaluated using gel imaging. The simulation of a water deficiency resulted in the perception of a stress and a subsequent response to NaCl in all of the parameters that were evaluated. The harsh effects of the NaCl were validated as the lack of the expression of low molecular weight proteins. Proteins with molecular weights of 110 and 30 kDa were indicative of water stress but not of salinity.
Phaseolus vulgaris L.; water deficiency; HSPs
PRODUÇÃO VEGETAL
Estresse hídrico com diferentes osmóticos em sementes de feijão e expressão diferencial de proteínas durante a germinação
Differential protein expression during germination as a result of a water deficit associated with variable osmotic pressure in snap-beans
Danielle Letícia Martins CoelhoI; Edna Antônia Torquato de AgostiniI; Luciana Machado GuabertoI; Nelson Barbosa Machado NetoII; Ceci Castilho CustódioIII,* * Autor para correspondência. E-mail: ceci@unoeste.br License information: This is an open-access article distributed under the terms of the Creative Commons Attribution License, which permits unrestricted use, distribution, and reproduction in any medium, provided the original work is properly cited.
IPrograma de Pós-graduação em Agronomia, Universidade do Oeste Paulista, Presidente Prudente, São Paulo, Brasil
IILaboratório de Cultura de Tecidos, Faculdade de Ciências Agrárias, Universidade do Oeste Paulista, Presidente Prudente, São Paulo, Brasil
IIIDepartamento de Biologia Vegetal e Fitossanidade, Faculdade de Ciências Agrárias, Universidade do Oeste Paulista, Rod. Raposo Tavares, km 572, 19067-175, Presidente Prudente, São Paulo, Brasil
RESUMO
O feijão (Phaseolus vulgaris L.) é de grande expressão alimentícia. A emergência da cultura é dependente de água e considerada a fase mais crítica. Os objetivos deste trabalho foram simular a deficiência de água no início da germinação em laboratório, em sementes de feijão 'Pérola', utilizando-se: manitol, CaCl2, MgCl2 e NaCl em potenciais de 0; -0,3; -0,6; -0,9 e - 1,2 MPa, estabelecidos pela equação de Van't Hoff e avaliar o perfil eletroforético de proteínas totais solúveis por meio de SDS-PAGE. Foram avaliados: germinação, classificação de vigor, massa seca de raiz e de parte aérea e resposta diferencial de expressão de proteínas. O delineamento experimental foi inteiramente casualizado. Os dados foram analisados pela aplicação do teste F, para análise de variância, regressão polinomial para os níveis de potencial osmóticos para cada uma das variáveis fisiológicas estudadas. O bandeamento eletroforético foi avaliado visualmente por imagem dos géis. A simulação do estresse permitiu avaliar a drasticidade do NaCl em todos os parâmetros avaliados e a ausência de proteínas de baixo peso molecular neste osmótico. As proteínas de 110 e 30 kDa foram indicativas de estresse hídrico, mas não do salino.
Palavras-chave:Phaseolus vulgaris L., deficiência de água, HSPs.
ABSTRACT
Snap-beans (Phaseolus vulgaris L.) have a high nutritionally value. Successful seedling emergence is dependent on the availability of water and is considered the most critical phase in plant development. The objectives of this work were to simulate water deficiency at the beginning of the germination period. Snap-bean seeds of the variety 'Pérola' were submitted to osmotic stress under laboratory conditions. Mannitol, CaCl2, MgCl2 and NaCl were used to develop five degrees of osmotic potential: 0, -0.3, -0.6, -0.9 and -1.2 MPa. Van't Hoff's equation was used to calculate the osmotic potential. The protein pattern of the total soluble proteins after electrophoresis was evaluated with SDS-PAGE. The response parameters were evaluated including the germination, the vigour classification, the root dry weight, the shoot dry weight and the resultant differential protein expression. The experimental design was completely randomised. Data were analysed using the F test (ANOVA), and polynomial regression was used for the osmotic potential levels for each parameter. The protein banding pattern was evaluated using gel imaging. The simulation of a water deficiency resulted in the perception of a stress and a subsequent response to NaCl in all of the parameters that were evaluated. The harsh effects of the NaCl were validated as the lack of the expression of low molecular weight proteins. Proteins with molecular weights of 110 and 30 kDa were indicative of water stress but not of salinity.
Key words:Phaseolus vulgaris L., water deficiency, HSPs.
Introdução
O feijão é considerado uma cultura de ampla adaptação climática, importante para a nutrição da população brasileira e fonte de renda dos pequenos, médios e grandes produtores. No entanto, o solo nem sempre oferece ambiente ótimo para a germinação das sementes, porque, quando ocorre deficiência hídrica, subentende-se que o solo apresenta potenciais hídricos que dificultam a absorção da água necessária para a germinação (MACHADO NETO et al., 2006).
No campo, o conteúdo de água do solo entre a capacidade de campo (CC) e o ponto de murcha permanente (PMP) foi definido como água disponível (AD) para plantas (TORMENA et al., 1999), sendo considerados para a CC valores entre -0,01 a -0,2 MPa e para o PMP, valores próximos de -1,5 MPa (TAIZ; ZEIGER, 2004).
A planta de feijão possui grande sensibilidade à falta de água após a semeadura; valores, no solo, de -0,15MPa induzem a plântula aos primeiros sintomas de deficiência na folha primária, enquanto -0,35 MPa podem reduzir drasticamente a germinação e a elongação de células; contudo, mesmo após seis dias em condições de deficiência, a -1,2 MPa, havia germinação, em laboratório (MACHADO NETO et al., 2006; CUSTÓDIO et al., 2009). Em condições de plena disponibilidade de água no solo, as sementes, principalmente as mais secas, podem absorver água rapidamente, ocasionando rupturas em seus tecidos, com consequentes prejuízos à germinação (BRAGA et al., 1999).
O metabolismo da planta é prejudicado pela deficiência de água ou acúmulo de sal nos solos. Em sementes de feijão, o vigor é mais afetado do que a germinação, quando submetidas a tratamento com NaCl (PAULA et al., 1994; MACHADO NETO et al., 2004). Em soja, o índice de germinação, de vigor das sementes e de massa seca total diminuiu quando as sementes foram expostas à deficiência induzida por solução contendo MgCl2 (MORAES; MENESES, 2003). O agente osmótico manitol causou reduções na germinação, no comprimento e massa seca de parte aérea e de raízes, e de plântulas normais de feijão em potenciais de -0,4 a -0,6 MPa. Porém, entre os potenciais hídricos de -0,001; -0,01 e -0,2 MPa, não foram constatadas diferenças na normalidade destas plântulas e nem em relação à matéria seca (BRAGA et al., 1999). O CaCl2 tem como limite máximo de tolerância o potencial de -1,2 MPa para a germinação; já em soluções de NaCl, KCl e manitol, as sementes não germinam nesses potenciais, comprovando-se que essas soluções foram mais restritivas que a de CaCl2 (MACHADO NETO et al., 2006).
A água constitui a matriz em que ocorre a maioria dos processos bioquímicos e fisiológicos, ativando, no desenvolvimento da plântula, processos essenciais, apresentando profunda influência na estrutura e nas propriedades das proteínas, das membranas, dos ácidos nucleicos e de outros constituintes celulares (BRAY, 1995; TAIZ; ZEIGER, 2004). Estresses ambientais, como alta temperatura, deficiência hídrica, estresses salinos e até mesmo infecções por patógenos estão direta e intimamente ligados a alterações no padrão de proteínas específicas, em função do tipo de estresse (ARAÚJO et al., 1998; MACHADO NETO et al., 2001).
Diversas podem ser as respostas de tolerância dos organismos aos estresses como a resposta diferencial de cultivares (CUSTÓDIO et al., 2002; MACHADO NETO et al., 2004; TEIXEIRA et al., 2008), via ativação (NEPOMUCENO et al., 2001; VERDOY et al., 2004) ou desativação (NEPOMUCENO et al., 2000) de genes que codificarão proteínas específicas, finalizando com diversas respostas fisiológicas, metabólicas e de desenvolvimento. Entre estas respostas ao estresse, encontramos fatores de transcrição (ZHU, 2001), proteínas de diversas classes, como as BiP (Binding Protein) (KALINSKI et al., 1995), Peroxidases (SIEGEL, 1993), proteínas LEA (Late embryogenesis abundant protein) (VERDOY et al., 2004), proteínas ricas em prolina (PRPs) (VERDOY et al., 2004) e Proteínas de Choque Térmico (Heat Shock Protein - HSPs), as quais deveriam ser específicas ao estresse de calor, porém, também são sintetizadas na presença de estresse hídrico ou como resposta universal ao estresse (VIERLING, 1991), sendo encontradas desde em procariotos até em eucariotos.
Não existem estudos que comprovem completamente as funções fisiológicas das HSPs; entretanto, existem evidências consideráveis demonstrando que a termotolerância está correlacionada com a síntese e o acúmulo de HSPs (JINN et al., 1993; SCHIRMER et al., 1994; PARK et al., 1996; PRANDL et al., 1998; RISTIC et al., 1998; JOE et al., 2000; ARAÚJO et al., 2003). Ristic et al. (1991) e Wood et al. (1998) citam que existe uma variação considerável, nos testes realizados, entre indivíduos da mesma espécie e de espécies diferentes, em função dos pesos moleculares das HSPs, podendo ser classificadas como proteínas de baixo peso molecular (Low Molecular Weight - LMW HSPs), as quais normalmente não são detectadas na ausência de estresse térmico (BOSTON et al., 1996; WATERS et al., 1996), e de alto peso molecular (High Molecular Weight HMW HSPs) como as HSPs de 60, 70 e 90 kDa, que são indispensáveis e têm síntese progressiva durante o período de estresse (ARAÚJO et al., 1998). A última é encontrada em condições normais, mas sua síntese é aumentada na presença de estresses (VIERLING, 1991).
HSPs, entre 100 a 110 kDa, são sintetizadas por plantas submetidas ao estresse, e essa síntese é exclusiva das primeiras horas, não sendo expressas em condições normais de desenvolvimento (VIERLING, 1991). Em plântulas de arroz, Pareek et al. (1995) constataram que as bandas de 90 e 104 kDa não foram encontradas em condições normais, sendo sintetizadas a partir dos estresses salino, hídrico, baixa temperatura e aplicação de ácido abscísico.
Dentro das HSPs ainda existe um grupo especial de proteínas que se destinam à recuperação de proteínas danificadas, chamadas de moléculas 'chaperonas', apresentando atividades voltadas para interagir com proteínas desnaturadas para facilitar a conformação correta, designadas à prevenção e manutenção de agregação ou desnaturação proteica, promovendo a renaturação, funções importantes em células que foram submetidas a estresses térmicos (BOSTON et al., 1996; BORGES; RAMOS, 2005). Vierling (1991) e Wu et al. (1993) afirmam que as HSPs de 60, 70 e 90 kDa têm funções essenciais para facilitar processos importantes, sendo as primeiras a receber o nome de 'chaperonas' (CRAIG et al., 1993; SCHMITZ et al., 1996).
Este trabalho teve como objetivo simular deficiência de água em sementes de feijão, da cultivar 'Pérola', durante o início da germinação em laboratório, utilizando-se diferentes osmóticos: manitol, CaCl2, NaCl e MgCl2 em potenciais de 0; -0,3; -0,6; -0,9 e -1,2 MPa, estabelecidos pela equação de Van't Hoff (SALISBURY; ROSS, 1991). Foram avaliados parâmetros relacionados à germinação, classificação de vigor, massa seca de raiz e de parte aérea, massa seca total, relação raiz/parte aérea e, posteriormente, foi determinada a expressão diferencial de proteínas totais solúveis por meio de eletroforese (SDS-PAGE).
Material e métodos
O experimento foi realizado nos Laboratórios de Sementes e de Cultura de Tecidos Vegetais da Universidade do Oeste Paulista - Unoeste - localizados em Presidente Prudente, Estado de São Paulo. Foram utilizadas para o experimento sementes de feijão (Phaseolus vulgaris L.) 'Pérola', submetidas à germinação em diferentes potenciais osmóticos, simulando-se situações de estresse hídrico. Foram utilizados: manitol, CaCl2, MgCl2 e NaCl em potenciais de 0; -0,3; -0,6; -0,9 e -1,2 MPa, estabelecidos pela equação de Van't Hoff, citado por Salisbury e Ross (1991), ou seja: ψ os= -RTC, em que: ψ os= potencial osmótico (atm); R= constante geral dos gases perfeitos (8,32 J mol-1 K-1); T= temperatura (K); C= concentração (mol L-1) e T (K)= 273+T(ºC). As concentrações de NaCl foram corrigidas de acordo com a curva de calibração estabelecida por Braccini et al. (1996), ou seja: ψ os = 0,194699+0,750394C R2 = 0,9999, em que: ψ os=potencial osmótico (bar); C=concentração (g L-1) (Tabela 1).
O teste de germinação consistiu em colocar quatro repetições de 50 sementes, envolvidas entre três folhas de papel-toalha para germinação (Germitest), sendo duas como bases e uma para cobrir, umedecidas com 2,5 vezes a sua massa com as soluções já mencionadas. Em seguida, os rolos foram envolvidos em sacos de polietileno e mantidos em germinador à temperatura constante de 25ºC. A contagem foi realizada no sexto dia, computando-se as plântulas normais 'fortes' e normais 'fracas', anormais e as sementes mortas (BRASIL, 2009; NAKAGAWA, 1999), sendo expressa em porcentagem.
Foram consideradas plântulas normais 'fortes' as que não apresentaram pequenas irregularidades em quaisquer de suas estruturas essenciais, como sistema radicular; hipocótilo (rachaduras, lesões, necroses ou rachaduras cicatrizantes); epicótilo (pouco desenvolvido ou sem uma folha primária); cotilédone (faltando um ou sem uma folha primária) e aspecto geral da plântula (afilada, pouco desenvolvida ou curta e fraca) (NAKAGAWA, 1999). Para o resultado de germinação, considerou-se a porcentagem de plântulas normais (somatório de fortes e fracas) e para a classificação do vigor, apenas as normais fortes.
O desempenho das plântulas foi avaliado por outro teste, que consistiu de quatro repetições de dez sementes, envolvidas entre três folhas de papel-toalha para germinação (Germitest), sendo duas como base e uma para cobrir, umedecidas com 2,5 vezes a sua massa com as soluções já mencionadas, formando linha única a 10 cm da borda superior da folha. Em seguida, os rolos foram envolvidos em sacos de polietileno e mantidos em germinador à temperatura constante de 25ºC. A avaliação foi realizada no sexto dia, seccionando-se a parte aérea (sem os cotilédones) e a raiz das plântulas normais, que foram acondicionadas separadamente, em sacos de papel fino e, posteriormente, levadas para secar em estufa a 60ºC por 48 horas. Ao término da secagem, os materiais foram resfriados em dessecador e pesados em balança analítica com precisão de 0,001 g (NAKAGAWA, 1999). O cálculo da relação raiz/parte aérea foi efetuado com base nas massas.
O delineamento experimental foi inteiramente casualizado em um arranjo fatorial de 4 x 5 (agentes osmóticos x potenciais hídricos), com quatro repetições. O software SANEST (ZONTA et al., 1984) auxiliou na análise dos dados que consistiu em aplicação do teste F, para a análise de variância, regressão polinomial para os níveis de potencial osmóticos para cada uma das variáveis fisiológicas estudadas: porcentagem de germinação, classificação de vigor, massa seca da parte aérea e da raiz, massa seca total e relação raiz/parte aérea.
Para se determinar a resposta molecular aos tratamentos, foi utilizado o método de eletroforese SDS-PAGE. Uma fração de tecido, cinco hipocótilos, por repetição, das plântulas normais, obtidas no teste de germinação no sexto dia, foram macerados com nitrogênio líquido e colocados em tubos de ensaio com tampão de extração Tris-HCL (0,625 mM) pH 6,8, contendo, 2% duodecil sulfato de sódio (SDS); 20% glicerol e 5% 2-mercaptoetanol na proporção de 1:10 (p:v) de amostra de tecido vegetal para o tampão de extração. Os tubos foram agitados e mantidos por, no mínimo, 1 hora em temperatura ambiente e depois aquecidos de 3 a 5 min. até atingirem ebulição. Posteriormente, a solução foi centrifugada a 9.500 rpm por 10 min. O sobrenadante foi congelado em tubos Eppendorf. As proteínas foram quantificadas de acordo com Bradford (1976), sendo os valores plotados contra uma curva de calibração construída com albumina bovina a 0,5 g mL-1 na faixa de zero a 100 µg.
A eletroforese foi conduzida de acordo com Laemli (1970) em um sistema composto por um gel de corrida, contendo 12,5% de acrilamida-bisacrilamida (30:0,8), Tris Glicina SDS pH 8,8 e um gel de empilhamento com 2,5% de acrilamida-bisacrilamida, Tris HCl pH 6,8. A corrida de eletroforese SDS-PAGE foi realizada em cuba vertical ligada à fonte elétrica por 30 min. a 50V e 20 mA por 4 horas em condições refrigeradas. O tampão de corrida foi composto de Tris (25 mM) - Glicina (38 mM) - SDS (0,7 mM), pH 8,8. Alíquotas, contendo a mesma quantidade de proteína por tratamento (20 µg), foram colocadas por poço. Os géis foram fixados com isopropanol:ácido acético:água (4:1:5) por 30 min. e permaneceram em solução contendo 2% Coomassie Blue R250 até aparecerem as bandas de proteína.
Quando a coloração mostrou-se muito escura, o gel foi descorado com 10% de ácido acético. Posteriormente, foi realizada a foto documentação digital em transluminador, permitindo a captura, a visualização e o processamento de imagens de bandas protéicas reveladas nos géis.
A análise do padrão eletroforético de cada tratamento foi realizada por meio de comparação visual e detecção diferencial da presença/ausência de bandas.
Resultados e discussão
As diferentes concentrações das soluções, neste estudo, foram empregadas em analogia às condições de campo e, a partir dessa simulação, observou-se que a germinação reagiu de maneira diferencial, dependente da concentração de cada soluto (Figura 1A).
Pôde-se observar que o manitol manteve a germinação independente do potencial utilizado, assim como em Machado Neto et al. (2006) que, no entanto, observaram aumento de plântulas anormais, fato também ocorrido com Braga et al. (1999). O MgCl2 e o CaCl2 apresentaram ponto de máximo próximos (-0,35 e -0,36 MPa, respectivamente); todavia, o MgCl2 manteve a germinação no potencial de -1,2 MPa, enquanto que, neste nível, a germinação foi drasticamente menor para o CaCl2 e o NaCl.
O NaCl apresentou um ponto de máxima germinação calculado em -0,25 MPa. A partir daí houve redução na germinação, apresentando-se o menor resultado em -1,2 MPa (Figura 1A). Santos et al. (1992) e Braccini et al. (1998) relatam que, em sementes de soja, os estresses causados por NaCl, CaCl2 e Na2SO4 influenciaram negativamente a germinação e o vigor de sementes.
À medida que a restrição hídrica aumentou, o vigor, avaliado por meio da classificação de vigor, foi reduzido (Figura 1B), sendo este mais afetado nos potenciais -0,9 e -1,2 MPa, principalmente no osmótico NaCl, corroborando Moraes e Meneses (2003) e Machado Neto et al. (2004). O vigor de plântulas é sempre mais afetado do que a germinação, nesse osmótico, em várias espécies como feijão (PAULA et al., 1994), soja (SANTOS et al., 1996; MACHADO NETO et al., 2004) e pepino (TORRES et al., 2000).
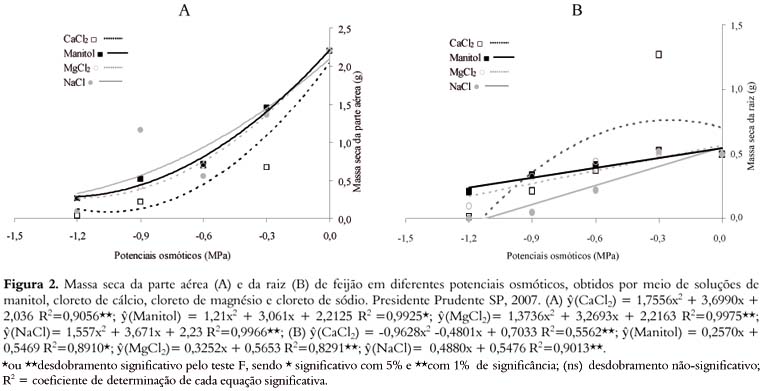
As massas secas de parte aérea e de raiz das plântulas sofreram interferência da diminuição de água. Ambas reduziram-se na presença dos osmóticos, como em Braccini et al. (1996), Moraes e Menezes (2003), Machado Neto et al. (2004), Costa et al. (2004), Machado Neto et al. (2006) e Custódio et al. (2009). Em relação à parte aérea, a solução de CaCl2, no potencial de -0,3 MPa, encontrou valores menores, quando comparada aos outros osmóticos e potenciais (Figura 2A), ocorrendo o contrário com a massa de raiz no mesmo potencial (Figura 2B), fato relacionado com a concentração de mitoses nas células da raiz, as quais poderiam estar sendo estimuladas pelo cálcio, pois as outras soluções apresentaram resultados análogos entre si (Figuras 2A e B).
Assim, ocorreu uma relação raiz/parte aérea máxima no osmótico CaCl2, enquanto os demais apresentaram relação estável com o aumento da deficiência de água (Figura 3B). O maior crescimento da raiz em detrimento da parte aérea foi observado principalmente no potencial -0,3 MPa, na presença de cálcio. Este íon (Ca2+) pode promover a modulação de processos celulares por meio de proteínas (calmodulinas), as quais, por sua vez, regulam uma cascata de eventos relacionados com as respostas das plantas a estresse biótico e abiótico (YANG; POOVAIAH, 2002), o que poderia ter potencializado a tendência de crescimento das raízes observada neste trabalho, nos maiores potenciais (-0,3 a -0,9 MPa, menor restrição de água).
Ocorreu redução na massa seca total (Figura 3A), da mesma forma que para Moraes e Meneses (2003). A solução, contendo NaCl, apresentou ponto de mínima calculado de -1,34 MPa, enquanto que o manitol, o CaCl2 e o MgCl2 tiveram pontos de mínima em potenciais menores (-1,54; -2,03 e -1,61 MPa, respectivamente), fato este, relacionado com a salinidade do NaCl (SANTOS et al., 1996, TORRES et al., 2000, MACHADO NETO et al., 2006).
Padrões de proteínas podem variar no número de bandas apresentadas em cada material ou espécie. Machado Neto et al. (2002) observaram diferentes padrões em espécies de Brachiaria variando de 12 bandas em Brachiaria jubata para seis bandas em B. nigropedata.
Amini et al. (2007) observaram que a mudança no padrão proteico de plântulas de tomate, em estresse salino in vitro, foi de apenas cinco proteínas pelo SDS-PAGE. Todavia, estes padrões, bem como os presentes no atual trabalho, foram revelados com Coomassie Blue R250, uma técnica que demonstra apenas proteínas em microgramas, o que não significa afirmar que apenas estas proteínas estejam presentes na amostra (ALFENAS, 1998).
O bandeamento variou de acordo com os osmóticos, mas foi praticamente estável com a diminuição do potencial hídrico. Bandas de proteínas, com peso molecular de 120, 100, 70, 50, 20, 15 e 11 kDa, extraídas de hipocótilos com seis dias, foram encontradas no potencial 0 MPa (água pura, Tabela 2) sendo o padrão proteico de plântulas não-estressadas, neste trabalho.
Os tratamentos com manitol e MgCl2 foram iguais nos perfis eletroforéticos, apresentando 16 bandas, as mesmas presentes em plântulas-controle (120, 100, 70, 50, 20, 15 e 11 kDa) mais as bandas diferenciadoras de 110, 90, 85, 65, 45, 40, 30, 25 e 18 kDa (Tabela 2), com correspondência de similaridade no comportamento de germinação (Figura 1A), massa seca de parte aérea e de raiz (Figura 2A e B), massa seca total (Figura 3A) e relação raiz/parte aérea (Figura 3B). As proteínas entre 90 e 60 e abaixo de 30 kDa parecem ter efeitos tanto de chaperonas como de funções basilares nas células vivas (SCHMITZ et al., 1996; BOSTON et al., 1996; KUMAR et al., 2004). A expressão das proteínas diferenciadoras, algumas descritas como chaperonas, pode ter refletido na melhor resposta fisiológica observada nestes osmóticos, em relação ao CaCl2 e NaCl, como, por exemplo, na germinação (Figura 1A) e na massa total de plântulas (Figura 3A) no potencial mais restritivo ao crescimento, -1,2 MPa.
As proteínas de 70 e 50 kDa foram expressas tanto em água como em condições de estresse. A proteína de 70 kDa poderia ser a HSP70 ou a BiP, que funcionaria como chaperona em condições desfavoráveis (KUMAR et al., 2004; KANG et al., 2005).
Houve a detecção de uma banda de 250 kDa no tratamento com CaCl2, que foi exclusiva dos menores potenciais (-0,9 e -1,2 MPa). A banda de 150 kDa foi encontrada nos tratamentos que contêm CaCl2 e NaCl (Tabela 2). Bandas de alto peso molecular (HMW HSP) estão presentes em diversas espécies quando ocorrem estresses (JOE et al., 2000; PAREEK et al., 1995; PARK et al., 1996; PRANDL et al., 1998; RISTIC et al., 1998).
Nas plântulas expostas ao NaCl não foram encontradas as bandas de 110, 30 e 20 kDa e, nos tratamentos com CaCl2, foram suprimidas as bandas de 120, 85, 45 e 40 kDa. Para ambos os osmóticos foram suprimidas as bandas de 100, 90, 65, 25, 18, 15 e 11 kDa (Tabela 2).
Como respostas ao estresse, independentemente do osmótico, houve a expressão de 11 bandas, sendo elas 250, 150, 110, 90, 85, 65, 45, 40, 30, 25 e 18 kDa e a supressão de três bandas do metabolismo normal, em comum, para o CaCl2 e o NaCl (100, 15 e 11 kDa), uma exclusiva para CaCl2 (120 kDa) e outra para o NaCl (20 kDa).
Neste trabalho, a presença de NaCl inibiu a expressão das bandas de 110, 100, 90, 65 e abaixo de 30 kDa, algumas de estresse e outras de metabolismo normal (100, 20 15 e 11 kDa) e que poderiam estar relacionadas ao desempenho inferior das sementes em todos os tratamentos contendo este osmótico (Figuras 1, 2 e 3).
As proteínas de 110 e 30 kDa foram expressas em condições de estresse hídrico (manitol, MgCl2 e CaCl2), mas não em estresse salino (NaCl) e água, podendo ser consideradas indicadoras de resposta ao estresse hídrico. Em Cucumis sativus, a expressão de uma proteína de 33,5 kDa foi relacionada à tolerância das plântulas ao estresse hídrico e ao frio, enquanto a ausência desta foi detectada apenas em plântulas não-submetidas aos estresses (KANG et al., 2005). Em arroz, Pareek et al. (1995) detectaram a presença de uma proteína de 104 kDa como resposta a diversos estresses, entre estes a salinidade, o que não se verificou neste trabalho. Em plântulas de tomate, cultivado em meio de cultura por 24 dias, em potenciais variando ente -0,17 a -0,67 MPa, cinco bandas proteicas foram encontradas, via SDS-PAGE, sendo 30, 62 e 75 kDa em raiz e 38 e 46 kDa em folhas, em resposta ao aumento de salinidade do meio (AMINI et al., 2007). Neste trabalho, foi detectada a expressão de duas proteínas de 45 e 40 kDa, ausentes nas plântulas-controle e expressas tanto em condições de salinidade quanto em estresse hídrico por manitol e MgCl2.
A ausência das proteínas de 100, 15 e 11 kDa, nas plântulas expostas a CaCl2 e NaCl, mas expressas em meio sem osmótico (água pura) e em ambiente contendo manitol ou MgCl2, poderia sugerir efeito destas na menor resposta fisiológica observada nos tratamentos contendo CaCl2 e NaCl (Tabela 2).
Conclusão
A simulação de deficiência hídrica, em laboratório, por meio dos osmóticos (manitol, CaCl2, MgCl2 e NaCl), permite a constatação dos efeitos do estresse, em plântulas de feijoeiro, pelo decréscimo dos parâmetros observados, e de que os tratamentos à base de NaCl foram os mais drásticos.
De acordo com o osmótico empregado, obtiveram-se expressões de proteínas diferentes, tanto de alto quanto de baixo peso molecular. As bandas de 70 e 50 kDa foram sintetizadas em todos os osmóticos empregados neste trabalho, sugerindo serem proteínas de função celular básica, presentes tanto em estresse hídrico como em condição normal.
A expressão de determinadas bandas é osmótico dependente, mas independente da concentração do mesmo. As proteínas de 110 e 30 kDa são indicativas de estresse hídrico, mas não do salino.
Received on August 6, 2008.
Accepted on November 3, 2008.
- ALFENAS, A. C. Eletroforese de isoenzimas e proteínas afins: fundamentos e aplicações em plantas e microrganismos. Viçosa: UFV, 1998.
- AMINI, F.; ESHANPOUR, A. A.; HOANG, Q. T.; SHIN, J. Sh. Protein pattern changes in tomato under in vitro salt stress. Russian Journal of Plant Physiology, v. 54, n. 4, p. 464-471, 2007.
- ARAÚJO, J. L. S.; MARGIS-PINHEIRO, M.; RUMJANEK, N. G. Proteínas de choque térmico e tolerância a altas temperaturas em plantas Seropédica: Embrapa Agrobiologia, 1998. (Documentos, 80).
- ARAÚJO, J. L. S.; RUMJANEK, N. G.; MARGIS-PINHEIRO, M. Small heat shock proteins genes are differentially expressed in distinct varieties of common bean. Brazilian Journal of Plant Physiology, v. 15, n. 1, p. 33-41, 2003.
- BORGES, J. C.; RAMOS, C. H. I. Protein folding assisted by chaperones. Protein & Peptide Letters, v. 12, n. 3, p. 257-261, 2005.
- BOSTON. R. S.; VIITANEN, V. P.; VIERLING. E. Molecular chaperones and proteins folding in plants. Plant Molecular Biology, v. 32, n. 1-2, p. 191-222, 1996.
- BRACCINI, A. L.; RUIZ, H. A.; BRACCINI, M. C. L.; REIS, M. S. Germinação e vigor de sementes de soja sob estresse hídrico induzido por soluções de cloreto de sódio, manitol e polietilenoglicol. Revista Brasileira de Sementes, v. 18, n. 1, p. 10-16, 1996.
- BRACCINI, A. L.; REIS, M. S.; SEDIYAMA, C. S.; SEDIYAMA, T.; ROCHA, V. S. Influência do potencial hídrico induzido por polietilenoglicol na qualidade fisiológica de sementes de soja. Pesquisa Agropecuária Brasileira, v. 33, n. 9, p. 1451-1459, 1998.
- BRADFORD, M. M. A rapid and sensitive method for the quantitation of microgram quantities of protein utilizing the principle of protein-dye binding. Analytical Biochemistry, v. 72, n. 1-2, p. 248-254, 1976.
- BRAGA, L. F.; SOUSA, M. P.; BRAGA, J. F.; SÁ, M. E. Efeito da disponibilidade hídrica do substrato na qualidade fisiológica de sementes de feijão. Revista Brasileira de Sementes, v. 21, n. 2, p. 95-102, 1999.
- BRASIL. Ministério da Agricultura. Regras para análises de sementes. Brasília: SNAD/DNDV/CLAV, 2009.
- BRAY, C. F. Biochemical processes during the osmopriming of seeds. In: KIGEL, J.; GALILI, G. (Ed.). Seed development and germination New York: Marcel Dekker, 1995. p. 767-789.
- COSTA, P.; CUSTÓDIO, C. C.; MACHADO NETO, N. B.; MARUBAYASHI, O. M. Estresse hídrico induzido por manitol em sementes de soja de diferentes tamanhos. Revista Brasileira de Sementes, v. 26, n. 1, p. 105-113, 2004.
- CRAIG, E. A.; GAMBILL, B. D.; NELSON, R. J. Heat shock proteins: molecular chaperones of proteins biogenesis. Microbiological Reviews, v. 57, n. 2, p. 402-414, 1993.
- CUSTÓDIO, C. C.; BOMFIM, D. C.; SATURNINO, S. M.; MACHADO NETO, N. B. Estresse por alumínio e por acidez em cultivares de soja. Scientia Agricola, v. 59, n. 1, p. 145-153, 2002.
- CUSTÓDIO, C. C.; SALOMÃO, G. R.; MACHADO NETO, N. B. Estresse hídrico na germinação e vigor de sementes de feijão submetidas a diferentes soluções osmóticas. Revista Ciência Agronômica, v. 40, n. 4, p. 617-623, 2009.
- JINN, T. L.; WU, S.-H.; YEH, C.-H.; HSIEH, M.-H.; YEH, Y.-C.; CHEN, Y.-M.; LIN, C.-Y. Immunological kinship of Class I low molocular weigth heat shock proteins and thermostabilization of soluble proteins in vitro among plants. Plant and Cell Physiology, v. 34, n. 7, p. 1055-1062, 1993.
- JOE, M. K.; PARK, S. M.; LEE, Y. S.; HWANG, D. S.; HONG, C. B. High temperature stress resistance of Escherichia coli induced by a tobacco class I low molecular weight heat-shock protein. Molecules and Cells, v. 10, n. 5, p. 519-524, 2000.
- KALINSKI, A.; ROWLEY, D. L.; LOER, D. S.; FOLEY, C.; BUTA, G.; HERMAN, E. M. Binding-protein expression is subject to temporal, developmental and stress-induced regulation in terminally differentiated soybean organs. Planta, v. 195, n. 4, p. 611-621, 1995.
- KANG, H. M.; PARK, K. W.; SALTVEIT, M. E Chilling tolerance of cucumber (Cucumis sativus) seedling radicles is affected y radicle length, seedling vigour and induced osmotic and heat-shock proteins. Physiologia Plantarum, v. 124, n. 2, p. 485-492, 2005.
- KUMAR, V.; MILLS, D. J.; ANDERSON, J. D.; MATTOO, A. K. An alternative agriculture system is defined by a distinct expression profile of select gene transcripts and proteins. PNAS, v. 111, n. 29, p. 10535-10540, 2004.
- LAEMLI, U. K. Cleavage of structural proteins during assembly of the head of bacteriophage T4. Nature, v. 227, n. 5259, p. 680-685, 1970.
- MACHADO NETO, N. B.; CUSTÓDIO, C. C.; TAKAKI. M. Evaluation of naturally and artificially aged seeds of Phaseolus vulgaris L. Seed Science and Technology, v. 29, n. 1, p. 137-149, 2001.
- MACHADO NETO, N. B.; CUSTÓDIO, C. C.; PENICHE, A. G. P. F Brachiaria access germplasm distinction using SDS PAGE. Acta Scientiarum. Agronomy, v. 24, n. 5, p. 1439-1445, 2002.
- MACHADO NETO, N. B.; SATURNINO, S. M.; BOMFIM, D. C.; CUSTÓDIO, C. C. Water stress induced by mannitol and sodium chloride in soybean cultivars. Brazilian Archives of Biology and Technology, v. 47, n. 4, p. 521-529, 2004.
- MACHADO NETO, N. B.; CUSTÓDIO, C. C.; COSTA, P. R.; DONÁ, F. L. Deficiência hídrica induzida por diferentes agentes osmóticos na germinação e vigor de sementes de feijão. Revista Brasileira de Sementes, v. 28, n. 1, p. 142-148, 2006.
- MORAES, G. A. F.; MENEZES, N. L. Desempenho de sementes de soja sob condições diferentes de potencial osmótico. Ciência Rural, v. 33, n. 2, p. 219-226, 2003.
- NAKAGAWA, J. Testes de vigor baseados nos desempenhos das plântulas. In: KRZYZANOWSKI, F. C.; VIEIRA, R. D.; FRANÇA NETO, J. B. (Ed.). Vigor de sementes: conceitos e testes. Londrina: Abrates, 1999. p. 2-24.
- NEPOMUCENO, A. L.; STEWART, J. M.; OOSTEHUIS, D. M.; TURKEY, R.; NEUMAIER, N.; FARIAS J. R. B Isolation of a cotton NADP(H) oxidase homologue induced by drought stress. Pesquisa Agropecuária Brasileira, v. 35, n. 7, p. 1407-1416, 2000.
- NEPOMUCENO, A. L. NEUMAIER, N.; FARIAS, J. R. B.; OYA, T. Tolerância à seca em plantas: mecanismos fisiológicos e moleculares. Biotecnologia, Ciência e Desenvolvimento, v. 4, n. 23, p. 12-18, 2001.
- PAREEK, A.; SINGLA, S. L.; GROVER, A. Immunological evidence for accumulation of two high molecular weight (104 and 90 kDa) HSPs in response to different stress in rice and response to high temperature stress in diverse plant genera. Plant Molecular Biology, v. 29, n. 2, p. 293-301, 1995.
- PARK, S. Y.; SHIVAJI, R.; KRANS, J. V.; LUTHE, D. S. Heat-shock response in heat-tolerance and nontolerant variants of Agrostis palustris Huds. Plant Physiology, v. 111, n. 2, p. 515-524, 1996.
- PAULA, S. V.; RUIZ, H. A.; ALVARENGA, E. M. Avaliação de plântulas de feijão como critério para seleção de cultivares tolerantes à salinidade. Revista Brasileira de Sementes, v. 16, n. 2, p. 220-224, 1994.
- PRANDL, R.; HINDERHOFER, K.; EGGERS-SCHUMACHER, G.; SCHÖFFL, F. HSF3, a new heat shock factor from Arabidopsis thaliana, derepresses the heat shock response and confers thermotolerance when overexpressed in transgenic plants. Molecular and General Genetics, v. 258, n. 3, p. 269-278, 1998.
- RISTIC, Z.; GIFFORD, D. J.; CASS, D. D. Heat Shock Proteins in two lines of Zea mays L. that differ in drought and heat response. Plant Physiology, v. 97, n. 4, p. 1430-1434, 1991.
- RISTIC, Z.; YANG, G.; MARTIN, B.; FULLERTON, S. Evidence of association between specific heat-shock protein(s) and the drought and heat tolerance phenotype in maize. Journal of Plant Physiology, v. 153, n. 3-4, p. 497-503, 1998.
- SALISBURY, F. B.; ROSS, C. W. Plant physiology 4th ed. Belmont: Wadworth, 1991.
- SANTOS, V. L. M., CALIL, A. C.; RUIZ, H. A.; ALVARENGA, E. M.; SANTOS, C. M. Efeito do estresse salino e hídrico na germinação e vigor de sementes de soja. Revista Brasileira de Sementes, v. 14, n. 2, p. 189-194, 1992.
- SANTOS, V. L. M.; SILVA, R. F.; SEDIYAMA, T.; CARDOSO, A. A. Utilização do estresse salino na qualidade das sementes de genótipos de soja (Glycine max (L.) Merril). Revista Brasileira de Sementes, v. 18, n. 1, p. 83-87, 1996.
- SCHIRMER, E. C.; LINDQUIST, S.; VIERLING, E. An Arabidopsis heat shock protein complements a thermotolerance defect in yeast. Plant Cell, v. 6, n. 12, p. 1899-1909, 1994.
- SCHMITZ, G.; SCHMITZ, M.; FEIRABEND, J. Characterization of a plastid-specific HSP90 homologue: identification of a cDNA sequence, phylogenetic descendence and analysis of its mRNA and proteins expression. Plant Molecular Biology, v. 30, n. 3, p. 479-492, 1996.
- SIEGEL, B. Z. Plant peroxidases: an organismic perspective. Plant Growth Regulation, v. 12, n. 3, p. 303-312, 1993.
- TAIZ, L.; ZEIGER, E. Fisiologia vegetal Porto Alegre: Artmed, 2004.
- TEXEIRA, L. R.; BRACCINI, A. L.; SPERANDIO, D.; SCAPIM, C. A.; SCHUSTER, I.; VIGANÓ, J. Avaliação de cultivares de soja quanto à tolerância ao estresse em substrato contendo polietileno glicol. Acta Scientarium. Agronomy, v. 30, n. 2, p. 217-223, 2008.
- TORMENA, C. A.; SILVA, A. P.; GONÇALVES, A. C. A.; FOLEGATTI, M. V. Intervalo ótimo de potencial da água no solo: um conceito para avaliação da qualidade física do solo e manejo da água na agricultura irrigada. Revista Brasileira de Engenharia Agrícola e Ambiental, v. 3, n. 3, p. 286-292, 1999.
- TORRES, S. B.; VIEIRA, E. L.; MARCOS-FILHO, J Efeitos da salinidade na germinação e no desenvolvimento de plântulas de pepino. Revista Brasileira de Sementes, v. 22, n. 2, p. 39-44, 2000.
- VERDOY, D.; LUCAS, M. M.; MANRIQUE, E.; COVARRUBIAS, A. A.; DE FELIPE, M. R.; PUEYO, J. J. Differential organ-specific response to salt stress and water deficit in nodulated bean (Phaseolus vulgaris). Plant Cell and Environment, v. 27, n. 6, p. 757-767, 2004.
- VIERLING, E. The role of Heat Shock Proteins in Plants. Annual Review of Plant Physiology and Plant Molecular Biology, v. 42, p. 579-620, 1991.
- WATERS, E. R.; LEE, G. J.; VIERLING, E. Evolution, structure and function of the small heat shock proteins in plants. Journal of Experimental Botany, v. 47, n. 3, p. 325-338, 1996.
- WOOD, C. K.; PRATT, J. R.; MOORE, A. L. Identification and characterization of cultivar-specific 22 kDa heat shock proteins from mitochondria of Pisum sativum Physiologia Plantarum, v. 103, n. 3, p. 369-376, 1998.
- WU, D. H.; LAINDMAN, D. L.; SMITH, C. J. Heat shock protein 70 levels in temperature stressed mung bean shoots. Journal of Experimental Botany, v. 44, n. 259, p. 457-461, 1993.
- YANG, T.; POOVAIAH, B. W. Hydrogen peroxide homeostasis: activation of plant catalases by calcium/calmodulin. PNAS, v. 99, n. 6, p. 4097-4102, 2002.
- ZHU, J. K. Plant salt tolerance. Trends in Plant Science, v. 6, n. 2, p. 66-71, 2001.
- ZONTA, E. P.; MACHADO, A. D.; SILVEIRA JUNIOR, P. Sistemas de análise estatística para microcomputadores - Sanest Pelotas: UFPel, 1984.
Datas de Publicação
-
Publicação nesta coleção
03 Mar 2011 -
Data do Fascículo
Set 2010
Histórico
-
Recebido
06 Ago 2008 -
Aceito
03 Nov 2008